Узи лимфатических узлов при меланоме
О меланоме лимфатических узлов говорят, когда меланома пускает метастазы в лимфатическую систему. Опухолевые клетки распространяются из первичного очага меланомы по лимфатическим сосудам, похожим на кровеносные. Таким образом, начинают поражаться лимфатические узлы, располагающиеся в области шеи, над ключицами, в паху и подмышечных впадинах. Лимфатическое поражение при меланоме значительно ухудшает прогностические данные. Попадание злокачественных клеток в лимфоток приводит к тому, что рак начинает поражать всё новые и новые органы, ткани, системы. Диагностика и лечение заболевания проводится докторами онкологами.
Меланома – это злокачественное новообразование, состоящее из меланоцитов. Течение меланомы часто скрытое, вплоть до стадии появления метастазов. Именно по этой причине злокачественные опухоли данного вида часто становятся причиной смерти больных. Патологические образования могут возникать на разных частях тела и поражают преимущественно кожный покров. Однако могут формироваться и на слизистых оболочках, а также глазных яблоках. На теле человека множество родинок, но не все они являются опасными. Меланома развивается из пигментного новообразования (невуса). Такие родинки имеют неправильную форму и быстро увеличиваются в размере. Распространенность меланомы – 6:100000.

Причины возникновения
Возможными причинами возникновения заболевания кожи меланомы могут быть:
- воздействие ультрафиолета;
- генетическая предрасположенность;
- травматизация родинок;
- гормональные перестройки.
Опухоль при меланобластоме метастазирует в лимфоузлы чаще у пожилых и ослабленных пациентов, однако, остальные возрастные группы больных также подвержены риску распространения метастазов.
Меланома может распространяться по организму гематогенным путем (по кровеносным сосудам) и лимфогенным. При втором варианте злокачественные клетки накапливаются в лимфатических узлах, разрастаются, становятся больше в диаметре. Первые лимфоузлы, которые поражают метастазы, в медицинской практике называют сторожевыми. Они могут располагаться в любой части тела, что зависит от локализации первичного очага рака.
Виды и степени
Меланома кожного покрова начинает метастазировать на третьей стадии развития.
Распространенность опухолевого процесса доктора обозначают буквой N в сочетании с цифрой:
- N0 – поражение лимфатических узлов отсутствует.
- N1 – новообразование поразило один близлежащий лимфатический узел.
- N2 – обнаружено поражение двух и более регионарных и сторожевых лимфоузлов.
- N3 – поражению подверглись дальние лимфоузлы, например, при меланоме головы происходит поражение паховых лимфоузлов.
Существует еще одна классификация, которая, помимо буквы N, содержит строчную букву:
- Na – злокачественный процесс уже выявлен в лимфоузлах, но увидеть его можно только с помощью микроскопа;
- Nb – раковые клетки достигли большого размера, а их наличие уже определяется при проведении тестов;
- N2c – злокачественные клетки находятся в лимфатических каналах около новообразования, но в сами лимфоузлы еще не проникли.
Меланома может метастазировать даже после проведения операции по иссечению новообразования. Несмотря на то что опухоль удаляется с частью здоровых тканей (отступая несколько сантиметров), она очень часто рецидивирует, и этого не могут предотвратить даже химическая и лучевая терапии. Меланома, удаленная на второй A стадии, возвращается в пятнадцати – тридцати процентах случаев. Если новообразование удалялось на второй B и C стадиях, то оно рецидивирует в сорока и семидесяти процентах случаев соответственно.
Симптомы
При появлении метастазов меланомы в лимфоузлах первым делом происходит увеличение размеров узлов, расположенных недалеко от первичного очага. Большой размер метастазов приводит к тому, что лимфоузлы становятся чрезмерно плотными, срастаются между собой и с окружающими тканями.
Больной резко теряет в весе, становится слабым, происходит развитие анемии, возникают головные боли и гипертермия. Могут присутствовать и дополнительные признаки, такие как мигрень, невроз, частые ОРВИ, воспалительные процессы кожных покровов.
Диагностика
- рентген пораженной области;
- биопсию сторожевых лимфоузлов для проведения гистологии;
- тонкоигольную аспирационную биопсию;
- ПЭТ (позитронно-эмиссионную томографию);
- КТ (компьютерную томографию);
- МРТ (магнитно-резонансную томографию);
- УЗИ (ультразвуковое исследование);
- лимфосцинтиграфию;
- анализ крови на онкомаркеры.
После диагностических мероприятий больной направляется на лечение в онкологическое отделение.
Методы лечения
Меланома лимфоузлов является злокачественным заболеванием, требующим лечения в неотложном порядке. Методов терапии может быть несколько. Если новообразование на коже имеет локальную форму, то доктор удаляет его, захватывая небольшой участок окружающих здоровых тканей, а также ближайшие группы лимфатических узлов. Если метастазы обнаруживаются в лимфоузлах, проводится их радикальное удаление. При регрессе меланомы проводится расширенное оперативное вмешательство, но оно не дает большого шанса на благоприятный прогноз. На последней стадии адъювантная терапия меланомы состоит из химиотерапии и облучения.

Кроме стандартной операции, существуют и другие методы лечения данной патологии:
- Лимфодиссекция – наличие клеток в лимфатических узлах служит показанием к удалению не только самих лимфоузлов места локализации, а и сосудов, жировых и других тканей конкретной лимфоидной структуры.
- Лучевая терапия – облучение ионизирующей радиацией проводится для того, чтобы опухоль прекратила развитие. Облучение также может применяться на последней стадии онкопатологии, чтобы уменьшить выраженность симптоматики и облегчить состояние больного.
- Химиотерапия – применяется для уменьшения новообразования до пятнадцати процентов от изначального размера, а также уменьшения клинической картины. После химиотерапии практически всегда возникают такие побочные эффекты, как тошнота, рвота, облысение, угнетение иммунной системы, потеря веса. Доктора подбирают лекарства для уменьшения побочного действия химиопрепаратов.
- Иммунологическая терапия – при помощи иммунотерапии доктора активизируют работу иммунитета, что улучшает прогностические данные.
Комплексное лечение помогает уменьшить метастазирование в лимфоузлы на сорок процентов. При опухоли последней стадии оперативное вмешательство не проводится. Таким больным назначается паллиативная терапия, состоящая из приема химических препаратов, облучения, наркотических обезболивающих препаратов.
Реабилитация
После оперативного вмешательства больной должен посещать доктора ежеквартально первые два года, а следующие десять лет – дважды в год.

На каждом приеме онколог оценивает состояние кожных покровов и лимфоузлов больного. В зависимости от того, на какой стадии была проведена операция, могут назначаться и другие методы обследования. В реабилитационный период пациенту назначается специальная диета, иммуностимуляторы и другие необходимые препараты.
Важно, чтобы больному была оказана психологическая поддержка родными или специалистами.
Прогноз и профилактика
Если метастазы меланомы обнаружены в одном лимфатическом узле, прогноз для больного составляет сорок три процента. Если поражен не один лимфоузел, через 5 лет болезнь возвращается в семидесяти пяти процентах случаев. При паллиативном лечении четвертой стадии онкопатологии больные, как правило, погибают в течение полугода или чуть больше. После проведения операции онкологическое заболевание чаще рецидивирует у мужчин, нежели у женщин.
Предотвратить появление метастазов меланомы в области лимфатических узлов можно при своевременном диагностировании болезни.

Уберечься от возникновения первичных очагов рака на коже помогут:
- Ведение здорового образа жизни (правильное питание, отказ от вредных привычек).
- Ограничение воздействия на кожу ультрафиолета (солнечных лучей и загорания в солярии).
- Избегание воздействия на кожу агрессивных веществ и химикатов.
- Предотвращение травматизации кожных покровов и родинок.
Чтобы раньше выявить наличие патологии на коже и обратиться к доктору за лечением, не стоит пренебрегать периодическим самостоятельным осмотром. Если на теле обнаружатся родинки или родимые пятна неправильной формы, которые увеличиваются в размерах или болят, необходимо сразу же посетить дерматолога или онколога.

Лидер продаж в высоком классе. Монитор 21,5" высокой четкости, расширенный кардио пакет (Strain+, Stress Echo), экспертные возможности для 3D УЗИ в акушерско-гинекологической практике (STIC, Crystal Vue, 5D Follicle), датчики высокой плотности.
В последние годы во всем мире отмечается стремительный рост заболеваемости злокачественными новообразованиями кожи, каждый год регистрируется до 3 млн новых случаев рака кожи.
Злокачественные опухоли кожи среди всех злокачественных новообразований человека занимают третье место, уступая раку желудка и легкого. Как и при другой онкологической патологии, вероятность развития заболевания повышается с возрастом: пожилые люди в возрасте старше 70 лет в 7 раз чаще болеют злокачественными опухолями кожи по сравнению с лицами в возрасте от 40 до 49 лет и в 230 раз чаще, чем в возрасте до 40 лет [1].
Злокачественные опухоли кожи по гистологическому строению можно разделить на 3 основные группы: рак (базальноклеточный, карцинома), меланома, саркома. Если рак и меланома возникают из элементов эпителия, то саркома - из соединительнотканных образований кожного покрова.
Рак достигает наибольшей частоты среди всех прочих злокачественных опухолей кожи - 12-14% (3-5 место); поражает почти одинаково часто мужчин и женщин. Показатели заболеваемости колеблются от 50 до 60, а у пожилых 140-145 на 100 тыс. жителей, пик заболеваемости приходится на возраст 60-70 лет [2].
Саркомы встречаются редко (менее 1% от всех злокачественных опухолей), развиваются в возрасте 35-50 лет, локализуются чаще на коже туловища и конечностей. Саркомы возникают на месте многократных травм, рубцов, на фоне туберкулезной волчанки, после лучевой терапии, а также в предшествующих фибромах, ангиофибромах, липомах (трансформация в саркому отмечается в 3-12% случаев).
В структуре злокачественных новообразований кожи на меланому приходится около 10%, причем заболеваемость этой опухолью во всем мире имеет тенденцию к росту на 2,6-11,7% в год, увеличиваясь приблизительно в 2 раза каждые 10-15 лет в первую очередь за счет лиц молодого трудоспособного возраста [3].
До недавних пор меланому кожи относили к заболеваниям с непременным фатальным исходом, однако внедрение в последние годы в практику новых химиои иммунопрепаратов позволило добиться улучшения результатов лечения и в настоящее время меланома кожи считается потенциально излечимым заболеванием при условии раннего выявления и назначения адекватной терапии [4].
Основными прогностическими факторами при меланоме кожи являются такие характеристики первичной опухоли, как ее толщина по Бреслоу (Breslow) и уровень инвазии по Силвен-Кларк (Sylven and Clark) (рис. 1), а также состояние регионарных лимфатических узлов как зоны возможного метастазирования [5].
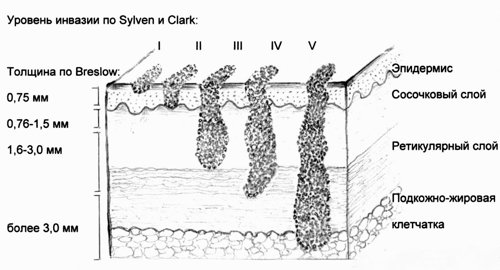
Уровни инвазии по Силвен и Кларк, толщина по Бреслоу.
В настоящее время хирургический метод является основным в лечении первичной меланомы кожи, причем с целью снижения вероятности метастазирования объем иссечения должен определяться толщиной опухоли. Так, при индексе Бреслоу 1,0 мм или меньше требуется отступить от края опухоли на 1,0 см; от 1,0 до 4,0 мм - 2,0 см; более 4,0 мм - более 2,0 см 6.
По общепринятой методике толщину первичной меланомы кожи определяют после ее удаления при гистологическом исследовании. Как следствие, либо возникает необходимость выполнения реэксцизии в соответствии со значением индекса Бреслоу, либо, во избежание повторной операции, планируется заведомо избыточный объем иссечения, что нежелательно с косметической точки зрения, особенно при расположении опухоли на открытых участках тела и лице.
Своевременная оценка местного распространения (толщины и уровня инвазии) опухоли и состояния регионарных лимфатических узлов до начала лечения имеет принципиальное значение, так как не только влияет на выбор адекватного объема операции, но и позволяет планировать адъювантную химио- и иммунотерапию еще на дооперационном этапе.
Такой неинвазивный метод прижизненного исследования тканей, как ультразвуковое исследование (УЗИ) выгодно отличается возможностью количественной оценки структур кожи и в последние 10-15 лет стал активно развиваться благодаря появлению высокочастотных датчиков - 17,5 МГц и более [9], хотя использование избыточного слоя геля позволяет получить детальное изображение слоев кожи и при рабочих частотах от 7,5 до 13,0 МГц. Таким образом, внедрение УЗИ кожи и стандартизация измерений является актуальной задачей.
Целью настоящей работы явилось уточнение возможности дифференциации слоев кожи и дооперационного определения распространенности первичной опухоли по критериям Бреслоу и Силвен-Кларка при исследовании обычными датчиками для поверхностных органов с частотой от 7,5 до 13,0 МГц.
Проанализированы результаты УЗИ 52 пигментных образований кожи у 21 мужчины и 31 женщины в возрасте от 24 до 89 лет (средний возраст 64,5±3,6 года).
Первичная опухоль располагалась на коже головы и шеи в 7 случаях, туловища - в 25, рук - в 14, ног - в 6. Исследования проводились за 8-60 дней до дня операции (в среднем за 26 дней).
При исследовании пользовались методикой, предложенной Г.С. Аллахвердян [10] заключающейся в применении в качестве акустического окна наполненного гелем колечка, накладываемого на кожу в зоне исследуемого образования. Применение колечка вместо стандартной гелевой насадки на датчик полностью исключает фактор сдавливания и без того часто крайне тонкого образования, что приводит к улучшению визуализации и к отсутствию искажений в измерениях.
УЗИ проводили на современных ультразвуковых аппаратах линейными датчиками с частотой от 7,5 до 13,0 МГц в режиме сканирования Small Parts Superficial. С целью оптимизации изображения в серой шкале применяли тканевую гармонику, режим HI ZOOM. Измеряли толщину опухоли в миллиметрах от наиболее поверхностной до наиболее глубокой границы опухоли, анализировали размеры, форму, эхогенность, структуру, контуры, локализацию образования относительно слоев кожи и подкожной жировой клетчатки, наличие дополнительных акустических эффектов, таких как тенеобразование или дистальное усиление эхосигнала. В режиме цветового допплеровского картирования оценивали наличие и характер васкуляризации, в режиме компрессионной эластографии (у 11 пациентов) - жесткость образования.
Эпидермис при УЗИ визуализировался в виде узкой гиперэхогенной полоски с несколько неровным наружным контуром толщиной от 0,03 до 1,0 мм. Минимальная толщина эпидермиса отмечалась на внутренней поверхности плеча и бедра, максимальная - в области крупных суставов и верхней части спины, что согласуется с литературными данными о зависимости толщины эпидермиса человека от локализации.
Описанная в литературе слоистость эпидермиса при исследовании с частотой 17,5 МГц, при частотах 7,5-10,0 МГц не прослеживалась. При частоте 13,0 МГц слоистость эпидермиса определялась нечетко и лишь при большом увеличении в режиме HI ZOOM (рис. 2).
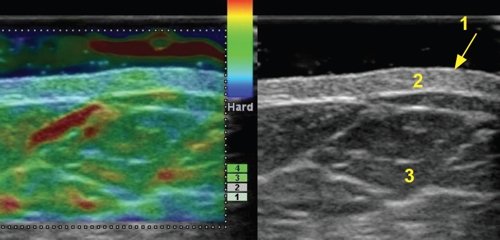
1 - эпидермис, 2 - дерма, 3 - подкожно-жировая клетчатка.
Дерма визуализировалась в виде полоски повышенной или средней эхогенности однородной структуры толщиной от 0,5 до 4,0 мм (также в зависимости от зоны исследования). Эхогенность дермы обусловлена наличием коллагеновых и эластических волокон. Сосуды в дерме и эпидермисе на неизмененных участках кожи не визуализировались, что объясняется их малым диаметром и низкой скоростью кровотока.
При осмотре в режиме эластографии гелевая прослойка внутри кольца между поверхностью датчика и кожей окрашивалась трехслойно (красный-зеленыйсиний), неизмененный эпидермис - равномерно в голубой цвет. Дерма окрашивалась по смешанному типу с преобладанием голубого цвета и участками зеленого цветов.
Отчетливо дифференцировать слои дермы - сосочковый и ретикулярный, и тем более поверхностную и глубокую зоны сосочкового слоя при исследовании датчиками 7,5-13,0 МГц ни в режиме серой шкалы, ни при эластографии не представлялось возможным.
Подкожно-жировая клетчатка визуализировалась в виде зоны пониженной эхогенности с наличием тонких гиперэхогенных перегородок, являющихся отражением пучков соединительной ткани, переплетающихся и образующих крупнопетлистую сеть, в ячейках которой находится жировая ткань в виде долек. В перегородках находятся коллагеновые волокна, кровеносные и лимфатические сосуды и нервы. В прилегающих к дерме участках подкожно-жировой клетчатки при осмотре в режиме ЦДК визуализировались мелкие артериальные и венозные сосуды. При осмотре в режиме эластографии подкожно-жировая клетчатка окрашивалась мозаично с равным количеством голубого, зеленого и красного цвета. Полученные данные согласуются с представлением о том, что эпидермис и дерма плотнее, чем подкожно-жировой слой.
При УЗИ получено 51 изображение из 52 пигментных образований кожи. В 1 случае пигментное образование не визуализировалось и никаких дополнительных акустических эффектов, утолщения слоев кожи или изменений васкуляризации или жесткости, не отмечалось.
Морфологически исследованные пигментные образования оказались в 22 наблюдениях - базалиомой, в 8 - раком кожи, в 18 - меланомой, в 4 - пигментным невусом.
Базалиома и рак кожи (рис. 3, 4) визуализировались как гипоэхогенные образования, чаще неправильной формы (реже - веретенообразные), имели преимущественно умеренно неоднородную структуру, контур чаще неровный, акустическая тень не определялась, в 1 случае отмечалось дорсальное усиление эхосигнала (при аденокистозной базалиоме вульвы). Толщина базалиомы составляла в среднем 4,9 мм (от 2,3 до 7,0 мм), толщина рака - в среднем 6,1 мм (от 2,1 до 10,0 мм). Во всех образованиях регистрировался кровоток в виде единичных питающих сосудов преимущественно с венозным спектром. При осмотре в режиме эластографии базалиома окрашивалась мозаично, рак кожи в режиме эластографии не исследован.
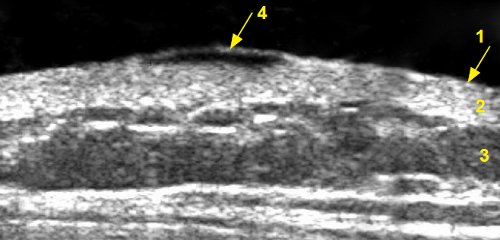
1 - эпидермис, 2 - дерма, 3 - подкожно-жировая клетчатка, 4 - базалиома толщиной 1,0 мм.
Биопсия сторожевых лимфатических узлов — процедура, с описания которой начинался мой блог в 2012г., и не смотря на то, что за годы существования сайт наполнился множеством сопутствующих материалов (лечение, лекарства, результаты клинических исследований и т.д.), основным лейтмотивом остается ранняя диагностика меланомы и предупреждение развития болезни, т.е., в первую очередь, хирургия.
Ну, и в связи с тем, что глядя вот на такие регулярные истории:
Обновлено 10.09.2018
ЧАСТЬ I . ПРАКТИЧЕСКАЯ
+ четырнадцать случаев обнаруженных уже после написания статьи и, соответственно, находящихся в самом конце.
ИТОГО: шестнадцать.
Обращаю ваше внимание на то, что речь идет только о метастазировании в регионарный лимфоузел, т.е. никаких транзиторных метастазов, метастазов в послеоперационный рубец и метастазов в отдаленные органы/ткани НЕТ.
Вопрос (основной): Почему это произошло? Вернее даже так: где все это время находилась клетка меланомы (возможно, небольшой конгломерат клеток)?
Итак, меланома — два клинических случая.
На самом деле такие случаи я и раньше наблюдал, просто не появлялось мысли их объединить в один пост .
I В 2011г. удалена меланома на голени. Толщина опухоли 1,3 мм. Кларк III, 2 митоза. Изъязвление отсутствует. Биопсия сторожевых лимфоузлов не проводилась. В 2017г. (через 6 лет) происходит рецидив в регионарный лимфоузел. Пациента зовут Ольга (все описано очень подробно)
II Здравствуйте Вадим! очень хочется услышать Ваш совет-ответ. Моей дочке 18 лет, несколько дней назад у нас удалили лимфоузел, и поставили диагноз узловая меланома , 8 лет назад мы удалили родинку, и все анализы были хорошие, а вот теперь пересмотрели стекла и подтвердили диагноз.
***Если первая история очень подробно описана, то по второй я могу дать только пару пояснений (хотя абсолютно все подтверждающие документы у меня имеются), т.к. во-первых, дело касается ребенка (на момент операции девочке было 10 лет), и во-вторых, для этой статьи важен только сам факт.
В 2009г удалена родинка. Гистология показывает «пигментный внутридермальный папилломатозный невус«. Пересмотр в 2017 — узловая меланома (без каких либо уточнений, т.к. патолог не посчитал нужным это сделать). Ну и, соответственно, метастаз в лимфоузел (опухолевая ткань распространяется за пределы капсулы).
По состоянию на 12.09.2018, множественные метастазы в головной мозг……
Это все, что нужно знать читателю в контексте данной статьи.
Ну шо, теперь можно высказывать предположения о том,
Меланома, как и простая родинка, в некоторых случаях бывает подвержена регрессу. Так было у меня с родинкой: Лечение в Израиле. Удаление родинки , и вот свежий пример гистологии меланомы (выделено красненьким):
**два слова выделенные зелененьким тоже очень важны, но о них ниже.
И вот у вас на коже появилось некое новообразование, ну как в этом примере: Беспигментная меланома (там фотка очень наглядная), а потом постепенно пропало (раз имеются случаи 50% регресса, то можно предположить, что и 100% бывает). И вот проходит несколько лет и вы обнаруживаете метастаз… можно ли найти первоисточник? Думаю да, но для этого надо всю кожу снять и на гистологию отправить, т.к. визуально ни один врач ничего не обнаружит.
Но в наших то примерах первичная опухоль есть и, соответственно, не думаю, что стоит сочинять дополнительные причины.
4. Тоже самое касается предположения, что клетка находилась в тканях между местом первичного удаления и нашим многострадальным лимфоузлом. Ну как вот в этом мультике (только вместо кровеносного сосуда представьте себе лимфатический):
Получается, что наша клетка сквозь стенку сосуда пролезла в ткани, но делиться не начала и через те же 5-6 лет вылезла обратно и продолжила движение к лимфоузлу. В этом случае это уже не клетка меланомы получается, а какой-то наноробот с искусственным интеллектом…
У вас есть другие предположения? Пишите в камментах. Я ничего другого придумать не могу
И теперь возникает промежуточный вопрос: вы все еще считаете, что биопсия сторожевых лимфатических узлов — это диагностическая процедура? Ню-ню. Задумайтесь на секундочку, что бы было, если бы через пару лет после удаления опухоли (даже не в течении 6 месяцев, как рекомендуют врачи), нашим пациентам были бы удалены сторожевые лимфоузлы вместе с находящейся в одном из них клеткой (конгломератом клеток) меланомы? В тот момент, когда никакого деления этой/этих клеток еще не было и в помине..
Вот такие у меня имеются мысли. Если вы ничего не поняли, то прочитайте еще разок, ибо пишу я, местами, витиевато 🙂
И тут еще добавлю: Добавочка от июля 2018.
Если вам не рекомендуют эту процедуру в принципе, то сие свидетельствует о том, что ваш онколог либо глуп, либо ленив, либо не представляет себе, о какой процедуре идет речь (а в случае со страховой медициной речь может идти о нежелании страховой компании платить деньги за операцию).
К сожалению, я нигде не встречал статистики по вышеприведенным случаям (думаю, ее нет), поэтому, если у вас лично, или у ваших пациентов, знакомых, друзей было нечто подобное (метастаз меланомы только в регионарный лимфоузел через несколько лет после удаления первичной опухоли), то я с удовольствием добавлю его на эту страницу, чтобы получилось как с меланомой после беременности .
ЧАСТЬ II. ТЕОРЕТИЧЕСКАЯ
Итак, начнем со строения кожи. Нас интересует 4 ее компонента:
Эпидермис, базальный слой, сосочковый слой дермы и сетчатый слой дермы.
Эпидермис — верхний слой кожи, который нас вообще не интересует, ибо в нем нет ни капилляров крови, ни капилляров лимфы. Поэтому, пока ваша меланома находится в эпидермисе и не преодолела базальный слой, отделяющий эпидермис от сосочкового слоя дермы, после удаления опухоли вы получаете полную индульгенцию.
Толщина эпидермиса на разных частях тела неравномерна и варьируется от 0,05мм до 1,5 мм (на пятках и ладонях, например). Поэтому, при идентичной толщине опухоли, инвазия по Кларку может быть не одинаковой у разных людей и на разных частях тела.
Базальный слой — отделяет эпидермис от сосочкового слоя дермы и является как-бы границей, после которой начинаются проблемы.
Тут тоже очень интересный момент: разрушившая базальный слой меланома стадируется как Кларк II (базальная мембрана, разделяющая эпидермис и дерму, разрушается опухолевыми клетками, которые начинают прорастать в верхний, сосочковый слой дермы), но все равно считается, что при отсутствии дополнительных факторов (изъязвление, митозы и т.д.) прогноз весьма благоприятный. Лично мне объяснить это очень сложно, но факт остается фактом.
Добавочка от июля 2018
В случаях описанных ниже, вы найдете историю про метастазирование меланомы Бреслой 1 мм и Кларк II
Сосочковый слой дермы — это самый интересный и важный слой кожи (с точки зрения меланомы), т.к. основная масса пациентов, как ни крути, имеют инвазию Кларк III (сосочковый слой целиком заполнен атипичными меланоцитами, но в сетчатом слое их не наблюдается).
Т.к начиная с этого момента всем требуется БСЛУ (а кто говорит, что не требуется, тот идет лесом), то остановимся на нем подробнее.
Вот как выглядят капилляры крови в дерме:
Естественно, все весьма схематично и нужно понимать что в реале все гораздо плотнее расположено (толщина ВСЕЙ дермы варьируется от 0,3 до 3 мм).
И как бы на первый взгляд получается, что проникнув в сосочковый слой дермы наша клетка меланомы сразу должна попасть в кровь, но этого не происходит (статистику не обманешь). Дык почему?
А потому, что помимо капилляров крови, в сосочковом слое (впрочем, как и во всех остальных тканях организма за небольшим исключением) присутствуют окончания лимфатических сосудов в виде «слепых капилляров«, которые называются так потому, что у них все движение идет только в одном направлении.
Выглядит это так (обратите внимание на размеры лимфатического капилляра и капилляра крови):
т.е. наш сосочковый слой кожи покрыт этой сетью , которая всасывает все чужеродное, лишнее, отработанное — все то, что в венозный капилляр попасть не должно (ну так природой предусмотрено).
И вот тут нужно подняться вверх статьи и прочитать два слова, которые выделены зелененьким цветом в результатах гистологии: ВНУТРИСОСУДИСТАЯ ИНВАЗИЯ отсутствует. Вот именно этим вполне себе можно объяснить то, что распространение меланомы начинается по лимфе. Можно ведь предположить, что в капилляр крови она попадает только тогда, когда в него прорастает?
И именно поэтому, опасность первоначального распространения по крови возрастает, когда опухоль достигает СЕТЧАТОГО слоя дермы, что обозначает, что в сосочковом слое уже жуть что происходит.
и вот еще подробнее:
И вот тут мы дошли до ответов на два интересных вопроса:
Что значит «метастазирование по крови«? А глобально НИЧЕГО НЕ ЗНАЧИТ и начавшаяся распространяться по лимфе меланома в любом случае попадает к вам в кровь (если ее не тормознуть, конечно), ибо лимфоток — это не закрытая система. Попав в кровь, через подключичную вену, наша клетка меланомы устремляется в сердце и затем куда? Правильно, дорогие мои малыши, следующая остановка — ЛЕГКИЕ. Вот вам и ответ на второй вопрос: почему чаще всего меланома метастазирует в легкие.
Последний вопрос: про «лимфодренажный массаж«, который очень часто задают.
Видимо да, ибо ничем другим такой запрет не объяснить. Вот и все.
Ну и напоследок рекомендую: «НаучФильм 1981 год СССР Строение и функции лимфатической системы«. Дело в том, что хоть наука за последние 40 лет и шагнула далеко вперед, базовые параметры работы нашего организма, которые, собственно, нас и интересуют, остались прежними. Я посмотрел уже достаточно разных мегафильмов и послушал лекций, но ничего лучше пока не нашел.
Онкообразование, возникающее в пигментных клетках кожных покровов, на слизистой оболочке или глазном яблоке, называется – меланома. Это очень агрессивная форма рака, которая долгое время проходит латентно, вплоть до метастатических стадий.
Наиболее склонны к поражению опухолью ближние или дальние лимфатические узлы ‒ небольшие скопления клеток иммунной системы, что находятся в области шеи, подмышек и паха.
Распространение рака кожи, при котором происходит трансляция опухолевых клеток в лимфоидную систему, классифицируется как меланома ‒ метастазы в лимфоузлы. Причина такого состояния кроется во вторжении онкологического процесса в кровеносно-сосудистую систему и его перемещении по организму.
Современная диагностика
При метастатической меланоме важно определить степень поражения. Развитие онкологического процесса, прежде всего, воздействует на лимфатические узлы, поэтому онколог проведет ряд исследований:
- Различные виды томографий:
- компьютерная и магнитно-резонансная томографии предвидят применение точных рентгеновских лучей или радиоволн с целью визуализации внутренних структур и потока крови;
- лимфосцинтиграфия представляет метод отображения лимфатических сосудов для отслеживания путей распространения опухолевых клеток. Голубой краситель вводится в кожу вокруг опухоли. Он проходит в жидкость лимфы, показывая способы возможного расширения с помощью специального сканера.
- позитронно-эмиссионная томография ‒ важный метод диагностики, отображающий измененные ткани, что, в отличие от нормальных, принимают участие в ускоренном метаболизме.
- Биопсия ‒ изъятие частицы патологической ткани. Зачастую метод рассматривается как единовременная хирургическая операция по изъятию лимфоузлов. Выделяются такие основные способы проведения:
- аспирационная биопсия: посредством тонкой иглы изымается образец клеток;
- биопсия сторожевого узла ‒ удаление ближайшего от меланомы лимфоузла с целью проверки на наличие аномальных клеток. Если такие присутствуют, нужно проверить отдаленные железы.
- Анализ крови. Сыворотка ЛДГ является маркером для выявления прогрессирования болезни в отдаленные участки.
Как понять по стадии, что есть метастазы меланомы в лимфоузлах?
Существует 2 вида постановки заболевания:
- Клиническая : основывается на исследованиях места основной меланомы и содержит сведения о болезни до применения лечения.
- Патологическая : использует всю клиническую информацию, но также учитывает результаты биопсии иных органов и систем, даже после примененных терапевтических мер.
На опухоли кожи, что распространились в лимфоузлы, обычно указывают 3 и 4 этапы. Но при этом нужно обязательно учитывать особенные обозначения. На распространение указывает буква N. Она сочетается с цифрой. Клиническая постановка включает знаки:
N 1 ‒ поражен 1 ближний узел;
N 2 ‒ затронуты 2 или 3 ближних узла или выявлен транзит ракового образования в сторону лимфатических сосудов;
N 3 ‒ поражены 4 и более лимфатических узла.
При патологической постановке иногда добавляются строчные буквы. Классификация имеет вид:
Любой Nа : онкопроцесс постиг лимфатические узлы, но он настолько мал, что виден только под микроскопом;
Любой Nb : означает, что рак довольно большой и отражается в тестах;
N2с : определяет меланому, выявленную в лимфоканалах вокруг опухоли, но не достигшую самых узлов.
Метастазы в лимфоузлы после удаления меланомы: когда происходят?
На 1 и 2 стадиях основным лечением является широкое иссечение. Во время операции удаляется сама меланома, а также часть здоровой ткани вокруг нее. В зависимости от диаметра опухоли, хирург изымает, как минимум, от двух до шести миллиметров вокруг. Если диагностические тесты не выявили опухолевых тканей в иных местах, лучевая терапия не рекомендована.
Однако, к сожалению, процедура не обеспечивает полное выздоровление, поскольку меланома склонна к частым рецидивам и быстрому прогрессу. Статистика гласит:
- между 15 и 35% первичных клинических 2А вернуться после операции на протяжении 5-ти лет;
- от 40 до 70% стадий 2В и 2С повторятся снова;
- больше половины формирований 3 этапа возникнут вновь.
Очень часто раковые заболевания кожи возвращаются в более продвинутой форме.

Метастазы меланомы в лимфоузлы
Тактика лечения
Лечебные мероприятия основываются на изучении полной картины онкозаболевания и представляют виды:
При выявлении меланомы в ближних сторожевых узлах, врачи рекомендуют удаление не только всех оставшихся лимфатических узлов в этой области, но и целой лимфоидной структуры, включая сосуды и жировые ткани.
Также способна уменьшить прогрессирование заболевания.
Для продвинутых этапов включает применение “Дакарбазина” (DYIC-Dome) и его орального варианта “Темозоломида”, а также иногда используются “Кармустин”, “Винбластин”, “Цисплатин”, “Доцетаксел” и др. Статистика документирует 12-15% уменьшения опухоли.
Иммунотерапия рака повышает защитные силы организма. В последние годы биологическое лечение достигло значительных успехов. Клинические испытания показывают, что люди, принимающие адъювантные препараты, имеют лучший прогноз, нежели те, кто принимал химиотерапию. Онкология пользуется такими средствами, как “Интерлейкин-2”, “Интерферон”, “Ипилимумаб” (моноклональное антитело CTLA4), “Ниволумаб” и “Кейтруда” (антитела PD-1, блокирующие поступление белка). Метастатический процесс при комплексном воздействии уменьшается на 30-40 %.
Прогноз и чего ожидать?
При региональных метастазах после хирургической лимфодиссекции долгосрочная раковая выживаемость существенно увеличивается и составляет:
Прогностические 5-летние результаты для людей, младше 50 лет с региональным распространением, выше. Они указывают на 48% выживших. Для женского пола шансы более высоки, нежели для мужского: 49% к 40%.
По данным, 4 из 10 человек (40%), которые воспользовались хирургической резекцией при метастатической опухоли, живы спустя 5 лет. Рецидивы наблюдаются лишь у 34% пациентов.
В зависимости от количества пораженных узлов, 5-летняя продолжительность жизни колеблется от 53% (для единичного метастаза) и до 25% (для 4-х и больше).
Средняя выживаемость для метастатического рака IV степени представляет 6-10 месяцев.
Когда заболевание прогрессировало до уровня меланома ‒ метастазы в лимфоузлы, нужно внимательно и адекватно оценить все возможные способы лечения, поскольку эффективная терапия способна значительно увеличить шансы на долгосрочное выживание и продлить жизнь больному.
Читайте также:

