Убивает красная химия раковые клетки в лимфоузлах
Лимфатическая система защищает наш организм от неблагоприятных факторов внешнего мира. В ее состав входит целый комплекс сосудов и узлов, которые соединены между собой. Как и любой другой орган, они склонны к негативному влиянию со стороны мутагенных клеток. Эти клетки склонны к делениям, которые невозможно контролировать, чем и вызывают онкологическое заболевание. Рак лимфоузлов встречается близко в 4% больных.
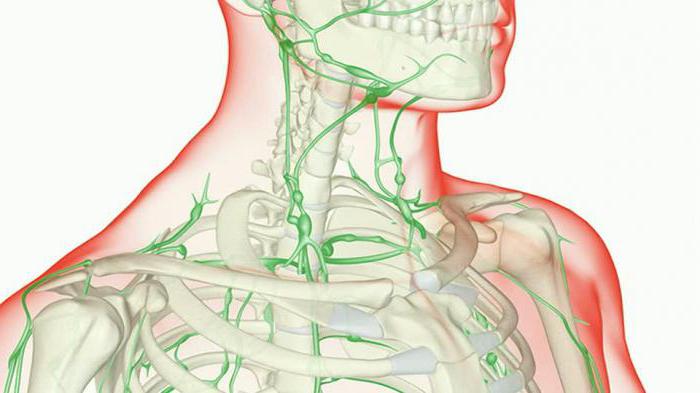
Стоит заметить, что существует свыше 50 видов гистологии опухолей.
В зависимости от этого выделяют две группы заболеваний:
- Неходжкинские лимфомы. Это злокачественные опухоли, которые встречается достаточно часто, в более 70% случаев. Неходжкинские лимфомы включают в свой состав около 30 разных злокачественных опухолей.
- Лимфома Ходжкина. При этой форме клетки очень быстро растут, и даже могут распространяться за пределы лимфатической системы. Встречается, как правило, в 30%
Лечится ли рак лимфоузлов (лимфома) – это первый вопрос, который, ошарашенный своим диагнозом больной, сразу же задаст врачу-онкологу. Как лечить рак лимфоузлов, с чего следует начать?
Лечение рака лимфоузлов дело длительное и кропотливое. Но своевременно поставленный диагноз и правильно оцененная стадия болезни – это уже половина пути, пройденная к поиску индивидуальной терапии!
Подход к лечению лимфомы должен быть комплексным.
Основными методами являются:
- химиотерапия;
- лучевая терапия;
- хирургическая операция;
- трансплантация костного мозга.
Лечение рака лимфоузлов зависит от места нахождение опухоли, стадии на которой находится процесс, наличия распространение метастаз, а также от присутствия еще каких-либо заболеваний.
Существует несколько современных способов лечения, которые могут помочь, в зависимости от стадии заболевания:
На сегодня, более эффективным способом, как лечить рак лимфоузлов является оперативное вмешательство, то есть операция, при которой вырезают не только саму опухоль, которая находится в лимфатическом узле, но и соседние региональные лимфоузлы, если это необходимо. Это делается с целью снижения возможности повторного развития болезни.
Для оценки наличия и состояния ракового процесса, который находится в лимфоузлах, хирург вводит специальный краситель или радиоактивный препарат в область, пораженную злокачественными клетками. Эта жидкость попадает в лимфоузлы.
Если при исследовании этих лимфоузлов в них обнаруживаются раковые клетки, хирург может порекомендовать удалить еще несколько лимфоузлов около сигнального узла. Если же в сигнальном лимфоузле не обнаружено клеток опухоли, то больше лимфоузлов не удаляется. В отличие от стандартного удаления подмышечных лимфоузлов иссечение сигнальных лимфоузлов характеризуется меньшим числом побочных эффектов.
Как правило, лучевая терапия проводится после хирургического вмешательства.
В зависимости от типа излучения, процедура может быть, как:
- Гамма-терапия.
- Облучение с использованием протона.
- Облучение с помощью нейтронов.
- Рентгенотерапия.
Для того, чтобы увеличить нагрузку на опухоль, проводят специальное встречное облучение. При таком способе лучи направляют из двух полей или используют метод ротации. Стоит заметить, что лучевой метод может быть с большим и мелким фракциями, и с расщеплением дозы.
Врачи, процедуру облучения, проводят в специальном кабинете. Пациент не чувствует никаких болевых или других ощущений. Перед самой процедурой больной занимает нужное положение, и для того, чтобы избежать облучения других органов врач надевает на него специальные блоки. Процесс может занимать от 1 до 5 минут, в зависимости от сложности и участка поражения. Специалист внимательно наблюдает за пациентом в течение всей процедуры облучения из специального помещения.
Химиотерапия при раке лимфоузлов может проводиться как до, так и после хирургического вмешательства. Использование химиопрепаратов позволит остановить рост опухоли полностью или даже уменьшить ее размеры.
Такую процедуру проводят курсами, так как организму необходимо отдохнуть и возобновиться после химиопрепаратов. Например, лечение могут проводить в течение 7 дней, после чего делают перерыв на 3 недели. После чего врач онколог редактирует дальнейшие рекомендации пациенту, опираясь на результаты анализов и исследований. Специалист может продолжить курс химиотерапии или отменить его, в зависимости от состояния пациента и особенностей развития онкозаболевания. Такую процедуру могут назначать до 2 лет, если не имеет никаких побочных эффектов и других заболеваний.
Благодаря оперативному вмешательству и курсу облучения, химиотерапии, обычно, можно добиться ремиссии болезни, стабилизировать при этом состояние пациента.
Трансплантация проводится с помощью исключения у донора стволовых клеток костного мозга. Такая процедура безболезненна. С помощью специального аппарата у человека забирают определенное количество крови, которое разделяется на отдельные фракции. Взятая у донора кровь дальше проходит специальную подготовку в лабораторных условиях. С помощью магнитного фильтра, кровь разделяют, выбирая лишь те клетки, которые будут нужны больному. Процесс трансплантации выглядит, как обычная процедура переливания крови.
Эта процедура позволит уничтожить клетки костного мозга, которые производят злокачественные, а также снизит иммунитет, чтобы снизить риск отторжения трансплантированных клеток. Больному, которую проводят такую процедуру, уже не сможет выжить без трансплантации клеток.
Риск, который может возникнуть при этой процедуре, зависит:
- от донора;
- метода проведения трансплантации (общая анестезия при получении клеток из костей таза или применение колониестимулирующих препаратов);
- квалификации работников, которые выполняют данную процедуру.
Лучше быть не запускать болезнь на первых этапах. Когда возникают метастазы рака в лимфоузлах, то лечение может быть достаточно тяжелым, а в некоторых случаях даже невозможным.
Не стоит забывать о том, что исходное состояние больного (т.е. перед началом лечения) влияет на исход заболевания. Чем раньше опухоль обнаружена, тем меньше факторов риска неблагоприятного исхода возникнет. К ним можно отнести массивные лимфоузлы (от 5 см и больше), возраст больше 60 лет, повышенная скорость оседания эритроцитов (СОЭ), экстранодальное расположение опухоли, интоксикационное поражение организма.
Лимфома Ходжкина
Лимфогранулематоз является опухолевым заболеванием лимфоидной ткани и одной из актуальных проблем в современной онкологической практике.
До сих пор этиология ходжкинской лимфомы неизвестна. Существует множество теорий по влиянию факторов риска на вероятность развития лимфомы, однако и они не дают ясной картины причины болезни.
Лимфогранулематоз имеет неуклонно растущее число встречаемости у населения. Частота на сегодняшний день составляет 2,3 случая на 100 тысяч. Пик заболеваемости приходится на возраст 15-25 лет (в этой категории больше женщин), и старше 60 лет.
Эффективность лечения зависит от множества факторов, в том числе от согласованности в работе врач-пациент, диспансер-поликлиника, наличия оригинальных препаратов (а не аналогов), от желания самого пациента к проведению полноценной терапии, и многого другого.
Неходжкинские лимфомы
Представляют собой группу различающихся по цитогенетике, экспрессии генов и белков, иммунологическому фенотипу, степени агрессивности и особенностям течения лимфопролиферативных новообразований.
Лимфомы не всегда происходят из клеток лимфатических узлов, а могут быть экстранодальными, причем абсолютно любой локализации.
Примером может послужить агрессивная форма рака – полиморфный ретикулёз из NKT клеток. Виновником развития этого вида неходжкинской лимфомы является вирус герпеса 4-го типа. Болезнь начинается в пазухах носа, глазницах, глотке. Далее уже могут быть обнаружены метастазы рака в лимфоузлах. На данном этапе лечение возможно только в самых жёстких условиях.
В диагностике опухолей и их метастазов применяется целый арсенал методов. Компьютерная томография для установления точной локализации и иммунная гистохимия для оценки степени пролиферации клеток – дают наиболее важные в оценке прогноза и тактики лечения данные.
Исходя из данных о многообразии форм неходжкинских лимфом, невозможно привести хотя бы приблизительную стратегию лечения.
На выбор терапии влияет множество факторов, но особенно важными являются:
- объем поражения;
- агрессивность течения;
- степень риска;
- иммунофенотип;
- молекулярно-биологическая особенность опухоли.
По данным этих и других показателей делается вывод о назначении протокола лечения, которых на сегодняшний день почти сотня. Разумеется, что врач будет исходить из принципов максимально эффективной, и одновременно щадящей терапии.
К примеру, лечение индолентной B-клеточной лимфомы будет складываться из лучевой терапии, моно- или комбинированной химиотерапии алкилирующими агентами и глюкокортикостероидами (Преднизолон и др.), а при прогрессировании – ещё и производными пуринов. Проводится и высокодозная химиотерапия с дальнейшей пересадкой стволовых клеток.
В случае агрессивных вариантов B-клеточной лимфомы, проводится комбинированная химиотерапия первой линии (3-6 циклов) и лучевая терапия. При отсутствии ремиссии возможно применение химиотерапии второй линии и высокодозная терапия с дальнейшей аутотрансплантацией костного мозга.
При рецидиве, снова назначается химиотерапия, экспериментальная или альтернативная. После чего врач наблюдает за ответной реакцией пациента. В случае резкого ухудшения состояния акцент делается на улучшение качества жизни, а не на продолжение массированного лечения.
Где лучше лечить онкологию?
Онкология является очень опасным заболевание, поэтому при выборе медицинского центра необходимо обратить внимание на следующие факторы:
- наличие современной и хорошей аппаратуры;
- правильное проведение специальных процедур: химической, лучевой, и других видов терапий;
- высокую квалификацию медицинских работников заведения;
- профессиональная и своевременная диагностика болезней;
- использование только качественных препаратов;
- проведение новых и эффективных методов;
- правильное проведение реабилитации.


Химиотерапия при лимфоме — это спасение жизни, которую иными способами сохранить не удастся. Конечно лекарства не обещают 100% радикальности, как операция при раке, но вместе с облучением это единственно возможное и эффективное лечение. Проблема в том, что лимфомы способны изменяться, что обещает рецидивы и независимость от терапии.
- Как проходит химиотерапия при лимфоме
- Химиотерапия при лимфоме Ходжкина
- Химиотерапия при неходжкинских лимфомах
- Возможные осложнения после химиотерапии при лимфоме
- Методы химиотерапии при лимфоме
- Противопоказания к применению химиотерапии при лимфоме
- Препараты, применяемые при химиотерапии
- Рацион и диета при химиотерапии при лимфоме
- Прогнозы для пациентов
Как проходит химиотерапия при лимфоме
При подавляющем большинстве злокачественных лимфом или лимфосарком химиотерапия подаётся на первое-второе и на третье, при некоторых клеточных вариантах после первой линии дополняется лучевой терапией в скромных, по сравнению с раковыми заболеваниями, дозах.
Роль облучения — поддержка достигнутого результата и дополнение его позитивом. Сегодня полностью отошли от радикальной программы лучевой терапии, несколько десятилетий доминировавшей при лимфоме Ходжкина, отказавшись от профилактического облучения не поражённых опухоль лимфоколлекторов. Из профилактического — только введение цитостатиков в спинномозговую жидкость, уменьшающее вероятность злокачественного поражения головного мозга и его оболочек.
Сегодняшнее противоопухолевое лечение лимфом отобрало самые результативные комбинации, учитывающие иммуногистохимические характеристики злокачественных клеток. Для каждого прогностического варианта определено оптимальное число циклов, возраст больного и его хронические болезни уже не противопоказание для активного лечения, потому что созданы лекарственные комбинации на все случаи болезни, тем не менее, ограничения по применению цитостатиков включены в стандарты.
Химиотерапия используется всегда, когда в ней есть необходимость и нет абсолютных противопоказаний. На выборе схемы лечения сказываются не только клеточный вариант и прогностические характеристики лимфомы, распространённость болезни по данным ПЭТ-КТ, но и исходное состояние здоровья пациента.
Химиотерапия при лимфоме Ходжкина
Лимфома Ходжкина (или по-старому лимфогранулематоз) — одно из самых благоприятно текущих заболеваний лимфоидной ткани. Ходжкинская лимфома входит в ограниченное число болезней, излечиваемых только одной химиотерапией, но важная ремарка: диагностированная на ранней стадии и с признаками благоприятного течения. Прогноз ожидается малооблачным при небольшом поражении — не более двух групп лимфоузлов в верхней или нижней половине тела — по одну сторону диафрагмы, лучше без вовлечения лимфоузлов средостения и с исходными нормальными клиническими и биохимическими анализами крови.
Каждого пациента после первичного обследования относят к трём основным группам, по стандартам которых будет проводится противоопухолевое лечение, во всех случаях на первом этапе проводится химиотерапия, затем результат закрепляется трёхнедельным облучением зон поражения.
Число курсов зависит от исходного поражения и прогноза, в лучшем случае при лимфоме I-II стадии предложат от 2 до 4 циклов четырёхкомпонентной схемы. При том же объёме поражения, но худших прогностических факторах, потребуется 4-6 курсов. Для повышения результативности первых два цикла у сохранных молодых пациентов заменяют на 6-компонентную схему, затем проводят 2 стандартных ABVD и можно уходить на облучение.
Распространенные стадии не обещают хорошего прогноза, поэтому химиотерапия длительная и многокомпонентная. Причём сколько циклов потребуется — 6 или 8, определят по результатам первых 4 циклов: если опухоль полностью ушла и ПЭТ это покажет — предложат пройти только два цикла, затем назначается трёх-четырёхнедельное облучение. При незначительном эффекте — 8 циклов и лучевая терапия на пораженные лимфоузлы.
У пожилых пациентов, в популяции это каждый третий больной, лечение выбирается с учетом хронической патологии. Так у курильщиков и страдающих болезнями легких в комбинацию не включают блеомицетин, накапливающийся в легочной ткани и вызывающий специфическое воспаление. При сердечной патологии кардиотоксичные антрациклины заменяют на другие противоопухолевые антибиотики.
Лимфома Ходжкина чувствительна к множеству цитостатиков, что позволяет найти оптимальную комбинацию, вплоть до применения одного-единственного цитостатика.
Химиотерапия при неходжкинских лимфомах
Неходжкинские лимфомы представлены множеством морфологических видов, каждый с особенностями течения и лечения. Разберём самые частые варианты заболевания.
Самая благоприятная по течению фолликулярная лимфома встречается в каждом пятом случае злокачественных лимфом у взрослых. В самом начале процесса без явных признаков активности не всегда требуется безотлагательная химиотерапия, у некоторых пациентов прогноз настолько неплох, что можно ограничиться облучением лимфомы либо длительным наблюдением с тщательным мониторингом анализов и регулярным обследованием каждые 3 месяца.
Сразу ХТ начинается только при вовлечении в злокачественный процесс любых органов или при поражении не менее трёх лимфатических зон с размером узлов более 3 сантиметров, или при лихорадке с потливостью, или при плохих показателях крови.
Оптимальный режим — R-CHOP, сочетающий сравнительно мягкие в плане осложнений алкилирующие цитостатики с иммунным препаратом ритуксимабом. Это моноклональное антитело при начальном и прогностически благоприятном процессе используют без ХТ — в монорежиме внутривенно, подкожно каждые 8 недель в течение двух лет применяют для поддержания позитивного результата после завершения циклов.
Вопрос о высокодозной химиотерапии с пересадкой костного мозга ставится при рецидиве или переходе фолликулярной лимфомы в более агрессивную, вероятность чего возрастает с течением времени, так через 10 лет переход в диффузную В-крупноклеточную лимфому отмечается у каждого шестого, а через 15 лет — у каждого второго. По истечении полутора десятилетий после первичного лечения частота рецидивов лимфомы сходит на нет.
У каждого третьего первичного пациента с лимфомой выявляют диффузную крупноклеточную В-клеточную лимфому (ДВКЛ), ежегодно её диагностируют только у пяти из каждых ста тысяч россиян.

Стандарт химиотерапии при неагрессивном варианте ДВКЛ, позволяющий 80% больных прожить дольше пятилетки — 6 циклов комбинации CHOP с ритуксимабом. При полном уничтожении новообразований в результате лекарственного воздействия, возможно подключение лучевой терапии в обычной для лимфом дозе 30-36 грей, а при остаточных опухолевых очагах дозу облучения доводят до 36-40 Грей.
Аналогичная комбинация цитостатиков с иммунным препаратом неважно работает при агрессивном варианте и большом распространении, поэтому химиотерапию усугубляют уменьшением интервалов между циклами R-CHOP или переводят на многокомпонентные комбинации.
При неблагоприятном прогнозе всем пациентам уже на первой линии проводится профилактика поражения головного мозга — введение высоких дох метотрексата и цитарабина в спинномозговую жидкость.
После завершения основной программы поддерживающая химиотерапия не проводится из-за не столь хорошей чувствительности опухолевых клеток к лекарствам. При рецидиве крупноклеточной лимфомы прибегают к комбинациям 2-й линии и трансплантации стволовых клеток крови после высокодозной ХТ.
Периферическая Т-клеточная лимфома — каждый четвёртый случай злокачественного поражения Т-клеточного ростка кроветворения или каждая шестая лимфома. Морфологически группа представлена разнообразными клеточными вариантами. Агрессивно текущее заболевание, как правило, вовлекает не только лимфатические узлы, но и другие органы.
В первой линии используют традиционный CHOP, но в редких случаях удается отказаться от ВДХТ с аутологичной трансплантацией клеток костного мозга. Некоторые виды лимфом благоприятного течения отзываются на облучение и L-аспарагиназу. При отсутствии эффекта лечение подбирается индивидуально.
Лимфомы одного названия предполагают множество различных морфологических вариантов заболевания, внутри групп клетки различаются ИГХ-характеристиками, предполагающими возможности индивидуального подбора противоопухолевого лечения, поэтому специалисты нашей Клиники могут предложить не один-два стандарта, а десятки комбинаций ХТ.
Возможные осложнения после химиотерапии при лимфоме
Тошноту и рвоту уменьшает включение в схемы глюкокортикоидных гормонов. Многокомпонентные комбинации обязательно предваряются введением антиэметиков , приём которых продолжается после завершения терапии.
Для профилактики нейтропении через сутки после цитостатика вводят стимулятор КСФ, что помогает не снижать следующую дозу и не увеличивать интервал без лечения.
Повреждение миокарда характерно для антрациклинов, облучение средостения дополнительно увеличивает кардиотоксичность. Осложнение может проявиться через несколько лет, профилактика не разработана, поэтому у страдающих сердечно-сосудистыми болезнями из схемы исключают антрациклины.
При чувствительности к ХТ и большом распространении лимфомы возможно развитие синдрома лизиса опухоли (СЛО), когда вышедшие из погибшие опухолевых клеток вещества отравляют организм, приводя к почечной недостаточности и гиперкалиемии с фатальной аритмией. Индуцированный лекарствами распад опухоли научились предотвращать.
При пересадке донорского костного мозга высока вероятность отторжения — реакция трансплантат-против-хозяина. При высокодозной терапии отдается предпочтение пересадке собственных клеток даже при угрозе рецидива лимфомы. Рецидив можно вылечить, отторжение трансплантата фатально для пациента.
Методы химиотерапии при лимфоме
Пациент получает лечение всеми способами, кроме внутримышечных инъекций из-за раздражающего действия цитостатиков и опасности осложнений со стороны мягких тканей.
Большинство цитостатиков вводится внутривенно струйно — болюсно или капельно.
Частый компонент схем — преднизолон принимается в таблетках, цитостатик прокарбазин — в капсулах.

Ритуксимаб применяется внутривенно и подкожно, подкожные инъекции удобны для поддержки.
Профилактика нейролейкемии проводится интратекально — введением препарата в спинномозговой канал, потому что организм специальным гематоэнцефалическим барьером защищает головной мозг от проникновения лекарства в крови.
Противопоказания к применению химиотерапии при лимфоме
Абсолютные противопоказания к ХТ при лимфомах — только декомпенсация других хронических заболеваний с существенным снижением функции органов.
Препараты, применяемые при химиотерапии
При лимфомах применяется почти два с половиной десятка противоопухолевых препаратов, из которых составляют несколько десятков схем. Можно пересчитать по пальцам цитостатики, не используемые при лимфосаркомах.
Рацион и диета при химиотерапии при лимфоме
Прогнозы для пациентов
Эффективность лечения оценивают в середине программы и по её окончании, причём оптимально ПЭТ-КТ обследование.
На прогнозе сказывается очень много факторов, для каждого заболевания разработан свой прогностический индекс, поэтому и в диагнозе обязательно указывают прогностическую группу.
В конечном итоге перспективы на дальнейшую жизнь определяет результат химиотерапии и скорость развития рецидива.
Каждому хочется знать — что ждёт впереди, при злокачественном процессе важнее — как лечат и где лечат, потому что без современного обследования невозможно подобрать оптимальную терапию. В Европейской клинике всё проходит на очень высоком уровне, вы можете лично убедиться в этом.
В экспериментальных исследованиях установлено, что некоторая доза цитотоксического препарата вызывает гибель определенной части клеточной популяции, а не определенного количества клеток. Рисунок схематически иллюстрирует эту гипотезу гибели фракции клеток. Например, введение однократной дозы препарата может привести к гибели 99% клеточной популяции, причем эта же доля клеток погибнет независимо от общего их количества: оно может быть, например, 10 12 (тогда останется 10 10 клеток) или 10 4 (останется 10 клеток).
Если это положение справедливо для солидных опухолей человека, то приходим к выводу о том, что для небольших опухолей более эффективной оказывается схема с применением меньшего количества циклов лечения, чем для более крупных опухолей. Поскольку в этом случае препарат назначается ограниченное количество раз, вероятность развития к нему лекарственной устойчивости снижается. Прием препарата может быть спланирован таким образом, чтобы обеспечить максимальный цитотоксический эффект.
Последний зависит от скорости репопуляции клеток опухоли и восстановления тканей здоровых органов, наиболее сильно поврежденных цитотоксическим препаратом. У человека обычно к этим органам относятся кишечник и костный мозг. По сравнению с большинством опухолей, они быстро регенерируют. По этой причине химиотерапевтические препараты назначают в ритмическом режиме через определенные интервалы, необходимые для протекания восстановительных процессов.
Такой подход имеет некоторые теоретические и практические ограничения.
Справедливость гипотезы гибели фракции клеток оценивалась на экспериментальной модели гомогенных быстрорастущих опухолей, и экстраполяция ее положений на медленнорастущие опухоли человека выявляет очевидные недостатки.
Предполагается, что для экспериментальных опухолей, растущих в виде асцита или развивающихся в жидкой среде организма (например, лейкозы), противоопухолевые препараты распределяются равномерно. Очевидно, что этого не происходит в случаях плохо васкуляризованных солидных опухолей, и кинетика гибели клеток при этом описывается гораздо более сложной функцией, чем уравнение первого порядка, справедливое для экспериментальных систем.
При повторных курсах химиотерапии скорость репопуляции опухоли может изменяться. Хотя для экспериментальных асцитных моделей этого не наблюдается, в случае солидных опухолей ситуация меняется.
Степень восстановления здоровых тканей, например, если судить по данным анализа крови, может оказаться полной после первых нескольких циклов лечения. Однако, по мере продолжения лечения, восстановление замедляется, что накладывает ограничения на дозы препарата, назначаемые в последующих циклах.
Существует крайне ограниченный клинический материал о характере зависимости доза-эффект для конкретных цитотоксических агентов и определенного типа опухолей. Клиническая фармакология химиотерапевтических препаратов крайне сложна и отличается от препарата к препарату. Существуют клинические данные, согласно которым противоопухолевый эффект препарата проявляется только при его назначении в максимальной дозе, и на практике различие между неэффективной и максимально-переносимой дозой может быть незначительным.
Тем не менее, несмотря на высказанные соображения, в химиотерапии широко используется ритмический режим назначения препаратов через определенные интервалы времени. Этот режим был разработан на основании экспериментальных исследований и клинических испытаний.
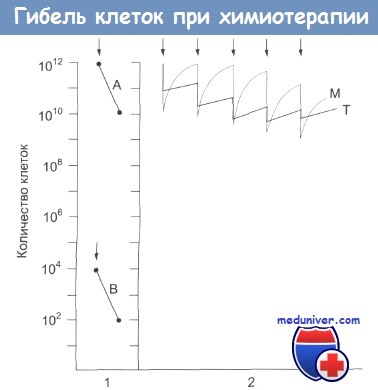
Фракционированная гибель клеток.
В первой части рисунка обозначена определенная доза препарата, вызывающая гибель 99% клеток как в случае А, так и в случае В.
В случае А количество клеток в опухоли снижается с 10 12 до 10 10 , а в случаев с 10 4 до 10 2 . Во второй части рисунка кривая Т иллюстрирует эффект повторных введений препарата (показаны стрелкой) на рост опухоли.
С введением каждой повторной дозы препарата гибель клеток снижается, что указывает на развитие у них устойчивости к препарату.
Кривая М иллюстрирует действие препарата на клетки-предшественницы в костном мозге. Эти клетки быстро восстанавливаются, однако по мере введения повторных доз препарата темпы восстановления снижаются и появляются клинические признаки подавления миелопоэза.
Даже в случаях таких чувствительных опухолей, как болезнь Ходжкина, назначение одного препарата редко приводит к излечению. Поэтому логично попытаться увеличить эффективность лекарственных средств и продолжительность их действия, одновременно назначая несколько препаратов. Цель применения рецептур заключается в попытке преодолеть возможно больше механизмов, ответственных за устойчивость опухоли к цитотоксическим агентам. Очень скоро такой подход оказался эффективным в лечении детских лейкозов и лимфом у взрослых, а также стал применяться для лечения больных с другими опухолями.
При разработке режима комбинированной химиотерапии необходимо соблюдать следующие общие принципы.
• Следует назначать только те препараты, которые оказываются эффективными при изолированном применении.
• По возможности необходимо назначать препараты, токсичность которых не перекрывается.
• Следует применять ритмический режим назначения препаратов с тем, чтобы обеспечить протекание восстановительных процессов в кишечнике и костном мозге.
• В идеале, каждое лекарственное средство должно назначаться в оптимальной дозе и по оптимальной схеме.
• По возможности, следует назначать препараты, характеризующиеся синергическим действием (правда, на практике такие агенты неизвестны).
• Если возможно, необходимо применять препараты, влияющие на различные фазы клеточного цикла.
• Большинство схем лечения разработаны эмпирически с учетом опыта врача.
Повышение эффективности, которое достигается при использовании рецептур, объясняется несколькими причинами.
• Опухоль подвергается воздействию нескольких препаратов, и вероятность развития лекарственной устойчивости снижается.
• Максимальный цитотоксический эффект достигается без увеличения токсичности.
• Существует меньшая возможность раннего появления популяции клеток, устойчивых к препаратам.
Это заболевание онкологической природы, которое поражает лимфатическую ткань и внутренние органы [3] .
Лимфатическая система человека сформирована из сети сосудов, которые пронизывают все внутренние органы и по этой сети течет лимфа. Лимфатическая система выполняет следующие функции:
- транспортную - транспортирует питательные вещества из кишечника к органам, а также осуществляет дренаж тканей;
- иммунную – лимфатические узла синтезируют лимфоциты, которые активно борются с бактериями и вирусами;
- барьерную – в лимфатических узлах задерживаются патогенные частицы в виде отмерших клеток и бактерий;
- кроветворную – в ней синтезируются лимфоциты.
При лимфоме лимфатические клетки начинают патологически активно делиться и формируют опухоли.
На этот вид раковых опухолей в мировой практике приходится около 5% случаев. В последнее десятилетий количество диагностируемых случаев этой патологии неуклонно растет.
Лимфома может проявляться в виде лимфогранулематоза, болезни Ходжкина или неходжкинской лимфомы.
Пока не установлен ни один конкретный фактор, который провоцирует развитие лимфомы. Однако существуют определенные условия, которые благотворно влияют на развитие данной патологии, к ним относятся:
- 1 Бактериальные инфекции. Достаточно часто лимфому сопровождают бактерии. К примеру, при лимфоме желудка у пациента нередко диагностируют и хеликобактер пилори, это единственный микроорганизм, который не гибнет в соляной кислоте желудка;
- 2 Употребление иммунодепрессантов. Подобные препараты рекомендуют больным с аутоиммунными патологиями для того, чтобы замедлить функционирование иммунной системы;
- 3 Вирусные заболевания могут провоцировать лимфому. Например, вирус Эпштейна-Барр помимо лимфомы может вызвать рассеянный склероз и гепатит;
- 4 Возраст и пол. Наиболее подвержена данной патологии возрастная категория людей от 55 до 60 лет или до 35 лет. Причем гораздо чаще лимфомой болеют мужчины;
- 5 Химический фактор предполагает негативное воздействие химических веществ на организм человека на производстве или в быту. В зону риска попадают рабочие, которые имеют дело с пестицидами, лаками, красками, растворителями и другими подобными канцерогенами.
Спровоцировать лимфому также может повышенное содержание в крови вируса герпеса 8 типа и цитомегаловирусов. Помимо этого, имеет значение и наследственная предрасположенность, клеточные мутации и повышенное содержание лейкоцитов в крови.
Лимфома может проявляться как индивидуальными симптомами, так и признаками, характерными для других патологий. Поэтому особам, входящим в зону риска необходимо знать отличительные признаки лимфомы:
- увеличенные лимфатические узлы – этот признак возникает на самых ранних стадиях заболевания в результате патологического деления клеток. У 90% пациентов с лимфомой увеличены лимфатические узлы. В первую очередь увеличиваются лимфоузлы в области затылка и шеи. Достаточно часто опухают лимфатические узлы в паху, в районе ключиц и подмышек. Лимфоузлы увеличиваются настолько, что это отчетливо видно визуально, если они находятся рядом, то они могут соединяться и образовать большие опухоли. При умеренной пальпации опухолей, больной не испытывает болезненных ощущений, однако, иногда лимфоузлы могут становиться болезненными после употребления алкогольных напитков;
- повышение температуры сопровождает все формы лимфомы. Субфебрильная температура может держаться в течение нескольких месяцев. Если болезнь прогрессирует и поражаются внутренние органы, то температура может повышаться до 39 градусов;
- ночная потливость характерна для больных синдромом Ходжкина, при этом пот имеет запаха и цвета;
- болевой синдром при лимфоме, как правило, проявляется головными болями, если лимфома затронула головной мозг. При поражении органов брюшной полости или грудной клетки, боль, соответственно локализируется в области живота и груди;
- зуд кожи считается характерным признаком лимфомы. Он может быть локальным или по всему телу, часто больного беспокоит зуд в нижней половине туловища, в ночное время зуд становится невыносимым;
- чувство слабости характерно для начальной стадии заболевания и появляется безосновательно. Также может наблюдаться апатия и повышенная сонливость.
К специфическим симптомам патологии можно отнести отеки, которые появляются из-за нарушенного кровообращения. При лимфоме в области грудной клетки пациента беспокоит сухой выматывающий кашель. Диарея, запор и тошнота являются следствием лимфомы в области брюшной полости.
Увеличение лимфоузлов может спровоцировать обструкцию дыхательных путей, ЖКТ, пищевода. Интенсивность сдавливания зависит от величины опухоли. В результате чего могут начаться кровотечения, перфорации, а обструкция желчных путей может спровоцировать желтуху.
Поражения ЦНС могут начаться в результате сдавливания головного мозга. При этом возможно развитие менингита, энцефалопатии, полимиозита и невропатии. При поражении легких развивается пневмония. Если лимфома затронула кожные покровы, то помимо зуда может возникнуть крапивница, дерматомиозит и эритема.
Изменения в крови могут обернуться анемией, в редких случаях тромбоцитозом. К самым распространенным метаболическим патологиям при лимфоме относят гиперкальциемию и гиперурикемию.
Причины развития лимфомы до сегодняшнего дня так и не выявлены. Поэтому в профилактических целях следует укреплять иммунитет и не реже раза в год проходить медицинские осмотры. Для того, чтобы свести к минимуму риск развития опухолей в лимфатических узлах следует придерживаться следующих рекомендаций:
- 1 свести к минимуму контакт с токсическими веществами;
- 2 во время полового акта со случайным партнером использовать барьерные контрацептивы;
- 3 не менее 2-х раз в год проводить витаминотерапию;
- 4 не забывать о регулярных умеренных физических нагрузках;
- 5 не использовать чужие полотенца, бритвы и зубные щетки.
Терапия лимфомы проводится после диагностики и уточнения диагноза и зависит от тяжести патологии. В первую очередь необходимо вылечить вирусные заболевания, если они стали первопричиной развития болезни.
Основным и самым эффективным методом лечения является лучевая терапия, химиотерапия, в некоторых случаях трансплантация костного мозга. Хирургическое вмешательство используют редко, только в тех случаях, когда большая опухоль мешает работе внутренних органов.
Правильно назначенные химиосредства оказывают противорецидивный эффект. Химиопрепараты пьют достаточно долго, от 3 до 5 месяцев. Для лечения агрессивных форм лимфом используют высокодозные химиопрепараты и трансплантацию кроветворных стволовых клеток.
Полезные продукты при лимфоме
Интенсивное использование химических препаратов при лечении лимфомы оказывает токсическое воздействие на организм пациента. Поэтом питание больного должно быть максимально сбалансированным, направлено на повышение иммунитета и восстановление организма. Поэтому рацион пациента должен состоять из следующих продуктов:
- всех видов каш;
- свежеотжатых соков;
- морских продуктов;
- нежирных кисломолочных продуктов;
- сока клюквы, разбавленного водой;
- красного сухого вина в небольших количествах;
- парного нежирного мяса птицы;
- зеленых овощей;
- зеленого чая;
- оранжево-красных фруктов и овощей.
- 1 пить как можно чаще ромашковый чай;
- 2 1 ст.л. сока чистотела развести в 100 г любого молочного продукта и употреблять перед сном [1] ;
- 3 6-7 свежесрезанных грибов саркосомы, которые растут на мхах, промыть, обработать спиртом, шприцем вытянуть слизь, принимать ежедневно по 1/3 ч.л.;
- 4 заготовить траву чистотела в период цветения, промыть, измельчить и плотно сложить в емкость. Через 4-5 дней отжать сок, добавить 0,5 л водки, принимать дважды в день по 1. ч.л.;
- 5 приготовить спиртовую настойку из зеленой кожуры неспелых грецких орехов, принимать ее 1 раз в день по 1 ст.л. [2] ;
- 6 3 ст.л. почек березы в течение 20 мин. кипятят в стакане воды, принимают по большой ложке перед едой;
- 7 принимать чай из березового гриба.
Агрессивная химиотерапия не только останавливает рост раковых структур, но и угнетает здоровые клетки. Правильное питание существенно облегчает побочные явления терапии. Для того, чтобы помочь организму справиться с недугом из рациона следует исключить вредные и тяжелые продукты:
- ограничить потребление сахара, его можно заменить медом;
- магазинные колбасы и копчености;
- полуфабрикаты;
- острые соусы и специи;
- алкоголь;
- сыры с плесенью;
- фаст-фуд;
- покупные кондитерские изделия;
- красное мясо;
- жирные сорта рыбы;
- консервированные продукты.
Запрещено использование любых материалов без нашего предварительного письменного согласия.
Администрация не несет ответственности за попытку применения любого рецепта, совета или диеты, а также не гарантирует, что указанная информация поможет и не навредит лично Вам. Будьте благоразумны и всегда консультируйтесь с соответствующим врачом!
Читайте также:

