Транспупиллярная термотерапия при меланомах хориоидеи
При анализе результатов лечения выявлено, что средняя проминенция опухоли до ТТТ была статистически значимо меньше у больных, которым было достаточно проведения 1 этапа ТТТ по сравнению с больными, у которых не получено желаемого эффекта от ТТТ (p

Рисунок 4. Динамика изменения средней проминенции меланомы хориоидеи после проведения повторной брахитерапии
Повторная БТ проведена успешно у 26 больных (86,7%) при сроке наблюдения от 1,5 до 11 лет (в среднем 4,5±1,1 года). На момент последнего обследования у 8 больных (26,7 %) сформировался плоский хориоретинальный рубец с полной резорбцией опухоли. В этой группе выполнена 1 энуклеация через 2 года после повторной БТ в связи с продолженным ростом опухоли и развитием неоваскулярной глаукомы. Одному больному из-за неэффективности повторной БТ спустя 14 месяцев проведена протонотерапия с положительным результатом. Двум больным из этой группы в связи с продолженным ростом опухоли после второго сеанса БТ проведено дополнительно лазерное лечение: ТТТ (через 1,5 года после повторной БТ) и разрушающая лазеркоагуляция (спустя 10 лет после повторной БТ).
Осложнения повторной брахитерапии: При проведении повторной БТ возникает достаточно много осложнений, связанных с лучевой нагрузкой на глазное яблоко: постлучевая атрофия ДЗН сформировалась после первой БТ у 15 больных (50%), у 2 больных (6,7%) возникла склеромаляция, потребовавшая выполнения склеропластики. Также отмечено развитие постлучевой катаракты (4 больных, 13,3 %), неоваскулярной глаукомы (1 больной, 3,3%), помутнения стекловидного тела (3,3%), гемофтальма (3,3 %), цилиохориоидальнаой отслойки (3,3%). Лечение проведено без осложнений у 8 больных (26,7%).
Острота зрения после проведенного лечения на момент последнего осмотра составила от 0 до 0,5 (средняя 0,05, 95%ДИ 0,01-0,08). Средняя острота зрения больного глаза с максимальной коррекцией после повторной БТ снизилась в 4 раза, при этом острота зрения снижается не только при центральной, но и при периферической локализации МХ. Средняя проминенция опухоли на момент последнего обследования больных составила 1,1 мм (95% ДИ=0,9-1,3).
У 5 больных выявлены отдаленные метастазы в печень и легкие спустя 4 -10 лет от момента постановки диагноза.
Таким образом, проведение повторной БТ остаточных МХ позволило достичь положительного результата у 86,7% больных при сроке наблюдения от 1,5 до 11 лет. У 6 из 8 больных, у которых опухоль локализовалась в 1 ДД от ДЗН и ближе, повторная БТ проведена успешно. У 2 больных с юкстапапиллярной локализацией остаточной опухоли повторная БТ была неэффективной: 1 глаз энуклеировали и 1 больному дополнительно провели ТТТ. Полной резорбции опухоли удалось достичь в 26,7 % случаев, в том числе у 3 больных с юкстапапиллярной локализацией остаточной опухоли. При проведении повторной БТ возникает достаточно много осложнений (73,3%), связанных с лучевой нагрузкой на глазное яблоко. Развитие серьезных необратимых осложнений ведет за собой значительное снижение остроты зрения.
Сравнительный анализ результатов транспупиллярной термотерапии и повторной брахитерапии в лечении остаточных меланом хориоидеи
Мы сравнили результаты лечения остаточных опухолей больных из 1 и 3 группы. При лечении больных 1 группы с помощью ТТТ нами достигнут положительный результат в 82,1% случаев при сроке наблюдения от 2 до 3 лет, а при применении повторной БТ – в 86,7% при сроке наблюдения от 1,5 до 11 лет. На момент трехлетнего наблюдения за больными из 3 группы, эффективность повторной БТ составила 90%, что статистически не отличается от эффективности ТТТ (p>0,05). Нами выявлено, что при проведении повторной БТ осложнения встречаются чаще (в 83,3%) по сравнению с ТТТ (в 12,8%), их характер необратим и ведет к более выраженному снижению остроты зрения (p
Сравнительный анализ применения транспупиллярной термотерапии первичных и остаточных меланом хориоидеи
Для определения особенностей влияния ТТТ на первичную (не леченную) и остаточную (ранее облученную) опухоль, мы сравнили результаты лечения 1 и 2 групп больных. По нашим данным эффективность метода достоверно одинакова для первичных и остаточных МХ, включая эффективность лечения МХ юкстапапиллярной локализации (р 0,05). Одного сеанса ТТТ было достаточно для лечения достоверно большего количества больных 1 группы (59%) по сравнению со 2 группой (25%), (р 0,05). Восстановительный период после проведенного лечения одинаков для этих групп больных и составляет около 1 месяца. В обеих группах средняя острота зрения с максимальной коррекцией после проведения лечения снизилась: в 1,7 раз у больных 1 группы и в 2 раза у больных 2 группы (p>0,05).
ВЫВОДЫ
- Необходимость лечения остаточных МХ определяется совокупностью параметров клинической и эхографической картины, свидетельствующих об отрицательной динамике, и данными специальных инструментальных методов исследования: флюоресцентной ангиографии и высокочастотного дуплексного сканирования, подтверждающих наличие собственных сосудов опухолевой ткани. Сохранение кровотока в сосудах опухоли спустя 3 месяца после проведения ТТТ и 1,5-2 года после проведения БТ является признаком жизнеспособности опухоли и показанием к проведению дополнительного лечения остаточной опухоли.
- ТТТ является методом выбора в лечении остаточных МХ с проминенцией 3,5 мм, расположенных центрально или на средней периферии глазного дна. ТТТ позволяет достичь положительного эффекта в 82,1% случаев и полной резорбции остаточной опухоли у 66,7 % больных при сроке наблюдения до 3 лет.
- Осложнения после ТТТ остаточных МХ встречаются в 12,8% случаев, большинство из них (10,2%) носят транзиторный характер и могут купироваться терапевтическими методами. Острота зрения после ТТТ снижается при центральной локализации опухоли и остается неизменной при периферической локализации.
- ТТТ и повторная БТ остаточных МХ имеют одинаковую эффективность при сравнении результатов лечения за 3 года наблюдения (p Pages: | 1 | 2 |
При анализе результатов лечения выявлено, что средняя проминенция опухоли до ТТТ была статистически значимо меньше у больных, которым было достаточно проведения 1 этапа ТТТ по сравнению с больными, у которых не получено желаемого эффекта от ТТТ (p

Рисунок 4. Динамика изменения средней проминенции меланомы хориоидеи после проведения повторной брахитерапии
Повторная БТ проведена успешно у 26 больных (86,7%) при сроке наблюдения от 1,5 до 11 лет (в среднем 4,5±1,1 года). На момент последнего обследования у 8 больных (26,7 %) сформировался плоский хориоретинальный рубец с полной резорбцией опухоли. В этой группе выполнена 1 энуклеация через 2 года после повторной БТ в связи с продолженным ростом опухоли и развитием неоваскулярной глаукомы. Одному больному из-за неэффективности повторной БТ спустя 14 месяцев проведена протонотерапия с положительным результатом. Двум больным из этой группы в связи с продолженным ростом опухоли после второго сеанса БТ проведено дополнительно лазерное лечение: ТТТ (через 1,5 года после повторной БТ) и разрушающая лазеркоагуляция (спустя 10 лет после повторной БТ).
Осложнения повторной брахитерапии: При проведении повторной БТ возникает достаточно много осложнений, связанных с лучевой нагрузкой на глазное яблоко: постлучевая атрофия ДЗН сформировалась после первой БТ у 15 больных (50%), у 2 больных (6,7%) возникла склеромаляция, потребовавшая выполнения склеропластики. Также отмечено развитие постлучевой катаракты (4 больных, 13,3 %), неоваскулярной глаукомы (1 больной, 3,3%), помутнения стекловидного тела (3,3%), гемофтальма (3,3 %), цилиохориоидальнаой отслойки (3,3%). Лечение проведено без осложнений у 8 больных (26,7%).
Острота зрения после проведенного лечения на момент последнего осмотра составила от 0 до 0,5 (средняя 0,05, 95%ДИ 0,01-0,08). Средняя острота зрения больного глаза с максимальной коррекцией после повторной БТ снизилась в 4 раза, при этом острота зрения снижается не только при центральной, но и при периферической локализации МХ. Средняя проминенция опухоли на момент последнего обследования больных составила 1,1 мм (95% ДИ=0,9-1,3).
У 5 больных выявлены отдаленные метастазы в печень и легкие спустя 4 -10 лет от момента постановки диагноза.
Таким образом, проведение повторной БТ остаточных МХ позволило достичь положительного результата у 86,7% больных при сроке наблюдения от 1,5 до 11 лет. У 6 из 8 больных, у которых опухоль локализовалась в 1 ДД от ДЗН и ближе, повторная БТ проведена успешно. У 2 больных с юкстапапиллярной локализацией остаточной опухоли повторная БТ была неэффективной: 1 глаз энуклеировали и 1 больному дополнительно провели ТТТ. Полной резорбции опухоли удалось достичь в 26,7 % случаев, в том числе у 3 больных с юкстапапиллярной локализацией остаточной опухоли. При проведении повторной БТ возникает достаточно много осложнений (73,3%), связанных с лучевой нагрузкой на глазное яблоко. Развитие серьезных необратимых осложнений ведет за собой значительное снижение остроты зрения.
Сравнительный анализ результатов транспупиллярной термотерапии и повторной брахитерапии в лечении остаточных меланом хориоидеи
Мы сравнили результаты лечения остаточных опухолей больных из 1 и 3 группы. При лечении больных 1 группы с помощью ТТТ нами достигнут положительный результат в 82,1% случаев при сроке наблюдения от 2 до 3 лет, а при применении повторной БТ – в 86,7% при сроке наблюдения от 1,5 до 11 лет. На момент трехлетнего наблюдения за больными из 3 группы, эффективность повторной БТ составила 90%, что статистически не отличается от эффективности ТТТ (p>0,05). Нами выявлено, что при проведении повторной БТ осложнения встречаются чаще (в 83,3%) по сравнению с ТТТ (в 12,8%), их характер необратим и ведет к более выраженному снижению остроты зрения (p
Сравнительный анализ применения транспупиллярной термотерапии первичных и остаточных меланом хориоидеи
Для определения особенностей влияния ТТТ на первичную (не леченную) и остаточную (ранее облученную) опухоль, мы сравнили результаты лечения 1 и 2 групп больных. По нашим данным эффективность метода достоверно одинакова для первичных и остаточных МХ, включая эффективность лечения МХ юкстапапиллярной локализации (р 0,05). Одного сеанса ТТТ было достаточно для лечения достоверно большего количества больных 1 группы (59%) по сравнению со 2 группой (25%), (р 0,05). Восстановительный период после проведенного лечения одинаков для этих групп больных и составляет около 1 месяца. В обеих группах средняя острота зрения с максимальной коррекцией после проведения лечения снизилась: в 1,7 раз у больных 1 группы и в 2 раза у больных 2 группы (p>0,05).
ВЫВОДЫ
- Необходимость лечения остаточных МХ определяется совокупностью параметров клинической и эхографической картины, свидетельствующих об отрицательной динамике, и данными специальных инструментальных методов исследования: флюоресцентной ангиографии и высокочастотного дуплексного сканирования, подтверждающих наличие собственных сосудов опухолевой ткани. Сохранение кровотока в сосудах опухоли спустя 3 месяца после проведения ТТТ и 1,5-2 года после проведения БТ является признаком жизнеспособности опухоли и показанием к проведению дополнительного лечения остаточной опухоли.
- ТТТ является методом выбора в лечении остаточных МХ с проминенцией 3,5 мм, расположенных центрально или на средней периферии глазного дна. ТТТ позволяет достичь положительного эффекта в 82,1% случаев и полной резорбции остаточной опухоли у 66,7 % больных при сроке наблюдения до 3 лет.
- Осложнения после ТТТ остаточных МХ встречаются в 12,8% случаев, большинство из них (10,2%) носят транзиторный характер и могут купироваться терапевтическими методами. Острота зрения после ТТТ снижается при центральной локализации опухоли и остается неизменной при периферической локализации.
- ТТТ и повторная БТ остаточных МХ имеют одинаковую эффективность при сравнении результатов лечения за 3 года наблюдения (p Pages: | 1 | 2 |
Меланома хориоидеи представляет собой одну из самых агрессивных злокачественных опухолей человека [2]. Частота выявления меланомы хориоидеи по различным регионам мира составляет 7–12 человек на 1 млн населения ежегодно. А пятилетняя выживаемость больных после проведенного лечения составляет 48–60 % [1; 4].
Развитие инструментальных и высокотехнологичных лучевых методов диагностики (биомикроофтальмоскопия, флуоресцентная ангиография, ультразвуковое цветное доплеровское картирование, МРТ, КТ) в офтальмологии позволяют выявлять злокачественные новообразования глаза на ранних стадиях [3]. Благодаря проведению профилактических осмотров, диспансеризации населения, улучшению качества диагностики изменился контингент первично выявленных больных, что создает условия для формирования органосохраняющего лечения опухолей глаза. С этой целью при меланоме хориоидеи используется способ транспупиллярной термотерапии. Однако опыт такого лечения пока еще сравнительно небольшой, и объем знаний, полученных в результате клинического наблюдения за этой категорией больных, пока нельзя считать достаточным.
Цель исследования
В этой статье мы представляем собственный опыт наблюдения пациентки после проведения органосохраняющего лечения по поводу меланобластомы хориоидеи глаза.
Материалы и методы исследования
При проведении фотодинамической терапии вводился внутривенно болюсно фотосенсибилизирующий препарат Радахлорин 3 мг/кг и проводилось облучение лазерным излучением с использованием лазерного фотодинамического комплекса Лидия, построенного на базе лазерного аппарата АЛХТ-ЭПОМЕД с длиной волны 662 нм. Транспупиллярное воздействие осуществляли лазерным излучением с длиной волны 810 нм с экспозицией времени 60 сек в каждой точке воздействия с нанесением аппликаций в виде черепицы до полного равномерного побеления опухоли. Воздействие осуществляли с мощностью 200–1 700 мВт в два этапа. На первом этапе в зависимости от размера опухоли, ее конфигурации и близости к сенсорным отделам сетчатки, использовали диаметр фокального пятна размером 1,0 или 1,8 или 3,0 или 5,0 мм. На втором этапе, через четверо суток, использовали диаметр фокального пятна размером 0,6 или 0,8 мм. При этом облучали только те участки, которые восстановили исходный цвет, существовавший до первого этапа воздействия.
Результаты исследования и их обсуждение
С диагнозом отслойка сетчатки левого глаза, подозрением на новообразование сетчатки пациентка О., направлена в клинику НИИ глазных болезней им. Гельмгольца РАМН, г. Москва, для уточнения диагноза и проведения лечения. После проведенного инструментального обследования клинически был установлен диагноз меланома хориоидеи левого глаза.
Пациентка О. с 13.09.2006 г. по 02.10.2006 г. прошла курс комбинированного лечения путем проведения фотодинамической терапии с фотосенсибилизатором Радахлорин. 26.09.2006 года пациентке проведена транспупиллярная термотерапия новообразования.
При выписке из клиники: офтальмоскопически появились четкие границы образования, частичное рассасывание образования, в центре которого кратер на месте регрессии опухоли, визуально размер около 4 мм. Острота зрения правого глаза 1,0, левого глаза 0,1, sph +2,0D = 0,7.
Пациентка О. находится на диспансерном наблюдении на протяжении десяти лет без признаков рецидива заболевания. В настоящее время острота зрения правого глаза 0,4, sph +2,0D = 1,0, левого глаза 0,5 sph +2,5D = 0,5. При офтальмоскопии правого глаза: положение глаза в орбите правильное, движения в полном объеме. Коньюктива бледно-розовая. Роговица прозрачная, гладкая. Передняя глазная камера средней глубины, влага прозрачная. Радужка структурирована, пигментная кайма сохранена. Глазное дно: диск зрительного нерва бледно-розовый, границы четкие, сосудистый пучок в центре, экскавация 0,4. При офтальмоскопии левого глаза: диск зрительного нерва бледно-розовый, четко оконтурирован, в нижнем наружном квадранте обширный рубец хориоидеи, хориосклероз.
Пациентка сохранила работоспособность, не потеряла свои профессиональные навыки, не испытывала проблем в трудоустройстве и необходимости переобучения для смены профессии.
Благодаря ранней диагностике и своевременно проведенному лечению пациентке удалось сохранить не только жизнь, но и орган зрения; она не испытывала действия ряда социальных, физических, экономических и бытовых проблем, которые проявляются в нарушении личностной сферы, затруднениях в производственной и бытовой деятельности.
Заключение
Возможность применения органосохраняющего комбинированного метода лечения больных меланобластомой хориоидеи глаза с использованием транспупиллярной и фотодинамической терапии позволяет сохранить зрительную функцию глаза и оптимально решить вопросы социальной и трудовой реабилитации.
Учитывая высокую ответственность за жизнь и здоровье пациента, выбор метода органосохраняющего лечения у больных с меланобластомой хориоидеи глаза необходимо решать совместно с онкологом и офтальмологом, выполнять его только в специализированном учреждении и обеспечивать строгое динамическое наблюдение за больным.

Содержание:
- 1 Меланома хориоидеи стадии T2 высотой более 6,0 мм: органосохраняющее лечение с использованием брахитерапии и транспупиллярной термотерапии или энуклеация? Анализ выживаемости
- 1.1 Материал и методы
- 1.2 Результаты и обсуждение
- 1.2.1 Заключение

Проведен сравнительный анализ выживаемости больных с меланомой хориоидеи (MX) стадии Т2 высотой более 6,0 мм после органосохраняющего лечения с использованием брахитерапии (БТ) с рутением-106 с одновременной лазерной транспупиллярной термотерапией (ТТТ) и после первичной энуклеации.
Основную группу составили больные, получавшие органосохраняющее лечение в виде самостоятельной БТ либо БТ с одновременной ТТТ, контрольную — пациенты с MX, у которых в качестве первичного лечения произведена энуклеация. Группы стандартизированы по возрасту больных (р = 0,063), средней высоте MX (р > 0,149), среднему максимальному диаметру основания (р > 0,85), количеству опухолей с неблагоприятной локализацией (юкстапапилляр-ные и цилиохориоидальные; р = 0,246), срокам наблюдения (р > 0,23).
При анализе по методу Каплана—Майера 5-летний уровень метастазирования после органосохраняющего лечения составил 16%, после энуклеации — 13% (р > 0,96).
Органосохраняющее лечение на основе БТ и ТТТ при MX высотой до 10 мм (стадии T2N0M0) позволяет сохранить не только глаз как орган, но и некоторое полезное зрение, и является целесообразным.
Брахитерапия с рутением-106 (БТ) — один из ведущих методов лечения меланомы хориоидеи (MX). Ограничение показаний к БТ MX при высоте 5,5—6,0 мм связано с соответствующей глубиной пробега электронов в ткани опухоли [1—3, 17], а при больших опухолях, имеющихся у значительной части больных с MX [6, 7], показанной считают энуклеацию.
Проведенные исследования показали возможность повышения эффективности лечения больных MX стадии Т2 (высота опухоли от 2,5 до 10,0 мм, протяженность от 10 до 16 мм) [8] за счет комбинирования БТ и лазерной транспупиллярной термотерапии (ТТТ) [4, 10, 22, 23]. Полученные результаты, однако, не давали ответа на вопрос, не является ли для пациента с опухолью высотой более 6,0 мм первичная энуклеация более безопасной, чем органосохраняющее лечение. Этому вопросу, обсуждаемому в соответствующих публикациях [2, 3], посвящены лишь единичные работы [5, 9, 20, 21].
Цель работы — провести сравнительный анализ выживаемости больных с MX стадии Т2 высотой более 6,0 мм после органосохраняющего лечения с использованием БТ и ТТТ и после первичной энуклеации.
↑ Материал и методы
Сравнительный анализ проведен в 2 группах больных. Основную группу составили пациенты, получавшие органосохраняющее лечение в виде самостоятельной БТ либо БТ с одновременной ТТТ (БТ + ТТТ). Методики БТ и БТ + ТТТ описаны ранее [4, 10]. Контрольную группу составили больные с MX, у которых в качестве первичного лечения произведена энуклеация.
Критериями включения в анализ были высота MX более 6,0 мм, срок наблюдения после лечения не менее 1 года, отсутствие признаков метастазирования MX до лечения, подтвержденные метастазы после лечения. В связи с тем что органосохраняющее лечение не проводили при опухолях высотой более 10,5 мм, в случаях распространения MX в корень радужки, при закрытии опухолью диска зрительного нерва или вовлечения последнего в опухолевый процесс, при вторичной глаукоме, экстрасклеральном распространении MX, соответствующие пациенты не были включены и в контрольную группу.
Для корректного сравнительного анализа и получения достоверных результатов проведена стандартизация групп по следующим основным показателям, имеющим влияние на показатели метастазирования и выживаемости: по возрасту больных, размерам MX — высоте и максимальному диаметру основания, по количеству опухолей с неблагоприятной локализацией — юкстапапиллярной и цилиохориоидальной и срокам наблюдения.
В итоге основную группу (органосохраняющее лечение) составили 39 пациентов (21 мужчина и 18 женщин) в возрасте от 39 до 74 лет (в среднем 54,3 + 9,0 года); моложе 50 лет были 17 (44%) пациентов. С использованием БТ как монотерапии пролечено 20 пациентов, комбинированным методом (БТ + ТТТ) - 19.
В основной группе высота опухоли составляла от 6,9 до 10,5 мм (в среднем 8,4 ± 1,03 мм), максимальный диаметр основания — от 9,6 до 18,9 мм (в среднем 13,7 ± 2,3 мм). Юкстапапиллярных опухолей было 3, цилиохориоидальных — 6. Максимальный срок наблюдения составил 98 мес, медиана 48 мес. Проведение органосохраняющего лечения у больных с MX высотой более 10,0 мм и диаметром основания более 16,0 мм (11 пациентов) объяснялось их категорическим отказом от энуклеации.
Контрольную группу (энуклеации) составили 28 пациентов (9 мужчин и 19 женщин) в возрасте от 32 до 75 лет (в среднем 58,6 ± 10,4 года); моложе 50 лет были 6 (21%) больных. Проми-ненция MX составляла от 6,7 до 10,5 мм (в среднем 8,8 ± 1,1 мм), максимальный диаметр основания опухоли — от 7,4 до 18,5 мм (в среднем — 13,6 + 3,2 мм). У 6 пациентов имели место юкста-папиллярные опухоли, у 5 — цилиохориоидальные. Максимальный срок наблюдения в этой группе составил 156 мес, медиана — 47,5 мес.
Таким образом, сформированы группы больных, статистически однородные по возрасту (р — 0,063), в том числе по количеству больных моложе 50 лет (р > 0,1), средней высоте MX (р > 0,149), среднему максимальному диаметру основания (р > 0,85), количеству опухолей с неблагоприятной локализацией (юкстапапиллярные и цилиохориоидальные; р = 0,246 по критерию х2), срокам наблюдения (р > 0,23).
↑ Результаты и обсуждение
В основной группе у 2 пациентов после самостоятельной БТ успешно проведены повторные курсы БТ (из них в одном случае троекратное облучение) в связи с частичной регрессией MX и признаками продолженного роста. Сроки повторного лечения — 31 и 43 мес. Острота зрения у пациентов после органосохраняющего лечения составляла от 0 до 1,0 (в среднем 0,12 + 0,24).
Подробная характеристика MX и больных, у которых выявлены метастазы после органосохраняющего лечения и после первичной энуклеации, представлена в табл. 1 и 2.


Согласно проведенному анализу по методу Каплана—Майера (логранговый тест), 5-летний показатель метастазирования (специфическая выживаемость) после органосохраняющего лечения составил 16%, после энуклеации — 13% с отсутствием достоверных различий между группами (р > 0,96; см. рисунок).
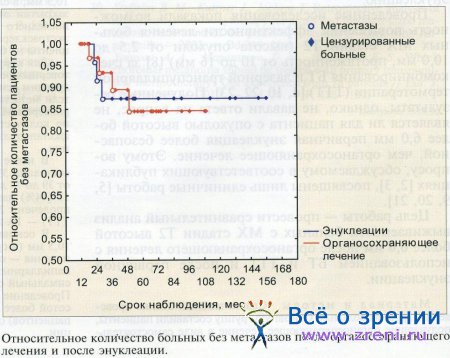
Нами была предпринята попытка решения вопроса о допустимости проведения органосохраняющего лечения при MX высотой более 6,0 мм. Для получения корректных результатов исследуемые группы были стандартизированы по важнейшим характеристикам, влияющим на риск диссеминации MX.
Проведенный анализ с высокой статистической достоверностью (р > 0,96) показал, что попытка сохранения глаза с использованием БТ и ТТТ при MX не повышает риска диссеминации по сравнению с первичной энуклеацией: количество больных с метастазами MX при 5-летнем сроке наблюдения после органосохраняющего лечения составило 16%, после лечения с удалением глаза — 13%. Наши данные вполне согласуются с неоднократно подтвержденным и в настоящее время признанным фактом сходного уровня диссеминации MX независимо от метода лечения [11 — 16, 18-21, 24].
Таким образом, органосохраняющее лечение на основе БТ и ТТТ при MX высотой до 10,0 мм (стадии T2N0M0) позволяет сохранить не только глаз как орган, важный в эстетическом отношении, но и некоторое полезное зрение, и является целесообразным даже при необходимости в отдельных случаях в проведении повторного облучения.
Патент 2318553
Способ повышения эффективности транспупиллярной термотерапии меланомы хориоидеи
Изобретение относится к медицине, офтальмологии, и может быть использовано для повышения эффективности транспупиллярной термотерапии меланомы хориоидеи. Для этого в течение 10 минут внутривенно вводят фотосенсибилизатор (ФС) хлоринового ряда в дозе 1,0 мг/кг. Затем осуществляют лазерное облучение новообразования с длиной волны, соответствующей максимуму поглощения ФС светового излучения, с перекрытием соседних полей на 5-10% площади. При этом облучают периферию опухоли с захватом здоровых тканей не менее чем на 1 мм от офтальмоскопически видимой границы опухоли с плотностью энергии на одно поле 25-40 Дж/см 2 . Затем одним полем с плотностью энергии 110-120 Дж/см 2 облучают центр опухоли. После этого проводят транспупиллярную термотерапию по стандартной методике. Проведение такого лечения позволяет потенцировать эффект локальной гипертермии, уменьшив теплоотведение вследствие циркуляции крови в сосудах за счет тромбоза и стаза крови в сосудах, питающих опухоль, обеспечить более равномерное и глубокое прогревание ткани опухоли.
Изобретение относится к медицине, а точнее к офтальмологии, и может быть использовано для повышения эффективности транспупиллярной термотерапии гиперваскулярных меланом хориоидеи с проминенцией до 4 мм.
Меланома хориоидеи (MX) относится к наиболее часто встречающимся внутриглазным новообразованиям, составляя почти 80% от общего их числа. MX характеризуется крайне неблагоприятным прогнозом, как в отношении зрительных функций, так и жизни больного, в связи с высоким риском метастазирования (от 3 до 16% при малых размерах MX).
С учетом расширяющихся возможностей раннего выявления начальных стадий хориоидальных меланом чрезвычайно актуальной проблемой является разработка органосохранных методов лечения, сочетающих в себе принципы радикальности в отношении новообразования с одновременным сохранением зрительных функций. Одним из таких методов является транспупиллярная термотерапия (ТТТ). В основе механизма действия ТТТ лежит локальная гипертермия (45-55°) опухоли, вызываемая инфракрасным излучением диодного лазера (810 нм), приводящая к локальному (в зоне воздействия) некрозу опухоли глубиной до 4,0 мм.
Одним из перспективных функционально-сберегающих методов лечения MX считается фотодинамическая терапия (ФДТ). Метод ФДТ основан на избирательном накоплении вводимого системно фотосенсибилизатора (ФС) в сосудах и строме опухоли, который при последующем лазерном облучении с длиной волны, соответствующей пику поглощения данного ФС, приводит к фототоксическому повреждению сосудистой системы новобразования.
В доступных источниках авторам не удалось найти данных по повышению эффективности ТТТ MX.
Задачей изобретения является создание способа повышения эффективности транспупиллярной терапии гиперваскулярных меланом хориоидеи.
Техническим результатом заявляемого способа является устранение теплоотведения вследствие циркуляции крови в сосудах, питающих опухоль, полная или частичная резорбция гиперваскулярных меланом хориоидеи, отсутствие рецидивов и метастазирования в отдаленном послеоперационном периоде. Технический результат достигается за счет того, что:
1. Применяемые ФС хлоринового ряда отличаются высокой степенью чистоты, низкой токсичностью, способностью накапливаться в опухолевых клетках и даже в малых дозах проявлять высокую фотохимическую активность при лазерном облучении.
2. Следующее после внутривенного введения ФС транспупиллярное облучение внутриглазного новообразования лазерным излучением с заданными параметрами (транспупиллярная фотодинамическая терапия (ФДТ)) вызывает стаз крови и светоиндуцированный тромбоз сосудов, питающих новообразование, что создает препятствие для теплоотведения в процессе ТТТ, а также приводит к гибели опухолевых клеток, накопивших ФС.
С целью подтверждения указанного фотодинамического воздействия на сосуды опухоли ФДТ было проведено 3 пациентам с гиперваскулярными MX с проминенцией от 2,5 до 4 мм. Данные комплексного ультразвукового исследования в режимах цветового допплеровского картирования (ЦДК) и энергетического допплеровского картирования (ЭДК) показали, что после ФДТ определяется или существенное уменьшение количества сосудистых цветовых эхосигналов в ткани опухоли, или полное исчезновение указанных эхосигналов по сравнению с исходными данными (до ФДТ), когда во всех случаях определялась повышенная степень васкуляризации опухоли, проявлявшаяся во множестве диффузно расположенных сосудистых цветовых эхосигналов (гиперваскулярная MX). Это позволяет сделать заключение об изменении гиперваскулярного характера васкуляризации MX на гипо- или аваскулярный после проведения ФДТ. Очевидно, что описанное изменение характера васкуляризации будет способствовать значительному уменьшению теплоотведения.
3. Проведение транспупиллярной термотерапии после ФДТ способствует равномерному и глубокому прогреванию ткани опухоли без существенных потерь тепловой энергии за счет ее отведения вследствие циркуляции крови в сосудах, питающих опухоль, что позволяет достичь деструкции ткани по всему объему новообразования.
Заявленный технический результат может быть получен только при использовании всей совокупности приемов предложенного нами способа.
Способ осуществляется следующим образом.
Пациенту вводится ФС хлоринового ряда, например фотодитазин, или фотолон, или радахлорин, внутривенно капельно в течение 10 минут в дозе 1 мг/кг веса. По окончании введения ФС проводят транспупиллярную ФДТ. В ходе ФДТ лазерное облучение новообразования с длиной волны, соответствующей максимуму поглощения ФС светового излучения, например с длиной волны 662 нм при использовании ФС хлоринового ряда, полями (диаметром 3 мм), с перекрытием соседних полей на 5-10% площади, осуществляют следующим образом: облучают периферию опухоли с захватом здоровых тканей не менее, чем на 1 мм от офтальмоскопически видимой границы опухоли с плотностью энергии на одно поле 25-40 Дж/см 2 , затем одним полем с плотностью энергии 110-120 Дж/см 2 облучают центр опухоли. По завершении транспупиллярной ФДТ проводят ТТТ по стандартной методике (Линник Л.Ф., Магарамов Д.А., Яровой А.А. и др. Трехлетний опыт использования транспупиллярной диод-лазерной термотерапии как самостоятельного метода лечения увеальных меланом. Офтальмохирургия. 2003; 4:17-24). Параметры ТТТ: длина волны - 810 нм, мощность излучения - 800 мВт, экспозиция - 60 сек, диаметр пятна облучения - 3 мм.
Изобретение поясняется следующими данными.
Острота зрения при поступлении - 0,7 не коррегируется.
Было получено информированное согласие пациентки на проведение очередного сеанса ТТТ с повышением его эффективности по предложенному способу.
В ходе лазерного облучения при проведении ФДТ с препаратом фотолон периферию опухоли с захватом здоровых тканей не менее чем на 1 мм от офтальмоскопически видимой границы опухоли облучали полями диаметром 3 мм, с перекрытием соседних полей на 10% площади, с плотностью энергии на одно поле 30 Дж/см 2 , затем одним полем с плотностью энергии 120 Дж/см 2 облучали центр опухоли. После ФДТ провели ТТТ по стандартной методике со следующими параметрами: длина волны - 810 нм, мощность излучения - 800 мВт, экспозиция - 60 сек, диаметр пятна облучения - 3 мм.
В сроки наблюдения от 3-х до 6 месяцев после лечения отмечалась постепенная регрессия опухоли. Толщина новообразования через 3 месяца составляла 1,5 мм, через 6 мес - 0,9 мм. Офтальмоскопически наблюдалось формирование плоского хориоретинального рубца с неоднородной пигментацией.
Через 6 месяцев острота зрения на пролеченный глаз составила 1,0. При исследовании поля зрения левого глаза определялась отрицательная относительная скотома в нижне-наружном квадранте, фовеальная светочувствительность осталась на прежнем уровне.
В сроки наблюдения до 2 лет достигнута полная резорбция опухоли, без рецидивов и метастазов.
Предлагаемый способ был применен у 4 пациентов с гиперваскулярными MX с проминенцией до 4 мм. Для ФДТ использовали фотодитазин, фотолон, радахлорин, лазерное облучение полями (диаметром 3 мм) проводили с перекрытием соседних полей на 5-10% площади. Периферию опухоли облучали с плотностью энергии на одно поле от 25 до 40 Дж/см 2 , центр опухоли - одним полем с плотностью энергии от 110 до 120 Дж/см 2 . Во всех случаях удалось повысить эффективность ТТТ с получением заявленного технического результата. Сроки наблюдения - от 1 до 2 лет: во всех случаях достигнута полная или частичная резорбция MX, признаков рецидивов и метастазирования не отмечено.
Таким образом, предлагаемый способ повышает эффективность ТТТ гиперваскулярных MX, обеспечивая устранение теплоотведения вследствие циркуляции крови в сосудах, питающих опухоль, при этом достигается полная или частичная резорбция гиперваскулярных меланом хориоидеи, отсутствие рецидивов и метастазирования в отдаленном послеоперационном периоде.
Способ повышения эффективности транспупиллярной термотерапии меланомы хориоидеи, заключающийся в том, что внутривенно вводят фотосенсибилизатор (ФС) хлоринового ряда в дозе 1,0 мг/кг в течение 10 мин, по окончании введения лазерное облучение новообразования с длиной волны, соответствующей максимуму поглощения ФС светового излучения, полями, с перекрытием соседних полей на 5-10% площади осуществляют следующим образом: облучают периферию опухоли с захватом здоровых тканей не менее чем на 1 мм от офтальмоскопически видимой границы опухоли с плотностью энергии на одно поле 25-40 Дж/см 2 , затем одним полем с плотностью энергии 110-120 Дж/см 2 облучают центр опухоли, после чего проводят транспупиллярную термотерапию по стандартной методике.
Читайте также:

