Степень окисления hclo4 с хлором
Задание 4. В соединении, формула которого HClO3, степень окисления хлора равна:
1) +5; 2) +3; 3) +1; 4) +7
Степень окисления определяют, как заряд атома элемента в соединении, который возник бы на данном атоме, если предположить, что все связи в соединении ионные.
Любая молекула электронейтральна, поэтому сумма всех степеней окисления атомов, входящих в состав молекулы, равна нулю.
Найдем степень окисления хлора в соединении HClO3. Степень окисления кислорода -2, а степень окисления водорода +1.
Степень окисления хлора в молекуле HClO3 равна +5.
- Все задания варианта
- Наша группа Вконтакте
- Наш магазин
- Наш канал
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 1
- Вариант 1. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 2
- Вариант 2. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 3
- Вариант 3. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 4
- Вариант 4. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 5
- Вариант 5. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 6
- Вариант 6. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 7
- Вариант 7. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 8
- Вариант 8. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 9
- Вариант 9. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 10
- Вариант 10. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 11
- Вариант 11. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 12
- Вариант 12. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 13
- Вариант 13. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 14
- Вариант 14. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 15
- Вариант 15. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 16
- Вариант 16. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 17
- Вариант 17. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 18
- Вариант 18. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 19
- Вариант 19. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 20
- Вариант 20. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 21
- Вариант 21. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 22
- Вариант 22. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 23
- Вариант 23. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 24
- Вариант 24. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 25
- Вариант 25. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 26
- Вариант 26. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 27
- Вариант 27. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 28
- Вариант 28. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 29
- Вариант 29. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- Вариант 30
- Вариант 30. Задания ОГЭ 2017. Химия. А.С. Корощенко. 30 вариантов
- Решения заданий по номерам
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
Для наших пользователей доступны следующие материалы:
- Инструменты ЕГЭиста
- Наш магазин
- Наш канал
Задача 823.
Как изменяются в ряду HOCl — HClO 2 — HClO3 — HClO 4: а) устойчивость; б) окислительные свойства; в) кислотные свойства?
Решение:
а) С увеличением степени окисления хлора устойчивость его кислородных кислот растёт в ряду HOCl — HClO 2 — HClO3 — HClO 4 . Объясняется это тем, что при
возрастании степени окисления хлора увеличивается заряд ионов , что усилит его притяжение к иону О 2- , связь Cl—O будет усиливаться.
б) С увеличением степени окисления хлора окислительные свойства кислородных кислот в ряду HOCl — HClO 2 — HClO3 — HClO 4 будут усиливаться. Объясняется это тем, что при увеличении степени окисления атома хлора будет уменьшаться способность его отдавать электроны. Так в HCO атом хлора находится в своей степени окисления +1, а в HClO2 – в степени окисления +3, поэтому ион хлора Cl + может отдать шесть электронов, а ион Сl 3+ - четыре электрона; присоединить ион Cl + может один или два электрона, а ион Сl 3+ - три или четыре. Таким образом, окислительная способность ионов уменьшается с увеличением степени окисления атомов хлора.
в) С увеличением степени окисления хлора сила его кислородсодержащих кислот возрастают в ряду HOCl — HClO 2 — HClO3 — HClO 4 . Из всех гидроксидов хлора самая слабая кислота это HOCl. При возрастании степени окисления хлора увеличивается заряд иона , что усилит его притяжение к иону О 2- и, тем самым, затруднит диссоциацию гидроксида по типу основания. Вместе с тем усилится взаимное отталкивание одноимённо заряжённых ионов и Н + , что облегчит диссоциацию по кислотному типу. Таким образом, с увеличением степени окисления хлора усиливаются кислотные свойства и ослабевают основные свойства его гидроксидов.
Задача 824.
Как изменяются кислотные и окислительно-восстановительные свойства в ряду НОСl — НОВг — НОI?
Решение:
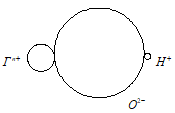
Увеличение радиуса иона Г n+ при неизменном его заряде приведёт к возрастанию расстояний между центром этого иона и центром ионов О 2- и Н + . В результате взаимное электростатическое притяжение ионов Г n+ и О 2- станет более слабым, что облегчит диссоциацию по основному типу; одновременно уменьшится взаимное отталкивание ионов Г n+ и Н + , так что диссоциация по кислотному типу затруднится. Следовательно, с возрастанием радиуса иона галогена (при неизменном его заряде) усиливаются основные свойства и ослабляются кислотные свойства. Поэтому изменение кислотных свойств в ряду
НОСl — НОВг — НОI будет идти в сторону уменьшения. Хлорноватистая кислота будет самой сильной, иодноватистая – самой слабой, бромноватистая – промежуточной по силе кислотой из трёх рассматриваемых кислот.
Ионная схема молекулы гидроксида ГОН:
Задача 825.
Почему из всех галогенов только йод образует многоосновные кислородные кислоты? Указать тип гибридизации АО галогенов в их высших кислородных кислотах.
Решение:
Из всех галогенов йод имеет самый большой заряд ядра атома и самое большое количество промежуточных энергетических уровней. У йода, как у атома, так и иона, самый большой радиус из всех галогенов. В результате у йода самое большое межмолекулярное дисперсионное взаимодействие, что обуславливает большую прочность его соединений. Из-за большого атомного объёма йода электростатическое взаимодействие между ионами и становится более слабым, чем между ионами других галогенов и , что, естественно, облегчает диссоциацию кислоты по основному типу; одновременно уменьшится взаимное отталкивание ионов и Н +, что, естественно, затрудняет диссоциацию гидроксида по кислотному типу. Поэтому гидроксиды йода будут являться более сильными основаниями, чем гидроксиды других галогенов, например, хлора и брома. В гидроксиде йода, где атом йода находится в своей высшей степени окисления, в водных растворах возможно образование многоосновных кислот. При взаимодействии йодной кислоты с водой, в зависимости от условий, может образоваться несколько соединений общей формулы (НIO4)n . (Н2О)m. Во всех этих соединениях водород воды способен замещаться на металл так же, как и водород самого гидроксида йода (VII). В связи с этим соединения подобного типа обычно рассматриваются как сложные кислоты и приписывают им следующие форомулы: HIO4 (n = 1, m = 0); H3IO5 (n = 1, m = 1);
H4I2O9 (n = 2, m = 1); H5IO6 (n = 1, m = 2); HIO5 (n = 1, m = 2). Например, были получены H4I2O9 и следующие серебряные соли: оранжевая AgIO4, красная Ag2HIO5, чёрная Ag3IO5, зеленовато-жёлтая Ag2HIO5, чёрная Ag5IO6. В последней из перечисленных выше солей H5IO6 выступает как пятиосновная кислота. Молекула H5IO6 представляет собой несколько искажённый октаэдр. В кристалле между такими молекулами осуществляются водородные связи. При нагревании H5IO6 в вакууме до 80 0 С получается H4I2O9. Свободная H3IO5 не выделена. Строение отвечает октаэдру с йодом в центре, а иона - тетраэдру с йодом в центре.
Типы гибридизации АО галогенов в их кислотах:
а) НГО – тип гибридизации отсутствует;
б) НГО2 - тип гибридизации отсутствует;
в) НГО3 - тип гибридизации sp 3 ;
г) НГО4 - тип гибридизации sp 3 ;
д) Н5IO6 - тип гибридизации sp 3 d 2 .
sp 3 d 2 – гибридные орбитали направлены к вершине октаэдра.
Задача 826.
Как получить НIО3, исходя из свободного йода, диоксида марганца и соляной кислоты? Составить уравнения соответствующих реакций.
Решение:
Получение НIО3 из свободного йода, диоксида марганца и соляной кислоты:
а) При действии раствора соляной кислоты на диоксид марганца можно получить хлор:
б) Йодноватую кислоту можно получить окислен7ием хлора йодом:
По этой реакции хлороводород выделяется в виде газа, который отводят из системы, а раствор выпаривают и получают кристаллическую кислоту НIО3. Йодноватая кислота довольно стойкое вещество, представляющее собой бесцветные кристаллы, которые вполне устойчивые при обычных условиях.
| Свойство | HClO | HClO2 | HClO3 | HClO4 |
| Степень окисления | +1 | +3 | +5 | +7 |
| Название | хлорноватистая (гипохлориты) | хлористая (хлориты) | хлорноватая (хлораты) | хлорная (перхлораты) |
| Константа диссоциации | 3,2 × 10 –8 | 1,1 × 10 –2 | 10 1 | 10 10 |
| Кратность связи Cl-O | 1,5 | 1,67 | 1,75 |
С увеличением степени окисления и с увеличением кратности связи происходит ослабление связи О – Н за счет смещения электронной плотности по кратной связи Cl – O, увеличивается подвижность Н + , следовательно, с увеличением степени окисления сила кислот увеличивается.
Какая из кислот является наиболее устойчивой? С увеличением кратности связи Cl – O увеличивается устойчивость аниона, а как следствие этого падает его реакционная способность.
Соединения хлора с положительной степенью окисления проявляют окислительные свойства (стремятся перейти в Cl – ).
Хотя с увеличением степени окисления должны усиливаться окислительные свойства, но решающее значение здесь имеет устойчивость аниона, которая увеличивается. В ряду HClO – HClO4 окислительная активность уменьшается. Максимум окислительных свойств приходится на хлористую кислоту HClO2.
Хлорноватистая кислота HClO в свободном состоянии неустойчива, быстро разлагается на ClO2 и Н2О, поэтому существует только в разбавленных водных растворах. Получают путем взаимодействия газообразного хлора с оксидом ртути (II):
Хлорноватистая кислота – слабая кислота. Раствор хлорноватистой кислоты и гипохлоритов имеют желто-зеленую окраску, резкий запах. В водном растворе HClO диспропорционирует:
В растворе под действием света HClO разлагается:
Прим. наибольший практический интерес представляет смешанный хлорид – гипохлорит кальция CaOCl2 (белильная известь) – смесь Ca(ClO)2, CaCl2, Ca(OH)2, который в промышленности получают взаимодействием хлора с гидроксидом кальция:
Белильная известь широко применялась в качестве дезинцифицирующего и отбеливающего средства, а также для получения хлора и кислорода:
Однако из-за низкого содержания активного хлора (36%) и плохой растворимости в воде ее производство резко сократилось. На смену белильной извести пришли гипохлориты кальция и натрия. Хорошим отбеливающим действием обладает жавелевая вода – раствор, образующийся при насыщении хлором раствора гидроксида натрия.
Соли хлорноватистой кислоты – гипохлориты – являются сильными окислителями. Например:
Гипохлориты более устойчивы, чем хлорноватистая кислота, но при комнатной температуре медленно диспропорционируют:
Хлористая кислота HClO2в свободном виде неустойчива. В разбавленных растворах быстро разлагается:
Водные растворы хлористой кислоты получают обработкой хлорита бария Ba(ClO2)2 разбавленной серной кислотой:
В водном растворе хлористая кислота – кислота средней силы. Хлориты используют для отбеливания.
Соли хлористой кислоты – хлориты. Из солей наибольшее применение находит хлорит натрия, получаемый по реакции:
Хлорноватая кислота HClO3существует только в растворе.
Получают действием разбавленной серной кислоты на раствора соответствующих солей:
В водном растворе хлорноватая кислота – сильная кислота.
Прим. хлорноватая кислота по свойствам похожа на азотную кислоту, в частности ее смесь с соляной кислотой является сильным окислителем.
Соли хлорноватой кислоты – хлораты. При нагревании хлораты диспропорционируют. Например, при нагревании твердого хлората калия при температуре 500 ºС протекает следующая реакция:
В присутствии катализатора хлорат калия разлагается с выделением кислорода:
Твердые хлораты являются сильными окислителями.
В смеси с восстановителями хлораты образуют легко взрывающиеся составы. Бертолетову соль используют в производстве спичек и смеси для фейерверков. Хлорат натрия NaClO3 применяется в качестве средства для борьбы с сорняками.
Прим. В водном растворе окислительная способность хлоратов проявляется только в кислой среде.
Хлорная кислота HClO4Чистая хлорная кислота – бесцветная дымящая на воздухе жидкость, смешивается с водой в любых соотношениях.
Хлорную кислоту получают действием концентрированной соляной кислоты на безводный перхлорат натрия NaClO4:
Хлорид натрия, нерастворимый в концентрированной соляной кислоте, отделяют фильтрованием, а фильтрат концентрируют дистилляцией при пониженной давлении в присутствии концентрированной серной кислоты.
Хлорная кислота взрывоопасна, взрывается при соприкосновении с органическими веществами.
Хлорная кислота – одна из наиболее сильных кислот. При охлаждении раствора образуется кристаллогидрат HClO4 × nH2O (n = 1 – 3). Хлорная кислота является окислителем только в концентрированных растворах. При нагревании легко разлагается:
Соли хлорной кислоты – перхлораты. Перхлорат калия получают нагреванием без катализатора:
Другие перхлораты получают взаимодействием хлорной кислоты с соответствующими основаниями или карбонатами. Большинство перхлоратов хорошо растворимы в воде (кроме KClO4, RbClO4, CsClO4). Безводный перхлорат магния Mg(ClO4)2 сильно поглощает воду, образуя кристаллогидраты. Это один из наиболее сильных осушителей (техническое название ангидрон). После поглощения воды нагреванием может быть обезвожен.
В растворе перхлораты не проявляют окислительных свойств, но в сухом состоянии при повышенной температуре – одни из сильных окислителей.
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Важнейшие соединения хлора.
Хлористый водород (соляная кислота) HCl.Cодержится в вулканических газах и водах, в желудочном соке. Является бесцветным газом, на воздухе дымит вследствие образования с парами воды капелек тумана. Обладает резким запахом, сильно раздражает верхние дыхательные пути, обладает очень кислым вкусом. tпл=-112 о С [1], tкип=-84 о С [1]. Плотность газообразного хлористого водорода относительно воздуха при 0 о С равна 1,3601. Химические свойства зависят от того, в каком состоянии он находится (может быть в газообразном, жидком состоянии или в растворе). В растворе HCl является сильной кислотой. Вытесняет более слабые кислоты из их солей. Молярная электропроводность при бесконечном разведении при 25 о С равна 426,15 Cм . см 2 /моль [4]. Применяют для получения водорода, хлора, хлоридов, различных органических соединений, в аналитической химии, металлургии и т.д.
Соединения хлора со степенью окисления +1.
Оксид хлора (I) Cl2O.Газ буровато-желтого цвета с резким запахом. tпл=-116 о С, tкип=2 о С. Поражает дыхательные органы. Плотность его относительно воздуха равна 3,007. Легко растворяется в воде, образуя хлорноватистую кислоту. При +4 о С сгущается в жидкость золотисто-красного цвета. Очень неустойчивое соединение, разлагается со взрывом. Получают методом Пелуза при взаимодействии HgO с хлором.
Хлорноватистая кислота HClO.Существует только в растворах. Это слабая и неустойчивая кислота. Легко разлагается на соляную кислоту и кислород. Сильный окислитель. Образуется при растворении хлора в воде.
Соединения хлора со степенью окисления +3.
Хлористая кислота HClO2.В свободном виде неустойчива, даже в разбавленном водном растворе она быстро разлагается. В водном растворе хлористая кислота - это кислота средней силы. Молярная электропроводность при бесконечном разведении при 25 о С равна 401,8 Cм . см 2 /моль [4].
Соединения хлора со степенью окисления +4.
Оксид хлора (IV) ClO2.Зеленовато-желтый газ с неприятным (резким) запахом, плотность относительно воздуха равна 2,315. tкип=11 о С, tпл=-59 о С. Газ легко сжижается в красно-коричневую жидкость. При +65 о С разлагается со взрывом. Фосфор, мышьяк и сера разлагают СlO2, разложение происходит со взрывом. Является сильным окислителем. В лаборатории получают действием крнцентрированной серной кислоты на бертолетову соль.
Соединения хлора со степенью окисления +5.
Хлорноватая кислота HClO3.В свободном виде нестабильна: диспропорционирует на ClO2 и HClO4. Молярная электропроводность при бесконечном разведении при 25 о С равна 414,4 Cм . см 2 /моль [4]. Получают действием на ее соли разбавленной серной кислоты.
Соединения хлора со степенью окисления +7.
Хлорная кислота HClO4.tпл=-101 о С, tкип=16 о С. В водных растворах хлорная кислота - самая устойчивая из всех кислородсодержащих кислот хлора. Безводная хлорная кислота, которую получают при помощи концентрированной серной кислоты из 72%-ной HСlO4 мало устойчива. Безводная хлорная кислота дымит на воздухе, взрывается при 92 о С. Разбавленные растворы окислительных свойств не проявляют, но по кислотным свойствам HСlO4 является самой сильной из кислородсодержащих кислот хлора. Молярная электропроводность при бесконечном разведении при 25 о С равна 417,1 Cм . см 2 /моль [4]. В разбавленных растворах находит применение в качестве реактива при химических анализах. Безводная окисляет бумагу, дерево, уголь до их воспламенения.
Свойства хлора.Хлор – тяжелый (в 2,5 раза тяжелее воздуха) желто-зеленый газ. Молекулы Cl2 легко диссоциируют на атомы при поглощении кванта света, а также при высокой температуре. При 730° С степень диссоциации составляет около 0,02%, а при 1730° С – уже почти 35%. При невысоких давлениях хлор близок к идеальным газам: 1 моль хлора при нормальных условиях занимает объем 22,06 л. При охлаждении до –34° С хлор сжижается, а при –101° С он затвердевает. Температуру сжижения газообразного хлора легко повысить, если увеличить давление; так при давлении 5 атм хлор кипит уже при +10,3° С.
Хлор неплохо растворяется в воде: при 10° С в 1 л воды растворяется 3,15 л хлора, при 20° С – 2,3 л. Образующийся раствор обычно называют хлорной водой. Если насытить хлором при атмосферном давлении холодную (ниже 9,6° С) воду, из раствора выделяются желтоватые кристаллы состава Cl2·6H2O. Такие же кристаллы гидрата хлора образуются при охлаждении влажного газообразного хлора. Нагревая гидрат хлора в одном колене запаянной изогнутой трубки и охлаждая второе колено льдом, Фарадей в 1823 получил жидкий хлор. Хлор хорошо растворяется во многих органических растворителях; так, в 100 г холодного бензола растворяется около 35 г хлора.
Химически хлор очень активен. Он реагирует почти со всеми веществами, даже с платиной (при температурах выше 560° С). А в хлорной воде растворяется и золото. В 1869 профессор химии в Эдинбурге Джемс Альфред Уанклин заметил, что хорошо высушенный хлор не действует на железо и некоторые другие металлы. В результате появилось возможность хранить безводный жидкий хлор в стальных баллонах. Промышленное производство жидкого хлора было налажено в 1888 немецкой фирмой БАСФ.
Хлор активно и с выделением значительного количества тепла реагирует с водородом:
Cl2 + H2 ® 2HCl + 184 кДж. Реакция идет по цепному механизму, и если скорость ее инициирования велика (сильное освещение ультрафиолетовым или сине-фиолетовым светом, нагрев до высокой температуры), смесь газов (если хлора в ней содержится более 11,5 и менее 95%) взрывается (см. также ЦЕПНЫЕ РЕАКЦИИ).
Хлор в своих соединениях может проявлять все степени окисления – от –1 до +7. С кислородом хлор образует ряд оксидов, все они в чистом виде нестабильны и взрывоопасны: Cl2O – желто-оранжевый газ, ClO2 – желтый газ (ниже 9,7 о С – яркокрасная жидкость), перхлорат хлора Cl2O4 (ClO–ClO3, светло-желтая жидкость), Cl2O6 (O2Cl–O–ClO3, ярко-красная жидкость), Cl2O7 – бесцветная очень взрывчатая жидкость. При низких температурах получены нестабильные оксиды Cl2O3 и ClO3. Оксид ClO2 производится в промышленном масштабе и используется вместо хлора для отбеливания целлюлозы и обеззараживания питьевой воды и сточных вод. С другими галогенами хлор образует ряд так называемых межгалогенных соединений, например, ClF, ClF3, ClF5, BrCl, ICl, ICl3.
Хлор и его соединения с положительной степенью окисления – сильные окислители. В 1822 немецкий химик Леопольд Гмелин путем окисления хлором получил из желтой кровяной соли красную: 2K4[Fe(CN)6] + Cl2 ® K3[Fe(CN)6] + 2KCl. Хлор легко окисляет бромиды и хлориды с выделением в свободном виде брома и иода.
Хлор реагирует со многими органическими соединениями. Он быстро присоединяется к непредельным соединениям с двойными и тройными углерод-углеродными связями (реакция с ацетиленом идет со взрывом), а на свету – и к бензолу. При определенных условиях хлор может замещать атомы водорода в органических соединениях: R–H + Cl2 ® RCl + HCl. Эта реакция сыграла значительную роль в истории органической химии. В 1840-х французский химик Жан Батист Дюма обнаружил, что при действии хлора на уксусную кислоту с удивительной легкостью идет реакция
СН3СООН + Cl2 ® CH2ClCOOH + HCl. При избытке хлора образуется трихлоруксусная кислота ССl3СООН. Однако многие химики отнеслись к работе Дюма недоверчиво. Ведь согласно общепринятой тогда теории Берцелиуса положительно заряженные атомы водорода не могли заместиться отрицательно заряженными атомами хлора. Этого мнения придерживались в то время многие выдающиеся химики, среди которых были Фридрих Вёлер, Юстус Либих и, конечно, сам Берцелиус.
Чтобы высмеять Дюма, Вёлер передал своему другу Либиху статью от имени некоего Ш.Виндлера (Schwindler – по-немецки мошенник) о новом удачном приложении якобы открытой Дюма реакции. В статье Вёлер с явной издёвкой написал о том, как в уксуснокислом марганце Mn(CH3COO)2 удалось все элементы, в соответствии с их валентностью, заместить на хлор, в результате чего получилось желтое кристаллическое вещество, состоящее из одного только хлора. Далее говорилось, что в Англии, последовательно замещая в органических соединениях все атомы на атомы хлора, обычные ткани превращают в хлорные, и что при этом вещи сохраняют свой внешний вид. В сноске было указано, что лондонские лавки бойко торгуют материалом, состоящим из одного хлора, так как этот материал очень хорош для ночных колпаков и теплых подштанников.
Либиху шутка понравилась, и он опубликовал ее (на французском языке) от имени Ш.Виндлера всего через несколько страниц после статьи Дюма. Намек получился очень прозрачным. Тем не менее прав оказался все же Дюма.
Реакция хлора с органическими соединениями приводит к образованию множества хлорорганических продуктов, среди которых – широко применяющиеся растворители метиленхлорид CH2Cl2, хлороформ CHCl3, четыреххлористый углерод CCl4, трихлорэтилен CHCl=CCl2, тетрахлорэтилен C2Cl4. В присутствии влаги хлор обесцвечивает зеленые листья растений, многие красители. Этим пользовались еще в XVIII в. для отбеливания тканей.
Читайте также:

