Соединения марганца с хлором
Содержится в количестве 0,03% по массе в земной коре. Наряду с железом и его сплавами относится к черным металлам.

Для соединений марганца характерны степени окисления +2, +3, +4, +6 +7. В соединения +2 и +3 марганец проявляет основные свойства, +4 - амфотерные, +6, +7 - кислотные.

Наиболее известными минералами, в которых содержится марганец, являются:
- MnO2 - пиролюзит
- MnO(OH) - бурая марганцевая руда, манганит
- 3Mn2O3*MnSiO3 - браунит

Получают марганец алюминотермией, восстановлением коксом, электролизом.
MnO2 + C = (t) Mn + CO
-
Реакции с неметаллами
На воздухе марганец вступает во взаимодействие с кислородом, пассивируется: на поверхности металла образуется оксидная пленка.
При нагревании марганец реагирует с азотом, углеродом, кремнием, бором и фосфором.

При нагревании марганец вытесняет водород из воды.
Реакции с кислотами
Марганец стоит в ряду напряжений до водорода и способен вытеснить его из кислот.
Под воздействием кислот, которые обладают окислительными свойствами, марганец окисляется.

Соединения марганца II
Для соединений марганца II характерны основные свойства. Оксид марганца II может быть получен разложением карбоната марганца, либо восстановлением оксида марганца IV до оксида марганца II.
При растворении (и нагревании!) марганца в воде образуется гидроксид марганца II.
Соединения марганца II на воздухе неустойчивы, Mn(OH)2 быстро буреет, превращаясь в оксид-гидроксид марганца IV.
Оксид и гидроксид марганца II проявляют основные свойства. При реакции с кислотами дает соответствующие соли.

Соли марганца II получается при его растворении в разбавленных кислотах. Эти соли способны вступать в реакции с другими солями, кислотами, если выпадает осадок, выделяется газ или образуется слабый электролит.
При действии сильных окислителей ион Mn 2+ способен переходить в ион Mn 7+
Соединения марганца IV проявляют амфотерный характер. Оксид марганца IV можно получить разложением нитрата марганца II.

В реакциях с щелочами марганец переходит в СО +6, в кислой среде - принимает СО +2.

Соединения марганца VI - MnO3, H2MnO4 - неустойчивы, в свободном виде не получены. Обладают кислотными свойствами. Наиболее устойчивые соли - манганаты, окрашивающие раствор в зеленый цвет.
Манганаты получают в ходе разложения перманганатов, а также реакциями в щелочной среде.

В водной среде манганаты разлагаются на с.о. +7 и +4. Манганаты окисляют хлором.
Соединения марганца VII - неустойчивый Mn2O7, и относительно устойчивая в разбавленных растворах HMnO4 - проявляют кислотные свойства. Соли марганцовой кислоты - перманганаты.
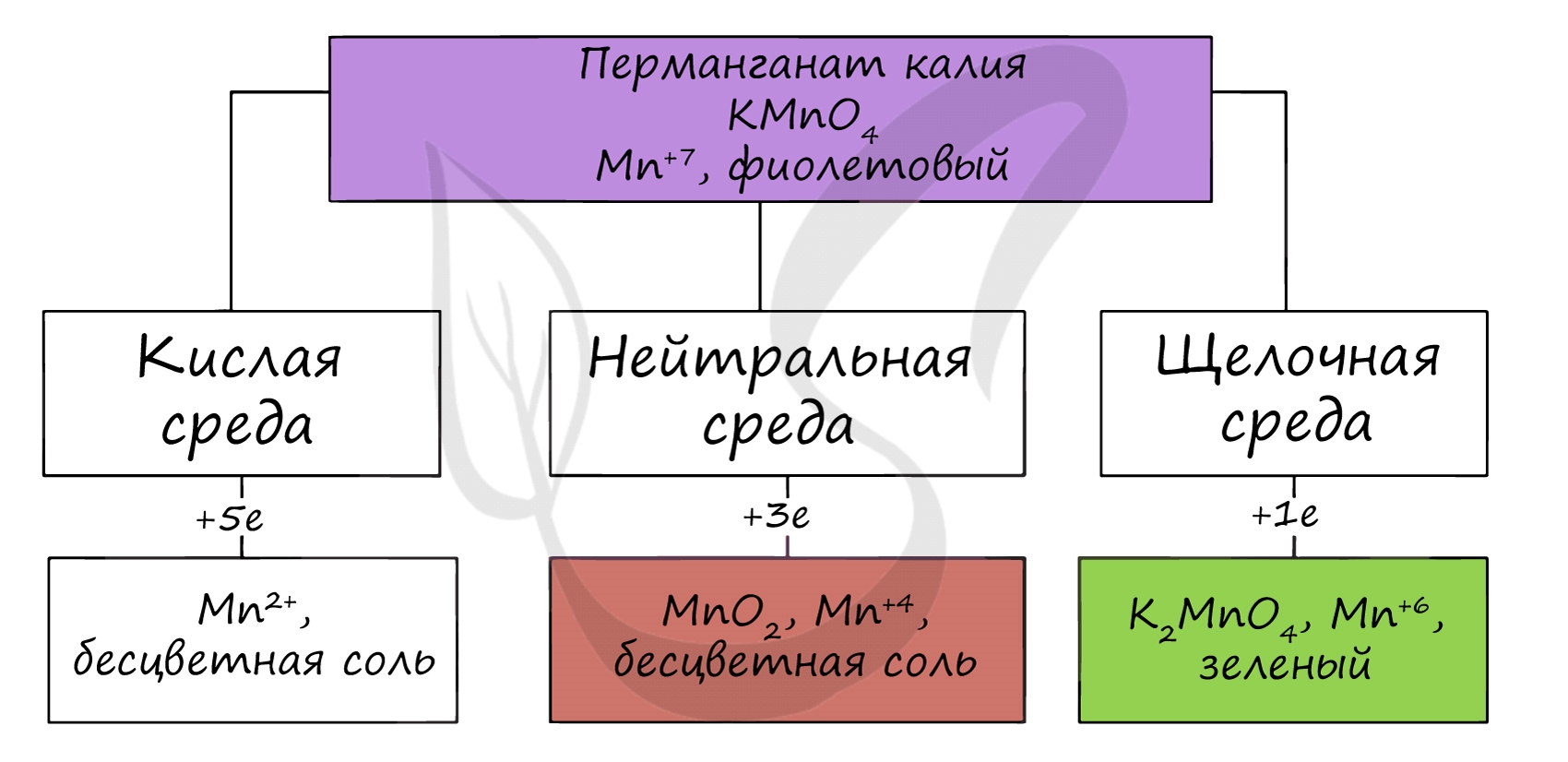
В различных средах - кислотной, нейтральной и щелочной - марганец принимает различные степени окисления. Внимательно изучите таблицу ниже.
Оксид марганца VII получают в реакции перманганата с сильными кислотами.
При растворении оксида марганца VII (кислотного оксида) в щелочи образуются соли марганцовой кислоты - перманганаты.
Марганцовая кислота получается в реакциях сильных окислителей с солями марганца II.
В растворах с концентрацией марганцовой кислоты более 20% происходит ее разложение.
При нагревании перманганата калия (в быту - марганцовка) разлагается с образованием бурого MnO2, выделением кислорода.

При стоянии в растворе постепенно разлагается водой.
В кислой среде марганец принимает наиболее устойчивую (для кислой среды) - Mn 2+ , в щелочной - Mn 6+ .
Название цинка, вероятно, связано формой его кристаллитов: в переводе с немецкого Zinke - зубец. С древнейших времен известен сплав меди с цинком - латунь.

Для цинка характерна постоянная степень окисления +2.

Наиболее известные минералы, в которых содержится цинк:
- ZnS - цинковая обманка, сфалерит
- ZnO - цинкит
- ZnCO3 - симсонит, цинковый шпат
- 2ZnO*SiO2*H2O - гемиморфит

Пирометаллургический метод получения цинка заключается в обжиге цинковой обманки, и последующем восстановлении оксида цинка различными восстановителями: чаще всего C, также возможно CO и H2.
ZnO + C = (t) Zn + CO
ZnO + CO = (t) Zn + CO2

Гидрометаллургический метод получения основывается на электролизе сульфата цинка.
-
Реакции с неметаллами (и аммиаком :)
На воздухе цинк покрывается оксидной пленкой. При нагревании цинк реагирует с галогенами, фосфором, серой, селеном.

Для цинка не характерны реакции с водородом, бором, кремнием, азотом, углеродом. Нитрид цинка можно получить в ходе реакции цинка с аммиаком.
Реакции с кислотами
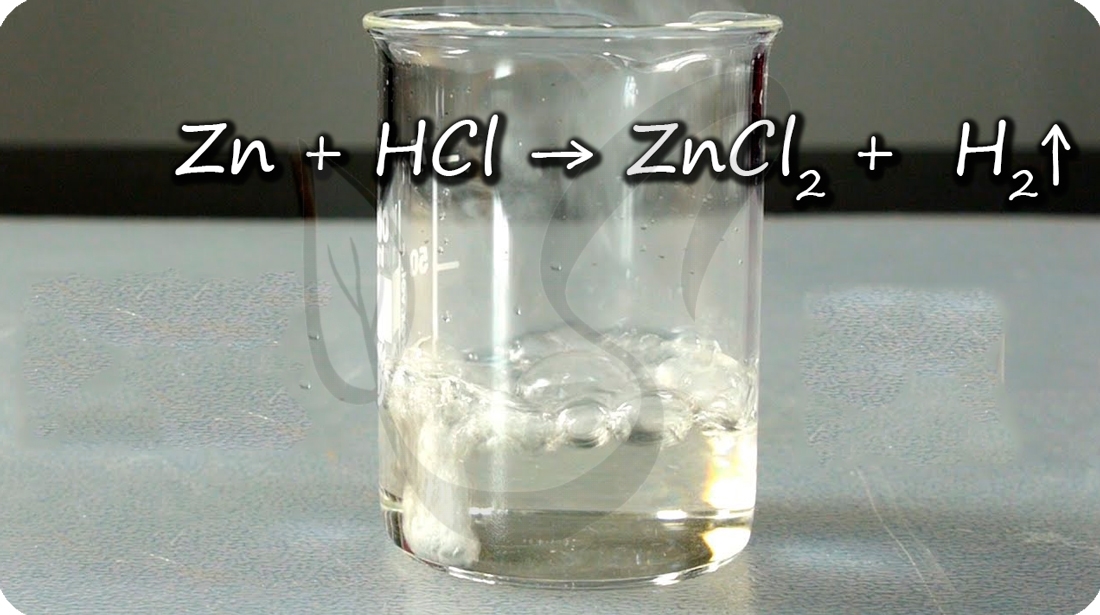
Цинк способен проявлять амфотерные (двойственные) свойства: реагирует как с кислотами, так и с основаниями. При добавлении цинка в раствор щелочи выделяется водород.
Zn + H2O + NaOH = Na2[Zn(OH)4] + H2↑ (тетрагидроксоцинкат натрия)
Соединения цинка II
Эти соединения обладают амфотерными свойствами. Оксид цинка II можно получить в ходе реакции горения цинка или при разложении нитрата цинка.
Оксид цинка II проявляет амфотерные свойства, реагирует как с кислотами, так и с щелочами.
ZnO + H2O + 2NaOH = Na2[Zn(OH)4] (тетрагидроксоцинкат натрия)
Комплексные соли образуются в растворе, при прокаливании они не образуются.
ZnO + 2NaOH = (t) H2O + Na2ZnO2 (цинкат натрия)
Оксид цинка II может быть восстановлен до чистого цинка различными восстановителями.
ZnO + C = (t) Zn + CO
ZnO + CO = (t) Zn + CO2
Гидроксид цинка II получается в ходе реакций между растворимыми солями цинка и щелочами.

Гидроксид цинка II обладает амфотерными свойствами, реагирует как с кислотами, так и с основаниями.
При прокаливании комплексные соли распадаются, вода испаряется.
Драгоценный металл, известный человеку с древнейших времен. Встречаемся в самородном виде. Будучи благородным металлом, серебро обладает низкой реакционной способностью.

-
Реакции с неметаллами
Серебро не окисляется кислородом даже при высокой температуре. Галогены легко окисляют серебро до соответствующих галогенидов. При нагревании с серой получается сульфид серебра.
Реакции с кислотами
Серебро не растворяется в соляной и разбавленной серной кислотах, однако способно реагировать с концентрированными кислотами.
Потемнение серебряных изделий обусловлено реакцией серебра с сероводородом в присутствии кислорода.

С органическими веществами
В дальнейшем, при изучении органической химии, вы не раз столкнетесь с соединением серебра - аммиачным раствором оксида серебра.
Будет полезно, если вы уже сейчас познакомитесь с его формулой на примере реакции окисления уксусного альдегида до уксусной кислоты.
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
- Интерактивное изображение
содержание
- 1 Получение
- 1.1 структуры
- 2 Химические свойства
- 2,1 - ЯМР
- 3 Приложения
- 4 Меры предосторожности
- 5 Ссылки
- 6 Внешние ссылки
подготовка
Марганец хлорид получают путем обработки оксида марганца (IV) с концентрированной соляной кислотой.
Эта реакция была когда - то использовали для производства хлора . Путем тщательного нейтрализации полученного раствора с МпСО 3 , можно селективно осадить соли железа, которые являются общими примесями в двуокиси марганца.

В лаборатории, хлорид марганца может быть получен путем обработки марганца металла или марганца (II) карбоната с соляной кислотой :
Безводный MnCl 2 принимает слоистый хлорид кадмия -подобной структуры. Тетрагидрат состоит из октаэдрических цис -mn (H 2 O) 4 Cl 2 молекул. Транс - изомер, который является метастабильной, также известен. Дигидрат MnCl 2 (Н 2 О) 2 представляет собой координационный полимер . Каждый центр Мп координируется к четырем двукратно мостиковых лигандов хлорида . Восьмигранник завершается парой взаимно транс aquo лигандов .

Химические свойства
Гидраты растворяются в воде с получением слегка кислые растворы с рН около 4. Эти растворы состоят из металла aquo комплекс [Mn (Н 2 О) 6 ] 2+ .
Это является слабой кислотой Льюиса , реакции с хлоридными ионами , чтобы произвести ряд твердых веществ , содержащих следующие ионы [MnCl 3 ] - , [MnCl 4 ] 2- и [MnCl 6 ] 4- . Оба [MnCl 3 ] - и [MnCl 4 ] 2- являются полимерными .
После обработки с типичными органическими лигандами, марганец (II) , подвергает окисление воздуха с получением Mn (III) комплексов . Примеры включают [Mn ( ЭДТА )] - , [Mn ( CN ) 6 ] 3- и [Mn ( ацетилацетонат ) 3 ]. Трифенилфосфин образует лабильный 2: 1 аддукт :
Безводный хлорид марганца (II) , служит в качестве отправной точки для синтеза различных соединений марганца. Например, манганоцен получают путем реакции MnCl 2 с раствором циклопентадиенилнатрий в ТГФ .
Водные растворы хлорида марганца (II) используют в 31 С-ЯМР для определения размера и ламеллярности из фосфолипидных везикул . Когда хлорид марганца добавл ют к раствору везикулярному, Mn 2+ парамагнитные ионы высвобождаются, возмущая время релаксации фосфолипидов фосфатных групп и расширение полученного 31 P резонансного сигнала . Только фосфолипиды , расположенные в наружном монослое воздействию Mn 2+ опыта это уширение. Эффект незначителен для многослойных везикул, но для больших однослойных везикул, наблюдается
уменьшение интенсивности сигнала 50%.
Приложения
Марганец хлорида в основном используется в производстве батарей сухих клеток. Это предшественник антидетонационная соединения трикарбонила метилциклопентадиенил марганца .
Меры предосторожности
Отравление марганцем , или отравление марганца, может быть вызвано длительным воздействием марганца пыли или паров.
Задание 417
Марганец окисляется азотной кислотой до низшей степени окисления, а рений приобретает высшую степень окисления. Какие соединения при этом получаются? Составьте электронные и молекулярные уравнения соответствующих реакций.
Решение:
а) Марганец взаимодействует с азотной кислотой с образованием нитрата марганца (II) оксида азота (II):
Уравнения электронного баланса:
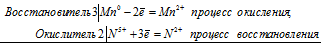
3Mn 0 + 2N 5+ = 3Mn 2+ + 2N 2+
Молекулярное уравнение реакции:
б) Рений окисляется азотной кислотой до высшей степени окисления. При этом образуются рениевая кислота HReO4 и оксид азота (II) NO:
Уравнения электронного баланса:
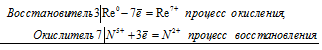
3Re 0 + 7N 5+ = 3Re 2+ + 7N 2+
Молекулярное уравнение реакции:
Задание 418
Хлор окисляет манганат калия К2MnO4. Какое соединение при этом получается? Как меняется окраска раствора в результате этой реакции? Составьте электронные и молекулярное уравнения реакции.
Решение:
При окислении хлором манганата калия образуются перманганат калия и хлорид калия:
Уравнения электронного баланса:
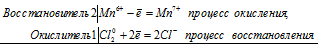
2Mn 6+ + Сl2 0 = 2Mn 7+ + 2Cl -
Молекулярное уравнение реакции:
Манганат-ионы MnO4 2- окрашивают раствор в ярко-зелёный цвет, перманганат-ионы MnO4 - в красно-фиолетовый. Поэтому при окислении манганата калия хлором раствор изменяет окраску с ярко-зелёного на красно-фиолетовый цвет.
Задание 419
Как меняется степень окисления марганца при восстановлении КМпО4 в кислой, нейтральной и щелочной средах? Составьте электронные и молекулярное уравнения реакций между КМпО4 и KNO2 в нейтральной среде.
Решение:
Степень окисления марганца при восстановлении КМпО4 в кислой, нейтральной и щелочной средах меняется следующим образом: в кислой среде марганец уменьшает свою степень окисления от +7 до +2 (перманганат-ион MnO4 - превращается в ион Mn 2+ ); в нейтральной среде марганец уменьшает свою степень окисления от +7 до +4 (ион MnO4- восстанавливается до MnO2); в щелочной среде марганец уменьшает свою степень окисления от +7 до +6 (ион MnO4 - превращается в ион MnO4 2- ).
Электронные и молекулярное уравнения реакций между КМпО4 и KNO2 в нейтральной среде:
Уравнения электронного баланса:
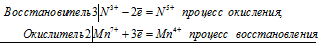
2Mn 7+ + 3N 3+ = 2Mn 4+ + 3N 5+
Молекулярное уравнение реакции:
Задание 420
На основании электронных уравнений составьте уравнение реакции получения манганата калия K2MnO4 сплавлением оксида марганца (IV) с хлоратом калия КСlО3 в присутствии гидроксида калия. Окислитель восстанавливается максимально, приобретая низшую степень окисления.
Решение:
При сплавлении MnO2 со щёлочью ) с хлоратом калия КСlО3 в присутствии гидроксида калия образуются манганат калия, хлорид калия и вода:
Уравнения электронного баланса:

3Mn 4+ + Сl 5+ = 3Mn 6+ + Cl -
Молекулярное уравнение реакции:
Задание 421
Почему оксид марганца (IV) может проявлять и окислительные, и восстанвительные свойства? Исходя из электронных уравнений, составьте уравнения реакций:
а)МnО2 + КI + Н2SO4 = ; б)МnO2 + КNO3 + КОН = .
Решение:
Марганец в MnO2 находится в своей промежуточной степени окисления +4, поэтому в окислительно-восстановительных реакциях атом марганца в оксиде марганца (IV) может как увеличивать свою степень окисления, т.е. проявлять свойства восстановителя, так и уменьшать свою степень окисления – проявлять свойства окислителя.
Уравнения реакций:
Уравнения электронного баланса:
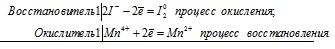
Mn 4+ + 2I - = Mn 2+ + I2 0
Молекулярное уравнение реакции:
Уравнения электронного баланса:
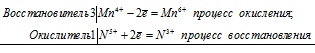
Mn 4+ + N 5+ = Mn 6+ + N 3+
Молекулярное уравнение реакции:
Задание 422
Для получения хлора в лаборатории смешивают оксид марганца (IV) с хлоридом натрия в присутствии концентрированной серной кислоты. Составьте электронные и молекулярное уравнения этой реакции.
Решение:
Уравнения электронного баланса:
Марганец — элемент 4-го периода и VII B-группы Периодической системы, порядковый номер 25. Электронная формула атома [18Аr]Зd 5 4s 2 ; характерные степени окисления + VII,+ VI, +IV, +III, +II и 0.
Шкала степеней окисления марганца:
По электроотрицательности (1,60) марганец занимает промежуточное положение между типичными металлами (Na, К, Са, Мg) и неметаллами (F, O,N, Cl). Соединения Мn ‖‖ — оксид и гидроксид — проявляют основные свойства, соединения Мn ‖‖‖ и Мn IV — амфотерные свойства, для соединений Мn VI и Мn VII характерно почти полное преобладание кислотных свойств. Марганец образует многочисленные соли и бинарные соединения.
В природе — четырнадцатый по химической распространенности элемент (восьмой среди металлов; второй, после железа, тяжелый металл).
Марганец Мn. Серебристо-белый (с серым оттенком) металл, более твердый и хрупкий по сравнению с железом. В виде мелкого порошка пирофорен. На воздухе покрывается оксидной пленкой. Пассивируется в воде, поглощает водород, но не реагирует с ним.
При нагревании сгорает в кислороде воздуха, реагирует с хлором и серой:
Mn→(O2, до450 o C) MnO2 →( O2, до 800 o C) Mn2O3
Mn→MnO+( Mn II Mn2 II )O4 “окалина “ ( O2, выше 800 o C)
Mn+Cl2→MnCl2 , (200 o C) Mn+S→ MnS (до1580 o C)
В ряду напряжений марганец стоит левее водорода, из разбавленных кислот НCl и Н2SO4 вытесняет водород:
Взаимодействует с кислотами-окислителями при нагревании, также образуя соли марганца (II):
Получение марганца в промышленности — восстановление пиролюзита МnO2 или гаусманита (Мn II Mn II I )O4 коксом или алюминием:
3(Мn II Mn III )O4 + 8Аl = 9Мn + 4А12O3(700-900 °С)
Наиболее чистый марганец выделяют электролизом раствора из солей марганца (П), например:
Промышленно важен сплав с железом — ферромарганец (> 70 % Мn), его получают восстановлением оксидных руд марганца и железа.
Применяется марганец для изготовления специальных и тугоплавких сплавов, зеркального чугуна и марганцевых твердых сталей, в качестве катализатора в органическом синтезе.
Оксид марганца (IV) МnO2. Черный, с коричневым оттенком, при нагревании разлагается. Из раствора осаждается в виде черного гидрата МnO2 nН2O. Не проявляет амфотерных свойств в силу малой реакционной способности по отношению к воде, разбавленным кислотам НCl и Н2SO4, азотной кислоте и щелочам в растворе. Типичный окислитель в растворе и расплаве, менее характерны свойства восстановителя.
Уравнения важнейших реакций:
В природе самое распространенное соединение марганца — минерал пиролюзит
Манганат калия К2MnO4. Оксосоль. Темно-зеленый, плавится под избыточным давлением О2. В растворе устойчив только в сильнощелочной среде. Зеленая окраска раствора отвечает иону МnO4 2- . Медленно разлагается при разбавлении раствора водой, быстро — при подкислении. Проявляет окислительно-восстановительные свойства.
Качественная реакция — появление фиолетовой окраски при подкислении раствора. Промежуточный продукт при синтезе КMnO4.
Уравнения важнейших реакций:
Получение: сплавление МnO2 с сильными окислителями (KNO3, КClO3).
Перманганат калия КМnO4. Оксосоль. Красно-фиолетовый (почти черный). При нагревании разлагается без плавления. Умеренно растворим в воде (интенсивно-фиолетовая окраска раствора отвечает иону МnO4), гидролиза нет. Медленно разлагается в воде, серной кислоте, щелочах. Сильный окислитель в растворе и при сплавлении; в сильнокислотной среде восстанавливается до Мn II , в нейтральной среде – до Mn IV в сильнощелочной среде — до Мn VI

Качественная реакция на ион МnO4 — исчезновение фиолетовой окраски раствора при восстановлении в кислотной среде.
Применяется как окислитель углеводородов до карбоновых кислот, реактив в фотографии, антисептик в медицине, средство для очистки газов и отбеливания тканей, твердый источник кислорода. Распространенный окислитель в лабораторной практике. Уравнения важнейших реакций:
МnO4 — + 8Н + + 5Fе 2+ = Мn 2+ + 5Fе 3+ + 4Н2O
Устойчивые оксиды и гидроксиды марганца:
- степень окисления +2:
- MnO - основной оксид
- Mn(OH)2 - основание
- степень окисления +3:
- Mn2O3 - основной оксид
- Mn(OH)3 - основание
- степень окисления +4:
- MnO2 - амфотерный оксид
- Mn(OH)4 - амфотерный гидроксид
- степень окисления +6:
- MnO3 - кислотный оксид
- H2MnO4 - кислота
- степень окисления +7:
- Mn2O7 - кислотный оксид
- HMnO4 - кислота
Свойства соединений марганца, указанных выше, изменяются с ростом степени окисления марганца (сверху-вниз) следующим образом:
- степень окисления - возрастает
- кислотные свойства - увеличиваются
- окислительная способность - увеличивается
Оксид марганца MnO(II)
- кристаллы серо-желтого цвета;
- плохо растворяется в воде;
- обладает свойствами полупроводника;
- как основной оксид реагирует с кислотами:
MnO+2HCl = MnCl2+H2O - реагирует в термических реакциях с водородом и активными металлами с образованием марганца:
MnO+H2 = Mn+H2O
MnO+Ca = Mn+CaO - получают MnO(II) разлагая гидроксид марганца (или нитрат марганца):
Mn(OH)2 = MnO+H2O
2Mn(NO3)2 = 2MnO+4NO2+O2
Гидроксид марганца Mn(OH)2(II)
- кристаллы светло-розового цвета;
- обладает слабыми восстановительными свойствами;
- как основание, взаимодействует с кислотами:
Mn(OH)2+2HCl = MnCl2+2H2O - реагирует с кислородом и другими окислителями, окисляясь до марганцовой кислоты или солей ее манганатов:
6Mn(OH)2+O2 = 2Mn2MnO4+6H2O - Mn(OH)2(II) получают взаимодействием щелочей на растворы солей марганца:
MnSO4+2NaOH = Mn(OH)2↓+Na2SO4
Оксид (диоксид) марганца MnO2(IV)
- вещество коричнево-черного цвета;
- нерастворимо в воде;
- обладает амфотерными свойствами:
MnO2+2KOH = K2MnO3+H2O
MnO2+2H2SO4 = Mn(SO4)2+2H2O - проявляет, как окислительные, так и восстановительные свойства, в зависимости от кислотных свойств другого взаимодействующего вещества:
2MnO2+3PbO2+6HNO3 = 2HMnO4+3Pb(NO3)2+2H2O (восстановитель)
MnO2+4HCl = MnCl2+Cl2↑+2H2O (окислитель)
- в производстве марганца и его соединений;
- в производстве коричневой краски;
- в сухих источниках энергии;
- в производстве стекла, в качестве осветлителя;
- в качестве окислителя в органической химии.
Оксид марганца Mn2O7(VII)
- жидкость зелено-черного цвета жирной консистенции;
- неустойчивое вещество;
- tпл = 5,9°C
- ρ = 2,4 г/см 3
- при нагревании выше 50°C разлагается на кислород и низший оксид марганца (при высокой температуре взрывается):
2Mn2O7 = 4MnO2+3O2 - является очень сильным окислителем, воспламеняет горючие вещества;
- как кислотный оксид реагирует с щелочами, образуя соли перманганаты:
Mn2O7+2KOH = 2KMnO4+H2O - взаимодействует с водой с образованием марганцовой кислоты, существующей только в растворах:
Mn2O7+H2O = 2HMnO4 - получают взаимодействием концентрированной серной кислоты на водный р-р перманганата калия:
2KMnO4+H2SO4 = Mn2O7+K2SO4+H2O
Соли марганца (II)
Соли марганца получают растворением марганца в разбавленных кислотах, при этом получается бесцветный раствор, который при взаимодействии с щелочами мутнеет по причине выпадения в осадок гидроксида марганца (II), быстро темнеющего на воздухе с переходом в гидроксид марганца (IV) бурого цвета.
2Mn(OH)2+O2+2H2O = 2Mn(OH)4
Марганцовая кислота
Как уже было сказано выше, марганцовая кислота является сильной кислотой, существующей только в водном растворе. Соли марганцовой кислоты называются перманганатами, самым известным из которых является, конечно же, перманганат калия KMnO4, который в быту называют "марганцовкой".
Во времена СССР ампулу с марганцовкой можно было купить в любой аптеке. Сейчас, перманганат калия "простому смертному" практически не достать, и дело тут не в дефиците, а в специфических свойствах марганцовки, о которых мы не будем распространяться.
Свойства перманганата калия:
- кристаллы темно-фиолетового цвета;
- умеренно растворяется в воде, окрашивая ее в цвет от малинового до темно-фиолетового, в зависимости от концентрации ионов MnO4 - , имеющих фиолетовый цвет;
- является сильным окислителем, в зависимости от кислотности среды, манганаты восстанавливаются с образованием:
- в кислой среде ионы MnO4 - восстанавливаются до ионов Mn 2+ - при добавлении сульфита калия к подкисленному серной кислотой фиолетовому раствору KMnO4, тот обесцвечивается по причине образования соли марганца (II):
2KMn +7 O4+5K2S +4 O3+3H2SO4 = 2Mn +2 SO4+6K2S +6 O4+3H2O - в нейтральной среде при действии сульфита калия образуется бурый осадок оксида марганца (IV), при этом марганец изменяет свою степень окисления с +7 до +4:
2KMnO4+3K2SO3+H2O = 2MnO2↓+3K2SO4+2KOH - в щелочной среде происходит восстановление до манганата, о чем свидетельствует образование манганат-ионов, окрашивающих раствор в зеленый цвет:
2KMnO4+K2SO3+2KOH = 2K2MnO4+K2SO4+H2O
- в кислой среде ионы MnO4 - восстанавливаются до ионов Mn 2+ - при добавлении сульфита калия к подкисленному серной кислотой фиолетовому раствору KMnO4, тот обесцвечивается по причине образования соли марганца (II):
- перманганаты разлагаются при термическом воздействии с выделением кислорода:
2KMnO4 = K2MnO4+MnO2+O2↑ - мелкораздробленные кристаллы марганца при нагревании растворяются в воде, выделяя водород:
Mn+2H2O = Mn(OH)2+H2↑
Если вам понравился сайт, будем благодарны за его популяризацию :) Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Читайте также:

