Шкала боли по баллам таблица при онкологии
Лечение болевого синдрома в онкологии
Несмотря на выдающиеся достижения современной онкологии, проблема терапии боли у пациентов с онкозаболеваниями остается актуальной и у нас, и за рубежом. Общеизвестно, что практически каждый третий пациент, впервые пришедший на прием к онкологу, испытывает боль разной степени интенсивности.
Подбор и назначение эффективной противоболевой терапии – сложная задача, требующая многокомпонентного подхода. Для правильного и адекватного обезболивания при раке врачу-онкологу необходимо собрать анамнез боли: причина, давность, интенсивность, локализация, тип, факторы, усиливающие или уменьшающие боль; время возникновения боли в течение дня, применявшиеся ранее анальгетики, их дозы и эффективность.


Осмотр и клинико-лабораторные исследования важны для выбора наиболее безопасного для конкретного пациента комплекса анальгетиков и адъювантных средств.
Причиной боли при онкологическом заболевании является:
-
Боль, вызванная самой опухолью (поражение костей, мягких тканей, кожи, внутренних органов, органов пищеварительного тракта);
Боль при осложнениях опухолевого процесса (патологический перелом, некроз, изъязвление, воспаление, инфицирование тканей и органов, тромбозы);
Боль при паранеопластическом синдроме;
Боль при последствиях астенизации (пролежни);
- при осложнениях хирургического лечения (например, фантомная боль),
- при осложнениях химиотерапии (стоматит, полинейропатия и др.),
- при осложнениях лучевой терапии (поражение кожи, костей, фиброз и др).
Классификация болевого синдрома:
Специалистами разработана классификация болевых синдромов при онкологии, каждый из которых требует особенного подхода в терапии.
По локализации источника боли
По временным параметрам
По степени выраженности боли
Оценка интенсивности хронического болевого синдрома
0 баллов – боли нет, 1 балл – слабая боль, 2 балла – боль умеренная, 3 балла – боль сильная, 4 балла – нестерпимая, самая сильная боль.
Нередко онкологи применяют визуально-аналоговую шкалу интенсивности боли от 0 до 10, на которой предлагают пациенту отметить степень своих болевых ощущений. Эти шкалы позволяют количественно оценить динамику хронического болевого синдрома в процессе лечения.

На основании данных диагностики врач-онколог устанавливает причину, тип, интенсивность хронического болевого синдрома, локализацию боли, сопутствующие осложнения и возможные психические нарушения.


Пример "болевого" опросника, который заполняет врач-онколог при первичном осмотре пациента
На последующих этапах наблюдения и терапии лечащий врач проводит повторную оценку эффективности обезболивания, выраженности побочных эффектов фармакотерапии. Этим достигается максимальная индивидуализация терапии болевого синдрома, отслеживаются возможные побочные эффекты применяемых анальгетиков и динамика состояния пациента.
Основные принципы назначения фармакотерапии боли у онкологических пациентов:
- Прием обезболивающих препаратов по часам, а не по требованию. Соблюдение этого принципа позволяет достичь наибольшего эффекта с минимальной суточной дозой обезболивающего препарата.
Адекватная доза и режим приема анальгетиков должны соблюдаться как основа противоболевого действия;
Лечение по восходящей - означает, что лечение боли у онкологических больных следует начинать с ненаркотических препаратов, постепенно переходя к более сильным препаратам.
Трехступенчатая схема обезболивания при раке

- На первом этапе лечения боли слабой и средней интенсивности применяются ненаркотические препараты (неопиды). Основными препаратами этой группы являютсяаспирин, парацетамол, анальгин, седальгин, пентальгин, диклофенак и пр.
Необходимо понимать, что использование ненаркотических анальгетиков в лечении более сильной боли ограничено их способностью к обезболиванию. Обезболивающий эффект имеет свои пределы и не усиливается бесконечно с увеличением дозы препарата. При этом возрастает только опасность побочных реакций и проявлений токсичности.
- Поэтому когда боль у онкологических пациентов усиливается, несмотря на увеличение дозы обезболивающих препаратов, наступает второй этап лечения боли – добавление мягких опиоидных анальгетиков. Это трамал, трамадол, кодеин, дионин.
Обращаем ваше внимание, что подбор и дозировку анальгетиков проводит только врач-онколог!
- Когда применение ненаркотических препаратов не дает нужного эффекта, лечащий врач переходит к использованию препаратов третьего этапа - сильных опиатов (просидол, норфин, морфин, дюрогезик, MST-Continus, фендивия).
Дюрогезик – трансдермальный пластырь - содержит фентанил в дозе 25, 50. 75 и 100 мкг/час и выпускается в виде пластыря, содержащего резервуар с обезболивающим препаратом. Доза зависит от размера пластыря. Длительность действия препарата составляет 72 часа.

Наряду с основными анальгетиками (опиаты и неопиаты) большое значение имеют адъювантные, то есть вспомогательные препараты – кортикостероиды (дексаметазон), антидепрессанты (амитриптилин), противосудорожные (карбамазепин), антигистаминные, транквилизаторы.
Эти препараты используются в основном при лечении отдельных симптомов и осложнений у онкологических больных.
Лечение нейропатической боли
Лечение нейропатической (жгучей) боли представляет собой значительно более сложную задачу вследствие недостаточной эффективности большинства анальгетиков.
По статистике более 50% пациентов, имеющих нейропатическую боль, продолжают испытывать ее на фоне назначенного лечения опиоидами, что свидетельствует о низкой эффективности традиционных обезболивающих препаратов.
В Европейских рекомендациях по лечению нейропатической боли препаратами первой линии названы антиконвульсанты, антидепрессанты и местные анестетики – это амитриптилин, габапентин и прегабалин.
Прегабалин – препарат последнего поколения, обладающий меньшими побочными эффектами, полной безопасностью, эффективностью начальной дозы и быстрым началом действия.
Важной особенностью прегабалина является его способность уменьшать и полностью нивелировать остроту болевых ощущений, что подтверждается значительным снижением (в 2-5 раз) числа жалоб на жгучие, простреливающие и режущие боли. Это способствует улучшению качества жизни онкологических больных с хроническими болевыми синдромами.


Подводя итоги, мы хотим еще раз подчеркнуть, что один из важнейших принципов лечения болевого синдрома в онкологии – принцип индивидуальности. Выбор препарата для обезболивания при раке, а также подбор дозировки в каждом конкретном случае зависит от причины, вызывающей боль, общего состояния пациента, от наличия и выраженности имеющихся расстройств отдельных органов и систем.
Важно прогнозировать возможные или уже имеющиеся на момент осмотра побочные эффекты предшествующей противоопухолевой или обезболивающей терапии. Следует осуществлять направленный выбор основного препарата для терапии, в зависимости от патогенеза боли (ноцицептивная, нейропатическая, психогенная).
В современной онкологии врачи обладают широким арсеналом препаратов для борьбы с болью онкологического генеза, поэтому почти во всех случаях (>90%) удается полностью купировать болевой синдром или же значительно уменьшить его интенсивность.
Боль – это всегда неприятное ощущение. Но ее интенсивность может быть разной: она зависит от того, какая болезнь развилась, и какой болевой порог имеет человек.
Чтобы врач мог понять, как именно болит – нестерпимо или более-менее умеренно– придуманы так называемые шкалы боли. С их помощью вы можете не только описать свою боль на данный момент, но и сказать, что изменилось с назначением лечения.
Визуальная аналоговая шкала
Это та шкала, которой чаще всего пользуются анестезиологи и онкологи. Она представляет собой возможность оценить интенсивность боли – без всяких подсказок.

Пациент должен поставить точку там, где, как он чувствует, располагается его боль. Врач берет линейку и смотрит, на какой отметке находится точка пациента:
- 0-1 см – боль крайне слабая;
- от 2 до 4 см – слабая;
- от 4 до 6 см – умеренная;
- от 6 до 8 см – очень сильная;
- 8-10 баллов – нестерпимая.
Модифицированная визуальная аналоговая шкала
Суть оценки боли – такая же, как и в предыдущем случае. Единственное отличие этой шкалы – в цветовой маркировке, на фоне которой и нарисована линия. Цвет идет градиентом: от зеленого, который начинается от 0, к 4 см сменяется желтым, а к 8 см – красным.
Вербальная ранговая шкала
Она очень напоминает визуальную аналоговую шкалу: так же линия длиной в 10 см, которую можно прочертить при пациенте самостоятельно. Но отличие есть: каждые 2 см следует надпись:
- на 0 см – боли нет;
- на 2 см – слабая боль;
- на отметке 4 см – умеренная боль;
- на 6 см – сильная;
- на 8 см – очень сильная;
- в конечной точке – невыносимая боль.
В этом случае человеку уже легче сориентироваться, и он ставит точку, исходя из того, с каким эпитетом у него больше всего ассоциируется собственное состояние.
Положительные стороны этого метода оценки боли в том, что с ее помощью можно оценивать и острый, и хронический болевой синдром. Кроме того, шкалу можно применять у детей, начиная от младших школьников, а также людей с начальными степенями деменции.

Эта шкала может применяться для определения интенсивности боли у людей в глубокой деменции. Она состоит из 7 рисунков лиц с эмоциями, каждая из которых схематично передает силу болевого синдрома. Расположены они по нарастанию боли.
Почему именно рисунки, да еще и такие примитивные? Потому, что с таких рисунков эмоцию легче считать и труднее неверно истолковать, чем с произведения искусства или фотографии.
Модифицированная лицевая шкала
Она состоит из 6 лиц, каждое из которых изображает эмоцию, соответствующую описанию боли по вербальной ранговой шкале. Она также используется для оценки интенсивности болевого синдрома при деменции и тоже проводится после короткого вступительного слова.
Шкала, которую используют для лежачих и потерявших речь больных
Реаниматологи применяют шкалу CPOT, которая позволяет им, не разговаривая с пациентом, оценить степень его боли. Они учитывают 4 параметра:
- Хронические запоры у пожилых людей: лечение и профилактика
- Почечная недостаточность в пожилом возрасте
- Реабилитация после эндопротезирования тазобедренного сустава
- Напряжение мышц рук.
- Выражение лица.
- Попытки говорить или сопротивление дыхательному аппарату.
- Двигательные реакции.
Каждый параметр оценивается от 0 до 2 баллов, после чего баллы суммируются.

Трактовка такая:
0-2 балла – боли нет;
3-4 балла – слабая боль;
5-6 баллов – умеренная боль;
7-8 баллов – боль сильная;
9-10 – очень сильная боль.
Наиболее полная оценка боли – опросник Мак-Гилла


Благодаря этому опроснику (анкете) можно оценить три основные системы формирования и проведения боли:
- нервные волокна, которые проводят непосредственно болевые ощущения;
- структуры, которые есть и в спинном, и головном мозге: ретикулярная формация и лимбическая система;
- отделы в коре головного мозга, которые занимаются оценкой и уже конечной интерпретацией боли.
Поэтому анкета условно разделена на 4 группы:
- для определения сенсорных характеристик боли;
- для оценки того, какие боль затрагивает эмоциональные компоненты;
- для оценки того, как боль оценивается головным мозгом;
- группа слов, которые направлены на оценку сразу всех критериев.
Физически опросник выглядит как 20 граф, в каждой из которых расположено от 1 до 5 эпитетов, расположенных по порядку – в соответствии с интенсивностью боли. Человеку нужно обвести столько из них, сколько поможет ему точно описать свои ощущения.
Оценка болевого индекса производится по тому, сколько слов было использовано для описания боли по каждому из 4 параметров. Также важно, какие порядковые номера применялись для оценки в каждом аспекте. И, наконец, суммируются порядковые номера выбранных эпитетов, вычисляется их среднеарифметическая величина.
Для чего нужны шкалы боли
Шкалами боли пользуются не все врачи. Их применяют, в основном, анестезиологи-реаниматологи, терапевты и онкологи. Иногда с ними сталкиваются врачи и других специальностей, когда речь идет о хронических больных.
В зависимости от того, как оценена боль, будет назначаться обезболивающее средство:
Любой из указанных препаратов имеет массу побочных эффектов. Поэтому в интересах пациента – максимально объективно оценивать собственную боль, а при ее изменениях – сообщать об этом врачу. Вот уже если врач никак не реагирует – то его нужно менять на другого специалиста.
Для диагностики болевого синдрома у онкологических пациентов из этических соображений принято применять только неинвазивные методы. В начале необходимо изучить анамнез боли (давность, интенсивность, локализация, тип, факторы, усиливающие или уменьшающие боль; время возникновения боли в течение дня, применявшиеся ранее анальгетики и их дозы и эффективность). В дальнейшем следует провести клинический осмотр пациента с целью оценки характера и распространенность онкологического процесса; изучить физический, неврологический и психический статус пациента. Необходимо ознакомиться с данными клинико-лабораторных методов исследования (клинический и биохимический анализ крови, анализ мочи), что важно для выбора наиболее безопасных для данного пациента комплекса анальгетиков и адъювантных средств (АД, ЧСС, ЭКГ, УЗИ, рентгенография и др.).
Оценку интенсивности хронического болевого синдрома проводят с помощью шкалы вербальных (словесных) оценок (ШВО), визуально аналоговой шкалы (ВАШ), болевых опросников (McGill Pain Questionaire и др.). Наиболее простой и удобной для клинического применения является 5-балльная ШВО, которая заполняется врачом со слов пациента:
0 баллов — боли нет,
1 балл — слабая боль,
2 балла — боль умеренная,
3 балла — боль сильная,
4 балла — нестерпимая, самая сильная боль.
Нередко применяют визуально-аналоговую шкалу (ВАШ) интенсивности боли от 0 до 100%, которую предлагают пациенту, и он сам отмечает на ней степень своих болевых ощущений.

Эти шкалы позволяют количественно оценить динамику хронического болевого синдрома в процессе лечения.
Оценка качества жизни онкологического пациента может быть достаточно объективно проведена по 5-ти балльной шкале физической активности:
- 1 балл — нормальная физическая активность,
- 2 балла — незначительно снижена, больной способен самостоятельно посещать врача,
- 3 балла — умеренно снижена (постельный режим менее 50% дневного времени,
- 4 балла — значительно снижена (постельный режим более 50% дневного времени),
- 5 баллов — минимальная (полный постельный режим).
Для оценки общего состояния онкологического больного применяется шкала оценки качества жизни по Карнофски, где динамику степени активности пациента измеряют в процентах:
| А: Нормальная активность и работоспособность. Никакой специальной помощи не требуется. | 100% Норма. Никаких жалоб. Никаких признаков болезни. |
| 90% Нормальная активность, незначительные признаки и симптомы болезни. | |
| 80% Нормальная активность, некоторые признаки и симптомы болезни. | |
| В: Пациент неработоспособен, но может жить дома и обслуживать себя сам, некоторая помощь требуется. | 70% Больной обслуживает себя, но не может осуществлять нормальную активность. |
| 60% Больной обслуживает себя в большинстве случаев. Иногда требуется помощь. | |
| 50% Необходима значительная и часто медицинская помощь. | |
| С: Пациент не может обслуживать себя. Требуется стационарная помощь. Болезнь может быстро прогрессировать. | 40% Инвалидность. Требуется специальная помощь и поддержка. |
| 30% Тяжелая инвалидность. Госпитализация показана, хотя угрозы жизни нет. | |
| 20% Госпитализация и активная поддерживающая терапия необходимы. | |
| 10% Фатальные процессы быстро прогрессируют. | |
| 0% Смерть |
Для более детальной оценки применяется целый комплекс критериев, рекомендуемый Международной Ассоциацией по изучению боли (IASP, 1994), включающий следующие параметры:
- общее физическое состояние
- функциональная активность
- социальная активность,
- способность к самообслуживанию
- коммуникабельность, поведение в семье
- духовность
- удовлетворенность лечением
- планы на будущее
- сексуальные функции
- профессиональная деятельность
Для оценки переносимости анальгетической терапии учитывают появление побочного эффекта, вызванного тем или иным препаратом (сонливость, сухость во рту, головокружение, головная боль и др.) и степень его выраженности по 3-х балльной шкале:
0 — нет побочных эффектов,
1 — слабо выражен,
2 — умеренно выражен,
3 — сильно выражен.
При этом следует помнить, что у больных с распространенными формами опухолей могут присутствовать симптомы, сходные с побочным действием многих анальгетиков (тошнота, сухость во рту, головокружение, слабость), поэтому важно начать оценку исходного статуса до начала анальгетической терапии или ее коррекции.
Для углубленной оценки боли в специальных научных исследованиях применяются нейрофизиологические методы (регистрация вызванных понтенциалов, ноцицептивный флексорный рефлекс, исследование динамики условно-негативной волны, сенсометрия, электроэнцефалография), проводится определение плазменного уровня стресс-факторов (кортизола, соматотропного гормона, глюкозы, бета-эндорфина и др.). Последнее время стало возможным объективизировать уровень болевых ощущений по данным активности различных отделов мозга с помощью позитронно-эмиссионной томографии. Но применение этих методов их в ежедневной практике ограничено из-за их инвазивности и высокой стоимости.
Академический интерес представляет тест на опиатную зависимость с налоксоном, который проводят в специализированных клиниках с согласия пациента при длительной (свыше месяца) терапии опиоидными анальгетиками. В обычной практике он не применяется, поскольку может привести к устранению анальгезии и развитию острого абстинентного синдрома.
На основании данных диагностики устанавливается причина, тип, интенсивность хронического болевого синдрома, локализация боли, сопутствующие осложнения и возможные психические нарушения. На последующих этапах наблюдения и терапии необходимо проводить повторную оценку эффективности обезболивания. При этом достигается максимальная индивидуализация болевого синдрома, отслеживаются возможные побочные эффекты применяемых анальгетиков и динамика состояния пациента.
Помогите докторам узнать о мигрени больше. Ваше мнение и ощущения очень важны, чтобы мы могли лучше помогать вам справляться с мигренью!
Болевой синдром при раке проявляется у 35-50% пациентов на ранних стадиях злокачественного процесса. По мере прогрессирования болезни уже до 80% чувствуют боль от умеренной до сильной. В терминальной стадии больно уже почти всем – 95% пациентов. Боль мешает спать, есть, двигаться, принимать осознанные решения, влияет на работу органов и систем.
Хорошая новость в том, что современная медицина научилась держать эту боль под контролем в 90% случаев. То есть либо купировать болевой синдром полностью, либо значительно уменьшать его интенсивность. Таким образом, на любых стадиях рака можно сохранять онкологическим пациентам нормальное качество жизни.
В России есть специфические проблемы, связанные как с получением анальгетиков, особенно наркотических, так и с несоблюдением в некоторых медучреждениях рекомендаций ВОЗ по обезболиванию.
Сегодня постараемся разобраться, какие же лекарства кому и когда нужны, и как еще современная медицина умеет бороться с болью.

Рефлекс отдергивания – здоровая биологическая реакция на острую боль
Но в нездоровом организме онкологического пациента (а также пациента с сердечно-сосудистым заболеванием или ВИЧ, или, например, туберкулезом) боль утрачивает свою полезную сигнальную функцию и наоборот, мешает как основной терапии, так и оказанию паллиативной помощи. Пациент впадает в депрессивное состояние, теряет силы, необходимые для борьбы с болезнью. Хронический болевой синдром превращается в самостоятельную патологию, которую нужно отдельно лечить.
Именно поэтому более чем миллиону человек в России ежегодно требуется обезболивание. Причем от 400 до 800 тысяч из них (по разным подсчетам) нуждаются в опиоидных анальгетиках.
Чтобы разобраться, какой подход нужен для купирования боли, врачу-онкологу нужно понять ее причину и происхождение.
Одна из больших трудностей диагностики ЗНО (злокачественных новообразований) – у пациента часто сначала вообще ничего не болит. Опухоль банально может быть пока слишком маленькой.
Еще такое случается, если опухоль растет в неплотных тканях (таких как молочная железа) или увеличивается внутри полости органа (например, желудка). Также без боли могут развиваться те виды рака, при которых нет солидных первичных опухолей – лейкозы, злокачественные заболевания системы кроветворения.
В нашей практике были случаи, когда бессимптомно протекали даже IV стадии онкологических процессов – вплоть до появления множественных метастазов пациенту не было больно.
Во всех остальных случаях, когда боль присутствует, врачу важно знать, из-за чего она появилась. По причинам возникновения выделим три основных группы.
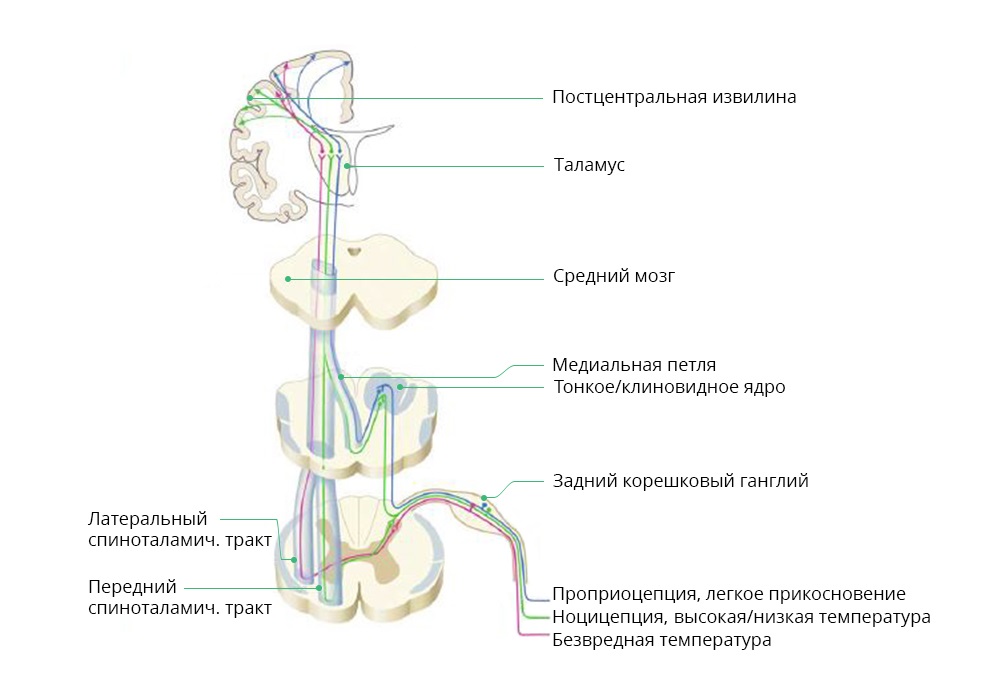
Схема прохождения ноцицептивного и других сигналов от внешних раздражителей
При онкологических заболеваниях ноцицептивная боль, чаще всего, является реакцией на саму опухоль или метастазы. Так, метастазы в позвоночнике могут давать прорывную, резкую боль при перемене положения тела пациентом. Нейропатическая боль. Ее причина – нарушение в работе нервных структур – нервов, спинного или головного мозга. Сочетает два фактора: с одной стороны, интенсивность – пациенту очень больно, иногда не помогают даже сильнодействующие анальгетики. С другой стороны – затруднена локализация. В отличие от острой ноцицептивной боли, пациент часто не может сказать, где именно у него болит.
Такая боль бывает вызвана ростом опухоли или метастаза, когда они давят, например, на позвоночник или защемляют нервные корешки. Также причиной, к несчастью, могут быть и побочные эффекты противоопухолевого лечения.
Дисфункциональная боль. Тот случай, когда органические причины боли отсутствуют, но она не уходит: например, опухоль уже удалили, заживление после операции прошло, а боль осталась. Бывает, что боль, по оценке самого пациента, гораздо сильнее, чем должна быть при его состоянии здоровья.
В таких случаях необходимо учитывать психологическое состояние пациента. Сильный стресс может заметно повлиять на изменения восприятия, вплоть до полностью психогенных болей.
Для выбора адекватной анальгезии врач должен понимать, насколько человеку больно, постараться понять, где именно болит и как долго. От этого зависят назначения в рецепте на обезболивание. Кроме уточняющих вопросов о характере и локализации боли, врач обязательно оценивает ее интенсивность.
Во всем мире для этого используют шкалы НОШ (нумерологическая оценочная шкала) и ВАШ (визуально-аналоговая шкала), либо гибридные варианты – в зависимости от возраста и состояния пациента. Совсем маленьким детям и очень пожилым людям, а также пациентам с когнитивными нарушениями бывает сложно ответить на стандартные вопросы. Иногда приходится работать с такими только по поведению и выражению лиц.

Шкала оценки боли от 0 (ничего не болит) до 10 (нестерпимо больно)
Важно при этом получить как можно больше дополнительной информации: если пациент считает, что терпеть – достойное занятие, а жаловаться – недостойное, или выяснится, что у пациента были периоды злоупотребления и зависимостей, это может внести коррективы в терапию болевого синдрома.
Мы уже затронули тему работы с психологическим состоянием больного, и коснемся ее еще раз – об этом важно помнить и врачам, и близким пациента. ВОЗ даже ввела для этого специальное понятие: суммарная боль. Она охватывает не только физические раздражители, но и эмоциональные и социальные негативные аспекты жизни пациента.
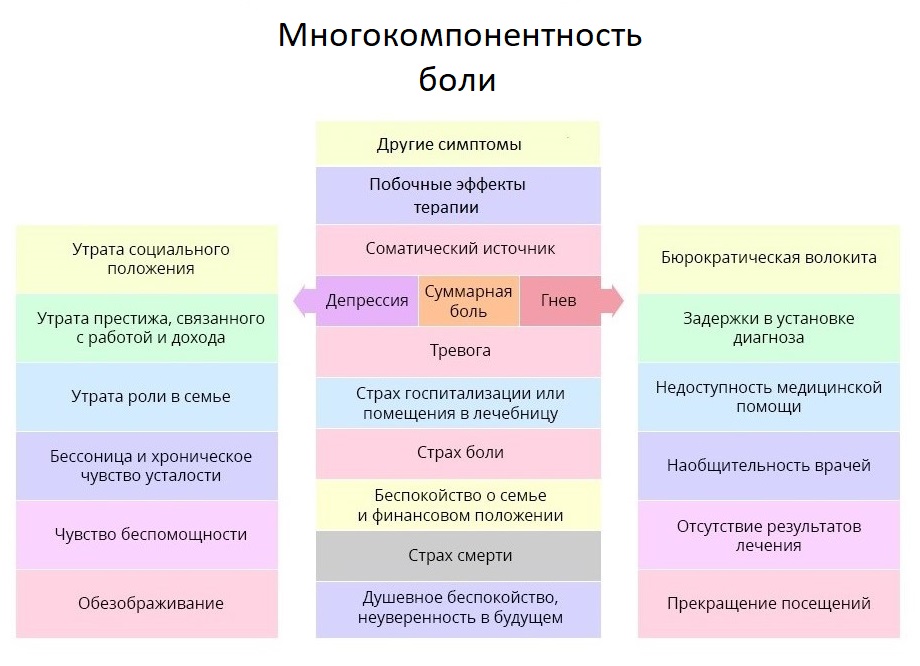
Боль онкопациента куда глубже и сложнее, чем кажется со стороны. Терапия боли – тот случай, когда врач должен относиться к субъективным оценкам пациента с особым вниманием.
Наверное, каждый врач считает более правильными и удачными те препараты, которые оказались наиболее действенными в его личном практическом опыте. Но любой онколог, стремясь купировать болевой синдром, должен помнить про рекомендации ВОЗ для лечения онкологических болей.
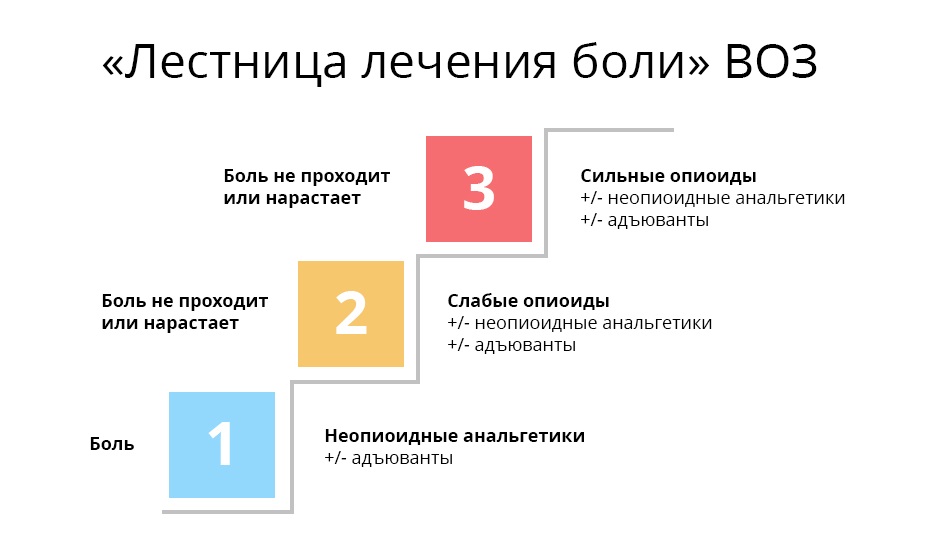
Первая ступень. При слабой боли начинают с ненаркотических анальгетиков и нестероидных противовоспалительных средств и препаратов (НПВС/НПВП). Это привычные безрецептурные парацетамол, ибупрофен, аспирин и др. При мышечной и суставной боли назначают диклофенак и др.

Схема действия НПВС – они блокируют фермент циклооксигеназу, снижая синтез простагландинов, тем самым уменьшая чувствительность болевых рецепторов.
Такие препараты не вызывают привыкания и зависимости, но в большой дозировке могут навредить ЖКТ, поэтому бесконечно и бесконтрольно дозу увеличивать нельзя, чтобы не усложнить ситуацию желудочным кровотечением.
Эндорфины – нейромедиаторы, одна из функций которых – тормозить передачу слабых болевых импульсов из спинного мозга в головной. Это позволяет нам не плакать от боли каждый раз, когда мы ставим локти на стол или спрыгиваем с высоты полуметра. Но при интенсивной боли выработка эндорфинов уменьшается. Опиоидные рецепторы освобождаются, нервные импульсы не тормозятся, человек испытывает боль.
Трамадол принимают вместе с анальгином, парацетамолом и другими медикаментами первой ступени – эффект получается комплексным: одновременное воздействие и на центральную, и на периферическую нервную систему.
Важно, что трамадол, хотя и является опиатом – относится к ненаркотическим анальгетикам. Пациенту проще его получить и не нужно бояться потенциальной зависимости.
Третья ступень. На этой ступени оказываются врач и его пациент, когда ему уже перестали помогать слабые опиаты. В дело вступают сильные опиаты, основной – морфин. Сильные опиаты связываются с опиоидными рецепторами гораздо надежнее слабых, поэтому действуют мощнее. Однако, такой эффект стоит дорого: эти препараты уже могут вызывать зависимость – но только, если употреблять их неправильно и бесконтрольно.
Важно, что на каждой ступени может использоваться так называемая адъювантная, то есть вспомогательная, терапия. Адъювантные препараты не обезболивают самостоятельно, но в сочетании с основными анальгетиками либо усиливают их действие, либо нивелируют побочные эффекты. В эту группу входят антидепрессанты, кортикостероиды, противорвотные и противосудорожные, антигистаминные и т.д.
Таким образом, ВОЗ дает основные принципы и рекомендации для плавного перехода со ступеньки на ступеньку, которые помогают избегать тупика в терапии – когда боль усиливается, а средств борьбы с ней уже не осталось.
Такое случается, если онколог назначает опиоидные препараты раньше времени или в дозе больше необходимого. Если прыгнуть с кеторола на промедол (как, к сожалению, делают некоторые врачи – кто по неопытности, кто из-за отсутствия нужных препаратов), то сначала эффект может превзойти ожидания. Но затем получается, что боль станет требовать увеличения дозировки быстрее, чем предписано безопасным режимом. Ступеньки закончатся раньше, чем вы пройдете нужное количество шагов. В этом случае врач сам у себя отнимает средства лечения.
Строго говоря, как раз уколы, сиречь инъекции, в современном обезболивании стараются не использовать. Выбирать для обезболивания самый болезненный метод введения как-то нелогично.
Поэтому все популярнее сейчас Трансдермальный метод введения – в виде пластырей.
В отличие от инъекций – максимально удобен для пациента. У него есть свои ограничения, конечно – по температуре тела, по количеству подкожно-жировой клетчатки, но в большинстве случаев он хорош:
- препарат (обычно фентанил) высвобождается постепенно, хватает на 72 часа;
- не требует контролировать время приема таблеток или введения препаратов;
- исключает передозировку (это важно для наркотического анальгетика).
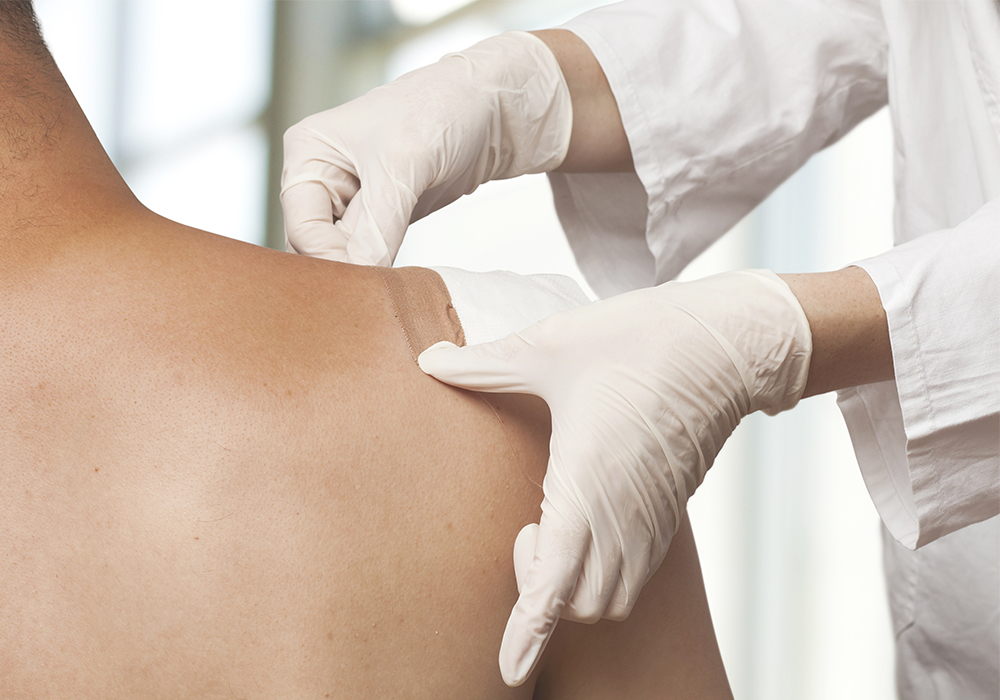
Фентаниловый пластырь – сильное, безопасное и комфортное обезболивание
Эпидуральная анестезия. Да, ее делают не только беременным. Те же препараты, что при спинальной анестезии, вводят в полость между твердой мозговой оболочкой и стенками позвоночного канала. Эпидуральная анестезия используется на поздних стадиях, при метастатическом поражении костей, когда боль не снимается инъекциями и препаратами перорально.
Паллиативная химио-, таргетная и лучевая терапия. Она используется не с целью разрушить опухоль, а с целью просто сделать ее меньше, чтобы освободить сдавленные нервные узлы, вызывающие боль.
Нейрохирургические методы. Нейрохирург надрезает корешки спинномозговых или черепных нервов. Это не приводит к утрате двигательной активности (хотя может потребовать реабилитации), но мозг лишается возможности получать болевые сигналы по этому пути.
Радиочастотная абляция (РЧА). В первом нашем посте, про паллиативную медицину, мы прикрепляли видео о том, как этот метод помог пациентке избавиться от болевого синдрома на последней стадии рака. Тогда РЧА применялась для того, чтобы разрушить метастазы, давившие на нервные корешки спинного мозга.
В случаях же, когда разрушить метастазы или саму опухоль невозможно, РЧА можно использовать для разрушения проводящих нервных путей. Это похоже на предыдущий вариант, только хирург действует не скальпелем, а специальной иглой, разогретой радиочастотными колебаниями до высокой температуры.
Нейролизис при помощи эндосонографии. Нейролизис – это разрушение нервного пути, проводящего боль, с помощью специальных химических растворов. Под контролем ультразвука эндоскоп подводят точно к чревному (солнечному) нервному сплетению через ЖКТ и разрушают часть нервных волокон. Обезболивающий эффект от процедуры наступает в 90% случаев при раке желудка или, например, поджелудочной железы. Сохраняется результат процедуры от месяца до года в редких случаях. Все зависит от скорости развития опухоли. При том, что в случае с применением препаратов-анальгетиков, их пришлось бы применять еженедельно.
Вертебропластика. Этот способ можем пояснить на живом примере из собственной практики. Повреждение позвоночника метастазами приводит к разрушению тела позвонка. Костная структура позвонка деформируется, происходит компрессия (сдавливание) спинномозговых корешков. Возникает корешковый компрессионный сидром, который сопровождается сильными болями. Вертебропластика укрепляет тело пораженного позвонка, чтобы он перестал давить на нервные корешки.
Операция малоинвазивная, ее проводят под местным обезболиванием и контролем компьютерной томографии. В тело позвонка вводится специальная игла-канюля, одновременно специальным инструментов восстанавливается высота позвонка. В полость позвонка вводится костный цемент. Результат вмешательства также контролируется КТ исследованием. В 98% случаев вертебропластика устраняет болевой синдром сразу же после окончания операции. Период реабилитации минимальный, через пару часов пациент может принимать вертикальное положение.
Так что, вариантов помочь пациенту с болевым синдромом у хорошего онколога сегодня много. Мы убеждены, что вне зависимости от стадии его рака, человек может максимально долго иметь нормальное качество жизни, без ограничений и страданий.
Проблема недостаточного обеспечения сильными анальгетиками больных с тяжелыми диагнозами – одна из самых, уж извините, больных проблем в российской онкологии в частности и паллиативной медицине в целом.
После самоубийства контр-адмирала Апанасенко в 2014 начались какие-то подвижки, но далеко не все так радужно, как обещалось.
Чтобы страха, а значит, и потенциальной ненужной боли, не осталось, давайте разъясним, какой порядок действий, нужный для получения наркотического препарата.
Кто выписывает рецепт?
- врач-онколог,
- участковый терапевт,
- врач любой специальности, который прошел обучение работе с наркотическими и психотропными веществами.
Сколько действует рецепт?
Нужно ли сдавать ампулы?
Нет. По закону, никто не вправе требовать от пациента или его родных сдавать использованные ампулы, пластыри и упаковки от наркотических анальгетиков.
Может кто-то из родственников получить рецепт и препарат от имени больного?
- Чтобы выписать рецепт, врач должен провести осмотр. Но если пациент не может добраться до больницы, он имеет право вызвать врача на дом.
- За печатью все же придется отправить кого-то из близких в поликлинику – печать лечебного учреждения на рецепте обязательна.
- Получить препарат в специально указанной аптеке может как сам пациент, так и его доверенное лицо (с паспортом и копией паспорта пациента)
Что делать, если возникли сложности с получением обезболивающего?
- Звонить на горячую линию Министерства здравоохранения: 8-800-200-03-89,
- Росздравнадзора: 8-800-500-18-35,
- В страховую компанию, у которой оформлен ваш полис ОМС.
В заключение хочется как-то обобщить все сказанное по этой тяжелой теме:
Читайте также:

