Сепсис при лейкозе после химии
У многих пациентов уже до начала лечения выявляются лихорадка и нейтропения. Нераспознанные инфекции могут быстро диссеминировать и закончиться фатально, поэтому недопустима отсрочка назначения антибиотиков до появления развернутой клинической картины.
Наиболее важным предрасполагающим фактором развития инфекций является нейтропения. Риск инфекции зависит от уровня и длительности постцитостатической нейтропении и возрастает при количестве нейтрофилов меньше 1 • 10 9 /л.
При развитии агранулоцитоза (нейтрофилов меньше 0,5 • 10 9 /л) вероятность инфекции очень велика, а при количестве нейтрофилов меньше 0,1 • 10 9 /л инфекции развиваются у большинства пациентов и имеют чрезвычайно тяжелое течение.
До середины 1980-х годов грамотрицательные бактерии кишечного происхождения были причиной 70-80% бактериальных инфекций у больных острым лейкозом. В настоящее время 60-80% бактериальных инфекций вызывается грамположительными микроорганизмами. Это обусловлено:
1) использованием сосудистых катетеров;
2) проведением деконтаминации кишечника, подавляющей грамотрицательную микрофлору;
3) выбором антибактериальных препаратов для эмпирической антибактериальной терапии.
Наряду с бактериальными инфекциями большое значение у больных с нейтропенией имеют грибковые (кандидоз, аспергиллез), вирусные (вызванные herpes simplex и zoster, ЦМВ) и протозойные инфекции.
Инфекционные осложнения при остром лейкозе отличаются атипичным течением. Это обусловлено следующими обстоятельствами:
1) агранулоцитоз существенно изменяет реакцию организма на инфекционный агент, что клинически чаще всего проявляется развитием фебрильной температуры без других признаков локальной или системной инфекции;
2) многие антибиотики нарушают микрофлору больного, подавляют чувствительные микроорганизмы и способствуют пролиферации резистентных бактерий и грибов рода Candida (суперинфекция);
3) большое влияние на защитные механизмы оказывает химиотерапия, вызывающая миелосупрессию и повреждение эндотелия;
4) глюкокортикостероиды, часто вводимые больным как часть специфической терапии, также отрицательно влияют на защитные механизмы;
5) интубация, зондовое энтеральное питание и использование сосудистых катетеров вызывают нарушение целостности кожных покровов и/или повреждение слизистых оболочек.
В связи с высокой вероятностью развития инфекционных осложнений у больных острым лейкозом разработан комплекс профилактических мероприятий:
1) изоляция больного в период нейтропении, которая обеспечивает снижение частоты инфекций, передающихся воздушно-капельным путем;
2) обработка кожи и слизистых оболочек дезинфицирующими растворами (хлоргексидин и др.);
3) деконтаминация кишечника (per os назначаются неабсорбируемые антибактериальные препараты, например канамицин, и противогрибковые средства, чаще всего нистатин или суспензия амфотерицина В), позволяющая снизить количество грамотрицательных организмов кишечного происхождения;
4) гигиена ротовой полости (регулярное полоскание и использование мягких зубных щеток с целью предотвращения травмирования десен);
5) системная профилактика (бисептол или фторхинолоны);
6) отказ от ректальных и вагинальных манипуляций (кроме проводимых по неотложным и жизненным показаниям);
7) назначение препаратов гранулоцитарного или гранулоцитарно-моноцитарного колониестимулирующего фактора (КСФ) для более быстрого восстановления нейтрофилов и уменьшения вероятности инфекционных осложнений.
Показанием к назначению эмпирической антибактериальной терапии на фоне агранулоцитоза является фебрильная температура тела (выше 38 °С) более 2 часов, не связанная с инфузиями или аллергическими реакциями. Оптимально сочетание антипсевдомонального пенициллина или цефалоспорина с аминогликозидом.
Допустима монотерапия цефалоспорином 3-го или 4-го поколения или карбепенемом, например имепенемом. При отсутствии эффекта в течение 2-3 суток необходимо дополнение эмпирической антибактериальной терапии ванкомицином; в случае сохранения лихорадки в течение 4-6 дней назначается амфотерицин В в связи с высокой вероятностью системной грибковой инфекции. После идентификации возбудителя проводится целенаправленная антибактериальная, противовирусная и антимикотическая терапия.
Антибактериальная терапия проводится до повышения абсолютного содержания нейтрофилов в крови больше 0,5 • 10 9 /л и нормализации температуры тела. Длительность терапии у пациентов с документированной инфекцией должна быть не менее 10-14 дней.
Трансфузии гранулоцитов используются крайне редко. Единственным показанием к трансфузии является развившийся на фоне агранулоцитоза бактериальный сепсис при отсутствии ответа на адекватную антибактериальную терапию.
У онкологических пациентов риск сепсиса повышен. Его развитию способствует снижение иммунитета, серьезные хирургические вмешательства. В Европейской клинике есть всё необходимое, чтобы вовремя выявить это осложнение и провести эффективное лечение.
Не совсем так. Между обычной инфекцией и сепсисом есть принципиальная разница.
Инфекция развивается, когда болезнетворные агенты – например, бактерии или вирусы – попадают в организм, повреждают органы. Естественно, наш иммунитет пытается дать чужакам отпор. У человека возникают определенные симптомы. Некоторые инфекции протекают легко, некоторые смертельны. Онкологические больные находятся в группе повышенного риска. Инфекция, которая не опасна для здорового человека, может стать для них фатальной из-за снижения защитных сил организма.
Сепсис – это когда иммунитет реагирует на попавшие в тело микроорганизмы слишком бурно. Он начинает повреждать собственные ткани по всему организму, из-за этого нарушается функция органов, и это опасно для жизни. То есть, помимо инфекции есть еще синдром системного воспалительного ответа. И здесь онкологические больные тоже находятся в группе повышенного риска.
Бактериемия и септицемия у больных раком
Бактериемией называют состояние, когда в крови человека присутствуют бактерии. Ее выявляют с помощью посева крови. Считается, что в норме кровь должна быть стерильна. Впрочем, некоторые исследования показали, что даже в крови здоровых людей могут находиться бактерии, но в целом это не доказано.
Бактериемия может возникать при некоторых инфекциях, например, при брюшном тифе, туляремии, сибирской язве. При пневмонии (воспалении легких) и менингите она уже считается тяжелым осложнением. Если бактерии попали в кровь, и иммунитет слишком бурно начал на них реагировать, развивается септицемия – это синоним сепсиса.
Самая тяжелая форма сепсиса – септический шок. Его диагностируют, когда сильно нарушается работа сердечно-сосудистой системы, ухудшается кровоснабжение всех органов, они перестают получать нужное количество кислорода и справляться со своими функциями. Такие пациенты часто погибают.
Причины возникновения сепсиса у больных раком
Существует несколько причин, из-за которых риск сепсиса у онкологических больных повышен:
- Эти пациенты часто и подолгу находятся в клиниках. Существует такое понятие, как внутрибольничная инфекция: как бы строго персонал больницы ни придерживался правил асептики и антисептики, как бы тщательно ни проводили уборки и ни включали ультрафиолетовые лампы – стопроцентной стерильности достичь невозможно, в медицинском учреждении всегда будут циркулировать микробы. Некоторые из них становятся особенно опасными, потому что постоянно существуют бок о бок с антибиотиками и успевают выработать к ним устойчивость.
- Химиопрепараты атакуют все быстро размножающиеся клетки без разбору: и раковые, и здоровые. Из-за этого могут развиваться осложнения, одно из них – снижение иммунитета.
- Организм многих онкологических больных ослаблен: из-за возраста, злокачественной опухоли и сопутствующих заболеваний, проблем с питанием. Естественно, в такой ситуации снижаются защитные силы организма.
- Для лечения в онкологии часто прибегают к инвазивным процедурам, хирургическим вмешательствам. Когда организм готов неправильно реагировать на инфекцию, сепсис может возникнуть даже из-за укола иглой, не говоря уже, например, о серьезных полостных операциях в брюшной полости.
Вывод: врачи в онкологической клинике должны внимательно наблюдать за состоянием пациентов, знать первые симптомы сепсиса, уметь его диагностировать и своевременно проводить эффективное лечение. Именно так работают в Европейской клинике. У нас есть современные методы диагностики. Например, мы одна из немногих клиник в Москве, где проводится анализ крови на бактериальный эндотоксин.
Причиной сепсиса могут стать самые разные микроорганизмы, как в результате внутрибольничной инфекции, так и заражения вне стен клиники. Согласно некоторым данным, более чем в половине случаев (52,9%) виновниками септицемии становятся грамположительные бактерии, в частности, стафилококки, стрептококки и энтерококки.
На втором месте (41,6%) – грамотрицательные бактерии: кишечные палочки, синегнойные палочки, протеи, клебсиеллы.
Реже встречается сепсис, вызванный грибками (4,1%), обычно кандидами – возбудителями молочницы.
Зачастую анализы показывают, что микроорганизмы, которые поселились в теле пациента, устойчивы ко многим антибиотикам. Поэтому подбор эффективного антибактериального лечения может стать непростой задачей.
Симптомы сепсиса при раке
Сепсис может проявляться разными симптомами, и они бывают выражены в различной степени. Иногда его сложно распознать из-за незначительных проявлений, легко спутать с другими состояниями, такими как инсульт, инфаркт, тромбоэмболия легочной артерии, анафилактический шок. Существуют специальные критерии, которые помогают врачам выявить начинающуюся септицемию и понять, что пациенту требуется обследование, лечение.
Например, если обнаружены два симптома из этого списка, диагностируют синдром системного воспалительного ответа:
- Температура тела менее 36° C или более 38° C.
- Частота сердечных сокращений более 90 ударов в минуту.
- Частота дыхания более 20 в минуту.
- Парциальное давление углекислого газа в крови более 32 мм рт. ст.
- Количество лейкоцитов в крови менее 4 000 или более 12 000 на литр.
Существуют критерии сепсиса по “быстрой” шкале qSOFA. Если есть все три из списка, скорее всего, это сепсис, нужно провести обследование:
- Частота дыхания более 22 в минуту.
- Систолическое (“верхнее”) артериальное давление 100 мм рт. ст. или менее.
- Изменение мышления.
Есть более точная шкала SOFA, она учитывает симптомы и результаты обследования.
В целом, наиболее распространенные симптомы сепсиса: повышение температуры тела, увеличение частоты сердечных сокращений, повышенная потливость, учащенное дыхание. При септическом шоке состояние резко ухудшается, падает артериальное давление, возникает спутанность сознания, ноги, руки и губы становятся холодными, синюшными. Возникают симптомы нарушений функций различных органов. Например, при поражении почек уменьшается суточный объем мочи, легких - развивается одышка, дыхательная недостаточность.
Методы лечения сепсиса при раке
Лечение при сепсисе носит комплексный характер. Основные направления:
- Если есть очаг инфекции - его нужно ликвидировать, например, вскрыть и обработать гнойник.
- Лечение антибиотиками, к которым чувствителен возбудитель (в случае с грибками - противогрибковые препараты).
- Препараты, которые помогают стабилизировать кровообращение: вазопрессоры (сосудосуживающие), инотропные (увеличивающие силу сердечных сокращений).
- Инфузионная терапия - внутривенные вливания растворов через капельницу.
- При необходимости - искусственная вентиляция легких, плазмаферез, переливание компонентов крови.
В Европейской клинике применяется инновационная методика лечения сепсиса - селективная сорбция на картриджах для экстракорпоральной гемоперфузии Toramyxin PMX-20R. Во время этой процедуры, напоминающей плазмаферез, кровь пациента пропускают через специальный фильтр, который очищает ее от эндотоксина. Этот метод помогает эффективно бороться с сепсисом, вызванным грамотрицательной и смешанной флорой.
Прогнозы на выздоровление
Смертность при септицемии составляет от 10 до 40%. Среди пациентов, у которых развился септический шок, она выше. Прогноз главным образом зависит от трех факторов:
- Разновидности и характеристик инфекционного агента.
- Особенностей, физиологии организма пациента.
- От того, насколько правильно и своевременно был установлен диагноз, начато лечение.
В Европейской клинике работает отделение интенсивной терапии, оснащенное всем необходимым оборудованием. У нас есть все возможности для того, чтобы быстро и в полном объеме оказать помощь пациенту в состоянии любой степени тяжести.
Химиотерапия при лейкозе является самым эффективным способом лечения этой патологии, несмотря на наличие большого количества побочных эффектов. Важно понимать, что лейкоз относится к онкологии, поэтому терапия должна быть максимально агрессивной, что позволит понизить количество бластных клеток, либо же устранить их вовсе. Они циркулируют в кровяном русле, а свое развитие берут из мутировавших участков костного мозга.
Показания к химиотерапии

Химиотерапия при остром лейкозе подразумевает назначение одного или нескольких препаратов, обладающих губительным воздействием на мутировавшие клетки. Этот этап лечения включает применение средств, которые вводятся перорально или парентерально, посредством внутривенных вливаний, либо же при помощи пункции, когда вещества вводятся подвздошную кость. Лейкемия, при своевременной постановке диагноза, хорошо реагирует на химию.
Побочные эффекты лечения лейкоза развиваются по причине того, что лекарственные средства, применяемые для химиотерапии, убивают и здоровые, неповрежденные структуры, а также значительно понижают эффективность работы иммунной системы за счет понижения количества здоровых лейкоцитов. Из-за этого организм человека становится более подверженным инфекционным заболеваниям. При этом, лечение лейкоза посредством химиотерапии – один из немногих шансов пациента на выздоровление и наступление ремиссии.
Необходимо учитывать, что подобная терапия при лейкозе имеет побочные эффекты, такие как высокий риск развития инфекций, из-за чего пациентам достаточно часто назначают антибиотики. Это одно из самых грозных осложнений в условиях нейтропении. Также отмечаются такие эффекты:
- снижение фертильности;
- явления диспепсии (тошнота и рвота относятся именно сюда);
- изменение картины крови по причине гибели форменных элементов;
- интоксикационный синдром.
Пациентам с лейкозом вводятся химиопрепараты сразу нескольких групп, поскольку это достаточно агрессивное заболевание, требующее такого же агрессивного лечения.
Риски химиотерапии

Введение химиотерапии вызывает гибель форменных элементов крови, из-за чего у пациентов отмечается:
- анемия;
- нейтропения;
- встречается развитие тромбоцитопении.
Из-за этого слабеют защитные резервы организма, снижается уровень гемоглобина. Риски для пациентов очень большие, однако, альтернативной методики пока что не изобрели. Использование средств, которые купируют эти явления, лишь незначительно снижают побочные действия химиотерапии и понижают вероятность присоединения вторичной инфекции.
Проведение такого лечения лейкоза напрямую обусловлено формой и стадией основного процесса. К ней прибегают, даже если возникли онкологии других органов, например заболевание поджелудочной железы, рак костей и другие. При этом основа лечения острого лейкоза – это химиотерапия.
За счет применения ретиноевой кислоты во время терапии рака крови, происходит дифференциация бластных клеток, что благоприятно отображается на прогнозе лечения этого процесса.
За счет поражения костного мозга лейкозом, происходят некоторые мутации. По этой причине стволовые клетки начинают продуцировать незрелые форменные элементы крови, которые очень быстро размножаются. Они, в свою очередь, вытесняют из кровяного русла здоровые.
Наполнение кровяного русла лейкозными клетками может приводить к тому, что они попадут в другие органы и системы, где появятся метастатические очаги рака. Поражению подвергается:
- нервная система;
- крупные суставы;
- печень;
- селезенка;
- лимфатические узлы.
При этом развиваются такие симптомы:
- нарушение походки, зрения, речи;
- появление болевых ощущений рук, ног, некоторые пациенты жалуются, что болят кости;
- увеличение внутренних органов;
- гипертрофия лимфатических узлов.
Назначение химиотерапии в таком случае подразумевает введение пероральных средств, а также внутривенных вливаний. Таким образом достигается воздействие не только на кровоток, но и на весь организм. Если существует необходимость локального применения лекарств, то их могут вводить в прилегающие к опухоли сосуды.
Терапия острого лейкоза проводится поэтапно – сначала выполняется индукция, затем консолидация, а после назначается поддерживающая терапия. Полностью устранить бластные мутировавшие клетки за один раз нереально. Они частично остаются, при этом они также быстро делятся и размножаются. Лечение заболевания подразумевает интенсивность на первых порах, а длительность составляет не менее двух лет, до момента полного уничтожения всех бластных клеток.
Осложнения химиотерапии при лейкозе ![]()
Курс химиотерапии лейкоза провоцирует целый ряд тяжелых осложнений. Среди них выделяют такие.
Чтобы предупредить развитие малокровия, пациентам назначается при лейкозе эритропоэтин и другие цитокины. Они также борются с такими симптомами, как тошнота и рвота, развивающиеся на фоне применения цитостатиков. Лечение этими препаратами вызывает дегидратацию, иногда анорексию, кровоизлияния во внутренние органы. С целью купирования этих состояний при лейкозе назначаются средства, обладающие противоположным действием:
- Метоклопрамид;
- Аминазин;
- Ондасетрон.
Химиотерапия острых миелоидных лейкозов
Лечение острого миелоидного лейкоза состоит из трех фаз – индукции и консолидации, целью которых является достижение ремиссии. Третий этап – назначение поддерживающей терапии. Такая схема применяется только тогда, когда лабораторно было подтверждено белокровие. Длительность зависит от индивидуальных особенностей пациентов.
Во время индукции происходит уничтожение бластных клеток, но здоровые также подвергаются деструкции. Она занимает около 7 дней. Здесь необходимо грамотное назначение средств, которые применяются для профилактики осложнений химиотерапии. Если не наступает ремиссии, то есть необходимость проведения повторных курсов.
Целью поддерживающей терапии является уничтожение выживших бластов. Она также продолжается около недели, затем пациент не принимает никаких препаратов, пока костный мозг восстанавливается. После этого проводится несколько повторных курсов.
Задачей этапа индукции является максимальное уничтожение мутировавших клеток за кратчайшие сроки. За счет этого достигается период ремиссии острого лейкоза. Здесь назначаются очень интенсивные и агрессивные препараты для химиотерапии. Пациенты плохо переносят этап индукции и физиологически, и психологически.
Первое время индукции регулярно вводятся внутривенные растворы. Также необходимо нагружать заболевших водой. Это обусловлено тем, что одним из побочных эффектов химиотерапии является дегидратация. Другой причиной врачи называют ускорение выхода метаболитов химиотерапии из организма.
О стадии ремиссии говорят тогда, когда анализ крови, пунктат спинномозговой жидкости и костный мозг не показывают наличия бластных клеток. Обычно такое состояние развивается спустя 7-14 дней после начала терапии. Если такового не случилось, проводят повторные курсы увеличенными дозировками.
Этот этап подразумевает закрепление уже полученных результатов. То есть лечение не заканчивается по достижению стадии ремиссии. Во время консолидации пациента обычно отпускают домой, но там он обязан соблюдать прописанный ему режим и придерживаться диетических рекомендаций. Родственникам рекомендуют поместить больного в свою комнату, из которой предварительно убирают все пылесборники – ковры, цветы, мягкие игрушки, там же ежедневно проводится влажная уборка.
Здесь иногда назначается еще и лучевая терапия, которая направлена на область головного мозга. Дозировка определяется индивидуально. В этот период пациентам:
- запрещают смотреть телевизор, заниматься у компьютера;
- рекомендуют хорошее и сбалансированное питание (с большим содержанием витаминов антиоксидантов, полезных веществ);
- прогулки на свежем воздухе.
Сон должен быть не менее 8 часов в ночные часы и не менее 2 днем. Наличие таких рекомендаций обусловлено необходимостью снижения вредного воздействия излучения на головной мозг.
Этот этап является заключительным. Его цель – устранение оставшихся бластных клеток. Здесь применяется низкодозированная химиотерапия, при этом прием лекарств осуществляется в домашних условиях. Длительность достигает двух лет. Периодически больные приходят на осмотр к своему лечащему врачу для того, чтобы сдать анализы и провести коррекцию поддерживающей терапии.
Лейкозы, или, говоря языком медицины, гемобластозы – это злокачественные опухоли, происходящие из кроветворных клеток. В зависимости от того, возник ли лейкемический клон из бластных (молодых) клеток крови, или зрелых их форм, лейкозы могут быть острыми и хроническими. Острый миелобластный лейкоз составляет 20% всех случаев детских гемобластозов. Среди взрослых заболеваемость резко возрастает после 60 лет.
Общая характеристика

Таким образом, острый миелобластный лейкоз – это опухоль, возникшая из незрелых клеток миелоцитарного ростка кроветворения.
Диагноз считается установленным, если в анализе костного мозга (миелограмме) оказывается более 20% бластных клеток.
Причины и механизмы развития
Острый миелоидный лейкоз (ОМЛ), как любые лейкозы, возникает из одной мутировавшей клетки, которая теряет способность созревать и начинает бесконтрольно размножаться. Сказать точно, какие именно из известных канцерогенных факторов спровоцировали мутации в каждом конкретном случае обычно невозможно, особенно если речь идет о детях. В целом это могут быть:
- синдром Дауна;
- нейрофиброматоз 2 типа;
- анемия Фалькони;
- тяжелая врожденная анемия;
- врожденная тромбоцитопения или тромбоцитопатия.
Именно замена здоровых клеток крови на массу бластов, неспособных выполнять их функции в силу незрелости, формирует симптомы белокровия.
Клиническая картина
Проявления острого миелолейкоза неспецифичны – это значит, что на начальном этапе симптомы напоминают признаки других заболеваний.
Из-за недостаточности кроветворения уменьшается количество эритроцитов. Общая слабость, бледность, ломкость ногтей и выпадение волос обычно либо не привлекают внимания пациента или его родственников, либо связываются с другими проблемами. По мере развития болезни слабость нарастает появляется одышка даже при минимальных нагрузках, дети перестают играть в подвижные игры (вообще, снижение активности ребенка – повод внимательно присмотреться к его здоровью).
В крови становится мало не только эритроцитов, но и тромбоцитов. Нарушается свертываемость крови. Возникают кровотечения различной интенсивности: от точечных подкожных кровоизлияний до обильных внутриполостных (желудочно-кишечных, маточных и т.д.).
Гранулоцитарные лейкоциты, принадлежащие к миелодиному ростку – это клетки, чья функция – защищать организм от микробов. Они содержат множество белков – естественных антибиотиков, перекисей, других веществ, направленных на уничтожение инфекционного агента. Угнетение кроветворного ростка затрагивает и их, нарушая способность организма бороться с болезнетворными микробами. Это проявляется различными гнойными воспалениями: кожными абсцессами, флегмонами, вплоть до сепсиса. Любое воспаление вызывает интоксикацию – отравление продуктами обмена веществ патогенных микроорганизмов. Интоксикационный синдром проявляется такими признаками как:
- слабость;
- повышение температуры;
- потливость;
- потеря аппетита, снижение веса;
- неопределенные боли в мышцах.
Отмечается у 30-50% пациентов. Опухолевые клетки заполняют не только костный мозг, но и лимфоузлы, печень, селезенку. Органы увеличиваются, оставаясь безболезненными, их консистенция становится тестообразной. Сама по себе гиперплазия не опасна, но если разрастаются лимфоузлы, которые находятся в замкнутом пространстве (например, полости средостения, где расположено сердце) они могут сдавить жизненно важные органы.
Лейкозные клетки могут образовывать участки экстрамедуллярных (в дословном переводе – расположенных вне костного мозга) опухолей в костях, на коже и слизистых, молочных железах, матке и придатках, простате, легких. При этом возникают симптомы, характерные для патологии этих органов.
Диагностика
Основным признаком лейкоза в анализах крови считается так называемый лейкемический провал: когда в анализе видны множество бластов, мало зрелых клеток и полностью отсутствуют переходные формы. Но на практике, как отмечается в клинических рекомендациях, на ранних стадиях болезни лейкозных клеток в гемограмме (анализе крови) может и не быть. Главное основание для постановки диагноза острого миелобластного лейкоза – более 20% бластов в миелограмме (анализе пунктата костного мозга).
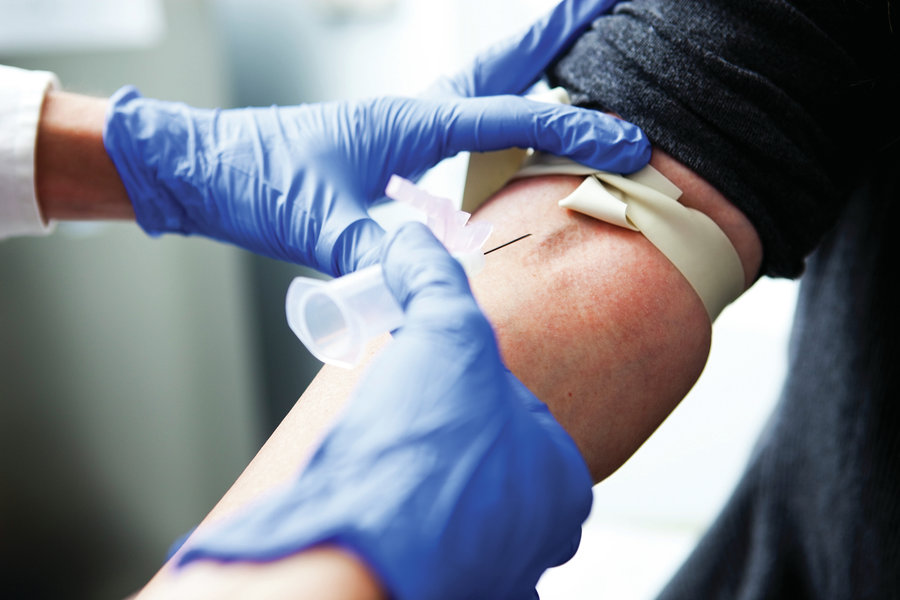
Теоретически диагностика должна включать в себя и цитогенетические тесты, когда изучаются конкретные мутации генов, вызвавшие лейкоз. Это один из важнейших прогностических факторов и современная классификация ВОЗ включает в себя описание более десяти геннных аномалий которые напрямую влияют на прогноз. К сожалению, в России цитохимию, цитогенетические, молекулярно-генетические и другие подобного рода исследования можно сделать только в крупных центрах.
Лечение: общие принципы
В период полихимиотерапии – лечения, направленного на гибель лейкозного клона, пациенту требуется госпитализация и особый уход: условия, близкие к стерильности. Питание должно быть полноценным, с высоким содержанием белка. Вся пища обязательно подвергается температурной обработке.
Помимо химиотерапии, направленной на причину болезни, при лейкозе обязательно проводят и поддерживающую терапию. Она нужна для того, чтобы лечить и корректировать основные синдромы болезни: при анемии переливают эритроцитарную масса, при геморрагиях – тромбоциты, инфекции лечат антибиотиками и так далее. Поддерживающее лечение бывает нужно и для профилактики осложнений химиотерапии.
Подходы к лечению детей и взрослых отличаются.
В детском возрасте стандарт – интенсивная полихимиотерапия, дополненная трансплантацией костного мозга.
Сначала нужно вызвать ремиссию. Для этого используют комбинацию из 5 препаратов которые вводят по определенной схеме. После того, как бластных клеток в костном мозге станет меньше 5%, переходят на поддерживающую терапию: до 4 курсов цитостатического препарата. Далее если есть возможность, делается пересадка костного мозга (за исключением пациентов из группы благоприятного прогноза). Но возможность трансплантации зависит от того, найдется ли подходящий донор. На практике это означает, что если его не окажется среди близких родственников, возможность трансплантации стремится у нулю: регистр доноров костного мозга в России составляется, но пока даже пройти типирование можно далеко не во всех крупных городах.
Принадлежность к группе благоприятного, промежуточного и неблагоприятного прогноза зависит от генотипических характеристик лейкоза. Кроме того, имеет значение индивидуальная реакция пациента на терапию: если через 2 недели после ее начала количество бластов в костном мозге снижается до 5-15%, вероятность благоприятного исхода резко возрастает.
Если ремиссия продолжается дольше 5 лет, лейкоз считается излеченным. Но возможны и рецидивы. Цикл рецидив-ремиссия может продолжаться либо до стабилизации состояния, либо до полного истощения ресурсов кроветворения – в этом случае прогноз неблагоприятен.
При рецидиве полихимиотерапию проводят в 3 этапа: индукция ремиссии, консолидация ремиссии и курс поддерживающей терапии.
В общих чертах прогноз выживаемости можно описать с помощью таблицы:
| Достижение ремиссии, % | Вероятность общей выживаемости в ближайшие 4 года, % | Вероятность безрецидивной выживаемости в ближайшие 4 года, % | |
| Все пациенты | 90 | 67 | 61 |
| Группа стандартного риска | 91 | 78 | 71 |
| Группа высокого риска | 87 | 55 | 46 |
Как видно, излечить острый миелоидный лейкоз у детей в принципе возможно.
Факторы, влияющие на прогноз у взрослых пациентов, можно разделить на 3 группы:
- Индивидуальные особенности организма и состояния здоровья;
- Биологические характеристики лейкемического клона;
- Правильный подбор метода лечения.
Как сам лейкоз, так и его лечение – огромная нагрузка на организм. Поэтому чем старше пациент, тем хуже прогноз. Во-первых, с возрастом хронических патология становится все больше, и протекают они тяжелее. И даже относительно здоровые пациенты старше 60 хуже переносят лечение, чем молодые.
Во-вторых, с возрастом накапливаются неблагоприятные воздействия на генотип, и вероятность мутаций с плохим прогнозом становится выше.
Точно так же, как и у детей, важнейший фактор прогноза – генотип клеток лейкемии. Цитогенетическое исследование и отнесение к группе благоприятного, неблагоприятного или промежуточного прогноза необходимо для правильного подбора схемы терапии. На практике в России такое исследование проводится не более 60% пациентов. Отсюда вытекает и третий фактор.

- возраст старше 40 лет;
- лейкоцитов крови > 100 х 10 9 /л;
- наличие экстрамедуллярных поражений;
- после первого курса химиотерапии не наступила ремиссия;
- вторичный ОМЛ (возник после курса химиотерапии другого злокачественного новообразования);
Полихимиотерапия – единственная возможность уничтожить клон лейкозных клеток. Но когда речь идет о взрослых пациентов с сопутствующими заболеваниями, приходится рассматривать противопоказания:
- инфаркт миокарда менее чем за месяц до начала лечения;
- застойная сердечная недостаточность;
- нарушения сердечного ритма, сопровождающиеся нестабильной гемодинамикой;
- почечная недостаточность кроме случаев, когда она вызвана лейкозным инфильтратом;
- острый вирусный гепатит;
- печеночная недостаточность кроме случаев, вызванных лейкозным инфильтратом;
- тяжелая пневмония, кроме вызванной лейкозными клетками;
- сепсис;
- кровотечение, угрожающее жизни;
- тяжелые патологии психики;
- истощение;
- сахарный диабет с показателем глюкозы крови >15 ммоль/л, не поддающийся компенсации;
- сопутствующая онкологическая патология с неконтролируемым течением.
- При этих состояниях агрессивная полихимиотерапия однозначно принесет больше вреда, чем пользы. Но если состояние удалось стабилизировать, то через неделю можно начать курс лечения.
Сама химиотерапия делится на 3 этапа:
- индукции ремиссии (1-2 курса);
- консолидации ремиссии (1-2 курса) – самый агрессивный и высокодозный этап;
- противорецидивное лечение.
Конкретные схемы и продолжительность курса различаются в зависимости от прогноза и предшествующих рецидивов.
После достижения ремиссии пациентам из группы высокого риска рекомендуется трансплантация костного мозга от совместимого донора. Как и при лечении детей, возможность использования этого метода ограничена доступностью донора. Несмотря на опасность трансплантации для возрастных пациентов (летальность 15-50%), рецидивов после нее практически не бывает.
Поддерживающая химиотерапия назначается в течение 1-2 лет после начала ремиссии (возможны варианты от 4 до 12 курсов). Количество и длительность курсов, а также интервалы между ними зависит от принадлежности больного к группе риска и реакции на лечение.
К сожалению, минимум у 60% взрослых пациентов рецидив наступает в течение 3 лет. Поэтому говорить о перспективах вылечиться довольно сложно.
Пятилетняя выживаемость колеблется от 4 до 46%. Прогноз зависит от генетических особенностей лейкоза, общего состояния больного и продолжительности ремиссии.
Читайте также:


