Саркома костей и мягких тканей презентация
Презентация была опубликована 3 года назад пользователемкарина жан
2 Общие сведения о происхождении сарком костей. К первичным злокачественным опухолям костей относят группу различных по особенностям клинического течения новообразований (от крайне медленно развивающихся до быстро растущих и рано метастазирующих опухолей). Саркомы костей могут локализоваться в любых костях скелета.
3 Остеосаркома (остеогенная саркома) Остеосаркома (остеогенная саркома) является наиболее часто встречающейся первичной злокачественной опухолью кости (35%). Наиболее часто остеосаркома выявляется в возрасте от 10 до 30 лет. Остеосаркома чаще поражает верхние и нижние конечности, а также кости таза.
4 Хондросаркома Хондросаркома развивается из хрящевых клеток и занимает второе место среди злокачественных опухолей костной и хрящевой тканей (26%). Хондросаркома обычно локализуется на верхних и нижних конечностях и в тазу, но может также поражать ребра и другие кости. Иногда хондросаркома развивается в результате злокачественного перерождения доброкачественной опухоли остеохондромы.
5 Саркома Юинга Саркома Юинга. Чаще всего опухоль возникает в кости, однако в 10% случаев саркому Юинга можно обнаружить в других тканях и органах. Она занимает третье место по частоте среди злокачественных опухолей костей. Наиболее часто поражаются длинные трубчатые кости верхних и нижних конечностей, реже - кости таза и другие кости.
6 Фибросаркома и злокачественная фиброзная гистиоцитома (6%) развиваются из так называемых мягких тканей, к которым относятся связки, сухожилия, жировая ткань и мышцы. Верхние и нижние конечности и челюсть - наиболее частые локализации фибросаркомы и злокачественной фиброзной гистиоцитомы.
7 Факторы риска Наследуемые гены. У некоторых больных остеосаркомой возникновение опухоли можно объяснить наличием наследственных факторов. Синдром Ли-Фраумени предрасполагает к развитию различных опухолей, включая рак молочной железы, опухолей головного мозга, остеосаркомы и других видов сарком. Ретинобластома является редкой опухолью глаза у детей. 6-10% ретинобластом объясняется наследственными факторами. У детей с наследственной формой опухоли повышен риск развития остеосаркомы. Проведенная лучевая терапия по поводу ретинобластомы также повышает риск возникновения остеосаркомы костей черепа. Болезнь Педжета может поражать одну или несколько костей и считается предопухолевым заболеваниям. Эта болезнь возникает чаще всего у людей старше 50 лет. При болезни Педжета кости утолщаются, но становятся хрупкими, что может приводить к переломам. В 5-10% случаев на фоне тяжелого течения болезни Педжета развиваются костные саркомы (обычно остеосаркомы).
8 Множественные экзостозы (разрастание костной ткани) повышают риск развития остеосаркомы. Множественные остеохондромы образованы костной и хрящевой тканями.Некоторые люди наследуют повышенную частоту развития множественных остеохондром, что увеличивает риск возникновения остеосаркомы
9 Диагностика опухолей костной и хрящевой тканей Признаки и симптомы заболевания Боль в пораженной кости - самый частый симптом опухолей костей и хряща. Поначалу боль не постоянна и беспокоит больше по ночам или при ходьбе в случае поражения нижней конечности. По мере роста опухоли боль становится постоянной.
10 Переломы встречаются нечасто и могут возникать как в области самой опухоли, так и в непосредственной близости от нее. Общие симптомы возникают при распространенном процессе и выражаются в виде потери веса и повышенной утомляемости.
11 Методы диагностики Стандартный рентгеновский снимок в большинстве случаев позволяет обнаружить опухоль кости, которая может выглядеть как полость или дополнительное разрастание костной ткани. Компьютерная томография (КТ) (иногда с дополнительным введением контрастного вещества) дает возможность выявить опухоли плечевого пояса, костей таза и позвоночника.
12 Магнитно-резонансная томография (МРТ) особенно целесообразна при поражении позвоночника и спинного мозга. Радиоизотопное сканирование костей с помощью технеция позволяет обнаружить как степень местного распространения опухоли, так и поражение других костей. Данный метод более эффективен по сравнению со стандартным рентгенологическим исследованием костей.
13 Биопсия (взятие кусочка опухоли для исследования) является обязательной, так как дает право подтвердить или исключить опухолевое поражение кости или хрящевой ткани. При этом биопсию можно выполнить иглой или во время операции.
14 Лечение опухолей костей и хряща Оперативное лечения Операция является наиболее важным методом лечения костных и хрящевых опухолей. Цель хирургического вмешательства - удаление всей опухоли в пределах здоровых тканей
15 Часть пораженной кости может быть удалена с последующим замещением дефекта другой костью или металлическим протезом для сохранения функции конечности. При значительных размерах опухоли сначала проводится химиотерапия или лучевая терапия, а затем после сокращения размеров опухоли выполняется сохранная операция.
16 Ампутации (удаление конечности) выполняются нечасто. В послеоперационном периоде больному изготавливают протез. В случае метастатического поражения легких иногда производятся операции по удалению опухолевых узлов.
17 Лучевая терапия Различают два вида лучевой терапии при лечении опухолей костной и хрящевой тканей: наружное облучение и брахитерапию. При наружном облучении источник находится вне тела. Лучи фокусируются на область опухоли.
18 Брахитерапия подразумевает использование радиоактивного материала, вводимого непосредственно в опухоль. Этот вид облучения можно применять как отдельно, так и в комбинации с наружным облучением. У некоторых больных, особенно при плохом общем состоянии, лучевая терапия может оказаться основным методом лечения.
19 У больных саркомой Юинга лучевая терапия является основным методом лечения. После нерадикальной операции лучевая терапия назначается для уничтожения оставшейся части опухоли. Облучение может быть использовано с паллиативной целью для уменьшения симптомов опухоли, например, боли.
20 Лучевая терапия, проводимая на область грудной клетки, способна вызвать повреждение легких, что в свою очередь может привести к одышке. Облучение в области верхних и нижних конечностей в ряде случаев сопровождается отеком, болью и слабостью. Лучевая терапия может усугубить побочные эффекты, вызванные химиотерапией.
21 Химиотерапия В зависимости от вида опухоли и стадии заболевания химиотерапия может быть использована как основное или вспомогательное (к операции) лечение. При этом применяется комбинация противо-опухолевых препаратов. Наиболее активными препаратами при этих опухолях являются: метотрексат (в высоких дозах в сочетании с лейковорином), доксорубицин и цисплатина.
22 Из временных побочных эффектов можно отметить: тошноту, рвоту, потерю аппетита, облысение, появление язв во рту. Уменьшение количества эритроцитов, лейкоцитов и тромбоцитов в крови в результате повреждения костного мозга может вызывать малокровие (анемию), повышенную восприимчивость к инфекции, кровотечения.
23 Выживаемость больных с опухолями костей и хряща Длительная (5-летняя) выживаемость больных, страдающих злокачественными опухолями костей и хряща, зависит от стадии заболевания и составляет 64-80% при ранних (I-II) стадиях и % при более поздних (III-IV) стадиях заболевания.
- Главная
- Медицина
- Опухоли мягких тканей и костей
Слайды и текст этой презентации

Опухоли мягких тканей и костей

Опухоли мягких тканей
ОМТ – наиболее трудный раздел онкоморфологии. Они характеризуются сходством клеточных структурных признаков различных по гистогенезу ОМТ.
Основная задача – определение злокачественной природы клеток опухоли, т.е. – диагностика саркомы.
Диагностическая точность дифференциации доброкачественных и злокачественных ОМТ – 94,5%, степени дифференцировки – 81%.


Определение степени дифференцировки клеток ОМТ
Форма и размеры клеток:
1 балл – мономорфность и небольшие изменения по форме и размерам (клетки саркомы сходны с клетками материнской ткани),
2 балла – выраженные изменения по форме и размеру, значительное число гигантских опухолевых клеток (клетки мало похожи на клетки материнской ткани).
Признаки атипии ядер (структура хроматина, гиперхромность, ядерная оболочка, ядрышки):
1 балл – изменения выражены слабо или умеренно,
2 балла – изменения выражены резко, в т.ч. большое количество клеток с полиморфными ядрышками.

Цитологическая оценка степени дифференцировки клеток опухоли:
высокая степень дифференцировки – 2-3 балла.
Низкая степень дифференцировки - 4-5 баллов.
Определение степени дифференцировки клеток ОМТ

Особенности морфологии клеток при ОМТ


Злокачественные опухоли мягких тканей и костей
При установлении диагноза саркомы в клетках злокачественной опухоли должны быть выявлены признаки:
1. злокачественности,
2. соединительнотканной, миогенной, ангиогенной, липогенной, синовиальной, хрящевой, остеогенной дифференцировки,
3. дополнительные диагностические признаки.
Первичный цитологический диагноз саркомы мягких тканей достаточен для планирования радикальной операции. При отсутствии корреляций между клинико-рентгенологическими данными и результатами цитологического исследования применяется гистологическое исследование (угроза диссеминации опухоли!)

Опухоли соединительной ткани. Фиброма
Разрозненные однотипные веретенообразные клетки, ядра вытянутые, гиперхромные, с четким контуром, заостренными концами на фоне оксифильного межуточного вещества. Клетки в виде переплетающихся пучков.

Признаки соединительно-тканной дифференцировки:
вытянутые клетки,
вытянутые ядра, много голых ядер,
в отдельных клетках заостренные концы цитоплазмы и ядер.
Дополнительные признаки: виментин, альфа1-антитрипсин.

Лейомиома: пучки однотипных клеток веретенообразной формы,
ядра расположены центрально, овальные с закругленными концами, ровным контуром, равномерным мелкозернистым хроматином,
цитоплазма сужена у полюсов с длинными волоконцами.

Признаки злокачественности: полиморфизм клеток и ядер, паукообразные клетки, длинные голые вытянутые ядра, гипер- или гипохромные.
Признаки миогенной дифференцировки: переплетающиеся или расположенные в виде параллельных структур вытянутые клетки с хвостатыми отростками и овальными ядрами, ядра в центре, многоядерные симпласты с отшнуровкой ядер, поперечная исчерченность (рабдомиосаркома), гиалиновые глобулы.
Лейомиосаркома. Полиморфизм
неровный контур ядра, голые ядра.

Полиморфноклеточная рабдомиосаркома. Резкий полиморфизм, вытянутые,
округлые многоядерные клетки, неравномерный, гиперхромный хроматин,
встречаются ядрышки, уродливые яра, поперечная исчерченность –
патогномоничный признак, метахроматическое межуточное вещество.

Признаки ангиогенной дифференцировки:
клетки в виде однополюсного или двуполюсного веретена
с гипохромными округлыми и бобовидными ядрами,
сосудистые трубки типа капилляров и синцитиальных структур,
способность к фагоцитозу.
Полиморфные клетки, структуры типа
примитивных сосудов.

Признаки липогенной дифференцировки:
Униполярные и мультиполярные жировые клетки
с признаками атипии.
Миксоидная липосаркома. Мелкие и крупные клетки типа липоцитов и липобластов с небольшим гиперхромным эксцентричным ядром и вакуолизированой цитоплазмой на фоне оксифильного межуточного вещества, единичные клетки типа фибробластов.

Первичные опухоли скелета – 0,25% всех опухолей. ОС:ОМТ=1:10.В 80% - у лиц моложе 20 лет, обычнов трубчатых костях конечностей.
Клетки - веретенообразной, округлой, полиморфной формы. Ядра - округлые, верененообразные, м.б. моногоядерность.
Включения в цитоплазме – гикоген, липиды,слизь.
Фон мазка – межуточное вещество (остеоид или хондроид – и в цитоплазме), кальцинаты, слизь, фиброз, воспаление, опухолевый диатез (детрит, фибрин, эритроциты).
Цитологические критерии степени дифференцировки – те же, что и для ОМТ.

Остеогенная саркома (гигантоклеточная опухоль)
Признаки остеогенной дифференцировки:
округло-овальные клетки типа остеобластов,
остеоидное метахроматическое оксифильное вещество.
Злокачественная гигантоклеточная
опухоль. Гигантские многоядерные
клетки с амфофильной цитоплазмой.
Овальные и вытянутые клетки с
округло-овальными ядрами, межуточное
вещество (остеоид).

Мелкие клетки типа лимфобластов,
мелкозернистый хроматин, единичные
клетки типа лимфоцитов, митозы.

Признаки хондроидной дифференцировки:
Крупные одноядерные или двухядерные злокачественные клетки со светлой цитоплазмой, напоминающие хондробласты,
оксифильное межуточное вещество.

Опухоли хрящевой ткани
Хондрома. Клетки полигональной
формы, цитоплазма вакуолизированная,
округлые ядра, оксифильное
межуточное вещество.
Хондросаркома. Гигантские
многоядерные клетки с
гиперхромными ядрами,
вакуолизацией цитоплазмы. Межуточное вещество.
Саркомы мягких тканей представлены четырьмя десятками злокачественных новообразований, развивающихся из 12 видов соединительной ткани. В группу включены несколько вариантов липосаркомы, фибросаркомы, лейомиосаркомы, рабдомиосаркомы, ангиосаркомы, ГИСО, РЕСомы, гломусная и опухоли неясной дифференцировки, недавно добавлены злокачественные опухоли нервного ствола и неклассифицируемые саркомы. Все эти процессы имеют характерные особенности, но схожи подходы к диагностике и лечению.

Отчего и почему возникают мягкотканные саркомы?
Причина развития сарком мягких тканей неизвестна, но есть доказательства неблаготворного канцерогенного действия давно — несколько десятилетий назад проводившегося облучения и длительного глубокого иммунодефицита. На жизненном пути 99% заболевших саркомой не наблюдалось ни того, ни другого фактора.
Поражают чуть меньше двух человек из каждых 100 тысяч россиян. Некоторые типы новообразований имеют невыраженные гендерные предпочтения, но чёткой статистики по встречаемости у мужчин и женщин не существует.
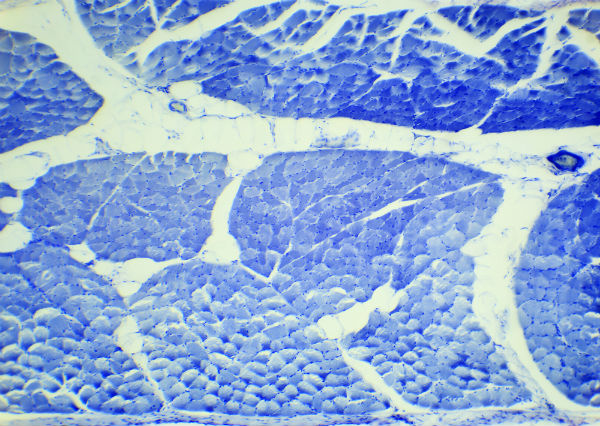
Что важно для прогноза течения саркомы мягких тканей?
Стадия заболевания определяется размером опухолевого узла и предусмотрено только два варианта — менее или более 5 см. Важно расположение опухоли относительно поверхностной фасции — соединительнотканной оболочки на мышечном массиве, как показателя интенсивности внедрения в окружающие структуры, тоже два варианта: над и под фасцией.
Для подбора оптимальной терапии необходимо знать степень злокачественности, которую выводят по сумме баллов, присуждаемых за определённый гистологический признак. Рассматриваются выявляемые при микроскопии кусочка саркомной ткани такие гистологические критерии:
- дифференцировка — степень отличия от нормальной мезенхимальной (соединительной) ткани; всего 3 степени, которым присуждается от 1 до 3 баллов;
- митозы — процесс деления клетки; их число градуируется тоже по 3 позициям, минимально число до 9 и максимально — больше 19 митозов;
- некроз — мёртвые клетки в массиве опухолевой ткани, до 50% и более.
Высокая степень агрессивности G3 отмечается при 6-8 баллах, низкая G1 — сумма до 3 баллов и в их интервале средняя G2.
Оставьте свой номер телефона
Как обнаруживают саркому?
Диагностика поверхностных образований несложная, но высокотехнологичная — рентгеноскопия и УЗИ, МРТ области поражения для выявления границ злокачественного процесса и степени внедрения в соседние структуры, особенно крупные нервные стволы и сосуды.
Обязательна биопсия саркомы мягких тканей более 5 см для предоперационного микроскопического исследования. Предпочтение отдано биопсии толстой иглой, позволяющей взятие столбика ткани, если не удаётся — прибегают к иссечению по краю опухолевого узла. Небольшие опухоли, планируемые на радикальное удаление без подключения предоперационного облучения или химиотерапии, изучают под микроскопом уже после операции.
Как лечат мягкотканные саркомы?
Веяние современности — радикальные, но сохраняющие орган операции, тем не менее, в части случаев невозможно избежать большой калечащей операции с удалением вовлечённых в злокачественный процесс костных структур, больших мышечных массивов и резекции крупных сосудов.
При высокой степени агрессивности или большом протяжении новообразования хирургический этап дополняется предварительным облучением и химиотерапией. Несмотря на длительность лечения, облучение перед операцией весьма полезно:
- меняет взаимоотношение саркомы со здоровыми мягкими тканями;
- уменьшает и отграничивает первичную опухоль;
- снижает биологическую активность и жизнеспособность клеток;
- купирует воспалительный компонент;
- улучшает технические условия для операции.
После операции лучевая терапия уменьшает вероятность рецидива в зоне рубца. Но самая эффективная и наисовременнейшая методика — облучение во время операции или интраоперационное. Оно решает те же задачи, что и послеоперационное облучение, но с меньшей травмой тканей. Инновационная методика лечения мягкотканной саркомы
При саркомах высокой злокачественности и сомнительно операбельных или вовсе не подлежащих оперативному лечению проводится инновационная терапия с сочетанием дистанционного облучения, локальной гипертермии и химиотерапии, получившая название терморадиохимиотерапия.
Стратегия такая:
- перемежаясь или параллельно с курсами химиотерапии все будние дни с перерывами на выходные 5 недель проводится лучевая терапия;
- дважды на неделе перед сеансом облучения по часу делают гипертермию 41-45˚С;
- по завершении цикла и перерыва для отдыха на 4 недели либо выполняется операция, либо повторный цикл терморадиохимиотерапии при невыраженном эффекте.

Оставьте свой номер телефона
Какая химиотерапия работает при саркоме?
К химиотерапии саркомы мягких тканей не особо чувствительны, но при изначально неоперабельных новообразованиях результат несомненно лучше при сочетании противоопухолевых цитостатиков с гипертермией и облучением.
При больших опухолях конечности, когда в перспективе обозначена калечащая операция, используется инновационный подход с локальной гипертермией и системной внутривенной химиотерапией или введением в питающий опухоль сосуд цитостатика мелфалана последовательно с фактором некроза опухоли.
После радикальной операции при некоторых морфологических видах тоже проводится профилактическая химиотерапия, считается, что она уменьшает вероятность рецидива в рубце и частоту метастазов в лёгкие и другие органы.
При метастатической стадии заболевания химиотерапия — единственный вариант помощи. При хорошем самочувствии пациента предпочтительно применение комбинации нескольких цитостатиков. Максимально высокие результаты демонстрирует сочетание доксорубицина с ифосфамидом. Ангиосаркомы хорошо отзываются на таксаны, а липосаркомы с лейомиосаркомами, фибросаркомы и ГИСТ — на таргетные препараты.
Особая сложность — лечение метастатических и неоперабельных форм заболевания, когда на фоне лекарственного воздействия появляется возможность для оперативного удаления метастатических очагов и высокодозной химиотерапии с трансплантацией собственных клеток крови. Клинические исследования доказали весомое увеличение продолжительности жизни пациентов, часто сложности вызываются не столько терапевтическими причинами, сколь процессом организации паллиативной помощи.
В нашей клинике пациенту предложат всё, что поможет ему жить лучше и дольше, а процесс организации — забота персонала.
- Главная
- Разное
- саркома костей


Является одной из наиболее частых и чрезвычайно злокачественных опухолей костей. По данным различных авторов остеосаркома регистрируется в 30-80% всех злокачественных опухолей костей, а по статистике клиники Мэйо, остеосаркома встречается в 2-8 раз чаще, чем другие первичные злокачественные опухоли костей и по своей частоте уступает лишь миеломной болезни. Наиболее характерна заболеваемость во втором, реже — третьем, десятилетиях жизни. Редко может встречаться и в более старшем возрасте. А в пожилом возрасте — чаще всего на фоне болезни Педжета. У мужчин встречается несколько чаще.
Клиника. Характерен выраженный болевой синдром, появляющийся с самых ранних стадий заболевания, усиливающийся по ночам, при приеме анальгетиков эффект незначительный, при приеме наркотиков — боли снимаются на время действия препарата. Локализуется чаще всего в метафизах длинных трубчатых костей, наиболее часто в области коленного сустава, реже в костях таза, но может поражать практически любую часть скелета. При осмотре выявляется увеличение объема (окружности) конечности над опухолью, усиление сосудистого рисунка, повышение местной температуры. Часто имеется ограничение движений в близлежащем суставе. Нередки патологические переломы. Болезнь неуклонно прогрессирует (без ремиссий), характерен небольшой срок от начала заболевания до момента обращения к врачу.

Диагностика. Ведущим диагностическим методом, наряду с клиникой, является рентгенография. Характерно наличие очага деструкции кости, не имеющего четких контуров. Отсутствует зона склероза вокруг очага деструкции. Кортикальный слой кости разрушен. Сравнительно рано выявляется выход опухоли в окружающие мягкие ткани. По типу роста выделены центральная и периферическая формы, по характеру очага деструкции — 3: остеолитическая, остеобластическая и смешанная. Остеолитическая форма — бесструктурный очаг разрушения кости, остеопластическая — очаг деструкции с участками склероза и уплотнения, смешанная форма — сочетание участков остеолитической и остеопластической форм. Во всех случаях очаг деструкции не имеет четких контуров. Характерна периостальная реакция в виде козырька Кодмэна или спикулообразного (игольчатого) периостита. Во внекостном компоненте опухоли возможны участки оссификации (патологическое костеобразование). На ранних стадиях заболевания опухоль может проявляться центрально или эксцентрически расположенным литическим очагом деструкции небольших размеров, с нечеткостью контуров кортикального слоя на ограниченном протяжении. Деструкция быстро нарастает, и уже через 2-3 недели определяются вышеописанные типичные рентгенологические симптомы. Патологические переломы чаще наблюдаются при литических формах. Характерно гематогенное метастазирование в легкие. Во всех случаях до начала лечения необходима морфологическая верификация опухоли. Материал для исследования получается при операционной или трепанобиопсии.
Патологическая анатомия. Опухоль отличается выраженным полиморфизмом с наличием большого количества митозов, с преобладанием при некоторых формах полиморфноклеточных или веретеноклеточных элементов. Обязательным признаком является наличие новообразованных остеоидных структур, от отдельных бесформенных полей остеоида до значительных очагов примитивного костеобразования. Встречается хондробластический вариант, который бывает трудно отличить от низкодифференцированной формы хондросаркомы.

Дифференциальный диагноз проводится с другими злокачественными опухолями костей (опухоль Юинга, фибросаркома и др.), от которых остеосаркому отличает выраженность, непрерывность и быстрота нарастания болевого синдрома, а также быстрый рост опухоли и нарушение функции конечности. Опухоль Юинга редко возникает в возрасте старше 20 лет и локализуется в метадиафизарном, а не в метафизарном отделе трубчатой кости. Другие злокачественные опухоли кости развиваются существенно медленнее остеосаркомы и редко встречаются в возрасте моложе 20-25 лет. Симулировать остеосаркому могут некоторые формы безсвищевых и не образующих секвестры остеомиелитов, а также некоторые формы посттравматических периоститов или посттравматических параоссальных гетеротопических оссификатов. У больных старше 40-45 лет дифференциальный диагноз необходимо проводить с метастатическим поражением костей.
Лечение. Любые локальные методы лечения, включая расширенные операции, не предупреждают гематогенного метастазирования, развивающегося в короткие сроки после начала лечения у абсолютного числа больных. Одним из факторов, позволяющих реально улучшить отдаленные результаты лечения остеосаркомы, является химиотерапия. В настоящее время стандартным является неоадьювантный подход. Использование химиотерапии в предоперационном периоде позволяет оказать ранее воздействие на микрометастазы, уменьшить размеры первичной опухоли и улучшить возможности для локального лечения.
До операции с интервалом в 4 недели проводятся 4 курса химиотерапии по схеме: Доксорубицин 90 мг/м2 в виде 96-часовой внутривенной инфузии (через центральную вену) и цисплатин 120 мг/м2, в виде четырехчасовой внутривенной или внутриартериальной инфузии на 5-й день химиотерапии. Цисплатин вводится на фоне гипергидратации 3.5-4 л и форсированного маннитолового диуреза.
Далее следует операция. При локализации опухоли в длинных трубчатых костях и небольших ее размерах могут производиться органосохраняющие операции в виде резекции суставного конца с удалением половины диафиза кости или тотальное удаление длинной трубчатой кости с эндопротезированием. При опухолях с большим внекостным компонентом показаны ампутации (экзартикуляции) на уровне вышерасположенного сегмента конечности.
Послеоперационная (адъювантная) химиотерапия определяется степенью лекарственного патоморфоза. При повреждении опухоли более чем на 90% (III-IV степень) основу лекарственной комбинации составляют те же препараты, что и до операции, при меньшем повреждении клеток режим меняется на другой, в частности, с включением метотрексата в высоких дозах (10-12 г/м2) или ифосфамида 1,5 г/м2 с этопозидом 100 мг/м2 в 1-5 дни. Подобный подход позволяет надеяться на > 60% 5-летней безрецидивной выживаемости. Несоблюдение режима лечения ухудшает результаты на 30% и более.

Составляет около 10% первичных злокачественных опухолей костей и встречается в 2 раза чаще опухоли Юинга и в 2 раза реже остеосаркомы. По некоторым статистическим данным хондросаркома наблюдается еще чаще (до 20% всех злокачественных опухолей костей). Различают первичную и вторичную хондросаркомы, последняя возникает в результате озлокачествления доброкачественных хрящевых опухолей или хрящевых дисплазий. Возникает в любом возрасте, но характерен средний возраст (40-50 лет). Мужчины болеют в 1,5-2 раза чаще женщин.
Частой локализацией первичной хондросаркомы являются кости таза, ребра, бедро и плечо. Редкая локализация — пальцы кисти.
Клиника. Проявления хондросаркомы зависят от особенностей морфологического строения. Для высокодифференцированных опухолей характерен длительный (4-5 лет) анамнез с малой выраженностью симптомов. Опухоли могут достигать больших размеров. Медленное, но неизменно завершающееся прогрессированием, развитие заболевания свойственно больным в возрасте старше 30 лет.
При анаплазированных хонросаркомах (чаще у лиц молодого возраста) длительность симптомов не превышает 1-3 мес. Хондросаркома склонна к рецидивам. Основным клиническим проявлением заболевания являются боли, припухлость. Боли отмечаются постоянством, прогрессивным нарастанием интенсивности. Увеличение размеров припухлости нередко идет месяцами, иногда годами, особенно при вторичных хондросаркомах. Другие местные симптомы при хондросаркоме такие, как расширение сети подкожных вен, местное повышение температуры, а также нарушение функции близлежащего сустава, выражены менее резко, чем при остеосаркоме или совсем отсутствуют. Лабораторные исследования не выявляют ничего характерного для хондросаркомы.


Лечение. Основным методом терапии хондросарком является радикальное оперативное удаление опухоли в пределах здоровых тканей. Чрезвычайно важным является абластичность проведения операции — удаление костной и мягкотканной опухоли единым блоком с запасом окружающих здоровых тканей, чтобы избежать попадания опухолевых клеток в рану. При отсутствии большого внекостного компонента опухоли показаны резекции суставных концов длинных трубчатых костей или их тотальное удаление с эндопротезированием дефекта. При локализации в лопатке и костях таза — межлопаточно-грудная и межподвздошно-брюшная резекции, соответственно. При больших размерах опухоли — ампутация (экзартикуляция). Прогноз после радикальной операции при хондросаркоме благоприятен. Но удаление опухоли технически оказывается невозможным при некоторых ее локализациях, например, в позвоночнике. Лучевое лечение хондросарком дает лишь временный, паллиативный (обезболивающий) эффект. Химиотерапия при хондросаркоме используется только при низкодифференцированных формах опухоли.
Исходы лечения и судьба больных хондросаркомой прямо коррелирует со степенью анаплазии этой опухоли. 3-, 5- и 10-летняя выживаемость больных соответственно составляла: при анаплазии I ст. — 90,9%; 83,3% и 77,2%; при анаплазии II ст. — 74,5%; 60%; 27%; при анаплазии III ст. — 33,3%;1 9,1%; 14,2%. При мезенхимальной хондросаркоме — 22,2%; 22,2% и 0%. При недифференцированной хондросаркоме — 11,1%; 11,10%. Частота рецидивирования в зависимости от гистологического варианта опухоли и степени анаплазии колеблется от 7,5 до 27,5%.

Клиника. Возраст — наиболее часто второе десятилетие жизни, реже — третье. Мужчины болеют в 2 раза чаще, чем женщины. Опухоль локализуется преимущественно в диафизах длинных трубчатых костей, однако может поражать и плоские и короткие трубчатые кости. Характерно быстрое начало. Ранним и частым симптомом при опухоли Юинга являются боли. Они возникают у 80% пациентов. Боли носят периодический и даже волнообразный характер. Доминирующим и наиболее важным признаком болезни Юинга является выявление опухоли, которое удается уже при первичном осмотре, что подчеркивает тенденцию этого новообразования разрушать кортикальный слой и распространяться на окружающие мягкие ткани. Дебют заболевания нередко подобен таковому при остеомиелите. Отмечаются: подъемы температуры — почти у половины больных, иногда до 38-39 градусов; повышение местной температуры, усиление сосудистого рисунка над опухолью, болезненность при пальпации, увеличение объема конечности, иногда гиперемия, возможна атрофия мышц. Часто выявляется умеренный лейкоцитоз. Симптомы обычно быстро нарастают, но наряду с быстрым и даже молниеносным течением у одних больных, у других отмечается более спокойное и длительное течение. Иногда отмечается волнообразное течение с периодами обострений и непродолжительными ремиссиями. Средняя длительность симптомов до обращения к врачу — 26 недель. Наиболее короткий анамнез по данным нашей клиники — 2 недели, наиболее продолжительный — 2 года. Важной биологической особенностью для опухоли Юинга является ее высокая чувствительность к лучевому воздействию, что иногда используется в диагностических целях. Опухоль Юинга — одна из наиболее злокачественных первичных опухолей костей, которая рано метастазирует в легкие, а также в другие кости скелета и регионарные лимфатические узлы.


В последние годы в режимы химиотерапии включают доксорубицин, циклофосфан, ифосфамид, винкристин, этопозид и актиномицин Д. Наибольшее распространение получили следующие комбинации этих цитостатиков: VAC, VACA, VAIA, EVAIA, VIDE, подробно описаны в справочниках по химиотерапии. Локальное лечение заключается в проведении лучевой терапии на область первичного опухолевого очага — СОД 60 Гр в течение 5-6 недель или операции. При нерадикальной операции (наличие опухолевых клеток по краю резекции) или слабо выраженном гистологическом ответе (лечебный патоморфоз) в ряде клиник проводится дополнительная лучевая терапия. Общая продолжительность комбинированного лечения составляет около года.
Исход лечения во многом зависит от объема опухоли. При объеме до 100 см3 (диаметр более 5 см), 3 года живут 78% пациентов, тогда как при больших объемах опухоли этот показатель снижался до 17%.
Современные сочетанные методы лечения обуславливают достоверное увеличение процента выживших 5 и более лет — до 60 и даже 80%. Частота рецидивирования доходит до 25% после лучевой терапии и 5-10% после использования хирургического метода.
Читайте также:





