Разработки в области борьбы с раком
Однако в последние 10-15 лет невероятными темпами развиваются новые виды антираковой терапии. В мировую медицину пришли современные биотехнологии, благодаря которым на патологический процесс можно воздействовать на уровне генов и молекул. Это открывает перед врачами и пациентами невиданные возможности: вместо массовой терапии больные получили шанс на персонализированное лечение.
Немногие фармацевтические компании в мире вплотную занимаются разработкой и внедрением новых технологий в борьбе с раковыми заболеваниями. В этом списке в основном присутствуют глобальные биофармацевтические концерны, такие как Roche Holding (Швейцария), Bristol-Myers Squibb (США), транснациональная фармкомпания Merck Sharp & Dohme (MSD) (США), англо-шведская фармацевтическая компания AstraZeneca. Единственной отечественной компанией, относящейся к этому списку, стала российская биотехнологическая компания BIOCAD.
Итак, какие новые разработки готова предложить наука для борьбы с раком? Наибольшее внимание ученых и врачей сегодня привлекают препараты на основе моноклональных антител, препараты на основе малых молекул, генная и CAR-T терапия, а также комбинированный подход, использующий все перечисленные методы.
Познакомимся поближе с новыми путями терапии раковых заболеваний, созданными с помощью биотехнологии.

Ученые подумали: а что если пометить раковые клетки произведенными на заводе антителами, чтобы они начали восприниматься как чужеродные и включали защитную реакцию организма, которая их уничтожит так же, как ежедневно уничтожает сотни инфекционных агентов?
Моноклональные антитела избирательно соединяются с чужеродными или сверхпредставленными белками на поверхности клетки опухоли и приводят к ее распознаванию и нацеливанию на нее иммунной системы, тормозят рост опухоли, дополнительно активируют иммунные клетки, маркируют, тормозят рост или маркируют для последующей лучевой терапии. Таргетная (направленная) терапия приводит к значительному повышению эффективности и снижению количества и тяжести побочных реакций.
Механизмов воздействия с помощью моноклональных антител на опухоль множество:
Еще одно направление научных разработок – создание антител, которые способны связываться сразу с двумя мишенями-антигенами. То есть если в одном участке белка раковой клетки была мутация, то антитело все равно свяжется со вторым участком, другими словами – не упустит врага. Это поможет пациентам, нечувствительным к определенным препаратам.
Колоссальный потенциал у биспецифических антител, которые распознают разные антигены (то есть их чувствительность к специфическим клеткам повышается). Они способны использовать эффект синергии нескольких механизмов действия.
Исход болезни зависит во многом и оттого, насколько рано она будет выявлена, поэтому необходима регулярная диагностика в соответствии с полом и возрастом. Например, при прохождении диспансеризации шанс на раннее выявление онкологического заболевания будет выше, чем без нее. А при первых признаках неблагополучия, не откладывая, обращайтесь к врачу!
– Есть ли новые методы терапии и какой из них наиболее эффективный?
– Онкология бурно развивается, но она опирается на три основные методики: хирургия, лучевая терапия, системная лекарственная терапия. Первые два метода остаются базой в лечении большинства новообразований на ранних стадиях, так как обладают мощным воздействием на опухоль. Но как только она дает метастазы, за ними уже не может угнаться ни нож хирурга, ни ионизирующий луч. Здесь в дело вступает лекарственное лечение. Потенциально, где бы ни находилась опухолевая клетка, ее должно настигнуть лекарство, попавшее в организм. Вопрос в том, как сделать эту терапию более эффективной и безопасной?
Современная онкология дает шанс на излечение того, что считалось смертельным еще 15-20 лет назад. Если излечения добиться не удается, мы получаем возможность контролировать болезнь в течение многих лет. Появились новые эффективные медицинские технологии: таргетная терапия (использование препаратов, блокирующих определенные пути стимуляции опухолевой клетки) – как в виде малых молекул, проникающих внутрь клетки, так и антител к конкретной мишени на поверхности опухолевой клетки, иммунотерапия (препараты, активирующие собственный иммунитет для борьбы с опухолью). Но пока нет ответа на вопрос: какая из имеющихся методик лучше? Главное – это грамотный врач-онколог, эффективно эти методики применяющий.
Также идут клинические испытания иммунотерапии следующего уровня, разработанной в стенах той же компании, – искусственно модифицированных клеток иммунной системы (CAR-Т клеток), обладающих потрясающей результативностью при лечении некоторых злокачественных опухолей крови.
– Российские врачи и пациенты сталкиваются с проблемой замены зарубежных препаратов на отечественные – более дешевые, но менее эффективные.
– Страна происхождения – не определяющий фактор. Препарат должен быть в первую очередь эффективным! А цена рассматривается как аргумент только при доказанном качестве. Если отечественный препарат произведен с пониманием того, что ему надо будет выдержать конкуренцию по правилам, принятым в развитых странах мира, то этот препарат, скорее всего, будет столь же эффективен и безопасен, как и препараты, произведенные за рубежом. И этому в отечественной науке уже сейчас есть доказательства.
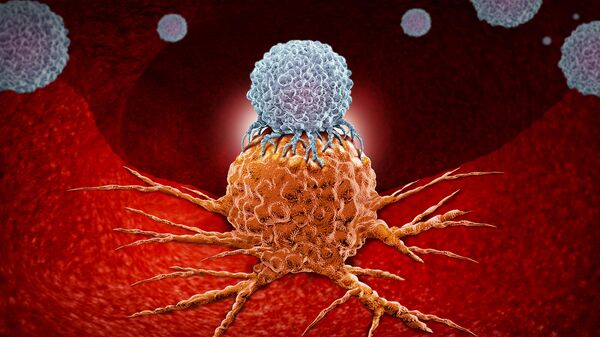

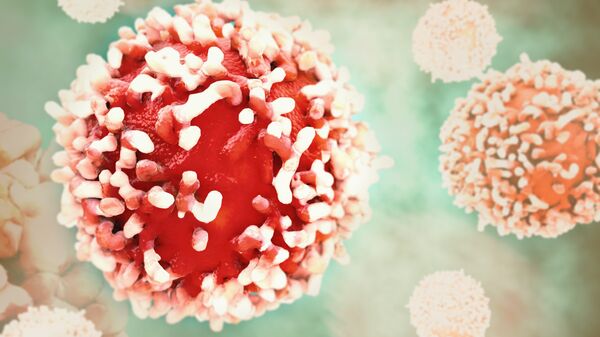
Исследователи берут кровь у животного, привитого антигеном-мишенью, и выделяют из нее иммунные клетки, несущие гены антител
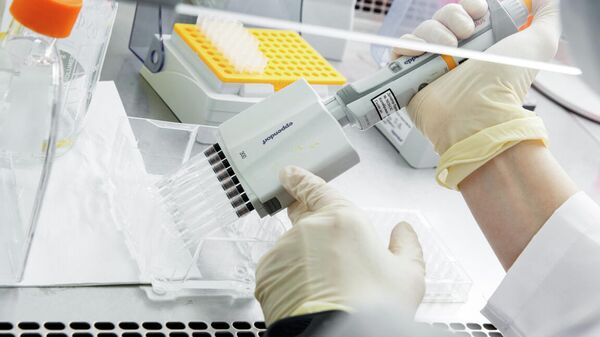
Исследователи берут кровь у животного, привитого антигеном-мишенью, и выделяют из нее иммунные клетки, несущие гены антител
Полученный генетический материал находится в библиотеках антител — пробирках с прозрачной жидкостью, внутри которых — миллиарды разных вариантов антител
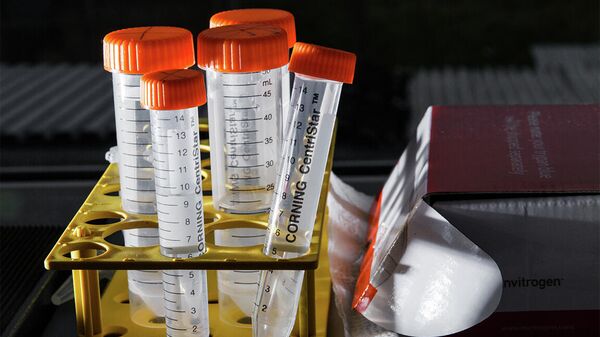
Полученный генетический материал находится в библиотеках антител — пробирках с прозрачной жидкостью, внутри которых — миллиарды разных вариантов антител
С помощью вирусов бактерий — фагов — ученые сужают число вероятных кандидатов. Затем выбирают из них два-три лучших варианта и переносят их на бактерии. Бактерии размножаются, и каждая несет на себе генетическую информацию одного варианта антитела

С помощью вирусов бактерий — фагов — ученые сужают число вероятных кандидатов. Затем выбирают из них два-три лучших варианта и переносят их на бактерии. Бактерии размножаются, и каждая несет на себе генетическую информацию одного варианта антитела
Из бактерий выделяют генетический материал и расшифровывают
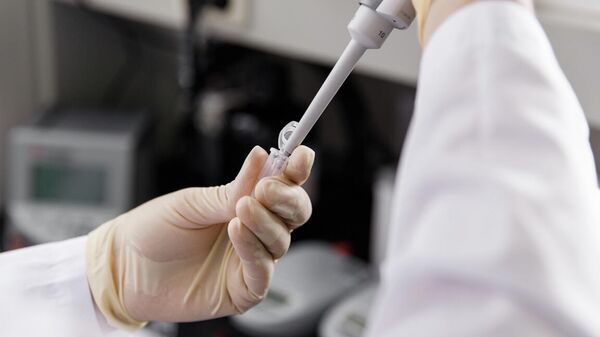
Из бактерий выделяют генетический материал и расшифровывают
Затем исследователи с помощью биоинформатических методов строят 3D-модель антитела, точечно меняя некоторые аминокислоты, чтобы улучшить свойства полученных белковых соединений и сделать их похожими на белок человека

Затем исследователи с помощью биоинформатических методов строят 3D-модель антитела, точечно меняя некоторые аминокислоты, чтобы улучшить свойства полученных белковых соединений и сделать их похожими на белок человека
Исследователи берут кровь у животного, привитого антигеном-мишенью, и выделяют из нее иммунные клетки, несущие гены антител
Полученный генетический материал находится в библиотеках антител — пробирках с прозрачной жидкостью, внутри которых — миллиарды разных вариантов антител
С помощью вирусов бактерий — фагов — ученые сужают число вероятных кандидатов. Затем выбирают из них два-три лучших варианта и переносят их на бактерии. Бактерии размножаются, и каждая несет на себе генетическую информацию одного варианта антитела
Из бактерий выделяют генетический материал и расшифровывают
Затем исследователи с помощью биоинформатических методов строят 3D-модель антитела, точечно меняя некоторые аминокислоты, чтобы улучшить свойства полученных белковых соединений и сделать их похожими на белок человека
Возможно ли обмануть рак? Ученые уверены, в арсенале организма есть антитела, способные расправиться со смертоносными клетками. Но, если бы все было так просто… Болезнь и сама может обмануть организм, замаскировавшись под здоровые клетки. В результате, частичное или полное отсутствие болевых синдромов позволяет онкозараженным клеткам развиться до неоперабельной стадии. Только в минувшем году онкология забрала юмориста Михаила Задорнова, всемирно известного оперного баритона Дмитрия Хворостовского, американского певца Чарльза Бредли, композитора Владимира Шаинского и еще тысячи людей по всему миру.

Данные о ежегодном росте числа онкобольных шокируют. Согласно статистике, через 15 лет каждый житель планеты будет болен раком. Об этом в интервью Пятому каналу рассказал Юрий Покровский, кандидат медицинских наук.

Самый распространенный вид борьбы с раком — хирургическое вмешательство. Удаление пораженного органа может излечить пациента, если только опухоль не пустила метастазы, тогда грядет череда курсов химиотерапии и постоянное беспокойство — поможет ли…
Открытие, способное уничтожить одну из самых опасных форм онкологии — рак головного мозга, сделали ученые из лондонского Университета Лидса и Института изучения рака. Именно рак мозга убил певицу Жанну Фриске и баритона Дмитрия Хворостовского. Ученые выяснили, что с опухолью могут бороться некоторые типы вирусов. Об этом сообщил журнал Science Translational Medicine. В ходе исследования реовирусов, оказалось, что они способны преодолевать гемато-энцефалический барьер, защищающий мозг позвоночных от микроорганизмов.

Девять онкопациентов получали капельницы с реовирусом, после курса им удалили опухоли хирургическим путем. Ученые исследовали удаленные клетки рака и установили, что вирус смог размножиться и атаковать пораженные клетки, тем самым активировав иммунную систему на борьбу с опухолью. Принцип действия нового метода раскрыл соавтор исследования профессор Алан Мельчер:

Вирус быстро распознал рак, и иммунитет начал свою борьбу с ним. Исследователи полагают, что вирусные капельницы станут хорошим подспорьем в сочетании с другими методами лечения. Идею высоко оценил Евгений Черемушкин, старший научный сотрудник Института клинической онкологии ОНЦ РАМН.


Видео: youtube / New Scientist
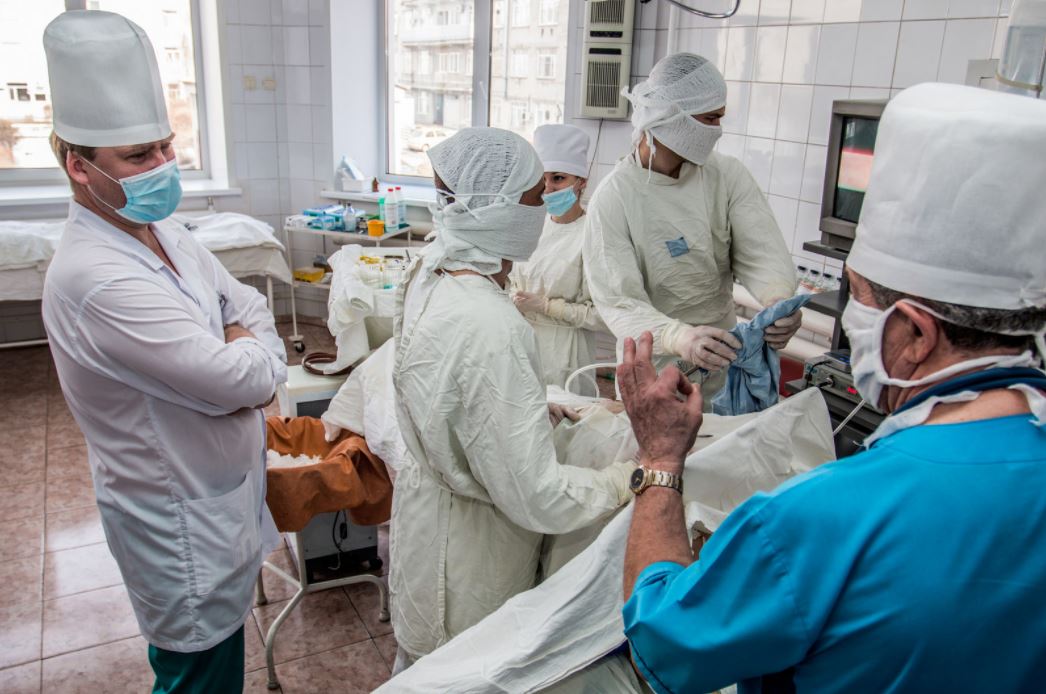
Победа над болезнью не всегда позволяет вернуться к прежней жизни. В петербургском онкоцентре постоянно ведется работа по реабилитации пациентов, победивших недуг. Специалисты этого медучреждения изобрели инновационный метод голосового протезирования, который уже называют главным достижением 2017 года. Врачи вернули голос 80 пациентам, пережившим рак гортани, при котором полностью удаляется трахея и человек теряет способность говорить.

Действительно, ученые доказали, что не только банальное курение может вызвать рак, но и, например, увеличение груди, а именно, воздействие силиконового импланта на организм. Злую шутку могут сыграть и лекарства. Так Минздрав предписал указывать на некоторых препаратах для лечения аденомы простаты и облысения, что они могут привести к раку груди у мужчин, так как содержат опасное вещество финастерид. Таких примеров много. Спровоцировать меланому — рак кожи — может агрессивное солнце. Опасность повсюду и надо быть на чеку.

По данным Всемирной организации здравоохранения за 2015 год (более свежей статистики пока нет) от рака умерло 8,8 миллионов людей. Онкологические заболевания унесли каждого шестого человека в мире. При этом ежегодно страшный диагноз ставится 10-14 миллионам новых пациентов. И хотя рак значительно уступает по уровню смертности сердечно-сосудистым заболеваниям, он до сих пор остается в сознании большинства приговором. Трагические случаи, максимально освещенные журналистами в России, – смерть Жанны Фриске, Михаила Задорнова и Дмитрия Хворостовского - на фоне чуть не ежедневных рапортов медиков об открытии новых эффективных средств против рака оставляют в недоумении. Неужели мы до сих пор бессильны перед опухолями? На самом деле за последние 10 лет в борьбе с раком произошел настоящий прорыв, однако его плоды пока не дошли до массового пациента, утверждает заведующий отделом науки "КП" Даниил Кузнецов.
Что такое рак?
Болезнь эта известна с древних времен. А термин ввел Гиппократ. Ему показалось, что опухоль напоминает клешню рака, поэтому он дал ей название carcinos – карцинома, откуда уже оно попало в латинский и затем английский язык – cancer, а потом было буквально переведено на русский. Строго говоря, современные врачи называют раком только злокачественные опухоли из эпителиальной ткани – карциномы. Однако такие новообразования могут возникать во всех тканях – костной, соединительной или мышечной (саркомы), нервной (глиомы), клетках лимфатической системы (лимфомы), крови и костного мозга (лейкемии) и т.д.
Все ткани живых организмов состоят из клеток. Они регулярно делятся, образуя новые "молодые" клетки, а старые или поврежденные отмирают – совершают добровольное "самоубийство", которое по-научному называется апоптоз. Как деление клеток, так и апоптоз регулируются посредством особых генов, содержащихся в ДНК. И вся проблема в том, что ДНК постоянно повреждается - как в процессе деления, так и из-за воздействия внешних факторов, таких как ультрафиолетовое (солнечный свет) или ионизирующее излучение (радиация), химические соединения (компоненты табачного дыма, токсины, асбест и прочее), разнообразные стрессы, а также вирусы, бактерии или паразиты.
Шутка ли, но в геноме одной соматической клетки может произойти до 10 000 ошибок в сутки! Однако наш организм активно борется с ними. Например, проводя репарацию ДНК – исправляя разнообразные повреждения и разрывы. Или "проверяя" контрольные точки клеточного цикла, прохождение которых либо "разрешает" клетке образовать какие-то компоненты, подготовиться к делению и, наконец, образовать новые клетки. Либо, наоборот, запускает "стоп-сигналы". Если репарация ДНК не завершилась успехом, а контрольные точки не были пройдены, то запускается апоптоз – запрограммированная клеточная смерть.
Проблема в том, что одновременно могут случиться сразу несколько мутаций. И тогда нарушатся как механизмы деления клетки, так и апоптоза. Она начнет постоянно, как заведенная, делиться и напрочь отказываться умирать. Впрочем, это ещё не значит, что она вызовет злокачественную опухоль, ведь у нас ещё работает иммунная система. Клетки со сбоями и даже "микроопухоли" возникают в организме человека регулярно, чаще всего с 20 лет. Однако естественные киллеры (клетки-убийцы) иммунной системы держат их под контролем.
И всё бы хорошо, но мутаций, особенно при неблагоприятных внешних условиях, проходит так много, что некоторые "клетки-мутанты" благополучно проскакивают все барьеры. А с возрастом наша иммунная система слабеет. Выжившая дефективная клетка делится, их становится всё больше, они приобретают новые неблагоприятные мутации и вот наступает тот момент, когда баланс может сместиться - клетка переродится и станет врагом организма. Она станет "бессмертной" и бесконтрольной. Превратится в организм-чужак, пожирающий организм хозяина.
Отдельные клетки опухоли эволюционируют, проходя жесточайший естественный отбор в борьбе с иммунной системой, и приобретают способность отделяться от "материнской" опухоли и путешествовать по кровеносным и лимфатическим сосудам, откуда попадают в другие органы, образуя метастазы. И это начало конца. Опухоли лишают нормального питания другие органы, разрушают их структуру, блокируют различные выводящие пути, снижают кроветворные функции, вызывают наполнение легких жидкостью, многочисленные тромбы, инсульты и совершенно дикие непереносимые боли. А в конечном итоге смерть.
Раннее предупреждение
Главный фактор риска - возраст. И действительно, в России у женщин количество диагностированных онкозаболеваний начинает расти по экспоненте с 25 лет. Риск практически удваивается каждые четыре года, достигая максимума между 60 и 70 годами. У мужчин нарастает вероятность появление рака с 35 лет. До 55 лет она примерно на 30% ниже, чем у женщин. В возрасте 55-59 практически сравнивается, а затем с 60 до 70 превосходит женские показатели.

Распространенность рака в России, 2014 год
В России отмечено серьезное увеличение заболеваемости онкологией, однако этот рост происходит вовсе не из-за ухудшения жизни и здравоохранения, а как раз наоборот: за последние полтора десятка лет рак научились очень хорошо диагностировать, причём на ранней стадии. Более того, прогнозы по успешной терапии злокачественных опухолей напрямую зависят от ранней диагностики. Поэтому первым и самым эффективным методом являются регулярные комплексные медицинские обследования, позволяющие выявить проблему до того, как она станет фатальной.
Последние пять лет в нашей стране бурно развивается генетическое тестирование. Напомним, что рак – это результат фатальных мутаций, де-факто болезнь генома. В наших ДНК существуют онкогены – их активация может превратить клетку в раковую. А также гены-супрессоры, которые предохраняют клетку от перерождения.
К последним, например, относится ген BRCA1. Он участвует в репарации поврежденной ДНК, сохраняя целостность генома. При этом в человеческой популяции есть большое количество носителей мутантной формы данного гена. Всего таких мутаций на сегодняшний день известно более 1000, и каждая из них связана с повышением риска (в среднем на 20 процентов) рака молочной железы, яичников, предстательной железы, кишечника, гортани, кожи и прочих органов и тканей. Наибольшую опасность мутации BRCA1 несут для женщин. Если генетический анализ показывает, что у 25-летней девушки мутантная форма, то вероятность заболеть раком молочной железы до 70 лет повышается для нее на 50-80 процентов (в зависимости от других факторов), а раком яичников - на 30-40 процентов.
Наибольшую известность этот ген получил благодаря Анджелине Джоли. Пройдя генетический тест, она узнала, что у неё дефектная копия BRCA1, такая же была и у её матери, страдавшей от рака 10 лет и умершей в 56. Боясь повторить её судьбу, Джоли, уже имевшая к тому времени детей, решилась на превентивное удаление молочных желез – двойную мастэктомию - и яичников – овариэктомию.
Превентивный подход набирает большую популярность на Западе, особенно среди состоятельных людей, способных оплатить не только операции по удалению органов, но и дорогие косметические импланты. Впрочем, удаление яичников – это радикальный шаг, который исключает материнство и вызывает искусственную менопаузу. Однако генетическое тестирование сейчас за вполне умеренные деньги доступно каждому. Только в Москве есть несколько фирм, где вы можете узнать не только про свои варианты генов BRCA1 и BRCA2, но и множество других онкогенов и супрессоров. Рак молочной железы легко диагностируется на ранних стадиях. Если вы получите неблагоприятный генетический прогноз, вам лишь нужно будет раз в год проходить обязательное обследование.
Борьба до победного конца
Ок, хорошо. Мне 25 лет или 35. Я прошел генетическое обследование и выявил наследственные факторы риска. Ежегодно прохожу полное обследование. Но всё же, если я заболею, что меня ждёт? Вопрос не праздный.
Ещё в начале 2000-х превалировали три классических подхода к терапии злокачественных новообразований: хирургия, лучевая терапия и химиотерапия. Первая подразумевает полное хирургическое удаление опухоли и части тканей, с которыми она контактирует. Метод работает, только если опухоль небольшая, хорошо локализована и ещё не дала метастазов. К примеру, женщинам практически полностью отрезают пораженную грудь.

Дэниэл Хэйс, президент Американского общества клинической онкологии
Далее (или иногда вместо) в ход идёт лучевая терапия – воздействие на опухоль или прилежащие ткани ионизирующим излучением, уничтожающим раковые клетки или предотвращающим их рост. Однако этот метод негативно действует и на здоровые клетки организма. Тот же эффект имеет и химиотерапия, использующая препараты, тормозящие бесконтрольное деление клеток. Они имеют генерализованное воздействие (затрагивающее весь организм в целом) и имеют массу побочных последствий (снижение иммунитета, выпадение волос и прочее). Но самое главное – ни один из них не дает гарантии полного излечения. Единичные клетки-мутанты могут выжить, а на фоне сниженного иммунитета вновь дать мощный рецидив.
Тем не менее в последние 15 лет развитие новых видов антираковой терапии идёт невероятными темпами. Президент Американского общества клинической онкологии Дэниэл Хэйс (Daniel Hayes) недавно заявил:
Когда 35 лет назад я пришёл в эту область, то не мог и вообразить, где мы окажемся сегодня. Сейчас мы можем эффективно выявлять рак на ранней стадии, осуществлять эффективную таргетную ("молекулярно-прицельную") терапию и минимизировать нежелательные последствия, чтобы наши пациенты могли жить дольше, лучше и более полноценно. Сегодня два из трёх пациентов с диагнозом рак продолжают жить спустя пять лет после его постановки.
Вторит ему и исполнительный директор Российского общества клинической онкологии Илья Тимофеев:
Я занялся онкологией в 2003 году. Тогда FDA (Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США – прим. ред.) зарегистрировало лишь один онкопрепарат, в течение следующих двух лет — еще два. А за десять месяцев 2017 года FDA одобрило двадцать четыре новых препарата. Такого прогресса в онкологии еще не было.
Главные успехи сейчас – это развитие по следующим основным направлениям: новые виды иммунотерапии, генная терапия, адресная доставка лекарств и наномедицина (использование экзотичеких способов уничтожения раковых клеток с помощью наночастиц), эксперименты с максимально широким количеством веществ, добываемых из ранее малоизученных растений (такие работы ведутся в российском Университете ИТМО) и глубоководных животных (здесь мировое лидерство за Дальневосточным федеральным университетом, сотрудничающим с лабораториями в Европе, США и Азии).

Илья Тимофеев
Полный и детальный обзор всех направлений может занять слишком много места, поэтому дадим лишь краткую характеристику всех направлений.
Иммунотерапия 2.0
Наша иммунная система вполне успешно подавляет клеток-мутантов и опухоли на начальных стадиях их возникновения. Однако в условиях такой беспощадной борьбы идёт и мощный естественный отбор раковых клеток. Выживают среди них наиболее приспособленные, умеющие использовать слабости нашей иммунной системы и её ограничения, обманывать клетки-киллеры. Иными словами, рак действует словно хакер, использующий уязвимости системы.
Основная цель всех разрабатываемых сейчас методов иммунотерапии – снять ограничения иммунной системы, которые мутанты используют в своих целях, и вновь заставить наши защитные системы атаковать "внутренних врагов". Раньше это удавалось в редких случаях. Лишь очень малое число пациентов демонстрировали стойкую ремиссию, однако сейчас идёт больше 1000 клинических исследований (на людях) различных форм иммунотерапии против разных видов рака. И результаты всё более обнадеживающие.
Генная терапия
Это подход, который может как дополнять иммунную терапию, так и выступать его альтернативой. Суть подхода заключается в переносе генов: в соматические клетки (это могут быть как раковые, так и клетки окружающих их тканей или иммунные) посредством обезвреженных вирусов или наночастиц вводят специальные генетические конструкции.
Работают они так: при введении в кровь вируса он распространяется по всему организму, но встраивается только в раковые клетки основной опухоли и метастазов. Там он экспрессирует (заставляет клетку вырабатывать) определенный белок, который запускает программу самоубийства. Раковые опухоли погибают.
Не так давно, в августе и октябре 2017 года, FDA одобрила препараты компаний Gilead Science и Novartis. Оба они комбинируют методы генной и иммунной терапии, перепрограммируя Т-лимфоциты пациента и обучая их распознавать раковые клетки – лимфомы и лимфобластного лейкоза. У больного делают забор Т-лимфоцитов, модифицируют их ex vivo в лаборатории, а затем вновь вводят пациенту, где они начинают охоту и уничтожение мутантов. Цена каждого курса терапии - 350 000 и 475 000 долларов.
Наномедицина
Крайне многообещающее направление. При химиотерапии необходимо принимать вредные лекарства в больших дозах, что чревато серьезными побочными эффектами. Раковые клетки во многом похожи на здоровые, из-за чего опасные для них соединения часто губительны и для нормальных клеток организма. Для преодоления этой проблемы используют наночастицы. Они способны доставлять крохотные дозы лекарства в нужную область и высвобождать его только там. Их ведут с помощью слабого магнитного поля по кровотоку, а когда они концентрируются в опухоли, резко усиливают внешнее магнитное поле (либо воздействуют иным способом). Высокотоксичное лекарство высвобождается прямо в опухоль, не повреждая здоровые ткани и не вызывая побочных эффектов.
Другой вариант – гипертермия. Например, недавно был проведен интересный эксперимент: мышам вводили золотые "нанозвезды" – наночастицы золота с множеством острых "лучей". Их вводили в организм грызунов с физиологическим раствором, после инъекции они быстро концентрировались внутри опухоли. Так происходило потому, что раковые клетки, в сравнении с обычными, имеют более высокий метаболизм и менее "разборчивы" к тому, что поглощают из окружающей среды.
После этого на опухоль воздействовали слабым лазером. Его излучение практически не поглощалось здоровыми клетками, зато крайне интенсивно - раковыми. Возникал сильный локальный перегрев, который приводил к гибели раковых клеток и исчезновению опухоли. Что интересно, затем пропадали и метастазы, так как погибшие клетки-мутанты утилизировались иммунной системой, и Т-лимфоциты невольно переобучались находить и уничтожать дефектные клетки.
Пока большинство таких исследований только на предварительных или доклинических стадиях (то есть пока ещё не было экспериментов с людьми). Однако всё это дело времени.
Новые вещества
Только перечисление всех новых веществ, которые сейчас проходят проверку в лабораториях, может занять не одну страницу. Так, в Университете ИТМО уже давно экспериментируют с крысами, имеющими маркеры высокого риска появления рака спинного и головного мозга. Их регулярно в условиях контролируемого эксперимента поят отваром таволги. Это в 2-3 раза снизило реальную заболеваемость грызунов по сравнению с контрольной группой.

Таволга
В ДВФУ уже много лет совместно с немецкими, американскими и японскими учеными ведут изучение различных белков у дальневосточных моллюсков, в том числе малодоступных, живущих на большой глубине. Уже сейчас ими обнаружено несколько перспективных претендентов для диагностики и терапии рака.
Вместо заключения
Мы действительно сейчас на пороге реального перелома в борьбе человечества с онкологическими заболеваниями. Рак теснят на всех фронтах, но большинство результатов пока достигнуто на грызунах, а уже одобренные и прошедшие клинические испытания препараты крайне дороги. Для редких форм рака они таковыми и останутся, но иммунотерапия в целом станет в ближайшее время более доступна, как когда-то сотовые телефоны, превратившиеся из роскоши в обыденный гаджет. Будет набирать силу и превентивная медицина, базирующаяся на оценке генетических и средовых рисков (за рамками статьи осталось такое направление, как этнография рака, изучающая влияние образа жизни на увеличение или уменьшение заболеваемости). Но не стоит забывать, что рак – это самое наглядное и очевидное подтверждение теории эволюции Дарвина, поэтому гонка вооружений между людьми и мутантами вряд ли когда-то прекратится.
Читайте также:

