Распадающейся опухоли кровотечении из опухоли
Распад опухоли — это закономерное следствие слишком активного роста ракового узла по периферии или осложнение избыточно высокой реакции распространённого злокачественного процесса на химиотерапию.
Не каждому пациенту доводится столкнуться с тяжелой проблемой распада ракового процесса, но при любой интенсивности клинических проявлений инициируемое распадом злокачественной опухоли состояние непосредственно угрожает жизни и радикально меняет терапевтическую стратегию.

Распад опухоли: что это такое?
Распад — это разрушение злокачественного новообразования, казалось бы, что именно к распаду необходимо стремиться в процессе противоопухолевой терапии. В действительности при химиотерапии происходит уничтожение раковых клеток, только убийство органичное и не массовое, а единичных клеток и небольших клеточных колоний — без гибели большого массива ткани с выбросами в кровь из распадающихся клеток токсичного содержимого.
Под действием химиотерапии клетки рака приходят не к распаду, а к процессу апоптоза — программной смерти. Останки раковых клеток активно утилизируются фагоцитами и уносятся прочь от материнского образования, а на месте погибших возникает нормальная рубцовая ткань, очень часто визуально не определяющаяся.
Регрессия злокачественного новообразования в форме апоптоза происходит медленно, если наблюдать за новообразованием с перерывами в несколько дней, то заметно, как по периферии раковый узел замещается совершенно нормальной тканью и сжимается в размере.
При распаде раковый конгломерат не замещается здоровыми клетками соединительной ткани, мертвые клеточные пласты формируются в очаг некроза, отграничивающийся от остальной раковой опухоли мощным воспалительным валом. Внутри злокачественного новообразования некроз не способен организоваться и заместиться рубцом, он только увеличивается, захватывая новые участки ракового узла, походя разрушая опухолевую сосудистую сеть. Из мертвого очага в кровь поступают продукты клеточного гниения, вызывая интоксикацию.
Массированный выброс клеточного субстрата становится причиной тяжелейшей интоксикации, способной привести к смерти.
Причины распада злокачественной опухоли
Инициируют распад ракового образования всего только две причины: сама жизнедеятельность клеток злокачественной опухоли и химиотерапия.
Первая причина спонтанного — самопроизвольного распада характерна для солидных новообразований, то есть рака, сарком, злокачественных опухолей головного мозга и меланомы. Вторая причина распада типична для онкогематологических заболеваний — лейкозов и лимфом, при онкологических процессах встречается чрезвычайно редко.

Второй вариант распада, типичный для онкогематологических заболеваний, можно констатировать по клиническим симптомам тяжелейшей интоксикации с осложнениями — тумор-лизис-синдрому (СОЛ) и биохимическим анализам крови, где резко повышена концентрация мочевой кислоты, калия и фосфора, но существенно снижен кальций. Конкретная побудительная причина для развития СОЛ — обширное злокачественное поражение с очень высокой чувствительностью к химиотерапии.
При онкологических процессах — раках, саркомах, меланоме реакция на цитостатики преимущественно умеренная и не столь стремительная, поэтому СОЛ принципиально возможен только в исключительных случаях мелкоклеточного, недифференцированного или анаплазированного злокачественного процесса.
Симптомы распада злокачественной опухоли
Клиническим итогом спонтанного распада раковой опухоли становится хроническая интоксикация, нередко сочетающаяся с симптомами генерализованного воспаления вследствие образования гнойного очага. Симптомы разнообразны, но у большинства отмечается прогрессивно нарастающая слабость, повышение температуры от субфебрильной до лихорадки, сердцебиение и даже аритмии, изменение сознания — оглушенность, нарушение аппетита и быстрая потеря веса.
Локальные проявления спонтанного разрушения раковой опухоли определяются её локализацией:
- рак молочной железы, меланома и карцинома кожи, опухоли ротовой полости — гнойная, обильно секретирующая открытая язва с грубыми подрытыми краями, часто источающая гнилостный запах;
- распадающаяся карцинома легкого — при прободении некротической полости в крупный бронх возникает приступообразный кашель с гнойной мокротой, нередко с прожилками крови, иногда случается обильное легочное кровотечение;
- разрушение новообразования органов желудочно-кишечного тракта — развитие локального перитонита при прободении ракового конгломерата в брюшную полость, кровотечение с чёрным стулом и рвотой кофейной гущей;
- распадающаяся карцинома матки — интенсивные боли внизу живота, нарушение мочеиспускания и дефекации при образование гнойных свищей.
Синдром опухолевого лизиса при лейкозах и лимфомах потенциально смертельное состояние, приводящее:
- в первую, очередь к осаждению кристаллов мочевой кислоты в почечных канальцах с выключением функции и острой почечной недостаточностью;
- дополнительно повреждает почки быстрое закисление крови — лактатацидоз;
- снижение уровня кальция и повышение фосфатов инициирует судорожный синдром, дополняемый неврологическими проявлениями вследствие выброса цитокинов;
- повышения калия негативно отражается на сердечной деятельности;
- выброс биологически-активных веществ из клеток приводит к повышению проницаемости мелких кровеносных сосудов, что снижает уровень белков и натрия крови, уменьшает объем циркулирующей плазмы, клинические проявляется падением давления и усугублением поражения почек;
- обширные и глубокие нарушения метаболизма во всех системах органов с исходом в полиорганную недостаточность.
Лечение распада опухоли
Формально при распадающейся опухоли невозможна радикальная операция, зачастую заболевание считается неоперабельным, но химиотерапия и облучение исключаются из программы, потому что способны усугубить некроз. Отчаянное положение пациента и вероятность массированного кровотечения из изъеденного раком крупного сосуда оправдывает выполнение паллиативной операции, основная цель которой — удаление очага хронического воспаления и интоксикации.
Синдром лизиса опухоли лечится многочасовыми капельными вливаниями при усиленном диурезе — выведении мочи, связыванием мочевой кислоты специальными лекарствами. Одновременно поддерживается работа сердечно-сосудистой системы, купируется интоксикация и воспаление. При развитии острой почечной недостаточности проводится гемодиализ.
Синдром лизиса опухоли сложно лечить, но можно предотвратить или хотя бы уменьшить его проявления. Профилактика начинается за несколько дней до курса химиотерапии и продолжается не менее трёх суток после завершения цикла. Кроме специальных препаратов, выводящих мочевую кислоту, назначаются продолжительные капельницы, вводятся недостающие микроэлементы, а избыточные выводятся или связываются другими лекарствами.
Профилактика лизиса опухоли стала стандартом лечения онкогематологических больных, чего нельзя сказать об онкологических пациентах с распадающимися злокачественными процессами, которым очень сложно найти хирурга, готового выполнить паллиативную операцию. Во вмешательстве по санитарным показаниям отказывают из-за сложности выхаживания тяжелого больного после обширного хирургического вмешательства. В нашей клинике никому не отказывают в помощи.
Коротких Н.Г. 1 , Ольшанский М.С. 2 , Степанов И.В. 1 , Щербинин А.С. 1 , Лесникова И.Н. 1
1) Воронежская государственная медицинская академия им. Н.Н. Бурденко, Москва, Россия
2) Воронежская областная клиническая больница №1, Воронеж, Россия
Лечение аррозивного кровотечения из распадающейся опухоли в области головы и шеи является значительной медицинской проблемой. Под нашим наблюдением находилось 14 человек с кровотечением из обширных распадающихся злокачественных опухолей челюстно-лицевой области в период с 2007 по 2012 гг. Всем больным проведена селективная каротидная ангиография для выявления сосудистого бассейна, питающего опухоль. После этого выполнена селективная эндоваскулярная эмболотерапия. Подтверждено преимущество эндоваскулярной эмболотерапии в качестве первоочередного метода остановки кровотечения из распадающейся опухоли.
Ключевые слова: аррозивное кровотечение, эндоваскулярная эмболотерапия, гемостаз, распадающаяся опухоль.
Злокачественные новообразования головы и шеи, включая опухоли полости рта, глотки и гортани, составляют около 5% в общей структуре онкопатологии [6, 8]. В 95% диагностируют плоскоклеточный рак [6, 8, 9, 11]. Как правило, следствием позднего обращения ряда больных за медицинской помощью является прогрессирование заболевания и повышение риска возникновения кровотечений из распадающейся опухоли [5]. Лечение таких заболеваний представляет серьезную проблему.
До недавнего времени лечение аррозивного кровотечения из такого новообразования, как правило, сводилось к перевязке ветвей наружной сонной артерии (НСА), кровоснабжающих опухоль и пораженный орган. В большинстве случаев лигируют наружную и, значительно реже, – общую сонную артерию (ОСА) на стороне поражения. Последнее чревато развитием необратимых ишемических расстройств как непосредственно в пораженном органе, так и в головном мозге. Кроме того, значительный объем опухоли и конгломераты метастатических узлов могут затруднять хирургический доступ к сосудисто-нервному пучку шеи [3, 4, 7].
В свою очередь ангиографические исследования, выполненные в различные сроки после перевязки ветвей НСА, показали восстановление гемоциркуляции в пораженном органе за счет быстрооткрывающихся коллатералей из смежных ветвей и сосудистых анастомозов контралатеральной сонной артерии [5, 10]. Последнее обстоятельство нередко ведет к повторным кровотечениям. В случае возникновения рецидива кровотечения на фоне лигированной наружной сонной артерии иногда приходится прибегать к реконструкции перевязанной артерии с целью выполнения эндоваскулярного вмешательства. Изложенное еще раз указывает на необходимость комплексного подхода к лечению гиперваскулярных образований лица и согласованных действий челюстно-лицевого хирурга и специалистов в области эндоваскулярных вмешательств [10].
Поиск надежных и в то же время малоинвазивных способов остановки кровотечения при злокачественных опухолях челюстно-лицевой области до сих пор является серьезной задачей онкологии, сосудистой и челюстно-лицевой хирургии [1, 2].
Альтернативой перевязке ветвей НСА может являться эндоваскулярная катетерная эмболотерапия. В онкологии она применяется, как правило, в качестве паллиативного воздействия при неоперабельных процессах [5]. Иногда данное вмешательство способствует переводу опухоли в резектабельный статус. Предоперационное использование эмболотерапии играет также определенную роль в снижении кровопотери во время операции. У части пациентов она дает возможность избежать обширной операции, оказывая хороший гемостатический эффект [2, 3].
Целью настоящего исследования является анализ результатов лечения аррозивных кровотечений из распадающейся опухоли области головы и шеи на основе комплексного мультидисциплинарного подхода, включающего использование различных комбинаций малоинвазивных рентгеноэндоваскулярных и хирургических методов.
Материалы и методы
За период с 2007 по август 2012 гг. под нашим наблюдением находились 14 пациентов с кровотечениями из местнораспространенных (Т3-Т4) опухолей головы и шеи. У всех выявлен плоскоклеточный рак различной степени дифференцировки. Локализация процесса представлена следующим образом. У пяти больных опухоль располагалась в области слизистой дна полости рта и языка (Т3-4N3M0), у трех отмечалось поражение (Т3N3M0) нижней челюсти с распространением на слизистую ротовой полости и кожу, у трех опухоль поражала кожу щечной, поднижнечелюстной, подподбородочной областей, верхнюю треть шеи (Т3-4N2-3M0). У двух больных имело место поражение (Т3N3M0) нижней губы, еще у одного − поражение (Т3N2M0) околоушной слюнной железы. Восьми больным ранее проведены различные варианты комбинированного лечения, шестеро обратились за медицинской помощью впервые.
При поступлении в стационар у всех пациентов отмечалось кровотечение из распадающейся опухоли. У четырех ранее проводили лигирование сосудов в ране и прошивание краев опухоли. После неудачной попытки проведения консервативной гемостатической терапии всем 14 пациентам была проведена селективная каротидная ангиография для определения технической возможности выполнения селективной эмболотерапии. По результатам ангиографического исследования у всех больных далее была осуществлена эндоваскулярная катетерная эмболотерапия.
Методика эмболизации. В рентгеноперационной под местной анестезией проводили пункцию правой общей бедренной артерии и устанавливали интрадюсер 5F. Через него в соответствующую сонную артерию проводили многоцелевой или специально моделируемый катетер JR 5F. Исследование выполняли в режиме дигитальной субтракционной ангиографии (ДСА) на ангиографах Angiostar Plus (Siemens) и Infinix (Toshiba) с использованием неионного контраста, вводимого вручную из шприца со скоростью 3 мл/с. При этом тщательно оценивали анатомию в области бифуркации ОСА. Далее проводили катетер в НСА и приступали к более детальной диагностике, выполняя селективную ангиографию соответствующих ветвей НСА. Во время исследования изучали не только сосуды, ответственные за кровоснабжение пораженного участка, но и возможные коллатерали из других сосудистых бассейнов.
Следует отметить, что даже при наличии явного кровотечения, обнаруживаемого визуально, диагностировать его источник ангиографически достаточно сложно.
Во всех наблюдениях удалось остановить кровотечение. Непосредственная эффективность эндоваскулярной селективной эмболотерапии составила 100%. У двух больных наблюдали рецидивное кровотечение из распадающейся опухоли через 48 часов после проведения эндоваскулярной процедуры. Повторно проведенная ангиография выявила открывшиеся анастомозы с другими соседними ветвями НСА. Повторная эмболизация вновь выявленных коллатералей позволила полностью купировать кровотечение. Проведение внутриартериальной химиотерапии у пяти больных позволило вводить большие дозы химиопрепарата с минимальными побочными проявлениями. При этом отмечен выраженный терапевтический эффект, заключающийся в уменьшении объема образования и купировании воспалительной реакции, что позволило проводить в дальнейшем радикальное лечение.
В качестве клинического примера приводим наше наблюдение. Б-ая К., 72 лет, и.б. №157/3, поступила 03.01.12 на лечение в ГБУЗ ВО ВОКБ №1 с диагнозом кровотечение из распадающейся опухоли поднижнечелюстной области. Из анамнеза выяснили, что около 2 лет назад впервые заметила появление опухолевой язвы в поднижнечелюстной области слева. За медицинской помощью не обращалась. Отмечала увеличение размеров опухоли. 03.01.12 отметила появление кровотечения из опухоли. Неотложной помощью доставлена в стационар. При объективном исследовании отмечается опухолевый инфильтрат поднижнечелюстной и подподбородочной области справа, распространяющийся на верхнюю треть боковой поверхности шеи справа. Там же определяется опухолевая язва с отечными валикообразными краями, размером 8,0×4,5 см. Дно язвы покрыто активно кровоточащими грануляциями (рис.1). На рентгенограмме отмечена деструкция в области тела нижней челюсти справа размером 4,0×2,0 см. Проведение консервативной гемостатической терапии, включающей нормализацию артериального давления, не привело к остановке кровотечения. В виду значительного объема опухоли, распространения опухолевого конгломерата на боковую поверхность шеи справа доступ для проведения лигирования ветвей НСА затруднен. С целью остановки кровотечения проведено обшивание краев раны. Назначено обследование, продолжена гемостатическая и гипотензивная терапия. Проведена морфологическая верификация диагноза (гистологическое исследование №164 от 14.01.12 – низкодифференцированный плоскоклеточный рак). Однако данное лечение к положительному результату не привело. Отмечалось постоянное капиллярное кровотечение со всей поверхности опухолевой язвы. При этом уровень гемоглобина снизился до 96 г/л. С целью выявления характера кровоснабжения опухоли, остановки кровотечения и воздействия на опухолевый очаг принято решение провести селективную каротидную ангиографию (СКАГ) с последующим проведением регионарной внутриартериальной химиотерапии и эмболизацией афферентных сосудов опухоли.

Рис. 1. Вид кровоточащей опухолевой язвы.

Рис. 2. а) селективная каротидная ангиография ветвей наружной сонной артерии справа в боковой проекции:
определяется суженное устье правой лицевой артерии.
б) селективная каротидная ангиография ветвей наружной сонной артерии справа в прямой проекции
(определяется суженное устье правой лицевой артерии).

Рис. 3. а) селективная каротидная ангиография ветвей наружной сонной артерии слева в боковой проекции:
определяется избыточная сосудистая сеть в области опухоли, ветвистое строение левой лицевой артерии.
б) селективная каротидная ангиография ветвей наружной сонной артерии слева в прямой проекции:
определяется избыточная сосудистая сеть в области опухоли, ветвистое строение левой лицевой артерии.

Рис. 4. а) селективная каротидная ангиография ветвей наружной сонной артерии
слева в боковой проекции после проведения химиоэмболизации:
отсутствует контрастирование опухоли и дистальных отделов левой лицевой артерии.
б) селективная каротидная ангиография ветвей наружной сонной артерии
слева в прямой проекции после проведения химиоэмболизации:
отсутствует контрастирование опухоли и дистальных отделов левой лицевой артерии.

Рис. 5. Вид опухолевой язвы после проведения химиоэмболизации.
Диагностика кровотечений из распадающихся опухолей головы и шеи должна проводиться на принципах мультидисциплинарного подхода, включающего использование различных лучевых методов. Особая роль при этом отводится рентген-эндоваскулярным вмешательствам. В ряде случаев первоочередным методом гемостаза должны быть эндоваскулярные вмешательства. Это способствует раннему более точному установлению диагноза, оценке степени распространения опухоли, выявлению источника кровотечения и выбору адекватной стратегии лечения. Селективная эмболизация ветвей НСА обеспечивает высокую частоту успеха ≥90%. В наших наблюдениях были подтверждены преимущества эндоваскулярной эмболотерапии в качестве первоочередного метода остановки кровотечения из распадающейся опухоли. Они заключаются в малой инвазивности, отсутствии необходимости в общем обезболивании, высокой эффективности, возможности проведения у ослабленных больных, не исключают в дальнейшем возможность проведения других методов лечения. Использование эндоваскулярной окклюзии для остановки кровотечения в облученных тканях также показало свою действенность. В ряде случаев оно является способом подготовки больного к радикальному хирургическому лечению.
Сайт использует файлы cookies для более комфортной работы пользователя. Продолжая просмотр страниц сайта, вы соглашаетесь с использованием файлов cookies, а также с обработкой ваших персональных данных в соответствии с Политикой конфиденциальности.
Одним из тяжелых осложнений рака желудка является кровотечение.
Частота кровотечений колеблется от 4,6 до 23,4% от всех заболевших раком желудка.
Кровотечения чаще возникают при расположении опухоли на малой кривизне желудка. Они могут возникнуть при любой стадии процесса, но чаще наблюдаются при III-IV стадии. Кровотечение возникает в результате распада или изъязвления опухоли или разрыва кровеносного сосуда, пораженного опухолью. В других случаях деструкция опухоли и развитие гнойного и воспалительного процессов ведут к тромбированию и аррозии питающих ее сосудов, что в свою очередь является причиной гангрены значительных участков опухоли и ее распада, сопровождающегося кровотечением. Более часто осложняются кровотечением язвенные формы рака. Чаще кровоточат опухоли желудка, расположенные в теле и антральном отделе, значительно реже кровотечение возникает при опухолях кардии. Это необходимо учитывать при определении локализации источника кровотечения, особенно при его профузном характере. Наиболее интенсивные кровотечения характерны для рака малой кривизны желудка, где проходят ветви левой желудочной артерии.
В связи с кровопотерей у больных развивается выраженная в той или иной степени картина малокровия (анемии). При незначительных кровотечениях симптомы острой анемии выражены в большинстве случаев нечетко или могут отсутствовать. При выраженных кровотечениях, сопровождающихся рвотой, дегтеобразным стулом, падением гемоглобина, больные жалуются на общую слабость, головокружение, наблюдаются бледность кожных покровов и видимых слизистых оболочек, тахикардия и снижение уровня артериального давления. При тяжелых профузных кровотечениях, сопровождающихся быстрым падением гемоглобина развивается тяжелый сердечно-сосудистый коллапс с падением уровня артериального давления до 60-40 мм рт.ст. и ниже. Пульс учащается до 120-140 ударов в одну минуту. Некоторые больные теряют сознание, кожные покровы их принимают восковидный оттенок и покрывается холодным потом, лицо делается мертвенно бледным, отмечается цианоз губ, расширение зрачков. В терминальной стадии пульс становится нитевидным, часто не сосчитывается, у больных появляется непроизвольное мочеиспускание и дефекация.
Скрытое кровотечение из раковой опухоли нередко не распознается на фоне раковой анемии и кахексии.
Выбор оптимальной лечебной тактики при кровотечении, обусловленном распадающейся опухолью желудка, зависит прежде всего от объема потерянной крови, и от того, остановилось кровотечение или нет. Большую помощь при этом может оказать срочная эндоскопия. Она позволяет не только определить локализацию источника кровотечения, но также установить факт его прекращения или продолжения.
Лечение больных с желудочным кровотечением ракового происхождения в большинстве случаев должно начинаться с консервативных мероприятий: холод на живот, голод, хлористый кальции, викасол, аминокапроновая кислота, гемотрансфузии, переливание кровезаменителей. Однако при проведении указанных мероприятий не всегда удается добиться успеха. Консервативная терапия при кровотечении у больных раком желудка позволяет в большинстве случаев лишь временно остановить кровотечение и подготовить больного к операции.
Определенную роль в лечении больных с кровоточащей опухолью желудка играют местные средства, способствующие остановке кровотечения. Сюда следует отнести все виды гипотермии желудка, начиная с наложения пузыря со льдом на эпигастральную область. Широко используют гемостатическое действие ледяной воды при промывании желудка.
Большие возможности для местной остановки желудочного кровотечения дает использование эндоскопических технологий. У тяжелобольных эндоскопию можно проводить только в тех случаях, когда обеспечены срочное оказание анестезиологического пособия и реанимационная помощь. При гастроскопии можно добиться гемостаза путем прицельного орошения источника кровотечения гемостатическими средствами или клипированием сосуда. В отдельных случаях кровотечение останавливается путем электрокоагуляции.
В специализированных лечебных учреждениях для остановки кровотечения из опухоли желудка стали использовать регионарный рентгеноэндоваскулярный гемостаз. Этот метод особенно показан при лечении больных с профузным кровотечением из злокачественной опухоли желудка, ослабленных кровопотерей и раковой интоксикацией, у которых риск оперативного вмешательства очень высок или операция невыполнима из-за тяжести состояния или неоперабельного поражения желудка. В этих случаях применяют такие способы эндоваскулярного гемостаза как селективное введение вазоконстрикторов или эмболизацию пораженного опухолевым процессом сосуда.
В ряде случаев подготовка больного к операции неоправданно затягивается, несмотря на очевидную безуспешность консервативной терапии, тем самым упускаются более благоприятные условия для проведения операции.
Показаниями к экстренному оперативному вмешательству являются:
1) не останавливающееся под влиянием консервативной терапии кровотечение,
2) прекратившееся кровотечение при угрозе его возобновления,
3) рецидив кровотечения после его остановки в условиях стационара,
4) сочетание кровотечения с перфорацией.
Следует иметь в виду, что одномоментная потеря 500 мл крови при продолжающемся кровотечении из раковой опухоли желудка является показанием к немедленной операции на высоте кровотечения. Таких больных следует сразу же направлять в операционную, где одновременно с анестезиологическим пособием им проводят интенсивную инфузионно-трансфузионную терапию.
Нередко весьма трудно выбрать метод хирургического лечения при кровотечении из раковой опухоли желудка непосредственно во время операции. Следует учитывать состояние больного, локализацию и стадию развития раковой опухоли и часто чрезвычайно сложные топографо-анатомические взаимоотношения, возникшие в результате распространения опухоли за пределы желудка. Методом выбора является выполнение радикальной или паллиативной резекции желудка либо гастрэктомии. Особенно сложно оперативное вмешательство при клинической картине неоперабельного рака желудка на фоне продолжающегося желудочного кровотечения. В этих случаях хирург должен ограничиться только остановкой кровотечения, не предпринимая других более сложных оперативных вмешательств.
Кроме паллиативной резекции возможны также прошивание и перевязка магистральных сосудов желудка, чаще всего левой желудочной артерии, прошивание сосудов вокруг опухоли или в самой опухоли. Прошивание сосудов вокруг опухоли может быть выполнено как со стороны серозной оболочки, так и со стороны слизистой после гастротомии. Обшитый таким образом участок, стенки желудка прикрывают сальником, который фиксируют к серозной оболочке.
Кровотечение из обширных распадающихся опухолей с зияющими сосудами нередко удается остановить только путем перевязки всех основные желудочных артерий и, прежде всего, левой. При кровоточащих опухолях кардиального отдела и дна желудка приходится перевязывать и короткие желудочные сосуды.
Для дополнительного гемостаза кровоточащей опухоли после гастротомии может быть использована электрокоагуляция. При проведении этих манипуляций необходимо обратить внимание на глубину коагуляции или, ограничиваясь воздействием лишь на поверхностные слои злокачественной опухоли во избежание перфорации опухоли в послеоперационном периоде.
После оперативного вмешательства по поводу желудочного кровотечения, обусловленного опухолевым процессом, продолжают интенсивную гемостатическую и заместительную инфузионно-трансфузионную терапию.
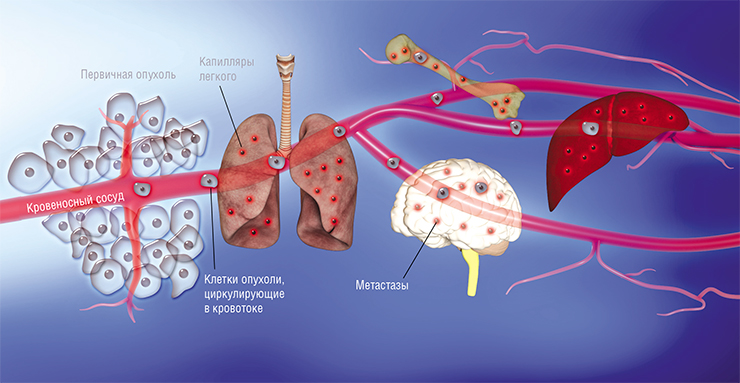
Разрушение очага онкологии обозначает гибель опухолевых клеток, которые рушатся и выделяют токсины. Распад опухоли сам по себе – это частое явление, отмечающееся у многих больных, страдающих от поражения онкологией. Данный процесс в еще большей степени ухудшает состояние пациента, отравляет организм опасными продуктами метаболизма, приводя в конечном итоге к гибели человека.

Предпосылки
Вся сложность ситуации, когда происходит распад опухоли, прежде всего в том, что часто такой процесс вызывается проводимым лечением, которое как раз направлено на уничтожение опухолевых клеток. Именно поэтому этот процесс является естественным последствием лечения против рака. Он может происходить спонтанно из-за терапевтического воздействия.
Спонтанное разрушение, как правило, характерно для новообразований, которые имеют внушительные размеры, поскольку при больших габаритах некоторые клетки отмирают. Опухолевые образования злокачественного характера, локализованные в кишечнике или слизистой желудка, могут повреждаться механически. Их могут повредить ферменты и соляная кислота.
Синдром стремительного распада
Отмирание опухолевых клеток вызывает образование синдрома стремительного распада опухоли, который сопровождается серьезной интоксикацией. Из-за этого высвобождаются соли мочевой кислоты, и она сама непосредственно. Помимо этого, происходит высвобождение фосфатов и калия. Все эти составляющие проникают в кровоток, через который попадают в различные области организма, где повреждают органы и создают щелочной дисбаланс. В массе крови образуется закисленность, которая губительно действует на почечное функционирование.
Химиотерапия как источник разрушения
Когда в кровяной массе циркулирует слишком большое количество мочевой кислоты, это рано или поздно приведет к закупорке просветов канальцев почек. Следствием подобного процесса обычно становится развитие почечной недостаточности.
Такое осложнение преимущественно затрагивает пациентов, которые и до появления опухоли имели нарушения в деятельности органа. Из-за высвобождения фосфата из погибших онкоклеток снижается концентрация кальция в сыворотке крови. Подобное явление вызывает судороги и усиливает сонливость. Помимо прочего, из онкоочага все время поступают излишки калия, что приводит к возникновению аритмии, а она, в свою очередь, может привести к летальному исходу.

Помимо описанных метаболитов, опухолевые клетки могут продуцировать ферменты и прочие агрессивные продукты. Именно поэтому опухолевый распад зачастую осложняется инфекционным поражением, воспалениями, повреждением габаритного сосуда, по причине чего начинается обильное кровотечение. Такие осложнения затрудняют лечение. Кроме того, происходит ухудшение состояния пациента в целом. Если отсутствует своевременная медицинская помощь, перечисленные нарушения грозят сильными потерями крови.
Симптомы
Наблюдаются следующие симптомы распада опухоли:
- появляется лихорадка;
- рвота и тошнота;
- болевой дискомфорт, который локализуется в области живота;
- быстрая потеря изначальной массы тела, что может стать причиной онкологической кахексии;
- изменение цвета кожных покровов (они бледнеют, может появиться желтушный оттенок);
- отклонения деятельности печени.
Нужно помнить о том, что при различных заболеваниях могут присутствовать свои симптомы, которые будут зависеть от вида рака и локализации ракового образования.
Виды рака и характерные симптомы
Для разных видов рака, кроме описанных выше общих признаков, характерны и другие симптомы, которые наблюдаются при определенной локализации новообразования.
Например, при распаде опухоли молочной железы зачастую появляются основания для отнесения патологии к четвертой стадии. При массивном клеточном некрозе, вовлечении в процесс кожи и ее инфицировании, образуются крупные и долго незаживающие язвы, не дающие онкологу в большинстве случаев приступить к лечению опухоли как можно быстрее, так как последняя может еще сильнее усугубить распад. Наряду с проведением дезинтоксикационной и антибактериальной терапии у пациента опухоль продолжает прогрессировать и расти, часто не оставляя возможности для лечения ее хирургическим путем.
Вопрос терапии распадающихся опухолей молочных желез стоит очень остро, особенно с учетом большого количества поздних обращений пациентов и запущенных форм болезни. Кстати, многим интересно, каков прогноз при распаде опухоли. Об этом ниже.
Распад кишечных злокачественных опухолей грозит сосудистым повреждением стенки кишечника и кровотечением, в прямой кишке может не только появиться сильное инфицирование, нагноение и воспаление, но и образуются свищевые ходы в прочие органы малого таза (матку у пациенток, мочевой пузырь).
Распад опухоли легкого опасен проникновением в плевральную полость воздуха (пневмоторакс), сильным кровотечением, появляются привычные симптомы одышки, кашель и боли осложняются отхождением огромного количества гнилостной мокроты.
Маточные опухоли могут распадаться при больших размерах новообразования. Если разрушаются раковые клетки, то происходит инфильтрация и выраженное воспаление окружающих тканей, в прямой кишке и мочевом пузыре появляются свищи, через которые будет распространяться неопластический процесс на данные органы.
Раковый распад при такой локализации отличается лихорадкой, сильной интоксикацией, распространением воспалительного процесса в малом тазу.

Симптомы начала распада опухоли при онкологии – всегда тревожный сигнал, который нельзя оставлять без внимания, в связи с чем любое ухудшение самочувствия человека должно стать поводом для избавления от такого опасного состояния. Очень важно контролировать состояние пациентов, которые проходят противоопухолевую терапию.
Диагностика
Ставится диагноз на основании клинических признаков, результатов инструментальных исследований и лабораторных анализов. Первым настораживающим симптомом чаще всего становится снижение объема выделяемой мочи.
Чтобы диагностировать распад опухоли (на фото его сложно увидеть), нужно определить уровень мочевой кислоты, креатинина, кальция и фосфатов в кровяной сыворотке. Оценивается состояние печени на основании результатов проведенных печеночных проб. В случае необходимости пациенту назначаются УЗИ почек, КТ и ЭКГ.
Лечение
Терапия синдрома опухолевого распада должна проводиться лишь под контролем врача в стационарных условиях. Она включает в себя:
- Противорвотные средства, слабительные препараты, сорбенты. В случае их неэффективности ставят клизмы, не только выводящие каловые массы, но и уменьшающие интоксикацию обменными продуктами.
- Инфузионное лечение для коррекции равновесия кислот и щелочей – введение пациенту препаратов кальция, гидроксида алюминия, раствора глюкозы и инсулина, алюминия, если повышаются фосфаты в кровяной сыворотке, гидрокарбоната натрия.
- Ацидоз при опухолевом распаде, пожалуй, является только одним обоснованным случаем использования соды при раке, однако такое лечение может проводиться лишь врачом и под строгим наблюдением за кислотно-щелочным состоянием крови.
- При появлении симптомов острой недостаточности почек проводится гемодиализ.
- Антиаритмическое лечение при нарушении сердечного ритма.
- При анемии назначаются препараты железа.
- Противовоспалительные и обезболивающие препараты, которые, кроме купирования синдрома боли, уменьшают лихорадку.
- Адекватный режим питья и полноценный рацион.
- До проведения химиотерапии в профилактических целях от осложнений требуется обильное питье, регидратационное лечение на протяжении суток или двух.
А теперь выясним, при распаде опухоли сколько осталось жить больному?

Прогноз
Если лечение начинается своевременно, прогноз при синдроме опухолевого распада чаще всего благоприятный. Когда корректируются нарушения метаболизма, отмечается восстановление деятельности почек. Если терапия отсутствует или начинается поздно, то может быть летальный исход из-за острой недостаточности почек, осложнений, вызванных распадом опухоли (внутреннего кровотечения, серьезных инфекционных осложнений, перитонита из-за перфорации стенок полого органа) или остановки сердца.
Сколько жить при распаде опухоли в случае рака 4 степени? К сожалению, в лучшем случае получится прожить несколько месяцев при правильной терапии.
Профилактика
Для предотвращения появления распада опухолевого синдрома нужно обильное питье за 1-2 суток до начала употребления химиопрепаратов, регулярный контроль уровня мочевой кислоты, креатинина, кальция и фосфатов в кровяной сыворотке. В первую неделю терапии анализы делают ежедневно. Если появляются лабораторные или клинические симптомы синдрома распада новообразования, лабораторные тесты делают несколько раз в сутки.
Читайте также:

