Пункция костного мозга при лимфоме ходжкина

Диагностическое обследование имеет две задачи: во-первых, оно должно подтвердить или опровергнуть факт наличия у пациента злокачественной опухоли, и во-вторых, если этот факт подтверждается, врач должен определить, где именно расположена опухоль, какого она размера, из какого типа клеток она развилась и дала ли она метастазы.
Лимфома Ходжкина обычно образуется из-за генетических изменений в белых кровяных тельцах (лимфоцитах).
Лимфатическая система состоит из лимфатических сосудов и лимфатических органов.
Лечение раковых опухолей направлено на то, чтобы полностью уничтожить злокачественную опухоль и метастазы.
В первый год контрольные обследования нужно проходить каждые три месяца.

В ходе консультации и составления истории болезни врач расспрашивает пациента о жалобах, о том, когда они появились, о ранее перенесенных и сопутствующих заболеваниях, а также о возможных факторах риска. Необходимо сообщить врачу всю информацию о своем здоровье, даже ту, которая кажется несущественной, так как она может оказаться важной для диагностики и составления плана лечения.
После сбора анамнеза врач проводит тщательное клиническое обследование. При подозрении на заболевание лимфатической системы особое внимание врач уделяет лимфатическим узлам: он проверяет, не увеличены ли они при пальпации. Также иногда проводится пальпация печени и селезёнки, так как при заболеваниях лимфатической системы они зачастую поражаются и, следовательно, увеличиваются (гепатоспленомегалия). Также врач прослушает сердце и легкие, измерит пульс и кровяное давление.
Биопсия лимфоузла подразумевает забор самого большого и доступного лимфоузла из определённого региона. Эта процедура обычно проводится амбулаторно. При диагностике лимфомы Ходжкина она необходима, так как для окончательной постановки диагноза требуется обнаружение характерных клеток Рид-Штернберга. Кроме того, требуется гистологическое исследование ткани лимфоузла.
Пункция костного мозга
Пункция костного мозга проводится под местной анестезией. Для этого производится прокол подвздошного гребня. После забора ткань костного мозга исследуют под микроскопом на предмет наличия в ней раковых клеток. В случае поражения костного мозга меняется стадия заболевания.
Рентгенологическое исследование грудной клетки проводится спереди и сбоку. На снимках врач прежде всего смотрит, нет ли у пациента опухоли за грудиной, так как если за грудиной обнаруживается крупное новообразование, это ограничивает возможности лечения.
Компьютерная томография (КТ) — это специальный диагностический метод, позволяющий получить послойное изображение определённого участка тела. При помощи КТ можно с высокой точностью оценить степень поражения лимфатических узлов и других органов (печени, лёгких и т.д.).
Альтернативой компьютерной томографии является магнитно-резонансная томография (МРТ) — диагностический метод, основанный на действии магнита и не связанный с лучевой нагрузкой. Он может проводиться в дополнение к КТ, а также в случаях, когда КТ противопоказано (например, при беременности). Этот метод позволяет получать изображения высокого разрешения. Она абсолютно безболезненна, однако при МРТ пациента помещают в относительно узкий тоннель, что для некоторых людей связано с неприятными ощущениями. Так как в МР-томографе применяются сильные магнитные поля, во время исследования необходимо снять с себя все металлические предметы. Людям с кардиостимулятором или металлическими имплантатами МРТ проводится лишь в исключительных случаях.
Ультразвуковое исследование (УЗИ, сонография) позволяет выявить опухоли в органах брюшной полости, например, в печени, почках, надпочечниках, селезенке, а также в лимфатических узлах. Зачастую УЗИ проводят для оценки размера шейных или подмышечных лимфоузлов. Также этот метод применяется для оценки эффективности лечения.
Преимущество УЗИ заключается в том, что его можно проводить как угодно часто, так как оно не связано с лучевой нагрузкой.
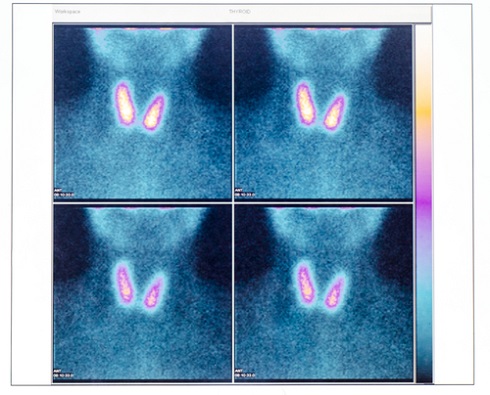
Радиоизотопное исследование (сцинтиграфия) — это диагностический метод, который заключается в том, что пациенту в вену в зависимости от исследуемого органа вводится радиоактивный индикатор, который накапливается в тканях, а затем это накопление фиксируется при помощи специальной камеры. Чем лучше кровоснабжение в определённой области, тем больше вещества в ней накапливается, а для опухолей и очагов воспаления характерно хорошее кровоснабжение. При диагностике лимфомы сцинтиграфия используется для выявления или исключения поражения костей и костного мозга.
Пункция печени
При помощи пункции печени проверяется, присутствуют ли в этом органе злокачественные клетки. Пункция проводится под местным обезболиванием. Врач проводит забор ткани при помощи длинной иглы, которая вводится через брюшную стенку под контролем УЗИ. После процедуры пациент должен несколько часов находиться под наблюдением врача, так как может возникнуть кровотечение. На сегодняшний день пункция печени проводится крайне редко.
Для оценки общего состояния пациента, а также функции отдельных органов, например, почек и печени, зачастую проводится анализ крови. При диагностике лимфомы проводится анализ на скорость оседания эритроцитов: в некоторых случаях этот показатель оказывается повышенным. Кроме того, кровь исследуется на наличие вирусных инфекций, таких как ВИЧ и гепатит B и С. Результаты этих анализов требуются для оценки рисков при проведении химиотерапии и лучевой терапии.
ПЭТ применяется как до начала лечения, так и во время лечения для оценки эффективности химиотерапии и лучевой терапии, и после окончания лечения — для своевременного выявления рецидива.
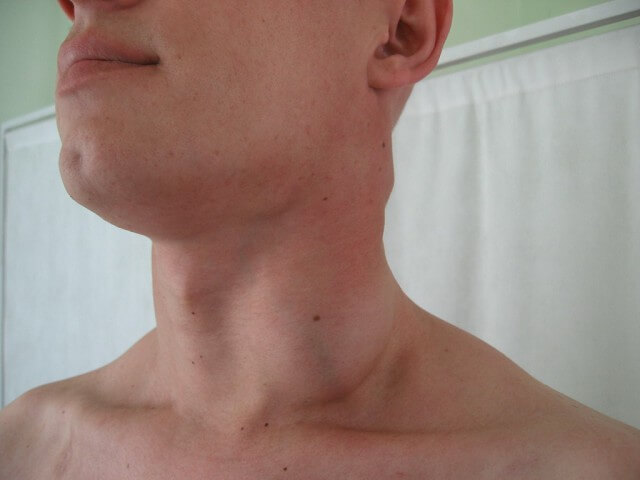
Что такое лимфогранулематоз
Лимфогранулематоз — это злокачественное редкое заболевание ткани лимфоузлов, которое приводит к образованию гигантоклеточной опухоли в лимфоузлах и других соединительных тканях и органах.
- Поражаются в первую очередь органы кроветворения, к которым, кроме лимфатических узлов, относятся: костный мозг, печень, селезенка, вилочковая железа.
- Частота заболеваний — около одного процента, что составляет до пяти случаев на 1 млн. человек.
- Страдают чаще представители европеоидной расы.
- Гендерная статистика патологии показывает большую частоту заболеваемости среди мужского населения (в полтора-два раза выше, чем у женщин).
- Возрастные критерии: диагностируется лимфогранулематоз у детей и у взрослых, но у взрослых все же несколько чаще.
Первопричиной образования лимфомы Ходжкина являются мутации лимфоцитов (чаще всего типа В) — клеток иммунной системы, вырабатывающих антитела, необходимые для борьбы с чужеродными объектами (раковыми клетками и вирусами).
Лимфоциты — одна из разновидностей иммунных клеток крови лейкоцитов. Есть три вида лимфоцитов:
- В-лимфоциты, которые запоминают противника в лицо и производят антитела.
- Т-лимфоциты: узнают и ликвидируют специфические раковые клетки-убийцы (так называемые Т-киллеры), регулируют иммунный ответ.
- NK-лимфоциты — убивают клетки опухолей и вирусов.
Мутации лимфоцитов приводят к тому, что опухолевидные клетки перестают ими распознаваться и запоминаться, из-за чего последние разрастаются до гигантских размеров: такие огромные атипичные структуры называются клетками Рид-Березовского-Штернберга и являются основным диагностическим признаком лимфогранулематоза.
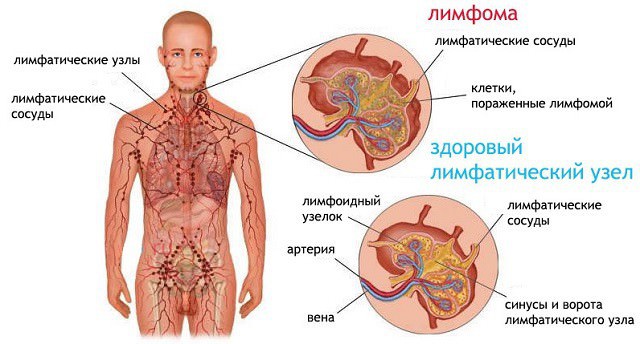
В первичном лимфоузле (ЛУ) начинает расти мезенхимальная опухоль. Это приводит:
- к увеличению и изменению соединительнотканной структуры поражённого ЛУ;
- фибротизации и образованию гранулём;
- распространению опухолевых клеток по лимфатической и кровеносной системе;
- изменениям в органах кроветворения;
- образовании патологических очагов в других лимфоузлах и внутренних органах.
Гистологически определяются четыре вида опухолей:
- Классическая лимфома, состоящая из В-лимфоцитов.
- Нодулярная лимфома со склеротическим изменением тканей ЛУ (диагностируется чаще всего в узлах средостения).
- Смешанно-клеточная Л. (гистология выявляет все виды лейкоцитов): в основном, диагностируется смешанно-клеточный лимфогранулематоз у детей и пожилых.
- Истощенный лимфоузел (ретикулярная форма лимфомы): ткани ЛУ полностью замещены фиброзными, а функции необратимо утрачены.
Лимфома Ходжкина по современной научной версии признана вирусным инфекционным заболеванием: одной из основных причин патологии считается вирус Эпштейн-Барра. Способствовать лимфогранулематозу могут также СПИД и генетическая наследственность.
Этой точке зрения предшествовали годы наблюдений за больными и носителями вируса Эпштейн-Барра, пациентами с синдромом иммунодефицита, а также теми, в семейном анамнезе которых есть болезнь Ходжкина.
Симптомы лимфогранулематоза
Болезнь Ходжкина чаще начинается с поражения вначале шейных и надключичных ЛУ.
Более поздний признак лимфомы — переход на ЛУ средостения: это происходит почти в половине случаев. В поздних стадиях лимфогранулематоза начинаются патологические изменения во внутренних органах и проявления системного злокачественного процесса.
Из-за того, что разросшиеся лимфоузлы сдавливают бронхи, пищевод, стенки сосудов, возникает разнообразная клиническая картина:
- больного может мучить кашель, удушье;
- возникает дисфагия (трудно глотать пищу);
- появляются отеки (при сдавлении верхних полых вен может отекать лицо, при сдавлении нижних — конечности);
- происходят сбои в работе ЖКТ (диарея, запор, непроходимость);
- изредка возможны нарушения в работе ЦНС и почек.
При болезни Ходжкина наблюдаются:
- увеличение печени и селезёнки;
- поражение лёгких (в 10% случаев);
- развитие апластической анемии;
- патологические костные переломы;
- симптомы дерматоза, кожного зуда (причина — повышение билирубина).
- температура до 40;
- ощущение озноба;
- обильное потоотделение;
- слабость, истощение, падение иммунитета (на поздних стадиях).
Возрастает подверженность другим инфекциям:
- опоясывающий герпес;
- кандидомикоз;
- ветряная оспа;
- токсоплазмоз;
- атипичная пневмония;
- менингит и пр.
ЛГМ имеет четыре стадии:
- Первая степень — поражение ЛУ одной группы, например, шейные или надключичные, либо какого-то органа.
- Вторая степень — поражение ЛУ нескольких групп выше или ниже дыхательной диафрагмы.
- Третья степень — тотальное поражение узлов с обоюдных сторон диафрагмы с гепатомегалией, спленомегалией и другими симптомами поражения органов или без них. Третья стадия подразделяется на две подстадии:
- 3(1) — поражение затрагивает верхние отделы брюшной полости;
- 3(2) — затронуты тазовая область или зона аорты.
- Четвёртая степень: помимо поражения лимфоузлов, имеются диффузные изменения во внутренних органах (печени, легких, кишечнике, селезенке, костном мозге и др.).
Врачи при обнаружении лимфомы в медицинской карте больного обычно пишут диагноз не словами, а стандартными символами:
- буква, А означает отсутствие клинических симптомов;
- В — есть один из следующих признаков (высокая температура, похудение, сильная потливость);
- Е — имеется поражение других тканей и органов;
- S — поражена селезенка;
- Х — есть большое объемное образование.
Это редкая болезнь у детей от шести до шестнадцати лет. Заболевание начинается часто с того, что на шее у ребёнка вскакивает безболезненная шишка — увеличенный лимфоузел. Также возможно, но реже, появление такого узла в области средостения (грудины) и ещё реже в брюшной или паховой области. Другие симптомы лимфомы могут поначалу отсутствовать.
- температура;
- ночная повышенная потливость;
- плохой аппетит и сон;
- частые болезни ребёнка.

Из клинических признаков может быть увеличенная селезенка, однако прощупать её удаётся не всегда. Гепатомегалия считается неблагоприятным признаком.
Лимфогранулематоз у детей требует как можно более ранней диагностики и лечения: один или два узла до появления системных симптомов необходимо удалить, после чего провести курс облучения.
Поражение многих лимфоузлов и органов требуют другой схемы лечения с применением химиотерапии. Один из вариантов лечения детей — аутотрансплантация костного мозга.
Есть два разных заболевания, которые порой путают:
Обе болезни лечатся совершенно по-разному:
- при болезни Ходжкина используется химиотерапия, радиотерапия, хирургические методы;
- при венерическом паховом лимфогранулематозе применяются антибиотики, сульфаниламидные препараты, сурьма.
Диагностика болезни Ходжкина
Цель диагностики — изучение показателей крови в ОАК, БАК, ИФА.
Так, общий анализ (с использованием пробы Кумбса) позволяет выявить такие симптомы лимфомы, как:
- тромбоцитопению;
- анемию;
- эозинофилию;
- склеивание эритроцитов;
- повышение СОЭ.
Биохимический анализ определяет:
- печеночные пробы (билирубин, АлАТ, АсАТ);
- наличие белка в крови (альфа и гамма-глобулин, фибриноген, С-реактивный белок и др.), которые являются следами воспалительного процесса;
- уровень железа;
- концентрацию трансферрина.
Иммуноферментный анализ выявляет ферритин, рецепторы трансферрина и эритропоэтина.
Анализы сдаются утром натощак.
Для постановки диагноза используют следующие инструментальные способы:
- рентгенографию;
- УЗИ;
- КТ (МРТ);
- эндоскопию (бронхов, пищевода, желудка, толстого кишечника);
- лапароскопию (малоинвазивный метод обследования органов брюшной полости и лимфоузлов;
- миелографию;
- ангиографию;
- сцинтиграфию.
Пункция костного мозга и гистология считаются самыми точными подтверждающими способами диагностики лимфомы:
- При пункции костного мозга производится забор красных клеток КМ из костного канала.
- Гистология ЛУ проводится по одному из трёх способов:
- пункция содержимого лимфатического узла;
- аспирационная биопсия с забором клеток тканей узла;
- инцизионная биопсия (полное удаление узла);
- биопсия при лапароскопии ЛУ.
Лечение лимфогранулематоза
Сегодня болезнь Ходжкина успешно лечится комбинированными способами:
- радиотерапия (РТ);
- химиотерапия (ХТ);
- хирургическое лечение;
- аутотрансплантация (пересадка) костного мозга.
- Радиотерапия проводится в течение четырёх-пяти недель (20 — 25 сеансов).
- Общая доза радиации — 35 грей (максимально — 44 гр.).
- Облучению подвергаются поражённые лимфоузлы.
- Внутренние органы, расположенные рядом с зоной облучения, закрываются защитным кожухом.
Для лечения лимфомы используется комбинация сильнодействующих препаратов, подавляющих рост опухоли, которые назначаются по стандартным схемам сеансами.
- При лимфоме Ходжкина первой-второй степени обычно проводят два сеанса ХТ и один курс радиотерапии.
- При гранулематозе третьей-четвёртой стадии проводят восемь сеансов ХТ.
- Одна из схем — ABVD, в которой применяют:
- антибактериальный препарат Адриамицин;
- противоопухолевые препараты Блеомицин и Винбластин;
- цитостатик Дакарбазин.
- Химиотерапия по схеме BEACOPP: Блеомицин + Этопозид + Адриабластин + Циклофосфан + Винкристин + Прокарбазин + Преднизолон.
- Применяются и старые традиционные схемы:
- DBVD — аналогичен ABVD, но используется доксорубицин вместо адриамицина;
- MOPP (мехлоретамин +Oncovin + прокарбазин + преднизолон).
Недостаток последней схемы МОРР — последствие в виде лейкоза в отдаленном будущем.
В 2011 г. было разработан селекционный таргетный препарат Адцетрис, который успешно применяется для лечения СД30 позитивных опухолей:
- после применения двух линий ХТ;
- после аутотрансплантации;
- при невозможности проведения аутотрансплатации;
- при анапластической лимфоме после одной линии ХТ.
С 2016 г. Адцетрис применяется и в России.
Преимущества таргетной химиотерапии в прицельном воздействии на опухолевые клетки, при этом здоровые ткани под удар почти не попадают. Такое лечение имеет меньше вредных последствий.
Последняя новинка среди лекарств, направленных на борьбу с лимфомой Ходжкина, разработана в 2017 г. — это иммунопрепарат Кейтруда, который применяется для лечения рецидивов.
Радикальная хирургия эффективна на первой стадии болезни, когда поражён один или несколько узлов, и нет метастазов в органах.
- Поражённые узлы удаляют, после чего проводят радиотерапию
- В некоторых случаях назначают дополнительно химиотерапию.
- На поздней стадии операция носит паллиативный характер и предназначена для облегчения состояния больного, но к выздоровлению она не приводит.
Этот способ в основном применяется для лечения молодых пациентов и детей. Основанием могут быть:
- поздняя стадия болезни;
- тип лимфомы, не поддающейся лечению другими способами (это происходит в двух-трёх процентах).
Успешная пересадка костного мозга при лимфоме Ходжкина может привести к полному выздоровлению или долгой ремиссии.
Серьёзные препятствия и причины неудач:
Сегодня болезнь Ходжкина не считается приговором и эффективно лечится. Выживаемость у неё довольна высока, причём на всех стадиях:
- при первой — второй стадии ЛГМ пятилетняя выживаемость отмечается у 90% больных;
- при третьей-четвёртой выживаемость в течение 5 лет немного ниже — у 80% пациентов.
Рецидивы заболевания случаются минимум у одной десятой и максимум у одной трети больных. Тяжёлые неизлечимые формы наблюдаются у 2−3% больных.
Когда врач начинает лечить больного с подозрением на лимфому или другую болезнь крови, то ему необходимо понять, в каком состоянии находится очень важный орган пациента, в котором происходит кроветворение – костный мозг. Для этого делаются специальные анализы, о которых мы постараемся рассказать подробнее.
При взятии костного мозга для анализа, как и при взятии любого другого материала из организма используются принципы максимальной пользы, безопасности и безболезненности. Делают это уже десятки лет, поэтому методики надежно отработаны. Чаще всего используют аспирационную биопсию и трепанобиопсию костного мозга.
Аспирационную биопсию выполняют так. Врач вместе с пациентом решают, из грудины или со спины брать костный мозг. Если выбирают первый вариант, то протирают спиртом кожу над верхней третью грудины, обезболивают новокаином мягкие ткани и специальной иглой и шприцем берут 0,5 миллилитра костного мозга. Если выбирают второй вариант, то на границе ягодичной и поясничной области, отступив от позвоночника в сторону на 10 см, обрабатывают кожу спиртом и обезболивают мягкие ткани. Затем также специальной иглой берут полмиллилитра костного мозга на анализ. Вся процедура от момента протирания кожи спиртом до окончания в опытных руках занимает времени меньше минуты. Как до, так и после нее можно сразу есть, пить, мыться, словом, заниматься повседневными делами.
Получение капельки костного мозга позволяет провести:
- исследование клеточного состава;
- исследование генов и хромосом опухолевых и стволовых клеток;
- проточную цитометрию клеток;
- молекулярно-генетические исследования.
В обычной врачебной работе трепанобиопсию костного мозга делают очень редко, и мало кто знает, что это такое. Именно поэтому кратко опишем, как она делается. Сразу скажем, что во время забора анализа любое прикосновение к любым нервам, позвонкам, спинному мозгу полностью отсутствует. Процедура достаточно простая и может проходить амбулаторно, но делает ее обязательно врач. Пациент может сидеть или лежать в зависимости от своего желания и навыков доктора.
Укажем точки на теле, откуда берут материал. На границе ягодичной и поясничной области, отступив 10 см от позвоночника в сторону, врач находит места, где очень близко к поверхности кожи подходят самые массивные кости человека – подвздошные кости таза. Врач протирает спиртом кожу, тонкой иглой обезболивает мягкие ткани и специальной иглой берет материал. Вся процедура от момента протирания кожи спиртом до получения маленького столбика костной ткани (длиной один-два см) в опытных руках занимает три-четыре минуты. Как до, так и после нее можно сразу есть, пить, мыться, одним словом, заниматься повседневными делами. На месте взятой кости быстро вырастает новая костная ткань. Полученный материал отправляют на гистологическое исследование. При необходимости выполняют углубленное иммуногистохимическое исследование.
Лабораторий, в которых могут квалифицированно проанализировать полученный материал, в городе мало. Кроме того, сама методика анализа очень трудоемкая, поэтому подготовка ответа занимает не менее двух недель.
Капелька костного мозга аккуратно распределяется по стеклышку, окрашивается специальными красками и отправляется в лабораторию. Как правило, микроскопический анализ и написание заключения занимает 1-2 дня. Этот метод относится к одному из самых технически простых, однако специалистов-цитологов, способных правильно оценить то, что видно под микроскопом, в городе очень мало.
Цитогенетическое исследование выявляет болезнь на уровне хромосом.
Ученые создали специальные реактивы – белки-ферменты, которые сами находят в исследуемой жидкости нужный ген и делают множество его копий, которые легко обнаружить. Этот метод называется полимеразная цепная реакция (ПЦР). С помощью ПЦР можно обнаружить любой ген – и опухолевый и инфекционный, даже если в организме больного организма опухолевые клетки присутствует в ничтожно малых количествах. Метод очень точен, прост в использовании, но тоже требует чрезвычайно дорогостоящего оснащения (оборудования, реактивов) и труда специалистов. Ответ выдается через 1-2 дня после постановки анализа.
Некоторые гены очень тяжело выявить полимеразной цепной реакцией, тогда на помощь приходит FISH-метод. При FISH-методе используют уже сделанные на заводе светящиеся крупные молекулы настроенные на те гены, которые необходимо обнаружить. Эти молекулы смешивают с кровью пациента, а потом врач лабораторной диагностики по характеру свечения определяет результат. Метод очень точен, однако имеет свои сложности в применении и требует чрезвычайно дорогостоящего оснащения (оборудования, реактивов) и труда высококлассных специалистов. Ответ выдается через 1-2 дня после постановки анализа.
Как же делается проточная цитометрия? Представим, что можно аккуратно кисточкой покрасить каждый волосок плода киви в свой цвет. Задача фантастически сложная. Тем не менее, с этой задачей справляются врачи-цитометристы, аппараты которых могут в автоматическом режиме за несколько минут покрасить и оценить десятки поверхностных молекул на сотнях тысяч клеток, найти и обозначить больные клетки. При этом метод позволяет исследовать любые клетки в любой жидкости: кровь, костный мозг, плевральную жидкость и т.д. Проточная цитометрия незаменима в диагностике лейкозов и многих других болезней крови, когда необходимо быстро и точно поставить диагноз.
Проточная цитометрия –это очень сложное дело, которое требует дорогого оснащения, труда очень квалифицированного специалиста. Выполняют этот анализ только в некоторых больницах. Несомненный плюс данной методики в том, что можно исследовать любой жидкий материал, что она быстрая и высочайше точная. Анализ и написание заключения занимает 1-2 дня, но сложные случаи могут потребовать больше времени.
При гистологическом исследовании врач-патологоанатом изучает материал на клеточном уровне. Для этого взятый при биопсии кусочек органа или ткани специальным образом обрабатывают, делают тончайшие срезы и смотрят под микроскопом. При многих заболеваниях имеются типичные изменения в тех или иных органах, поэтому иногда достаточно только гистологического анализа, чтобы точно поставить диагноз. Если же врач обнаруживает изменения, похожие на опухолевые, то для более точного диагноза необходимо дополнительное проведение иммуногистохимического исследования.
С помощью гистологического исследования костного мозга можно ответить на многие вопросы. Например, при необъяснимом уменьшении количества каких-то клеток крови (тромбоцитов, лейкоцитов, эритроцитов) это единственный метод, который позволяет с вероятностью 100% исключить поражение костного мозга лимфомой или другим опухолевым процессом. Этот метод позволяет выяснить, правильно ли происходит кроветворение или есть в нем какие-либо нарушения. Гистологическое исследование незаменимо для выявления поражения костного мозга, например, метастазами, болезнями крови, инфекцией. В связи с длительной лабораторной обработкой материала для анализа время до выдачи результата составляет не менее двух недель.
Суть данного метода в целом близка методу проточной цитометрии. С помощью специальных красок и приборов окрашиваются молекулы на поверхности клеток, и врач-патологоанатом изучает результат. Различия состоят в том, что в данной ситуации исследуют не жидкую часть, а твердые кусочки тканей и органов, взятые при биопсии. Этот метод тоже высокотехнологичен, дорогостоящ и требует работы специалиста высокого класса. Немногие лечебные центры способны качественно выполнять данное исследование.
Пересадка костного мозга при лимфоме является одним из способов лечения. Она позволяет восстановить функции системы кроветворения, избавляет от опасного заболевания. Но процедура отличается высокой степенью сложности, имеет ряд противопоказаний, что сказывается на стоимости трансплантации.
Эффективность пересадки костного мозга при лимфоме

Лимфома – это группа онкологических заболеваний, поражающих лимфатическую систему больного. Развитие злокачественных опухолей наблюдается в любом органе, через который проходит лимфа. Последние годы показали высокую эффективность химиотерапии при лечении этого заболевания. Но для ряда больных единственным шансом остается пересадка костного мозга.
Основные причины гибели костного вещества при лимфоме:
- Поражение при метастазировании на 2–4 стадии. Чаще развивается при неходжкинских лимфомах В-типа.
- Развитие рецидива, при котором клетки новой опухоли не реагирует на применяемые протоколы, уничтожает иммунную систему.
- Клетки костного мозга могут погибнуть при лечении высокодозной химией, превышении допустимой дозы при лучевой терапии.
В этой ситуации костный мозг больного перестает производить кровяные клетки и тельца, полностью отсутствует иммунная защита. Больной может погибнуть от любой инфекции в течение нескольких суток. С помощью трансплантации врачам удается победить аплазию костного мозга, добиться его восстановления и эффективного функционирования.
Трансплантация костного мозга при лимфоме применяется нечасто. Этот метод лечения используется только в ситуациях, когда более простые и доступные терапевтические способы не дают результата. Его эффективность зависит от многих факторов и достигает 80% при лимфоме разного типа. Последние исследования, проводимые онкологическими центрами Беларуси и России, показали уровень стойкой ремиссии у 88,1% людей, перенесших пересадку. Более 51% пациентов живут после процедуры без дополнительной поддерживающей терапии свыше 5 лет.
Виды пересадок костного мозга
В медицинской практике выделяют несколько видов трансплантации:
- пересадка костного мозга;
- введение препарата на основе стволовых клеток;
- переливание пуповинной крови.
При лечении лимфомы пересадка осуществляется разными способами:
- Аутологичным.
- Аллогенным (аллотрансплантация).
Некоторые врачи относят аутологичную пересадку к поддерживающей терапии, которую применяют на 2–3 стадии лимфогранулематоза или лимфомы Ходжкина. Стволовые клетки вводят только при стойкой ремиссии или на стадии, когда метастазы еще не поразили костный мозг больного. В качестве донора выступает сам пациент, что снижает риск отторжения до минимального.
Аллотрансплантация делится на несколько видов:
- Сингенная – забор материала производится от близнеца-донора, генетические данные которого совпадают максимально.
- Гаплоидентичная – успешность операции во многом зависит от уровня совместимости. Поэтому кандидат подбирается из числа близких родственников-доноров с совместимостью 50% и выше (родители, братья, сестры).
- Пересадка от совместимого неродственного донора – при отсутствии других вариантов больному подбирается кандидат из числа людей, генетический материал которых совпадает минимум на 35%.
При аллогенной трансплантации значительно повышен риск отторжения и осложнений после проведения операции.
Пересадка при болезни Ходжкина
Лимфома Ходжкина в большинстве случаев хорошо реагирует на химиотерапию, достигая стойкой ремиссии. Но остается определенный процент больных, которым не помогают традиционные методики лечения. На 2–3 стадии может возникнуть поражение костного мозга, требующее принятия срочных мер. Для данного типа лимфом рекомендуется аутологичный вид трансплантации.
Пересадка костного мозга при лимфоме Ходжкина чаще производится путем переливания специального раствора. Его заранее изготовляют из стволовых клеток больного, которые получают путем фильтрации костного мозга и периферической крови. Перед проведением процедуры больному проводится курс полихимиотерапии, которая помогает остановить развитие онкологии.
Первые результаты появляются через 4–6 недель, когда начинается активная выработка собственных кровяных клеток. Если проведена пересадка костного мозга при лимфоме Ходжкина, прогноз зависит от многих факторов: возраст, наличие хронических болезней, острые инфекции во время реабилитации. Но при отсутствии отторжения длительная ремиссия возникает у 60–80% заболевших, против 0,8–3% без проведения уникальной процедуры.
Трансплантация при неходжкинских лимфомах
При неходжкинских лимфомах поражение костного мозга встречается гораздо чаще, протекает более агрессивно. Оно является результатом распространения метастазов или первичного поражения органа кроветворения.
Основные задачи трансплантации:
- Если наблюдается опухоль с низкой реакцией на химиотерапию, больной может погибнуть при проведении агрессивного лечения. После пересадки костного мозга организм быстрее восстанавливается, вырабатывает здоровые стволовые клетки, выдерживает усиленную терапию, побеждая смертельное заболевание. Методика сочетания аутологической пересадки и интенсивной химиотерапии уже активно применяется в клиниках Израиля и США, показывает хорошие результаты.
- При поражении и гибели костного мозга пересадка остается единственным способом его восстановления: без эффективной работы системы кроветворения больной не выживет даже при устойчивой ремиссии.
Дабы уменьшить риск рецидива после проведения трансплантации, применяется инфузия тромбомассы и лимфоцитов, защищающая от инфекций.
Показания и противопоказания для пациента
Трансплантация костного мозга при лимфоме требуется при лечении наиболее тяжелых видов онкологии:
- неходжкинские лимфомы;
- лимфома Ходжкина;
- миелоидный лейкоз;
- лимфобластная лимфома;
- миелодиспластический синдром.
В европейских онкологических центрах 30% всех пересадок костного мозга приходится на неходжкинские формы, 11% на лимфому Ходжкина.
Но процедура имеет ряд противопоказаний, которые делают трансплантацию невозможной:
- наличие хронических инфекций (мононуклеоза, сифилиса, грибковых патологий);
- опухоль не восприимчива к препаратам химиотерапии, поэтому невозможно провести процесс подготовки к переливанию стволовых клеток от донора;
- иммунная деструкция тромбоцитов, при которой риск отторжения максимальный;
- дисфункция почек или печени, серьезные патологии сердца, способные привести к летальному исходу.
Перед процедурой проводится ряд обследований и анализов, помогающих оценить общее состояния пациента.
Что должен знать донор?
Подавляющее большинство пересадок приходится на костный мозг и стволовые клетки, полученные от неродственного донора. В европейских странах и США существует огромный реестр добровольных кандидатов, который используется для лечения больных лейкемией и лимфомами.
Донорство является добровольной процедурой, поэтому кандидат всегда может отказаться от его проведения. Учитывая высокую стоимость забора и обработки биоматериала, донор должен со всей ответственностью подойти к процедуре, заботиться о своем здоровье.
Он обязан предупредить врачей о любых изменениях, способных повлиять на качество костного мозга:
- перенесенные недавно грипп, ОРВИ;
- менструация;
- последний день приема алкогольных напитков.
После процедуры забора костного мозга донору можно покинуть лечебное учреждение уже на следующий день. Иногда в течение 2–5 суток сохраняется болезненный синдром, который легко снимается обезболивающими препаратами, не требует лечения. На полное восстановление мозгового вещества требуется 14–20 дней. В это время рекомендуется уменьшить физические нагрузки, наполнить рацион полезными продуктами, обогащенными витаминами и минералами.
Показания и противопоказания для донора
Среди потенциальных доноров биоматериала проводится тщательный отбор. Поэтому к забору и допускаются только здоровые люди возрастом от 18 до 45 лет. После донорства костный мозг таких кандидатов восстанавливается быстро без осложнений для здоровья. Как правило, они легко переносят процедуру, понимая всю ответственность и важность решения.
Даже при самой тщательной фильтрации и подготовке остается риск загрязнения инфицированными донорскими клетками. Поэтому при пересадке к потенциальному донору предъявляются строгие требования.
Противопоказаниями являются следующие болезни и патологии:
- аутоиммунные заболевания;
- ВИЧ;
- перенесенный ранее туберкулез, сыпной тиф;
- гепатит С;
- хронические инфекции;
- психические заболевания.
Донором костного мозга при пересадке не может стать человек, имеющий хронические заболевания:
- печени (цирроз, холецистит);
- почек (мочекаменная болезнь, дисфункция);
- гиперплазию щитовидной железы;
- язву желудка или кишечника;
- бронхиальную астму;
- сахарный диабет.
Временными противопоказаниями к включению в донорский реестр становятся переливание крови, поездки в экзотические страны, контакт с носителями вирусного гепатита. Такие кандидаты могут приступить к сдаче анализов только через полгода после события.
Забор донорской кроветворной ткани

Забор материала для последующей трансплантации производится разными способами. Наибольшая концентрация клеток костного мозга у взрослого человека наблюдается в бедренной или подвздошной тазовой кости. Перед процедурой донора госпитализируют, проводят ряд анализов, чтобы убедиться в отсутствии воспалений и инфекций. Все манипуляции проводятся под общей или эпидуральной анестезией.
Для забора ткани хирург делает несколько проколов в кости донора специальной иглой. Через них производится пункция. В среднем за один прием врачам необходимо получить от 15 до 20 мл костного вещества. После выхода из наркоза и оценки общего состояния донор может возвращаться к привычному образу жизни. При таком способе удается получить максимальное количество материала и стволовых клеток всего за 30–40 минут.
Гораздо реже используется методика забора венозной крови. За 2–3 недели потенциальный донор начинает принимать специальные препараты, стимулирующие выброс стволовых клеток. Это повышает ценность биоматериала. После очищения и выделения ценных элементов кровь возвращают донору, что ускоряет процесс восстановления. Среди недостатков метода – на процедуру забора уходит несколько часов, могут наблюдаться головокружения, тошнота, дискомфорт. Кроме того, для получения необходимого объема забор повторяют до 6 раз.
Подготовка и процедура пересадки КМ при лимфоме
Чтобы трансплантация прошла успешно для больного, проводится специальная подготовка. Обязательная часть – проведение нескольких курсов полихимиотерапии в сочетании с облучением.
Предназначение иммуносупрессивной терапии (конденсирования):
- Такое интенсивное лечение позволяет добиться временной ремиссии, во время которой производится трансплантация.
- Необходимо разрушить собственный костный мозг пациента, чтобы освободить пространство для донорского.
- Происходит полное подавление иммунной системы больного, которая может стать причиной быстрого отторжения костного мозга.
Пациента перед трансплантацией помещают в асептическую (стирильную) палату, чтобы не допустить контакта с носителями вирусных или бактериальных заболеваний, попадания в кровь патогенных возбудителей. В этот период проводится процедура подготовки донорской ткани, последние контрольные исследования.
Трансплантация мало напоминает хирургическую операцию: во время процедуры материал из стволовых клеток переливается с помощью капельницы. Он смешивается с кровью пациента, равномерно распределяется по всему организму. Трансплантат оседает в трубчатых костях, запуская процесс формирования здорового костного мозга. Для поддержки организма в этот ответственный период времени проводится вливание тромбоцитов донора, которые уменьшают риск отторжения.
Что происходит после трансплантации КМ?
Ежедневно больному следует сдавать анализы крови: врачи контролируют показатели, отслеживают динамику. Ему проводится поддерживающая терапия с применением антибиотиков, витаминов и антисептиков. Пациент остается в полной изоляции, чтобы исключить заражение инфекцией. В этот период человек испытывает не только физические, но и психологические проблемы, опасаясь осложнений и рецидива лимфомы.
Осложнения и побочные эффекты
Наиболее опасные осложнения, с которыми может столкнуться пациент после пересадки:
- у каждого второго больного через несколько дней начинается отторжение, способное привести к летальному исходу;
- анафилактический шок при аллергии на донорские клетки или тромбоциты;
- инфицирование различными заболевания при отсутствии иммунной защиты;
- происходит отказ почек из-за интоксикации.
В первые 2 недели после процедуры реципиент может столкнуться с побочными эффектами, осложняющими процесс приживления:
- болезненное воспаление слизистой желудка и кишечника;
- сильная слабость, постоянная сонливость;
- головные боли;
- сердечная аритмия;
- проблемы с мочеиспусканием;
- полное отсутствие аппетита.
Для снижения неприятных ощущений реципиенту дают специальные питательные растворы, содержащие необходимые организму вещества и микроэлементы. Они вводятся в кровь, чтобы уменьшить нагрузку на пищеварительную систему.
Питание и диеты до и после проведения процедуры

До трансплантации костного мозга больному рекомендуется легкое питание без большого количества ограничений. Как правило, в этот период проходит химиотерапия, поэтому аппетит практически отсутствует Лучше исключить жареные и жирные блюда, мясо, заменив животные белки творогом.
После пересадки необходимо придерживаться определенных рекомендаций:
- отказ от алкоголя, тонизирующих напитков;
- употребление большого количества овощей, фруктов;
- включение в пищу продуктов, улучшающих состояние крови (свекла, печень, гранатовый сок);
- ежедневное употребление свежих соков, морсов, компотов;
- снижение в рационе сахара, сдобы и сладостей.
До восстановления пищеварения некоторым пациентам рекомендуется употребление детских пюре. Они имеют гомогенизированную структуру, не содержат искусственных добавок и специй.
Прогноз жизни
Пересадка костного мозга при лимфоме или других заболеваниях кроветворной системы проводится с 1990 года.
Многочисленные наблюдения и исследования доказали, что прогноз выживаемости зависит от некоторых факторов:
- возраст (наилучшие результаты фиксируются у детей и молодых людей до 25 лет);
- половая принадлежность (гормональный фон женщины является дополнительной защитой от отторжения);
- степень поражения лимфатической системы при лимфоме.
При онкологии сложно составить прогноз жизни после пересадки костного мозга. Но последние данные показали, что после трансплантации до 80% пациентов прожили от 5 до 8 лет. Свыше 10 лет живет каждый второй пациент, не имевший шанса на выздоровление без трансплантации.
Где можно пройти процедуру в России, какая ее стоимость?
Донорство костного мозга только развивается в России, а реестр доноров насчитывает не более 10 000 кандидатов (против 7 млн. в Германии).
Но существует ряд клиник, которые проводят пересадку при лимфоме на высоком уровне:
Стоимость процедуры складывается из затрат на многочисленные анализы, подготовительный период, реагентов для приготовления препарата из стволовых клеток и многих других факторов. В зависимости от ситуации трансплантация стоит от 1 до 3 млн. рублей.
Если вы нашли ошибку просто выделите ее и нажмите Shift + Enter или нажмите здесь. Большое спасибо!
Спасибо за ваше сообщение. В ближайшее время мы исправим ошибку
Читайте также: