Программы для больных меланомой
Дата публикации: 25.04.2018
Введение
Меланома кожи – злокачественная опухоль нейроэктодермального происхождения, исходящая из меланоцитов (пигментных клеток) кожи [1]. Заболеваемость меланомой резко возросла за последние 60 лет, увеличиваясь быстрее, чем все другие солидные опухоли [2]. В РФ в 2014 году прирост заболеваемости составил 8,3% у мужчин (4-5 место по величине прироста) и 10% у женщин (8 место по величине прироста), а летальность на первом году жизни после постановки диагноза составила 11,9%. Под наблюдением на конец 2014 года состояло 79945 больных (54,8 на 100 000 населения), из них 5 лет и более наблюдались 45686 больных (57,2%) [3].
Меланома на ранних стадиях (I, II и III операбельная стадия) успешно лечится хирургическими методами, но более поздние стадии, для которых типично метастазирование, обычно считаются некурабельными. Несмотря на внедрение таргетной и иммунобиологической терапии, меланома остается крайне агрессивным заболеванием. У значительной части пациентов развивается устойчивость к ингибиторам BRAF или наблюдается прогрессия даже на фоне иммунотерапии. На поздних стадиях это заболевание имеет крайне неблагоприятный прогноз, при этом медиана 5-летней выживаемости составляет менее 10%.
К наблюдательной программе планируется подключение медицинских организаций, занимающихся курацией пациентов, страдающих меланомой. Их количество не ограничено, а участие – добровольно.
Программа рассчитана на 3 года, если не будет принято решение о ее продолжении. Планируемый период набора и мониторинга пациентов – 2017-2020 гг., с возможностью продления.
В состав научного комитета входят:
• Проценко Светлана Анатольевна - д.м.н., зав. отделением химиотерапии и инновационных технологий НМИЦ онкологии им. Н. Н. Петрова, ведущий научный сотрудник отдела инновационных методов терапевтической онкологии и реабилитации НМИЦ онкологии им. Н. Н. Петрова.
• Вальков Михаил Юрьевич - д.м.н., зав. кафедрой лучевой диагностики и лучевой терапии с курсом клинической онкологии СГМУ, г. Архангельск.
Администрированием проекта занимается АО "Астон Консалтинг".
Основной целью программы является модернизация системы учета пациентов, страдающих меланомой, и получение достоверной информации о рутинной клинической практике. В рамках программы планируется оценить заболеваемость по обращаемости, смертность, выживаемость; частоту использования различных терапевтических подходов и схем лекарственной терапии; эффективность и безопасность лекарственной терапии на разных стадиях течения процесса; частоту назначения таргетных и иммунобиологических препаратов для лечения меланомы; выявить потребность в таргетных, иммунобиологических препаратах и организовать экспертную поддержку врачебных решений.
Первые результаты
Список литературы
1.Clark WH, Jr., Elder DE, Guerry Dt, Epstein MN, Greene MH, Van Horn M: A study of tumor progression: the precursor lesions of superficial spreading and nodular melanoma. Hum Pathol 1984, 15(12):1147-1165.
3. Давыдов М. И., Аксель Е. М.: Статистика злокачественных новообразований в 2014 г. Данные по России. Евразийский онкологический журнал 2016, 4(4):824-861.
+7(925)191-50-55
В настоящее время в мировой онкологической практике докторами успешно применяется инновационная программа лечения продвинутых стадий меланомы, именуемая TIL (сокр. От tumour-infiltratinglymphocytes).
Этот уникальный в своем роде подход относится к иммунологическим методикам лечения, основанным на активации собственных защитных сил человеческого организма, и поэтому имеет минимум побочных и неблагоприятных эффектов.
Еще одним важнейшим преимуществом протокола TIL является его универсальность. Это означает, что в отличие от прочих воздействий, основанных на иммунных механизмах защиты, TIL-терапия способна помочь лицам с различными генетическими вариантами опухолевых клеток. Суть ее заключается в инфильтрации новообразования лимфоцитами, благодаря чему уничтожаются злокачественно-перерожденные клетки.
Технология TIL предполагает выделение из ткани метастазов (вторичных очагов) меланомы TIL-элементов и клеток опухоли. Из полученных TIL-клеток специалисты отбирают те, которые обладают наибольшим потенциалом для уничтожения меланомных клеток, и искусственно, в лабораторных условиях размножают их, а потом вводят в кровь больного.

Согласно наблюдениям, активность подобных клеток-убийц, на создание клона которых у экспертов уходит от двух недель до одного месяца, довольно высока.
Если результативность TIL-терапии у конкретного пациента подтверждается, ему в целях усиления лечебного эффекта назначается курс подготовительной химиотерапии флударабином (Fludarabinum) и циклофосфамидом (Cyclophosphamidum), первоочередная цель которого – нейтрализация биологических систем, способных помешать борьбе выведенной популяции лимфоцитов с меланомными клетками.
После окончания химиотерапии больному внутривенно капельно вливают миллионы TIL-клеток. Чтобы дополнительно простимулировать эти лимфоциты-киллеры используется интерлейкин-ΙΙ –медпрепарат из группы так наз. иммуномодуляторов.
Так как TIL-протокол лечения меланомы предполагает применение собственных лимфоцитов пациента, его организм не расценивает их как чужеродные агенты. Благодаря этому удается избежать нежелательных реакций и получить весьма стойкие результаты лечения.
Метод не является панацеей и, к сожалению, не обладает безграничными возможностями. Он не способен полностью излечить пациента с запущенной формой меланомы, однако на современном этапе TIL-терапия считается одним из самых безопасных и высокоэффективных средств, помогающих продлить и улучшить качество жизни больных, у которых диагностирован злокачественный онкопроцесс ΙΙΙ-ΙV стадии.
Это очень важно, ведь еще совсем недавно обнаружение метастазирующих, неоперабельных меланом означало для больных, среди которых, кстати, немало молодых людей в возрасте от тридцати до сорока лет, неотвратимую и быструю гибель.
Опухолево-перерожденные клетки достаточно быстро распространяются при меланоме и лимфогенным способом в лимфоузлы, и гематогенным путем в отдаленные от первичного очага ткани и органы. Причем нередко метастазы меланомы возникают при относительно малых размерах материнской опухоли.
Благодаря TIL-терапии можно приостановить дальнейшее развитие это опасного онкозаболевания, обратить вспять рост метастатических очагов, уменьшить выраженность симптомов раковой интоксикации и заметно улучшить общее самочувствие пациента.
Решение о целесообразности участия пациента в программе принимается только во время консультации с его лечащим врачом-онкологом после предварительного тщательного обследования. Основными ограничениями служит вероятность корректного подбора клеток, которая сейчас составляет приблизительно 50%. Если необходимый для терапии тип клеток в лабораторных условиях воспроизвести не удается, TIL-программу прекращают. В качестве альтернативы больному дозировано вводят те лейкоциты, которые уже удалось получить за непродолжительный промежуток времени.
+7(925)191-50-55
г. Москва, Духовской переулок, 22б
+7(925)191-50-55 - европейские протоколы лечения в Москве

Российские онкологи предостерегают граждан от чрезмерного пребывания на солнце и в солярии, особенно в летний период. Ультрафиолетовое излучение является одним из главных факторов, вызывающих рак кожи, а за последние 10 лет прирост пациентов с этим диагнозом в мире составил 30%.
— Светлана Анатольевна, специальная сессия, посвящённая меланоме кожи, стала одним из центральных событий IV международного онкологического форума.
— Еще несколько лет назад считалось, что рак кожи — это смертельное заболевание. Что-то изменилось с тех пор?
— Много ли больных меланомой в России и в мире, если есть статистика?
— В мире на протяжении последних десятилетий отмечается неуклонный рост заболеваемости меланомой кожи, в год выявляется более 200 тысяч новых случаев.
В России ежегодно регистрируются около 10 000 новых случаев меланомы кожи. Причём большинство заболевших — это люди трудоспособного возраста. К сожалению, в нашей стране около четверти всех пациентов на момент постановки диагноза имеют местно-распространённую или метастатическую форму заболевания (III-IV стадию), при которой прогнозы обычно неблагоприятны.
Результаты лечения и показатели выживаемости напрямую зависят от того, на какой стадии заболевания был диагностирован опухолевый процесс. Если на раннем этапе 5-летняя выживаемость превышает 90%, при второй стадии составляет около 65%, то при локально-регионарной, третьей стадии снижается до 45%, а при метастатической (четвертой стадии) составляет не более 20%.
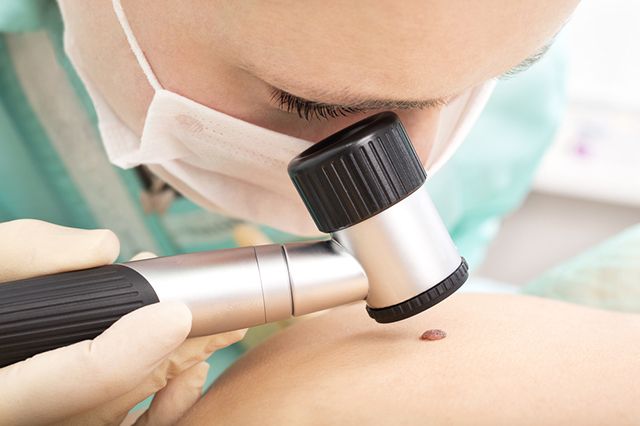
— Кто, прежде всего, находится в зоне риска?
— Один из главных факторов риска развития меланомы кожи, по мнению исследователей, связан с избыточным воздействием ультрафиолетовых лучей, как на открытом солнце, так и в солярии. Шансы развития меланомы увеличиваются у людей с первым и вторым фототипом кожи (белокожий/рыжий, светлокожий), при котором образуется меньше всего защитного пигмента. Поэтому хочу призвать всех читателей: при малейшем подозрении немедленно обращайтесь к врачу. Выявление меланомы на ранней стадии — как правило, залог полного излечения. И, конечно, по-прежнему актуальная рекомендация: не злоупотребляйте естественным или искусственным ультрафиолетом!

— Насколько эффективно сегодня борются с меланомой в России? У нас свои препараты, методики лечения и химиотерапии или в основном зарубежные?
— В России сейчас зарегистрированы и применяются в клинической практике все современные противоопухолевые препараты для лечения меланомы кожи (таргетные, иммуноонкологические). Они могут использоваться как при монотерапии, так и в комбинации. Эффективность комбинированной терапии выше, но и частота побочных эффектов значительно увеличивается. Поэтому применение противоопухолевой терапии должно осуществляться строго по показаниям и только в специализированных онкологических учреждениях. Благодаря использованию современных препаратов удалось добиться увеличения выживаемости пациентов, как общей, так и без прогрессирования заболевания.
Конечно, в основном сегодня мы пользуемся импортными противоопухолевыми препаратами, однако в настоящее время есть и отечественные разработки. Сейчас проводятся клинические исследования двух лекарственных образцов. Мы с нетерпением ждём результатов!
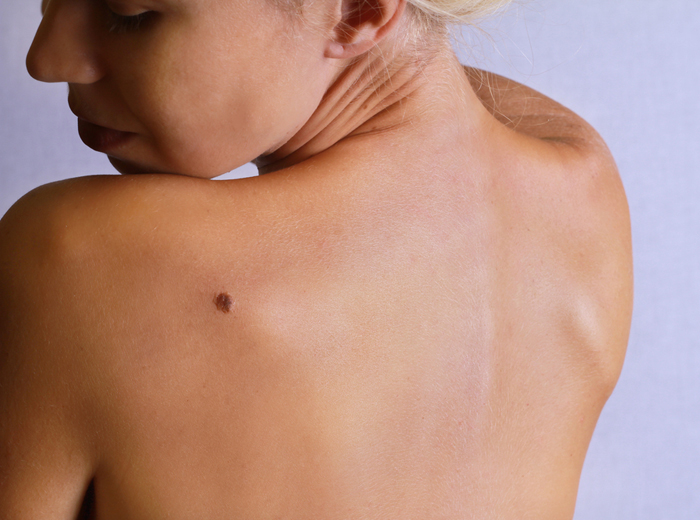
Заболеваемость
Средний показатель заболеваемости меланомой кожи варьирует от 3-5 случаев на 100 тыс. чел. в год в странах Средиземноморья до 12-20 случаев на 100 тыс. чел. в год в странах Северной Европы и продолжает расти. Показатель смертности составляет 2-3 случая на 100 тыс. чел. в год с небольшими изменениями в зависимости от географического положения, и остается относительно стабильным в последнее десятилетие. Однако, показатель смертности у мужчин, в отличие от женщин, увеличился в течение последних 25 лет. Возросшая экспозиция к ультрафиолетовому излучению генетически предрасположенной популяции, по меньшей мере, отчасти обусловливает постоянный рост заболеваемости на протяжении последних десятилетий.
Диагноз
Подозрительные образования характеризуются асимметричностью, нечеткостью границ, неоднородным цветом, а также изменением цвета, уровня и размеров в течение последних месяцев («правило ABCD”). В настоящее время многие первичные новообразования имеют диаметр менее 5 мм [B]. Демография, проведенная опытным врачом, повышает диагностическую достоверность [B].
Диагноз должен быть поставлен после выполнения полной эксцизионной биопсии опухолевого образования с отступом от края опухоли с последующим морфологическим исследованием материала в специализированном онкологическом учреждении.
Гистологическое заключение должно соответствовать классификации AJCC (Американский объединенный онкологический комитет) и включать в себя максимальную толщину опухоли в миллиметрах (по Below), уровень инвазии (по Clark I-V), наличие изъязвления, наличие и выраженность признаков регрессии, и расстояние до краев резекции. Однако в определенный момент оценка уровня инвазии по Clark была опущена и заменена определением скорости митозов в первичной опухоли.
Стадирование
Необходимы общий осмотр пациента и особое внимание к подозрительным пигментированным образованиям на коже, сателлитным образованиям, транзиторным метастазам, метастазам в регионарные лимфоузлы и системным метастазам [V,D].
При меланоме с низким риском рецидива (толщина
Лечение локальных стадий
Необходимо широкое иссечение первичной опухоли в пределах здоровых тканей с краями резекции от границы опухоли [II, B]:
- 0,5 см для меланомы in situ;
- 1,0 см при толщине опухоли по Breslow 1–2 мм;
- 2,0 см при толщине опухоли 2 мм. Модифицированные варианты резекции возможны для сохранения функций при меланоме кожи пальцев или кожи ушной раковины.
Не рекомендуется рутинное выполнение избирательной лимфаденэктомии или проведение лучевой терапии на регионарные лимфатические узлы [II, B].
В настоящее время не существует стандартной адъювантной терапии для пациентов с высоким риском рецидива заболевания после удаления первичной опухоли (стадия IIB/C) или радикального удаления регионарных лимфоузлов (стадия III).
В ряде проспективных рандомизированных исследований изучалось лечение низкими, средними и высокими дозами интерферона (ИФН-.). Проведение данной терапии после резекции первичной опухоли улучшило показатели безрецидивной выживаемости (RFS), однако не повлияло существенно на общую выживаемость (OS).
Первым исследованием, в котором отмечалось улучшение общей выживаемости, было исследование ECOG 1684: в него было включено 287 пациентов, 1-я группа пациентов получала терапию высокими дозами ИФН-альфа, 2-я группа была оставлена под наблюдением. Из-за тяжелых побочных эффектов лечение у 25% пациентов было отменено. 5-летняя безрецидивная выживаемость составила 37% против 26%, общая выживаемость была 46% против 37%. Результаты этого протокола привели к регистрации FDA данного режима терапии в качестве адъювантного лечения. Мета-анализ исследований тяжелой высокодозной терапии интерфероном не выявил статистически значимого влияния на показатель общей выживаемости. Тогда было сделано предположение, что лечение ИФН наиболее эффективно при длительной терапии.
Предположение о целесообразности пролонгированного назначения ИНФ в высоких дозах послужило предпосылкой для проведения Европейской организацией по исследованию и лечению рака (EORTC) крупного проспективного рандомизированного исследования для изучения эффективности пегилированного интерферона-альфа2b (ПЭГ-ИФН-альфа-2b) в адъювантном режиме у пациентов с III стадией меланомы. Всего 1256 больных только III стадией меланомы после удаления первичного образования были рандомизированы в лечебную группу или группу наблюдения. Рандомизация была стратифицирована в соответствии с микроскопическим (N1) и макроскопическим (N2) поражением лимфатических узлов, количеством вовлеченных узлов, наличием изъязвления и толщиной опухоли. Безрецидивная выживаемость (первичная конечная точка), выживаемость без отдаленных метастазов и общая выживаемость были проанализированы у всех, включенных в исследование пациентов, принявших хотя бы одну дозу препарата.
Это исследование показало, что пролонгированная адъювантная терапия ИФН-альфа улучшает безрецидивную выживаемость и выживаемость без отдаленных метастазов в подгруппе пациентов с небольшой массой опухоли.
Таким образом, в данной популяции пациентов пегилированный интерферон может быть рекомендован к использованию, если пациент хорошо переносит его применение [C].
Адъювантную терапию пациентов с резекцией пораженных макроскопических узлов предпочтительно проводить в рамках рандомизированных клинических исследований в специализированных центрах. И, тем не менее, данный диагноз является утвержденным показанием к применению высоких доз ИФН-альфа-2b.
Адъювантная химиотерапия или гормонотерапия не улучшают результаты лечения.
Адъювантная иммунотерапия другими цитокинами с включением интерлейкина- 2, вакцинотерапия и иммунохимиотерапия являются экспериментальными лечебными подходами [III], которые не рекомендуется использовать вне клинических исследований.
Возможность проведения лучевой терапии должна быть рассмотрена в случае неадекватной резекции краев опухоли при невозможности выполнения повторной резекции у больных меланомой типа злокачественного лентиго или при неадекватной резекции (R1) метастазов меланомы [B].
Лечение локорегионарных стадий
В случае изолированного поражения регионарных лимфоузлов всем пациентам должна выполняться радикальная лимфодиссекция. Удаление только пораженного лимфоузла является недостаточным объемом операции [II–III,C].
При наличии транзиторных метастазов или неоперабельных первичных опухолей конечностей может быть применена изолированная регионарная перфузионная терапия с включением мелфалана и фактора некроза опухоли (TNF) [II–III,C]. Данная терапия требует расширенного хирургического вмешательства и должна быть использована в отдельных лечебных учреждениях, имеющих опыт проведения подобного лечения. Лучевая терапия может использоваться в качестве альтернативы, хотя не существует четких данных о ее положительном влиянии на результаты лечения [V,D].
Лечение диссеминированных стадий (стадия IV; классификация AJCC 2002 г.)
Преимущественно лечение должно проводится в рамках клинических исследований. Однако не все пациенты c отдаленными метастазами меланомы могут в них участвовать. В этих случаях в качестве паллиативной терапии распространенного процесса с метастазами в нескольких различных анатомических областях для начала можно использовать хорошо переносимые цитостатики, такие как дакарбазин (DTIC), таксаны, фотемустин и др., а также цитокины (интерферон, интерлейкин-2) или их комбинации. Не cуществует стандартной терапии. Однако в таких ситуациях дакарбазин рассматривается как препарат выбора. При агрессивном метастатическом процессе многокомпонентная полихимиотерапия [C], включающая паклитаксел и карбоплатин или цисплатин, виндезин и дакарбазин дают частичный ответ и стабилизацию процесса у большого числа пациентов.
Рандомизированных клинических исследований интерлейкина-2 в монотерапии нет.
Некоторые центры до сих пор используют его в качестве первой линии терапии при небольшой массе опухолей. Рандомизированных исследований не выявили улучшения выживаемости при интенсивной терапии ИЛ-2. За последние десятилетия несколько клинических исследований II фазы показали возможность блокады CTLA4, а также ее применение в комбинации с вакцинами или химиотерапией. Лечение с использованием CTLA4 блокады способствовало увеличению выживаемости больных меланомой с метастатическим поражением до двух лет и больше. Однако эти перспективные результаты должны быть подтверждены рандомизированными клиническими исследованиями III фазы (таблица №2).
Хирургическое удаление висцеральных метастазов может быть проведено в отдельных случаях у больных с хорошим соматическим статусом и изолированным опухолевым поражением.
Возможности паллиативной лучевой терапии рассматриваются при наличии симптомов поражения головного мозга или локализованного поражения костей.
Наблюдение за больными с локальными и локорегионарными стадиями
Пациенты и члены их семей (особенно маленькие дети) должны быть предупреждены о необходимости регулярного осмотра кожи и лимфоузлов, а также о необходимости избегать появление солнечных ожогов или продолжительного воздействия искусственного UV-излучения без защитных средств. Пациенты должны быть предупреждены о повышенном риске развития заболевания у членов их семей [B].
Повторное заболевание развивается у 8% пациентов в течение 2-х лет после выявления первичной меланомы. Пациенты с меланомой кожи имеют повышенный риск развития других опухолей кожи. У пациентов со злокачественным лентиго вероятность развития других опухолей кожи в течение 5 лет достигает 35%.
Больные меланомой после первичного лечения активно мониторируются с целью более раннего выявления рецидива или повторной опухоли.
В настоящее время нет единого мнения в отношении необходимой частоты наблюдения за больными и рекомендуемого объема обследования. Не существует достаточных оснований для рекомендации регулярного проведения анализов крови, радиографического обследования с включением УЗИ, КТ и ПЭТ исследования вне протоколов по изучению адъювантной терапии и наблюдения за больными.
Больные с наследственным или спорадическим синдромом диспластического невуса имеют высокий риск и должны наблюдаться в течение жизни.
Рекомендации по наблюдению за пациентами строятся в зависимости от риска рецидива заболевания.
Клинический осмотр рекомендуется проводить каждые 3 месяца в течение первых 3 лет и далее каждые 6-12 месяцев. Поскольку пациенты с первичной опухолью методов исследования или специфических анализов крови при наблюдении за больными.


— Заболеваемость и смертность, ассоциированные с меланомой кожи, в России, как и в мире в целом, растут из года в год. В нашей стране ежегодно диагностируется 11 тыс. новых случаев меланомы кожи. Этот рост в большей степени связан с изменением образа жизни людей. К сожалению, в настоящее время наблюдается высокий показатель запущенности меланомы кожи – 19% всех случаев меланомы выявляются на поздних (III–IV) стадиях. Более того, среди всех онкологических заболеваний именно метастатическая форма меланомы имеет наибольший риск распространения в центральную нервную систему. Частота метастазирования в головной мозг для данной нозологии достигает 43% по объединенным данным клинических исследований.
— Зачастую люди не знают, что у них развивается меланома. Из-за дефицита информации общество не осознает важность данной проблемы. Сейчас наша главная задача – добиться ранней диагностики меланомы кожи: заболевание на первой стадии хорошо поддается терапии, при второй стадии вероятность излечиться преобладает над вероятностью хронической болезни. Однако говорить о полном излечении при второй стадии нельзя.
При этом нужно понимать, что массовый скрининг в данном случае малоприменим: показатель заболеваемости – 7 человек на 100 000, именно поэтому на первую роль выходит информирование людей о заболевании и активная работа с врачами первичного звена – дерматологами, хирургами и терапевтами.
— Существует ассоциация специалистов по проблемам меланомы, которая имеет интернет-ресурсы, где представлена важная медицинская информации и для пациентов, и для их родственников. Главное – достоверность источника: информация о меланоме или другом онкологическом заболевании не должна искажаться. Иногда читаешь какую-нибудь статью в интернете, и волосы просто дыбом встают. Там совершенно не то, что на самом деле в жизни. Поэтому я призываю обращать внимание на достоверные источники информации.
В 2020 году планируется продолжение проекта после стабилизации эпидемиологической ситуации.
— Что сейчас нового в лечении метастастической меланомы кожи, удается онкологам повысить выживаемость в этой группе пациентов?
— Важным этапом в лечении онкологических заболеваний стало развитие иммуноонкологии. Меланома кожи – одна из тех локализаций, которая тяжелее всего поддается другим методам лечения: стандартная химиотерапия дает короткий ответ в 20% случаев, а пятилетняя выживаемость пациента при этом не превышает 5%. При использовании современных иммунотерапевтических препаратов этот показатель выше в разы. Это очень хороший результат в сравнении с результатами химиотерапии.
В апреле этого года Минздрав РФ одобрил применение первого российского противоопухолевого препарата Фортека® (МНН – пролголимаб), который предназначен для лечения пациентов с неоперабельной метастатической меланомой. Препарат стал первым российским оригинальным PD-1 ингибитором, представляющим собой моноклональное антитело изотипа IgG1 с Fc-фрагментом, модифицированным методом генной инженерии.
Механизм действия пролголимаба направлен на восстановление способности Т-лимфоцитов распознавать и уничтожать злокачественные клетки, в результате чего иммунная система человека может снова начать бороться с опухолью.
На протяжении десятилетий вера онкологов, да и простых людей, кто косвенно или напрямую коснулся проблемы рака, часто от безысходности сводилась к вере в таинственную силу самой иммунной системы. И вот наступило время, когда эта вера перестала быть слепой. Но для этого мысли человека пришлось пройти огромный путь от самой веры до создания препаратов, способных помочь иммунной системе осуществить наяву это чудо.
— Результаты были представлены компанией BIOCAD в прошлом году. В исследование MIRACULUM было включено 126 пациентов с нерезектабельной метастатической меланомой из России и Белоруссии. Полный или частичный ответ на терапию наблюдался у 48% пациентов с меланомой кожи, которые получали пролголимаб в режиме дозирования 1 мг/кг 1 раз в 2 недели в качестве первой линии терапии. У большинства ответивших на терапию ответ сохранялся на протяжении всего срока наблюдения. 12-месячная выживаемость без прогрессирования в данной группе пациентов составила 44,6%, а общая выживаемость достигла 71,8% Также исследование показало, что новый препарат обладает благоприятным профилем безопасности с низкой частотой отмены терапии из-за нежелательных явлений (3,2%).
— Достаточно высокая эффективность и благоприятный профиль безопасности. Этот метод может помочь больным, для которых химиотерапия и другие методы лечения не были эффективны.
— Разработка и создание новых молекул, клинические исследования и производство оригинального препарата в нашей стране является важным приоритетом. При этом терапия онкологических больных не будет зависеть от курса доллара и ввоза препаратов из-за рубежа. Вывод на рынок российских оригинальных продуктов говорит о том, что отечественные производители, научно-исследовательские институты, биотехнологические компании, как в случае с BIOCAD, способны сделать эту область более конкурентоспособной, а также развивать экспортный потенциал.
Для начала вот чего — в последнее время ко мне стали приходить люди по запросу « куда делся vladlive «. Это весьма лестно, должен вам сказать, т.к. понимаешь что кто-то твоей судьбой интересуется 🙂 .
Сообщаю: я никуда не делся, здоров аки бык, в мае планирую наконец-то посетить Израиль (и киношки будут новые и все остальное прочее).
Теперь к теме поста.
ЭПИГРАФ
Раз я обновляю американские рекомендации по лечению меланомы, которые, по большому счету, интересны только тем, кто лечится и будет лечиться в Израиле, или (допустим, в отношении адъювантной терапии) тем, у кого имеются финансы, то естественно надо и наши рекомендации обновлять, тем более, что в отличии от США, наши тексты имеются в свободном доступе и написаны понятным нам русским языком.
Можно все почитать и ознакомиться. Меня же заинтересовало несколько вопросов:
Единственное что позволю себе указать: наконец-то мы пришли к общемировой практике (ну, по крайней мере в виде рекомендаций) и теперь приступая к лечению меланомы кожи, биопсию сторожевых лимфоузлов рекомендуется делать начиная с толщины 0,75 мм по Бреслоу.
Обнаружил я на неком сайте АОР (Ассоциация онкологов России) проект обновленных рекомендаций Минздрава (когда появятся, то ссылка будет тут: Рекомендации по лечению меланомы. Официоз от Минздрава ). Правда сайт какой-то мутно-недоделаный (может просто в разработке находится по состоянию на 02.04.2018) и ссылаться на него я не буду.
Выглядит это так:
По факту, они не отличаются от рекомендаций 2016, кроме последней сносочки про 2 месяца (собственно по этому я и решил, что это обновление).
И тут возникает два вопроса:
1. Чем должен руководствоваться онколог в работе? Какие рекомендации ему использовать? RUSSCO, Минздрава? Или может еще какие имеются?
В общем, как обычно, все очень сложно, загадочно и непонятно.
*Классификация TNM есть тут (обратите внимание на то, что без проведения БСЛУ даже диагноз точный поставить невозможно): Рекомендации NCCN по лечению меланомы 2018
*Все что сказано про адъювантную терапию просто песня!
*И наконец-то мы видим совершенно здравое и очень своевременное обращение к коллегам по цеху.
Ну и на основе этого выступления можно написать несколько выводов:
Пациентам:
Далее… Пациенты делятся на две категории: на тех, у кого деньги есть и тех, у кого денег нет (это совершенно объективно и никуда от этого не деться). С теми у кого деньги есть все понятно — люди садятся в самолет и посещают маленькую, но гордую страну под названием Израиль, где получают и точную гистологию, и качественную БСЛУ, и назначения на возможную адъювантную терапию , и т.д. и т.п.
А как быть тем, у кого денег нет?
Вот идеальный вариант:
— 27.03.2018. Добрый вечер. Пришла гистология. Врачи говорят все ОК. Дословно: на границе эпидермиса в участках его погружного роста скопление меланоцитов меланоцитов с пигментом. В прилежащей дерме полиморфноклеточная воспалительная инфильтрация. Гистологическая картина не противоречит клиническому диагнозу. Рекомендуется консультация в ООД. Последнее предложение крайне смущает
— В ООД был выполнен пересмотр и подтверждено что все в порядке.
И тут надо понимать одну простейшую вещь: человечество еще не научилось путешествовать во времени и через годик обнаружив на плановой флюорографии затемнение в легком, вы не сможете вернуться обратно (вообще никак).
2. БСЛУ. На сегодняшний день биопсия сторожевых лимфоузлов проводится в Санкт-Петербурге , Обнинске, Челябинске и Екатеринбурге . Процедура бесплатна (по крайней мере должна быть бесплатна, т.к. полис ОМС действует по всей стране). Биопсия сторожевых лимфоузлов обязательна для тех, у кого толщина меланомы превышает 1 мм и обязательно должна обсуждаться с теми, у кого толщина от 0,75/0,8 до 1 мм. Хотя опять же, в рекомендациях Минздрава стоит 1,5 мм 🙂
Будут ли вот такие ошибки ? Ну конечно будут, хотя бы с учетом радиофармпрепарата, НО, это грозит не всем, ну а вовремя обнаруженные микрометастазы, пусть даже не во всех сторожевых лимфоузлах, дадут вам возможность раньше перейти к адъювантной терапии. Т.е выполнять эту процедуру надо в любом случае!
3. Адъювантаная терапия для III стадии. Как выбирать между Опдиво/Кейтрудой (которую тоже скоро зарегистрируют для адъюванта, я уверен) и Тафиналаром с Мекинистом я не знаю (см рекомендации NCCN по ссылке указанной выше). Но то, что при третьей стадии меланомы колоть интерферон практически бесполезно, должен уже понимать каждый пациент.
И тут возникает вопрос: Вот ты тут понаписал всяко, а деньги то где брать? Ведь все равно мы возвращаемся к тому, что все упирается в финансы, ведь кроме интерферона никакой адъювантной терапии, у нас , по состоянию на март 2018, не предусмотрено.
Вот вам два примера :
I
Речь идет не о дорогостоящих препаратах, а о древнейшей химии.
И вот задайтесь вопросом: в какой момент лучше начинать тратить заначки, просить деньги у общественности и т.д.? В превентивном режиме, или когда от этого зависит жизнь и каждый день на счету?
И таких историй вагон и маленькая тележка.
ВРАЧАМ:
Товарищи врачи. Вы , видимо, не совсем понимаете что происходит в стране (или понимаете, но совершенно игнорируете происходящее).
Т.е. вот от таких действий (цитата 01/04/2018. Меланома 4 ст. BRAF V600E имеется):
в ***** в онко мсэ они назначили химиотерапию и вообще о таргетной терапии не разговаривают и не назначают. все сведения нарыли сами в инете. говорят что есть негласный приказ — дорогостой не назначать!
I Как и чем обосновывать вот такое :
II Или вот этот бардак
В общем, пока так. Отправили письма в региональный Минздрав и Росздравнадзор с просьбой разъяснить, на каком основании на второй раз отправляют на ПЭТ, когда уже есть заключение о прогрессировании заболевания из федерального центра. Собираюсь после назначения препаратов покупать их сама (по истечении 10 рабочих дней), потом обращаться в городской суд для возмещения средств.
III Или вот это (немного назад откатимся)
27.02.2017
Здравствуйте. В конце декабря (2016 прим Дядя Вадик)было анонсировано об испытании нового препарата, для лечения злокачественной меланомы ,так же было анонсирование о выпуске этого препарата в 2018 году.Хочется узнать подробно,будет ли этот препарат доступен для больных,которые борются с этим заболеванием.
Мой муж,45 лет, стоит на учете в ***** онкологическом диспансере с 2015 года. Диагноз — узловая пигментная меланома шеи справа. В октябре 2016 года была сделана 3-я операция по удалению метастаз в лимфоузлах. После каждой операции проходил курс химиотерапии. Изучая статьи об этом заболевании, шансы у него небольшие.После анонсирования этого препарата появилась маленькая надежда. Вот только очень хочется узнать, насколько этот препарат будет доступен и когда? Есть такое лекарство зелбораф как нам его можно получить в Твери ничего не говорят подскажите пожалуйста опухоль на шеи опять растёт . Если действительно новый препарат поможет то как нам выжить до следующего года
Ну, во-первых, bcd-100 появился давно (вернее разработан) /vse/nabolelo/importozameshhen.. по этому то, что ляпнула по телеку наша Министр здравоохранения вызывает лишь улыбку (ну и недоумение /vse/nabolelo/pd-1-lekarstvo-b.. )
Вопрос: вам предлагали сдать анализ на БРАФ мутацию? Зелбораф и Тафинлар действуют только при наличии оной.
У нас в **** ничего не предлагают и никуда не направляют добиваться надо самим только бы знать чего и с чего начинать ничего не говорят и орут как будто потерпевшие они, а не пациенты (простите за выражение) к ним боишься подойти чтоб чего-нибудь спросить
С этим то как быть?
Вот пример того, что будет происходить дальше:
Пока писал статью, нашел еще интересную видюшку с прошлого года. Как будто все мои мысли в реальность воплощаются 🙂
Читайте также:


