Признак синдрома опухолевой интоксикации при лейкозах
Виды лейкозов - острые и хронические
Анатомия и физиология костного мозга
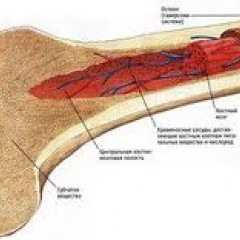
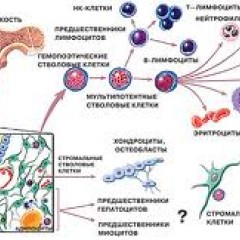
Костный мозг – это ткань находящаяся внутри костей, преимущественно в костях таза. Это самый главный орган, участвующий в процессе кроветворения (рождение новых клеток крови: эритроцитов, лейкоцитов, тромбоцитов). Этот процесс необходим организму, для того чтобы, заменить погибающие клетки крови, новыми. Костный мозг состоит из фиброзной ткани (она образует основу) и кроветворной ткани (клетки крови на разных этапах созревания). Кроветворная ткань включает 3 клеточные линии (эритроцитарный, лейкоцитарный и тромбоцитарный), по которым образуются соответственно 3 группы клеток (эритроциты, лейкоциты и тромбоциты). Общим предком этих клеток, является стволовая клетка, которая запускает процесс кроветворения. Если нарушается процесс образования стволовых клеток или их мутация, то нарушается процесс образования клеток по всем 3 клеточным линиям.
Эритроциты – это красные кровяные клетки, содержат гемоглобин, на нём фиксируется кислород, при помощи которого питаются клетки организма. При недостатке эритроцитов происходит недостаточное насыщение клеток и тканей организма кислородом, в результате чего проявляется различными клиническими симптомами.
Лейкоциты к ним относятся: лимфоциты, моноциты, нейтрофилы, эозинофилы, базофилы. Представляют собой белые клетки крови, они играют роль в защите организма и выработке иммунитета. Их недостаток вызывает снижение иммунитета и развитие различных инфекционных заболеваний.
Тромбоциты – это кровяные пластинки, которые участвуют в образовании тромба. Недостаток тромбоцитов приводит к различным кровотечениям.
Подробнее о видах кровяных клеток читайте в отдельной статье пройдя по ссылке.
Причины лейкоза, факторы риска
Симптомы различных видов лейкозов
- При острых лейкозахотмечаются 4 клинических синдрома:
- Анемический синдром: развивается из-за недостатка выработки эритроцитов, могут присутствовать множество симптомов или некоторые из них. Проявляется в виде усталости, бледности кожи и склер, головокружение, тошнота, быстрое сердцебиение, ломкость ногтей, выпадение волос, патологическое восприятие запаха;
- Геморрагический синдром: развивается в результате недостатка тромбоцитов. Проявляется следующими симптомами: вначале кровотечения из десен, образование синяков, кровоизлияния в слизистые оболочки (язык и другие) или в кожу, в виде мелких точек или пятен. В дальнейшем при прогрессировании лейкоза, развиваются и массивные кровотечения, в результате ДВС синдрома (диссеминированное внутрисосудистое свёртывания крови);
- Синдром инфекционных осложнений с симптомами интоксикации: развивается в результате недостатка лейкоцитов и с последующим снижением иммунитета, повышение температуры тела до 39 0 С, тошнота, рвота, потеря аппетита, резкое снижение веса, головная боль, общая слабость. У больного присоединяются различные инфекции: грипп, пневмония, пиелонефрит, абсцессы, и другие;
- Метастазы - по току крови или лимфы опухолевые клетки попадают в здоровые органы, нарушая их структуру, функции и увеличивая их в размере. В первую очередь метастазы попадают в лимфатические узлы, селезёнку, печень, а потом и в другие органы.
Эритробластный острый лейкоз, поражаются клетки предшественницы, из которых в дальнейшем должны развиться эритроциты. Чаще встречается в пожилом возрасте, характеризуется выраженным анемическим синдромом, не наблюдается увеличение селезёнки, лимфатических узлов. В периферической крови снижено количество эритроцитов, лейкоцитов и тромбоцитов, наличие молодых клеток (эритробластов).
Монобластный острый лейкоз, нарушается выработка лимфоцитов и моноцитов, соответственно они будут снижены в периферической крови. Клинически, проявляется, повышением температуры и присоединением различных инфекций.
Мегакариобластный острый лейкоз, нарушается выработка тромбоцитов. В костном мозге при электронной микроскопии обнаруживают мегакариобласты (молодые клетки, из которых образуются тромбоциты) и увеличенное содержание тромбоцитов. Редкий вариант, но чаще встречается в детском возрасте и обладает неблагоприятным прогнозом.
Хронический миелолейкоз, усиленное образование миелоидных клеток, из которых образуются лейкоциты (нейтрофилы, эозинофилы, базофилы), в результате чего, уровень этих групп клеток будет повышен. Долгое время может протекать бессимптомно. Позже появляются симптомы интоксикации (повышение температуры, общая слабость, головокружение, тошнота), и присоединение симптомов анемии, увеличение селезёнки и печени.
Хронический лимфолейкоз, усиленное образование клеток - предшественниц лимфоцитов, в результате уровень лимфоцитов в крови повышается. Такие лимфоциты не могут выполнять свою функцию (выработка иммунитета), поэтому у больных присоединяются различные виды инфекций, с симптомами интоксикации.
Диагностика лейкоза
- Повышение уровня лактатдегидрогеназы (норма 250 Ед/л);
- Высокий АСАТ (норма до 39 Ед/л);
- Высокая мочевина (норма 7,5 ммоль/л);
- Повышение мочевой кислоты (норма до 400 мкмоль/л);
- Повышение билирубина ˃20мкмоль/л;
- Снижение фибриногена 30%;
- Низкий уровень эритроцитов, лейкоцитов, тромбоцитов.
- Трепанобиопсия (гистологическое исследование биоптата из повздошной кости): не позволяет точно поставить диагноз, а лишь определяет разрастание опухолевых клеток, с вытеснением нормальных клеток.
- Цитохимическое исследование пунктата костного мозга: выявляет специфические ферменты бластов (реакция на пероксидазу, липиды, гликоген, неспецифическую эстеразу), определяет вариант острого лейкоза.
- Иммунологический метод исследования: выявляет специфические поверхностные антигены на клетках, определяет вариант острого лейкоза.
- УЗИ внутренних органов: неспецифический метод, выявляет увеличенные печень, селезёнку и другие внутренние органы с метастазами опухолевых клеток.
- Рентген грудной клетки: является, неспецифическим метом, обнаруживает наличие воспаления в лёгких при присоединении инфекции и увеличенные лимфатические узлы.
Лечение лейкозов
- Полихимиотерапия, применяется с целью противоопухолевого действия:
- Трансфузионная терапия: эритроцитарная масса, тромбоцитарная масса, изотонические растворы, с целью коррекции выраженного анемического синдрома, геморагического синдрома и дезинтоксикации;
- Общеукрепляющая терапия:
- применяется с целью укрепления иммунитета. Дуовит по 1 таблетке 1 раз в день.
- Препараты железа, для коррекции недостатка железа. Сорбифер по 1 таблетке 2 раза в день.
- Иммуномодуляторы повышают реактивность организма. Тималин, внутримышечно по 10-20 мг 1 раз в день, 5 дней, Т-активин, внутримышечно по 100 мкг 1 раз в день, 5 дней;
- Гормонотерапия: Преднизолон в дозе по 50 г в день.
- Антибиотики широкого спектра действия назначаются для лечения присоединяющих инфекций. Имипенем по 1-2 г в сутки.
- Радиотерапия применяется для лечения хронического лейкоза. Облучение увеличенной селезёнки, лимфатических узлов.
Использование солевых повязок с 10% солевым раствором (100 г соли на 1 литр воды). Намочить льняную ткань в горячем растворе, ткань немного сжимать, сложить в четверо, и накладывать на больное место или опухоль, закрепить лейкопластырем.
Настой из измельчённых игл сосны, сухая кожа лука, плоды шиповника, все ингредиенты смешать, залить водой, и довести до кипения. Настоять сутки, процедить и пить вместо воды.
Употреблять соки из красной свеклы, граната, моркови. Кушать тыкву.
Настой из цветков каштана: взять 1 столовую ложку цветков каштана, залить в них 200 г воды, вскипятить и оставить настаиваться на несколько часов. Пить по одному глотку на один приём, необходимо выпить 1 литр в день.
Хорошо помогает в укреплении организма, отвар из листьев и плодов черники. Кипятком примерно 1 литр, залить 5 ложек листьев и плодов черники, настоять несколько часов, выпивать всё за один день, принимать около 3 месяцев.
Опухолевая интоксикация констатирует отравление организма продуктами жизнедеятельности злокачественной опухоли. Патологическое состояние не удостоилось отдельного места в классификациях, но его не минует ни один пациент с генерализованным процессом, эпизоды возможны и во время лекарственного лечения.
Причины опухолевой интоксикации
Главная причина — наличие клеток, выделяющих биологически активные вещества. Некоторые новообразования вырабатывают вредные субстанции, но после удаления первичной опухоли все признаки отравления бесследно исчезают. Такого рода интоксикация возникает ещё до обнаружения опухоли, так бывает при аденокарциноме легкого, когда вырабатываемые клетками вещества вызывают боли в суставах, при злокачественных лимфомах токсины инициируют слабость с потливостью и высокой температурой.
Интенсивность проявлений зависит от биологических особенностей клеток и их общей массы, при прогрессировании с увеличением объема опухоли усиливаются и симптомы хронического отравления. Особенно выраженные признаки наблюдаются при распаде опухоли, аналогичное по проявлениям, но гораздо более тяжелое состояние может развиться при массированной гибели злокачественных клеток в результате химиотерапии. При лечении высокочувствительных к цитостатикам новообразований лимфатической ткани и крови проводится профилактика синдрома лизиса опухоли.
Симптомы интоксикации характерны для множественных метастазов в костях, когда к токсичным клеточным продуктам присоединяется негативное действие выходящего из распадающейся костной ткани кальция — гиперкальциемия.
Симптомы опухолевой интоксикации
Интоксикация — это отравление, но не острое, а хроническое, то есть признаки его нарастают постепенно. Исключение составляет только синдром лизиса опухоли во время химиотерапии, когда клинические проявления нарастают стремительно вплоть до острой почечной недостаточности.
Типичны для интоксикации слабость и быстрая утомляемость, доводящие пациента до постоянного пребывания в постели. Возможно повышение температуры — от субфебрилитета при генерализованном процессе до 40°С при распаде крупного опухолевого конгломерата с образованием некротической полости диаметром в несколько сантиметров.
У всех пациентов изменяется цвет кожи — от бледного до землистого, всё индивидуально, но заметно окружающим. Присоединяется небольшая отечность поверхностных тканей — пастозность, повышается потливость, особенно ночная.
Продукты ракового метаболизма циркулируют в крови, оседая в органах и нарушая их функционирование. Повреждение сердечно-сосудистой системы проявляется изменением ритма сердца и учащением дыхания, нервной системы — депрессией с дневной сонливостью при нарушениях ночного сна. Почечные канальцы забиваются продуктами метаболизма, снижая выделительную функцию.
Частично токсичные продукты выводятся слизистой оболочкой желудочно-кишечного тракта, что приводит к её сухости и, как следствие, нарушению аппетита. Печень активно борется с токсинами, но и она перестает справляться, изменяя содержание в плазме микроэлементов и вязкость крови. При тяжелой опухолевой интоксикации постоянная тошнота сменяется не приносящей облегчения рвотой.
Диагностика и лечение опухолевой интоксикации
В первую очередь об интоксикационном синдроме свидетельствует совокупность жалоб пациента и его внешний вид, начиная с нездоровой окраски кожи.
В общем анализе крови интоксикацию заметить непросто, но в биохимическом может повыситься концентрация печеночных трансаминаз, креатинина, мочевой кислоты, калия и фосфатов.
Стимуляция аппетита заключается не только в приеме противорвотных и даче стимуляторов аппетита, необходима тщательная коррекция микроэлементов и макронутриентов — белков, жиров и углеводов. Недостаточно вызвать аппетит, надо предоставить питание, не усугубляющее опухолевую интоксикацию и помогающее восстановлению.
Длительность и интенсивность медикаментозной терапии зависит от степени выраженности интоксикации. В тяжелых случаях может потребоваться гемосорбция — очищение крови специальной аппаратной системой, или только очищение плазмы при плазмаферезе.
Адекватная терапия опухолевой интоксикации не только улучшит состояние пациента, но и увеличит продолжительность его жизни, сделав её качественней и спокойнее.
Не всегда при злокачественном заболевании возможно остановить протекание болезни, но необходимо стремиться сделать жизнь онкобольного достойной. В нашей клинике помогают всем онкологическим пациентам и в любой период развития опухоли.
Сущность синдрома: интоксикация организма резорбированными продуктами распада клеток.
Клинические проявления:
- лихорадка – частый признак лейкоза, развивается вследствие пирогенного действия продуктов распада форменных элементов крови. Субфебрильная лихорадка наблюдается при миелолейкозе, лимфолейкозе, волнообразное повышение температуры до 38 0 С характерно для лимфогранулематоза
- слабость, утомляемость, потливость, прогрессирующее снижение веса обусловлены постепенно нарастающей интоксикацией, вызванной большим распадом в организме лейкозных клеток.
Лабораторные методы исследования:
- увеличение СОЭ, диспротеинемия.
Синдром иммунной недостаточности
Сущность синдрома: нарушение одного или нескольких звеньев иммунной защиты организма.
Основные причины развития синдрома:
1)снижение количества или угнетение функции Т - лимфоцитов (синдром недостаточности клеточного иммунитета);
2)снижение количества или угнетения функции В - лимфоцитов (синдром недостаточности антител, гипоиммуноглобулинэмия);
3)сочетание 1-2 : комбинированный иммунодефицитный синдром;
5)нарушение системы комплемента.
Синдром иммунной недостаточности может быть обусловлен первичным иммунодефицитом в результате нарушения практически любой стадии дифференцировки клеток иммунной системы. Вторичный иммунодефицит может развиваться и как следствие недостаточности питания, лимфопролиферативных заболеваний, вирусных инфекций, рентгеновского облучения, воздействия цитотоксических лекарственных препаратов.
Иммунная недостаточность – это одно из самых частых последствий злокачественного роста лимфоидной ткани.
Основные клинико-лабораторные симптомы:
язвенно-некротическая ангина характеризуется кратерообразным изъязвлением миндалин, покрыты грязно-зеленым некротическим налетом, при этом отмечается боль при глотании, гнилостный запах изо рта, увеличение подчелюстных лимфоузлов. Некроз может быть по дужкам мягкого неба, язычку. При бактериоскопическом исследовании налета обнаруживается в большом количестве фузоспириллезная флора.
недостаточность системы комплемента, фагоцитов или В – клеток приводит к бактериальным инфекциям.
недостаточность Т – клеток обусловливает повышенную чувствительность организма к вирусам и грибам.
лимфопролиферативные заболевания, такие как хронический лимфолейкоз, миеломная болезнь, сопровождаются различной степени гипогаммаглобулинемией и нарушением реакций гуморального иммунитета. Указанные заболевания осложняются гнойными инфекциями, особенно стафилококковой этиологии (чаще это заболевания дыхательной системы и мочеполовых путей).
при развитии лимфогранулематоза имеет место недостаточность клеточного иммунитета и вследствие этого чувствительность к туберкулезным микобактериям, вирусам опоясывающего лишая и др.
снижение в крови содержания лимфоцитов.
снижение фагоцитарной активности лейкоцитов крови.
снижение числа Т- и В-лимфоцитов.
снижение в крови содержания иммуноглобулинов.
Острый лейкоз – опухолевое поражение кроветворной системы, морфологической основой которого выступают незрелые (бластные) клетки, вытесняющие нормальные гемопоэтические ростки. Клиническая симптоматика острого лейкоза представлена прогрессирующей слабостью, немотивированным подъемом температуры, артралгиями и оссалгиями, кровотечениями различных локализаций, лимфаденопатией, гепатоспленомегалией, гингивитами, стоматитами, ангинами. Для подтверждения диагноза необходимо исследование гемограммы, пунктата костного мозга, биоптата подвздошной кости и лимфоузлов. Основу лечения острых лейкозов составляют химиотерапевтические курсы и сопроводительная терапия.


- Причины острого лейкоза
- Классификация острого лейкоза
- Симптомы острого лейкоза
- Диагностика острого лейкоза
- Лечение острого лейкоза
- Цены на лечение
Общие сведения
Причины острого лейкоза
Первопричиной острого лейкоза является мутация гемопоэтической клетки, дающей начало опухолевому клону. Мутация кроветворной клетки приводит к нарушению ее дифференцировки на ранней стадии незрелых (бластных) форм с дальнейшей пролиферацией последних. Образующиеся опухолевые клетки замещают нормальные ростки гемопоэза в костном мозге, а в дальнейшем выходят в кровь и разносятся в различные ткани и органы, вызывая их лейкемическую инфильтрацию. Все бластные клетки несут в себе одинаковые морфологические и цитохимические признаки, что свидетельствует в пользу их клонального происхождения от одной клетки-родоначальницы.
Причины, запускающие мутационный процесс, не известны. В гематологии принято говорить о факторах риска, повышающих вероятность развития острого лейкоза. В первую очередь, это генетическая предрасположенность: наличие в семье больных с острым лейкозом практически утраивает риск заболевания у близких родственников. Риск возникновения острого лейкоза повышается при некоторых хромосомных аномалиях и генетических патологиях - болезни Дауна, синдроме Клайнфельтера, Вискотта-Олдрича и Луи-Барра, анемии Фанкони и др.
Вероятно, что активация генетической предрасположенности происходит под действием различных экзогенных факторов. В числе последних могут выступать ионизирующая радиация, химические канцерогены (бензол, мышьяк, толуол и др.), цитостатические препараты, используемые в онкологии. Нередко острый лейкоз становится следствием противоопухолевой терапии других гемобластозов – лимфогранулематоза, неходжкинских лимфом, миеломной болезни. Подмечена связь острых лейкозов с предшествующими вирусными инфекциями, угнетающими иммунную систему; сопутствующими гематологическими заболеваниями (некоторыми формами анемий, миелодисплазиями, пароксизмальной ночной гемоглобинурией и др.).
Классификация острого лейкоза
В онкогематологии общепринята международная FAB-классификация острых лейкозов, дифференцирующая различные формы заболевания в зависимости от морфологии опухолевых клеток на лимфобластные (вызываемые низкодифференцированными предшественниками лимфоцитов) и нелимфобластные (объединяющие остальные формы).
1. Острые лимфобластные лейкозы взрослых и детей:
- пре-В-форма
- В-форма
- пре-Т-форма
- Т-форма
- ни Т ни В-форма
2. Острые нелимфобластные (миелоидные) лейкозы:
- о. миелобластный (вызван неконтрорлируемой пролиферацией предшественников гранулоцитов)
- о. моно- и о. миеломонобластный (характеризуются усиленным размножением монобластов)
- о. мегакариобластный (связан с преобладанием недифференцированных мегакариоцитов – предшественников тромбоцитов)
- о. эритробластный (обусловлен пролиферацией эритробластов)
3. Острый недифференцированный лейкоз.
Течение острых лейкозов проходит ряд стадий:

Симптомы острого лейкоза
В развернутом периоде острого лейкоза развиваются анемический, геморрагический, интоксикационный и гиперпластический синдромы.
Анемические проявления обусловлены нарушением синтеза эритроцитов, с одной стороны, и повышенной кровоточивостью – с другой. Они включают бледность кожных покровов и слизистых, постоянную усталость, головокружение, сердцебиение, повышенное выпадение волос и ломкость ногтей и др. Усиливается выраженность опухолевой интоксикации. В условиях абсолютной лейкопении и упадка иммунитета легко присоединяются различные инфекции: пневмонии, кандидоз, пиелонефрит и т. д.
В основе геморрагического синдрома лежит выраженная тромбоцитопения. Диапазон геморрагических проявлений колеблется от мелких единичных петехий и синяков до гематурии, десневых, носовых, маточных, желудочно-кишечных кровотечений и пр. По мере прогрессирования острого лейкоза кровотечения могут становиться все массивнее вследствие развития ДВС-синдрома.
Гиперпластический синдром связан с лейкемической инфильтрацией как костного мозга, так и других органов. У больных острым лейкозом наблюдается увеличение лимфоузлов (периферических, медиастинальных, внутрибрюшных), гипертрофия миндалин, гепатоспленомегалия. Могут возникать лейкозные инфильтраты кожи (лейкемиды), оболочек мозга (нейролейкоз), поражение легких, миокарда, почек, яичников, яичек и др. органов.
Полная клинико-гематологическая ремиссия характеризуется отсутствием внекостномозговых лейкемических очагов и содержанием бластов в миелограмме менее 5% (неполная ремиссия – менее 20%). Отсутствие клинико-гематологических проявлений в течение 5 лет расценивается как выздоровление. В случае увеличения бластных клеток в костном мозге более 20%, их появления в периферической крови, а также выявления внекостномозговых метастатических очагов диагностируется рецидив острого лейкоза.
Терминальная стадия острого лейкоза констатируется при неэффективности химиотерапевтического лечения и невозможности достижения клинико-гематологической ремиссии. Признаками данной стадии служат прогрессирование опухолевого роста, развитие несовместимых с жизнью нарушений функции внутренних органов. К описанным клиническим проявлениям присоединяются гемолитическая анемия, повторные пневмонии, пиодермии, абсцессы и флегмоны мягких тканей, сепсис, прогрессирующая интоксикация. Причиной смерти больных становятся некупируемые кровотечения, кровоизлияния в мозг, инфекционно-септические осложнения.
Диагностика острого лейкоза
С целью подтверждения и идентификации разновидности острого лейкоза выполняется стернальная пункция с морфологическим, цитохимическим и иммунофенотипическим исследованием костного мозга. При исследовании миелограммы обращает внимание увеличение процента бластных клеток (от 5% и выше), лимфоцитоз, угнетение красного ростка кроветворения (кроме случаев о. эритромиелоза) и абсолютное снижение или отсутствие мегакариоцитов (кроме случаев о. мегакариобластного лейкоза). Цитохимические маркерные реакции и иммунофенотипирование бластных клеток позволяют точно установить форму острого лейкоза. При неоднозначности трактовки анализа костного мозга прибегают к проведению трепанобиопсии.
С целью исключения лейкемической инфильтрации внутренних органов производится спинномозговая пункция с исследованием ликвора, рентгенография черепа и органов грудной клетки, УЗИ лимфатических узлов, печени и селезенки. Кроме гематолога, больные острым лейкозом должны быть осмотрены неврологом, офтальмологом, отоларингологом, стоматологом. Для оценки тяжести системных нарушений может потребоваться исследование коагулограммы, биохимического анализа крови, проведение электрокардиографии, ЭхоКГ и др.
Дифференциально-диагностические мероприятия направлены на исключение ВИЧ-инфекции, инфекционного мононуклеоза, цитомегаловирусной инфекции, коллагенозов, тромбоцитопенической пурпуры, агранулоцитоза; панцитопении при апластической анемии, В12 и фолиеводефицитной анемии; лейкемоидных реакций при коклюше, туберкулезе, сепсисе и др. заболеваниях.

Лечение острого лейкоза
Пациентов с острым лейкозом лечат в стационарах онкогематологического профиля. В палатах организуется усиленный санитарно-дезинфекционный режим. Больные с острым лейкозом нуждаются в проведении гигиенической обработки полости рта, профилактики пролежней, туалета половых органов после физиологических отправлений; организации высококалорийного и витаминизированного питания.
Непосредственно лечение острых лейкозов проводится последовательно; основные этапы терапии включают достижение (индукцию) ремиссии, ее закрепление (консолидацию) и поддержание, профилактику осложнений. Для этого разработаны и используются стандартизированные схемы полихимиотерапии, которые подбираются гематологом с учетом морфологической и цитохимической формы острого лейкоза.
При благоприятной ситуации ремиссия обычно достигается в течение 4-6 недель усиленной терапии. Затем, в рамках консолидации ремиссии проводится еще 2-3 курса полихимиотерапии. Поддерживающая противорецидивная терапия осуществляется еще в течение не менее 3-х лет. Наряду с химиотерапией при остром лейкозе необходимо проведение сопроводительного лечения, направленного на предупреждение агранулоцитоза, тромбоцитопении, ДВС-синдрома, инфекционных осложнений, нейролейкемии (антибиотикотерапия, переливание эритроцитарной, тромбоцитарной массы и свежезамороженной плазмы, эндолюмбальное введение цитостатиков). При лейкемической инфильтрации глотки, средостения, яичек и др. органов проводится рентгенотерапия очагов поражения.
В случае успешного лечения достигается уничтожение клона лейкозных клеток, нормализация кроветворения, что способствует индукции длительного безрецидивного периода и выздоровления. Для предупреждения рецидивов острого лейкоза может быть проведена трансплантация костного мозга после предварительного кондиционирования путем химиотерапии и тотального облучения.
По имеющимся статистическим сведениям, использование современных цитостатических средств приводит к переходу острого лейкоза в фазу ремиссии у 60-80% больных; из них у 20-30% удается добиться полного выздоровления. В целом прогноз при острых лимфобластных лейкозах более благоприятен, чем при миелобластных.
Лейкемоидная реакция.
Лимфоцитоз
Абсолютный:характерно повышение числа лимфоцитов в единице объема крови в результате увеличения процентного содержания лимфоцитов при нормальном или повышенном содержании лейкоцитов в единице объема.
3 фазы лейкоцитоза при инфекционных заболеваниях, туберкулеза, сифилиса, эндокринных заболеваний (Базедова болезнь), коклюша, лейшманиоза, лимфогранулематоза, лепры.
Относительный: преобладание лимфоцитов в единице объема крови за счет снижения содержания других форм лейкоцитов. Наблюдается при снижении общего количества лейкоцитов или повышения процентного содержания лимфоцитов. Характерен для: брюшного тифа, кори, гриппа.
Лейкоцитоз возникает как реакция системы крови на особые тяжелые воздействия, картина крови напоминает лейкоз. В зависимости от характера клеток бывают:
- миелоидные (токсогенная зернистость, увеличение НФ до 40*10 9 /л, гиперрегенеративный сдвиг влево),
- моноцитарные,
- лимфоцитарно-моноцитарные,
- эозинофильные.
Отличия от лейкозов:
- Возникают как симптом (без неоплазии костного мозга).
- Лейкемоидная реакция исчезает при успешном лечении заболевания, её вызвавшего.
- При лейкемоидной реакции нет неопластических изменений костного мозга.
Механизмы развития лейкоцитозов:
- Клеточные механизмы регуляции лейкопоэза.
- Гуморальные.
- Гормональные.
- Нервно-рефлекторные.
Результатом является: стимуляция лейкопоэза (увеличение выработки лейкоцитов), ускорение их выхода из костного мозга.
При инфекционных заболеваниях развитие лейкоцитоза проходит в 3 фазы:
- НФ лейкоцитоз (начало заболевания, клеточные и гуморальные механизмы→гормональные).
- Моноцитарный лейкоцитоз (разгар).
- Лимфоцитарный лейкоцитоз (выздоровление).
Свойства стволовой клетки:
- способность к самоподдержанию пула:
первая дочерняя СК становится СК, вторая дочерняя СК уходит в дифференцировку,
- полипотентность - способность дифф-ки в различные ряды.
Механизмы развития лейкопений:
- Нарушение образования лейкоцитов (радиация, интоксикация, аутоиммунные процессы).
- Нарушение выхода лейкоцитов в периферическую кровь.
- Быстрое разрушение лейкоцитов.
- Перераспределение лейкоцитов в сосудистом русле.
Лейкоз – системное опухолевое заболевание кроветворной ткани, характеризующееся бесконтрольной пролиферацией клеток и нарушением их дифференцировки.
Этиология:
- Вирусная теория (выделены онковирусы, вирус гепатита В – рак печени.)
- Теория химических канцерогенов (экзогенные химические канцерогены – гл.14 Зайко, эндогенные химические канцерогены образуются в ходе обмена в-в – холестерина и его производных, триптофана, эстрогенов).
Общие свойства канцерогенов:
- способность проникать через мембраны клеток,
- способность влиять на геном,
- дозированность эффектов,
- органотропность,
- синканцерогенез – способность канцерогенов усиливать действие друг друга.
- Теория физического воздействия – действие радиации.
Условия превращения нормальных клеток в опухолевые:
- Наследственная предрасположенность.
- Конституция человека.
- Особенности питания (мало молока, много пищи содержащей холестерин и жирные кислоты).
- Гиповитаминоз (А, Е, С).
- Возрастные особенности нервной, эндокринной, и кроветворной систем.
Патогенез опухолевого роста:
Основное звено – образование мутантной клетки.
Сначала она латентная, затем превращается в опухолевую.
Механизмы превращения:
- Геномный (мутация)
- Эпигеномный (нарушение регуляции геномов, в результате чего происходит репрессирование генов, регулирующих клеточное размножение).
Развитие лейкозов характеризуются стадийностью:
- Стадия трансформации (инициации) – образование мутантной клетки носит обратимый характер.
- Стадия активации (промоции) – из мутантной клетки образуется опухолевая клетка.
- Стадия опухолевой прогрессии.
Ведущие факторы патогенеза:
- Неэффективность иммунного надзора.
- Нарушение регуляции и саморегуляции клетки.
При лейкозах изменения происходят на следующих уровнях:
- молекулярном,
- клеточном,
- тканевом,
- органном,
- системном,
- организменном.
В результате нарушения саморегуляции формируются основные свойства опухолевой клетки: изменение белкового синтеза (антигенного и рецепторного аппарата), активация гликолиза и перекисного окисления (образуются свободные радикалы и она становится вооруженной по отношению к другим клеткам), способность бесконтрольной пролиферации и автономность, образование клеткой токсичных веществ, способность к метастазированию, способность с помощью ферментов раздвигать соседние ткани и осуществлять инфильтративный рост.
Признаки опухолевой прогрессии при лейкозах:
- Утрата ферментативной специфичности.
- Морфологические и структурные изменения в клетках (нарушение соотношения ядра и протоплазмы в сторону увеличения ядра).
- Способность клеток выходить за пределы кроветворного аппарата и размножаться в различных органах и тканях (вытеснение опухолевым ростком других ростков кроветворения).
- Увеличение числа клеток в крови (развитие лейкоцитоза и гиперлейкоцитоза, если увеличено количество бластных клеток – бластный криз).
- Постепенный или скачкообразный выход клеток из под контроля цитостатиков.
Гематологические изменения со стороны белой крови и других ростков:
- Анемия
- Тромбоцитопения
- Резкое ↑ СОЭ
- Геморрагический синдром
- Лихорадка
- Нарушение функции ЖКТ, печени, селезенки вследствие их лейкозного поражения.
Классификация лейкозов:
- В зависимости от степени дифференцировки клеток и скорости течения:
ii.хронические
- По характеру пораженного ростка:
- По количеству клеток в крови:
i. лейкемические (выше 50*10 9 /л)
ii. сублейкемические (10-50*10 9 /л)
iii. алейкемические (норма или до 10*10 9 /л)
iv. лейкопенические (меньше 4*10 9 /л )
Механизмы развития анемии при лейкозах:
- Вытеснение эритроидного ростка опухолевым.
- Угнетение эритропоэза токсинами лейкоз.клеток.
- Нарушение всасывания витамина В12 и железа в результате повреждения ЖКТ лейкозными инфильтратами, уменьшение секреции желудочного сока → дисэритропоэтическая анемия.
- Снижение РОЭ (снижение устойчивости эритроцита к гемолизу) → гемолитическая анемия.
- Кровотечения в результате геморрагического синдрома → постгеморрагическая анемия.
По патогенезу анемии при лейкозах смешанные!
(постгеморрагическая, гемолитическая, дисэритропоэтическая).
Механизмы развития геморрагического синдрома анемии при лейкозах:
- Вытеснение мегакариоцитарного ростка опухолевым.
- Токсическое повреждение его опухолевыми клетками.
- Токсические васкулиты.
- Инфильтративные васкулиты (лейкозная инфильтрация сосудистой стенки).
- Коагулопатия потребления из-за увеличения расхода прокоагулянтов в результате ДВС-синдрома.
- Нарушение синтеза факторов свертывания крови в печени в результате её лейкозного поражения.
Картина крови при отдельных видах лейкоза:
- Острый миелолейкоз:
- Лейкоцитоз с наличием миелобластов.
- Наличие лейкемического провала (отсутствие промежуточных форм клеток между зрелыми клетками и бластами).
- Базофильно-эозинофильная диссоциация – 0-БФ, ↑-ЭФ.
- Хронический миелолейкоз:
- Лейкоцитоз (без миелобластов, без терминальных стадий).
- Отсутствие лейкемического провала.
- БФ-ЭФ ассоциация – ↑-БФ, ↑-ЭФ.
- Хронический лимфолейкоз:
- Лейкоцитоз лимфоцитарный.
Качественные изменения клеток: наличие в мазке клеток Боткина-Гумпрехта, веретенообразных и голоядерных лимфоцитов.
- Острый лимфолейкоз
Лейкоцитоз с наличием лимфобластов (клетки средних размеров, ядро округлой формы, занимает большую часть цитоплазмы, зернистости нет).
Принципы лечения лейкозов:
Факторы риска в развитии лейкозов:
Лейкопении, лейкоцитозы непонятной этиологии.
Радиационное воздействие (внутриутробный период).
Различные вирусные заболевания.
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Читайте также:

