При раке мочевого пузыря пэт-кт
Медицина и наука
- НА ГЛАВНУЮ
- КАРТОГРАФ
- КОНТАКТЫ
- ВНУТРЕННИЕ БОЛЕЗНИ

- Мера здоровья и счастья
- Тысяча движений
- Нежелательные минералы
- Правда об аборте
- Бронхиальная астма у детей
- Глисты
- Грибковые заболевания
- Медицина и наука
ПЭТ имеет ограниченное значение при раке мочевого пузыря. Исторически стадирование рака мочевого пузыря при помощи имеющихся методов диагностики также ограничено. При КТ можно диагностировать только значительное распространение опухоли за пределы мочевого пузыря с точностью 64-92%. Кроме того, точность диагностики лимфатических узлов составляет 70-90%, при этом частота ложно-отрицательных результатов составляет 40%. Подобным образом МРТ малоинформативно в установлении стадии рака - точность диагностики составляет 60-75%. А ложно-отрицательные результаты в оценке состояния лимфатических узлов еще выше, чем при КТ. Оба метода (КТ и МРТ) часто завышают стадию рака, т.к. анатомические изменения не соответствуют опухолевым. В последнее время начали изучать возможности ПЭТ в диагностики и стадировании рака мочевого пузыря.
В связи со значительным выделением ФДГ через мочевые пути диагностика рака мочевого пузыря и прилежащих лимфатических узлов затруднена. Тем не менее, при помощи ПЭТ возможно определить местное и отдаленное метастазирование рака мочевого пузыря с определенной долей точности. В исследовании Kosuda et al. использовали ПЭТ у 12 больных с гистологически доказанным раком мочевого пузыря, которым выполнили оперативное лечение и/или ЛТ по поводу местного рецидива. Точная диагностика была в 66,7% случаев, ложно-отрицательные результаты в 33,3% случаев. В 100% случаев диагностированы отдаленные метастазы (в легкие, кости, отдаленные лимфатические узлы) и в 66,7% (2/3) случаев при поражении тазовых лимфатических узлов. В другом исследовании также в 66,7% случаев диагностировали метастаза в л/узлы. Рецидивные местные или остаточные опухоли не так хорошо диагностировались (60%), т.к. радиопрепарат накапливался в мочевом пузыре, несмотря на ирригацию или дренирование последнего катетером Фолея. Тем не менее, при помощи ПЭТ выявляли экстравезикальное распространение опухоли у некоторых больных. В одном случае - при наличии инвазии в сигмовидную кишку, которое не смогла выявить КТ. При помощи ПЭТ у двух больных удалось дифференцировать рецидивную опухоль от изменений, вызванных ЛТ/ХТ в мочевом пузыре.
Другие исследователи пытались улучшить чувствительность ПЭТ, используя другой радиоизотоп. Например, (Ahlstrom et al), сравнивая ФДГ и С-methionine (который не выделяется с мочой), чувствительность последнего была выше. Тем не менее, чувствительность диагностики составила всего 78% (18/23) при использовании этого метода. В данном исследовании также было определено, что накопление радиоизотопа прямо пропорционально стадии рака.
Таким образом, при РМП ПЭТ имеет ограниченное применение в связи с артефактами радиоизотопа. Имея низкую чувствительность для диагностики первичной, высоко-дифференцированной опухоли мочевого пузыря, ПЭТ можно использовать (в сочетании с традиционными методами) для диагностики местно-распространенных стадий. Кроме того, ПЭТ полезен для выявления метастазов в л/узлах и отдаленных метастазов, а также для дифдиагноза между рецидивом и изменениями тканей после ЛТ.
Узнайте больше .
Роль иммунопатологий в развитии вирусных заболеваний у детей и взрослых
В современной медицине под названием вирусы понимаются мельчайшие неклеточные частицы, являющиеся внутриклеточными паразитами. Размножаясь только в живых клетках, вирус встраивается в клетку, изменяет ее генетический аппарат и, используя ее ферментативный аппарат, переключает клетку на синтез своих зрелых вирусных частиц - вирионов, которые в свою очередь лавинообр .
70-летний мужчина с прошлой историей гемикоэктомии из-за рака толстой кишки подвергся последующей компьютерной томографии брюшной / тазовой области. КТ выявил правильный метастаз надпочечников, а затем он прошел исследование ФДГ-ПЭТ / КТ для поиска другого возможного рецидива опухоли. В ПЭТ-изображениях, кроме правого надпочечников, наблюдалось неожиданное интенсивное поглощение ФДГ в правой паховой области, и сначала он считался паховым метастазом. Однако корреляция изображений ПЭТ с одновременными данными КТ показала, что это грыжа мочевого пузыря. Этот случай является примером того, что анализ изображений ПЭТ без соответствующих изображений КТ может привести к недостаточной интерпретации или ложноположительному диагнозу. Следовательно, радиологи должны знать о важности совместного анализа данных ПЭТ и КТ при интерпретации интегрированных ПЭТ / КТ и редких, но интригующих условиях, таких как грыжа мочевого пузыря, во время оценки ПЭТ-сканирования у больных раком толстой кишки.
Флуороксиглюкоза-позитронно-эмиссионная томография фтордезоксиглюкозы (ФДГ-ПЭТ) играет важную роль в выявлении и оценке рецидивирующего колоректального рака.1,2 FDG-PET обладает общей чувствительностью обнаружения более 90%, но специфичность может быть только приблизительно 70 % .2,3 Существует несколько распространенных причин ложноположительных диагнозов, связанных с ФДГ-ПЭТ, а именно нормальное физиологическое поглощение желудочно-кишечного тракта или мочеполового тракта и доброкачественных инфекционных или воспалительных поражений.2,4 Чтобы избежать ложноположительных диагнозов, часто необходима тщательная корреляция с анатомией от КТ-анализа. Текущая система ПЭТ / КТ продемонстрировала улучшение точности диагностики рецидивирующего рака толстой кишки по сравнению с изображениями ПЭТ. [4] В этом отчете мы представляем случай паховой грыжи мочевого пузыря, который был правильно диагностирован путем комбинированного обзора ПЭТ / КТ, но первоначально смоделированный узловой рецидив во время первой изолированной интерпретации ПЭТ.
70-летний мужчина с историей расширенной правой гемикоэктомии из-за аденокарциномы восходящей ободочной кишки оценивался каждые 6 месяцев для оценки рецидива опухоли. На 12-месячном контрольном осмотре брюшной / тазовой КТ выявили новую твердую массу, возникающую из правой надпочечниковой железы, которая появилась как метастаз надпочечников, и пациент проходил исследования ФДГ ПЭТ / КТ, чтобы обнаружить любые другие рецидивирующие поражения.
Исследования ПЭТ / КТ проводились с использованием сканера GEMINI Dual PET-CT (медицинские системы Philips). Двойной сканер GEMINI представляет собой открытую систему PET-CT, которая сочетает в себе винтовой двухслойный CT с 3D-сканером PET, оснащенным собственным источником передачи. Пациентов сканируют через 1 час после инъекции 0,14 мКи / кг ФДГ. Сначала сканирование эмиссии ПЭТ получают без КТ с низкой дозой. Сканирование эмиссии состоит из 9 положений кровати по 2 минуты 30 секунд каждый, охватывающих 85,2 см, а затем сканирования Cs-137. Высокая активность источника Cs-137 (10 мКи с периодом полураспада 30 лет) и обнаружение одного события позволяет быстро сканировать передачу. Общая продолжительность сканирования передачи Cs-137 составляет приблизительно 1 минуту (длина сканирования 100 см). Проведено диагностическое высокоточное КТ-сканирование (поле сканирования 500 мм, приращение 3 мм, толщина среза 3,0 мм, шаг 1,5 секунды на оборот, матрица 512 × 512, 120 КВ, 450 мА) после автоматической внутривенной инъекции 120 мл низкоосмолярного , неионогенный, йодированный контрастный агент (2 мл / кг, Омнипак, здоровье Амершама). Общее время сбора ПЭТ / КТ составляло 35 минут.
Для ПЭТ пациенты голодали по крайней мере за 6 часов до внутривенной инъекции 18F-FDG, с началом сканирования через 60 минут. Изображения от шеи до проксимального бедра были получены на сканере Allegro PET (Philips-ADAC Medical Systems) с пространственным разрешением 5,3 мм в центре поля зрения. Аллегро получил данные в трехмерном режиме после введения 5,18 МБк (0,14 мКи) / кг 18F-FDG. Передача сканирования (2 минуты 30 секунд на кровать) для коррекции неравномерного затухания была получена с использованием точечных источников 137Cs. Сканирование передачи было чередованием между множественными сканированием эмиссии. Изображения были восстановлены с использованием алгоритма итеративной реконструкции, алгоритма максимального правдоподобия низкого действия.
CT живота и таза выполнялась на HiSpeed CT (GE Medical System) с использованием толщины среза 7 мм, с 200 мА и 120 кв.
Наш институт использовал тот же алгоритм для анализа сканирования PET / CT. Первоначально изображения ПЭТ читались независимо от изображений КТ. Оценка изображений ПЭТ включала только изображения с коррекцией затухания. Интерпретация поражения как доброкачественного или злокачественного была основана главным образом на визуальном анализе. SUVmaxs служил исключительно в качестве руководства. После обзоров ПЭТ был проведен комбинированный обзор изображений ПЭТ и КТ. Повреждения, классифицированные как злокачественные ПЭТ, сохраняли злокачественный статус, когда соответствующий КТ-образ выявил морфологическую корреляцию, например аномалию лимфатических узлов. Любые аномалии на КТ без соответствующего увеличения поглощения 18F-FDG были интерпретированы как незначительные. Представленные результаты основаны главным образом на информации, предоставленной ПЭТ, а КТ была использована для точной анатомической локализации.
У нашего пациента ПЭТ-изображения показали интенсивное поглощение ФДГ в правой надпочечной железе, соответствующее поражению, ранее обнаруженному на брюшной полости. Кроме того, неожиданное интенсивное поглощение ФДГ наблюдалось в правой паховой области и считалось метастазом пахового лимфатического узла (рис.1). Ультразвук был проведен для дальнейшей оценки правой паховой области. Однако это не выявило аномальной массы тела, соответствующей области поглощения ФДГ в ПЭТ, но только несколько небольших доброкачественных лимфатических узлов, размер которых был менее 1 см с жировой хелой.
Впоследствии изображения ПЭТ / КТ были ретроспективно рассмотрены вместе с соответствующими анатомическими данными КТ, специально ориентированными на паховую область. Поражение с интенсивным поглощением ФДГ было интерпретировано как грыжа правой передней стенки мочевого пузыря в правом паховом канале. Затем была проведена предварительная КТ-диагностика живота / таза, и масса паховой части была переименована в грыжу мочевого пузыря, а не метастазирование (рис.2).
Мы ретроспективно оценили поглощение 18FDG полуколичественным анализом, используя максимальную стандартизованную величину поглощения (SUVmax) для каждого очага метастазирования надпочечников, мочевого пузыря, грыжи и мочеточника. SUVmax составлял 9,3 для метастазов надпочечников, 33,8 для мочевого пузыря, 28,6 для грыжевого сегмента и 1,2 для фокального слабого поглощения радиотравмы в правом мочеточнике. Высокий уровень SUVmax в мочевом пузыре и грыже объяснялся накопленной интенсивной активностью радиотерапевта путем экскреции ФДГ в моче.
Позднее было подтверждено, что пациент страдал в течение 30 лет от грыжи в паховой области, которая часто распространялась на область мошонки, когда он шел длительное время. Грыжа межпозвоночных сегментов были легко уменьшены путем ручного пособия и путем изменения положения от стояния до спины. Пациент был бессимптомным и не испытывал затруднений при мочеиспускании даже во время грыжа межпозвоночного состояния. Пациентку лечили химиотерапией для рецидива опухоли без герниоррафии.
Грыжа мочевого пузыря составляет от 0,5% до 3% от всех нижних брюшных грыж и наиболее распространена среди мужчин в возрасте от 50 до 70 лет5, а мочевой пузырь участвует в приблизительно от 1% до 4% всех паховых грыж. 6 Грыжа мочевого пузыря редко имеют клинические последствия и обычно обнаруживаются случайно при исследованиях изображений или при паховой грыже.
Большинство пациентов с грыжей мочевого пузыря являются бессимптомными, а у пациентов с симптомами наиболее частыми клиническими результатами являются двухфазные или двойные мочеиспускания8. Пациент, описанный здесь, не испытывает затруднений с мочеиспусканием и не страдает от двухфазной мочеиспускания, что, вероятно, связано с относительно широкая шейка грыжа межпозвоночного сегмента мочевого пузыря. Шестнадцать процентов грыж мочевого пузыря диагностируется после операции с интраоперационным повреждением мочевого пузыря во время восстановления паховой грыжи8, поэтому важно заранее признать наличие грыжи мочевого пузыря. Грыжа, связанная с мочевым пузырем, обычно является прямым типом, так как в этом случае 9 и типичные радиологические данные включают аномальную локализацию грыжнейших структур и асимметрии, выпячивание мочеточника вне тазовых костей и углубление стенки мочевого пузыря.10
В представленном случае грыжа мочевого пузыря представлена как область интенсивного поглощения ФДГ в правой паховой области, имитирующей паховой метастаз. Пирсон и др. 11 сообщили об аналогичном случае 67-летнего мужчины с церебральным метастазом, где для определения первичного фокуса пациенту подвергся ПЭТ ФДГ, который показал повышенное поглощение ФДГ в головном мозге, правой кишке и в паховой области. В то время как повышенное поглощение ФДГ в головном мозге соответствовало метастазированию головного мозга, КТ выявило, что паховое поглощение было вызвано паховой грыжей.
Необходимо также проявлять осторожность при интерпретации изображений ПЭТ ФДГ у пациентов, перенесших операцию на тазовом отделении, чтобы избежать интерпретации изменений нормальной анатомии таза как патологических поражений. Во время обнаружения рецидива таза у пациентов с ректальным раком, которые подверглись абдоминальной или передней резекции, тринадцать (35%) из 37 тазовых мест поглощения 18F ФДГ были либо ложноположительными, либо двусмысленными, используя только ПЭТ. Эта скорость была уменьшена путем комплексного обследования ПЭТ / КТ.4 Сообщалось, что комбинированное ПЭТ / КТ-изображение повышает точность и достоверность обнаружения повреждений при колоректальном раке по сравнению с ПЭТ.
Наш отчет о случаях демонстрирует возможность неправильного толкования изображений ПЭТ без объединения соответствующих данных КТ. Мы регулярно изучаем данные КТ ПЭТ / КТ вместе с данными ПЭТ. Однако в этом случае мы поспешно классифицировали паховое горячее поглощение как злокачественное, используя только изображение ПЭТ, прежде чем применять морфологическую корреляцию с соответствующим изображением КТ. У пациента была предыдущая история рака толстой кишки, а паховая область — обычное место метастазирования лимфатических узлов. В этом случае мы поняли, что общий анализ данных ПЭТ и КТ важен в любой ситуации. Правильная интерпретация PET / CT предполагает комбинированный анализ данных ПЭТ и КТ с учетом возможных неточностей местоположения поглощения ФДГ, создаваемых перистальтическими движениями, происходящими между приобретениями КТ и ПЭТ-изображений.13
В заключение, в этом отчете описывается случай, когда паховая грыжа части стенки мочевого пузыря имитировала узловой рецидив рака толстой кишки, как это определено с помощью ПЭТ-изображения. Параллельная интерпретация ПЭТ с соответствующими данными КТ выявила правильный диагноз. Важно, чтобы радиологи знали об этом редком состоянии во время оценки ПЭТ-сканирования для колоректального рака. Кроме того, этот случай демонстрирует важность комбинированного анализа данных ПЭТ и КТ при интерпретации интегрированного ПЭТ / КТ.
Последовательный осевой (A) и корональный (B) ФДГ ПЭТ показал неожиданное интенсивное поглощение ФДГ в правой паховой области, которое считалось паховым узловым метастазом (стрелками).
Начальная КТ живота / таза показала, что правая передняя стенка мочевого пузыря была изъязвлена в правый паховой канал без усиления контраста в грыжевом мешке. Шея грыжевого мешка была относительно широкой (A и B), а внутри грыжевого мешка была гомогенная кистозная низкая плотность из-за захваченной мочи без кальцификации (C и D).
Начиная сверху, были видны ПЭТ (A), CT (B) и изображения слияния (C). Интенсивное поглощение ФДГ в правой паховой области обусловлено накоплением ФДГ в ловушке мочи грыжевого сегмента мочевого пузыря.

Позитронно - эмиссионная томография (ПЭТ) это диагностическое исследование ядерной медицины позволяющее оценить работу (функцию) органов и тканей. Метод основан на введении в организм радиофармацевтических препаратов испускающих энергию в виде гамма-лучей, которые во время исследования фиксируются гамма-камерой (датчиками, позитронно-эмиссионным сканером). Компьютер, который связан с позитронно-эмиссионным томографом измеряет количество радиоактивного вещества, поглощенного организмом, и, исходя из этого, строит изображения, сочетающие в себе данные о структуре и функции органов и тканей.
В отличие от компьютерной или магнитно-резонансной томографии, радионуклидные исследования в большей степени отражают функцию органа, а не его строение, так как содержание радиоактивной метки в исследуемом органе зависит от его функциональной активности. Области с большей интенсивностью сигнала называются "горячими очагами" и указывают, где накопилось большое количество радиоактивной метки, то есть области с высоким уровнем химической активности. Области с менее интенсивным сигналом или "холодные очаги", указывают на меньшую концентрацию радиоактивной метки и, соответственно, на меньшую химическую активность.
FDG, таким образом, скапливается в нездоровых, перерожденных клетках. На снимке ПЭТ опухоль выделяется на фоне здоровой ткани. С помощью ПЭТ можно обнаружить даже небольшие метастазы диаметром в несколько миллиметров.
Что такое ПЭТ-КТ?
Уникальное совмещение позитронно-эмиссионной и компьютерной томографии (ПЭТ-КТ) дает возможность получить не только изображения процесса обмена веществ, но и внутренних органов, тканей и участков скелета. В то время как ПЭТ выявляет даже самые мелкие опухолевые структуры, КТ очень точно определяет их локализацию.
Данная технология позволяет более точно локализовать опухоли, более тщательно наблюдать за течением болезни, оптимально подобрать индивидуальную терапию и следить за ее успехом. Например, с помощью ПЭТ-КТ можно установить, насколько эффективна химиотерапия, и подтвердить наличие рецидива или его отсутствие. Преимущество ПЭТ-КТ состоит в том, что одновременно проводятся два обследования. Таким образом, пациенты могут сократить время и расходы на лечение, а также получить более точный результат.
ПЭТ-КТ часто используется при диагностике и лечении рака в Германии, однако, его применение показано не при всех видах онкологических заболеваний. Применение этого вида исследования ошибочно считать универсальным.
Как подготовиться к ПЭТ и ПЭТ / КТ исследованиям?
Женщины обязаны информировать своего врача или радиолога о возможной беременности или, о том, что кормят грудью своего ребенка. Дополнительную информацию о радионуклидных исследованиях во время беременности или кормления грудью Вы можете получить у своего врача или врача-радиолога.
Вы должны сообщить своему врачу и врачу-радиологу, выполняющему исследование, обо всех лекарствах, которые Вы принимаете, включая витамины и народные средства. Также Вы должны рассказать: были ли у Вас аллергические реакции, о недавно перенесенных заболеваниях или других состояниях.
Вы получите рекомендации, которые зависят от необходимого Вам типа ПЭТ исследования. Пациентам, страдающим сахарным диабетом, необходима специальная подготовка к исследованию.
Если Вы кормите грудью, Вы должны спросить своего врача или врача-радиолога, когда можно возобновить грудное вскармливание после исследования. Можно сцедить грудное молоко до исследования, хранить и использовать в течение времени, которое необходимо для того, чтобы ПЭТ радиоактивный фармацевтический препарат и контраст КТ вывелись из организма.
Металлические объекты, включая драгоценности, очки, зубные протезы и шпильки, могут вызвать помехи при КТ исследовании, поэтому их необходимо оставить дома или снять перед исследованием. Вас также могут попросить снять слуховой аппарат и съемные зубные протезы.
Перед проведением ПЭТ/КТ необходимо отказаться от приема пищи в течение минимум 6 часов, так как пища может изменить распределение ПЭТ радиоактивной метки в организме, привести к ошибкам в интерпретации результатов и потребовать дополнительного исследования. Таким образом, соблюдать рекомендации относительно приемов пищи очень важно. В течение нескольких часов перед ПЭТ/КТ. Вы должны отказаться от жидкостей, содержащих сахар или калории. Воду пить можно. Если Вы страдаете сахарным диабетом, то Вам дадут дополнительные, специальные рекомендации. Вы должны сообщить своему врачу обо всех лекарствах, которые Вы принимаете, а также были ли у Вас аллергические реакции, особенно на контрастные материалы, йод или дары моря.
Как проводят ПЭТ, ПЭТ/КТ?

Аппарат для позитронно-эмиссионной томографии, внешне подобен аппаратам для КТ исследований. Внутри ПЭТ сканера находится круговая система датчиков, которые записывают выделение энергии радиоактивного препарата в организме.
Пациенту вводится позитронные излучатели, после чего он должен 1-2 часа подождать их распространение по организму (время подготовки к процедуре). После этого пациент ложится на специальную кушетку, которая каждую минуту постепенно движется через кругообразный сканер, где проходит так называемое сканирование - запись данных об организме пациента. Сама процедура длится около 45 минут.
Большинство исследований ядерной медицины являются безболезненными, проходят без существенных осложнений и побочных эффектов. Если радиоактивный препарат будет вводиться внутривенно, то Вы почувствуете небольшой укол в месте, где иглу введут в вену. При введении радиоактивного материала может возникнуть ощущение холода, проходящего через руку, но чаще всего нет никаких неприятных ощущений и побочных эффектов.
Радиоактивный препарат не имеет ни вкуса, ни запаха, поэтому не вызывает неприятных ощущений при ингаляции или проглатывании.
Если потребуется исследование области таза, то возможно понадобится введение мочевого катетера в мочевой пузырь, что может вызвать неприятные ощущения.
Важно оставаться неподвижным при регистрации изображений. Хотя само ядерное исследование безболезненно, но Вам, возможно, будет тяжело находиться без движения или оставаться в одной позе в течение длительного времени.
Если Ваш врач не дал Вам других рекомендаций, Вы можете вернуться к обычному образу жизни сразу после ПЭТ/КТ исследования. Если будут необходимы дополнительные, специальные рекомендации, то о них Вам сообщат медсестра или врач до того, как Вы покинете отделение ядерной медицины.
Путем естественного распада небольшое количество радиоактивного препарата быстро потеряет свою радиоактивность. Радиоактивный препарат выведется из организма с мочой и стулом в течение нескольких часов или дней после исследования. Вам необходимо соблюдать гигиену после мочеиспускания, в туалете дважды за собой спускать воду и тщательно мыть руки. После исследования необходимо пить много воды, чтобы ускорить выведение радиоактивного материала из организма.
Показания к ПЭТ и ПЭТ/КТ исследованиям:
- диагностика рака (например, рака простаты, лимфомы и других видов рака).
- определение распространения опухоли в организме.
- оценка эффективности лечения, например лечения рака.
- диагностика рецидива рака.
- определение кровотока в сердечной мышце.
- определение результата сердечного приступа или инфаркта миокарда в областях сердца.
- выявление областей сердечной мышцы, в которых возможна ангиопластика или шунтирование сердца - коронарных артерий (в комбинации с миокардиальным перфузионным сканированием).
- диагностика патологии головного мозга, такой как опухоли, нарушения памяти, эпилептические приступы и другие поражения центральной нервной системы.
- изучение нормальной функции сердца и головного мозга человека.
ПЭТ и ПЭТ- КТ в онкологии. Используется для выявления, локализации, определения стадии опухоли, особенно, что особенно важно при раке легких, лимфоме, опухолях желудочно-кишечного тракта, раке простаты, нейроэндокринных опухолях, меланоме, опухолях головного мозга. ПЭТ помогает в планировании лучевой терапии, особенно при необходимости стереотаксического облучения или радиотерапии.
ПЭТ и ПЭТ- КТ в неврологии. Используется для выявления таких дегенеративных заболеваний как деменция, болезни Альцгеймера, нарушения двигательного аппарата (например, болезнь Паркинсона или Хантингтона). ПЭТ также используется при локализации эпилептических очагов.
ПЭТ и ПЭТ- КТ в кардиологии. Используется для оценки поражения миокарда перед реканализацией у пациентов с заболеваниями коронарной артерии.
Преимущества и риски ПЭТ, ПЭТ/КТ.
- Информация, полученная при радионуклидных исследованиях, уникальна, и ее нельзя получить при использовании других методов диагностики.
- При многих заболеваниях методы ядерной медицины позволяют получить наиболее полную информацию, необходимую для диагностики и лечения.
- Ядерная медицина менее дорога и может дать более точную информацию, чем диагностическая хирургическая операция.
- Выявляя изменения в организме на клеточном уровне, ПЭТ может обнаружить ранние признаки заболевания прежде, чем произойдут структурные изменения, видимые при МРТ и КТ.
- Преимущества комбинированного ПЭТ/КТ включают:
- большая детальность изображения с более высоким уровнем точности; потому что оба исследования выполняются в одно время, без необходимости изменять позицию пациента, что дает меньше возможностей для ошибки.
- большее удобство для пациента, который подвергается двум исследованиям (ПЭТ и КТ) за один раз.
- В связи с тем, что в методах ядерной медицины используют небольшие дозы, быстро распадающихся радиоактивных материалов, то пациент получает очень маленькую дозу облучения. Таким образом, риск облучения низок по сравнению с потенциальными преимуществами исследования.
- Методы ядерной медицины используются больше пяти десятилетий, и не известно никаких долгосрочных отрицательных воздействий введения низкой дозы радиоактивного материала.
- Аллергические реакции на радиоактивные медицинские препараты возможны, но чрезвычайно редки и обычно умеренны. Однако Вы должны сообщить персоналу отделения ядерной медицины о любых аллергических реакциях или о других проблемах, которые имели место во время предыдущего исследования.
- Введение радиоактивного препарата может вызвать небольшую боль и покраснение в месте инъекции, которая быстро проходит.
- Женщины должны всегда сообщать своему врачу или врачу-радиологу о своей беременности (или подозрениях о возможной беременности) или о том, что кормят грудью.
Как получить консультацию?
- Позвоните координатору по бесплатному номеру 8 800 707 39 95 и расскажите о своей ситуации.
- Отправьте комплект медицинских документов, описывающих ваше заболевание и состояние (если их нет, мы подскажем, что делать).
- Мы БЕСПЛАТНО сделаем перевод документов и предложим варианты лечения.
Вопрос №2. Что такое радиофармпрепарат?
Радиофармпрепарат (РФП) – это соединение, состоящее из специального вещества и радионуклида (изотопа, радионуклидной метки). Специальное вещество отвечает за то, в каком органе накопится РФП, а радионуклидная метка позволяет врачу-диагносту увидеть это накопление на изображении.
В настоящее время для производства РФП используется очень широкий спектр как специальных веществ, так и радионуклидных меток. Во всем мире самым часто используемым у онкологических больных соединением специального вещества и радионуклидной метки является 18 F-фтордезоксиглюкоза ( 18 F-ФДГ). В данном соединении 18 F выполняет функцию радионуклидной метки, ФДГ – специального вещества.
Вопрос №3. Что такое физиологическое накопление РФП?
Физиологическое накопление (гиперфиксация) РФП – это повышенное накопление РФП, определяющееся в различных органах и системах в норме.
Физиологическое накопление наблюдается при исследованиях со всеми РФП: 18 F-ФДГ, 11 С-холином, 11 С-метионином, 68 Ga-ПСМА и т.д. В зависимости от типа РФП меняется лишь местоположение физиологической гиперфиксации. Например, при ПЭТ и ПЭТ/КТ с самой часто используемой 18 F-ФДГ физиологическое накопление РФП определяется в коре головного мозга, ротоглотке, носоглотке, мышцах гортаноглотки, миокарде левого желудочка, чашечно-лоханочных системах почек, фрагментарно по ходу петель толстой кишки, мочевом пузыре.
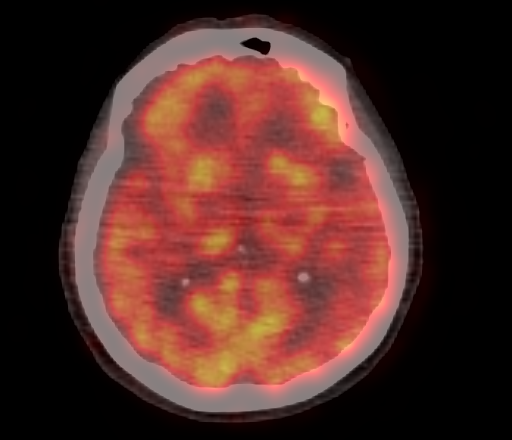 | 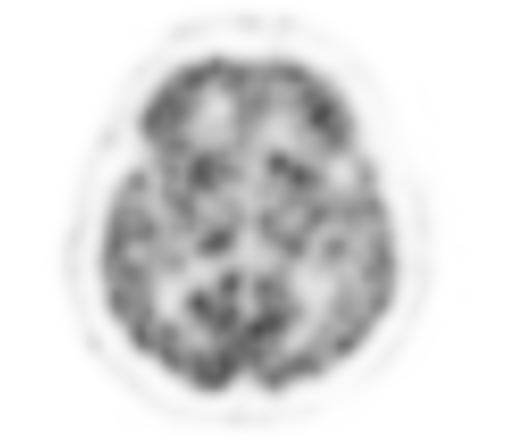 |
| Физиологическое накопление 18 F-ФДГ в коре головного мозга. | |
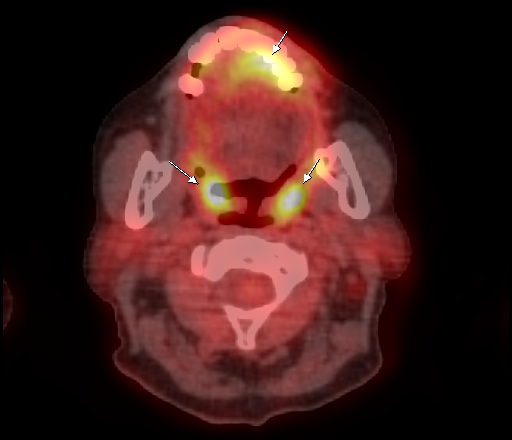 | 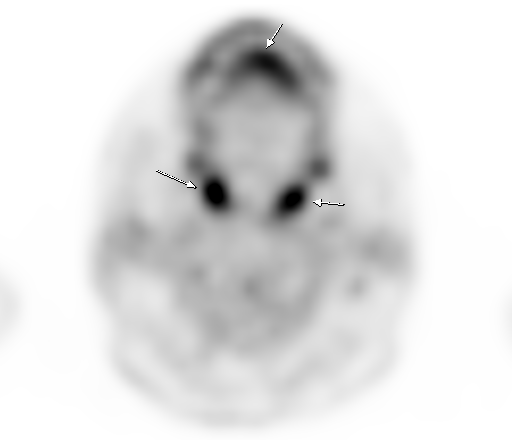 |
| Физиологическое накопление 18 F-ФДГ в ротоглотке. | |
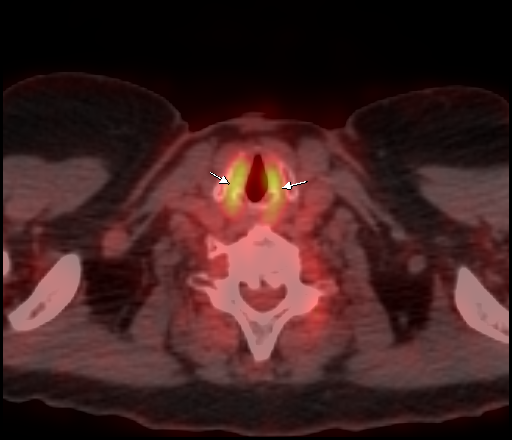 | 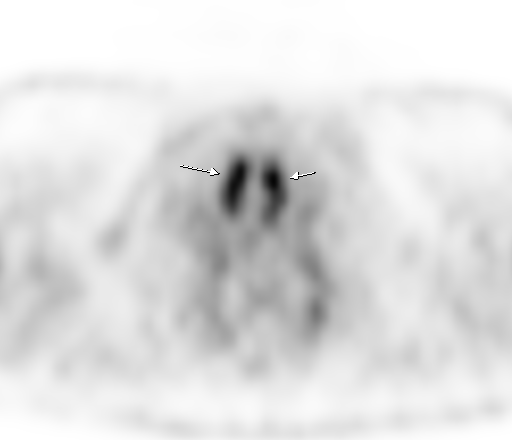 |
| Физиологическое накопление 18 F-ФДГ в мышцах гортаноглотки. | |
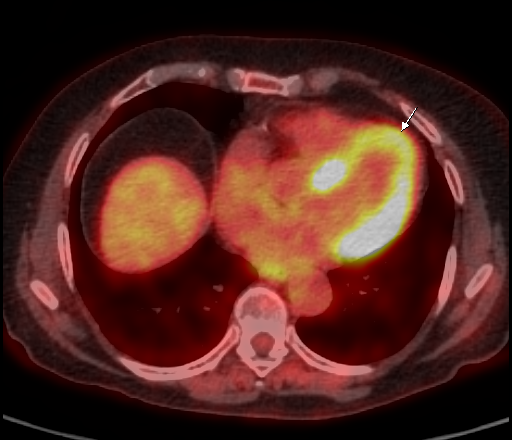 | 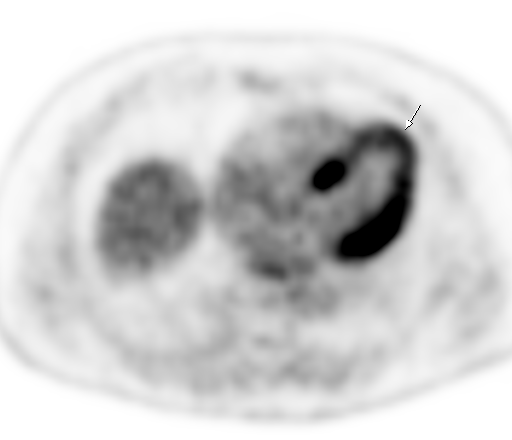 |
| Физиологическое накопление 18 F-ФДГ в миокарде левого желудочка. | |
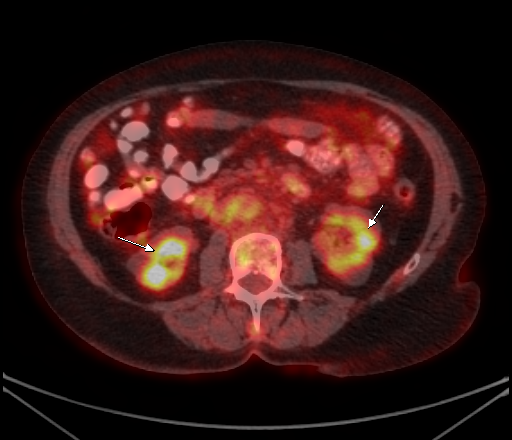 | 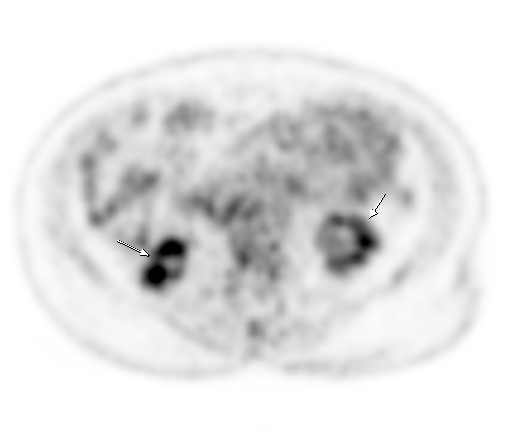 |
| Физиологическое накопление 18 F-ФДГ в чашечно-лоханочных системах почек. | |
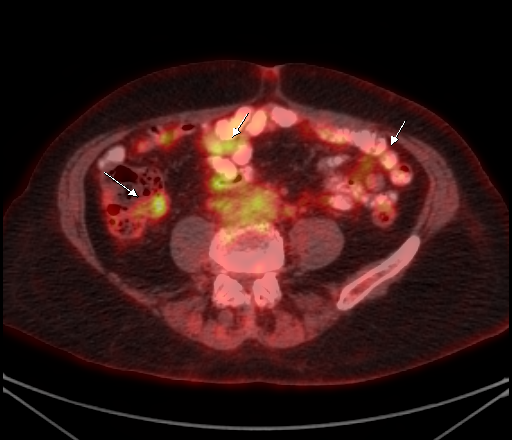 | 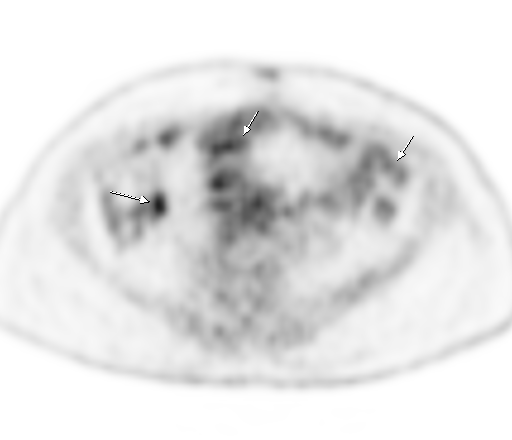 |
| Физиологическое накопление 18 F-ФДГ по ходу петель толстой кишки. | |
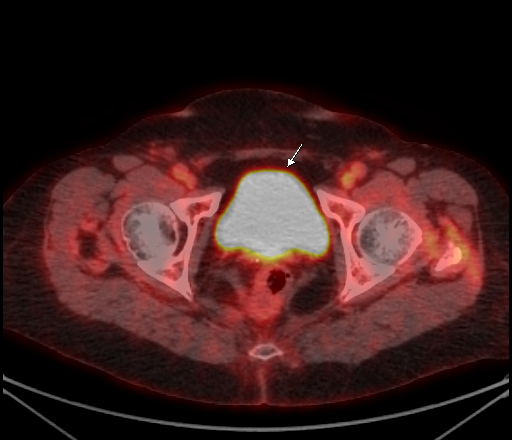 | 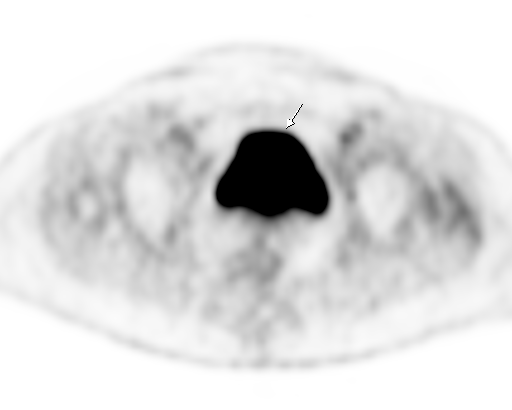 |
| Физиологическое накопление 18 F-ФДГ в мочевом пузыре. | |
Вопрос №4. Что такое патологическое накопление РФП?
Патологическое накопление РФП – это повышенное накопление РФП в органах и тканях, регистрирующееся при заболеваниях, чаще всего в злокачественных опухолях.
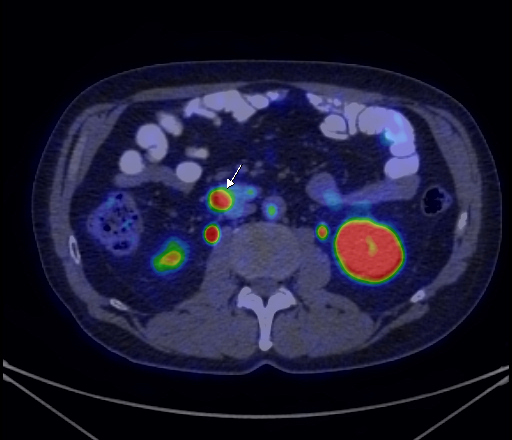 |
| Данные ПЭТ/КТ с 68 Ga-DOTA-TATE у пациента с нейроэндокринной опухолью тощей кишки. В проекции злокачественной опухоли, расположенной в тощей кишке, определяется очаг патологической гиперфиксации РФП. |
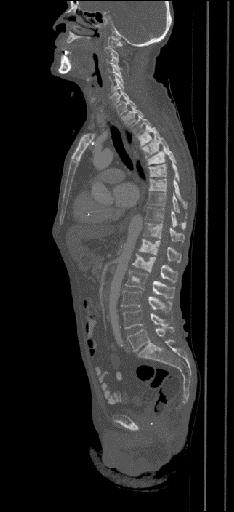 | 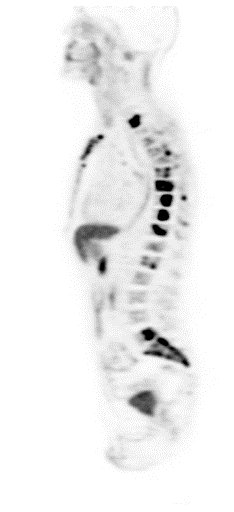 | 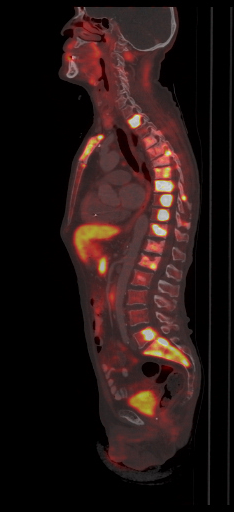 |
| Данные ПЭТ/КТ с 11 С-холином у пациента с раком предстательной железы. Состояние после простатэктомии. В костях скелета визуализируются множественные очаги патологического накопления РФП (метастазы). | ||
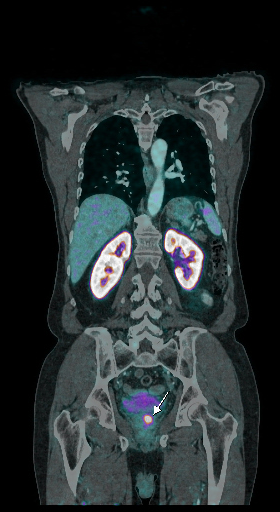 | 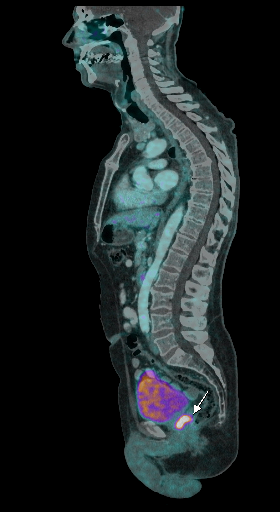 | 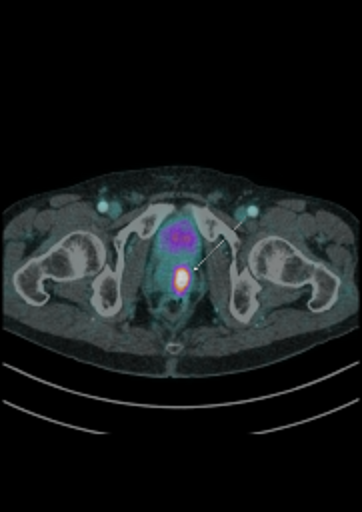 |
| Данные ПЭТ/КТ с 68 Ga-ПСМА у пациента с местным рецидивом рака предстательной железы. Состояние после лучевой терапии. В левых отделах предстательной железы определяется очаг патологического накопления РФП. | ||
Вопрос №5. Что такое метаболически активное и метаболически неактивное образование?
Метаболически неактивное образование – это образование, которое не накопило РФП. Чаще всего отсутствие повышенного накопления РФП в опухоли свидетельствует о ее доброкачественной природе.
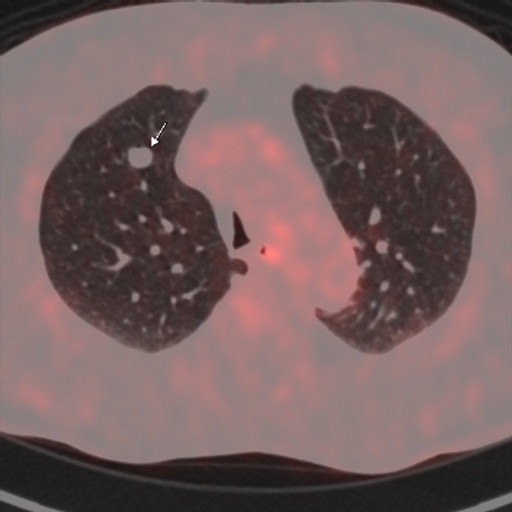 |
| Данные ПЭТ/КТ с 18 F-ФДГ у пациента с метаболически неактивным образованием правого легкого (доброкачественная опухоль - гамартома). |
Метаболически активное образование – это образование, в котором накопился РФП в повышенном количестве. Повышенное накопление РФП в опухоли чаще всего свидетельствует о ее злокачественном характере.
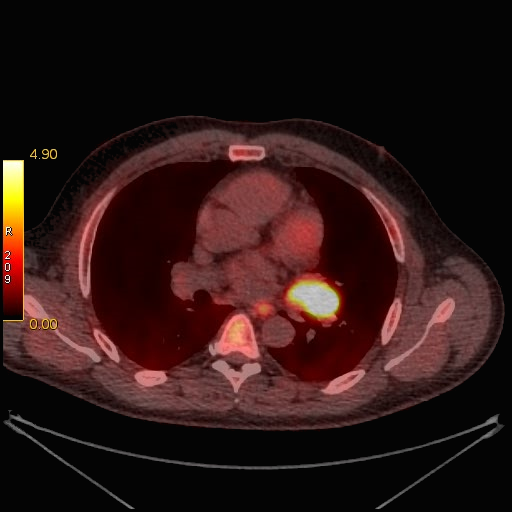 |
| Данные ПЭТ/КТ с 11 С-метионином у больного с метаболически активным образованием корня левого легкого (типичный карциноид). |
Вопрос №6. Что такое SUV?
SUV (Standardized Uptake Value, стандартизированный уровень захвата) – это величина, отражающая интенсивность накопления РФП в зоне интереса, например, в опухоли.
Показатель SUV рассчитывается программным комплексом автоматически и измеряется в различных единицах. В нашем Центре, как и в большинстве отечественных и зарубежных медицинских учреждений, где проводится позитронная эмиссионная томография, в качестве единиц измерения показателя SUV принято использовать г/мл (g/ml).
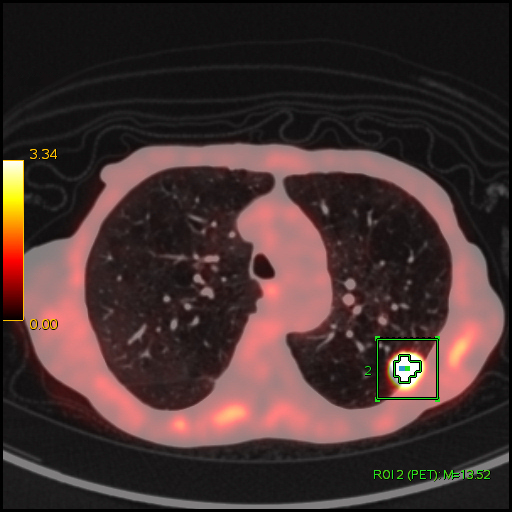 |
| Данные ПЭТ/КТ с 18 F-ФДГ. Оконтуривание метаболически активной злокачественной опухоли левого легкого для измерения показателя SUV. В данном случае величина SUV в опухоли определяется на уровне 13,52 g/ml. |
Вопрос №7. Для чего используется величина SUV?
Величина SUV в основном используется для оценки ответа злокачественной опухоли на проведенное лечение. Важно подчеркнуть, что в ряде клинических ситуаций показатель SUV в опухоли является единственным критерием, позволяющим оперативно получить информацию о чувствительности образования к только что начатой терапии.
Если опухоль чувствительна к лечению, то уровень SUV в ней при повторном ПЭТ-исследовании будет снижаться, если нечувствительна или малочувствительна (резистентна, устойчива) – значение SUV останется без изменений или увеличится. Следует помнить, что своевременная диагностика устойчивости опухоли к лечению позволит скорректировать план лечения, а в некоторых случаях и радикально его изменить.
Как уже было сказано выше, для оценки эффективности терапии врач-радиолог оценивает динамику показателя SUV до и после лечения.
Существует четыре варианта метаболического ответа опухоли на проведенное лечение:
- Частичный метаболический ответ – устанавливается при уменьшении значения SUV в опухоли на 25% и более;
- Полный метаболический ответ – заключается в отсутствии повышенного накопления РФП в опухоли;
- Метаболическое прогрессирование – устанавливается при увеличении SUV на 25% и более и/или при появлении новых очагов патологической гиперфиксации РФП;
- Метаболическая стабилизация – регистрируется при отсутствии достоверных (менее 25%) изменений показателя SUV в опухоли.
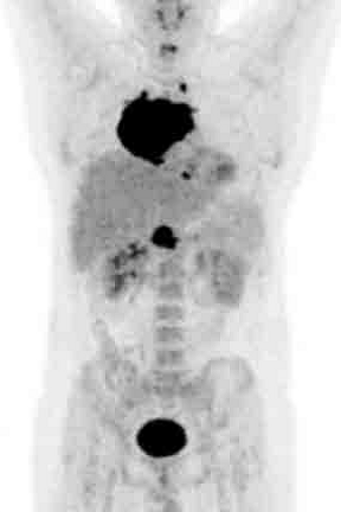 | 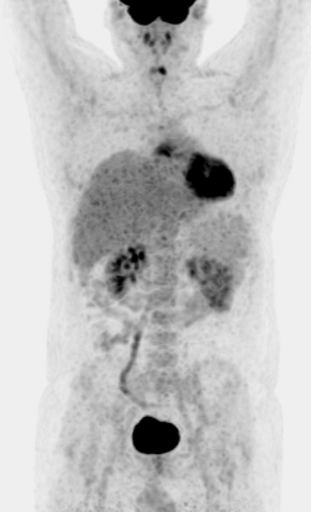 | 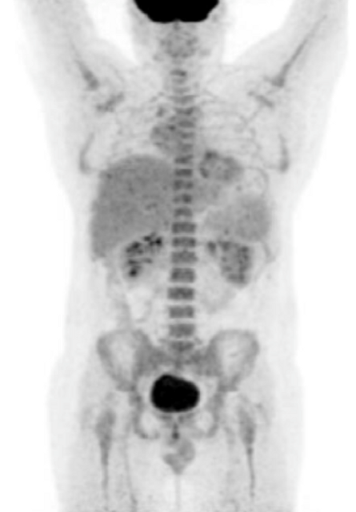 |
| а | б | в |
Результаты ПЭТ с 18 F-ФДГ у пациента с диффузной В-клеточной крупноклеточной лимфомой до лечения (а), после 2 курса ПХТ (б) и через 13 месяцев после окончания терапии (в).
а – до лечения в средостении визуализируется массивное метаболически активное образование с уровнем SUV=12,6;
б – после 4 курса ПХТ отмечается значительное уменьшение метаболического объема опухоли и снижение показателя SUV до 3,4 (достигнут частичный метаболический ответ, т.е. опухоль чувствительна к выбранной ПХТ);
в – через 13 месяцев после окончания ПХТ очагов патологической гиперфиксации РФП в проекции органов средостения не обнаружено (достигнут полный метаболический ответ).
Читайте также:

