При хроническом лейкозе у пациента можно выявить
Содержание:
- Отличие лейкоза: острого и хронического
- Классификация лейкозов
- Симптоматика
- Диагностика
- Лечение
← Как происходит пересадка костного мозга при лейкемии?
Сведения об остром промиелоцитарном лейкозе →
Фазы развития заболевания
В развитии патологии медики выделяют три стадии. Первая стадия носит название медленной, или хронической, которая может протекать до трех лет. Ухудшение симптомов заболевания после этого периода говорит о вступлении болезни в новую фазу – фазу акселерации. В этой фазе при мощном и своевременном лечении рак крови можно перевести в предыдущую фазу. Обычно такая фаза длится до полутора лет. После чего либо проходит ухудшение состояния здоровья пациента, либо его здоровье стабилизируется. а опухоль поддается контролю.
Отличие лейкоза: острого и хронического
Ранняя стадия острого лейкоза характерна накапливанием незрелых клеток и отсутствием их роста. Их переизбыток в 80% случаев угнетает нормальное кроветворение ростков. Хронический лейкоз способствует синтезу развитых клеток — гранулоцитов для постепенного замещения в периферической крови здоровых клеток.
Важно знать. Лейкоз хронический НЕ становится острым лейкозом и наоборот.
Симптомы у взрослых в начальной стадии острого лейкоза нередко проходят незамеченными, поскольку в крови больших колебаний биохимических показателей в сторону повышения или понижения не бывает. Позднее:
- появится ощущение ослабленности;
- имеющиеся хронические болезни обострятся;
- возможно активирование вируса герпеса и иного вида вирусных и бактериальных инфекций.
Рекомендуем изучить по данной теме также:
Химиотерапия как способ лечения острого миелобластного лейкоза
В развернутом периоде начинают ярко выражаться клинические и гематологические проявления острого лейкоза. Обострения переходят в ремиссии. Болезнь полностью излечивается или переходит в терминальную стадию.
Важно. В течение 5 лет при отсутствии бластных клеток в периферической крови устанавливается клинико-гематологическое излечивание (полная ремиссия).
В терминальной стадии цитостатики, используемые для лечения острого лейкоза, перестают действовать. Это становится причиной полного угнетения кроветворной системы. Даже при трансплантации костного мозга в этот период крайне высока смертность людей.
Если лейкоз хронический, то в крови присутствуют дозревшие клетки, многие из которых не способны выполнять свою прямую функциональную работу. При исследовании лабораторных анализов в крови выявляют повышенный уровень бесполезных лейкоцитов. Они не защищают организм от инфекций.
Тогда у пациентов возникает вопрос: хронический лейкоз — болезнь проходит или нет? При переизбытке гранулоцитов, мешающих кровотоку, избыток лейкоцитов и онкоклеток удаляют посредством лейкофареза. Процедура обеспечивает быстрый, но временный эффект.
Начальной фазы у хронического заболевания может и не быть, в 50% его выявляют по анализу крови по другому поводу. Даже при подтверждении диагноза хроническая болезнь может протекать на моностадии доброкачественно, поскольку опухоль состоит из одного клона клеток.
На последующей стадии появляются вторичные клоны опухоли. Поликлоновая стадия протекает быстро на фоне увеличения количества бластов. Эту стадию еще называют бластным кризом, поскольку 80% пациентов при этом погибают.
Лейкоз хронический проявляется:
- сплено- и гепатомегалией — увеличиваются в размере печень и селезенка;
- общей анемией с хроническим течением;
- генерализованные поражения лимфоузлов.
Причины заболевания
Хронический лейкоз возникает чаще всего у людей зрелого возраста, заболевание диагностируется в большинстве случаев у пациентов старше сорока лет. Преимущественно страдают хроническим лейкозом мужчины. У детей белокровие диагностируется довольно редко – всего в одном проценте случаев.
Точные причины заболевания установить до сегодняшнего времени не удалось. Сейчас разрабатывается вирусно-генетическая теория гемобластозов, согласно которой пусковым механизмом для заболевания может стать проникновение в организм определенных вирусов, например, Эпштейна-Барра, ретровирусов, способных встраиваться в незрелые клетки крови и провоцировать их бесконтрольное деление.
Врачи утверждают, что определенную роль в заболевании играет и наследственный фактор, ведь по статистике у значительного числа пациентов с лейкозом подобные заболевания диагностировались и у ближайших родственников. Также может возникать хроническая лейкемия и по вине 22 хромосомы, которая может нести в себе аномалию.
Не последнюю роль играет и негативное внешнее воздействие на организм – получение высоких доз радиации, рентгеновское облучение, работа во вредной промышленности (например, производство лакокрасочных изделий, фармацевтических препаратов, работа на золотоприисках). Риск развития увеличивается при табакокурении, чрезмерном употреблении алкогольных напитков, контакте с химикатами, удобрениями.
Классификация лейкозов
Если подтверждены хронические лейкозы — классификация включает две подгруппы:
- миелоидную;
- лимфоидную.
Миелоидная подгруппа состоит из хронических миелопролиферативных лейкозов:
- миелолейкоза;
- миелоза сублейкемического (остеомиелосклероза, миелофиброза);
- эритремии (истинной полицетемии);
- миеломоноцитарного;
- моноцитарного;
- мегакариоцитарного (идиопатической тромбоцитемии).
Важно. При хроническом миелолейкозе происходит пролиферация стволовой клетки в сопровождении повышения уровня предшественников гранулоцитов, эритроцитов и тромбоцитов.
Лимфоидная подгруппа состоит из лимфопролиферативных лейкозов:
- лимфолейкоза хронического;
- плазмоцитомы (миеломной болезни);
- лимфогранулематоза;
- лимфомы неходжкинской.
Ранее мы уже писали о лейкозе у детей и рекомендовали добавить эту статью в закладки.
Важно. При лимфолейкозе хронической стадии происходит пролиферация малых лимфоцитов: мозга костей, ЛУ, печени, селезенки и периферической крови.
Симптоматика
Опасные симптомы у взрослых проявляются признаками лейкемии: соматическими и гематологическими. Первичные соматические проявления белокровия характерны:
- ощущением постоянного утомления, слабости и недомогания;
- постоянным желанием спать или бессонницей;
- нарушением деятельности мозга: больные жалуются на ухудшение памяти, невозможность сосредоточиться;
- изменением цвета кожи (она становится бледной), долгим заживлением ран, синяков и мелких царапинок, проявлением нагноений;
- кровотечениями из десен и носа;
- ломотой и болями в любом суставе или кости;
- увеличением печени, селезенки и лимфоузлов;
- настырными простудами, обострением хронических форм болезней, как герпес, тонзиллит, бронхит, пиелонефрит;
- снижением веса на фоне отсутствия аппетита.
- повышается или понижается СОЭ;
- повышаются лейкоциты и проявляется лейкоцитоз;
- снижается гемоглобин в крови (проявляется анемия).
Диагностика
По анализу крови узнают количество кровяных клеток. При хроническом лейкозе лейкоциты повышаются, эритроциты и тромбоциты — снижаются. По биохимическому анализу крови уточняется функция почек и состав крови.
- красного мозга костей подтверждается диагноз и оценивается лечение хронического лейкоза;
- спинномозгового экссудата (пункции) — выявляются онкоклетки и проводится химиотерапия.
Чтобы уточнить тип лейкоза, исследуют цитохимию, проточную цитометрию, иммуноцитохимию, цитогенетику и молекулярную генетику. По рентгенограмме грудины и костей выявляют пораженные лимфоузлы средостения, костных суставов.
По КТ обнаруживают пораженные ЛУ в грудине и животе. МРТ исследуют мозг головы и спины. УЗИ необходимо для отличия новообразований: опухолевых и кистозных, выявления поражений в почках, печени, селезенке и ЛУ.
Лечение
Тактику лечения выбирают, зависимо от группы риска. Пациентов в группе с низким риском наблюдают, а при появлении явных симптомов назначают лечение. Прогноз выживаемости — 20-25 лет.
В группе с промежуточным и высоким риском больным терапию временно не применяют, если отсутствуют симптомы. Далее основным лечением будет являться химиотерапия с применением мощных лекарств. Препараты уничтожают лейкозные клетки, которые быстро и бесконтрольно делятся, нарушая важные этапы цикла. При этом могут повредиться и нормальные клетки.
Лечение лимфобластного лейкоза проводится рядом агентов: L-аспарагиназой или PEG-L- аспарагиназой, Даунорубицином (Дауномицином), Винкристином, Преднизолоном. Из других препаратов — Доксорубицином, Цитарабином, Этопозидом, Дексаметазоном.
Применяют Хлорамбуцил, или заменяют его Циклофосфамидом с меньшими побочными эффектами Как рассчитывается для взрослых максимальная доза Дексаметазона при лечении хронических лейкозов?
Дозировку внутривенных струйных или капельных вливаний, инъекций внутримышечных назначает врач. За первые сутки вводят 4-20 мг 3-4 приемами. Курс — 3-5 дней. Для капельного введения пользуются раствором натрия хлорида изотонического или 5%-ного декстрозного раствора.
Если лейкоз хронический, лечение Дексаметазоном в таблетках назначают по 0,5 мг или 1,5 мг с едой. За сутки максимальная доза составляет 15 мг (не более), минимальная — 1 мг. При установлении стабильного состояния дозу снижают до 3 мг/сутки. Детям рассчитывают 83,3-333,3 мкг/кг.
Эффективно лечение хронического миелоидного лейкоза Мезилатом иматиниба (Гливеком). Хронического лимфолейкоза — Флударабином с Циклофосфамидом.
Нередко проводят трансплантацию костного мозга в самом начале комплексной терапии для улучшения результатов. При этом проводится химиотерапия и облучение (редко) для уничтожения онкоклеток, а также вливание стволовых клеток для прорастания в костный мозг и вырабатывания нормальных здоровых клеток.
Проводят радиоиммунотерапию, Т клеточную иммунотерапию для облучения онкоклеток с минимальным повреждением здоровых тканей, для минимилизации токсичности для больного и предотвращения рецидива. Лучевой терапией по спирали вокруг опухоли достигают эффекта и уменьшают травматизацию здоровых клеток, что снижает количество осложнений.
Для лечения хронического лейкоза необходимо применять комплексную терапию: химиотерапию, операции, радиоиммунотерапию, Т клеточную иммунотерапию, моноклональные антитела и стволовые клетки для трансплантации.
← Как происходит пересадка костного мозга при лейкемии?
Сведения об остром промиелоцитарном лейкозе →
Прогноз
Дальнейшая жизнь пациента, ее качество и длительность зависит от типа рака и своевременности лечения. В среднем при раннем диагностировании большинство больных живут 10 лет и больше, при средне запущенной болезни – 5-7, при поздней медицинской помощи – 1-3 года. Так же на прогноз влияет возраст. Чем меньше возраст пациента, тем больше шансов на длительную ремиссию или даже полное выздоровление.
Стоит отметить, что повторный криз еще не означает смерть – если прошлое лечение хорошо подействовало и прошло много времени, это же лечение может исцелить пациента снова. В крайнем случае врач может назначить другую химиотерапию, которая, возможно, окажется более эффективной.
Хронический лейкоз – это первичное опухолевое заболевание системы кроветворения, субстратом которого выступают зрелые и созревающие клетки миелоидного или лимфоидного ряда. Различные формы хронического лейкоза протекают с преобладанием интоксикационного (слабость, артралгии, оссалгии, анорексия, похудание), тромбогеморрагического (кровоточивость, тромбозы различной локализации), лимфопролиферативного синдромов (увеличение лимфоузов, спленомегалия и др.). Решающее значение в диагностике хронического лейкоза принадлежит исследованию ОАК, биоптатов костного мозга и лимфоузлов. Лечение хронических лейкозов проводится методами химиотерапии, лучевой терапии, иммунотерапии, возможна трансплантация костного мозга.
МКБ-10


- Причины
- Факторы риска
- Патогенез
- Классификация
- Симптомы хронического лейкоза
- Хронический миелоидный лейкоз
- Хронический лимфолейкоз
- Осложнения
- Диагностика
- Лечение хронического лейкоза
- Прогноз
- Цены на лечение
Общие сведения
Хронический лейкоз – хронические лимфопролиферативные и миелопролиферативные заболевания, характеризующиеся избыточным увеличением количества кроветворных клеток, сохраняющих способность к дифференцировке. В отличие от острых лейкозов, при которых происходит пролиферация низкодифференцированных гемопоэтических клеток, при хронических лейкозах опухолевый субстрат представлен созревающими или зрелыми клетками. Для всех типов хронических лейкозов характерна длительная стадия доброкачественной моноклоновой опухоли.
Хронические лейкозы поражают преимущественно взрослых в возрасте 40-50 лет; мужчины болеют чаще. На долю хронического лимфоидного лейкоза приходится около 30% случаев, хронического миелоидного лейкоза - 20% всех форм лейкемии. Хронический лимфолейкоз в гематологии диагностируется в 2 раза чаще, чем хронический миелолейкоз. Лейкозы у детей протекают в хроническом варианте крайне редко - в 1-2% случаев.
Причины
Истинные причины, приводящие к развитию хронического лейкоза, неизвестны. В настоящее время наибольшее признание получила вирусно-генетическая теория гемобластозов. Согласно данной гипотезе, некоторые виды вирусов (в числе которых – вирус Эбштейна-Барр, ретровирусы и др.) способны проникать в незрелые кроветворные клетки и вызывать их беспрепятственное деление.
Не подвергается сомнению и роль наследственности в происхождении лейкозов, поскольку доподлинно известно, что заболевание нередко носит семейный характер. Кроме этого, хронический миелолейкоз в 95% случаев ассоциирован с аномалией 22-й хромосомы (филадельфийской или Рh-хромосомы), фрагмент длинного плеча которой транслоцирован на 9-ю хромосому.
Наиболее значимыми предрасполагающими факторами к различным видам и формам хронических лейкозов выступают воздействия на организм:
- высоких доз радиации;
- рентгеновского облучения;
- производственных химических вредностей (лаков, красок и др.);
- лекарственных препаратов (солей золота, антибиотиков, цитостатиков);
- длительный стаж курения.
Риск развития хронического лимфоцитарного лейкоза повышается при длительном контакте с гербицидами и пестицидами, а хронического миелоидного лейкоза – при радиационном облучении.
Патогенез
В патогенезе хронического лимфолейкоза значимая роль принадлежит иммунологическим механизмам – об этом свидетельствует его частое сочетание с аутоиммунной гемолитической анемией и тромбоцитопенией, коллагенозами. Вместе с тем, у большинства больных хроническими лейкозами причинно значимых факторов выявить не удается.
Классификация
В зависимости от происхождения и клеточного субстрата опухоли хронические лейкозы делятся на:
- Лимфоцитарные: хронический лимфолейкоз, болезнь Сезари (лимфоматоз кожи), волосатоклеточный лейкоз, парапротеинемические гемобластозы (миеломная болезнь, макроглобулинемия Вальденстрема, болезни легких цепей, болезни тяжелых цепей).
- Миелоцитарные (гранулоцитарные): хронический миелолейкоз, эритремия, истинная полицитемия, хронический эритромиелоз и др.
- Моноцитарные: хронический моноцитарный лейкоз и гистиоцитозы.
В своем развитии опухолевый процесс при хроническом лейкозе проходит две стадии: моноклоновую (доброкачественную) и поликлоновую (злокачественную). Течение хронического лейкоза условно подразделяется на 3 стадии: начальную, развернутую и терминальную.

Симптомы хронического лейкоза
В начальном периоде хронического миелолейкоза клинические проявления отсутствуют или неспецифичны, гематологические изменения выявляются случайно при исследовании крови. В доклиническом периоде возможно нарастание слабости, адинамии, потливости, субфебрилитета, болей в левом подреберье.
Переход хронического миелоидного лейкоза в развернутую стадию знаменуется прогрессирующей гиперплазией селезенки и печени, анорексией, похуданием, выраженными болями в костях и артралгиями. Характерно образование лейкемических инфильтратов на коже, слизистых полости рта (лейкемический периодонтит), ЖКТ. Геморрагический синдром проявляется гематурией, меноррагией, метроррагией, кровотечениями после экстракции зубов, кровавыми поносами. В случае присоединения вторичной инфекции (пневмонии, туберкулеза, сепсиса и др.) температурная кривая приобретает гектический характер.
Терминальная стадия хронического миелоидного лейкоза протекает с резким обострением всех симптомов и выраженной интоксикацией. В этот период может развиваться плохо поддающееся терапии и угрожающее жизни состояние – бластный криз, когда из-за резкого увеличения количества бластных клеток течение заболевания становится похожим на острый лейкоз. Для бластного криза характерна агрессивная симптоматика: лейкемиды кожи, тяжелые кровотечения, вторичные инфекции, высокая температура, возможен разрыв селезенки.
Долгое время единственным признаком хронического лимфолейкоза может быть лимфоцитоз до 40-50%, незначительное увеличение одной-двух групп лимфоузлов. В развернутый период лимфаденит принимает генерализованную форму: увеличиваются не только периферические, но и медиастинальные, мезентериальные, забрюшинные узлы. Возникает сплено- и гепатомегалия; возможно сдавление холедоха увеличенными лимфатическими узлами с развитием желтухи, а также верхней полой вены с развитием отеков шеи, лица, рук (синдром ВПВ). Беспокоят упорные оссалгии, кожный зуд, рецидивирующие инфекции.
Тяжесть общего состояния больных хроническим лимфоидным лейкозом обусловлена прогрессированием интоксикации (слабость, потливость, лихорадка, анорексия) и анемического синдрома (головокружение, одышка, сердцебиение, обморочные состояния).
Терминальная стадия хронического лимфоидного лейкоза характеризуется присоединением геморрагического и иммунодефицитного синдромов. В этот период развивается тяжелая интоксикация, возникают кровоизлияния под кожу и слизистые, носовые, десневые, маточные кровотечения.
Осложнения
Иммунодефицит, обусловленный неспособностью функционально незрелых лейкоцитов выполнять свои защитные функции, проявляется синдромом инфекционных осложнений. У больных хроническим лимфолейкозом часты легочные инфекции (бронхиты, бактериальные пневмонии, туберкулезные плевриты), грибковые поражения кожи и слизистых, абсцессы и флегмоны мягких тканей, пиелонефриты, герпетическая инфекция, сепсис.
Нарастают дистрофические изменения внутренних органов, кахексия, почечная недостаточность. Летальный исход при хроническом лимфоидном лейкозе наступает от тяжелых инфекционно-септических осложнений, кровотечений, анемии, истощения. Возможна трансформация хронического лимфолейкоза в острый лейкоз или лимфосаркому (неходжкинскую лимфому).
Диагностика
Предполагаемый диагноз устанавливается на основании анализа гемограммы, с результатами которой пациент должен быть немедленно направлен к врачу-гематологу. Для подтверждения диагноза проводится:
- Общий анализ крови. Типичные для хронического миелоидного лейкоза изменения включают: анемию, присутствие единичных миелобластов и гранулоцитов на разной стадии дифференцировки; в период бластного криза количество бластных клеток увеличивается более чем на 20%. При хроническом лимфолейкозе определяющими гематологическими признаками выступают выраженный лейкоцитоз и лимфоцитоз, наличие лимфобластов и клеток Боткина-Гумпрехта.
- Пункции и биопсии. С целью определения морфологии опухолевого субстрата показано выполнение стернальной пункции, трепанобиопсии, биопсии лимфоузлов. В пунктате костного мозга при хроническом миелолейкозе увеличено количество миелокариоцитов за счет незрелых клеток гранулоцитарного ряда; в трепанобиоптате определяется замещение жировой ткани миелоидной. При хроническом лимфоидном лейкозе миелограмма характеризуется резким усилением лимфоцитарной метаплазии.
- Инструментальные исследования. Для оценки выраженности лимфопролиферативного синдрома применяются УЗИ лимфатических узлов, селезенки, рентгенография грудной клетки, лимфосцинтиграфия, МСКТ брюшной полости и ряд других.
Лечение хронического лейкоза
На ранней доклинической стадии лечение неэффективно, поэтому больные подлежат динамическому наблюдению. Общережимные мероприятия предполагают исключение физических перегрузок, стрессов, инсоляции, электропроцедур и теплолечения; полноценное витаминизированное питание, длительные прогулки на свежем воздухе.
В развернутом периоде миелолейкоза назначается химиотерапевтическое лечение (бусульфан, митобронитол, гидроксимочевина и др.), при выраженной спленомегалии проводится облучение селезенки. Подобная тактика, хоть и не приводит к полному излечению, но существенно тормозит прогрессирование болезни и позволяет отсрочить наступление бластного криза. Кроме медикаментозной терапии, при хроническом миелоцитарном лейкозе используются процедуры лейкафереза. В ряде случаев излечение достигается с помощью трансплантации костного мозга.
При переходе хронического миелолейкоза в терминальную стадию назначается высокодозная полихимиотерапия. В среднем после установления диагноза больные хроническим миелолейкозом живут 3-5 лет, в отдельных случаях – 10-15 лет. Также проводится цитостатическая терапия (хлорбутин, циклофосфамид), иногда в сочетании со стероидной терапией, облучением лимфоузлов, селезенки, кожи. При значительном увеличении селезенки выполняется спленэктомия. Применяется трансплантация стволовых клеток, однако ее эффективность еще требует подтверждения.

Прогноз
Продолжительность жизни больных хроническим лимфоидным лейкозом может составлять от 2-3 лет (при тяжелых, неуклонно прогрессирующих формах) до 20-25 лет (при относительно благоприятном течении).
Отвечаем на самые важные вопросы про лейкоз
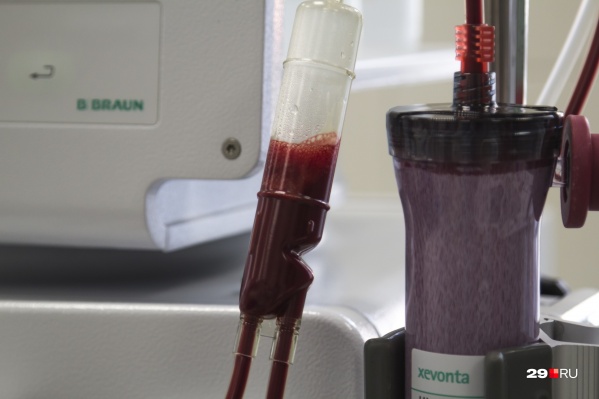
" title="Показать лейкоз может исследование периферической крови
" itemprop="contentUrl">
Показать лейкоз может исследование периферической крови
Фото: Сергей Яковлев
В сентябре мы познакомились с архангелогородкой Вероникой Рожновской, жизнь которой изменилась, когда у её дочери Даши диагностировали лейкоз. Девочка в тот момент училась в пятом классе, а на недомогания врачи не обращали должного внимания. Специалисты отмечают, что рак крови действует тем агрессивнее, чем моложе организм, который поражает болезнь. На другие важные вопросы об этом раке отвечают профессор кафедры онкологии и медицинской радиологии Уральского государственного медицинского университета Сергей Берзин и гематолог из Уфы Нэлли Янтурина.
Лейкоз — опухолевое заболевание клеток крови. При лейкозе происходит патологическая трансформация лейкоцитов и их бесконтрольное деление. В итоге они замещают собой нормальные клетки костного мозга, из которых образуются циркулирующие в крови лейкоциты, эритроциты и тромбоциты.
При хронических лейкозах деление клеток идёт медленнее, и клиника тоже развивается с меньшей скоростью. Лейкозный клон током крови разносится по всей кроветворной ткани. Органами-мишенями, где откладываются метастазы, становятся почки и кости. Оседая в костной ткани, эти клетки, по-другому они называются миеломные, нарушают ее структуру. Это может проявляться частыми переломами, болью в позвоночнике, ребрах. Хронические лейкозы могут годами протекать без каких-либо явных отклонений в самочувствии, тогда выявить их можно только при исследовании крови.
Начало заболевания нередко протекает без выраженных симптомов. Больные отмечают общую слабость, утомляемость, неопределенную боль в костях, непостоянную температуру по вечерам в пределах 37,1–38 градусов. Но уже в этот период у некоторых больных можно обнаружить небольшое увеличение лимфатических узлов, селезенки. В анализе крови тоже будут изменения — повышение или снижение количества лейкоцитов, анемия.
Лейкоз может проявляться разнообразными симптомами. При острой форме пациенты могут жаловаться, что стали часто простывать, у них возникли инфекционные осложнения или синяки на теле, а кого-то будет беспокоить резкая потеря веса, появление шишек на теле или увеличение лимфоузлов.
Симптомы лейкоза неспецифичны, они таковы:
- слабость;
- головокружения;
- высокая температура без явных на то причин;
- боли в руках и ногах;
- кровотечения.
При замещении патологически размножающимися лейкоцитами других клеток крови на первое место выходят анемии и кровотечения из-за уменьшения числа других клеток крови — эритроцитов и тромбоцитов. Из-за накопления лейкоцитов в лимфоузлах, печени или селезёнке эти органы могут увеличиться, но обнаружить эти симптомы уже может только врач.
При лейкозе субстратом опухоли является костный мозг, который находится во всех трубчатых и плоских костях. Здесь же развиваются предшественники крови: эритроциты, лейкоциты и тромбоциты. Когда в ткани начинают развиваться опухолевые клетки, места для нормальных здоровых клеток крови просто не остается. Если в случае с раком желудка пораженный участок можно удалить, вовремя провести химиотерапию и добиться длительной ремиссии, то при раке крови такая тактика не приемлема.
Есть формы острого лейкоза, которые могут развиваться с первых дней жизни человека. Хроническим формам лейкоза подвержены люди старшего возраста. Чем моложе возраст, тем агрессивнее протекает болезнь, но при современных методиках лечения больной может жить до 5–7 лет. На течение хронического миелолейкоза (и это научно доказано) большое влияние оказывает состояние нервной системы больного — если есть стрессы, депрессии, люди сгорают буквально на глазах.
Лечение лейкоза — это достаточно длительный процесс. В среднем на достижение ремиссии при острых лейкозах уходит от 3 месяцев до 2–3 лет.
Первый и самый сложный этап в лечении острого лейкоза — это интенсивная химиотерапия, с помощью которой мы должны убить опухолевые клетки. Пациенты должны находиться в специальном асептическом блоке, в котором созданы стерильные условия, чтобы исключить их контакт с любой инфекцией. Больные в этот момент не имеют никаких собственных факторов защиты, потому что кроветворение у них пострадало от самой болезни и применяемых химиопрепаратов. Для закрепления результатов терапии после этапа восстановления (или поддержки ремиссии) принимается решение о необходимости трансплантации костного мозга.
Пересадку можно делать, если пациента ввели в ремиссию. Она бывает двух видов: аутотрансплантация, когда пересаживается костный мозг самого больного, и аллотрансплантация, в этом случае ткани забирают у донора.
В первом случае у пациента из вены берется периферическая кровь, из нее при помощи сепаратора извлекают стволовые клетки, консервируют и передают на хранение в банк. Затем пациенту проводят сильнейшую химиотерапию, а следом проводят пересадку — так же, через вену, вводят стволовые клетки, и они начинают творить новое потомство. Технически это выглядит как переливание крови. Пересадка может быть сделана и при хроническом лейкозе.
Аллотрансплантация дает хорошие результаты, если доноры — родные сестра или брат, у них самый близкий фенотип. Пересадка даже от двоюродных родственников не всегда бывает столь успешна, но все равно это шанс на то, что человек будет жить.
Лучшие доноры костного мозга — это мужчины в возрасте 30–40 лет, семейные, имеющие постоянное место работы. Желательно — на промышленном производстве, на заводах. Практика показывает, что именно такие люди относятся к донорству с наибольшей ответственностью.
Женщина тоже может стать донором костного мозга. Но здесь важно учесть, что после родов и беременностей в крови у женщин циркулируют антитела, и их лейкоциты уже настроены бороться с чужеродными антигенами. Поэтому результат пересадки может оказаться хуже.
Врач-гематолог, доктор медицинских наук Сергей Семочкин про острый лимфобластный лейкоз

Врач-гематолог, профессор кафедры онкологии, гематологии и лучевой терапии РНИМУ им. Н. И. Пирогова Минздрава России, доктор медицинских наук Сергей Семочкин рассказал: можно ли распознать острый лимфобластный лейкоз (ОЛЛ) на ранней стадии и поставить диагноз по анализу крови; объяснил, как лечат ОЛЛ и кому показана трансплантация костного мозга (ТКМ).
Как правило, в анализе крови есть ярко выраженные показатели: изменены ростки кроветворения, количество лейкоцитов выходит за пределы нормы - может упасть ниже нормальных значений, а может стать запредельно огромным. Мне встречались пациенты, у которых количество лейкоцитов при норме от 4 до 9 тысяч повышалось до 200 тысяч на мкл. Тромбоциты тоже в ряде случаев очень сильно снижены, но главное – изменение количества лейкоцитов. Очень важным маркером является выход опухолевых клеток в кровь, когда в крови появляются незрелые ранние клетки, которые называют бластными. Если в анализе крови выявили бластные клетки, то это, скорее всего, либо острый лейкоз, либо миелодиспластический синдром.
Анализ крови с характерными изменениями - повод для немедленного вызова скорой помощи и госпитализации пациента в профильный стационар. При лечении детей и подростков у онкогематолога, как правило, есть один-два дня ни диагностику, лечение необходимо начинать, как можно раньше. В диагностику входит повторный анализ крови, затем – верификация диагноза, для которой проводят биопсию костного мозга. У маленьких детей ее проводят под общей анестезией, у взрослых - под местной. С помощь небольшой иглы делаю прокол грудины или подвздошной кости. У детей пункцию грудины не делают. Полученный образец костного мозга, который выглядит как обычная пробирка с кровью, отправят в лабораторию, где для подтверждения диагноза проведут целый спектр исследований. Главный критерий – увеличение количества бластных клеток. Только по внешнему виду и по количеству бластных клеток определить вариант лейкоза – невозможно. Еще в 1913 году установили, что есть лимфоидный, а есть миелоидный вариант лейкоза. Для верификации применяются специальные лабораторные методы: иммунологические и химические. Существует специальный прибор – проточный цитометр, с помощью которого определяют маркеры, характеризующие данный тип клеток. Для определения подвида острого лейкоза, применяют целый спектр генетических исследований, чтобы выйти на более целевую терапию у этих пациентов.
Истинную причину возникновения лейкоза у взрослых можно выявить только в 5% случаев, в 95% совершенно непонятно, что там к чему привело. У детей все несколько интересней.
Как возникает лейкоз? В генетическом материале клетки возникает некая первичная мутация, которая сама по себе далеко не всегда приводит к лейкозу. В дальнейшем к этой мутации присоединяются другие, и когда болезнь все же возникает, в клетке накоплено уже много молекулярных событий, сочетание которых привело возникновению заболевания. Пик острого лимфобластного лейкоза приходится на детей от двух до четырех лет, потом заболеваемость падает. Следующий пик приходится на 18-29 лет, потом снова спад. После 60 лет - опять небольшой рост.
У части детей раннего возраста прослеживается некая врожденная составляющая этой проблемы. Встречаются случаи ОЛЛ у плода или новорожденного, когда ребенок рождается уже с заболеванием, либо заболевает в течение первого года жизни. Исследования пуповинной крови показали, что у новорожденных встречаются лейкемические поломки, врожденные мутации, которые могут привести к возникновению лейкоза. И мутацию эту вызывает наследственный фактор, сработавший во время внутриутробного развития. По разным данным, общее количество таких младенцев составляет от 1 до 5%. Дальше многое зависит от инфекционной обстановки, сложившейся вокруг ребенка. Многочисленные инфекции, перенесенные в детстве, способствуют формированию нормальной иммунной системы, которая нейтрализует наследственный фактор.
Если говорить про экологические проблемы, то с ними четкой связи не выявлено.
В Хиросиме и Нагасаки повышенная заболеваемость держалась около 12 лет. После Чернобыля у многих пострадала щитовидная железа, но заболеваемость лейкозами не выросла. Все зависит от типа изотопов попавших в окружающую среду. В Фукусиме тоже этого не случилось, потому что концентрация радиоактивных веществ сильно разбавилась морской водой.
Вред ультрафиолета научно доказан только в отношении меланомы. Четкой связи с ОЛЛ нет. Своим бывшим пациентам мы не разрешаем посещать солярий и не рекомендуем загорать, потому что хотя связь и не доказана, совсем исключать этот фактор тоже нельзя.
Если говорить об СВЧ-излучении, домашние микроволновые печи абсолютно безопасны.
В отличие от острого миелоидного лейкоза, показаний к аллогенной (от донора) ТКМ меньше. Ее назначают пациентам, которые не достигли ремиссии в указанные протоколом сроки или имеют неблагоприятный цитогенетический вариант заболевания. В детской практике выздоравливают более 90% детей, и примерно 15-20% являются кандидатами для аллогенной ТКМ. У взрослых процент пациентов нуждающихся в трансплантации несколько выше, за счет того, что генетических операций высокого риска становится намного больше и ответ на стандартное лечение хуже. Когда мы обсуждали хронический миелолейкоз, там фигурировала филадельфийская хромосома - транслокация (9;22). При ОЛЛ это абсолютно негативный фактор прогноза. У детей такая мутация встречается меньше чем в 5% случаев, у людей старше 50-60 лет примерно половина В-линейных ОЛЛ будет с филадельфийской хромосомой. В отличие от хронического миелолейкоза, применение ингибиторов тирозинкиназы при остром лимфобластном лейкозе не столь успешно. Вот поэтому во взрослой практике ТКМ необходимо проводить примерно 30% пациентов. Возрастной порог для аллогенной ТКМ - в районе 55 лет, это разумно.
Если мы говорим про взрослых людей, то рецидивы случаются почти в 40% случаев. Бывают ранние рецидивы, которые случаются прямо на терапии. В таком случае необходимо менять лечение, делать его более интенсивным и тяжелым. В таких случаях, как правило, показана ТКМ. Поздний рецидив может случиться и через 20 лет. К сожалению мы не можем убрать причину, которая вызывает это заболевание - оно может вернуться.
Длительная химиотерапия нарушает фертильность, поэтому лучше провести криоконсервацию спермы/яйцеклетки, а еще лучше эмбриона - это более надежный способ. У мужчин, как правило, серьезно нарушается сперматогенез, но у женщин дело обстоит несколько лучше. Вероятность забеременеть и выносить здорового ребенка высока. Если прошло не менее пяти лет в ремиссии, никаких ограничений нет.
Скорее, нет. Это не такое частое явление, как при некоторых других заболеваниях, где беременность действительно может стать провоцирующим фактором.
Лимфобластный лейкоз – редкое заболевание, поэтому вероятность того, что он случится у ребенка, рожденного от родителей после ОЛЛ, крайне мала.
Представляется, что в основе лечения онкологических заболеваний в будущем станет активация собственного иммунитета. Нам необходимо настроить иммунную систему таким образом, чтобы она распознавала и убирала раковые клетки. Сейчас мы находимся на раннем этапе развития CAR-T-терапии, но через какое-то время технологии настолько усовершенствуются, что, скорее всего, она станет одним из основных методов терапии при целом ряде онкогематологических заболеваний. Суть метода заключается в том, что у пациента собирают его собственные Т-лимфоциты и отправляют в специальную лабораторию. Эта лаборатория может быть в другом городе, стране - не важно. В лаборатории эти Т-лимфоциты перепрограммируются: в них появляется информация об опухолевых клетках, присутствующих в организме пациента. После перепрограммирования Т-лимфоциты вводят обратно пациенту, она находят раковые клетки и возникает ремиссия. Основные проблемы – создать качественный процесс распознавания и разработать стандартные протоколы лечения.
Много вопросов возникает в понимания биологии заболевания, потому как каждый конкретный случай весьма индивидуален. Мы знакомы только с грубыми поломками, но каждая отдельная поломка провоцирует различное течение болезни. Мы уже сейчас можем полностью секвенировать геном опухолевой клетки и главное научиться понимать, что в патогенезе является ключевым и как на это можно воздействовать, тогда мы ближе подойдем к полному излечению болезни. За этим будущее.
Читайте также:

