Постлучевой некроз опухоли головного мозга

Лучевой (радиационный) некроз, представляющий собой очаговое структурное поражение в месте локализации опухоли, является отдаленным осложнением со стороны центральной нервной системы (ЦНС) после радиотерапии либо радиохирургии.
Отек тканей и присутствие новообразования вызывают в паренхиме органов ЦНС, находящейся в ложе опухоли, изменения, которые повышают вероятность развития лучевого некроза. Радиационный некроз может возникнуть в том случае, когда радиотерапия назначается по поводу первичных новообразований ЦНС, метастатических поражений головного мозга либо опухолей головы и шеи. Лучевой некроз может развиться после любого применения ионизирующего излучения для лечения опухолей или использования любого протокола такого лечения.
Диагностика лучевого некроза и его лечение представляют значительные трудности, поскольку проявления этого осложнения радиотерапии часто перекрываются симптомами рецидива опухоли. Ошибочный диагноз (рецидив новообразования вместо лучевого некроза) может стать причиной назначения неправильного лечения, способного представлять опасность для жизни пациента.
Симптомы лучевого некроза
Нужно понимать, что лучевой некроз является отдаленным осложнением радиотерапии, развитие которого нередко происходит месяцы, а то и годы спустя после завершения лечения ионизирующим излучением. Чаще всего он проявляется в период от 6 месяцев до 2 лет после завершения последнего курса радиотерапии.
В современной медицинской литературе встречаются данные о частоте развития лучевого некроза, которые отличаются значительной вариативностью – от 5% до 37% всех пациентов, получавших радиотерапию по поводу внутричерепных опухолей.
При этом некоторые авторы сообщают о том, что до 10% всех случаев этого осложнения радиотерапии были бессимптомными и выявление лучевого некроза в подобных случаях целиком является заслугой прогресса в методах нейровизуализации. Лечащим врачам необходимо принимать во внимание возможное отсутствие симптомов лучевого некроза у больных, несмотря на развитие патологического процесса.
В тех случаях, когда развитие лучевого некроза все же сопровождается симптоматикой, у пациентов чаще всего наблюдаются следующие признаки:
- головная боль;
- тошнота;
- когнитивные нарушения;
- судорожные припадки;
- очаговая неврологическая симптоматика, связанная с локализацией очага некроза;
- изменение личности;
- апатия;
- гемипарез.
Мозговые кровоизлияния при лучевом некрозе явление редкое, но, тем не менее, встречающееся в практике нейроонкологов.
Лучевой некроз: диагностика
МРТ является наиболее распространенным методом диагностики лучевого некроза. Однако при этом нужно отметить, что изображения ЛН, полученные с помощью этого метода, очень часто напоминают картину рецидива опухоли – с увеличением контрастности в пораженном участке и отеком, расположенным по периферии патологического очага.
В результате из-за низкой прогностической ценности обычной МРТ большее значение приобрели более современные методы диагностики:
- магнитно-резонансная спектроскопия;
- перфузионная МРТ;
- позитронно-эмиссионная томография (ПЭТ).
Диагностика лучевого некроза с помощью первого из этих методов (магнитно-резонансной спектроскопии) основана на том, что жизнеспособная опухоль обладает ненарушенной сосудистой системой, вследствие чего объем кровотока в ней больше по сравнению с некротической тканью.
Для дифференциального диагноза в этом случае используется показатель относительного церебрального объема крови, полученный с помощью динамической контрастной МРТ. При опухолях этот показатель выше по сравнению с лучевым некрозом.
Оценка состава метаболитов в метастатической опухоли головного мозга с помощью магнитно-резонансной спектроскопии является еще одним ценным методом дифференциальной диагностики. Повышенные показатели соотношения холин/креатинин и холин/N-ацетиласпартат могут свидетельствовать в пользу рецидива опухоли, а не лучевого некроза.
Перспективным направлением в дифференциальной диагностике лучевого некроза можно назвать и ПЭТ с фтортирозином. Некоторые авторы сообщают о чувствительности этого метода в 100% и специфичности 93% при диагностике ЛН.
Что же касается использования гистологического исследования для диагностики лучевого некроза, то надо подчеркнуть, что объем биоптата должен быть таким, чтобы иметь возможность полностью исключить рецидив опухоли и вместе с тем не вызвать клинически значимого неврологического дефицита. При заборе биоптата следует избегать нарушения целостности структур мозга, расположенных в глубине центральной части таламуса, двигательной области коры головного мозга, затылочной области и центров речи.
Обычно в образцах ткани, пораженной некрозом, не обнаруживается преобладание злокачественных клеток. Вместе с тем, ткани облученной опухоли могут содержать некротизированные участки, что не всегда указывает на лучевой некроз.
При лучевом некрозе исследование биоптата может выявлять утолщение кровеносных сосудов с пролиферацией эндотелия и/или гиалинизацию с фиброзом и умеренной инфильтрацией лимфоцитов и макрофагов.
Лучевой некроз: лечение
Для эффективного лечения лучевого некроза первостепенное значение имеет правильно поставленный диагноз, так как ошибочный диагноз рецидива опухоли и последующее противоопухолевое лечение могут привести к нежелательным тяжелым последствиям.
В отношении пациентов без симптомов лучевого некроза, у которых в период наблюдения с помощью МРТ выявляется некротическая масса, может быть избрана выжидательная тактика. Если выбор стратегии лечения не зависит от того, выявлен ли у больного лучевой некроз или рецидив глиомы, состояние такого больного нужно контролировать с помощью серии МРТ.
Однако тактика лечения должна быть другой при наличии таких симптомов как синдром объемного образования в полости черепа, повышенное внутричерепное давление, неврологические нарушения. В подобных случаях возможно использование таких методов лечения (раздельно или в комбинации):
- назначение кортикостероидов;
- в случае неэффективности стероидов можно рассмотреть использование бевацизумаба (моноклональное антитело, которое селективно связывается с биологически активным фактором роста эндотелия сосудов (VEGF) и нейтрализует его);
- гипербарическая оксигенотерапия (подача кислорода под давлением 2-3 атм. На курс лечения: 20-30 сеансов продолжительностью 90-120 минут каждый).
Хирургическое лечение лучевого некроза имеет свои преимущества и недостатки. Удаление некротической массы способствует быстрому снижению повышенного внутричерепного давления и восстановлению неврологических функций. Вместе с тем, такая операция связана с риском серьезных осложнений и проводится в основном пациентам, у которых консервативное лечение оказалось безрезультатным.
Факторы риска лучевого некроза
К настоящему времени установлены несколько факторов риска, которые способствуют развитию лучевого некроза. По мнению ведущих специалистов в области нейроонкологии, несмотря на то, что эти факторы риска были в основном обнаружены у пациентов с артериовенозными мальформациями, которым назначалось радиохирургическое лечение, а также пациентов с глиомой, они могут быть экстраполированы и на всех больных с метастазами в головной мозг:
- объем опухоли и поглощенная доза;
- применение химиотерапии наряду с радиотерапией;
- локализация опухоли (риск развития ЛН является максимальным при облучении лобного отдела коры мозга и значительно меньшим при облучении стволовой области мозга);
- гистологические особенности опухоли.
Установлено также, что радиотерапия некоторых метастатических опухолей головного мозга связана с повышенным риском развития лучевого некроза в зависимости от формы первичной опухоли. Увеличение частоты развития ЛН наблюдается при радиотерапии метастазов в головной мозг при следующих опухолях:
- карцинома почки;
- аденокарцинома легкого;
- меланома кожи с мутацией онкогена BRAF V600;
- HER2-позитивный рак молочной железы.
Кроме того, способствует развитию лучевого некроза и повышенная индивидуальная чувствительность к действию ионизирующего излучения.
а) Терминология:
1. Сокращения:
• Лучевое повреждение (ЛП)
2. Синонимы:
• Изменения, вызванные лучевой терапией (ЛТ), химиотерапией, а также обусловленные лечением изменения
3. Определение:
• Лучевое повреждение (ЛП) может быть острым (во время или вскоре после лучевого воздействия), подострым/ранним отсроченным (обычно до 12 недель после облучения) и поздним (через несколько месяцев после завершения курса лучевой терапии)
• Термин включает собственно лучевое повреждение (отек, артериит), лучевой некроз, лейкоэнцефалопатию, минерализирующую микроангиопатию, некротизирующую лейкоэнцефалопатию, синдром задней обратимой энцефалопатии (СЗОЭ), индуцированные облучением опухоли
б) Визуализация:
1. Общие характеристики поражения головного мозга после лучевой терапии и химиотерапии:
• Лучший диагностический критерий:
о Собственно лучевое повреждение: от легкого вазогенного отека до некроза
о Лучевой некроз: негомогенный характер контрастирования очага(ов)
о Лейкоэнцефалопатия: повышение интенсивности сигнала от белого вещества (БВ) на Т2-ВИ, сохранность субкортикальных U-волокон
о Минерализующая ангиопатия: кальцификация базальных ганглиев (БГ), субкортикального БВ, атрофия
о Некротизирующая лейкоэнцефалопатия (НЛЭ): распространенный некроз БВ ± кальцификация
о СЗОЭ: отек субкортикального БВ в бассейне кровоснабжения сосудов задней циркуляции
• Локализация:
о Лучевое повреждение возникает в зоне воздействия
о Перивентрикулярное БВ особенно чувствительно к лучевому воздействию
о Субкортикальные U-волокна и мозолистое тело сохранны
2. КТ признаки поражения головного мозга после лучевой терапии и химиотерапии:
• Бесконтрастная КТ:
о Подострое/раннее отсроченное ЛП: сливные гиподенсные зоны отека в БВ
о Позднее ЛП:единичныелокальные/множественныеочагиснижения плотности в БВ
о Лейкоэнцефалопатия: симметричное снижение плотности БВ
о Минерализирующая микроангиопатия: кальцификация БГ, субкортикального БВ, атрофия о НЛЭ: распространенный некроз БВ, кальцификация
о СЗОЭ: отек субкортикального БВ в бассейне кровоснабжения сосудов задней циркуляции
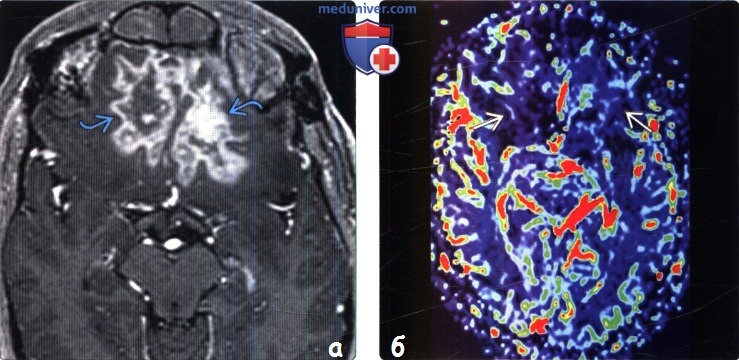
(а) МРТ, постконтрастное Т1-ВИ, аксиальный срез: у пациента, перенесшего лучевую терапию по поводу эстезиобластомы шесть месяцев назад, в нижних отделах лобных долей визуализируются объемные образования с волнообразным характером контрастирования.
(б) Перфузионная МРТ, карта rCBV: у этого же пациента не наблюдается какого-либо значимого увеличения объема мозгового кровотока в области контрастного усиления. Данные признаки характерны для лучевого некроза. Лучевой некроз может развиваться через месяцы или годы после лучевой терапии. В 85% случаев он возникает в течение двух лет.
4. Ангиография:
• Индуцированная облучением васкулопатия: прогрессирующее сужение супраклиноидных частей внутренних сонных артерий и проксимальных отделов сосудов передней циркуляции; может наблюдаться картина, характерная для мойамойа
5. Радионуклидная диагностика:
• ФДГ ПЭТ: при лучевом некрозе наблюдается гипометаболизм
• ОФЭКТ с Th-201: при лучевом некрозе наблюдается гипометаболизм, ↓ захвата радиофармпрепарата
6. Рекомендации по визуализации:
• Совет по протоколу исследования:
о При дифференциальной диагностике между ЛП и рецидивом опухоли проведите МРТ с контрастированием ± МР-спектроскопию, перфузионную МРТ, ПЭТ
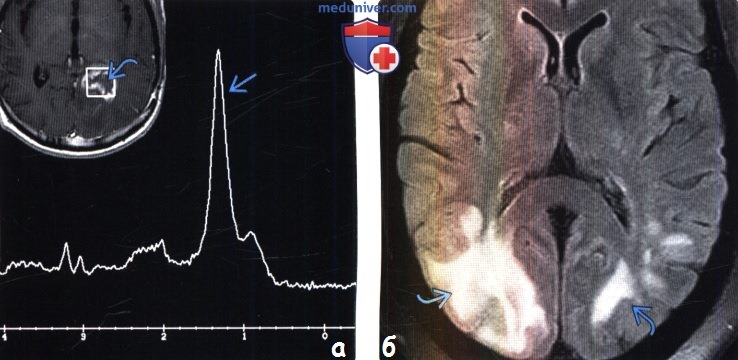
(а) Одновоксельная МР-спектроскопия, ТЕ = 35: у пациента после хирургического удаления метастазов и проведения лучевой терапии в левой теменной доле возникло поражение с некротическим компонентом, накапливающее контраст. Отмечается значительное увеличение пика липидов/лактата и уменьшение пиков других метаболитов.
(б) MPT, FLAIR, аксиальный срез: у пациента, перенесшего трансплантацию почки и находящегося на терапии циклоспорином, визуализируются характерные для СЗОЭ изменения в виде асимметричного отека коры/субкортикального белого вещества затылочных долей.
в) Дифференциальная диагностика поражения головного мозга после лучевой терапии и химиотерапии:
1. Рецидив мультиформной глиобластомы (ГБМ):
• Накапливающее контраст объемное образование с центральным некрозом и масс-эффектом
• ↑ пика Cho, ↓ пика NAA + лактат по данным МР-спектроскопии
2. Метастатическое поражение:
• Характерны множественные очаги поражения, локализующиеся на границе между серым и белым веществом, выраженный отек
• ↑ пика Cho, ↓ пика NAA ± лактат по данным МР-спектроскопии
• Объемное образование с кольцевидным характером контрастного усиления, которое может имитировать лучевой некроз
3. Абсцесс:
• Объемное образование, накапливающее контраст по типу кольца с более тонким краем на уровне желудочка
• Гипоинтенсивный на Т2-ВИ ободок, признаки ограничения диффузии
• При МР-спектроскопии определяются такие метаболиты, как сукцинат, аминокислоты
4. Рассеянный склероз:
• Часто участок контрастирования имеет незамкнутую подковообразную форму, обращенную открытой частью к коре
• Другие поражения типичной локализации, молодой возраст пациентов
5. Сосудистая деменция:
• Инфаркты крупного и малого размеров, поражение БВ
• Обычно пожилые пациенты, наличие клинического диагноза
6. Прогрессирующая мультифокальная лейкоэнцефалопатия:
• Повышение интенсивности сигнала от БВ на Т2-ВИ с вовлечением субкортикальных U-волокон
• Изменения могут пересекать мозолистое тело; контрастирование обычно не наблюдается
• Пациенты с иммуносупрессией
7. Реакция на инородное тело:
• Гранулематозная реакция (на желатиновую губку)
• Может имитировать рецидив опухоли, лучевой некроз
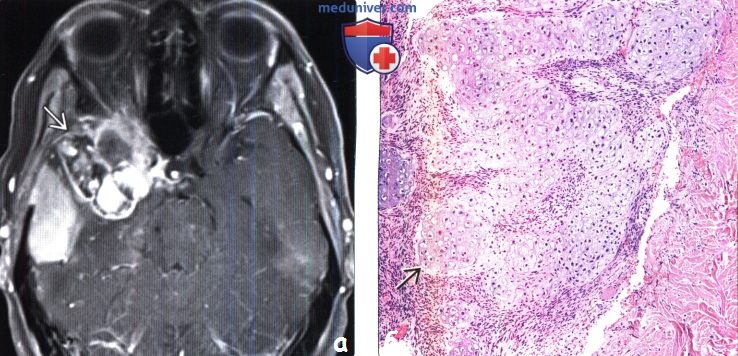
(а) МРТ, постконтрастное Т1 -ВИ, режим подавления сигнала от жира, аксиальный срез: у пациента, перенесшего оперативное и лучевое лечение по поводу менингиомы (I степень злокачественности по классификации ВОЗ [grade I]) в передних отделах средней черепной ямки определяется объемное образование гетерогенной структуры.
(б) Микропрепарат опухоли после ее повторной резекции (у этого же пациента): обнаруживаются элементы хондроскаркомы. Вторичные новообразования наблюдаются у 3-12% пациентов, перенесших курс лучевой терапии. Индуцированные облучением опухоли встречаются редко (в 3-12% случаев) и чаще всего представлены менингиомами (70%), глиомами (20%) или саркомами (10%).
г) Патология:
1. Общие характеристики поражения головного мозга после лучевой терапии и химиотерапии:
• Этиология:
о Индуцированное облучением повреждение сосудов:
- Нарушение проницаемости, повреждение эндотелия и базальной мембраны, ускоренное развитие атеросклероза, формирование телеангиэктазий
о Индуцированная облучением нейротоксичность:
- Повреждение глии и БВ (чувствительность олигодендроцитов >> нейронов)
о Индуцированные облучением опухоли (саркома):
- Более высокий риск у пациентов, которым ЛТ была проведена
Редактор: Искандер Милевски. Дата публикации: 30.4.2019
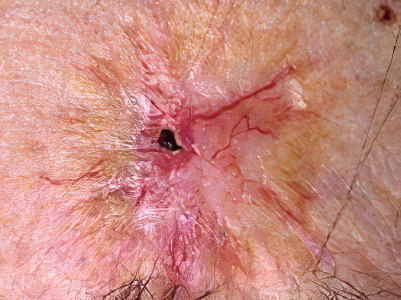
Применение ионизирующего облучения при лечении опухолей, заболеваний крови, скелета и различных органов и систем сопряжено с риском развития осложнений. Нередко люди, чья профессия связана с радиационными приборами становятся жертвой негативного воздействия высоковольтного облучения. Сроки развития некротических очагов в тканях после облучения зависят от величины дозы, объема облучаемой зоны и т. д.
Проникающая радиация способна вызывать тяжелые виды омертвений тканей. Пока механизм и характер патологических изменений от радиационного излучения полностью не изучен. Известно, что причинами возникновения лучевого некроза являются сосудистые, морфологические и дегенеративные нарушения. Не исключено также иммунодепрессивное действие ионизирующего излучения на ткани.
Облучение организма способствует подавлению ферментных систем содержащих железо и принимающих участие в дыхательном процессе тканей в аэробной фазе. Это влечет за собой образование в тканях недоокисленных продуктов обмена веществ. Лучевая терапия может вызывать поражение нервной системы и привести к появлению свободных радикалов. При гистологическом исследовании, как правило, выявляется деминерализацию нервных волокон, уплотнение ткани мелких артерий и некроз ткани головного мозга.
Нервы плечевого и пояснично-крестцового сплетения, подвержены развитию лучевого некроза одновременно с лучевым некрозом Центральной нервной системы. Лучевая болезнь – следствие действия на весь организм в целом рентгеновских гамма-лучей, потоков нейтронов. Как правило, течение болезни сопровождается некрозом. В облученных тканях подавляется регенерация, слизистая оболочка рта и губ отекает, могут возникать точечные кровотечения.
В разгаре болезни ухудшается общее состояние, изменяется трофика слизистой полости рта, наблюдается чувство жжения, анемия, сухость. Возникает лучевой стоматит. Явления геморрагического синдрома, наличие инфекции (гнилостной) провоцируют образование язв и некроза. Некроз развивается в ротовой полости, всегда наиболее выражен в области прилегания к слизистой оболочке металлических протезов и пломб, в таких местах обычно присутствует больше бактерий. Появляются признаки поражений краев десен и миндалин, за этим следует поражение боковых поверхностей языка и неба, сильный отек оболочки рта, губ и лица.
После того как край десен некротизируется, они становятся рыхлыми, кровоточащими. Размягчение костной ткани альвеолярного отростка становится причиной расшатывания и выпадения зубов. Методы терапевтических мероприятий зависят от состояния различных органов и систем. Без лечения лучевой некроз имеет объемные очаги, но под действием глюкокортикоидов, степень активного развития снижается.
Лучшим методом лечения прогрессирующего лучевого некроза является хирургическая операция. Перед любым облучением необходимо принимать препараты, замедляющие радиохимические реакции. Снижается риск негативных последствий от лучевой терапии при использовании гормональных, антигистаминных, антибактериальных средств.
Для восстановления работы кровеносной системы и предупреждения геморрагического диатеза вызывающего развитие некроза назначают рутин, викасол, глюконат кальция и поливитаминный комплекс. Если рассматривать облучение гипоталамуса и гипофиза, то после этого процесса происходят сбои в эндокринной системе. Через несколько месяцев после лучевого влияния эмаль зубов тускнеет, теряет блеск, появляются участки некроза темного цвета, образуется рыхлая некротическая масса.
Постепенно участки некроза охватывают значительную часть зуба, появляются полости с неровными изъеденными краями, выпадают пломбы. Прогрессирующий радиационный некроз поражающий твердые ткани зуба лечится в несколько этапов методом удаления разложившихся тканей и заполнения дна и стенок полости кальцифицирующей пастой. Прежде чем приступать к лучевой терапии, для уменьшения прямого действия радиации на зубы нужно надевать капу из свинца, проводить курс реминерализующей терапии и принимать антиоксиданты.
Все эти способы максимально защитят организм от негативных последствий или снизят степень возможных воздействий. Облучение внутричерепных опухолей, новообразований на голове и на шеи неблагоприятно для организма. Впоследствии могут наблюдаться некрозы мозга. Такие осложнения развиваются быстро или в течение нескольких месяцев и лет. Механизмом, запускающим развития позднего некроза центральной нервной системы, считают повреждение сосудистой сети мозга.
Для определения вероятности развития лучевого некроза мозга учитывают дозу и длительность облучения. Клинические проявления при этом виде патологи весьма разнообразны, им могут содействовать разные причины и условия. В случае развития некроза может быть полезно иссечение пораженного участка ткани.
К сожалению, ресурс человеческого здоровья является исчерпаемым, а одной из наиболее уязвимых зон является голова. Головной мозг подвержен различным заболеваниям, самые страшные из которых могут проявляться в виде опухолей, как доброкачественного, так и злокачественного характера.
Основным методом лечения таких патологий является лучевая терапия. Но нередко она приводит к такой проблеме, как лучевой некроз головного мозга – Вследствие воздействия радиации на опухоль происходит отмирание соседствующих тканей.
Немного об опухолях головного мозга

Опухоль представляет собой зону, в которой сосредоточены клетки, претерпевшие патологические изменения в процессе своего развития. В случае с головным мозгом опухоль может образовываться как непосредственно на веществе, так и вокруг него. Таким новообразованиям свойственно развитие и последующее разрушение вокруг себя здоровых клеток.
Опухоли разделяются на два вида: злокачественная и доброкачественная. Первая отличается стремительным развитием, а также созданием прямой опасности для здоровья и жизни человека. Доброкачественные новообразования развиваются медленнее и проявляют себя не столь агрессивно.
Существует две основных группы опухолей: первичные и метастатические. Первичная опухоль может быть как злокачественной, так и доброкачественной, и берет свое начало из тканей мозга. Метастатическое же новообразование бывает исключительно злокачественным, так как оно всегда является элементом опухоли другой локализации, проникшим в структуру головного мозга. То есть, метастазы – это производная развития какой-либо злокачественной опухоли.
По причине своей специфичности злокачественные опухоли подлежат детальному исследованию с медицинской стороны. Они классифицируются по степеням и стадиям, которые определяются следующими критериями:
- скорость развития раковых клеток;
- наличие участков тканей, подверженных некрозу (отмиранию);
- объем кровоснабжения опухоли;
- способность и темпы распространения злокачественных элементов на другие (здоровые) ткани;
- уровень схожести аномальных клеток с нормальными.
На сегодняшний день современная медицина не знает ответа на вопрос, откуда берется первичное новообразование, а точнее – почему это происходит. Наиболее доступным объяснением является генетическая предрасположенность и фактор окружающей среды, включающий в себя некачественные продукты питания и плохую экологию. Иногда в качестве причины возникновения опухоли головного мозга называют последствия излучений, имеющих, в том числе, терапевтическую природу, которые могли быть перенесены в детстве.
Среди симптомов, которыми проявляет себя заболевания, в первую очередь следует перечислить:
- головные боли;
- тошнота и рвота;
- зрительная и слуховая дисфункция;
- судороги;
- изменения в поведении;
- ухудшение памяти и т. д.
Как лечат опухоли головного мозга
Методика лечения опухоли определяется в зависимости от ее размеров, характера и прочих клинических факторов. Среди основных видов лечения следует перечислить:
- химиотерапия;
- хирургическое вмешательство;
- лучевая терапия;
- комбинированные методики.
Если новообразование дает осложнение в виде критического повышения внутричерепного давления, принимается решение о хирургическом вмешательстве, путем прямой резекции опухоли.
В последнее время усилия врачей, лечащих опухоли головного мозга, направлены не только на прямое воздействие на сам очаг, но и на защиту от облучения соседних тканей. Лучевая терапия может быть применена в случае с теми образованиями, на которые облучение оказывает положительное влияние.
Такой метод лечения продолжается, как правило, на протяжении нескольких недель, а в случае наличия нескольких патогенных очагов может быть принято решение об облучении всей зоны головы. Одной из негативных сторон такого облучения довольно часто становится лучевой некроз головного мозга.
Хирургическое вмешательство путем резекции происходит в случае с первичными опухолями, которые и удаляются во время операции.
Химиотерапия может применяться в качестве самостоятельного лечения, а нередко используется в комплексе с лучевой терапией. Наряду с этим, эффективность радиотерапии может быть увеличена за счет назначения радиосенсибилизирующих препаратов.
Возможные осложнения
Основным побочным эффектом такого действенного метода, как облучение, может стать лучевой некроз головного мозга. Это может случиться вследствие повреждения здоровых клеток и тканей во время лечения. Такая проблема сопровождается судорогами и сильными головными болями, а в некоторых случаях может наступать смерть пациента.
Лучевой некроз головного мозга может развиваться на протяжении от полугода до нескольких лет. Сегодняшняя статистика указывает на тенденцию уменьшения случаев с некрозом, причиной чему являются новые достижения в медицинской сфере.
В качестве осложнений после лучевой терапии можно перечислить рецидив опухоли и различные неврологические расстройства.
При лечении детей посредством излучения могут возникать нарушения в различных отделах мозга, включая гипофиз, что напрямую отражается на их последующем развитии. Поэтому сегодняшней целью является замена радиотерапии в случаях с детскими опухолями на лечение химиотерапевтическими препаратами.
В нашей статье мы кратко коснулись видов существующих опухолей, их классификаций и возможных причин возникновения. Также мы рассмотрели основные методы лечения доброкачественных и злокачественных новообразований.
Как и в любых других случаях с серьезными заболеваниями, радикальные методы лечения имеют свои риски, осложнения и последствия. В статье мы обговорили лучевой некроз головного мозга, что это такое и в виде каких признаков может проявляться такая проблема.
В свете прогрессивно развивающейся медицины появляется надежда на то, что год от года будет уменьшаться не только число прецедентов с побочными эффектами после лечения, но количество самих случаев заболевания.

Американские исследователи сообщают, что препарат бевацизумаб (Avastin) уменьшает степень некроза тканей мозга у пациентов, которые подвергаются облучению по поводу рака мозга.
Точно известно, что существует значительный риск радиационного некроза тканей мозга при стереотаксической радиохирургии по поводу мультиформной глиобластомы.
Ранее предпринималось множество попыток уменьшить степень радиационного некроза мозга при помощи самых разных препаратов. Но результаты, полученные исследователями из Мичигана, впечатляют.
Только у 6% пациентов при адъювантной терапии бевацизумабом и у 3% пациентов при сопутствующем приеме препарата развивался некроз тканей мозга после облучения. Это хороший результат по сравнению с пациентами, которые не получали данный препарат – здесь некроз тканей мозга возникал в половине случаев (P
Новые технологии, похоже, коснулись всех аспектов нашей жизни: как мы ведем себя в обществе, как мы ведем дела, как выбираем наше правительство, и т.п. Но насколько очевидно, что эти новые технологии оказывают влияние и на то, как мы думаем? Изменяется ли под воздействием этих технологий сам мозг на.

Мозговая аневризма представляет собой патологические выпячивание стенки одного из сосудов мозга. Крупная аневризма на сосуде может выглядеть как округлый плод, висящий на веточке. Мозговая аневризма очень опасна, она может разрываться, давать течь, что приводит к кровоизлиянию в мозг (геморрагич.

Понятие глиомы охватывает широкую группу первичных опухолей головного и спинного мозга, которые возникают из глиальных клеток – основных клеток мозга. Симптомы, прогноз и лечение злокачественной глиомы зависят от возраста больного, конкретного типа опухоли, ее расположения в мозге.

Нейробиолог из Швейцарского Федерального Технологического Института планирует построить мозг человека и описывает последовательность шагов, необходимых для создания полной виртуальной модели мозга человека, на котором будет возможным проведение разнообразных экспериментов, которых нельзя провести на.

Метастатические опухоли мозга превосходят по частоте возникновения первичные опухоли приблизительно в 10 раз (!). Метастазы в мозг наблюдаются почти у 20% онкологических больных. Даже в Соединенных Штатах не ведется детальная статистика метастатических опухолей мозга, поэтому их точная ч.

Опухоли мозга являются, к сожалению, распространенным онкологическим заболеванием. Они составляют, по разным данным, от 80% до 90% всех первичных опухолей центральной нервной системы. По данным исследований SEER, в США в конце 1990-х годов первичные инвазивные опухоли ЦНС ежегодно регистриро.

От табачной зависимости страдают миллионы жителей нашей планеты. Американские ученые создали вакцину, которая поможет избавиться от этой вредной привычки.
Компания Selecta Biosciences, в которой работают специалисты из Гарвардского и Массачусетского университетов, приступила к клиничес.
- Новые
- Популярные
Протонная терапия опухолей мозга является новой разновидностью лучевой.
Предлагаем вашему вниманию научные данные об эффективности гомеопатии .
Популяризация щелочной диеты и приема питьевой соды для лечения и проф.
Вопрос использования витаминов для лечения и профилактики онкологическ.
Арсенал иммунотерапии меланомы включает анти-PD-1 и анти-CTLA-4 препар.
Читайте также:


