Постлучевой эпителиит при раке шейки матки
Лучевую терапию (ЛТ) обычно применяют для лечения рака шейки матки (РШМ) и злокачественных новообразований влагалища (иногда — диссеминированиого рака вульвы), а также в качестве адъювантной терапии у больных с высоким риском рака эндометрия (РЭ).
Индивидуальный подход к лучевой терапии (ЛТ) может быть применен практически при любых злокачественных новообразованиях женских половых органов, чтобы достичь временного облегчения. Осложнения после адекватной лучевой терапии (ЛТ) у больных раком шейки матки (РШМ) и раком влагалища обычно минимальны.
Однако, к сожалению, существует неправильное представление о частоте осложнений после лучевой терапии (ЛТ) как у медицинского персонала, так и у населения в целом. Можно предположить несколько источников происхождения такого мнения.
Во-первых, многие исследователи не понимают, что нежелательные побочные эффекты есть следствие неправильной техники терапии, и не должны экстраполировать их на адекватное использование методик лучевой терапии (ЛТ).
Во-вторых, осложнения лучевой терапии (ЛТ), как правило, отмечаются у неоперабельных больных с обширным опухолевым процессом.

Результаты лучевой терапии (ЛТ) в этих случаях не могут быть экстраполированы на применение оптимальных методик при местно-распространенных новообразованиях. Наконец, часто игнорируется тот факт, что большинство осложнений, приписываемых облучению, на самом деле есть результат неконтролируемого опухолевого процесса (например, прямокишечно-влагалищные и пузырно-влагалищные свищи).
Поскольку тонкая кишка, мочевой пузырь и прямая кишка примыкают к женским половым органам, большинство побочных эффектов и осложнений после лучевой терапии (ЛТ) связано с этими прилегающими органами. Осложнения, вызванные ЛТ, зависят от дозы, размера облучаемого поля и типа использованного оборудования. При неизменной дозе чем больше поле, тем больше риск осложнений. Как правило, при увеличении размера поля дозу снижают.
И наоборот, если поле уменьшается, можно использовать более высокую дозу. Применение брахитерапии также увеличивает риск местных осложнений. Наконец, по-видимому, использование комбинированной XT и ЛТ несколько увеличивает риск некоторых осложнений (например, нейтропении), но не приводит к серьезным отдаленным последствиям.
Осложнения, индуцированные лучевой терапией (ЛТ), можно разделить на острые и отсроченные. Осложнения лучевой терапии (ЛТ) вызываются ионизирующим и лучевым повреждением клеток, которые имеют митотическую активность, например желудочно-кишечный эпителий. Разрушение клеток слизистой оболочки приводит к ее истончению и обнажению, что сопровождается нарушением всасывания и потерей жидкости и электролитов (вследствие диареи).
Стволовые клетки слизистой оболочки ЖКТ, как правило, полностью восстанавливаются, и острые симптомы исчезают. Поздние осложнения могут быть вызваны различными механизмами тканевого нарушения, основанного на повреждении эндотелия. Облучение приводит к эндартерииту и постепенной закупорке мелких сосудов, последующая тканевая гипоксия — к фиброзу пораженных тканей.
Эти изменения прогрессируют и могут усугубляться в дальнейшем другими факторами поражения сосудов, такими как диабет, артериальная гипертензия и возрастные изменения сосудов. В тяжелых случаях можно обнаружить изъязвление, стриктуры, перфорацию и образование свищей.
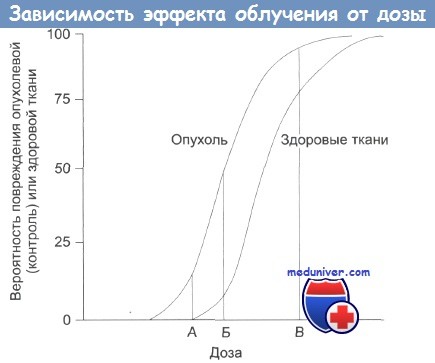
Зависимость терапевтического эффекта от дозы облучения.
А — нижняя безопасная доза;
Б — увеличение дозы: растет поражение здоровых тканей;
В — наивысшая вероятность успешного лечения, но и высокая вероятность поражения здоровых тканей, многочисленные побочные эффекты, некоторые из которых могут проявиться в отдаленном будущем

Влияние ионизирующего излучения на эпителий шейки матки может продолжаться в течение нескольких лет, после проведенного лечения у 20% больных радиационные изменения развиваются в течение 3 лет, однако имеются сообщении об их присутствии и через 20 лет (Титмушш Э., Адамс К., 2009).
Под действием облучения тканей изменения наблюдаются как в клетках опухоли, так и в неизмененных клетках. При исследовании цитологических препаратов женщин, пришедших на контрольный осмотр в различные сроки после лучевой терапии, большое значение имеет обнаружение клеточных элементов, свидетельствующих о продолжающемся росте опухоли или нечувствительности клеток рака к радиации. В некоторых случаях дифференциальный диагноз клеточных изменений при лучевом патоморфозе и рецидиве рака затруднен.
Цель исследования – изучить клеточные изменения в мазках с шейки матки после лучевой терапии для дифференциальной диагностики лучевого патоморфоза и рецидива рака.
Результаты исследования. Плоскоклеточный рак был диагностирован у 223 (70,2%) женщин, аденокарцинома – у 95 (29,8%).
Независимо от формы рака в цитологических препаратах после лучевой терапии наблюдаются дистрофические изменения в клетках. При изменении клеток плоскоклеточного рака при лучевой терапии сохраняются признаки ороговения цитоплазмы, нарастает количество гигантских многоядерных клеток. Для аденокарциномы изменения при лучевой терапии менее выражены. В клетках сохранившихся комплексов аденокарциномы нарастает ядерный полиморфизм, выражена вакуолизация ядер и цитоплазмы, наблюдается пикноз ядер.
В клетках плоского эпителия в отличие от злокачественных элементов происходит увеличение и ядра, и цитоплазмы в одинаковой пропорции, ядерно-цитоплазматическое соотношение остается неизменным.
Изменения эпителия при лучевой терапии у 14 (4,4%) женщин при контрольном осмотре вызывали затруднения в определении процесса: при цитологическом диагнозе дифференцировали лучевой патоморфоз и рецидив рака. У 4 из них при повторном заборе материала на исследование дифференциальный диагноз расценен в пользу лучевого патоморфоза. С учетом изученной информации остальные 10 из 14 пациенток продолжили лучевую терапию в сроки после первичного лечения от 8 мес до 11 лет. Клеточные элементы, свидетельствующие о продолжающемся росте опухоли, состояли из отдельных клеток и комплексов с крупными округлыми ядрами, четким ядерным краем, равномерным мелкопетлистым хроматином, резко базофильной цитоплазмой.
Выводы
1. Изменения эпителия при лучевой терапии женщин, расцененные как лучевой патоморфоз, по нашим данным наблюдаются в сроки от 8 мес до 15 лет.
3. Трудности дифференциальной диагностики при цитологическом диагнозе лучевого патоморфоза и рецидива рака возникали у 4,4% пациентов.
4. Для рецидива рака характерны комплексы клеток с крупными округлыми ядрами, четким ядерным краем, равномерным мелкопетлистым хроматином, резко базофильной цитоплазмой.
5. Клеточные изменения при аденокарциноме при лучевой терапии менее выражены, чем при плоскоклеточном раке.
Консультации врачей (в том числе онкологов) - здесь и здесь
Выгодные аптеки (низкие цены, дефицитные лекарства) - аптека №1, аптека №2
Онлайн-сервис по поиску клиник, врачей и записи к ним

Необходима консультация лечащего врача.
ЛУЧЕВЫЕ ПОВРЕЖДЕНИЯ тканей и органов возникают в результате воздействия ионизирующего излучения. Наиболее часто развиваются при облучении ограниченных участков тела. Тяжесть любых Л. п. увеличивается с повышением поглощенной дозы ионизирующего излучения.
При раке влагалища в основном показано внутриполостное облучение, которое у больных II-III стадий остается с дистанционным облучением зон местного распространения и регионарного лимфогенного метастазирования. Эндовагинальное облучение требует большого врачебного искусства, чтобы получить максимум эффекта и минимум лучевых осложнений.Это возможно только при строгом расположении аппликаторов в соответствии с формой опухоли. Особые трудности лучевой терапии наблюдаются в случае расположения опухоли в нижних двух третях влагалища. В таких случаях используются восковые маски и муляжи, куда помещаются радиоактивные препрараты.В последние годы для лечения рака влагалища применяются источники повышенной мощности дозы излучения с короткой экспозицией.
По времени проявления и особенностям клин, течения различают острые (ранние) и отдаленные во времени (поздние) Л. п. Острые местные Л. п. чаще всего возникают в результате аварийных ситуаций при массивном, обычно однократном облучении. Они проявляются в виде ожогов кожи, напоминающих термические ожоги и отличающихся от них тем, что лучевые ожоги кожи развиваются не сразу после воздействия, а спустя нек-рое время (латентный период). Длительность латентного периода сокращается с увеличением дозы ионизирующего излучения, т. е. она обратно пропорциональна этой дозе. Отдаленные во времени Л. п. чаще всего являются последствиями лучевой терапии злокачественных опухолей и реже результатом длительного профессионального облучения (так наз. хронические Л. п. ). Клин, картина Л. п. независимо от того, каким видом ионизирующего излучения они вызваны, обусловливается, кроме дозы ионизирующего излучения, ее распределением во времени, а также объемом облученных тканей и локализацией повреждения.
Для профилактики и лечения ранних Л. п. (эритемы, сухого эпидермита) эффективны аппликации 10% р-ра димексида. При влажном сливном эпителиите и дерматите следует применять повязки с витаминизированными маслами (облепиховое масло, масло шиповника и др. ), а также дибунол, олазол, ируксол, левосин, метилурациловую мазь и др. Полезно применение кортикостероидных мазей (преднизолоновой мази, локакортена, синалара, деперзолона, дермазолона). При лечении лучевого фиброза кожи целесообразны аппликации или электрофорез с 10-30% р-ром димексида, а также с лидазой (ронидазой) и препаратами глюкокортикостероидов. Лечение лучевых язв кожи проводят в соответствии с общехирургическими принципами. В фазе некробиоза и экссудации применяют антисептические р-ры (0, 5% р-р хлорамина, р-р фурацилина 1: 1000, 1% р-р перекиси водорода, 5-10% р-р димексида) в сочетании с некротомией. По мере очищения язвы и появления грануляций переходят к применению повязок с мазевыми композициями. В лечении поздних лучевых язв кожи используют также радикальное иссечение поврежденных тканей с последующим замещением дефекта кожным лоскутом (применяют кожную пластику расщепленным кожным лоскутом, филатовским стеблем и др. ). Перспективной является пластика дефекта кожно-мышечным трансплантатом с микрохирургическим восстановлением кровоснабжения.
Лечение остеорадионекроза консервативное с назначением по показаниям анаболических стероидов (напр., ретаболила) в сочетании с препаратами кальция. Лечение лучевого остеомиелита оперативное - резекция поврежденной кости. При Л. п. внутренних органов применяют препараты, оказывающие противовоспалительное действие, в частности димексид. Местное лечение Л. п. всегда сочетают с терапевтическими мероприятиями, направленными на нормализацию нарушенных функций организма.
Профилактика Л. п. и возникновения повторных злокачественных новообразований радиационного происхождения предусматривает также максимальное снижение лучевых нагрузок с помощью Радиомодифицирующих агентов, избирательно усиливающих действие ионизирующего излучения на ткань опухоли и ослабляющих лучевое поражение окружающих нормальных тканей.
Что такое лучевая терапия?
Лучевая или радиотерапия оказывает действие на патологические ткани посредством ионизирующего облучения. Именно оно и блокирует деление и распространение пораженных раком клеток в теле женщины. Пучок элементарных частиц формируется посредством медицинских ускорителей. В процессе облучения пораженные патологией ткани не распадаются, однако терапия видоизменяет их ДНК, тем самым притормаживая деление злокачественных клеток.
Вдобавок курс лучевой терапии при раке шейки матки приводит к разрыву молекулярных связей в патологических тканях. Трансформации подвергаются сугубо атипичные клетки, а здоровые структуры остаются незатронутыми. Особенность процедуры лучевой терапии при раке шейки матки – это систематическое изменение направления излучения. Такой подход позволяет сконцентрировать максимум облучения в очаге патологии.
Несмотря на то, что радиотерапию считают отдельным методом коррекции недуга, однако она может быть дополнением к оперативному вмешательству. К тому же очень важное место отводится лучевой терапии в борьбе с метастазами, а также в облегчении болей у пациенток на терминальных стадиях недуга. Методики операции
При такой патологии специалисты могут назначать:
- гамма-терапию;
- рентгенотерапию.
Если же рассматривать положение аппарата по отношению к больной, то может использоваться:
- контактный метод;
- внутриполостное облучение;
- внутритканевая радиотерапия;
- дистанционное действие на образование.
Также радиотерапия может быть внешней и внутренней. Как правило, для борьбы с опухолью используют сразу два типа воздействия. Лишь в редких случаях уместен сугубо внешний или внутренний метод облучения.
Как процедуры проводятся
Специалист при принятии решения — раковый очаг выявлен, и его необходимо лечить, ориентируется на структуру опухоли, злокачественный ли он, размеры, возрастная категория больного.
Учитывается и тот факт, что радиоактивные лучи представляют непосредственную угрозу для не пораженных атипией тканей. Подобная терапия обязательно проводится в несколько этапов — с перерывами в несколько недель между процедурами. По потребности, отдельные процедуры применяются для воздействия на определенные участки.
Предварительная настройка оборудования – обязательный этап. Осуществляется тщательный подбор правильности направленности лучей, для точного попадания на опухолевый очаг. После выполнения ряда снимков, информация выводится на экран, и специалист выявляет локализацию карциномы, ее границы, вычисляет нагрузку лучевой терапии.
Затем система аппарата сама будет руководить процессом размещения и последующего поворота пациента, самого излучателя, а также настраивает положение защитных устройств. Если на снимках были четко обозначены контуры новообразования, то лазерный луч будет высвечивать на теле облучаемого точку непосредственного воздействия.
Несколько сложнее если злокачественное поражение переместилось на соседние ткани и органы. Однако, современное оборудование облегчает задачу специалистов – томографы позволяют получать трехмерное изображение опухоли с последующим оставление программы лучевого воздействия.
Наружная форма облучения
Подобная форма лучевой терапии особенно действенна при терапии на терминальных стадиях и существенно помогает улучшить состояние пациентки. Курс внешней радиотерапии способствует прекращению кровотечений и помогает обезболить область таза. Внешняя радиотерапия обычно продолжается 5-6 недель и проходит в стационаре.
Перед процедурой пациентка проходит комплексное обследование для точного выявления локализации образования. Затем, перед облучением, на кожных покровах женщины проводят маркировку – она нужна для более точной направленности излучения аппарата. Сеансы проводятся 5 раз в неделю, а их длительность не превышает 2-3 минуты.
Радиотерапия не провоцирует болевого синдрома. И существует лишь одно правило, что должно неукоснительно соблюдаться – это полная обездвиженность тела при процедуре. Если в силу каких-то причин женщина пропустила один из сеансов, то можно провести две процедуры облучения в один день с интервалом в 6-8 часов. Но только лечащий врач решает насколько это уместно.
Цены на курс химиотерапии в Европейской клинике
- Консультация химиотерапевта — 6 900 руб.
- Проведение внутрипузырной химиотерапии (без стоимости лекарственных препаратов) — 21 500 руб.
- Проведение внутрибрюшинной химиотерапии (без стоимости лекарственных препаратов) — 19 100 руб.
- Проведение иммунотерапии (без стоимости лекарственных препаратов) — 15 000 руб.
- Проведение интратекальной химиотерапии — 21 000 руб.
- Проведение гипертермической интраперитонеальной химиотерапии — 280 000 руб.
- Проведение химиотерапии с использованием инфузионной помпы 1 сутки (без стоимости лекарственных препаратов) — 17 900 руб.
- Проведение анти PD-1 терапии — 334 000 руб.
Запись на консультацию круглосуточно
Внутренняя форма облучения
Такой тип терапии тоже проводят лишь в амбулатории. Чтобы добиться позитивного эффекта от радиотерапии, в шейку или полость матки внедряются аппликаторы, посредством которых и проводят облучение. Введение трубки в маточную полость матки проводится лишь после предварительной анестезии. Но и в дальнейшем женщине приходится пить анальгетики.
Во избежание смещения трубки, во влагалище больной помещают еще и тампон из марли. До начала терапии врач назначает КТ, для оценки правильности размещения аппликатора. Внутреннее облучение могут проводить либо одним длительным курсом или же несколькими непродолжительными. Длительность терапии определяется доктором.
Как правило, внутреннюю лучевую терапию проводят с применением низких, высоких или импульсных доз облучения. Но, как правило, зачастую применяются высокие дозы облучения. Процедуры проходят с интервалом в 2-3 дня, а их продолжительность не превышает 10 минут. В перерывах между сеансами трубку могут удалять из полости или шейки.
Стадии рака матки
Лечение рака матки зависит от его типа. Для определения стадии заболевания назначаются рентген грудной клетки, компьютерная томография (КТ), позитронно-эмиссионная томографии (ПЭТ) и анализы крови. В некоторых случаях стадия окончательно определяется уже после операции.
- На 1 стадии лечение рака матки ограничивается терапией в полости матки. Злокачественные клетки не обнаружены в других областях.
- На 2 стадии раковые клетки присутствуют также еще и в шейке матки.
- На 3 стадии опухоль распространяется за пределы матки, но не затрагивает прямую кишку и мочевой пузырь. Болезнь может поражать лимфоузлы в области малого таза.
- На 4 стадии заболевание может уже затрагивать мочевой пузырь и прямую кишку. Возможно появление метастазов в других частях тела (чаще всего в легких)
Эффективность лучевой терапии
Естественно, радиотерапия не дает полной гарантии выздоровления после онкологии шейки матки, но эффективность сеансов лучевой терапии довольно высока и демонстрирует позитивные результаты. Процедура помогает минимизации рисков появления вторичных очагов, а риск рецидива появляется лишь через 20 лет после прохождения радиотерапии.
Лучевая терапия помогает добиться следующих положительных эффектов:
- уменьшение болевых ощущений;
- ликвидация остаточных раковых структур;
- сводит к минимуму риск метастазов в близлежащих тканях;
- дает шанс полного излечения онкологической патологии на ранних стадиях.
Поскольку эффективность лучевой терапии при раке шейки матки довольно высока, то ей отводят довольно важную роль в лечении патологии. Так, после оперативного устранения образования на I стадии недуга радиотерапия используется в качестве дополнения к операции. На II-III стадии лучевуя терапия – единственная возможная лечебная альтернатива. Что же до терминальной IV стадии недуга, то в этом случае процедура имеет паллиативную направленность и обеспечивает лишь облегчение состояния пациентки.
Причины
Рак шейки матки развивается в результате диспластических изменений. В действительности дисплазия подразумевает предраковое состояние.
Под диспластическим процессом подразумевают изменения структуры клеток, касающиеся нарушения их созревания и дифференцировки. Известно, что в норме клетки располагаются в трех слоях плоского эпителия. При дисплазии возникают последствия в виде изменения формы и структуры клеток, исчезновения деления на слои.
Предраковый процесс имеет несколько степеней течения:
- поражение 1/3 эпителия (CIN I),
- вовлечение половины толщи эпителиальной ткани (CIN II),
- обнаружение атипичных клеток во всём эпителиальном слое (CIN III).
- округлые клетки становятся бесформенными,
- количество ядер увеличивается,
- деление на слои исчезает.
Если атипичные клетки приобретают способность к интенсивному размножению и прорастанию в окружающие ткани, развивается последствие в виде рака.
Основной причиной появления диспластических изменений становится заражение ВПЧ. Науке известно более ста штаммов вируса, однако, только некоторые отличаются высокой степенью онкогенности и способностью вызывать рак. Например, обычно рак шейки матки вызывают штаммы 16 или 18. Некоторые штаммы оказывают не трансформирующее, а продуктивное действие, что выражается в образовании папиллом, кондилом.
Однако при наличии опасных штаммов рак развивается, если в анамнезе у пациентки существуют сопутствующие патологии. Здоровый иммунитет выводит вирус из организма в течение нескольких месяцев.
Последствия в виде рака развиваются при следующих неблагоприятных факторах:
- половые инфекции, особенно комплексные, например, ВПЧ и герпес,
- игнорирование презерватива при случайных половых контактах,
- наличие нескольких половых партнёров,
- ранние интимные отношения, повышающие риск заражения половыми инфекциями, травматизации шейки матки,
- хронические воспалительные процессы в малом тазу,
- роль наследственности,
- повреждения эпителия шейки матки,
- курение,
- неблагоприятные условия окружающей среды,
- канцерогенное воздействие мужской смегмы не шейку матки.
Женщинам с ВПЧ следует регулярно проходить профилактические осмотры с целью предупреждения последствия в виде рака шейки матки.
Побочные эффекты
Зачастую радиотерапия при опухолях шейки матки неплохо переноситься больными. Самое частое осложнение, появляющееся после терапии, – это влагалищные кровотечения. Но, как правило, это проявление докучает недолго. Если же кровотечение не прекращается дольше двух недель, то пациентке нужно обратиться за помощью к гинекологу. Тем не менее возможны и иные неприятные последствия после лучевой терапии при раке шейки матки.
- Диарея. Проблемы со стулом довольно распространенный симптом после радиотерапии. При возникновении такого нарушения больным советуют употреблять больше воды во избежание обезвоживания организма.
- Тошнота. Этому признаку нередко сопутствует полнейшая утрата аппетита и рвота. В особо тяжелых случаях пациенткам могут назначаться высококалорийные коктейли, которые должны полностью заменить привычную пищу.
- Ослабленность. Не менее частое последствие радиотерапии – повышенная утомляемость. Оптимальный метод ликвидации этой проблемы – полноценный отдых.
- Воспаления на кожных покровах. В местах, подвергшихся облучению, может появляться сыпь. Именно поэтому в восстановительном периоде специалисты не советуют женщинам применять косметические средства. Подбор уходовой косметики осуществляется сугубо лечащим врачом.
- Сужение влагалища. Подобная проблема возникает вследствие поражения клеток и существенно усложняет как гинекологический осмотр, так и последующее введение аппликатора для проведения дальнейших процедур облучения. Чтобы сохранить привычный диаметр влагалища гинекологи советуют женщинам использовать дилататоры (трубки). При их верном применении риск повреждения слизистой влагалища практически минимальный.
Кроме озвученных осложнений, могут отмечаться и другие негативные проявления. Самые серьезные среди них – раннее наступление менопаузы и развитие лимфодемы при комплексном применении оперативного лечения и радиотерапии.
К сожалению, такие осложнения довольно сложно поддаются коррекции.
Особенности строения
Шейка матки не рассматривается специалистами как отдельный орган. В действительности , это нижняя часть матки, её самый узкий отдел, выполняющий ряд необходимых функций. Шейка защищает матку от вредоносной флоры, являясь своеобразным барьером. Посредством шейки выводится отторгнутый эндометрий в период месячных. Кроме того, шейка матки принимает непосредственное участие в родах и зачатии.
Шейка матки может быть как конической, так и цилиндрической формы. Внешний вид матки зависит от реализованности женщиной детородной функции. Шейка напоминает узкую мышечную трубку, которая имеет незначительную длину.
В структуре шейки матки выделяют два отдела.
- Надвлагалищный. Это самый значительный по величине отдел, который, тем не менее не визуализируется при осмотре.
- Влагалищный. Это участок, который примыкает к влагалищу и исследуется во время гинекологического осмотра.
Влагалищная часть шейки матки имеет следующие характеристики:
- бледно-розовый окрас,
- гладкая ровная поверхность,
- однородность эпителия по цвету и текстуре.
Любые отклонения от нормы могут говорить о патологии и иметь серьёзные последствия.
Шейка матки выстилается следующими видами эпителия:
- плоский многослойный (влагалищная часть),
- цилиндрический однослойный (цервикальный канал).
Влагалищная часть шейки матки выстилается эпителием, состоящим из многослойных плоских клеток. Клеточные элементы располагаются в трех основных слоях и отличаются разной степенью зрелости.
- Базальный слой содержит незрелые округлые клетки с одним большим ядром внутри.
- Промежуточный слой включает созревающие уплощённые клетки с одним уменьшенным ядром.
- Поверхностный слой состоит из зрелых плоских клеточных элементов с одним ядром маленького размера.
Цервикальный канал располагается внутри матки. Вход в канал у рожавших женщин щелевидный. Поверхность цервикального канала образована цилиндрическими однослойными клетками. В цервикальном канале также функционируют железы, вырабатывающие защитную слизь. Узость канала и слизь предотвращают проникновение инфекции в полость матки.
Поверхность слизистой цервикального канала имеет красноватый оттенок и бархатистую текстуру. Верхний конец канала открыт в маточную полость, что формирует внутренний зев. Нижний край цервикального канала открывается во влагалище, таким образом, образуя наружный зев. В его глубине располагается переходная зона, называемая областью трансформации.
По статистике, значительное количество злокачественных опухолей формируются в зоне трансформации.
Восстановительный период
Ключевая роль в восстановительном периоде отводится питанию. При продолжительной лучевой терапии рака шейки матки, особо важна сбалансированность меню женщины. Именно хорошо подобранный рацион поможет избежать таких осложнений, как тошнота и диарея.
Специалисты советуют есть маленькими порциями, и отдавать предпочтение разнообразным витаминизированным продуктам. При этом женщине лучше исключить из меню:
- алкоголь;
- газировки;
- специи и пряности;
- копченые, жирные блюда;
- консервированные продукты.
Также доктора настаивают на ограничении употребления молочной продукции, в силу плохой усвояемости лактозы после облучения. Параллельно переменам в питании доктора советуют пациентке достаточно отдыхать и гулять на свежем воздухе, отказаться от горячих ванн и применения жестких мочалок, а также указывают на необходимость ограниченного использования косметических средств.
Питание
Вылечить раковую опухоль маточной шейки диетой невозможно, но правильный и сбалансированный рацион поспособствует укреплению иммунитета, а сильная иммунная система не даст развиться многим сопутствующим заболеваниям. Продукты, которые должны регулярно присутствовать в рационе женщины:
- свекла и морковь;
- куркума;
- чай зеленый.
Эти продукты помогут вывести из организма токсины и канцерогены. Не рекомендуется употреблять при раке:
- консервы, копчения, маринады;
- алкоголь;
- специи и пряности;
- жареная и жирная пища.
Избавившись от онкопатологии, женщина должна питаться правильно, не перегружать организм тяжелой пищей и продуктами, в составе которых находятся консерванты и усилители вкуса.
Питание должно быть скорректировано с учетом действия облучения на прилегающие к матке нижние отделы кишечника и мочевой пузырь. Из рациона следует исключить продукты богатые лактозой (молоко) и клетчаткой (овощи, хлеб с отрубями и т.д.), животные жиры, острые соусы, копченую и жареную пищу. Есть нужно часто и понемногу, выпивать не менее 2,5-3 литров воды в течение дня.
1. Предоперационная ЛТ - применяется у пациенток, когда есть шанс перевода неоперабельной опухоли в операбельную (используется внутриполостное облучение).
2. Послеоперационная ЛТ - выполняется в случаях обнаружения метастазов в регионарных лимфатических узлах или разрастания опухоли за пределы шейки матки (используется дистанционное облучение).
К сожалению, у 20-30% больных РШМ после ЛТ вследствие различных причин формируются лучевые повреждения (ЛП) прямой кишки и мочевого пузыря. Они могут возникать сразу непосредственно после лучевой терапии или в сроки свыше 3-х месяцев после окончания курса (поздние лучевые поражения).
По клиническим проявлениям ЛП прямой кишки и мочевого пузыря различаются на легкие (катаральные, эрозивные) и тяжелые (язвенные и свищевые).
К числу основных факторов, которые определяют вероятность возникновения и степень тяжести ЛП, относятся:
- величина суммарной поглощенной дозы;
- режим фракционирования дозы;
- объем облучаемых тканей;
- сопутствующие заболевания, прежде всего органов, входящих в зону облучения;
- индивидуальная радиочувствительность тканей у конкретной пациентки.
Профилактика
Первым шагом в данном направлении было использование локальной радиомодификации (Г.М. Жаринов, 1993). В клинике Центрального научно-исследовательского рентгенорадиологического института МЗ РФ (ЦНИИРИ МЗ РФ) была разработана система мероприятий по активной профилактике поздних ЛП прямой кишки и мочевого пузыря. Она включает в себя:
- коррекцию общесоматического статуса больных;
- общеукрепляющую терапию, направленную на активизацию иммунозащитных систем организма;
- симптоматическую терапию сопутствующих заболеваний;
- нормализацию функций желудочно-кишечного тракта;
- диагностику и лечение воспалительных процессов урогенитальных органов;
- лечебную физкультуру;
- психотерапию, социальную адаптацию;
- местное применение (внутрипузырное и/или интраректальное) лечебных препаратов (дибунол, смеси витаминов, гидрокортизон, антибиотики, аналгетики, диметилсульфоксид и пр.).
Подобные результаты свидетельствуют о том, что осуществление относительно несложных и недорогостоящих мероприятий у больных РШМ с высоким риском возникновения ЛП, начатое сразу после курса ЛТ, позволяет значительно снизить частоту и степень тяжести поздних ректитов и циститов.
Новые подходы к лечению
Лечение сформировавшихся ЛП прямой кишки и мочевого пузыря представляет серьезную проблему и требует комплексного подхода. Общепринятой для лечения подобных осложнений является методика, разработанная в ЦНИРРИ МЭ РФ (А.А. Габелов, 1970). Она включает в себя коррекцию соматического состояния больной, нормализацию функций кишечника, санацию мочевыводящих путей, а также местного (внутрипузырного и/или интраректального) применения лечебных препаратов. Стандартный курс лечения продолжается 3-4 недели.
Известно, что при проведении лучевой терапии ослабляются репаративные процессы в окружающих опухоль тканях и органах. У онкологических больных значительно снижаются процессы адаптации. В последние десятилетия в клинической практике достаточно широко применяется низкоинтенсивное лазерное излучение. Оно обладает метаболическим, противовоспалительным, анальгетическим, иммуномодулирующим, денсенсибилизирующим и бактерицидным действием. На фоне лазерного воздействия более выражена пролиферация элементов соединительной ткани и эпителия, усиление фибринолитической активности крови, более интенсивное заживление ран (Kleinkort, Foley, 1984; В.П. Арсютов,1989; Гуща с соавт., 1989; А.К. Полонский, 1995). Эффект лазерного воздействия опосредуется сложной гаммой процессов, в числе которых доминируют реакции организма, ответственные за клеточную адаптацию и повышение регенераторного потенциала. Низкоинтенсивный лазер использовался нами для лечения поздних лучевых повреждений прямой кишки и мочевого пузыря у больных раком шейки матки, подвергшихся сочетанной лучевой терапии в различных клиниках Санкт-Петербурга в период с 1979 по 1996 годы. Лазеротерапия применялась у пациенток с катаральными и эрозивно-десквамативными ректитами и циститами. Такой выбор определялся тем, что эффективность лечения ЛП легкой и средней степени тяжести может быть оценена количественно по срокам достижения клинического результата, а также по частоте последующих обострений.
Рак шейки матки является одной из наиболее распространенных опухолей у женщин. На земном шаре ежегодно выявляется около 500 тыс. новых случаев этого заболевания. В 90-95% случаев опухоль имеет гистологическое строение плоско-клеточного рака, в 3-5% - аденокарциномы.
В зависимости от метода лечения все больные были разделены на три группы. Каждая группа состояла из 20 пациенток (10 с катаральными и 10 с эрозивными ректитами и циститами), выбор методики лечения осуществлялся методом "слепого" отбора.
Первой группе пациенток проводилось лечение по стандартной методике. Во второй группе, помимо стандартной терапии, осуществлялось локальное воздействие низкоинтенсивным лазером "Узор-Янис" с длиной волны 890 нм. Использование матричного излучателя с 16 световодами позволило увеличить площадь лазерного воздействия и сместить в глубину область энергетического максимума (Л.Г. Малышева с соавт., 1998). Зонами лазерного воздействия являлись надлобковая и крестцово-ягодичная области. Сеанс лазеротерапии на каждую область продолжался 10 минут, всего за курс лечения проводилось 12-15 лазерных воздействий.
В третьей группе пациенток стандартная - "базовая" - терапия и локальная лазеротерапия сочетались с системным лазерным воздействием, зонами которого были область грудины, шейный, грудной и поясничный отделы позвоночника, подвздошные и седалищные кости, а также кубитальная вена. Продолжительность лазеротерапии на каждую зону составляла 10 минут, курс лечения также состоял из 12-15 сеансов.
В качестве критериев эффекта оценивались сроки исчезновения клинических симптомов лучевых повреждений. Момент полного прекращения болей, макрогематурии и выделения крови из прямой кишки считался началом ремиссии. Все больные после завершения лечения наблюдались не менее двух лет с контрольными осмотрами через 2-3 месяца. Частота обострений, а также время их наступления также являлись количественными характеристиками эффективности проведенного лечения. Среди 20 больных первой группы у 18 (90%) в результате проведенного лечения удалось полностью ликвидировать клинические проявления лучевых повреждений. Средний срок наступления полной ремиссии составил 25+/-4 сут.
Во второй и третьей группах у всех больных удалось добиться наступления полной клинической ремиссии в сроки соответственно 16+/-2 и 10+/-2 сут. По частоте полных ремиссий различий между группами не было. Средние сроки наступления ремиссии достоверно (р
Читайте также:

