Помощь при опухоли пациенту
Обезболивающая терапия при онкологических заболеваниях — один из ведущих методов паллиативной помощи. При правильном обезболивании на любых стадиях развития рака пациент получает реальную возможность сохранять приемлемое качество жизни. Но как должны назначаться обезболивающие препараты, чтобы не произошло необратимого разрушения личности наркотическими средствами, и какие альтернативы опиоидам предлагает современная медицина? Обо всем этом в нашей статье.
Боль как неизменный спутник рака
Боль при онкологии чаще возникает на поздних стадиях заболевания, вначале доставляя пациенту существенный дискомфорт, а впоследствии делая жизнь невыносимой. Около 87% раковых больных испытывают боли той или иной степени выраженности и нуждаются в постоянном обезболивании.
Онкологические боли могут быть вызваны:
- самой опухолью с поражением внутренних органов, мягких тканей, костей;
- осложнениями опухолевого процесса (некрозы, воспаления, тромбозы, инфицирование органов и тканей);
- астенизацией (запоры, трофические язвы, пролежни);
- паранеопластическим синдромом (миопатия, нейропатия и артропатия);
- противоопухолевой терапией (осложнение после хирургических операций, химиотерапии и лучевой терапии).
Онкологическая боль также может быть острой и хронической. Возникновение острой боли нередко свидетельствует о возникновении рецидива или распространении опухолевого процесса. Она, как правило, имеет ярко выраженное начало и требует короткого по времени лечения препаратами, дающими быстрый эффект. Хроническая боль при онкологии обычно необратима, имеет тенденцию к усилению и поэтому требует длительной терапии.
По интенсивности боль при раке может быть слабой, умеренной и сильной.
Онкологические боли также могут подразделяться на ноцицептивные и невропатические. Ноцицептивная боль вызывается повреждением тканей, мышц и костей. Невропатическая боль обусловлена поражением или раздражением центральной и/или периферической нервной системы.
Невропатические боли возникают спонтанно, без видимых причин и усиливаются при психоэмоциональных переживаниях. Во время сна они, как правило, ослабевают, тогда как ноцицептивная боль не изменяет своего характера.
Медицина позволяет достаточно эффективно управлять большинством видов боли. Одним из лучших способов контроля боли является современный комплексный подход, сочетающий медикаментозные и немедикаментозные методы обезболивания при раке. Роль обезболивания в терапии онкологических заболеваний является исключительно важной, поскольку боль у раковых больных не является защитным механизмом и не носит временного характера, причиняя человеку постоянные страдания. Обезболивающие препараты и методики применяют для того, чтобы предотвратить негативное воздействие боли на пациента и по возможности сохранить его социальную активность, создать приближенные к комфортным условия существования.
Всемирная организация здравоохранения (ВОЗ) разработала трехступенчатую схему обезболивания онкологических больных, в основе которой лежит принцип последовательности применения препаратов в зависимости от интенсивности боли. Очень важным является немедленное начало фармакотерапии при первых признаках появления боли, чтобы предупредить ее трансформацию в хроническую. Переход со ступени на ступень необходимо производить только в тех случаях, когда лекарственный препарат неэффективен даже в своей максимальной дозировке.
Внутримышечные инъекции наркотических анальгетиков очень болезненны и не обеспечивают равномерного всасывания препарата, поэтому этого способа следует избегать.
Для достижения максимального эффекта следует вместе с анальгезирующими средствами использовать и адъювантные, такие как кортикостероиды, нейролептики и антиконвульсанты. Они усиливают эффект обезболивания в том случае, если боль вызвана поражениями нервов и нейропатией. При этом доза обезболивающих может быть существенно уменьшена.
В оценке болевого синдрома врач также должен ориентироваться на следующие показатели состояния пациента:
- особенности роста опухоли и их связь с болевым синдромом;
- функционирование органов, влияющих на активность человека и качество его жизни;
- психическое состояние — тревожность, настроение, болевой порог, коммуникабельность;
- социальные факторы.
Кроме того, врач обязательно должен собрать анамнез и провести физикальное обследование, включающее:
- этиологию боли (рост опухоли, обострение сопутствующих заболеваний, осложнения в результате лечения);
- локализацию очагов боли и их количество;
- время появления боли и ее характер;
- иррадиацию;
- методы лечения боли в анамнезе;
- наличие депрессии и психологических расстройств.
При назначении обезболивания врачами иногда допускаются ошибки в выборе схемы, причина которых кроется в неправильном установлении источника боли и ее интенсивности. В некоторых случаях это происходит по вине пациента, который не хочет или не может правильно описать свои болевые ощущения. Среди типичных ошибок можно выделить:
- назначение опиоидных анальгетиков в тех случаях, когда можно обойтись менее сильными препаратами;
- неоправданное увеличение дозы;
- неправильный режим приема обезболивающих средств.
При грамотно выбранной схеме обезболивания не происходит разрушения личности пациента, при этом его общее состояние значительно улучшается.
Общее обезболивание (аналгезия) — это состояние, характеризующееся временным выключением болевой чувствительности всего организма, вызванное воздействием наркотических веществ на центральную нервную систему. Больной находится в сознании, но поверхностная болевая чувствительность отсутствует. Общее обезболивание устраняет осознанное восприятие боли, но не обеспечивает блокады ноцицептивных импульсов. Для общего обезболивания в онкологии применяются в основном фармакологические препараты, принимаемые перорально или путем инъекций.
Местное (регионарное) обезболивание основывается на блокировании болевой чувствительности на определенном участке тела пациента. Применяется для лечения болевых синдромов и в комплексной терапии травматического шока. Один из видов регионарной анестезии — блокада нервов местными анестетиками , при которой препарат вводится в область крупных нервных стволов и сплетений. При этом устраняется болевая чувствительность в области блокируемого нерва. Основные препараты — ксикаин, дикаин, новокаин, лидокаин.
Спинальное обезболивание — один из видов местной анестезии, при котором раствор препарата вводят в позвоночный канал. Анестетик действует на нервные корешки, в результате чего происходит анестезия части тела, находящейся ниже места прокола. В том случае, если относительная плотность введенного раствора меньше плотности спинномозговой жидкости, то возможно обезболивание и выше места пункции. Вводить препарат рекомендуется до позвонка Т12, поскольку в противном случае может произойти нарушение дыхания и деятельности сосудодвигательного центра. Точным показателем попадания обезболивающего препарата в позвоночный канал является вытекание жидкости из иглы шприца.
Эпидуральные методики — вид местного обезболивания, при котором анестезирующие средства вводятся в эпидуральное — узкое пространство, находящееся снаружи позвоночного канала. Обезболивание обуславливается блокадой спинномозговых корешков, спинальных нервов и непосредственным воздействием обезболивающих средств. При этом не оказывается воздействия ни на головной, ни на спинной мозг. Обезболивание захватывает большую зону, поскольку препарат опускается и поднимается по эпидуральному пространству на весьма значительное расстояние. Такой вид обезболивания может проводиться однократно через иглу шприца или многократно через установленный катетер. При подобном методе с использованием морфина требуется доза во много раз меньше дозы, применяемой при общем обезболивании.
Нейролизис . В тех случаях, когда больному показана постоянная блокада, проводится процедура нейролизиса нервов, основанная на денатурации белков. При помощи этилового спирта или фенола разрушаются тонкие чувствительные нервные волокна и другие виды нервов. Эндоскопический нейролизис показан при хроническом болевом синдроме. В результате процедуры возможно повреждение окружающих тканей и сосудов, поэтому он назначается только тем больным, у которых исчерпаны все другие возможности обезболивания и с предполагаемым сроком жизни не более полугода.
Введение препаратов в миофасциальные триггерные пункты . Триггерными пунктами называют небольшие уплотнения в мышечных тканях, возникающие в результате различных заболеваний. Боль возникает в мышцах и фасциях (тканевой оболочке) сухожилий и мышц. Для обезболивания применяют медикаментозные блокады с применением прокаина, лидокаина и гормональных средств (гидрокортизон, дексаметазон).
Вегетативные блокады являются одним из эффективных местных методов обезболивания при онкологии. Как правило, они используются при купировании ноцицептивной боли и могут применяться для любого отдела вегетативной нервной системы. Для проведения блокад используются лидокаин (эффект 2–3 часа), ропивакаин (до 2 часов), бупивакаин (6–8 часов). Вегетативные медикаментозные блокады также могут быть однократными или курсовыми в зависимости от тяжести болевого синдрома.
Нейрохирургические подходы применяются в качестве метода местного обезболивания при онкологии в том случае, когда паллиативные средства не справляются с болью. Обычно такое вмешательство применяется для разрушения путей, по которым болевые ощущения передаются от пораженного органа к головному мозгу. Этот метод назначается довольно редко, поскольку может вызвать серьезные осложнения, выражающиеся в нарушении двигательной активности или чувствительности определенных участков тела.
Анальгезия, контролируемая пациентом . По сути, к анальгезии такого типа можно отнести любой метод обезболивания, при котором больной сам контролирует потребление анальгетиков. Самая распространенная ее форма — это применение в домашних условиях ненаркотических препаратов типа парацетамола, ибупрофена и других. Возможность самостоятельно принимать решение об увеличении количества препарата или его замене в случае отсутствия результата дает пациенту ощущение владения ситуацией и снижает тревогу. В стационарных условиях под контролируемой анальгезией понимают установку инфузионного насоса, который подает больному дозу внутривенного или эпидурального обезболивающего каждый раз, когда тот нажимает кнопку. Количество подач лекарства в сутки ограничено электроникой, особенно это важно для обезболивания при помощи опиатов.
Обезболивание при онкологии — одна из важнейших проблем здравоохранения во всем мире. Эффективная борьба с болью является первоочередной задачей, сформулированной ВОЗ, наряду с первичной профилактикой, ранним выявлением и лечением заболевания. Назначение вида противоболевой терапии проводится только лечащим врачом, самостоятельный выбор препаратов и их дозировки недопустим.
Паллиативное лечение – подход, направленный на улучшение качества жизни онкобольных и уменьшения страданий при протекании болезни.
Онкологические заболевания в последнее время диагностируются часто. В медицине разработано немало методов ранней диагностики, но больше половины больных онкологией обращаются к врачам уже в запущенной форме. Ситуация усложняется для медиков тем, что совместно с применением передовых методов лечения приходится искать возможности помощи людям, которым уже нельзя помочь.
Сущность паллиативной помощи
Онкологических больных на последней неоперабельной стадии мучают мучительные боли и страх перед смертью. Людям требуется поддерживающая терапия, которая снизит болевые симптомы. Также требуется обеспечить таким больным максимально возможные комфортные условия в последние дни или месяцы жизни. Паллиативное лечение старается эти нужды выполнить и поддержать близких родственников – понятие метода заключается в упомянутых принципах. Уход за человеком с онкологией и переживания ложатся на плечи ближайших родственников.
Обеспечение комфорта в жизни человека с неизлечимым диагнозом – это главная цель сотрудников паллиативной медицины. В онкологии задача врачей – удалить злокачественное новообразование и вернуть пациента к привычному ритму. Паллиативная медицина таких задач перед собой не ставит – этого не требуется. Пациент, нуждающийся в паллиативном лечении, имеет диагноз – 4 стадия рака.
Последние месяцы перед смертью для больного и родственников – непростое испытание. Человек знает, что его ждёт, также это знают и родные. Изменить ситуацию невозможно. Здесь требуется придерживаться многих принципов – этических, эмоциональных, физических и проч. Помощь требуется и умирающему, и близкому окружению. Паллиативная медицинская помощь в период тяжёлого напряжения приносит ощутимое облегчение каждой стороне.
Применение паллиативной помощи обширно – в онкологии, кардиологии, болезнях опорно-двигательного аппарата, патологиях неврологического характера и прочих.
Этапы паллиативной помощи
Метод паллиативной медицины иногда применяется к людям на раннем сроке заболевания. В этой ситуации используется основная терапия с дополнительным курсом паллиативного ухода. С прогрессированием болезни основная терапия отходит на второй план.
При паллиативном способе оказание помощи применяется:
- В условиях стационара, когда для пациента используется хирургическое, лучевое лечение и химиотерапия;
- Оказание помощи в отделении дневного пребывания;
- Роль медсестры важна, она заключается в уходе за больным в домашних условиях;
- Переоценить значение сестринского ухода в хосписе за пациентами нельзя.
Хосписы заменяют людям перед уходом дом и близких родственников. От рака лёгких, печени, желудка, головного мозга зафиксирован высочайший процент смертности. Люди переносят сильнейшие боли и психологические страдания, которые требуется снять.

Медицинский паллиативный метод в хирургии применяется при удалении части опухоли, что помогает продлить жизнь. Проводится мероприятие по купированию тяжёлых симптомов при раке и прочих заболеваниях. К примеру, делают выходное отверстие в брюшной стенке при тяжёлой кишечной непроходимости. Это помогает человеку устранить дискомфорт и вернуться к социальному окружению.
Лучевая терапия совместно с курсом химиотерапии уменьшает размер злокачественного новообразования и позволяет блокировать прогрессирование на некоторое время. В этот период снижается интоксикация организма продуктами ракового образования.
Больные в области онкологии больше находятся дома под присмотром родственников. Здесь требуется опыт специалиста, который разъяснит правила приёма лекарственных средств, поддержит общение с больным и поможет советом в трудный момент.
При невозможности проводить симптоматическое лечение дома пациента помещают в хоспис. Хосписные движения обрели популярность в России после 2011 года. Хоспис – это специализированное учреждение, где оказывается специализированная медицинская помощь бесплатно. Здесь находятся люди, у которых нет родственников либо отсутствует возможность присматривать дома.
Принципы паллиативной медицины
- Манипуляции, направленные на купирование болевых ощущений;
- Устранение симптомов расстройства органов пищеварения – запора и тошноты с рвотой;
- Корректировка рациона питания;
- Психологическая помощь.
Смерть, которая может наступить в любой момент, приносит эмоциональные страдания и психологический дискомфорт. Усугубляет положение присутствие постоянных болей и нарушений в функционировании организма. Помощь сотрудников заключается в максимальном купировании нежелательных симптомов.
Большинство злокачественных новообразований на последней стадии протекает с интенсивной и мучительной болью. Испытывая боли, человек не может заниматься обычными делами – общаться, самостоятельно совершать прогулки, делать домашние дела. Значит, требуется правильно подобранный курс терапии по устранению неприятных признаков. В условиях стационара используют лучевое облучение. Для дома подбирается комплекс лекарств из группы анальгетиков.
Препараты подбираются индивидуально. Рассчитывается режим приёма, однократная доза и схема ввода. Учитывается физическое состояние пациента и характер болезненного течения. Схема приёма применяется с учётом того, чтобы действие предыдущей дозы пока не прекратилось. Это снижает болевой синдром.

Иногда используется другой метод борьбы с болью – начинать с анальгетиков без наркотического воздействия, затем меняется на препарат со слабым наркотическим действием и уже на последней стадии используется сильнодействующий опиат (к примеру, морфин). Подобная схема часто применяется в лечении детей. Многие родители против применения сильных опиатов, но приём позволяет снять боль и облегчить состояние ребенка. А это означает, что сотруднику паллиативной помощи требуется объяснить родителям необходимость данной процедуры.
Приём различных лекарственных средств, интоксикация от продуктов жизнедеятельности опухоли, курсы химиотерапии часто приводят к расстройствам в органах пищеварения. В этом случае применяется патогенетическое лечение. Присутствие тошноты с рвотными позывами демонстрирует интенсивный мучительный характер, купируемый приёмом специальных противорвотных препаратов. Рекомендуется использовать данный метод в лечении детей – это поможет сохранить доверие к лечащему доктору и предотвратит развитие нежелательного рефлекса на процедуры химиотерапии.
Часто использование опиоидных препаратов и химиотерапия провоцирует развитие запоров. Восстановить стул помогает комплекс слабительных средств. Детям рекомендуется лактулоза.
В онкологии большую роль играет правильно составленный рацион питания. Требуется это для хорошего самочувствия больного, чтобы восполнить дефицит витаминов с микроэлементами, предотвратить потерю веса и тошноту с рвотой. Паллиативная медицина призвана направлять пациентов и родных к правильному питанию.

Рацион составляется с учётом того, чтобы ослабленный болезнью организм получал необходимую суточную норму белков, жиров и углеводов. Пища должна быть приемлемо калорийной и с содержанием требуемых витаминов с микроэлементами.
Для отдельных людей (особенно детей) большую роль играет внешний вид блюда. Привлекательный вид и соответствующая атмосфера способствуют хорошему аппетиту и усвояемости пищи. Задача профессионалов – объяснить это родственникам и научить, как добиться подобного.
Этичное отношение во время неоперабельной стадии рака играет огромную роль в данный период. Люди, знающие о диагнозе и прогнозе, самостоятельно справиться с тяжким грузом не смогут. Также тяжело родственникам – они не знают, как себя вести, говорить о диагнозе, возникает масса других вопросов. Психологическая помощь требуется каждой стороне. Больному назначается курс успокоительных средств. Психолог общается со всеми – спокойные, наполненные любовью и радостью последние дни жизни необходимы не только больному, но и родным людям.
В рассуждениях, говорить либо нет диагноз пациенту – врачи склоняются к тому, что человек имеет право знать. Считается, что правда помогает легче перенести последние дни. Избранные люди с онкологией успевают за этот период совершить ряд невозможных действий, которые откладывали прежде долгие годы. Справиться со страхом перед смертью не удастся до конца, но можно как-то притупить эмоцию. В этом помогут специалисты.
Лечение онкологического заболевания – тяжёлый труд для врачей и родных людей. Медицинский персонал выполняет действия по устранению физических неприятных симптомов. Психологический комфорт создают родственники. Паллиативная медицина помогает снизить тяжесть эмоционального груза и физического дискомфорта.
Распространение опухолевого процесса может вызвать дальнейшие онкологические осложнения. Такой больной нуждается в срочной медицинской помощи, возможно даже потребуются реанимационные мероприятия.
Вовремя оказанная помощь не только сохранит человеку жизнь, но и улучшит его самочувствие, нормализует анализы, что чрезвычайно важно для дальнейшего прохождения лечения.
Пациентам, госпитализированным в состоянии, требующем незамедлительной медицинской помощи, таковая оказывается без промедления. Рассмотрим основные виды тех осложнений, которые могут потребовать срочной онкологической помощи.
Дыхательная недостаточность
Синдром, обусловленный нарушением газообмена в легких и сопровождающий многие онкологические заболевания.
В организме непрерывный газообмен поддерживается с помощью внешнего дыхания. Любое нарушение его функций вызывает нарушение газообмена между находящимся в альвеолах легких воздухом и газовым составом крови. Из-за этого в крови возрастает количество углекислоты и уменьшается количество кислорода, что вызывает кислородное голодание головного мозга.
При дыхательной недостаточности, которая сопровождается снижением парциального давления в артериальной крови значительно ниже 60 мм рт. ст. и повышением парциального давления углекислоты выше 45 мм рт. ст. развивается состояние, угрожающее жизни.
Синдром распада опухоли
Синдром лизиса или синдром распада опухоли может развиться при быстрой регрессии любого типа опухоли, происходящей в результате гибели опухолевых клеток вследствие химиотерапии. Наиболее часто это имеет место в ходе лечения острого лейкоза и высокодифференцированных лимфом, несколько реже – при заболевании рак легких.
Синдром распада опухоли проявляет себя метаболическими нарушениями: гиперкалиемией, повышением уровня мочевины, гиперфосфатемией, ведущей к гипокальциемии. У больных с ХПН данный синдром возникает чаще из-за нарушений в выведении продуктов распада клеток опухоли.
К тяжелым проявлениям синдрома лизиса относят также ОПН и выраженные симптомы аритмии, включая тахикардию и фибрилляцию желудочков. По этой причине необходимо своевременно распознавать больных, имеющих высокий риск развития такого синдрома, контролировать их состав крови и быстро начинать лечение при возникновении соответствующих признаков.
Тромбоэмболия легочной артерии
Тромбоэмболией называют явление закупорки магистрального ствола сосуда или его ветви раковыми клетками, жидкостью или тромбами, которые преимущественно образуются в венах таза или нижних конечностей. Из-за присутствия данного патологического процесса дыхание может ослабеть до такой степени, что больной не сможет получать нужное ему количество кислорода без подачи воздуха в легкие принудительным способом.
Как следствие этого у него возникает острая дыхательная недостаточность. Часто тромбы блокируют ток крови с правой стороны и направляют его в легкие, что вызывает мгновенную гибель больного. Чтобы избежать летального исхода, больного подключают к аппарату искусственной вентиляции легких, который способен целиком принять на себя дыхательные функции.
Тромбоз нижней полой вены
Тромбоз, распространившийся на печеночные вены, может повлечь развитие тяжелого заболевания, схожего с болезнью Киари. Начинается оно с тромбоза печеночных вен и нарушения печеночных функций с последующим тромбозом воротной вены. Развитие первичного тромбоза печеночных вен (Бадда-Киари) может быть обусловлено причинами разного рода.
Среди них – опухолевый процесс, начинающийся в теле или хвосте поджелудочной железы. Проявления первичного тромбоза печеночных вен характеризуются следующими симптомами:
• заметным увеличением размеров печени;
• болями в животе, преимущественно в эпигастрии;
• скоплением жидкости в брюшной полости;
• расширением поверхностных вен в верхней части живота;
• увеличением селезенки;
• изменением цвета кожи;
• диспепсическими расстройствами.
Синдром верхней полой вены
Данный синдром осложняет течение множества заболеваний и является неотложным состоянием. Вызывается он нарушениями кровообращения в бассейне верхней полой вены. Наиболее распространенным онкологическим заболеванием, сопровождающимся данным синдромом, является рак легкого.
Симптомы, возникающие при СВПВ, могут вызвать гибель больного. Самыми перспективными способами лечения данного синдрома являются лучевая терапия, эффективность которой составляет 70-90% и баллонная ангиопластика, заключающаяся в установке стента на суженном участке вены.
Портальная гипертензия
Синдром повышенного давления в портальной вене, которая обеспечивает поступление крови от кишечника к печени, называется портальной гипертензией. Симптомами данной проблемы являются варикозное расширение вен пищевода, а также скопление жидкости в брюшной полости, печеночная энцефалопатия, черный стул, рвота, помутнение сознания.
В норме давление в системе должно быть 5-10 мм рт. ст. Превышение более 12 мм рт. ст. считается повышенным и говорит о начале портальной гипертензии. Кровотечения из варикозно расширенных вен пищевода часто становятся основной причиной смерти. Главным способом лечения данной патологии является оперативное вмешательство.
Механическая желтуха
Желтуха механическая является состоянием, способным привести к смерти. Возникает она при опухолях и метастазах печени по причине нарушения свободного прохождения желчи по естественным протокам из печени в 12-перстную кишку. Такая патология является следствием сдавливания желчных путей, что чаще всего происходит при желчекаменной болезни (29%) и злокачественных опухолях (67%).
Симптомами механической желтухи являются желтушность кожи и слизистых, темный цвет мочи, обесцвечивание кала, кожный зуд, возможны высокая температура. Показатели билирубина при этом превышают 1.6-2 мг% (20 мк моль/л). Без своевременного лечения далее следует развитие печеночной недостаточности и летальный исход.
Лечение заключается в снятии причин нарушения желчетока и его восстановление. Иногда проводится операция баллонной дилатации, при которой в желчных протоках устанавливаются специальные стенты, служащие внутренними каркасами, обеспечивающими свободное прохождение желчи.
Другие неотложные состояния
• Перфорация или прорастание опухоли;
• Кровотечения из опухоли;
• Стеноз полых органов;
• Некроз или разрыв опухоли;
• Кишечные и желчные свищи.
Все перечисленные неотложные состояния требуют срочной онкопомощи. Помимо них существуют и другие, к которым относятся почечная недостаточность, электролитные расстройства. Неотложные состояния, возникающие в результате медицинских мероприятий, важно устранять по мере их появления.
К примеру, при химиотерапии частыми осложнениями бывают почечная недостаточность, тромбоз мозговых сосудов. Зачастую устранить их можно только в реанимационном отделении с помощью специальной аппаратуры.
Для подбора эффективного метода лечения вы можете обратиться за
- методы инновационной терапии;
- возможности участия в экспериментальной терапии;
- как получить квоту на бесплатное лечение в онкоцентр;
- организационные вопросы.
После консультации пациенту назначается день и время прибытия на лечение, отделение терапии, по возможности назначается лечащий доктор.

Спорим, вы не угадаете, что это? Это стент в просвете пищевода
Не каждый из тех, кто кашляет весной 2020 – болен COVID-19. Есть пациенты, кому еще хуже: они задыхаются, и им не помогут 2 недели в инфекционной больнице. У них рак. Рак легких, или молочной железы, или яичников, или, возможно, лимфома.
При многих опухолях частое осложнение – скопление жидкости в плевральной полости (вокруг легких). Ее бывает много, до нескольких литров (!) – и она сдавливает легкие, мешая им работать. Это называется гидроторакс.
Заметьте, хирург позволяет человеку жить дальше, хотя не действует на главную причину беды: злокачественную опухоль. Это один из примеров паллиативной хирургии.
Паллиативная хирургия – это такая, которая не устранит главную проблему – раковую опухоль, не вылечит человека полностью. Но паллиативная операция, вероятно, продлит ему жизнь и заметно повысит ее качество: он сохранит способность к самообслуживанию и социальную адекватность, сможет сам передвигаться, есть или ходить в туалет, перестанет мучиться от боли.
Почему бывает нельзя просто вырезать опухоль?
Хирургическое лечение в онкологии многие считают только радикальным: когда все очаги поражения можно просто иссечь. А иначе ведь – зачем и связываться с травматичными вмешательствами и вообще впустую размахивать скальпелем? Это распространенный стереотип.
Если, например, кроме опухоли в молочной железе у женщины метастазы в печени, легких и позвоночнике – придется удалять слишком много тканей из разных органов сразу, и риск умереть от такой операции у нее будет выше, чем от прогрессирования болезни.

Органы, куда чаще всего метастазирует рак молочной железы
Но это не значит, что таким людям ничем нельзя помочь! Паллиативная помощь может значительно облегчить состояние пациента и улучшить качество его жизни, а иногда и продлить ее – не прибегая к радикальному лечению.
Паллиативная медицина чаще всего использует химио- и лучевую терапию. К сожалению, это отложилось в головах у многих российских врачей слишком плотно: они не готовы применять хирургию, когда заранее понимают, что оставят опухоль или часть ее внутри пациента. Хотя в онкологических отделениях по миру до 20% всех операций – паллиативные.
И их становится больше. Показания к хирургическому лечению на любой стадии рака – даже при распространённом процессе – расширяются. Появляются новые малоинвазивные способы вмешательства – они снижают риски для пациента и после них легче восстановиться.
Паллиативная хирургия становится частью комплексного лечения. У нас этому очень помогает налаженное междисциплинарное взаимодействие. Когда хирург, онколог, химиотерапевт, врач лучевой терапии и реаниматолог собираются вместе, они не тянут одеяло на себя (как вы могли подумать), а находят оптимальную лечебную тактику, чтобы избавить пациента от мучительных симптомов максимально безопасно, и насколько возможно долго.
На сегодня успехи таковы. С помощью паллиативной операции можно:
- Уменьшить размер опухоли, чтобы появилась возможность действовать на нее химиотерапевтическими методами.
- Снизить опухолевую интоксикацию.
- Убрать тягостные симптомы.
- Остановить/предотвратить внутреннее кровотечение.
- Уменьшить боли.
- Реконструировать поврежденную часть тела и помочь реабилитации после радикальных методов лечения.
Не можем удалить – уменьшим. Циторедуктивные операции
а) продлить пациенту жизнь,
б) убрать тягостные симптомы,
в) предотвратить жизнеугрожающие состояния.
Часто опухолевые очаги нельзя удалить целиком. Например, опухоль слишком крупная – вместе с ней пришлось бы удалять жизненно важный орган или очень большой его участок. Или поражены слишком много систем организма – множественные отдаленные метастазы. Или очаги метастазирования мелкие, до микроскопического размера, зато их тысяча – как при канцероматозе брюшины.
Хотя в таких случаях часто есть возможность удалить не всю, но максимально возможную часть опухоли. Это уменьшит тяжелые симптомы, вызванные жизнедеятельностью раковых клеток. А главное – не остановит, но замедлит распространение злокачественного процесса, позволит пациенту выиграть время, даст больше шансов на то, что химио- и лучевая терапия подействуют – они работают тем эффективнее, чем меньше объем опухолевой ткани в организме.
Циторедуктивные операции становятся частью комплексного лечения. Мы уже рассказывали про HIPEC, гипертермическую внутрибрюшинную терапию, которая помогает пациентам на последних стадиях рака яичников, желудка, различных отделов кишечника, печени. Циторедуктивная операция занимает в процедуре HIPEC первое место: сначала хирург удалит все очаги, которые сможет найти, а затем брюшную полость пациента обработают горячим химиопрепаратом. После такой операции люди могут жить годы вместо месяцев, а в некоторых случаев – добиться ремиссии.
На этом видео можно посмотреть, как проходит циторедуктивная операция при канцероматозе брюшины. Осторожнее, если вы не любите заглядывать людям слишком глубоко внутрь!
Одна из наших пациенток, которой удаляли аденокарциному яичников, выполняет циторедуктивную операцию в сочетании с HIPEC уже 5-й раз подряд – и это 5 лет жизни.
Кроме рака яичников, циторедуктивные операции, как один из этапов лечения, показывают улучшение показателей по выживаемости при колоректальном раке, раке желудка, аденокарциноме аппендикса, саркомах мягких тканей – даже на тех стадиях, когда опухоль уже начала метастазировать.
Циторедуктивная операция нередко оказывается способом избежать худшего в ситуации, когда пациенту угрожают серьезные, опасные осложнения. Например, такое вмешательство помогает предотвратить перфорацию кишечника или сильное кровотечение из-за распада опухоли.
Эти меры, хотя и являются паллиативными – не дают пациенту уйти из жизни раньше времени.
Поэтому мы стараемся всегда найти максимум возможных вариантов лечения и следить за прогрессированием, даже когда невозможно выполнить радикальное вмешательство или опухоль плохо реагирует на химиотерапию.
Не можем удалить причину – режем следствия. Симптоматические операции
Симптоматические паллиативные хирургические вмешательства вообще не затрагивают опухоль, в отличие от циторедуктивных операций, но борются с опасными последствиями для пациента, которые вызывает рост злокачественного новообразования.
Например, про торакоцентез при скоплении жидкости в грудной клетке мы описали в самом начале статьи. Но не реже происходит скопление жидкости в брюшной полости – асцит. Это обычное осложнение при раке желудка, яичников, колоректальном раке и др.
При асците (скоплении жидкости в брюшной полости) объем жидкости может достигать 10 и более литров. Пациент чувствует себя очень плохо: одышка, нарушение в работе ЖКТ и внутренних органов. Чтобы облегчить это состояние, выполняют лапароцентез – прокол в стенке брюшной полости, чтобы вывести жидкость. Если жидкость скапливается быстро, устанавливают дренаж – он выводит излишки непрерывно.
Однако чаще всего симптоматические операции нужны, чтобы организм, по сути, продолжал производить с окружающей средой обмен, который всем нам так привычен и воспринимается здоровыми людьми как должное.
Для обеспечения функционирования пищеварительной системы
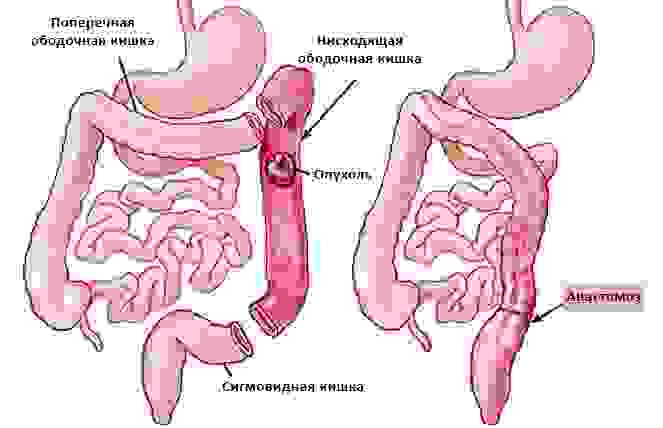
Удаление части ободочной кишки и формирование анастомоза
Однако, анастомоз наложить удается не всегда: например, пищевод или кишечник может быть слишком сильно поврежден опухолью. Существует еще ряд ситуаций, когда возникает необходимость создать прямое сообщение между полостью любого органа и окружающей средой.
На этот случай существуют стомы – отверстия, хирургическим путем сформированные на коже, к которым подшивают края нужной полости, в зависимости от локализации неоперабельной опухоли, которая закрывает просвет.
Например, гастростома – если не удается задействовать для питания пищевод: желудок подшивают к стенке брюшной полости и формируют отверстие на коже, через которое вводят полужидкую пищу.
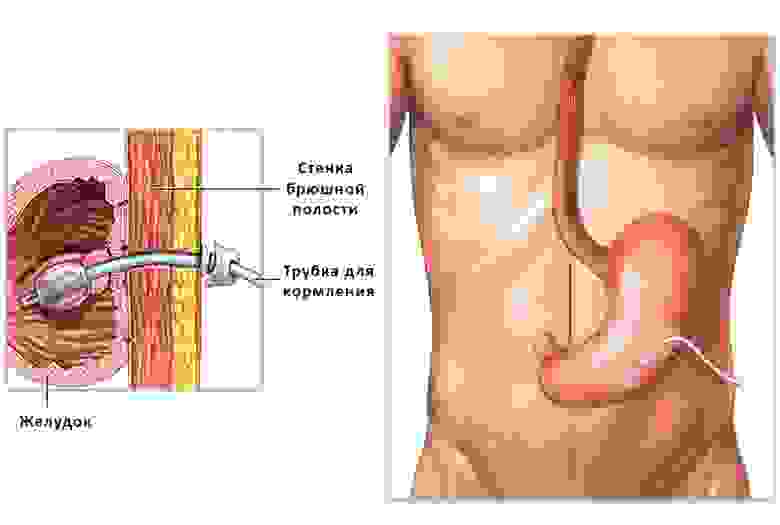
Устройство гастростомы
Колостома и илеостома. Если предыдущее отверстие было предназначено для питания пациента, то это – наоборот. При колостомии на кожу живота выводят отверстие из ободочной кишки, при илеостомии – подвздошной кишки. Через коло- или илеостому в специальный мешок-калоприемник отходят продукты жизнедеятельности.
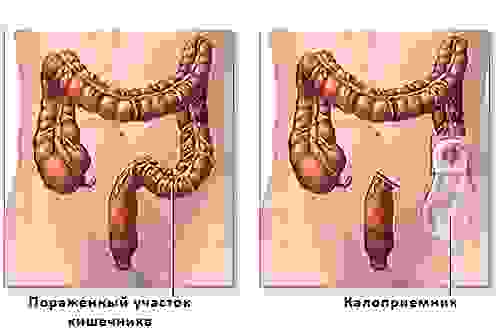
Резекция толстой кишки с выведением колостомы
Обеспечение функции дыхания
Трахеостома. При опухолях гортани, чтобы не допустить удушья, проводят трахеостомию — на кожу выводят отверстие из трахеи, через которое человек может дышать.

Трахеостома и проведение процедуры трахеостомии
Обеспечение мочевыделения
Нефростома – специальная полая трубка, которая выполняет функцию дренирования при нарушениях оттока мочи. Ее устанавливают в почечную лоханку через прокол на коже под контролем УЗИ.
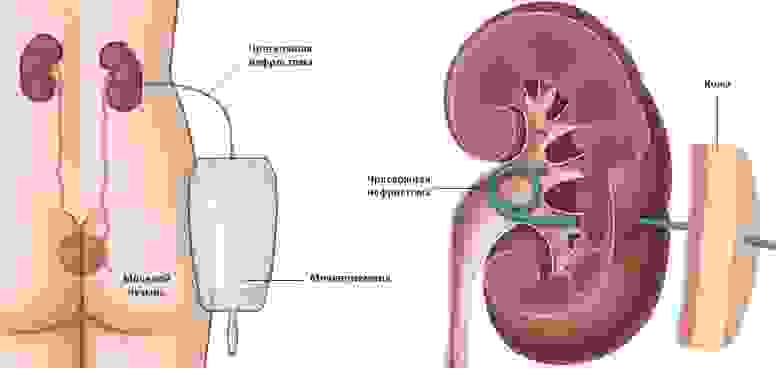
Нефростома
Когда возможно – не режем, а используем эндоскоп
Когда опухоль разрастается и вовлекает какой-либо полый орган (пищевод, желудок, желчный проток, мочеточник, и т.д.), это может приводить к сдавливанию стенок органа, сужению просвета и полной непроходимости.
Зачастую в таких случаях есть возможность установить стент — металлический или полимерный сетчатый цилиндр-расширитель, который автоматически расправляется внутри полости органа и создает каркас, чтобы поддерживать достаточный просвет и проходимость.

Билиарный стент (для желчного протока)
С помощью стентирования у нас получается сохранить физиологические функции многих органов даже на поздних стадиях опухолевого процесса.
Нормальное отведение желчи и лечение механической желтухи. Стентирование желчных протоков восстанавливает беспрепятственный отток желчи из печени в двенадцатиперстную кишку. Во-первых, пациент избавится от опасного состояния: механической желтухи. Она вызывается нарушением оттока желчи, провоцирует повышение уровня билирубина в крови и токсическое действие на ЦНС. Во-вторых, пациенту не придется ходить с выходящими наружу дренажами. В-третьих, естественный ток желчи сохранит нормальную работу кишечника. Так одна малоинвазивная операция делает очень много для сохранения качества жизни.

Стентирование желчного протока с помощью эндоскопа
Обеспечение работы пищевода и возможности самостоятельно питаться. Мы можем стентировать пищевод и желудок в случаях, когда опухоль находится в самом органе, или разрастается, придавливая его снаружи, или сужение просвета стало результатом более ранних вмешательств или иных повреждений (рубцов от химического ожога, например).

Работа стента в пищеводе, сдавленном опухолью
Судите сами: пациента привезли на реанимобиле с механической желтухой и стенозом пищевода, а выписали через 10 дней в состоянии, когда он может самостоятельно принимать пищу через рот и нормально ее переваривать.
Удалить всё и восстановить красоту. Санационные операции и реконструктивные
Когда опухоль не оперировали, и не слишком успешно лечили иными методами, она продолжает расти, а потом начинает распадаться. Эта опухолевая ткань может инфицироваться, вызывать массивные кровотечения, некрозы, оказывать токсическое действие на организм пациента, и сильно ухудшает его состояние.
Чтобы не допустить этого, нужно удалить как можно большее количество инфицированной опухолевой ткани. Такие паллиативные операции в онкологии называются санационными. Их выполняют, например, при раке молочной железы. Необходимость в таких операциях возникает у 30-40% женщин на III-IV стадиях. Также такие операции проводятся при угрозе распада и нагноения опухолей других органов: например, печени, ободочной кишки.
Часто после объемных оперативных вмешательств с полным удалением пораженного органа требуется последующая реконструкция. Например, молочной железы, частей лица или части кишечника, мочевого пузыря – для восстановления жизнедеятельности организма.
Это крайне важно и для психоэмоционального настроя пациента – чтобы он снова чувствовал себя нормальным человеком, с симметричными молочными железами и способностью ходить в туалет без дренажей и мочеприемников. От этого в большой мере зависит, будет ли человек находить радость в жизни и мотивацию для продолжения лечения.
Этой статьей мы хотим, во-первых, напомнить в нынешнее тревожное время, как счастливы те из нас, чей организм не нуждается в поддержке хирургов, чтобы есть или дышать.
А во-вторых, показать: даже в запущенных и тяжелых случаях все еще остается довольно много возможностей помочь онкологическому пациенту, продлить жизнь, убрать или облегчить мучительные симптомы. Даже если по прогнозам, жизни осталось совсем немного – есть очень большая разница в том, как ее прожить. В качестве, а не только в количестве. Паллиативная медицина – и паллиативная хирургия в частности, сегодня могут многое сделать для качества.
Читайте также:

