Пластика при раке полости рта
К трем основным методам лечения рака полости рта относятся хирургическое удаление, лучевая терапия и химиотерапия. На ранних стадиях (I—II) можно использовать лишь один метод лечения (хирургическая резекция или лучевая терапия).
При распространенных опухолях (III—IV) необходимо использовать как минимум два метода, в запущенных случаях требуются все три метода лечения. Если опухоль имеет признаки агрессивного роста (экстракапсулярное распространение, периневральная или сосудистая инвазия), то даже на ранних стадиях требуется комбинированное лечение.
Основные цели лечения: (1) излечить рак; (2) сохранить или восстановить форму и функцию пораженного органа; (3) свести к минимуму возможные побочные эффекты от лечения.
При планировании лечения также необходимо оценить положение опухоли в переднезаднем направлении, ее близость к костям, глубину инвазии, гистологический тип. Небольшие опухоли, располагающиеся в передних отделах полости рта, могут быть удалены внутриротовым доступом, какие-либо функциональные нарушения минимальны.
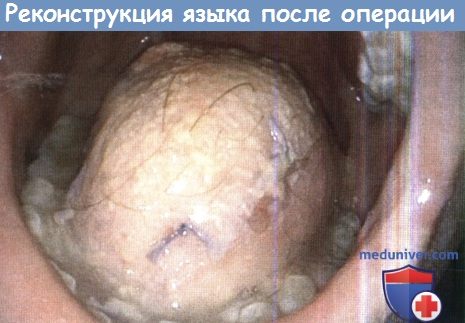
Реконструкция ротовой части языка при помощи свободного латерального лоскута бедра после практически тотальной глоссэктомии.
Пациент может есть и разборчиво говорить.
При опухолях ранних стадий предпочтительным методом лечения является хирургический, поскольку лучевая терапия сопровождается значительным риском развития ксеростомии, кариеса зубов, остеорадионекроза. Опухоли языка и дна полости рта со значительной инвазией в подлежащие ткани достаточно часто метастазируют в лимфатические узлы, поэтому если принято решение об их хирургическом удалении, даже при клинической N0 стадии поражения лимфоузлов необходимо выполнять селективную шейную лимфодиссекцию.
У пациентов с клиническими признаками поражения лимфоузлов при пальпации рекомендуется выполнять шейную лимфодиссекцию уровней I-V.
При больших опухолях рекомендуемым методом лечения является их хирургическое удаление с реконструкцией и последующей лучевой или химиолучевой терапией. Метод хирургического удаления зависит от локализации очага. К возможным доступам относятся мандибулотомия, верхний щечный лоскут, нижний щечный лоскут, visor flap.
В зависимости от степени поражения костной ткани или близости к ней может планироваться выполнение вертикальной, горизонтальной, либо сегментарной резекции нижней челюсти. Наиболее часто для восстановления формы и функции полости рта используют свободный малоберцовый лоскут, радиальный лоскут предплечья, антеро-латеральный лоскут бедра.
В некоторых случаях могут использоваться лоскуты на ножке, например, мышечно-кожный лоскут большой грудной мышцы или местные ротационные лоскуты, но их использование не является оптимальным.
Пациенты с тяжелыми сопутствующими заболеваниями могут не перенести длительных операций по пересадке свободных лоскутов с наложением микроваскулярных анастамозов, поэтому у них должны использоваться другие методы реконструкции, подразумевающие менее короткие сроки операции.
При дефектах, требующих реконструкции для предотвращения функциональных нарушений (например, при фиксации языка), но недостаточно больших для свободного лоскута с микрососудистым анастомозом приемлемы местные тканевые лоскуты и/или кожные трансплантаты.
К возможным осложнениям операции относятся кровотечение, аспирационная пневмония, формирование фистул. Возможные поздние осложнения: низкая разборчивость речи, нарушения жевания и глотания.
Ранними побочными эффектами лучевой терапии являются мукозит и нарушения вкуса, а поздними — перманентная ксеростомия, кариес зубов, остеорадионекроз. Химиотерапия может осложняться подавлением функции костного мозга, тошнотой и рвотой, аллопецией, мукозитом, нарушением функции легких, печени, почек, нейропатией, включая ото- и вестибулотоксичность вследствие поражения VIII пары черепных нервов.
Прогноз в первую очередь зависит от того, на какой стадии было выявлено заболевание. Общая пятилетняя выживаемость при заболевании I и II стадии составляет 80% и 70% соответственно; на III и IV стадиях выживаемость составляет 55% и 30%.
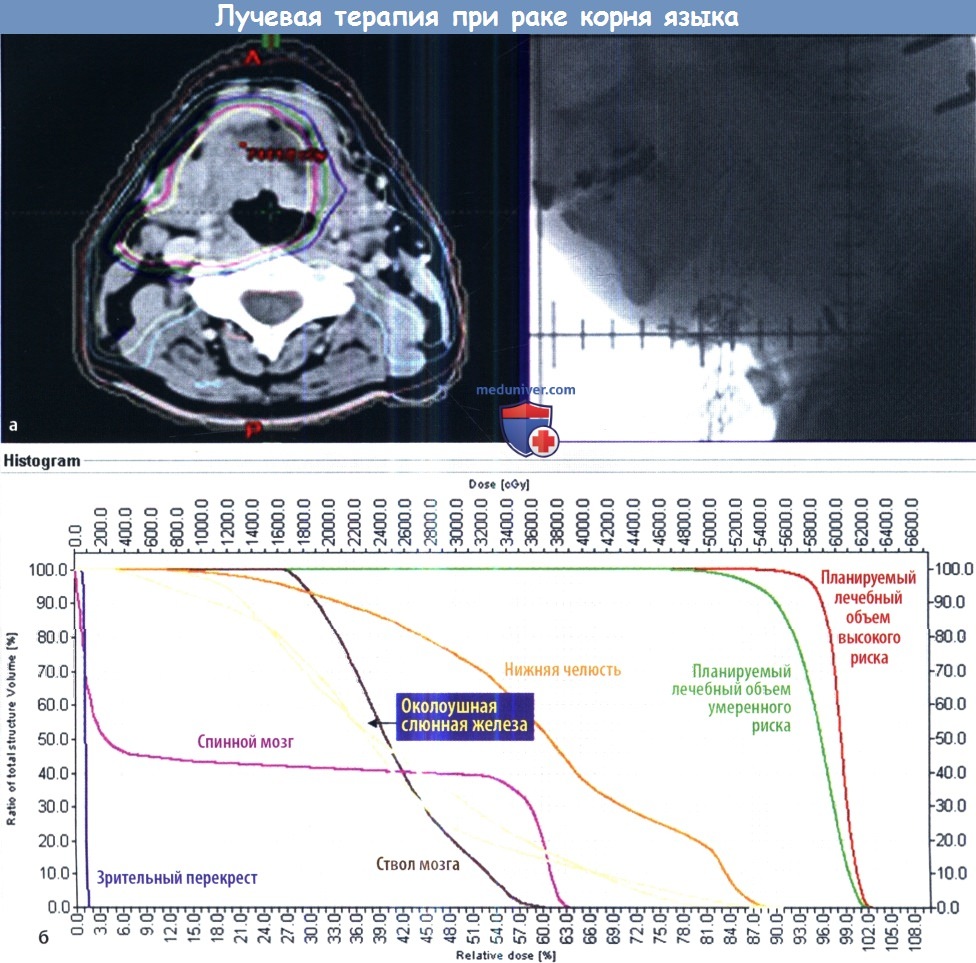
(а) Мужчина 62 лет болен раком корня языка стадии T2N2bM0. Проводилась наружная дистанционная лучевая терапия в сочетании с химиотерапией, брахитерапия и лимфодиссекция.
Облучение очага и первичных лимфоузлов проводилось в пониженной дозе в 5940 сГр, после чего проводился сеанс брахитерапии в дозе 20 Гр.
(б) Гистограмма доза-объем, демонстрирующая распределение дозы облучения в курсе лучевой терапии с модулированной интенсивностью.
Общие сведения о реабилитации
В настоящее время реабилитация онкологических больных приобретает все большее значение в связи с увеличивающимся числом излеченных больных (Герасименко В. Н., 1977).
Необходимо отметить, что выживаемость больных при раке далеко не равноценна полному выздоровлению.
Обширные хирургические операции, интенсивная лучевая, цитостатическая и гормональная терапия, используемые в онкологической практике, приводят к серьезным нарушениям различных функций организма.
Больной может считать себя здоровым только в том случае, если он сохраняет способность к нормальной жизни и работе. Конечной целью лечения является оказание помощи больному с тем, чтобы он снова мог занять свое прежнее положение в семье и обществе. Реабилитация онкологического больного должна рассматриваться как итог, достигнутый в области профилактики, диагностики и лечения злокачественного заболевания.
За последнее десятилетие накоплен значительный опыт в лечении больных злокачественными опухолями головы и шеи. Развитие методов комбинированного лечения привело к продлению жизни больных на многие годы. Как уже было отмечено, основным методом лечения больных с местнораспространенными злокачественными опухолями головы и шеи является комбинированный, где расширенное хирургическое вмешательство занимает ведущее положение.
Расширенные и комбинированные оперативные вмешательства в хирургии рака головы и шеи связаны с определенными трудностями, обусловленными прежде всего образованием послеоперационных дефектов, возможность закрытия которых местными тканями ограничена.
Кроме того, после расширенных операций по поводу местнораспространенных злокачественных опухолей головы и шеи возникают обезображивающие изъяны, ведущие к нарушению ряда важных функций, в частности, акта глотания, жевания, речи, дыхания. Поэтому удаление местнораспространенных злокачественных опухолей головы и шеи — это только один из этапов лечения больных.
Другой, не менее важной и ответственной задачей, является реабилитация этих больных, возвращение их к обычному образу жизни и труду, что достигается различными путями. С одной стороны, разрабатываются способы устранения послеоперационных дефектов с помощью лицевого (эктопротезы) и зубного протезирования (Чуйков В. М., 1976).
Это в известной мере позволяет уменьшить степень наносимых операцией функциональных и косметических нарушений. С другой стороны, имеются попытки устранения дефектов посредством косметических и функциональных пластических операций (Матякин Г. Г., 1977; Клим К. И., 1979).
Большинство авторов при удалении злокачественных новообразований считают целесообразным производить пластические операции, включающие наименьшее число этапов. В пользу преимущества первичных восстановительных операций высказываются Н. Н. Блохин (1956), Н. М. Михельсон (1962), П. В. Наумов (1966), А. Т. Аббасов (1967), И. А. Сорочан (1971), Б. М. Втюрин, К. И. Клим (1976), Н. Н. Блохин, Б. Е. Петерсон (1979).
В настоящее время продолжается поиск наиболее эффективных методов первичной пластики дефектов кожи и слизистой оболочки после расширенных и комбинированных операций в области головы и шеи.
Это ключ к хирургической реабилитации больных после расширенных операций. В этом плане мы на протяжении нескольких лет изучали возможность реабилитации больных с опухолями головы и шеи.
Поскольку расширенные и комбинированные операции по поводу местнораспространенных злокачественных опухолей слизистой оболочки полости рта, гортани и щитовидной железы приводят не только к обезображивающим дефектам, но и к нарушению функции глотания, дыхания, жевания и речи, мы решили осветить вопросы медицинской реабилитации больных с указанной локализацией опухоли.
Операции на слизистой оболочке органов полости рта
Первичная пластика послеоперационных дефектов слизистой оболочки органов полости рта
Первичную пластику послеоперационных дефектов слизистой оболочки органов полости рта мы выполняли при помощи шейного и дельто-пекторального кожно-фасциальных лоскутов на питающей сосудистой ножке. Первичная пластика шейным лоскутом применена у 22 больных, дельто-пекторальным лоскутом — у 7.
Шейный кожный лоскут на ножке выкраивается на боковой поверхности шеи в проекции грудино-ключично-сосцевидной мышцы с основанием в зачелюстной области. Такое расположение лоскута позволяет включить в него наиболее крупные артериальные сосуды кожи шеи, что обеспечивает хорошее кровоснабжение, высокую жизнеспособность его тканей, а непосредственная близость к ожидаемому дефекту позволяет восстановить поверхность образовавшегося изъяна в самых оптимальных условиях.
В отличие от других авторов, мы в подкожную клетчатку лоскута включаем и наружную яремную вену. Это значительно увеличивает жизнеспособность шейного лоскута. Заготовленный кожный лоскут имеет удлиненную языкообразную форму с округленными краями на конце. Ширина ножки лоскута составляет 5-7 см, длина — 10-14 см (рис. 64, а).

Рис. 64. Первичная пластика послеоперационных дефектов слизистой оболочки полости рта: а — разрез кожи и выкраивание шейного лоскута: б — этап перемещения шейного лоскута к дефекту; в — окончательный вид послеоперационной рамы. Формирование оростомы в зачелюстной области
Опрокидывание кверху выкроенного лоскута и широкая мобилизация кожи обеспечивают хороший обзор операционного поля, а также создают оптимальные условия для проведения операции на лимфатических путях шеи.
Наряду с этим опрокидывание лоскута и перегиб его питающем ножки на 180° на время выполнения основного этапа операции — удаления первичной опухоли и клетчатки шеи — позволяют оценить состояние его кровоснабжения. При адекватном кровоснабжении мы перемещали лоскут и пришивали его к краям дефекта тканей (рис. 64, б). В области основания питающей ножки формировали временную оростому (рис. 64, в).
Изучение особенностей заживления ран после 22 подобных операций (табл. 35) показывает, что полное приживление перемещенного лоскута отмечено у 10 больных. Некоторое натяжение трансплантата, которое наблюдалось при закрытии дефекта бокового отдела дна полости рта и языка, при закрытии изъянов, расположенных в области переднего отдела дна полости рта, привело к расстройству кровообращения с последующим краевым или более распространенным некрозом лоскутов.
При заживлении ран первичным натяжением с полным приживлением шейного лоскута реабилитация функций глотания и дыхания наступала в среднем в течение 1,5 месяца. В противном случае лечение затягивалось на более продолжительное время (в среднем 0,5 года).
На основании собственных наблюдений мы считаем, что показанием к использованию шейного лоскута на ножке являются дефекты слизистой оболочки отделов средней, задней трети и корня языка, дна полости рта, щек и ретромолярного пространства, а также большие кожные изъяны околоушно-жевательной, щечной, подчелюстной областей и сонного треугольника шеи.
Опыт показывает, что не следует использовать этот лоскут для замещения дефектов тканей переднего отдела дна полости рта, нижней губы и подбородка при сохранении непрерывности нижней челюсти, так как в результате натяжения тканей и перегиба питающей ножки возникает нарушение кровообращения в дистальном отделе лоскута.
Нецелесообразно использование шейного лоскута для пластики изъянов, если его питающая ножка до операции попадала в зону облучения. Примером успешной пластики шейным лоскутом может служить следующее клиническое наблюдение.
Больная П., 56 лет, находилась в отделении опухолей головы и шеи НИИ онкологии с 5.11.1977 г. по 12.01.1978 г. по поводу рака слизистой оболочки альвеолярного отростка нижней челюсти справа, IIIа стадии, T3N0M0. Биопсия № 180097 — плоскоклеточный ороговевающий рак.
Послеоперационное течение гладкое. Заживление раны первичным натяжением. 4.10.1977 г. под местным обезболиванием с помощью 20,0 мл 0,25% раствора новокаина произведено закрытие оростомы. В настоящее время здорова. Срок наблюдения — 8 лет.
Пластика дельто-пекторальным лоскутом
Возмещение послеоперационных дефектов слизистой оболочки дна полости рта, значительной части языка может быть успешно проведено дельто-пекторальным кожным лоскутом на медиальной питающей ножке.
После радикального удаления злокачественной опухоли с резекцией переднего сегмента нижней челюсти дистальный участок выкроенного лоскута вводят в полость рта через разрез тканей в подчелюстной области и помещают так, чтобы кожная поверхность его восполняла дефект слизистой оболочки дна полости рта и языка (рис. 66, а).

Рис. 66. Методика пластики дефектов мягких тканей слизистой оболочки дна полости рта и языка дельто-пекторальным лоскутом: а — раневая поверхность и дефекты тканей после удаления злокачественной опухоли; б — замещение дефекта мягких тканей слизистой оболочки дна полости рта кожей — дистальным участком дельто-пекторального лоскута на медиальном основании; в — окончательный вид послеоперационной раны. Формирование оростомы в подчелюстном треугольнике и застебление питающей ножки лоскута
Подкожную клетчатку лоскута по краям и среднюю часть его фиксируют несколькими узловатыми кетгутовыми швами к мышцам языка и жировой клетчатки кожи подчелюстной области. Затем накладывают узловатые шелковые швы между краями лоскута и дефекта слизистой оболочки полости рта, формируя культю языка, дно полости рта и подбородочную область (рис. 66, б).
В подчелюстном треугольнике у места введения дельто-пекторального лоскута в полость рта формируют оростому путем сворачивания лоскута в форме трубки эпидермисом внутрь. У основания лоскуту придается вид круглого кожного стебля (рис. 66, в).
Наши наблюдения позволяют говорить о том, что с целью создания контура дна полости рта следует использовать формирующие тампоны из быстротвердеющей пластмассы, покрытые йодоформной марлей. Ими закрывают участок кожного лоскута, восполняющий дефект тканей между слизистой оболочкой нижней губы и нижней поверхностью культи языка.
Тампон фиксируют лигатурами. Оростому закрывают турундой с ксероформом на ближайшие 2-3 недели, до полного приживления кожного трансплантата. После приживления лоскута в полости рта питающую ножку отсекают под местной анестезией.
Необходимо отметить, что, несмотря на благоприятное расположение сосудов в лоскуте, протяженность застебленной питающей ножки следует сократить до минимума, с тем чтобы предупредить перегибы, отрицательно отражающиеся на кровоснабжении трансплантата. Недопустимо также натяжение ножки. Избежать этих ошибок можно путем тщательного планирования пластической операции.
Описанный метод пластики послеоперационных дефектов мягких тканей переднего отдела слизистой оболочки дна полости рта и языка нами был использован у 7 больных (табл. 36) и у 2 — с дефектами щеки. Полное приживление лоскута имело место в четырех наблюдениях (рис. 67, а-в). Нарушение кровообращения в виде краевого некроза отмечено у трех больных.
Таблица 36. Непосредственные результаты пластики дельто-пекторальным лоскутом на медиальном основании


Рис. 67. Больной Л. со злокачественной опухолью дна полости рта. Блок удаленных тканей. Кратерообразная опухолевая язва охватывает ткани дна полости рта. языка, фронтальной и горизонтальной ветви нижней челюсти
В двух случаях — частичный некроз лоскута из-за присоединения банальной инфекции в подлоскутном пространстве. Иссечение некротизированных участков лоскута производили на 8-10-е сутки. К этому времени жизнеспособный участок лоскута срастался с подлежащими тканями и тем самым уменьшались возможность попадания слюны и инфекции под лоскут и его дальнейшее отторжение.
Следует отметить, что из двух больных, которым дефект слизистой щеки был возмещен дельто-пекторальным лоскутом, в обоих случаях было нарушение кровообращения в виде краевого и частичного некроза лоскута. Поэтому мы считаем, что дельто-пекторальный лоскут может с успехом применяться только при первичной пластике дефектов переднего отдела слизистой дна полости рта и языка.
Таким образом, наши наблюдения показали, что применение дельто-пекторального лоскута расширяет показания к хирургическому лечению и способствует реабилитации утраченных функций дыхания, глотания и речи в среднем в течение 1,5-2 мес у больных с местнораспространенными опухолями слизистой оболочки дна полости рта.
Из 30 больных, подвергшихся расширенным и комбинированным операциям по поводу местнораспространенного рака слизистой оболочки полости рта, которые жили 3 года и более, 13 занимались умственным трудом, 5 — физическим. Остальные 12 пациентов находились на II группе инвалидности.

Врачи в Вене в 2003 году провели первую в мире успешную пересадку человеку языка. Тогда это стало сенсацией, ведь до этого подобные операции проводились только на животных. Специалисты отмечали, что хоть пациент и не может первое время двигать языком и у него, скорее всего, будут проблемы с ощущением вкуса продуктов, в целом операция прошла успешно.
Анатомия органа
В медицинской энциклопедии язык определяется как мышечный орган полости рта. За этим сухим определением скрывается орган, состоящий из верхушки, тела и корня. По размеру и форме такой орган индивидуален у каждого человека. Весит язык 70-95 граммов.
Язык — крайне важный орган. Он участвует в обработке пищи при нахождении ее во рту, способствует ее продвижению и перемещению при жевании, перемешиванию со слюной. Также язык требуется, чтобы подготовленный пищевой комок правильно проглотился.

Язык отличается высокой чувствительностью — с его помощью можно определить наличие твердых (т. е. неразжеванных) комков или несъедобных фрагментов. Также с помощью языка разделяется дыхание на носовое и ротовое. И, естественно, язык принимает непосредственное участие в процессе говорения, влияет на артикуляцию и даже тембр голоса.
Если есть дефекты языка, например из-за пороков развития, у человека могут наблюдаться проблемы с артикуляцией, проблемы с едой, развиваются вторичные деформации зубов и прикуса. Как правило, патологические ситуации в таком случае корректируются с помощью операции. Уздечки, ожоги, обморожения — список повреждений языка довольно велик. Но во всех ситуациях есть варианты терапии, которые позволят восстановить работоспособность и функциональность языка.
Свое воздействие на работу языка могут оказывать воспалительные заболевания, развившиеся абсцессы и флегмоны, отечность органа. Такие проблемы также становятся причиной того, что человеку сложно есть и пить, а также разговаривать. Иногда могут развиться и проблемы с дыханием.
Одна из серьезных проблем, с которой может столкнуться человек, — опухоли языка. При этом доброкачественные встречаются редко, растут медленно и могут озлокачествляться. Вмешательство по коррекции ситуации также преимущественно оперативное.
На долю злокачественных опухолей приходится 16-2 5% образований и 60% раков слизистой оболочки полости рта. Опухоль такого плана может развиваться на фоне трещин, язв и папиллом. Раку языка по статистике чаще подвержены мужчины в возрасте 40-70 лет. Опухоль прогрессирует быстро, бывает болезненной и кровоточащей. Поражения бывают разные — от тех, что затрагивают кончик, до тех, что отмечаются в районе корня. Процесс лечения — хирургический, отдаленные метастазы нередко не появляются. Но прогнозы зачастую неблагоприятные.
И именно при онкологии языка проводили операцию по пересадке органа мужчине в Вене. Но при этом больше новостей о столь сложной и необычной операции не было.
Реконструкция
На данный момент врачи для реабилитации при утере части языка практикуют больше реконструкцию органа, то есть пластику. Такое вмешательство необходимо после проведенной резекции, то есть удаления части органа, пораженного опухолью. В зависимости от места локализации органа и масштаба вмешательства выбирается оптимальное решение по восстановлению языка. Так, пересадка требуется, если орган не может функционировать или возникла необходимость удалить его практически полностью. В журнале Jama Network, издаваемом Американской медицинской ассоциацией, есть большая статья, посвященная методам реконструкции языка.
Так, в ней указано, что для восстановления крупных дефектов языка используют кожные трансплантаты и локорегиональные лоскуты. Такие методы не обеспечивают необходимой гибкости и должного объема ткани, чтобы восстановление органа было более функциональным. Рабочей лошадкой, пишут авторы статьи, в ситуации с реконструкцией языка называют использование фасциокутального лоскута. Они выгодно отличаются небольшой толщиной при сохранении кожного покрова в донорской области. С помощью такого лоскута может закрываться даже глубокий дефект. Восстановительная пластика языка проводится тканями кожи, которые берут с предплечья, бедра или спины. Подбирают оптимальный донорский участок в зависимости от размера повреждения. Причем стараются забирать ткань с питающими сосудами и нервами, чтобы обеспечить более качественную реабилитацию.
C помощью специальных методик восстанавливают даже утерянные на три четверти языки. Реконструкции и пластика языка при наличии онкопатологии сложны тем, что развитие рака нередко сопровождается такими осложнениями, как прорастание новообразований в глубокие ткани полости рта. И тут надо решать сразу несколько проблем.
Комбинированная пластика с использованием нескольких трансплантатов выполняется у больных с распространенными процессами. Ее применение необходимо в тех случаях, когда повреждается несколько эпителиальных поверхностей (кожа, слизистая оболочка полости рта, придаточных пазух). Эти операции выполняются редко и являются одними из самых сложных.
Так, за последние 25 лет в нашей клинике РОНЦ им. Н.Н. Блохина РАМН выполнены 856 реконструктивных операций при замещении дефектов, образующихся после удаления местно-распространенных опухолей головы и шеи, из них у 154 (17,8%) больных применялись комбинированные пластические операции. Больных раком слизистой оболочки полости рта и ротоглотки, которым выполнены подобные операции, было 66 (7,7%). Первичная комбинированная пластика выполнена у 57 (86,4%) больных, отсроченная – у 9 (13,6%) больных. Распространенность опухолевого процесса у 42 больных соответствовала III-IV стадиям, 24 больных оперированы по поводу рецидива опухоли. Локализация опухолевого процесса была в следующих зонах (табл. 1).
Выбор вида пластики
Следует отметить, что для замещения дефектов средней зоны лица (щека, угол рта) можно использовать сравнительно ограниченное число вариантов пластики. В нашей клинике отдают предпочтение эполетному, лобно-теменно-затылочному лоскутам, а в последнее время все чаще применяют лучевой лоскут на микро-сосудистых анастомозах, преимуществом которого является одномоментность пластики, а донорский материал берется в зоне, где возможно скрыть последующую деформацию тканей.
Значительно больше вариантов пластического замещения при дефектах нижней зоны лица. В подавляющем большинстве это больные раком слизистой оболочки языка, дна полости рта, альвеолярного отростка нижней челюсти. Реже пластику приходится выполнять при распространенных опухолях нижней челюсти. Для замещения мягкотканых дефектов используют кожно-мышечные лоскуты: дельто-пекторальный, лоскуты с включением большой грудной либо кивательной мышц. Достоинством данных методик является хорошо выраженный осевой сосудистый рисунок, что определяет жизнеспособность лоскута. Недостаток использования лоскута с включением m. sternocleidomastoideus заключается в затруднении последующего контроля за регионарными зонами контралатеральной стороны шеи, что при раке полости рта имеет большое значение.
При необходимости одномоментного восстановления непрерывности нижней челюсти чаще используют реконструктивные титановые пластины, однако через 1,5-2 года требуется их замена либо выполнение костной пластики. Поэтому при отсутствии противопоказаний к выполнению операций с использованием микро-сосудистой техники применяют следующие свободные кожно-мышечно-костные лоскуты: лопаточный, малоберцовый, подвздошный, а также лоскут на сосудистой ножке с включением 5 ребра и большой грудной мышцы.
У 48 (72,7%) больных возникли различные осложнения:
частичное расхождение швов с образованием свищей и оростом;
частичный либо тотальный некрозы лоскутов;
Большинство этих осложнений к моменту выписки больных были ликвидированы консервативными методами. В 26 случаях наличие оростомы требовало пластического замещения дефекта (отсроченная пластика). Следует отметить, что у 18 из 26 пациентов оростома оформлена планово.
В случаях тотального некроза лоскута (7 пациентов), обусловленного проведением лучевой терапии по радикальной программе (50-70 Гр), рана зажила вторичным натяжением. Большинство больных, получивших полную дозу лучевой терапии, лечились в других клиниках.
При использовании титановых трансплантатов в одном случае через год после операции имел место перелом реконструктивной пластины, и непрерывность нижней челюсти была восстановлена новой пластиной.
У 4 больных отмечалось расхождение швов с обнажением пластины, что потребовало ее удаления.
В развитии указанных осложнений играют роль:
возраст и общее состояние больных;
наличие сосудистых нарушений, связанных с сопутствующими заболеваниями (сахарный диабет, гипертоническая болезнь, различные виды коагулопатий);
доза предоперационной радиотерапии;
технические погрешности в выкраивании лоскута, имевшие место в основном в период освоения методики.
Продолженный рост, рецидивы первичной опухоли, регионарные и отдаленные метастазы выявлены у 24 (36,4%) больных. Столь высокая частота их вполне объяснима, так как в анализируемой группе собраны наиболее тяжелые больные со значительной распространенностью процесса.
Рецидивы и продолженный рост первичной опухоли возникали, в основном, у пациентов, получавших радиотерапию в других учреждениях. Мы считаем эту группу больных прогностически неблагоприятной. Это объясняется тем, что первоначального поражения мы не видели и ориентировались лишь на размер остаточной опухоли. Операции, выполняемые после радикального курса терморадиотерапии, известны в литературе как "salvage surgery". Данные операции выполнены 27 больным.
От полугода и свыше 5 лет прослежены (78,8%) 52 пациента. В эти сроки живы 30 (45,5%) больных, из которых 12 прослежены свыше 5 лет. Без рецидивов и метастазов живы 26 (50%) больных. От прогрессирования процесса умерли 15 (28,8%) пациентов, от интеркурентных заболеваний и опухолей других локализаций - 7 (13,5%) больных; паллиативную химиотерапию получают 4 (7,7%) пациента с рецидивами опухоли и регионарными метастазами.
По нашим данным 98% пациентов, причиной смерти которых является продолженный рост, рецидив первичной опухоли или регионарные метастазы, умирают в течение 2-х лет после лечения. Столь невысокие показатели выживаемости вполне объяснимы и обусловлены крайне неблагоприятным прогнозом этих пациентов.
Полученные нами данные говорят, в первую очередь, о множестве разных вариантов закрытия послеоперационных дефектов у больных раком слизистой оболочки полости рта и ротоглотки с использованием комбинированной пластики, что позволяет не только продлить (сохранить) им жизнь, но и повысить функциональные и косметические результаты.

Бесплатная консультация по лечению в Москве.
Звоните 8 (800) 350-85-60 или заполните форму ниже:
Операция при раке слизистой оболочки полости рта — методика хирургического устранения злокачественной опухоли в пределах здоровых тканей. Как самостоятельный способ борьбы с заболеванием применяется редко, так как высок процент возобновления патологии. Поэтому проводится в комплексе с лучевой терапией. Патогенные клетки могут локализоваться в следующих органах и участках челюстно-лицевой области:
- • язык;
- • небо;
- • десна;
- • щека;
- • нижняя и верхняя челюсть.

Запущенная форма онкологии влечет за собой резекцию лицевых органов, тканей и костей. В результате возникают серьезные косметические дефекты лица пациента и нарушаются функции приема пищи, речи и дыхания. Для их возвращения проводится восстановительная пластика как во время основной процедуры по устранению онкообразования, так и после нее. Конкретика реконструктивных манипуляций зависит от сложности расположения карциномы и ее разрастания на соседние участки. Стоимость операции при раке слизистой оболочки полости рта включает в себя все медицинские мероприятия для сохранения здоровья и внешнего вида.
Если вам или вашим близким нужна медпомощь, свяжитесь с нами. Специалисты сайта посоветуют клинику, в которой вы сможете получить эффективное лечение:
Как проводится и сколько длится операция при раке слизистой оболочки полости рта?
Если онкообразование операбельное, то оперативные действия показаны после облучения. Хирург иссекает раковое образование, при этом захватывает 2-4 см здоровой ткани. Данный метод позволяет устранить поражение и добиться клинической ремиссии. На начальных стадиях эта патология излечивается в 90% случаев при комплексном лечении.
Наиболее распространенными местами поражения считается альвеолярный край обеих челюстей и твердое небо. При широком распространении заболевания резекции подвергается половина языка и часть челюсти. При этом следует обязательное извлечение шейных лимфоузлов. Челюстно-лицевая хирургия — крайне сложный технический процесс и занимает у врачей до нескольких часов.
При столь радикальных мерах наблюдаются серьезные последствия после операции по удалению рака слизистой оболочки полости рта. Если резецируются челюстные кости, то необходимо протезирование, которое восполнит отсутствующую кость и сохранит геометрию лица.
Стоимость операции по удалению рака слизистой оболочки полости рта
Операции бывают продолжительные и сложные, а бывают и такие, с которыми хирурги справляются за 10-20 минут. Именно сложность удаления рака определяет конечную цену на операцию, проводимую на слизистой оболочке полости рта в онкологических клиниках Москвы. Некоторые онкоцентры оказывают полный спектр услуг при диагностировании любого типа челюстной онкологии. Другим медучреждениям не хватает оснащенности для проведения максиллэктомии или глоссэктомии. Поэтому от укомплектованности онкоцентра и квалификации врачей будет зависеть и ценообразование.

Реабилитация после операции при раке слизистой оболочки полости рта
ЛФК и лечебная гимнастика считаются второстепенными способами восстановления и носят скорее психотерапевтический характер. В послеоперационный период при раке слизистой оболочки полости рта важно уделить большое внимание рациональному кормлению пациента. В первые дни оно осуществляется через носопищеводный зонд. Пища подается в кашеобразном состоянии не более 3 литров в сутки.
Зондовое питание сохраняет в покое прооперированную область, не позволяет загрязняться, что столь важно на послеоперационном этапе. Швы промывают раствором марганца. При правильной гигиене удается избежать остеомиелита и орофарингостомы.

Лечение рака слизистой оболочки полости рта в Израиле
Лечение рака слизистой оболочки полости рта в Израиле — это применение совокупности медицинских методик, направленных на.

Облучение при раке слизистой оболочки полости рта
Лучевая терапия при раке слизистой оболочки полости рта может практиковаться как самостоятельное лечение, в составе комбинированной.

Рак слизистой оболочки полости рта
Рак слизистой оболочки полости рта — это злокачественная опухоль, которая развивается из эпителия, выстилающего полость изнутри.

Лечение рака слизистой оболочки полости рта
Лечение рака слизистой оболочки полости рта — это применение комплекса методик в специализированных медучреждениях Москвы.

Бесплатная консультация по лечению в Москве.
Звоните 8 (800) 350-85-60 или заполните форму ниже:
Читайте также:

