От чего может быть острый миелобластный лейкоз у пожилых
Как уже отмечалось ранее, острый миелоидный лейкоз (ОМЛ) — болезнь пожилых людей: медиана возраста больных острым миелоидным лейкозом составляет 64 года. Острый миелоидный лейкоз (ОМЛ) у лиц старше 60 лет имеет особенности, обусловленные как их возрастом, так и биологическими характеристиками опухолевого процесса.
Прежде всего рассмотрим некоторые особенности острых нелимфобластных лейкозов у лиц старше 60 лет. Предполагают, что злокачественная трансформация кроветворной клетки, котороя становится источником опухоли, происходит на ранних этапах миелоидной дифференцировки, на что указывает и значительно более частое обнаружение экспрессии антигена CD34. Это, как известно, относится к неблагоприятным факторам прогноза. У пожилых людей практически в 3 раза чаще определяется предшествующая миелодисплазия, что однозначно связывают с плохим прогнозом заболевания.
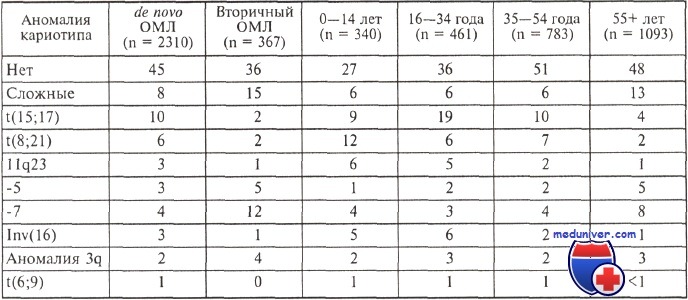
Существенно выше и процент обнаружения неблагоприятных хромосомных аберраций (особенно -5,-7,5q-,7q-,+8), притом что редко диагностируют формы заболевания с благоприятным кариотипом. Эти биологические особенности острого миелоидного лейкоза у пожилых пациентов определяют более низкую эффективность химиотерапии.
Помимо особенностей лейкемического процесса, у пожилых больных следует учитывать неизбежные функциональные изменения в организме, которые связаны со старением и которые обусловливают худшую переносимость лечения и как следствие этого его более низкую эффективность, поскольку приходится уменьшать дозы лекарственных препаратов и увеличивать интервалы между их введением.
Одними из наиболее значимых являются нарушения деятельности сердечно-сосудистой системы, которые выражаются в дистрофии миокарда вследствие атеросклеротического процесса и соответственно изменения метаболизма мышцы сердца, а в терапии острого миелоидного лейкоза (ОМЛ) базисными препаратами являются антрациклиновые антибиотики (даунорубицин, идарубицин), оказывающие кардиотоксическое действие. В процессе старения также отмечается прогрессирующее снижение функции почек. Величина эффективного почечного кровотока у практически здоровых пожилых людей снижается более чем в 2 раза и составляет в среднем 42 % от его величины у людей молодого возраста.
К глубокой старости (80 лет) более чем в 3 раза снижается азотвыделительная функция почек. В связи с этим может изменяться клиренс лекарственных препаратов, в результате чего может увеличиваться их токсическое действие. Кроме того, многие лекарственные препараты, используемые в программах химиотерапии и вспомогательного лечения (цитостатические, антибактериальные, противогрибковые, противовирусные), характеризуются выраженной нефротоксичностью. Главной проблемой при проведении вспомогательной терапии становится сочетанная токсичность применяемых препаратов, оказывающих повреждающее действие на ткань почек.
Рассматривая метаболизм и клиренс цитостатических и других лекарственных препаратов у пожилых пациентов, следует упомянуть о структурных и функциональных изменениях печени, в основе которых лежит процесс возрастной атрофии клеток ее паренхимы. Значительно изменяется кровоснабжение печени, снижаются ее белковосинтетическая и антитоксическая функции, существенно снижается активность эндоплазматического ретикулума гепатоцитов.
Возрастные изменения в деятельности желудочно-кишечного тракта характеризуются нарушением эвакуаторной функции желудка, изменениями кровоснабжения кишечника, уменьшением всасывания, что также может оказывать влияние на эффективность лечения лейкоза у пожилых больных. Таким образом, изменения, происходящие в органнизме при старении, несомненно, отражаются на эффективности терапии, обусловливая ее более высокую токсичность и худшую переносимость у пожилых больных.
При оценке эффективности терапии острого миелоидного лейкоза исключение из группы анализируемых пациентов старше 70 лет способствует повышению показателей достижения ремиссии на 15—20 %. Отмечено, что лиц пожилого возраста реже включают в какиелибо исследования, которые предполагают жесткое выполнение цитостатического протокола и терапии выхаживания. Соответственно шансов на достижение длительной безрецидивной выживаемости у них значительно меньше.
Тем не менее следует подчеркнуть, что при отсутствии явных соматических заболеваний больные любого возраста удовлетворительно переносят программы терапии, предусмотренные для соответствующего типа острого лейкоза, и у них удается достичь полные ремиссии достаточной продолжительности.

Острый миелобластный лейкоз (ОМЛ) — термин, который объединяет ряд острых миелолейкозов, характеризующихся развитием сбоев в механизме созревания миелобластов.
На ранних этапах развития болезнь проявляется бессимптомно и диагностируется слишком поздно.
Чтобы выявить лейкоз своевременно, необходимо знать, что это такое, какие симптомы говорят о начале развития заболевания и какие факторы влияют на его возникновение.
Код МКБ-10
Код заболевания — C92.0 (Острый миелобластный лейкоз, относится к группе миелоидных лейкозов)
Что это такое?
ОМЛ — злокачественная трансформация, охватывающая миелоидный росток кровяных клеток.
Пораженные кровяные тельца постепенно заменяют здоровые, и кровь перестает полноценно выполнять свою работу.
Это заболевание, как и другие типы лейкозов, именуют раком крови в повседневном общении.
Слова, из которых состоит это определение, дают возможность понять его лучше.
Лейкоз. При лейкозе измененный костный мозг начинает активно вырабатывать лейкоциты — кровяные элементы, которые ответственны за поддержание иммунной системы — с патологической, злокачественной структурой.
Они замещают собой здоровые лейкоциты, проникают в разные части организма и формируют там очаги поражения, схожие со злокачественными новообразованиями.

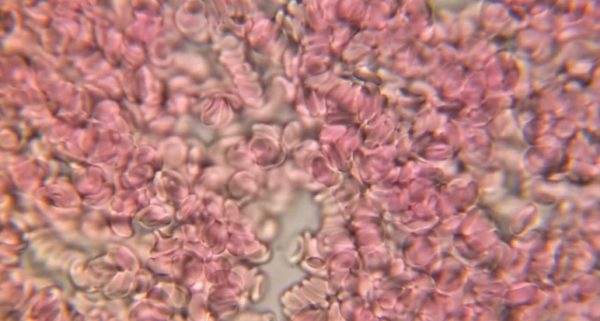
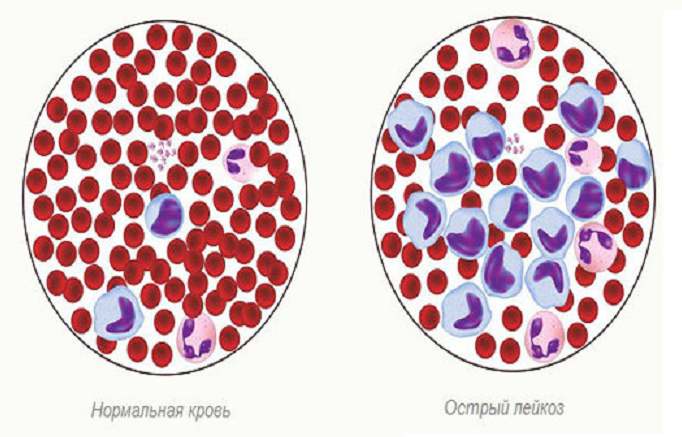
Отличия здоровой крови от больной лейкозом
Миелобластный. При ОМЛ начинается избыточное продуцирование пораженных миелобластов — элементов, которые должны превратиться в одну из разновидностей лейкоцитов.
Они вытесняют здоровые элементы-предшественники, что приводит к дефициту других кровяных клеток: тромбоцитов, эритроцитов и нормальных лейкоцитов.
Острый. Это определение говорит о том, что продуцируются именно незрелые элементы. Если пораженные клетки находятся в зрелом состоянии, лейкоз называется хроническим.
Острый миелобластоз отличается стремительным прогрессированием: миелобласты в крови разносятся по организму и вызывают тканевую инфильтрацию.

Симптомы
Обычно ОМЛ развивается у взрослых и пожилых людей. Ранние стадии миелобластной лейкемии характеризуются отсутствием ярко выраженной симптоматики, но, когда заболевание охватило организм, возникают серьезные нарушения многих функций.
Развивается из-за тканевой инфильтрации под действием лейкоза. Разрастаются периферические лимфоузлы, увеличивается селезенка, нёбные миндалины, печень.
Поражаются лимфоузлы области средостения: если они разрастаются значительно, то передавливают верхнюю полую вену.
Кровоток в ней нарушается, что сопровождается возникновением отечности в зоне шеи, учащенного дыхания, синюшности кожных покровов, набуханием сосудов на шее.
Также поражаются десна: появляется стоматит Венсана, который характеризуется развитием тяжелых симптомов: десны отекают, кровоточат и сильно болят, есть и ухаживать за полостью рта затруднительно.

Более половины больных имеют те или иные его проявления, развивается из-за острой нехватки тромбоцитов, при которой стенки сосудов истончаются, нарушается свертывание крови: наблюдаются множественные кровотечения — носовые, внутренние, подкожные, которые долгое время не удается остановить.
Увеличивается риск геморрагического инсульта — кровоизлияния в мозг, при котором летальность составляет 70-80%.
На ранних стадиях острого миелобластного лейкоза нарушение свертываемости проявляется в виде частых носовых кровотечений, кровоточивости десен, синяков на разных частях тела, которые появляются от незначительных воздействий.
Характеризуется появлением:
- Выраженной слабости,
- Быстрой утомляемости,
- Ухудшением трудоспособности,
- Раздражительности,
- Апатии,
- Частых болей в голове,
- Головокружений,
- Обмороков,
- Стремления есть мел,
- Сонливости,
- Болей в области сердца,
- Бледности кожи.
Затруднена даже незначительная физическая активность (наблюдается сильная слабость, учащенное дыхание). Волосы при анемии часто выпадают, ногти ломкие.
Температура тела повышена, вес падает, аппетит пропадает, наблюдается слабость и избыточное потоотделение.
Начальные проявления интоксикации наблюдаются на начальных этапах развития заболевания.
Если инфильтрация затронула мозговые ткани, это ухудшает прогноз.
Наблюдается следующая симптоматика:
- Многократная рвота,
- Острая боль в голове,
- Эпиприступы,
- Обмороки,
- Внутричерепная гипертензия,
- Сбои в восприятии реальности,
- Нарушения слуха, речи и зрения.
Развиваются на поздних стадиях заболевания, когда количество пораженных миелобластов в крови становится выше 100000 1/мкл.
Кровь густеет, ток крови становится медленным, нарушается кровообращение во многих органах.
Мозговой лейкостаз характеризуется возникновением внутримозговых кровотечений. Нарушается зрение, возникает сопорозное состояние, кома, возможен летальный исход.
При легочном лейкостазе наблюдается учащенное дыхание (возможно возникновение тахипноэ), озноб, повышение температуры. Количество кислорода в крови сокращается.
При остром миелобластном лейкозе иммунная система крайне уязвима и не способна защищать организм, поэтому высока восприимчивость к инфекциям, которые протекают тяжело и с массой опасных осложнений.
Причины
Точные причины развития ОМЛ неизвестны, но существует ряд факторов, которые увеличивают вероятность развития заболевания:
- Радиационное облучение. В группе риска люди, которые взаимодействуют с радиоактивными материалами и приборами, ликвидаторы последствий ЧАЭС, пациенты, проходящие лучевую терапию при другом онкологическом заболевании.
- Генетические заболевания. При анемии Факони, синдромах Блума и Дауна риск развития лейкоза увеличивается.
- Воздействие химических веществ. Химиотерапия при лечении злокачественных заболеваний негативно воздействует на костный мозг. Также вероятность повышается при хроническом отравлении ядовитыми веществами (ртуть, свинец, бензол и прочие).
- Наследственность. Люди, близкие родственники которых страдали лейкозами, также могут заболеть.
- Миелодиспластический и миелопролиферативный синдромы. Если лечение одного из этих синдромов будет отсутствовать, заболевание может трансформироваться в лейкоз.
У детей крайне редко фиксируется этот тип лейкоза, в группе риска — люди старше 50-60 лет.
Формы ОМЛ
Миелобластная лейкемия имеет ряд разновидностей, от которых зависит прогноз и тактика лечения.
| Название и классификация по FAB | Описание |
| ОМЛ с незначительной дифференциацией (М0). | Низкая восприимчивость к химиотерапевтическому лечению, легко приобретает резистентность к ней. Прогноз неблагоприятный. |
| ОМЛ без созревания (М1). | Отличается стремительным прогрессированием, бластные клетки содержатся в большом количестве и составляют порядка 90%. |
| ОМЛ с созреванием (М2). | Уровень моноцитов при этой разновидности — менее 20%. Не меньше 10% миелобластных элементов развиваются до стадии промиелоцитов. |
| Промиелоцитарный лейкоз (М3). | В костном мозгу интенсивно накапливаются промиелоциты. Относится к наиболее благоприятным по течению и прогнозу лейкозам — в течение 10-12 лет живут не менее 70%. Симптоматика схожа с остальными разновидностями ОМЛ. Лечится с применением оксида мышьяка и третиноина. Средний возраст заболевших — 30-45 лет. |
| Миеломоноцитарный лейкоз (М4). | Диагностируется у детей чаще, чем другие разновидности заболевания (но в целом ОМЛ в процентном соотношении, по сравнению с другими типами лейкозов, выявляется у детей редко). Лечится с применением интенсивной химиотерапии и пересадки стволовых клеток (ТГК). Прогноз неблагоприятный — показатели выживаемости в течение пяти лет — 30-50%. |
| Монобластный лейкоз (М5). | При этой разновидности в костном мозгу содержится не менее 20-25% бластных элементов. Лечится химиотерапией и ТГК. |
| Эритроидный лейкоз (М6). | Редко встречающаяся разновидность. Лечится с применением химиотерапии и пересадки стволовых клеток. Прогноз неблагоприятный. |
| Мегакариобластный лейкоз (М7). | Этой разновидности ОМЛ подвержены люди с синдромом Дауна. Характеризуется быстрым течением и низкой восприимчивостью к химиотерапии. Детские формы болезни чаще текут благоприятно. |
| Базофильный лейкоз (М8). | Чаще встречается в детском и юношеском возрасте, прогноз жизни М8 неблагоприятный. Помимо злокачественных элементов, в крови выявляются аномальные элементы, которые затруднительно выявить без специального оборудования. |
Также, помимо упомянутых разновидностей, существуют и другие редкие виды, не внесенные в общую классификацию.
Диагностика
Острая лейкемия выявляется с применением ряда диагностических мероприятий.
Диагностика включает в себя:
- Развернутый анализ крови. С его помощью выявляется содержание в крови бластных элементов и уровень остальных кровяных телец. При лейкемии обнаруживается избыточное количество бластов и сниженное содержание тромбоцитов, зрелых лейкоцитов, эритроцитов.
- Взятие биоматериала из костного мозга. Применяется для подтверждения диагноза и проводится после проведенных обследований крови. Этот метод применяется не только в процессе диагностики, но и на протяжении лечения.
- Биохимический анализ. Дает информацию о состоянии органов и тканей, содержании различных ферментов. Этот анализ назначается для получения развернутой картины поражения.
- Другие виды диагностики: цитохимическое исследование, генетическое, УЗИ селезенки, брюшной полости и печени, рентген зоны груди, диагностические мероприятия для выявления степени поражения головного мозга.
Могут быть назначены и другие методы диагностики, в зависимости от состояния пациента.
Лечение
Лечение ОМЛ включает применение следующих методов:
- Химиотерапия. Медикаменты воздействуют на клетки, подавляя их активность и размножение. Ключевой метод лечения лейкемии.
- Консолидация. Лечение, назначаемое во время ремиссии, нацелено на снижение вероятности рецидива.
![]()
Трансплантация стволовых клеток. Пересадка костного мозга при лейкозе применяется при лечении больных младше 25-30-летнего возраста и необходима в тех ситуациях, когда заболевание течет неблагоприятно (наблюдается нейролейкоз, концентрация лейкоцитов крайне высока). Пересаживаются либо собственные клетки, либо донора. Обычно донорами становятся близкие родственники.- Дополнительная терапия. Восстанавливает состояние крови, включает введение кровяных элементов.
Также может быть применена иммунотерапия — направление, использующее иммунологические препараты.
Применяются:
- Медикаменты на основе моноклональных антител,
- Адаптивная клеточная терапия,
- Ингибиторы контрольных точек.
При таком диагнозе, как острый миелолейкоз, продолжительность лечения составляет 6-8 месяцев, но может быть увеличена.
Прогноз жизни
Прогноз зависит от следующих факторов:
- Типа ОМЛ,
- Чувствительности к химиотерапии,
- Возраста, пола и состояния здоровья пациента,
- Уровня лейкоцитов,
- Степени вовлеченности головного мозга в патологический процесс,
- Продолжительности ремиссии,
- Показателей генетического анализа.
Если заболевание чувствительно к химиотерапии, концентрация лейкоцитов умеренная, а нейролейкоз не развился, прогноз положительный.
При благоприятном прогнозе и отсутствии осложнений выживание в течение 5 лет составляет более 70%, частота рецидивов менее 35%. Если состояние пациента осложнено, то выживаемость равняется 15%, при этом рецидивировать состояние может в 78% случаев.
Чтобы своевременно выявить ОМЛ, необходимо регулярно проходить плановые медицинские обследования и прислушиваться к организму: частые кровотечения, быстрая утомляемость, возникновение синяков от небольшого воздействия, длительное беспричинное повышение температуры могут говорить о развитии лейкоза.
Видео: Острый миелолейкоз
Острый миелобластный лейкоз (ОМЛ) – это злокачественный процесс в костном мозге, нарушающий функцию кроветворения. Заболевание поражает миелоидный росток. Здоровая клетка лейкоцит не созревает и выходит в кровоток в изменённом виде. Начинается неконтролируемое деление. Лейкоциты лишены способности защищать организм от микроорганизмов и инфекций. Угнетается производство эритроцитов и тромбоцитов. Начинает развиваться анемия и тромбоцитопения. Изменяется состав периферической крови.
Причины, провоцирующие развитие болезни, до конца не изучены. Учёные связывают ряд факторов с мутациями кроветворной системы, к примеру, наследственность, облучения или генетические аномалии.
Миелоидная лейкемия наиболее часто диагностируется у взрослых пациентов. Болезнь поражает людей после 50 лет. Пик развития рака приходится на 63 года. Миелоидному лейкозу больше подвержены пожилые мужчины. Среди молодого поколения одинаково страдают представители обоих полов.
У детей заболевание носит первичный характер. Ребёнок подвергается лейкозу при аномалиях в генетическом коде, при контакте матери с тяжёлыми отравляющими веществами (радиация, канцерогены) или если история болезней кровных родственников содержит онкологические патологии. Симптомы болезни как у взрослых.
В начале заболевания клиническая картина смазана. Постепенно больной замечает необычные изменения в состоянии. При остром течении болезни пациент отмечает симптомы самочувствия:

- Утомляемость;
- Одышка;
- Синяки и мелкие кровоподтеки;
- Кровоточивость слизистой ротовой полости;
- Инфекционные поражения организма, не поддающиеся классическому лечению и имеющие ярко выраженную симптоматику.
Для лейкозов терминальной стадии развития костный мозг лишается работоспособности, метастазы поражают органы и системы человеческого тела. Для этого характерны признаки:
- Значительное снижение веса;
- Бледность кожных покровов;
- Желудочно-кишечные и носовые кровотечения;
- Слабость;
- Боль и ломота в костях;
- Обмороки;
- Рвота с кровью;
- Чёрный стул;
- Боли в животе;
- Если поражается мочеполовая система, отмечается частичная или полная задержка мочи.
Лечением занимаются онкогематологи. Код по МКБ-10 миелолейкоза С92.
Классификация онкологической патологии
Нелимфобластный лейкоз представляет группа подвидов болезни. Для каждого вида шансы выживаемости и тактика лечения подбираются индивидуально.
Система ФАБ состоит из 9 разновидностей острого миелоидного лейкоза. Формы отличаются по типам предшественников лейкоцитов и степеням их зрелости. Клетки определяют при проведении микроскопического и цитогенетического исследования.
- Показатель М0 означает минимально-дифференцированную острую миелоидную лейкемию.
- М1 характеризует миелоцитарный лейкоз без созревания. В единичных бластах обнаруживаются азурофильные гранулы и палочки Ауэра.
- При М2 для лейкоза характерно созревание. Бласты преимущественно с палочками Ауэра и азурофильными гранулами.
- М3 обозначает острую форму промиелоцитарного рака крови. Клетки гипергранулированы. Палочки Ауэра присутствуют множественно.
- М4 представляет острый миеломонобластный онкологический процесс.
- При М4ео наблюдается миеломоноцитарная патология с повышенным уровнем эозинофилов в костном мозге.
- М5 определяет острый монобластный (-цитарный) лейкоз.
- М6 характеризует острые эритроидные заболевания крови.
- М7 означает мегакариобластную лейкемию.
- Подвид М8 представляет базофильное малокровие.
Исследования при лейкозах
Диагностика лейкозов заключается в изучении состава крови и костного мозга. Точный диагноз определяется только после забора биоптата из бедра или ребра для дальнейшего исследования.
Вначале проводят анализ крови. Наблюдаются отклонения в показателях лейкоцитов. Результат может быть представлен от 0,1*109/л до 10*100*109/л. Небольшие нарушения свидетельствуют о монобластной лейкемии или о эритромиелозе. В сыворотке крови не обнаруживаются базофилы. Скорость оседания эритроцитов (СОЭ) увеличена.
Эритроциты представлены низкими показателями. В крови преобладают бласты и клетки зернистого ряда. Отмечаются созревшие моноциты. Снижен уровень гемоглобина.
С помощью биохимического исследования определяется количество общего белка, билирубина, альбумина, мочевины и креатинина.

Для острого лейкоза первой фазы анализ крови может иметь следующую картину:
- Показатели общего белка – 78 ммоль/л.
- Общего билирубина – 14-17 ммоль/л.
- Прямого билирубина – 3,5-4,5 ммоль/л.
- Уровень креатинина – 108 мкмоль/л.
Благодаря цитохимическим показателям изучается активность ферментов, состав крови, костного мозга и других тканей организма.
Иммунологический тест является комплексным исследованием нарушений в работе иммунитета. Для анализа используют венозную кровь. Определяются иммунные клетки, их функции, активность и способность уничтожать бактерии.
Для выявления метастазов в миокарде используют электрокардиограмму и эхокардиографию.
Ультразвуковая диагностика выявляет отклонения во внутренних органах человека. Метод позволяет изучить печень, органы желудочно-кишечного тракта и мочеполовой системы, лимфатические узлы.
Вариант глобальной диагностики всех органов и систем представлен проведением магнитно-резонансной и компьютерной томографии. Методы послойно сканируют участки тела. Выявляются даже незначительные изменения в тканях.
Лечебная тактика
На первом этапе лечения назначенные препараты без разбора убивают здоровые и раковые клетки. Развиваются побочные явления:
- Тошнота;
- Рвота;
- Вялость;
- Язвенные поражения полости рта;
- Назальные кровотечения;
- Организм больного подвержен присоединению опасных инфекций.
На втором этапе назначают несколько курсов цитостатиков. Для уничтожения рака важен приём высокой дозы цитозин-арабинозида. Препарат препятствует созданию частиц, переносящих наследственную информацию. При печёночной и почечной недостаточностях или угнетении костного мозга приём препарата запрещен.
Для угнетения функций костного мозга и борьбы с опухолевыми клетками назначают Идарубицин.
Митоксантрон подавляет иммунитет и уничтожает опухоли.
Для достижения максимальной эффективности используют протоколы с тремя блоками постремиссионной химии.
Прогноз жизни на фоне химиопрепаратов значительно улучшается.
При поражении органов центральной нервной системы рекомендована лучевая терапия. Ионизирующее излучение вступает в реакцию с аномальными клетками, нарушает их структуру и провоцирует гибель.
Среди людей ходят истории об исцелении рака крови с помощью народной медицины. Однако ни один метод или препарат не показал 100% эффективности. Отказываясь от врачебного вмешательства, больной позволяет лейкозу стремительно развиваться и нарушать работу жизненно важных органов! Лечением может заниматься только квалифицированный врач онколог после проведения тщательной диагностики. Нетрадиционные методы обычно только усугубляют течение болезни.
Полное выздоровление наступает после пересадки костного мозга. Метод имеет нюансы и последствия:
- До начала проведения операции (вливание донорского материала через установленный в артерию катетер) больному уничтожают костный мозг с помощью ударных доз химиотерапии.
- При отсутствии иммунитета любые инфекции и болезни, к примеру, ОРЗ или царапина могут привести к летальному исходу.
- Трансплантируемый материал может не взаимодействовать с организмом пациента:
- В первом случае чужой костный мозг организм человека воспринимает за чужеродный и отторгает его. Нарушается работа всех органов. Иммунные клетки убивают все на своем пути. Однако при этом окончательно уничтожаются раковые клетки без возможности развиться снова. Иммуносупрессивная терапия помогает наладить нормальный кроветворный процесс.
- Организм пациента отвергает введенные стволовые клетки. Иммунитет не формируется. Выработка кровяных телец не начинается.
- При введении биоматериала развивается аллергия или анафилактический шок.
- Половина пациентов умирают в первый месяц после операции.
Подходящий костный мозг трудно достать. Лучшими донорами являются однояйцевые близнецы, родные братья и сестры. Материал родителей подходит очень редко.
Стволовые клетки могут быть взяты у самого пациента в период ремиссии или у постороннего человека.
Прогнозы на жизнь
Шанс на полное выздоровление имеют 90% пациентов до 60 лет. Пожилой организм не справляется с раком и нагрузками при химиотерапии. Пациент до конца жизни использует паллиативное лечение. Пятилетняя выживаемость пожилых людей составляет 12-25%.
Шанс на выживаемость снижается при наличии сопутствующих онкологических проблем или заболеваний генетического типа (болезнь Дауна). Рецидив развивается в любой момент. Вторичное заболевание не поддаётся лечению.
Если больной в течение 5 лет не отмечал симптомы лейкоза и не обращался за помощью, его снимают с онкологического учёта и считают здоровым.
Специфическая профилактика лейкемии отсутствует.
Лейкоз — одна из самых опасных форм онкологического заболевания, которую иначе можно назвать рак крови. Опухоли при этом зарождаются в кровяных клетках, тем самым нарушая весь процесс кроветворения.
В медицине выделяют миелоидную (миелобластную) и лимфоидную формы лейкоза в зависимости от того, в каких клетках был запущен раковый процесс.
Что такое острый миелоидный лейкоз?
Острый миелобластный (миелоидный, миелоцитарный, нелимфобластный) лейкоз — это онкологический процесс, который возникает из-за нарушений в цепочке ДНК незрелых кровяных клеток и клеток костного мозга.
При заболевании чрезмерно активному делению подвержены клетки лейкоциты, что неизбежно ведет к снижению численности тромбоцитов, эритроцитов и здоровых лейкоцитов.
Из всех видов острого лейкоза, миелобластная форма встречается чаще всего, причем может обнаруживаться в любом возрасте.
Однако у детей это заболевание диагностируется лишь в 15% случаев нарушений кроветворения, тогда как остальные 85% приходятся на острый лимфобластный лейкоз.
Справка! Острый миелоцитарный лейкоз чаще встречается у детей до 14 лет. Пик заболеваемости приходится на возраст 2-5 лет.
Острый миелолейкоз (код по МКБ 10- С92.0) протекает значительно быстрее, чем его хроническая форма, и в этом его опасность.
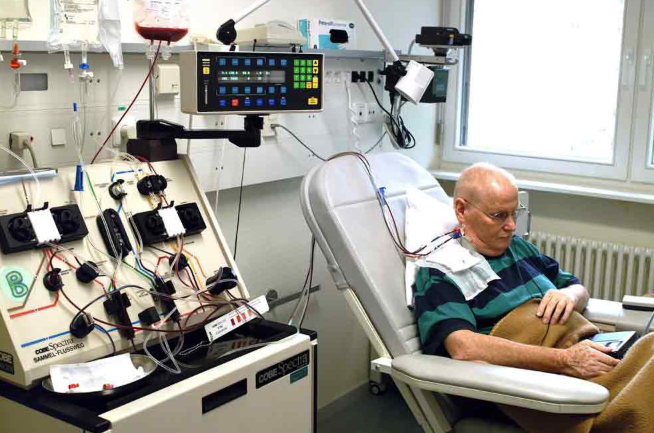
Иногда миелобластный лейкоз обнаруживается уже на той стадии, когда единственный метод лечения — трансплантация костного мозга.
В медицине до сих пор нет единого мнения относительно причин дефекта размножения бластных клеток.
Часто факторами риска называют:
- воздействие радиации,
- отравление химическими веществами,
- курение,
- неблагоприятную экологическую среду,
- генетическую предрасположенность (если у кого-то из родственников был диагностирован лейкоз).
Нередко предшественником заболевания является другое нарушение кроветворения (миелодиспластический синдром) или определенные генетически обусловленные аномалии (синдром Дауна, анемия).
Что такое острый миелолейкоз рассказывается на видео:
Прогноз жизни у взрослых
Острый миелобластный лейкоз развивается очень стремительно, поэтому диагностировать заболевание часто удается только на поздних стадиях. Если человек и вовсе не обратился к врачу, всего за несколько недель наступает летальный исход.
У данного диагноза есть существенная особенность: чем старше пациент, тем ниже вероятность благоприятного исхода. Так, у людей старше 60 лет длительная ремиссия возможна лишь в 5-15% случаев.
Дальнейшие прогнозы зависят от многих факторов: от своевременности диагностики, возраста и состояния здоровья пациента, эффективности лечения. У людей среднего возраста миелолейкоз, обнаруженный на первых стадиях, приводит к благоприятному исходу в единичных случаях.
Справка! Под благоприятным исходом имеется в виду полное выздоровление, когда рецидивов не случается более 5-6 лет после лечения.
Выживаемость до 6 лет встречается в 40-55% случаев.
Можно ли вылечиться?
Несмотря на сложность и быстротечность данного заболевания, шансы на полное выздоровление все же есть, пусть и не большие.
К примеру, хроническая форма миелобластного лейкоза стала первым видом рака крови, для которого было разработано комплексное целенаправленное лечение. Благодаря новым технологиям удается добиться полного излечения гораздо чаще.
Что же касается острого миелобластного лейкоза, основными способами лечения по-прежнему остаются:
- химиотерапия,
- медикаментозная терапия,
- трансплантация стволовых клеток.
Внимание! Проблема последнего самого эффективного метода в поиске подходящего донора, дороговизне и больших очередях. Поскольку при миелолейкозе счет идет не на месяцы, а на дни, многие пациенты даже не успевают дождаться своей очереди.
Кроме того, поиском донора занимается семья больного, а не медицинское учреждение. При всем этом, если саму трансплантацию оплачивает государство, то оплата транспортировки материала — задача больного и его семьи.
В России банк костного мозга весьма скудный, поэтому часто приходится привозить материал из Европы, США и других стран, что может обойтись в сумму, неподъемную обычным семьям.
Иными словами, трансплантация костного мозга увеличивает шансы на полное выздоровление, но возможность быстро найти донора и средства для трансплантации (транспортировки, реабилитации), особенно без очереди, практически отсутствует.
Справка! Вероятность полного излечения в клинических условиях без трансплантации костного мозга достигает 20-45% при условии, что лейкоз был обнаружен на I или II стадиях.
Рецидивы же чаще всего возникают прямо во время лечения или восстановления (в течение 100 дней после курса терапии). При ремиссии длительностью 5 лет рецидивы случаются очень редко.
На видео рассказывается, почему погибают от лейкоза:
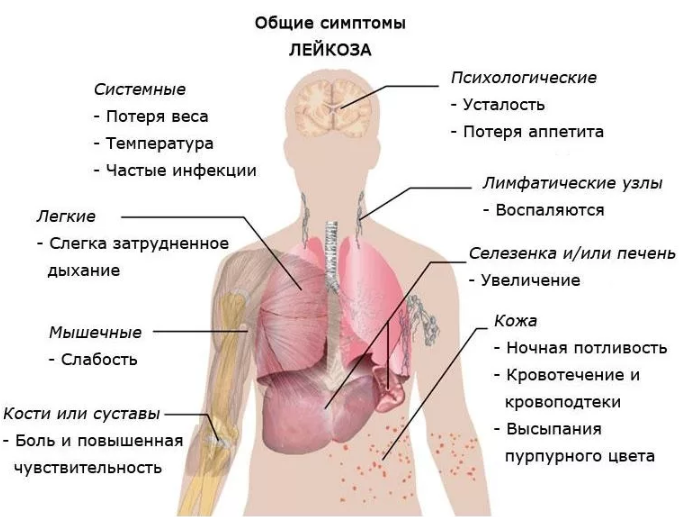
Симптомы
Поскольку при лейкозе аномально делиться начинают только одни кровяные тельца, наблюдается дефицит других. Чаще всего заболевание характеризуется бледностью кожных покровов, иначе — признаками анемии. Бледность кожи может сопровождаться одышкой, слабостью и утомляемостью.
Из-за недостатка тромбоцитов снижается свертываемость крови, поэтому могут наблюдаться чрезмерная кровоточивость даже небольших ран и царапин, носовые кровотечения, появление гематом и синяков без предшествующих ушибов.
Снижение иммунной системы из-за дефицита здоровых лейкоцитов приводит к частым инфекциям, которые с трудом поддаются лечению. Отмечаются поражения слизистых оболочек рта и желудка, небольшое повышение температуры, припухлость десен, боли в костях.
Диагностика
Ключевым методом диагностики острого миелолейкоза является клинический анализ крови, на котором, как правило, отчетливо выражен недостаток одних клеток (чаще тромбоцитов и эритроцитов) и избыток других (незрелых лейкоцитов). Однако на основании одного исследования крови ставить диагноз нельзя.
Обязательно исследуется образец костного мозга, который позволяет с точностью диагностировать лейкоз.
Справка! По данным ВОЗ, основанием для постановки диагноза является выявление не менее 20% миелобластов в костном мозге.
Для назначения лечения одного только подтверждения диагноза недостаточно.
Врачу необходимо как можно скорее определить форму заболевания: лимфобластный лейкоз отделить от миелобластного, лейкоз — от миелобластического синдрома. После этого должна быть выявлена конкретная форма миелобластного лейкоза.

Для этого показательны методы:
- Морфологическое исследование клеток (окрашивание их специальным красящим раствором и изучение под микроскопом),
- Цитохимический анализ,
- Иммунофенотипирование (анализ белков-антигенов на поверхности клеток),
- Цитогенетическое исследование для обнаружения хромосомных перестроек.
После проведения всех методов диагностики пациента относят к той или иной группе риска, после чего назначается лечение.
На видео рассказывается о методах диагностирования лейкоза:
Заболевание у детей
У детей миелобластный лейкоз встречается в 20% всех клинических случаев лейкоза. На первом месте остается острый лимфобластный лейкоз. Среди других форм рака, лейкозам отводится 4,2%.
Что же касается групп риска, заболевание часто диагностируют у детей, особенно в возрасте до 5 лет. Мальчики болеют чаще.
Лейкоз у детей на клеточном уровне протекает так же, как у взрослых: стволовые клетки подвергаются мутации и начинают беспорядочно делиться. И если причина лейкоза понятна — это генетическая мутация предшественников определенных групп клеток, то причины мутаций до сих пор неизвестны.
Ученые считают, что лейкоз развивается, когда соединяется несколько генетических изменений в одном организме (например, синдром Дауна и мутация кровяных клеток, анемия и мутация кровяных клеток).
Справка! Состояние иммунодефицита увеличивает риск заболевания лейкозом в раннем детстве или подростковом возрасте.
Причиной лейкоза может стать и неправильный образ жизни родителей (алкоголизм, табакокурение), особенно матери при беременности.
Родители редко отделяют симптоматику лейкоза от другого заболевания у детей:
- Ребенок становится вялым, слабым, бледным, отказывается играть.
- Из-за ослабленного иммунитета часто присоединяются вирусы и инфекции, поэтому родители даже не подозревают о серьезной патологии ребенка.
- Когда клетки распространяются по всему организму, у детей начинают сильно болеть руки и ноги, из-за чего они становятся плаксивыми, часто просятся на ручки и предпочитают лежать (в раннем детстве) без движений, а не играть и резвиться.
- Температура почти всегда повышается. Иногда может отсутствовать аппетит.
История болезни и симптомы лейкоза у детей сильно разнятся. Все зависит от того, какой орган будет поражен в результате деятельности аномальных клеток.
Диагностируют лейкоз у детей теми же методами, что и у взрослых.
Методы лечения:
- химиотерапия,
- лучевая терапия,
- трансплантация костного мозга.
Вероятность благоприятного исхода в детском и подростковом возрасте значительно увеличилась за последние годы.
Так, полное выздоровление наступает в 70% случаев. Остальные 30% связаны, в основном, с рецидивами, которые случаются почти сразу же после окончания терапии, а также с неэффективностью терапии.

Острый миелобластный лейкоз — одна из самых опасных форм рака, которая встречается у людей любого возраста и характеризуется быстрым распространением.
Согласно мнению и отзывам врачей самым эффективным методом лечения на сегодняшний день является трансплантация костного мозга, которая, к сожалению, не всегда доступна прямо здесь и сейчас.
Прогнозы при лейкозе неутешительны, особенно если речь идет о пожилых людях. У детей шансы выздороветь выше.
Читайте также:


