Опухоль гипофиза у мужчин и фсг
Фолликулостимулирующий гормон вырабатывается в организме женщин и мужчин в передней доле гипофиза. Это один из гонадотропных гормонов, необходимых для развития половой системы и репродукции. Его снижение может замедлить половое развитие организма. 
Повышение ФСГ у мужчин и женщин также является симптомом различных нарушений и заболеваний.
У женщин начиная с периода полового созревания, и до менопаузы наблюдаются колебания ФСГ в крови, связанные с менструальным циклом, после менопаузы его повышение у женщин бывает и в норме. А у мужчин фолликулостимулирующий гормон постепенно увеличивается с самого рождения, наибольший рост наблюдается после 9—10 лет, когда происходит развитие вторичных половых признаков. После 18 лет ФСГ у мужчин находится в пределах 0,7—11,1.
Какое количество фолликулостимулирующего гормона продуцируется в организме, может зависеть от нескольких факторов, поскольку регуляция выработки этого гормона – сложный процесс в котором участвует гипоталамус, половые гормоны, вырабатываемые в яичках. Так, повышение уровня тестостерона снижает выработку ФСГ, кроме того, на этот процесс могут влиять токсические, лекарственные вещества, облучение.
Причины повышение ФСГ у мужчин
Повышение ФСГ у мужчин может произойти по следующим причинам:
- опухоли гипофиза;
- болезни мочевыделительной системы;
- генетические заболевания;
- алкоголь, курение;
- рентгеновское облучение;
- медикаментозные препараты;
- стресс, физические нагрузки;
- возраст.
Определение уровня фолликулостимулирующего гормона обычно назначают совместно с другими гормонами (ЛГ, пролактин, тестостерон), так как их соотношение, нередко позволяет поставить правильный диагноз. Если ФСГ повышен при нормальном уровне тестостерона, мужчина должен обследоваться для выявления заболеваний гипофиза, болезней почек. Сниженный уровень тестостерона, говорит о болезнях яичек, недостаточности половых желез.
| Мужчины | Уровень ФСГ, Ед/л |
| Мальчики 0-1 месяц | менее 1,2 |
| Мальчики 1 месяц-3 года | менее 5,5 |
| Мальчики 3-9 лет | менее 1,9 |
| Мальчики 9-18 лет: пубертат, стадии по Таннеру*: | |
| 1-я стадия | 0,16-3,5 |
| 2-3-я стадия | 0,44—6,0 |
| 4-я стадия | 1,4- 11,8 |
| 5-я стадия | 1,28- 14,9 |
| жчины старше 18 лет | 0,7—11,1 |
Но еще большее влияние на мужчин оказывает пониженный уровень этого гормона. Если продукция ФСГ уменьшается в детском возрасте, а причиной этого являются различные наследственные заболевания, нарушается развитие половых органов, замедляется половое развитие, поскольку ФСГ стимулирует образование семенных канальцев, выработку половых гормонов и сперматогенез.
Как повысить гормон ФСГ у мужчины? Если фолликулостимулирующий гормон повышен у мужчин, лечение нужно проводить только после консультации с врачом. Ни в коем случае нельзя заниматься самолечением, необходимо обратиться к эндокринологу, чтобы выявить причину, и только после этого, врач решит какое лечение необходимо.
Вредные привычки и уровень ФСГ
Так, если изменение уровня ФСГ связано с вредными привычками, то необходимо отказаться от них. В некоторых случаях требуется лечение основного заболевания, например, при орхите. При опухолях гипофиза может понадобиться хирургическое вмешательство, или гормональная терапия. Повышение ФСГ на фоне рентгеновского облучения проходит самостоятельно через 6—8 месяцев.
Снижение или повышение уровня фолликулостимулирующего гормона, указывает на проблемы в организме, оно требует тщательного исследования и лечения, поскольку может быть вызвано серьезными заболеваниями и приводить к бесплодию.
Как снижение, так и повышение ФСГ у мужчин часто говорит о бесплодии. Иногда нехватка этого гормона становится первопричиной нарушения репродуктивной функции. В иных случаях это лишь лабораторный симптом, свидетельствующий о гипогонадизме.
Секреция фолликулостимулирующего гормона может увеличиваться за счет одного из двух механизмов:

- в крови меняется концентрация гормонов, которые влияют на уровень ФСГ (чаще всего к этому приводит снижение уровня тестостерона);
- неправильно работает сам гипофиз (гормонопродуцирующие опухоли).
Снижается количество фолликулостимулирующего гормона за счет аналогичных механизмов:
- в крови меняется уровень гормонов, которые оказывают влияние на секрецию ФСГ (чаще всего – повышается концентрация тестостерона, например, при опухолях яичек или инъекциях андрогенов для наращивания мышц);
- неправильно работает сам гипофиз (он поврежден в результате сосудистых нарушений, инфекций, хирургических вмешательств, поэтому не способен вырабатывать гонадотропины в адекватных количествах).
ФСГ и гипогонадизм
Очень часто как повышенный, так и пониженный уровень ФСГ говорит о гипогонадизме. Это состояние, при котором в крови снижается количество тестостерона. Данное заболевание может быть вызвано механизмами, близкими к вышеописанным. Только теперь это касается функции яичек. Механизмы следующие:
Оба состояния успешно поддаются лечению. Только схемы терапии используются совершенно разные.
Лечение бесплодия при повышенном или пониженном ФСГ
У мужчин с высоким или низким уровнем гонадотропинов обычно обнаруживается бесплодие. Его непосредственной причиной является недостаточная выработка тестостерона. Подходов к лечению этого состояния существует два:
- введение тестостерона в виде препаратов – по сути, применяется заместительная терапия (например, в ситуациях, когда яички повреждены в результате несвоевременно выполненной хирургической операции при варикоцеле);
- стимуляция функции яичек, если они не повреждены и способны вырабатывать тестостерон.
Для стимуляции функции яичек при гипогонадотропном гипогонадизме используются гонадотропные гормоны. К ним относятся ХГЧ, ФСГ и ЛГ. Начинают терапию обычно только с ХГЧ. Препарат вводят в дозе 2 тысячи МЕ, дважды в неделю. 
Каждый месяц мужчина сдает анализ крови на гормоны, а также спермограмму.
Бывает так, что уровень тестостерона в крови возрастает, но это не приводит к улучшению качества спермы. В таком случае в схему терапии вводятся препараты ФСГ и ЛГ. Они вводятся инъекционно, трижды в неделю, в дозе 75 МЕ, три раза в неделю. Если в течение 4 месяцев нормализации показателей спермограммы не происходит, дозировку каждого гормона повышают до 150 МЕ, трижды в неделю.
В большинстве случаев эндокринное бесплодие имеет благоприятный прогноз. Оно успешно поддается лечению тем или иным способом. Поэтому мужчины с повышенным или пониженным ФСГ в итоге могут зачать ребенка. Под действием терапии случится это, скорее всего, лишь через несколько месяцев, потому что сперматозоиды созревают длительное время.
Механизм воздействия ФСГ у мужчин определяется доставкой тестостерона к яичкам. Если этот гормон не будет выполнять необходимые функции, то даже при достаточном уровне тестостерона у мужчины ухудшается самочувствие, у него появляется эректильная дисфункция. Вырабатывается не менее важный, чем тестостерон, гормон в гипоталамусе.
Влияние ФСГ на мужской организм
Функция фолликулостимулирующего гормона в организме мужчины:
- Обеспечивает формирование клеток Сертоли.
- Влияет на развитие семенников и семенных канальцев.
- Запускает сперматогенез в подростковом возрасте и поддерживает его в течение репродуктивного периода.
- Стимулирует выработку андроген-связывающего белка в клетках Сертоли.
- Обеспечивает транспорт тестостерона к придатку яичка и создает условия для правильного развития сперматозоидов.
Клетки Сертоли продуцируют гормон ингибин, усиливающий синтез тестостерона, защищают зародышевые клетки от иммунологической атаки и принимаю участие в созревание сперматозоидов из сперматогоний, стволовых клеток находящиеся в мужских половых железах.
Регуляция синтеза ФСГ осуществляется по механизму обратной связи. В выработке гормона участвуют гипоталамус, гипофиз, яички. Опосредованно влияют на синтез ФСГ органы-мишени.
- Гипоталамус синтезирует гонадотропин-рилизинг гормон (Гн-РГ). Выработка гормона зависит от сигналов, поступающих в центральную нервную систему от внутренних органов и внешней среды.
- Гн-РГ запускает выработку фолликулостимулирующего и лютеинизирующего гормона в гипофизе. Выработка ФСГ и ЛГ идет в прерывистом режиме (каждые 1-4 часа по 15 минут) и зависит от концентрации Гн-РГ.
- ФСГ контактирует с клетками Сертоли и Лейдига через мембранные рецепторы и обеспечивает биологические процессы .
Лечение
Как понятно из приведенной выше информации, нарушение синтеза фолликулостимулирующего гормона является следствием большого количества заболеваний.
Для того чтобы эффективно вылечить данное нарушение необходимо в первую очередь определить причину. Для этого нужно после сдачи крови на анализ и определения избытка или недостатка гормонов нужно провести полное обследование. После этого следует приступить к устранению первопричины.
В том случае, если нарушение синтеза объясняется генетическим заболеванием, то в таких ситуациях назначается гормональная терапия.
Стоит отметить, что на сегодняшний день очень часто генетические заболевания, которые могут стать причиной нарушения гормонального фона у мужчин, диагностируются в первые годы жизни ребенка. Так что прием гормональных препаратов назначается с самых ранних лет и часто продолжается в течение всей жизни.
Если же в ходе исследования было выявлено, что причиной выработки гормона является опухоль надпочечника или гипофиза, то назначается лечение, которое может включать в себя оперативное вмешательство. После операции может быть назначена гормональная терапия, которая должная восстановить гормональный фон организма мужчины.
Мужское бесплодие и гормоны
Фолликулостимулирующий гормон – один из показателей репродуктивного здоровья мужчины. Анализ на ФСГ назначают для диагностики заболеваний половых желез.
Показания для обследования:
- Задержка или ускорение полового развития у подростка.
- Бесплодие. Диагноз выставляется в том случае, если паре не удается зачать ребенка в течение года половой жизни без использования контрацепции. Важно исключить отклонения в работе репродуктивной сферы у обоих партнеров.
- Снижение полового влечения.
- Эректильная дисфункция.
Направление на исследование дает андролог. Расшифровка анализа проводится врачом с учетом всех имеющихся данных и полной оценки состояния здоровья мужчины.
Уровень ФСГ влияет на сперматогенез и определяет возможность зачатия. Для выяснения причины мужского бесплодия оценка ФСГ проводится вместе с определением концентрации иных половых гормонов.
Методы коррекции гормонального баланса
Для определения лечебной тактики необходимо установить причину, спровоцировавшую изменение уровня ФСГ. Нарушения в деятельности гипофиза могут быть устранены посредством гормональной терапии. В некоторых случаях может потребоваться хирургическое вмешательство, например, при наличии новообразований в этом придатке мозга.
Всем мужчинам с отклонениями в уровне ФСГ необходимо придерживаться следующих рекомендаций:
- нормализовать рацион питания, придерживаться режима приёма пищи,
- регулярно давать организму умеренные физические нагрузки,
- нормализовать психоэмоциональный фон, стараться не нервничать, спокойно реагировать в стрессовых ситуациях,
- придерживаться распорядка дня: ложиться и вставать в одно и то же время, уделять достаточное время на сон.
Если у мужчины есть избыток массы тела, необходимо приложить усилия к нормализации веса. В этом помогут разумные ограничения в питании и физическая активность.
Как сдавать анализ на ФСГ
Правила сдачи крови у мужчин:
- Анализ крови на ФСГ сдается в любой удобный день.
- Проходить обследование нужно утром с 7 до 11 часов – в этот период выработка ФСГ максимальна.
- Обследование проводится утром натощак (голодание не менее 8 часов).
- За 3 дня до сдачи крови нужно исключить физические нагрузки, стрессы.
- За сутки до обследования нужно прекратить прием алкоголя.
- За один час до сдачи крови нельзя курить.
Если условия не соблюдаются, полученные данные будут не показательны. Рекомендуется пересдать анализ с выполнением всех условий сдачи крови.
Факторы, влияющие на результаты обследования:
- Гормональные препараты и иные лекарственные вещества.
- Ядерно-магнитное резонансное сканирование организма.
- Курение.
- Прием алкоголя.
- Физические нагрузки.
Симптоматика при дисбалансе гормона
Изменение концентрации ФСГ в крови постепенно приводит к ухудшению самочувствия и снижению качества жизни мужчины. При незначительных отклонениях от нормы никаких симптомов не наблюдается. При отсутствии лечения может измениться тип оволосения – рост волос замедляется на груди и в области лица. Часто происходит смена локализации жировых отложений – при гормональном дисбалансе жиры откладываются по женскому типу, на бедрах и в области талии.
Основной симптом нарушения выработки ФСГ – снижение либидо — нарушение потенции. Кроме половой дисфункции наблюдаются чрезмерная усталость, вялость, апатия.
Норма фолликулостимулирующего гормона у мужчин
Норма ФСГ у мужчин зависит от возраста:
- До 1 года – менее 3,5 мМЕд/мл.
- 1-5 лет – менее 1,45 мМЕд/мл.
- 6-10 лет – менее 3 мМЕд/мл.
- 11-14 лет – 0,3-6,3 мМЕд/мл.
- 15-20 лет – 0,5-10 мМЕд/мл.
- Старше 21 года – 0,95-11,95 мМЕд/мл.
У новорожденных мальчиков отмечается высокое содержание ФСГ. С возрастом количество гормона падает, и после года его уровень становится в 2-3 раза меньше. До пубертатного периода концентрация ФСГ остается стабильной. Уровень гормона растет в период полового созревания.
Для оценки состояния мужской репродуктивной системы нужно оценить соотношение ФСГ и ЛГ. В норме ФСГ/ЛГ – 1-1,5. Изменение этого соотношения указывает на гормональный дисбаланс и ведет к нарушению репродуктивной функции.
Почему повышен или понижен уровень
Повышенный ФСГ указывает на нарушение работы эндокринных желез. Фолликулостимулирующий гормон у мужчин увеличивается по следующим причинам:
- дефицит тестостерона в сыворотке крови;
- алкогольный абстинентный синдром;
- хроническое воспаление легких;
- воспаление органов репродуктивной системы: простатит, уретрит, баланит;
- прием гормональных препаратов;
- побочный эффект лучевой терапии;
- болезнь Клайнфельтера;
- травмирование семенников;
- печеночная недостаточность;
- заболевания почек.
Важная информация: На какой день цикла лютеиновая фаза
Если у мужчины низкий ФСГ, значит в организме возник гормональный дисбаланс. Причиной такого явления может быть:
- злокачественные новообразование головного мозга;
- неправильный прием или побочный эффект от употребления анаболических стероидов;
- длительное истощение организма;
- нарушение психического состояния;
- стресс;
- отсутствие эякулята, дисфункция семенников.
Чтобы поднять уровень гормона, перед проведением лекарственной терапии назначают специальную диету. Вернуть пониженный уровень гормона позволяет дробное питание небольшими порциями каждые 2-3 часа. Категорически запрещается испытывать чувство голода. В качестве перекуса допускается прием фруктов или свежих овощей.
В рацион включают продукты, которые способны повышать плазменную концентрацию ФСГ:
- орехи;
- ламинария;
- жирные сорта морской рыбы;
- брокколи, шпинат, авокадо;
- льняное масло.
Если ФСГ понижен, диетотерапия не дает результатов, назначают лечение гормональными препаратами. При низкой концентрации ФСГ уровень гормона эффективно увеличивает рыбий жир, насыщенный жирными кислотами омега-3 и омега-9.
Чтобы снизить высокий ФСГ, требуется лечить гипоталамус. Структура головного мозга отвечает за выработку гормона. Если у мужчины наблюдается повышенная концентрация ФСГ, это говорит о нарушениях работы гипоталамуса. Проводится лекарственная терапия для подавления активности мозговой структуры.
Если ФСГ повышен, необходимо проведение комплексной диагностики. На время лечения назначают заместительную терапию аналогами мужских гормонов. При облучении и химиотерапии к лечению не прибегают. Уровень гормона вернется в норму самостоятельно через год.
Причины повышения ФСГ
Повышенный уровень ФСГ указывает на патологию гонад.
Причины повышения ФСГ:
- Первичный гипогонадизм. Встречается при анорхизме и монорхизме (отсутствие обоих или одного яичка), крипторхизме (неопущение яичника), гипоплазии гонад.
- Вторичный гипогонадизм. К развитию патологии ведут травмы яичника, тяжелые инфекционные заболевания (паротит, ВИЧ, туберкулез), метаболические нарушения (ожирение, сахарный диабет, патология щитовидной железы), опухоли.
- Генетические заболевания: синдром Клайнфельтера, синдром де ля Шапеля, синдром Якобса.
- Гипогонадизм в результате облучения рентгеновскими лучами, на фоне длительного приема алкоголя, химиотерапии.
- Опухоли гипофиза, повышающие выработку гормона.
- Гормонпродуцирующие новообразования иной локализации (опухоли легкого, пищеварительного тракта).
- Почечная недостаточность.
ФСГ и гипогонадизм
Очень часто как повышенный, так и пониженный уровень ФСГ говорит о гипогонадизме. Это состояние, при котором в крови снижается количество тестостерона. Данное заболевание может быть вызвано механизмами, близкими к вышеописанным. Только теперь это касается функции яичек. Механизмы следующие:
Оба состояния успешно поддаются лечению. Только схемы терапии используются совершенно разные.
Норма лютропина
у женщин, как и ФСГ, изменяется с определенной цикличностью. А в мужском теле он должен сохраняться на одном уровне, меняясь по причине возраста.
Для каждого этапа взросления мужчин существует норма:
- с рождения уровень ЛГ постепенно растет;
- в 6–8 лет снижается;
- по мере взросления, полового созревания уровень повышается, с 8 до 18 лет норма держится в рамках 0,1–6 мЕд/мл;
- с 18 до 70 лет норма равна 1,5–9,3 мЕд/мл;
- для пожилых мужчин норма составляет 3,1–34 мЕд/мл.
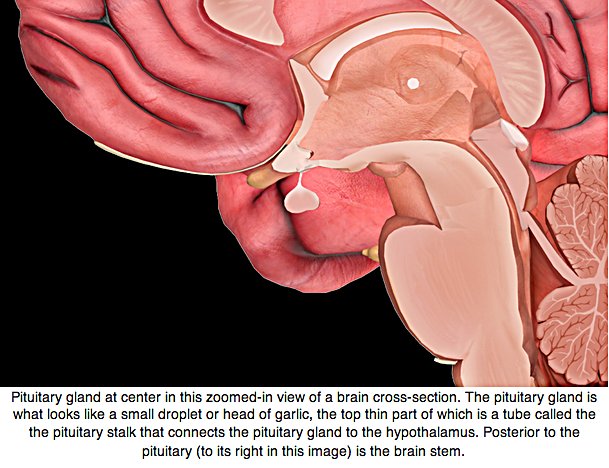
АДЕНОМА ГИПОФИЗА ГОЛОВНОГО МОЗГА — ЧТО ЭТО ТАКОЕ?
Гипофиз является важнейшей железой организма, поскольку контролирует большинство эндокринных функций. Он состоит из двух долей: передней и задней. Передняя доля гипофиза выделяет 6 гормонов: тиреотропный гормон (ТТГ), адренокортикотропный гормон (АКТГ), фолликуло-стимулирующий гормон (ФСГ), лютеинизирующий гормон (ЛГ), соматотропный гормон (СТГ, или гормон роста) и пролактин (ПЛ). Задняя доля секретирует вазопрессин и окситоцин. При возникновении опухолевого роста из гормональных клеток говорят об аденоме гипофиза.
Аденомы гипофиза почти всегда доброкачественны и не обладают злокачественным потенциалом. По своим функциональным свойствам опухоли железы подразделяются на секретирующие и несекретирующие опухоли, другие интраселлярные опухоли и параселлярные опухоли. Последняя группа представляет собой опухоли, которые возникают вблизи турецкого седла и по вызываемым симптомам могут напоминать опухоли гипофиза. Гормонально неактивные опухоли размером до нескольких миллиметров весьма часты и встречаются примерно в 25% аутопсийного материала. Они могут медленно расти, нарушая нормальную гормональную функцию железы (гипопитуитаризм), или же могут сдавливать подлежащие структуры головного мозга, провоцируя неврологическую симптоматику.
Секретирующие, или гормонально-активные аденомы клинически подразделяются не несколько типов в зависимости от выделяемых ими гормонов. Эти опухоли вызывают специфические симптомы вследствие выделения ими гормонов, но редко достигают размеров, достаточных для сдавления прилежащих структур. По мере роста опухоли происходит разрушение нормальной ткани гипофиза, что приводит ко множеству гормональных нарушений. В редких случаях наблюдаются спонтанные кровоизлияния в опухоль или инфаркты. Давление, оказываемое опухолями на прилежащие структуры, может спровоцировать онемение лица и двоение в глазах. Непосредственно над гипофизом расположен перекрест зрительных нервов (хиазма), поэтому опухоли могут вызвать прогрессирующую потерю зрения. Потеря зрения обычно начинается с обоих полей зрения и приводит сначала к туннельному зрению, а затем к слепоте.
ОПУХОЛЬ ГИПОФИЗА: СИМПТОМЫ У МУЖЧИН И ЖЕНЩИН
Симптомы, связанные с секреторной активностью опухоли
Клинические признаки аденомы гипофиза значительно различаются в зависимости от расположения и размера, а также от способности опухоли секретировать гормоны. Аденомы гипофиза обыкновенно возникают в достаточно молодом возрасте независимо от пола. Гормонально-активные аденомы обычно невелики по размеру и не вызывают неврологической симптоматики или гипопитуитаризма, но возможно и обратное. Симптомы гормонально-активной опухоли связаны с действием того специфического гормона, который она вырабатывает.
Неврологическая симптоматика аденом гипофиза включает в себя головные боли, диплопию; потерю периферического зрения, приводящую к слепоте, лицевые боли или онемение. Гипопитуитаризм проявляется выраженной слабостью, потерей веса, тошнотой, рвотой, запорами, аменореей и бесплодией, сухостью кожи, повышенной пигментацией кожи, повышенной зябкостью и изменениями в ментальном статусе (например, сонливость, психозы, депрессивные расстройства).
Пролактинома является наиболее частой опухолью гипофиза у женщин. Признаки опухоли гипофиза у женщин, обусловленные пролактиномой, включают аменорею (отсутствие кровянистых выделений при менструации), нерегулярность менструального цикла, галакторею (выделение молока из сосков), женское бесплодие и остеопороз. Также с пролактиномой могут быть связаны гипогонадизм, потеря полового влечения и импотенция у мужчин.
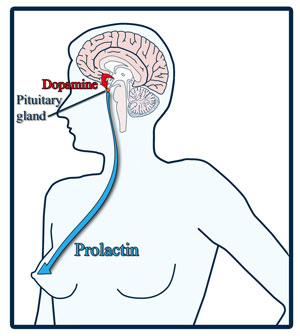
Признаки аденомы гипофиза у женщин обусловлены типом гормона, который продуцируют опухолевые клетки. Наиболее частый вариант — пролактинома, вызывающая патологическую активность молочных желез.
Опухоли, секретирующие избыточное количество СТГ, вызывают гигантизм у детей и акромегалию у взрослых. При акромегалии наблюдаются укрупнение черт лица, увеличение кистей и стоп, заболевания сердца, гипертензия, артрит, запястный туннельный синдром, аменорея и импотенция.

Аденома гипофиза — симптомы у мужчины средних лет. Акромегалия, наблюдающаяся при повышенной выработке соматотропного гормона опухолью гипофиза. Наряду с высоким ростом, наблюдается увеличение носа, нижней челюсти, надбровных дуг.
АКТГ-секретирующие аденомы приводят к развитию болезни Кушинга, для которой, в свою очередь, характерны округлое лицо с акне и гиперемией, отложения жира по задней стороне шеи, растяжки и склонность к образованию синяков на коже, избыточный рост волос на теле, сахарный диабет, потеря мышечной массы, утомляемость, депрессия и психозы.
Опухоли, выделяющие ТТГ, характеризуются симптомами тиреотоксикоза, такими как непереносимость тепла, потливость, тахикардия, легкий тремор и потеря веса. Некоторые секретируют более одного гормона, например, СТГ и ПЛ одновременно.
Реже встречаются опухоли, секретирующие ЛГ или ФСГ (гонадотропины). Когда опухоль начинает оказывать влияние на секреторные клетки гипофиза, первые признаки секреторной недостаточности обычно касаются функций гонадотропинов. Таким образом, первым признаком аденомы гипофиза у женщин может быть прекращение менструаций. У мужчин самым частым признаком гормональной недостаточности гонадотропинов является импотенция. Редко наблюдается изолированный дефицит ЛГ или ФСГ. У мужчин изолированный дефицит ЛГ приводит к развитию клинической картины фертильного евнуха. При этом состоянии нормальный уровень ФСГ позволяет достичь созревания сперматозоидов, но вследствие дефицита ЛГ у пациента могут развиться признаки гормональной кастрации. Опухоли также могут продуцировать избыточное количество ЛГ или ФСГ; кроме того, нередки опухоли, секретирующие только неспецифические гормонально неактивные альфа-субъединицы гликопротеиновых гормонов.
Симптомы, связанные с компрессией окружающих структур
Аденомы гипофиза условно подразделяются на микроаденомы (размером до 1 см) и макроаденомы (размером >1 см). Если первые обычно не вызывают объемного воздействия на мозг или нервы ввиду своих небольших размеров, то вторые по мере роста все больше сдавливают окружающие ткани.
Зрительные расстройства обычно связаны со сдавлением структур проводящего пути зрительного анализатора и включают битемпоральное сужение полей зрения, нарушение цветового зрения, двоение и офтальмоплегию. При исследовании глазного дна признаком длительной компрессии зрительного перекреста является, в первую очередь, атрофия зрительного нерва. Тяжелая атрофия зрительного нерва указывает на худший прогноз для восстановления зрения после хирургической декомпрессии. У беременных женщин битемпоральное сужение полей зрения и головная боль могут указывать на апоплексию гипофиза.
Апоплексия гипофиза является потенциально жизненно-угрожающим состоянием. Беременные женщины с аденомами гипофиза и МРТ-признаками субарахноидального кровоизлияния нуждаются в проведении кесарева сечения, чтобы избежать апоплексии гипофиза во время родов. Послеродовое кровотечение может вызвать инфаркт гипофиза с последующим развитием гипопитуитаризма (синдрома Шихана).
КАК ДИАГНОСТИРОВАТЬ ОПУХОЛЬ ГИПОФИЗА?
Клинический диагноз аденомы гипофиза основывается на сочетании признаков и симптомов, зависящих от размера опухоли и выделяемых ею гормонов.
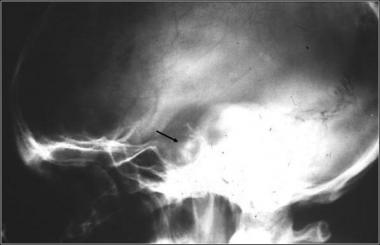
На рентгенограмме турецкого седла в боковой проекции у пациента с аденомой гипофиза видно увеличенное турецкое седло и участки кальцинации в аденоме (указано стрелкой).
Если в прошлые десятилетия основным методом визуализации гипофиза была рентгенография турецкого седла, то в последние годы КТ и МРТ полностью вытеснили ее, поскольку стандартная рентгенография плохо отображает мягкие ткани, в отличие от томографических методов, которые отображают тело человека в виде множества срезов. Сегодня рентгенография турецкого седла назначаться не должна, так как информативность ее мала, присутствует лучевая нагрузка, а главное — решение о тактике лечения аденомы принимается на основе современных методов, таких как КТ и МРТ.
Стандартная односрезовая КТ имеет весьма ограниченное применение в визуализации гипофиза; в диагностике микроаденом чувствительность метода составляет 17-22%. Может применяться мультиспиральная КТ с 64 детекторами, особенно у пациентов, которым невозможно провести МРТ. КТ лучше визуализирует особенности костных структур и кальцификаты в опухолях, таких как герминомы, краниофарингиомы и менингиомы. КТ-ангиография отлично визуализирует морфологию параселлярных аневризм и может использоваться при планировании хирургического вмешательства. КТ-снимки полезны в случаях, когда имеются противопоказания к МРТ, например, у пациентов с установленными водителями ритма или внутриглазными/внутримозговыми металлическими имплантами.
В целом, МРТ предпочтительнее, чем КТ, в диагностике аденом гипофиза, поскольку лучше определяет наличие небольших образований в турецком седле и их анатомическую характеристику на предоперационном этапе. МРТ также рекомендуется для постоперационного наблюдения.
Нередко результаты МРТ оказываются сомнительными, недостоверными или спорными. В таких случаях рекомендуется повторный анализ снимков с диска опытным врачом экспертного уровня. Если такого врача нет поблизости, второе мнение можно получить удаленно, обратившись в Национальную телерадиологическую сеть — всероссийскую службу консультаций врачей-диагностов.
Ангиография используется редко; при наличии показаний, стандартная ангиография заменяется КТ- или МРТ-ангиографией. Ангиография играет определенную роль, когда требуется уточнение состояния кавернозного синуса или кавернозной части сонной артерии.
Соматостатин-рецепторная сцинтиграфия может быть использована для дифференциальной диагностики рецидива опухоли или остаточной опухолевой ткани в зоне рубца или некроза тканей после операции.
НЕДОСТАТКИ И ОГРАНИЧЕНИЯ МЕТОДОВ
Стандартная рентгенография плохо отображает мягкие ткани. МРТ дороже, чем КТ, но является более предпочтительным методом для исследования гипофиза, поскольку лучше визуализирует мягкие ткани и сосудистые структуры. Таким образом, к ограничениям КТ относятся худшее отображении мягких тканей по сравнению с МРТ, необходимость использования внутривенного контрастного вещества для улучшения изображений, а также лучевая нагрузка на пациента.
Потенциальным ограничением к применению МРТ является пневматизация передней части клиновидной кости или ее кальцификация, что может напоминать особенности тока крови в аневризмах. Кроме этого, МРТ противопоказана пациентам с установленными водителями ритма или ферромагнитными имплантами в головном мозге или в глазах. По данным КТ или МРТ, остаточная ткань аденомы гипофиза может быть с трудом отличена от индуцированного лучевой терапией фиброза, особенно у пациентов с клинически неактивными аденомами гипофиза, у которых отсутствуют циркулирующие маркеры, позволяющие оценивать прогрессирование или ответ на лечение
КТ ПРИ АДЕНОМЕ ГИПОФИЗА
Современные 64-срезовые томографы позволяют получать реформатированные корональные изображения с высоким пространственным разрешением. Использование быстрого сканирования на многосрезовом аппарате помогает снизить лучевую нагрузку.
Микроаденомы являются небольшими округлыми опухолями в паренхиме гипофиза. Неосложненные кровоизлиянием или образованием кист микроаденомы обычно имеют пониженную рентгеновскую плотность по сравнению с прилежащей нормальной тканью гипофиза. Поэтому микроаденомы гипофиза могут быть не видны на КТ без контрастного усиления. Контрастирование микроаденом после ввода контрастного вещества происходит с задержкой по сравнению с быстрым и сильным усилением неизмененного гипофиза. Таким образом, около двух третей микроаденом обычно характеризуются пониженной рентгеновской плотностью на динамической КТ с контрастным усилением, в то время как одна треть микроаденом демонстрирует раннее накопление контраста.
Крупные опухоли — макроаденомы отличаются значительным разнообразием. Большинство из них имеют плотность, аналогичную коре мозга на КТ-снимках без контрастного усиления и характеризуются умеренным накоплением контраста на изображениях с контрастным усилением. Кальцинаты редки (1-8%). Очаги некроза, образование кист и кровоизлияния могут соответствовать образованиям с неравномерной рентгеновской плотностью. КТ также визуализирует костные изменения стенок турецкого седла и объемные образования, распространяющиеся за его пределы. Гормонально-активные аденомы прорастают в кавернозный синус гораздо чаще, чем гормально-неактивные макроаденомы.
КТ-ангиография очень полезна при планировании операционного вмешательства в случае макроаденом. Хирургу крайне важно представлять взаимное расположение опухоли, передних мозговых артерий и зрительного нерва. Протоколы визуализации тонкосрезовой КТ также полезны во время проведения самой операции.
Несмотря на то, что МРТ является методом выбора в обследовании пациентов с аденомами гипофиза, КТ все еще играет определенную роль в случаях, когда проведение МРТ невозможно. КТ также отображает кальцинаты, что может повлиять на проведение дифференциального диагноза. КТ вносит свой вклад в планирование хирургической операции, в частности, в отношении пневматизации и анатомических особенностей клиновидного синуса. Недостатком КТ является более низкое качество визуализации мягких тканей по сравнению с МРТ. Кроме этого, КТ часто требует использования контрастных веществ, а пациенты подвергаются лучевой нагрузке.
МРТ ГИПОФИЗА В НОРМЕ
При анализе результатов МРТ гипофиза нужно знать, как он выглядит на снимках в норме. У детей высота здорового гипофиза зависит от возраста. Высота гипофиза измеряется на строго сагиттальных Т1-взвешенных изображениях, полученных при помощи срезов толщиной 3-7 мм. Измерение проводится в точке наибольшей высоты, которая обычно соответствует середине железы. В норме высота увеличивается при рождении, в период полового созревания (6-7мм), в течение беременности ( 99 m Tc(V)DMSA также информативна в выявлении большинства аденом гипофиза, секретирующих СТГ и ПЛ, а также гормонально-неактивных аденом с соотношением накопления в опухоли и окружающих тканях, равным 25. Функциональная визуализация остаточной опухоли (размером более 10 мм) с использованием 99 m Tc(V)DMSA выявляет жизнеспособную остаточной ткань аденомы гипофиза.
Сцинтиграфия с использованием 111 In-DTPA-октреотида является новым методом, определяющим рецепторы к соматостатину во многих нейроэндокринных опухолях (например, в аденомах гипофиза). Это вещество обладает высокой чувствительностью и является легко отслеживаемым маркером при определении наличия соматостатиновых рецепторов в аденомах гипофиза.
Роль сцинтиграфии с 111 In-DTPA-октреотидом в выявлении гормонально неактивных опухолей гипофиза еще не установлена. Лечение немеченым октреотидом может, вероятно, помешать захвату метки опухолями гипофиза. Таким образом, пациенты, которым планируется проведение сцинтиграфии, должны приостановить лечение на 2-3 дня перед исследованием.
АДЕНОМА ГИПОФИЗА ГОЛОВНОГО МОЗГА — ЛЕЧЕНИЕ
Опухоли гипофиза, не вызывающие эндокринных нарушений и не сдавливающие окружающие ткани, не требуют лечения. В таких случаях ограничиваются наблюдением в виде выполнения повторных МРТ-исследований, желательно с получением второго мнения. При появлении симптомов л ечение зависит от типа опухоли, ее размера и от степени воздействия на головной мозг или нервы. Также имеют значение возраст и общее состояние здоровья.
Решение о методах лечения принимается группой медицинских специалистов, включая нейрохирурга, эндокринолога и, иногда, онколога. Врачи обычно используют хирургическое вмешательство, лучевую терапию или лекарственную терапию, как самостоятельно, так и в сочетании.
ОПЕРАЦИЯ ПО УДАЛЕНИЮ АДЕНОМЫ ГИПОФИЗА
Хирургическое удаление опухоли гипофиза обычно необходимо, если опухоль давит на зрительные нервы, или если опухоль перепроизводит определенные гормоны. Успех операции зависит от типа опухоли, ее местоположения, ее размера и того, вторглась ли опухоль в окружающие ткани. Перед операцией необходимо точно оценить изменения на МРТ-снимках, при этом необходима расшифровка МРТ опытным нейрорадиологом. После удаления аденомы гипофиза могут некоторое время беспокоить выделения из носа.
Двумя основными хирургическими методами лечения опухолей гипофиза являются:
Эндоскопический трансназальный трансфеноидальный доступ. Эта методика представляет собой удаление аденомы гипофиза через нос и околоносовые пазухи без внешнего разреза. При этом остаются неповрежденными ткани головного мозга и черепно-мозговые нервы. Видимого шрама также не остается. Опухоли большого размера указанным доступом удалить трудно, особенно если опухоль внедрилась в близлежащие нервы или ткани головного мозга.
Транскраниальный доступ (краниотомия, трепанация черепа). Опухоль удаляется через верхнюю часть черепа через отверстие в его своде. С помощью этой методики легче удалить большие опухоли или образования сложного строения.
ЛУЧЕВАЯ ТЕРАПИЯ
Радиотерапия использует высокоэнергетические рентгеновские лучи для воздействия на опухоли. Ее можно использовать после операции или самостоятельно, если операция не решает проблему радикально. Также л учевая терапия применяется при остаточной ткани опухоли, при ее рецидиве, а также при неэффективности препаратов. Методы лучевой терапии включают:
- Гамма-нож — стереотаксическая радиохирургия.
- Дистанционная гамма-терапия.
- Протонная лучевая терапия.
ЛЕЧЕНИЕ ПРЕПАРАТАМИ
Можно ли вылечить аденому гипофиза без операции? Лечение препаратами может помочь блокировать избыточную гормональную секрецию и иногда уменьшать размеры определенных типов аденом гипофиза:
Пролактин-секретирующие опухоли (пролактиномы). Препараты каберголин и бромокриптин уменьшают секрецию пролактина и уменьшают размер опухоли.
Опухоли, выделяющие гормон роста (соматотропиномы). Для этих типов образований доступны два типа лекарств:
- аналоги соматостатина вызывают уменьшение выделения гормона роста и могут уменьшить опухоль
- пегвизомант блокирует действие избыточного гормона роста на организм.
Замена гипофизарных гормонов. Если опухоль гипофиза или хирургическое вмешательство приводят к уменьшению выработки гормонов, вам, вероятно, потребуется использовать замещающую гормонотерапию.
При написании статьи использованы следующие материалы:
Читайте также:

