Обогащенная тромбоцитами плазма онкология
Достижения современной науки позволяют нам решать многие проблемы со здоровьем, однако не стоит забывать и о резервах нашего организма. Порой с помощью собственных ресурсов можно поправить, казалось бы, трудную ситуацию. Яркий пример: молодое, но перспективное направление в лечении суставов — PRP-терапия. Это лечебная процедура, в ходе которой используют собственные тромбоциты пациента для заживления и регенерации тканей. В последнее десятилетие как в отечественной, так и в западной научной литературе появилось большое количество публикаций, посвященных применению PRP в ортопедии и спортивной медицине. Исследователи называют данную методику многообещающей, благодаря ее безопасности, простоте и получаемым результатам.
Существует много синонимов методики — PRP (англ. platelet rich plasma), или обогащенная тромбоцитами плазма, ACP (autologous conditioned plasma), аутоплазмотерапия, плазмолифтинг, но по сути все они означают одно и то же.
В чем суть PRR-терапии?
Еще в 1905 году хирург Август Бир описал свойство собственной крови пациента (гематом) помогать заживлению переломов. Однако причины этого явления долго оставались неизвестными.
Наша кровь состоит из жидкой части — плазмы, и из клеток — эритроцитов, лейкоцитов и тромбоцитов. Все они участвуют в регенерации тканей. Тромбоциты — самые маленькие из клеток крови — содержат гранулы с огромным количеством белков, ферментов и биологически активных веществ. Если происходит активация тромбоцитов (например, при повреждении сосуда), то содержимое гранул попадает в окружающее пространство. Активные вещества тромбоцитов способствуют синтезу коллагена, делению клеток и образованию новой ткани.
Для того чтобы получить плазму, обогащенную тромбоцитами, используются либо специальные системы, либо обычная лабораторная центрифуга. При центрифугировании более тяжелые клетки (эритроциты) оседают на дно, а тромбоциты остаются в плазме крови.
Метод PRP активно применяется в стоматологии и челюстно-лицевой хирургии для восстановления участков кости, в дерматологии и косметологии для повышения упругости тканей, а также в кардиологии, офтальмологии и у ожоговых больных. Рассмотрим более подробно, как может использоваться PRP-процедура в ортопедии.
Лечение PRP-плазмой может применяться при поражениях различных суставов. Например, PRP-терапия коленного сустава помогает при тендинитах надколенника и поражениях МКС (медиальной коллатеральной связки) колена. Игроки в теннис или гольф нередко страдают эпикондилитами, и одним из решений становится PRP-терапия локтевого сустава. Методика PRP-терапии применяется и при оперативных вмешательствах, например при операциях на плечевом суставе. Для больных коксартрозом различной степени может быть полезна PRP-терапия тазобедренного сустава.
Основные показания к проведению PRP-терапии в ортопедии:
- поражение хрящевой ткани сустава (артрозы, артриты, остеохондриты, хондромаляция);
- поражение связок, сухожилий и мышц (тендиниты, миозиты);
- поражение позвоночника (остеохондроз, повреждение межпозвоночного диска);
- неполные разрывы связок, сухожилий, капсулы суставов;
- воспалительные процессы;
- применение во время и после операций на суставах для ускорения заживления.
К побочным эффектам процедуры можно отнести болезненность в месте инъекции, особенно при уколах в сухожилие. Для устранения этого эффекта обеспечивают покой и применяют холод на пораженную зону в первые сутки после лечения. Также при инъекции возможно кровотечение, повреждение нерва или инфицирование. Для исключения таких рисков необходимо проводить процедуру PRP-терапии в надежном медицинском центре и у квалифицированного специалиста.
Противопоказания к проведению PRP-терапии:
- беременность;
- острые инфекционные заболевания;
- обострение хронических заболеваний;
- заболевания кроветворной системы;
- системные заболевания соединительной ткани.
При проведении PRP-терапии подготовка пациента заключается в осмотре врача, при необходимости могут быть назначены дополнительные исследования.
- Для получения обогащенной тромбоцитами плазмы пациента забирают 20–50 мл крови из вены. Эта процедура практически безболезненна. Кровь, смешанную с антикоагулянтом, помещают в центрифугу для разделения на фракции. Затем из обработанного образца выделяют плазму, богатую тромбоцитами.
- Полученный образец вводят в зону поражения с помощью специальной очень тонкой иглы. Перед этим в зоне укола проводят местную анестезию, так что сама процедура не более болезненна, чем обычная инъекция. Пациент сидит или лежит на кушетке. Схему введения обозначает врач, и при необходимости точность PRP-инъекции контролируется с помощью УЗИ. Сама процедура проходит довольно быстро, в среднем 20 минут.
- Восстановление после процедуры PRP-терапии не требуется, пациент может сразу вернуться к повседневным делам. В редких случаях может быть назначен режим покоя. Однако необходимо исключить интенсивные нагрузки и поднятие тяжестей.
После проведения PRP-терапии результат можно почувствовать через несколько недель, а долгосрочные эффекты отмечаются через 6–12 месяцев. Сразу после проведения терапии возможно усиление воспаления, скованность и болевые ощущения, что связано с активацией регенерации. Однако в дальнейшем пациенты отмечают уменьшение боли и воспаления, улучшение подвижности в суставе, также происходит улучшение эластичности связок и повышение защитных свойств хрящевой ткани.
Лечение методом PRP в ортопедии широко распространено за рубежом, а также в центральных регионах России. В других областях этот метод пока представлен меньше. Стоимость одной инъекции составляет от 4 до 10 тысяч рублей. Многие клиники предлагают сразу несколько типов лечения суставов с помощью обогащенной тромбоцитами плазмы, которые отличаются по цене. В первую очередь это зависит от способа получения плазмы. Использование сертифицированных европейских систем для получения PRP повышает стоимость. Некоторые клиники предлагают сразу целый курс PRP-терапии, который выходит чуть дешевле, чем если оплачивать каждую инъекцию отдельно. Для проведения лечения также потребуется консультация специалиста и, возможно, дополнительные исследования, которые не входят в цену инъекции.
В любом случае применение PRP для лечения суставов в настоящее время становится все доступнее. Благодаря опыту зарубежных коллег эта процедура приобретает все больше поклонников в медицинском сообществе. И даже если это не панацея, то один из самых безопасных путей к долгожданной свободе движения.
P.S. Ознакомиться с лицензией медцентра, сертификатами врачей и перечнем услуг можно на официальном сайте клиники.
Лицензия № ЛО-77-01-008730 от 06 августа 2014 г. выдана Департаментом здравоохранения города Москвы.

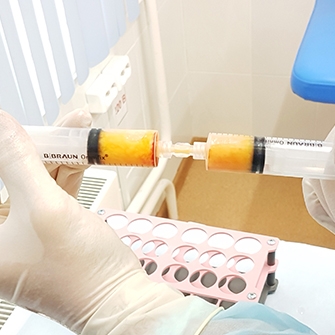
Услуга реинфузии крови призвана улучшить обменные процессы в организме и способствовать регенерации и росту клеток.
Ограничение подвижности и боль — частые спутники заболевания суставов.

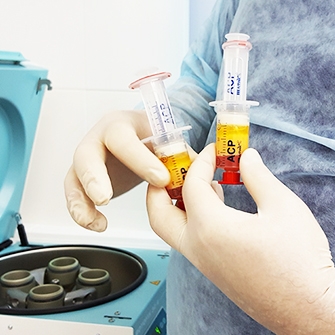
Стоимость лечения с помощью реинфузии крови может зависеть от стадии заболевания и длительности курса лечения.
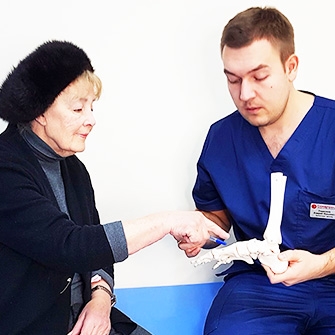
Реинфузия крови может способствовать сокращению длительности реабилитации, а также увеличению периода ремиссии.
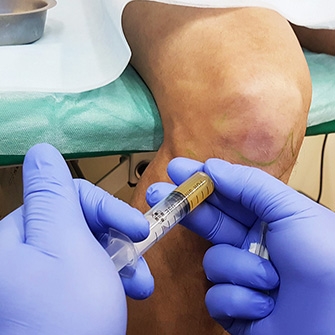
Реинфузия крови может применяться для лечения различных заболеваний суставов и позвоночника, таких как:
- артрит;
- радикулит;
- остеохондроз;
- разрывы сухожилий и мышц и пр.
Современные клиники могут предлагать сезонные скидки и акции на услуги по лечению суставов и позвоночника.

Каадзе Анастасия Геннадьевна Ответственный редактор
В первые часы после инъекции пациент может ощущать боль в месте укола. Чтобы снять неприятные ощущения, можно приложить на некоторое время прохладный компресс, а затем сделать легкий массаж. Однако лучше не надавливать на кожу сильно, чтобы не спровоцировать появление гематомы.
Давно хотел рассказать, да простят меня чудотворцы с электрическими лампами и исцеляющими лазерами, что давно и успешно существует методика PRP терапия.
В течение последних нескольких лет было много написано о препарате, который называется плазмой, обогащенной тромбоцитами (PRP), много рассказано о потенциальной эффективности при лечении травм и заболеваний.
Несмотря на то, что PRP получила широкую огласку, все еще остаются затяжные вопросы, такие как:
Что такое плазма, богатая тромбоцитами?
Как это работает?
Эффективно ли лечение PRP?
Что такое плазма, богатая тромбоцитами (PRP)?
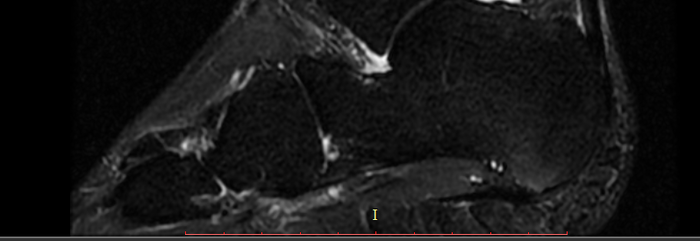
Наша пациентка давно страдает болью в месте прикрепления плантарной фасции к пяточной кости. Усугубляет этот процесс возраст и вес. С возрастом связываем приобретенное плоскостопие.
Назначено МРТ исследование. Справа на картинке это пяточная кость. Оттенок ее неоднородный: снизу участок просветления, видите?. К этому месту и крепится плантарная фасция.
Хотя кровь в основном представляет собой жидкость (называемую плазмой), она также содержит небольшие твердые и тяжелые компоненты (красные клетки, белые клетки и тромбоциты). Тромбоциты известны своей важностью в свертывании крови. Тем не менее, тромбоциты также содержат сотни белков, называемых факторами роста, которые очень важны для заживления травм.
PRP представляет собой плазму с большим количеством тромбоцитов, чем то, что обычно содержится в крови. Концентрация тромбоцитов и, тем самым, концентрация факторов роста - может быть в 5-10 раз больше, чем обычно.
Как подготавливается плазма?
Забор крови у пациента.
Тромбоциты отделяются от других клеток крови, и их концентрация увеличивается во время процесса, называемого центрифугированием.
Инъекция в патологический участок.
Вернемся к нашему пациенту. Инъекция будет проведена в пяточную кость, в место прикрепления плантарной фасции.
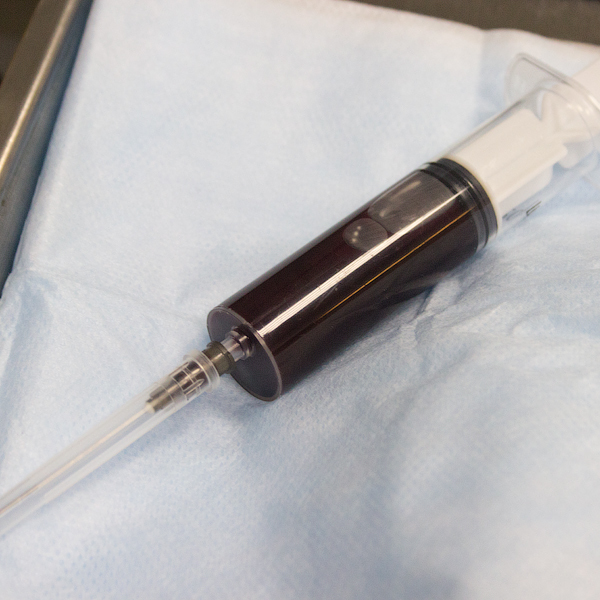
Это цельная кровь нашего пациента.
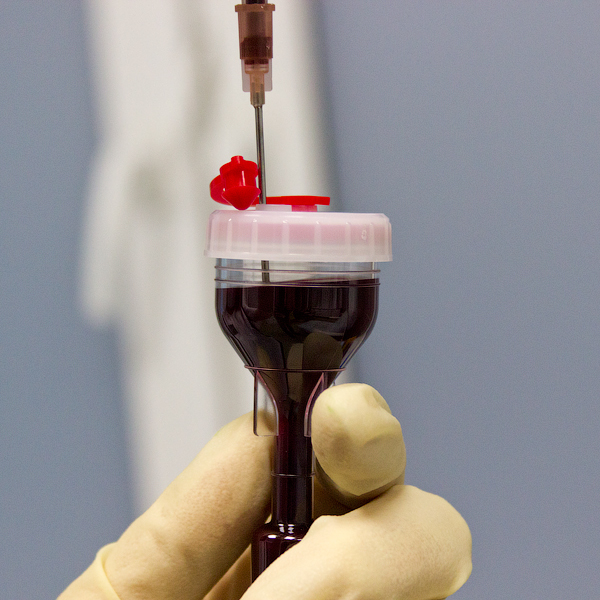
Кровь пациента помещается в пробирку. Центрифугируется на определенных значениях и на определенное время. Эти значения даны производителем центрифуги и пробирок (в целом- системы), и они у всех немного отличаются. Процедура подготовки занимает в среднем 15 мин.
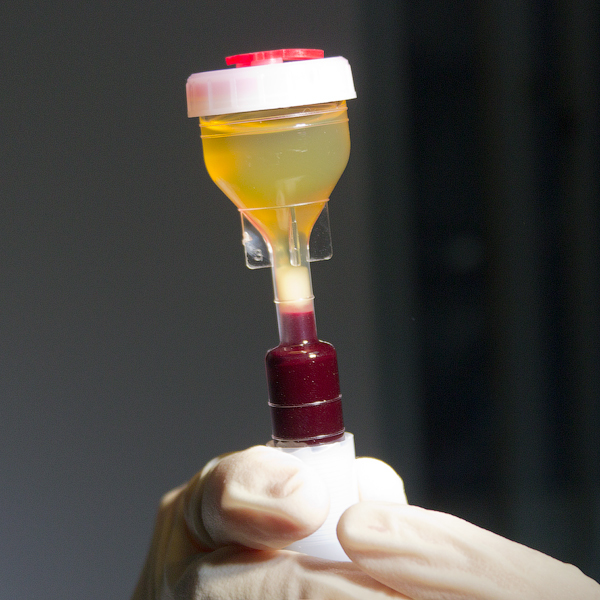
Полученный слой находится по центру песочных часов. Посмотрите, он белесоватый. Оттуда извлечем его иглой, не забирая красную кровь. Это важный момент!
Следующим этапом в стерильных условиях обрабатываем кожные покровы и делаем инъекцию PRP.
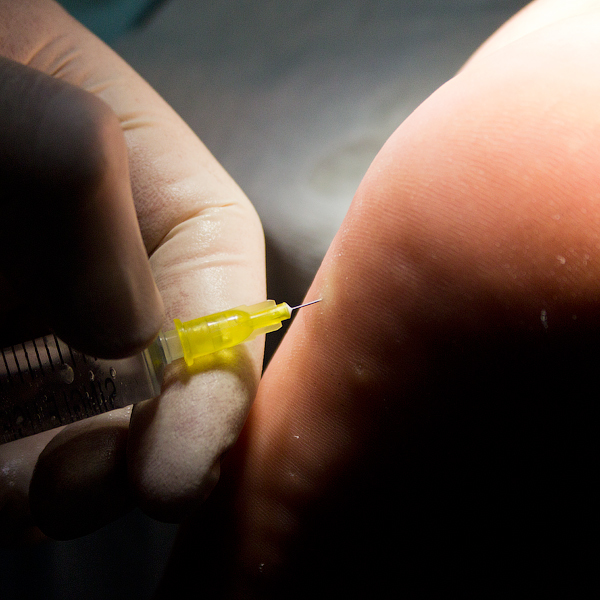
Примечание: в данном случае мы вводим анестетик внутри и подкожно. В область патологии анестетик не вводим. Считается, что в таком случае происходит "угнетение" факторов роста.
Вот и всё, отпускаем пациента. Рекомендациями общими будут следующие: постельный режим 2-3 дня. Прикладывание льда к месту инъекции. Будет беспокоить боль около 7 дней, больше чем обычно. Далее постепенно пойдёт на спад, пока совсем не пройдет.
На сегодняшний день такое лечение используется многими современными клиниками мира. Эту технологию применяют современные спортивные клубы для лечения своих игроков. Это доступно и безопасно.
Известно, что использование собственной крови для лечения различных заболеваний началось в древние времена, т. е. с момента зарождения медицины. В настоящий момент использование богатой тромбоцитами плазмы (ОТП, РRР) является одним из успешных направлений тканевой инженерии и клеточной терапии в медицине. В эволюции терминологии встречается множество различных вариантов названий обогащенной тромбоцитами плазмы как конечного продукта. В клинической практике считается, что стимулирующий эффект обогащенной тромбоцитами плазмы возможен при концентрации тромбоцитов в ней не менее 1000000/ мкл. При повреждении тканей тромбоциты играют огромную роль в заживлении и регенерации тканей благодаря высвобождению факторов роста. Факторы роста – это естественные полипептиды, которые обладают широким биологического локального воздействия на многие кетки, посредством влияния на основные звенья регенераторного процесса: хемотаксис, клеточную пролиферацию, миграцию клеток, дифференцировку, реструктуризацию и ангиогене.
ОТП содержит такие факторы роста как: PDGF – тромбоцитарный фактор роста, TGF-β – трансформирующий фактор роста, EGF – фактор роста эпителия, VEGF – фактор роста эндотелия сосудов, но и адгезивные молекулы (фибрин, фибронектин и витронектин), цитокины. При центрифугировании, полученная плазма содержит белки, фибриноген, питательные вещества (глюкоза, липиды), гормоны, витамины, ферменты, промежуточные и конечные продукты обмена веществ, неорганические ионы, которые участвуют в каскаде процесса регенерации тканей [12, 20].
Учитывая, что ОТП является неотъемлемой частью собственной крови пациента, ее преимуществом является отсутствие риска парентеральной передачи ВИЧ инфекции, вирусного гепатита или возникновение иммунных реакций.
Существуют различные протоколы получения ОТП путем центрифугирования цельной крови в 1 или 2 этапа, после или без добавления антикоагулянта с получением различных конечных продуктов [12, 20].
В настоящее время существует простая классификация, основанная на характеристике молекул фибрина и содержания клеток (главным образом лейкоцитов), в которой выделяют 4 основных группы: 1) чистая обогащенная тромбоцитарная плазма (P-PRP); 2) обогащенная тромбоцитами и лейкоцитами плазма (L-PRP); 3) чистый обогащенный тромбоцитами фибрин (P-PRF); 4) обогащенный тромбоцитами и лейкоцитами фибрин (L-PRF). Эти 4 группы имеют различные способы получения, механизмы действия, соответствующие области применения [20].
Существуют мнения исследователей, что многие параметры получения ОТП, такие как количество оборотов и длительность центрифугирования, выбирались эмпирически и оценить их результаты объективно в сравнении с другими не представляется возможным [20].
Ряд авторов [17] определили, что концентрация тромбоцитов в ОТП коррелировала с количеством тромбоцитов в цельной крови донора. Однако какой-либо статистически значимой корреляции между количеством тромбоцитов в ОТП и в цельной крови донора выявлено не было. Было обнаружено значимое, но не имеющие клинического значения, влияние пола обследуемых на концентрацию тромбоцитов. Влияние возраста обнаружено не было.
При использовании ОТП у ряда исследователей возникла дискуссия о возможном влиянии ее клеточного состава. Так, некоторые авторы утверждают, что при инъекционном введении ОТП присутствие лейкоцитов может отрицательно влиять на клинические исходы из-за риска стимуляции воспалительного процесса [31]. Другие авторы оспаривают этот взгляд и говорят о выработке противоболевых медиаторов и действии лейкоцитов с естественной противовоспалительной способностью, как регулятора процесса заживления [31, 33].
Наибольшее применение ОТП нашла в стоматологической имплантологии [2]. Так, применение ОТП для костной пластики и профилактики атрофии челюстей перед дентальной имплантацией авторы добились формирования костной ткани в ранние сроки [4].С целью повышения качества и количества вновь формирующейся костной ткани при процедуре увеличения костного объема альвеолярной области верхней челюсти предложено использовать ОТП, в сочетании с трансплантацией аутологичной кости и различными остеозамещающими материалами [21, 29, 30].
Одним из основных механизмов регенерации является усиление кровоснабжения в тканях за счет стимуляции ангиогенеза при разрушении тромбоцитов и выделении ими факторов роста. В ОТП эти полипептидные факторы роста находятся в биологически предопределенных соотношениях.
В челюстно-лицевой реконструктивной медицине успешно используют гель из тромбоцитарный аутоплазмы, а также L-PRF мембраны, в том числе у детей с врожденными расщелинами верхней губы и неба [18, 24].
Плазма, обогащенная тромбоцитами нашла широкое применение в пародонтологии[18].
Описан инъекционный метод локальной стимуляции регенеративных процессов с применением ОТП, полученный после центрифугирования в пробирках Plasmolifting ТМ. В ходе исследования доказаны регенерационные свойства ОТП в виде снижения степени воспаления, уменьшения количества воспалительно-клеточных инфильтратов и воспалительных клеток в очаге воспаления тканей десны [11].
Многочисленные исследования, направленные на изучение эффективности использования ОТП в сердечно-сосудистой хирургии, доказали её положительное влияние у пациентов, после кардиохирургических операций. Реинфузия аутологичной обогащенной тромбоцитами плазмы улучшает гемостаз после искусственного кровообращения, может позволить снизить кровопотерю, проводить операцию без переливания гомологичной крови, а также купировать ряд гематологических нарушений [16, 19, 21].
Описано наблюдение тяжелой клинически проявляющейся фиброзной дисплазии лобно-глазничной области, по поводу которой проведена реконструкция с помощью ОТП [26]. Была достигнута длительная ремиссия симптомов и ранее формирование костной ткани. Сочетание введения ОТП с аллотрансплантацией или трансплантацией измельченной кости является безопасным, простым методом лечения.
Результаты клинических исследований в абдоминальной хирургии подтвердили эффективность клея с высоким содержанием фибрина при пластике по Лихтенштейну у пациентов с коагулопатиями на фоне заболеваний печени, а также длительно получавших антикоагулянты Использование фибриновых герметиков улучшает исходы хирургических вмешательств, ускоряет гемостаз, снижает кровопотери и число осложнений [5].
Полученные результаты экспериментального гистологического исследования структурно-функциональной организации при заживлении асептических ран мягких тканей на фоне применения ОТП показали, что данный метод лечения стимулирует процессы коллагенезации, эпидермизации, васкуляризации, происходит более быстрое формирование рубца [10].
В своей практике успешно применяют ОТП при хирургических и консервативных видах лечения воспалительных заболеваний суставов [23, 27].
На искусственно созданной модели остеоартроза коленного сустава у крыс применяли внутрисуставное введение тромбоцитарного геля [23], а также в работах по лечению травм мягких тканей опорно-двигательного аппарата (надрыв связок, мышц, сухожилий, тендопатий) использование ОТП в виде основного, а также дополнительного методов лечения (после хирургического вмешательства) подвергаются сомнению.
По мнению Л. Ю. Широковой с соавт. (2012) наблюдаются достоверные улучшения функционального состояния коленных суставов при локальном применение ОТП у пациентов гонартрозом с начальными проявлениями остеоартроза. При типичном гонартрозе II-III стадий, подтвержденных рентгенологически, ОТП оказывает кратковременное положительное влияние лишь в первый месяц наблюдений, тогда как при тяжелом гонартрозе, осложненном синовитом, лечение неэффективно.
Интраартикулярное введение ОТП в экспериментальной модели дефекта суставной поверхности коленного сустава на кроликах оказывает стимулирующее влияние на регенерацию гиалинового хряща, улучшая как качественные, так и количественные его характеристики [14].
Особый интерес приобретает вопрос использования конечных продуктов ОТП в эстетической пластической хирургии [25].
Имеются публикации об использовании ОТП в оториноларингологии для стимуляции регенерации барабанной перепонки при маленьких дефектах и после тимпанопластики [13]. Использование ОТП для герметизации пространства вокруг протеза при поршневой стапедопластике уменьшает риск развития сенсоневральной тугоухости по сравнению с использованием жировой клетчатки или свободным положением протеза. Вместе с тем уменьшается вероятность появления и интенсивность ушного шума после поршневой стапедопластики [7].
На основе проведенных исследований пациентов с хроническим гнойным средним отитом с применением ОТП при одновременном проведении санирующей операции и тимпанопластики в качестве опоры для неотимпанального трансплантата отмечалось более быстрое заживление послеоперационной полости, восстановление слуха [3], а также применение ОТП предупреждает возникновение перфораций, атрофических изменений барабанной перепонки и развитие спаечного процесса во вновь сформированной барабанной полости [9].
В результате экспериментального изучения функционального состояния звукопроводящей системы среднего уха и морфологических изменений в барабанной полости после заполнения ее ОТП у 6 свиней определена сохранность вентиляционной функции слуховой трубы, полная элиминация сгустка из барабанной полости, без образования рубцов и спаек [8].
Облитерация лобной пазухи с помощью трансплантата большеберцовой кости и введение ОТП после промывания и кюретажа пазухи может быть эффективным методом лечения хронического остеомиелита лобной пазухи [22].
Использование фибринового клея более эффективно, чем тампонада полости носа гемостатической губкой, а также применение химической и диатермокоагуляции у пациентов с носовым кровотечением [32].
Однако, при применении ОТП после эндоназальных эндоскопических хирургических вмешательств никакого благоприятного влияния не выявлено, исследование было прекращено досрочно [28].
Выполненные у 257 пациентов ринопластические и септопластические операции с использованием белково-тромбоцитарных свертков из обогащенной тромбоцитами плазмы показали их существенное преимущество над другими покровными материалами [1].
Местное применение ОТП после тонзиллэктомии позволяет существенно снизить вероятность послеоперационного кровотечения, уменьшает интенсивность болевых ощущений в глотке, а также снижает бактериальную обсемененность раневой поверхности в глотке, ускоряя процесс регенерации тканей [15].
Выводы: таким образом, ОТП является новой биотехнологией в клинической практике. Безопасность и эффективность ее использования широко освещены в литературе, но остается много нерешенных вопросов. На основании анализа научных публикаций новым шагом с биологической точки зрения необходима характеристика клеточного состава конечного продукта (наличие лейкоцитов, количества тромбоцитов и др.), которые могут влиять на процесс регенерации тканей. Возможность систематизация протоколов получения ОТП облегчит возможность использования в повседневной клинической практике.

Тромбоциты – форменные элементы крови, участвующие в образовании тромбов и остановке кровотечения.
Эти безъядерные частицы несут ряд ценных протеинов, называемых факторами роста.
Терапия обогащенной тромбоцитами плазмой (Platelet-rich plasma, PRP) основана на представлении врачей, что эти факторы роста способствуют заживлению, восстановлению поврежденных тканей.
Более правильно называть этот материал аутологичной обогащенной тромбоцитами плазмой, поскольку ОТП для последующего введения получают из крови самого пациента. Взяв определенное количество биоматериала, лаборатория отделяет клетки от плазмы и увеличивает концентрацию тромбоцитов. Полученная плазма насыщена стимулирующими протеинами, которые позволяют ускорять регенерацию поврежденных тканей при травмах, артрозе, других острых и хронических заболеваниях.
Исследования показывают, что ОТП может оказаться эффективным средством при болях в коленном суставе, особенно при безуспешности традиционных методов лечения.
Аутологичная обогащенная тромбоцитами плазма (ОТП) применяется в таких случаях:
• Нестабильность и боль в различных суставах
• Травмы суставов, в том числе коленного, плечевого, локтевого
• Дегенеративные заболевания суставов (гонартроз, коксартроз)
• Синдром запястного канала
• Растяжения связок
Хотя исследователи уверены в целебных свойствах факторов роста, до сих пор непонятно, каким образом ОТП способствует восстановлению поврежденных тканей. Наблюдения показывают, что улучшение испытывают не все пациенты, причем эффект (нормализация функций и/или уменьшение боли) отмечают в течение нескольких недель после начала терапии тромбоцитарной плазмой.
Если эффект от терапии ОТП наблюдается, он обычно длительный. Однако определенный процент пролеченных пациентов с заболеваниями коленного сустава нуждаются в повторном курсе.
Обогащенная тромбоцитами плазма против обогащенной протеинами плазмы
Как и тромбоциты крови, ОТП богата протеинами (белками), среди которых присутствуют те самые стимуляторы роста и другие ценные биологически активные молекулы. Эти понятия взаимозаменяемые.
Хотя аутологичная обогащенная тромбоцитами плазма относительно новое средство, накопилось достаточно сведений об эффективности данной терапии. Но давайте по хронологии.
Исследование 2013 года с участием 78 пациентов, страдающих двусторонним гонартрозом. Терапия обогащенной плазмой приводила к существенному уменьшению боли по сравнению с группой плацебо.
Исследование 2012 года, в котором задействовано 120 добровольцев с гонартрозом разной степени. Терапию ОТП сравнивали с внутрисуставными инъекциями гиалуроновой кислоты. Тромбоцитарная плазма оказалась эффективнее гиалуроната в плане улучшения боли и функций пораженного сустава.
Исследование 2009 года с участием 100 пациентов, страдающих дегенеративными заболеваниями хрящевой ткани коленного сустава. Группа участников на ОТП демонстрировала значимое улучшение самочувствия и функций сустава на протяжении 6 месяцев наблюдения после терапии.
Однако по истечении 12 месяцев ко многим участникам боль вернулась. Это позволяет предположить, что реципиенты нуждаются в периодических инъекциях ОТП с интервалом в несколько месяцев.
Исследование 2006 года продемонстрировало высокую эффективность обогащенной плазмы в лечении локтевого тендинита: улучшение функций сустава сразу после терапии составило порядка 60%.
Поскольку используется собственный биоматериал, вероятность иммунных реакций ничтожно мала.
Большинство научных работ сообщает о хорошей переносимости ОТП и минимальных, редких побочных эффектах. Современные данные позволяют некоторым зарубежным врачам рекомендовать тромбоцитарную плазму при артрозе и травмах коленного сустава как альтернативу оперативному лечению.
Чего ожидать от лечения обогащенной тромбоцитами плазмой?
В солидных западных клиниках, практикующих терапию ОТП, процесс начинается с всестороннего обследования пациента, уточнения показаний к этому экспериментальному лечению и ограничений.
На первом этапе производится забор крови из вены. Материал поступает в специальную лабораторию, где кровь разделяют, концентрируют тромбоцитарную плазму и возвращают в клинику. Внутрисуставное введение ОТП выполняют под ультразвуковым контролем, чтобы инъекция была максимально безопасной для пациента. Ультразвук безболезненный и не вредит здоровью.
Некоторые люди переживают о болезненности процедуры. Действительно, забор крови из вены неприятная манипуляция, некоторые люди чувствуют легкое головокружение. Однако при правильном выполнении она не представляет никакой опасности.
Сама внутрисуставная инъекция плазмы может быть болезненной, в зависимости от болевой чувствительности сустава и конкретного места введения препарата. Процедура займет 1-2 минуты. После инъекции возможна припухлость, но боли быть не должно.
В следующие недели после инъекции ОТП нужно соблюдать несколько правил:
• Избегать тяжелых физических упражнений, резких движений и переноса тяжестей.
• Не принимать нестероидные противовоспалительные препараты, такие как ибупрофен и аспирин. Эти лекарства могут повлиять на эффективность лечения. При болях обращаться к врачу!
• Носить первое время бандаж для стабилизации коленного сустава. Некоторые американские клиники рекомендуют пользоваться тростью, чтобы избежать ненужной нагрузки.
• Пользоваться холодными компрессами, чтобы уменьшить отек и болезненность в суставе. Некоторым людям помогает чередование теплых и холодных компрессов.
• Ночью спать на спине, чтобы больная нога была выровнена и приподнята на подушках.
Сильный отек, усиление боли и температура могут быть признаками осложнений и требуют срочного обращения к специалисту. То же самое нужно сделать в случае падения и других травм.
Через 1-2 месяца после лечения тромбоцитарной плазмой можно начинать физиотерапию, которая поможет быстрее восстановить движения в суставе, уменьшить риск последующих падений и травм.
Константин Моканов: магистр фармации и профессиональный медицинский переводчик
Читайте также:

