Нпо в онкологии что это такое
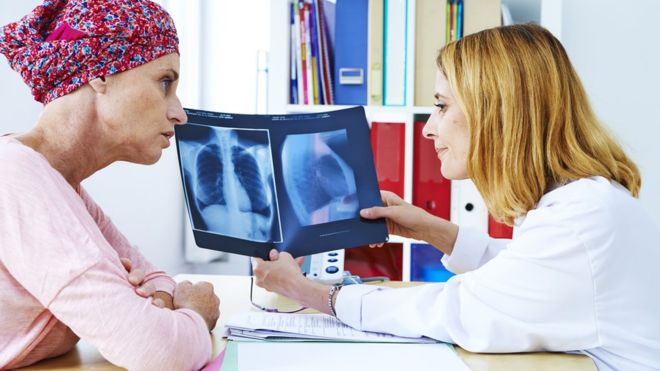
Рак из НПО (невыявленного первичного очага) — новообразование злокачественного характера, причину возникновения которого не удается установить методами стандартного и дополнительного обследования. При этом заболевание имеет морфологическое подтверждение.
Помимо отсутствия материнской опухоли опухолевый процесс характеризуется такими клиническими проявлениями, как непредсказуемость характера метастазирования, агрессивное течение заболевания, ранняя диссеминация.
Особой ситуацией с диагностической точки зрения считаются метастазы в шейных и паховых лимфоузлах. Поражение шейных лимфатических узлов (обычно средней и верхней третей), является показанием к эндоскопическому исследованию ротоглотки, носоглотки, глотки, гортани, а также верхних отделов пищевода. Одновременно проводится биопсия всех участков слизистой оболочки, вызывающих подозрение. Пациентам с метастазами плоскоклеточного рака в надключичных лимфоузлах и нижней трети шеи назначается бронхоскопия.
Гинекологическое исследование женщин проводят при обнаружении злокачественных клеток в паховых лимфоузлах. При этом шейка матки и влагалище обследуются в первую очередь. Одновременно проводится исследование аноректальной зоны, в том числе ректоскопия (аноскопия).
Световая микроскопия — основополагающее морфологическое исследование необходимое для определения тактики лечения рака из невыявленного первичного очага. Материал из метастатических образований забирается в объеме, необходимом для гистологических, лабораторных исследований, иммуногистохимического в том числе.
Группы опухолей НПО
Классификация рака из невыявленного первичного очага необходима для определения схемы дальнейших диагностических мероприятий и при выборе лечебной тактики. По результатам световой микроскопии, выделяют 5 групп злокачественных образований из НПО:
• плоскоклеточный рак;
• высоко- или умеренно дифференцированная аденокарцинома;
• рак с нейроэндокринной дифференциацией;
• злокачественная опухоль недифференцированная;
• аденокарцинома с низкой дифференцировкой.
Для лучшей дифференциации злокачественных новообразований от лимфом, герминоклеточных опухолей и других потенциально курабельных заболеваний назначают иммуногистохимическое исследование. Лечение меланомы, лимфомы, саркомы осуществляется на основе результатов и рекомендаций иммуногистохимического и светового микроскопического исследований. Только в некоторых случаях достаточно иммуногистохимического исследования для постановки окончательного диагноза, т. к. выявленные маркеры не специфичны для рака из НПО. Информация, полученная в результате этого диагностического метода необходима для определения лечебной схемы.
Плоскоклеточный рак
Он составляет 5–10 % от всех случаев злокачественных новообразований из невыявленного первичного очага. Чаще всего плоскоклеточным раком локализовано поражаются лимфатические узлы шеи или паховой области. Добиться продления срока выживаемости в этих случаях помогают методы специфической терапии. В нее входит лечение рака методами, аналогичными терапии, проводимой пациентам с плоскоклеточным раком ЛОР- органов. Пациентам с такой формой назначается комплексное лечение с использованием химиолучевой терапии. Оно наиболее эффективно, чем локальное воздействие на злокачественное новообразование или стандартное чередование химиотерапии и облучения.
В случае невозможности установления первичной опухоли при поражении паховых лимфоузлов, больному назначается лимфаденэктомия. После нее проводят курс лучевой терапии, иногда в комплексе с химиотерапией с препаратами платины. В ряде случаев проводится системная химиотерапия с использованием флуороурацила, цисплатина, иногда с добавлением паклитаксела. Методика входит в комплекс паллиативного лечения злокачественной опухли НПО
Низкодифференцированная нейроэндокринная карцинома
Иммуногистохимические исследования позволили отдельно выделить эту группу из всех опухолей из невыявленного первичного очага. Симптоматика и лечение заболеваний этого типа значительно отличаются от нейроэндокринных опухолей (карциноида). По мере совершенствования методики группа увеличивается.
Для подбора эффективного метода лечения вы можете обратиться за
- методы инновационной терапии;
- возможности участия в экспериментальной терапии;
- как получить квоту на бесплатное лечение в онкоцентр;
- организационные вопросы.
После консультации пациенту назначается день и время прибытия на лечение, отделение терапии, по возможности назначается лечащий доктор.



Рак из невыявленного первичного очага (НПО) – это морфологически подтвержденное злокачественное новообразование или метастаз, происхождение которого не может быть установлено в ходе стандартного и дополнительного обследования. В одной трети случаев первичный очаг проявляется в ходе течения болезни, еще в трети – на вскрытии, у оставшейся трети первоисточник так и не удается обнаружить.
Возможные объяснения этому – инволюция или самоизлечение первичной опухоли, возможность возникновения рака из клеток, имеющих дизэмбриональное происхождение, а также возможность злокачественной трансформации циркулирующих клеток после попадания в орган-мишень. Клинически, помимо отсутствия первичного очага, опухолевый процесс характеризуется ранней диссеминацией, агрессивностью течения и непредсказуемым характером метастазирования.
Прогноз, как правило, неблагоприятен, медиана выживаемости – 6–9 месяцев. Системная химиотерапия в большинстве случаев малоэффективна и носит сугубо паллиативный характер, однако в ряде случаев клинические и морфологические характеристики опухоли позволяют проводить эффективное специальное лечение.
Диагностика
Целью обследования больных раком из невыявленного очага является не установление определенного диагноза любой ценой, а выделение тех, кого возможно вы- лечить, в первую очередь больных с опухолями головы и шеи, лимфомами, экстрагонадными герминогенными опухолями, дифференцированным раком щитовидной железы, а также тех, кому можно провести эффективную химио- и гормонотерапию (при раке молочной и предстательной железы, мелкоклеточном раке легкого, раке яичников).
Прежде всего, выполняются диагностические обследования, направленные на ранее выполненные опухоли, спонтанно регрессировавших опухолевидных образований, резецированных в ходе предшествующих операций органов и тканей. При наличии соответствующей клинической симптоматики нужны эндоскопические исследования.
Дообследование необходимо и в ряде частных случаев:
- маммография – при подозрении на метастазирующий рак молочной железы (например, женщинам с поражением подмышечных лимфатических узлов, кроме маммографии, целесообразно проводить определение рецепторов к эстрогену и прогестерону в ткани метастаза);
- определение сывороточного ПСА (у мужчин с подозрением на рак предстательной железы, например при наличии метастазов в костях);
- определение уровня сывороточного бета-хорионического гонадотропина и альфа-фетопротеина у молодых мужчин с недифференцированными злока- чественными новообразованиями (особенно при локализации опухолевого процесса забрюшинно и/или в средостении) ввиду большой вероятности экстрагонадных герминогенных опухолей;
- КТ / МРТ органов головы и шеи – при поражении шейных лимфоузлов плоскокле- точным раком.
- ПЭТ КТ всего тела – наиболее информативное исследование, показывающее возможные очаги опухолей и метастазы, даже небольшого размера.
Новое в Израиле: молекулярный тест для выявления источника рака

Помимо этого, тест желателен в случаях, когда патологический диагноз опухоли вызывает сомнения или неокончателен, и перед принятием решения о конкретном виде лечения желательно получить более точный диагноз.
Метастазы в лимфоузлы
Одним из решающих моментов в определении тактики лечения больных раком из НПО является морфологическое исследование (световая микроскопия). Необходимо отметить, что забор материала, производимый, как правило, из очевидно метастатического образования, должен быть достаточен не только для гистологического исследования, но и для дополнительных лабораторных тестов, в первую очередь иммуногистохимического исследования, то есть речь должна идти как минимум о трепанобиопсии.
На этапе световой микроскопии злокачественные новообразования из НПО подразделяются на пять групп, что необходимо для дальнейших диагностических и лечебных мероприятий:
высоко- и умеренно дифференцированная аденокарцинома;
- низкодифференцированная аденокарцинома, или низкодифференцированный рак; плоскоклеточный рак;
- недифференцированная злокачественная опухоль;
- рак с нейроэндокринной дифференцировкой.
Иммуногистохимическое исследование необходимо, прежде всего, при недифференцированных злокачественных опухолях с целью исключить ряд потенциально курабельных заболеваний (лимфомы и герминоклеточные опухоли).
В случаях, когда после световой микроскопии и иммуногистохимического исследования устанавливается диагноз саркомы, меланомы либо лимфомы, лечение проводится в соответствии с рекомендациями для данных нозологических форм. При этом окончательный диагноз редко может быть выставлен только на основании иммуногистохимического исследования ввиду того, что указанные маркеры не являются абсолютно специфичными для соответствующих типов опухоли. Тем не менее, эта информация крайне важна для выработки тактики лечения.
Лечение
Лечение рака из невыявленного источника начинается после получения всех результатов обследований и состоит как правило, из курсов химиотерапии. Даже паллиативное лечение значительно улучшает качетсво жизни и улучшает прогноз. Что самое важное - в Израильских клиниках имеются высокопрофессиональные команды онкологов, радиологов и патологоанатомов, совместными усилиями специалистов большинству пациентов выставляется правильный диагноз в короткие сроки, по данным исследований выявляется первичный очаг рака и назначается правильное лечение - операция и последующая химиотерапия.

Внимание! Химиотерапия в Израиле носит персональный характер и назначается по возможности, таргетная и биотерапия, имеющие высокую эффективность и небольшой уровень побочных эффектов. Данный подход является стандартом современной онкологии.

Внимание! Регистрация желающих принять личное участие в конференции завершена.
Зарегистрироваться для онлайн-участия вы можете перейдя по ссылке
- Чем ЦАОП отличается от первичного онкологического кабинета?
Центр амбулаторной онкологической помощи (ЦАОП) создается как структурное подразделение медицинской организации для оказания первичной специализированной медико-санитарной помощи. Его основными задачами будут являться диагностика и лечение онкологических пациентов.
В первичном онкологическом кабинете в первую очередь ведется учет пациентов, наблюдение, контроль за их своевременной госпитализацией, оказывается всесторонняя помощь больному. Во многих субъектах вся диагностика и лечение проводятся на базе онкологического диспансера, иногда это может существенно влиять на время ожидания пациентами медицинской помощи.
Создание ЦАОП предполагает наличие всего спектра диагностического оборудования, необходимого для полного обследования пациента при подозрении на наличие злокачественного новообразования еще до его направления в онкодиспансер. Это позволяет сократить сроки начала его диагностики. Дополнительно в ЦАОП планируется создание коек дневного стационара.
Установление диагноза и определение методов лечения пациента, конечно, происходит на базе онкодиспансера. При этом для проведения некоторых схем химиотерапии пациента можно направлять в ЦАОП. Здесь же можно осуществлять оценку эффективности и переносимости проводимого лечения, проводить восстановительную и корригирующую терапию, связанную с возникновением побочных реакций на фоне лечения. И все это теперь пациент сможет получать ближе к своему дому.
ЦАОП может быть организован на базе поликлиники, центральной районной больницы, многофункционального медицинского центра, иногда даже онкодиспансера. Все зависит от индивидуальных особенностей каждого субъекта РФ. Как правило, ЦАОП организуется на базе той медицинской организации, которая уже достаточно оснащена всем необходимым диагностическим оборудованием. Если же его недостаточно, то многие региональные власти берут на себя решение этой задачи. В большинстве случаев это оборудование используется не только для пациентов ЦАОП, но и для других посетителей данной медицинской организации. Поэтому поддержка региональных властей проектов по организации ЦАОП крайне важна для жителей региона.
Организация ЦАОП не предполагает ликвидацию первичных онкологических кабинетов. Пациент может быть направлен врачом поликлиники в первичный онкологический кабинет или в ЦАОП. Это зависит от особенностей региона – его площади, плотности населения, транспортной доступности и в целом состоянии ресурсной базы онкологической службы региона. Поэтому принимать решение об открытии ЦАОП, определять их требуемое количество, место их организации, количество прикрепленного населения необходимо только по результатам глубокого анализа ситуации.
- Как пациенты попадают в ЦАОП?
Они могут обратиться туда самостоятельно, а могут быть направлены из поликлиники или первичного онкологического кабинета. Никаких ограничений нет. Многие регионы стараются широко информировать население об открытии ЦАОП, где он находится, как туда можно попасть, как добраться. Подробно прописывают маршрутизацию пациента с подозрением на онкологическое заболевание так, чтобы каждый врач знал, какие шаги он должен предпринять, чтобы направить пациента в ЦАОП.
- В чем еще особенность ЦАОП?
Хотите узнать больше о конференции? Подробности здесь
Онкологические заболевания в современном мире встречаются все чаще. Это связано с особенностями экологии, множеством новых вирусов, а также с большим количеством канцерогенов. Ежегодно ученые вводят новые методы борьбы с раком. Однако прежние способы лечения применяются до сих пор. Одним из них является ПХТ. Расшифровка этой аббревиатуры – полихимиотерапия. Системное введение цитостатических препаратов помогает устранить атипичные клетки, из которых состоит опухоль. Несмотря на то что данный вид лечения нелегко переносится пациентами, он является одним из самых эффективных методов.
ПХТ в онкологии: расшифровка аббревиатуры
В медицинской документации людей, страдающих от раковых заболеваний, часто встречается такое понятие, как химиотерапия. Сокращенно ее называют ПХТ. В онкологии расшифровка данной аббревиатуры - полихимиотерапия, что означает сочетанное воздействие сразу нескольких цитостатических средств. Данный вид лечения направлен на полное устранение опухоли или ее уменьшение.
В большинстве случаев ПХТ сочетают с другими методами лечения. Среди них – хирургическое удаление патологического образования и лучевая терапия. Иногда полихимиотерапия является самостоятельным методом лечения. Выбор ПХТ зависит от расположения и стадии рака, а также от состояния больного. Назначать цитостатические препараты может только врач-онколог.
Виды химиотерапии в онкологии

Противоположным понятием является адъювантная ПХТ в онкологии. Расшифровка аббревиатуры проста. АПХТ – это профилактическое лечение рака после операции. Имеется в виду, что саму опухоль полностью удалили, однако для предотвращения рецидива требуется цитостатическая терапия. Перечисленные виды ПХТ относятся к комбинированному или комплексному лечению злокачественных опухолей. То есть, помимо назначения препаратов, пациенту проводится операция, а иногда – и облучение.
Отдельным видом терапии является самостоятельный (лечебный) курс ПХТ в онкологии. Расшифровка подобного медицинского термина понятна не каждому врачу. Зачастую отличить лечебный курс от профилактической терапии может только онколог. Самостоятельная ПХТ проводится в тех случаях, когда другие методы оздоровления не показаны. Например, при мелкоклеточном раке легкого или наличии метастазов в отдаленные органы.
Показания к проведению терапии
Стоит отметить, что каждая злокачественная опухоль лечится по-разному. Иногда достаточно только оперативного лечения или облучения, в других случаях – требуется химиотерапия. ПХТ назначают лишь по специальным медицинским показаниям, когда это необходимо. Если подобное лечение не было предложено после операции врачом, значит злокачественный процесс был ограничен небольшим участком и не поразил глубокие слои органа. Кроме того, некоторые типы опухолей не поддаются химиотерапии. Выделяют следующие показания для ПХТ в онкологии:
- Злокачественные образования лимфоидной ткани.
- Рак крови.
- Опухоли пищеварительного тракта.
- Мелко- и крупноклеточный рак легкого.
- Новообразования головы и шеи.
Следует отметить, что эффективность химиотерапии зависит от гистологического типа опухоли. К примеру, железистый рак поддается цитостатическому лечению лучше, чем плоскоклеточная карцинома или саркома. Зачастую ПХТ не назначают на первых стадиях болезни, если опухоль можно удалить оперативным путем. Адъювантная терапия показана пациентам, у которых после хирургического лечения была обнаружена 2 или 3 стадия рака. Если опухоль имеет большой размер и проросла в соседние органы, назначают самостоятельный курс ПХТ. Иногда данный вид лечения применяется на поздней стадии рака, когда другие методы бессильны.
Что такое курс химиотерапии?
Большинство людей знает, что химиотерапию принято назначать курсами. Это означает, что цитостатические средства вводятся в организм неоднократно, а на протяжении длительного времени - с определенными промежутками. Подобная схема лечения необходима, потому что препараты разрушают не только саму опухоль, но и другие клетки организма. Введение большой дозы единовременно невозможно, так как цитостатики обладают кардио-, нефро- и гепатотоксичным действием. Чтобы организм восстановился после курса ПХТ, требуется время. В среднем это занимает 2-4 недели. За этот период клетки крови успевают обновиться, и общее самочувствие пациента приходит в норму.
Количество курсов ПХТ в онкологии может быть различным. Оно зависит от переносимости препаратов, состояния больного и эффективности лечения. После 3 курсов проводится обследование, благодаря которому врач делает соответствующее заключение. Если опухоль полностью исчезла или частично уменьшилась, химиотерапию продолжают. В случаях, когда имеется прогрессирование злокачественного процесса, схему ПХТ меняют. При этом отсчет курсов начинается заново.
Подготовка и сопроводительная терапия
Противопоказания к назначению химиотерапии
Несмотря на то что химиотерапия относится к одним из самых эффективных методов лечения рака, ее проведение не всегда необходимо. В некоторых случаях цитостатические средства приносят больше вреда, чем пользы. Проведение ПХТ противопоказано в следующих случаях:
- Старческий возраст (от 70 лет).
- Непереносимость цитостатических средств.
- Наличие тяжелых патологий со стороны сердца.
- Почечная и печеночная недостаточность.
- Прогрессирование заболевания, несмотря на проводимую терапию.
- Наличие множественных метастазов.
- Кахексия.
Перед тем как назначить ПХТ, проводится комплекс обследований. К ним относятся: общий и биохимический анализ крови, ЭКГ, ОАМ, коагулограмма, УЗИ сердца. При выявлении декомпенсированных заболеваний лечение цитостатиками нецелесообразно.
Возможные результаты химиотерапии
Для контроля эффективности ПХТ проводится повторное обследование. Благодаря этому оценивается результат терапии. К благоприятным исходам лечения относятся: полный и частичный регресс опухоли, а также стабилизация. В первом случае новообразование исчезает или уменьшается в размере в 2 раза и более. Стабилизация процесса означает, что опухоль осталась прежней. Однако это расценивается как положительный результат, ведь без лечения рак быстро прогрессирует.
Если при обследовании выявлено, что злокачественное образование растет, или появились метастазы, схему лечения меняют. При удовлетворительном состоянии пациента количество курсов химиотерапии неограниченно. Однако постоянное прогрессирование служит показателем того, что лечение не приносит результата, а только вредит организму. Это служит противопоказанием для назначения ПХТ.

Список лекарственных средств
- Отделение анестезиологии и реанимации
- Метастазы рака
- Химиотерапия
- Хоспис для онкологических больных
- Иммунотерапия в центре платной онкологии Медицина 24/7
- КТ-исследования
- МРТ-исследования
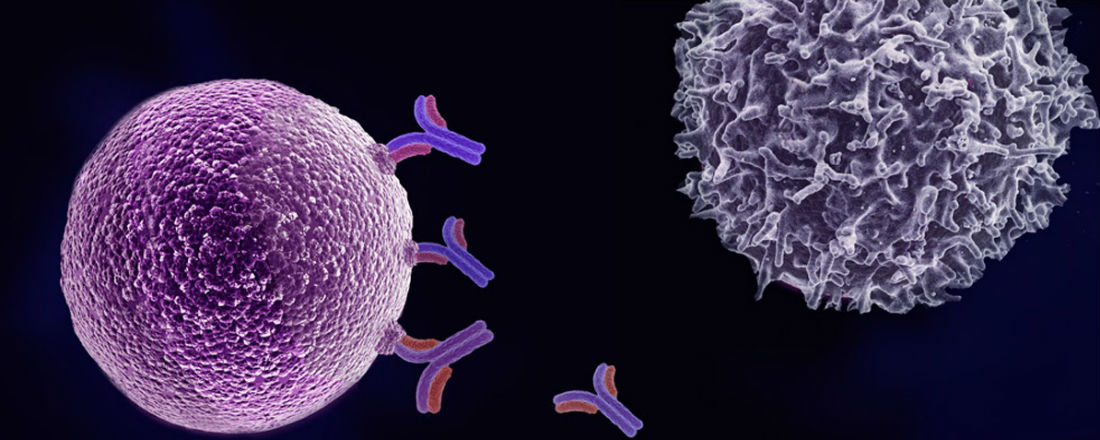
Что такое иммунотерапия?
Объясните, как это работает?
Откуда вообще взялся этот метод лечения?
Первые попытки вылечить пациентов, больных раком, с помощью иммунотерапии были предприняты более ста лет назад. Одним из родоначальников метода считается хирург Уильям Коли. Он заметил, что у некоторых пациентов с рожистым воспалением (бактериальной кожной инфекцией) онкологическое заболевание полностью регрессировало. Коли предположил, что инфекция стимулирует иммунитет на уничтожение опухолевых клеток, и решил подтвердить свои догадки экспериментально. В 1891 году он ввел стрептококковые бактерии пациенту с саркомой кости и смог добиться сокращения злокачественной опухоли.
Тогда его исследования подверглись активной критике, так как не имели внятного теоретического обоснования. Постепенно накапливались знания о физиологии иммунитета, вместе с этим предпринимались новые попытки активировать собственные защитные силы организма для борьбы со злокачественными опухолями — иммунотерапия получила развитие.
Если иммунотерапия существует так давно, почему о ней активно заговорили только сейчас?
Потому что настоящие прорывы произошли лишь в последние годы. Так, в 2018-м Нобелевскую премию по медицине вручили ученым Джеймсу Эллисону из США и Тасуку Хондзё из Японии за открытие контрольных точек — благодаря этому было создано несколько иммунотерапевтических препаратов. Короткий промежуток между теоретическим открытием и внедрением его результатов в медицинскую практику — еще одна причина того, что о новой методике активно говорят. Иммунотерапия открыла новые возможности для борьбы с онкологическими заболеваниями, которые лечатся с большим трудом, например с меланомой и раком легких. Теперь некоторые такие пациенты могут жить на несколько лет дольше без прогрессирования болезни.
Любой ли рак можно вылечить с помощью иммунотерапии?
Это зависит от препарата и особенностей опухоли. Так, препарат пембролизумаб стал первым, который можно назначать вне зависимости от места возникновения рака, если опухоль имеет специфический биомаркер — микросателлитную нестабильность, или PDL-экспрессию. Иммунотерапию применяют для лечения меланомы, рака легких, почки, желудка, мочевого пузыря, простаты, поджелудочной железы, глиобластомы, лимфомы Ходжкина и еще нескольких видов опухолей. Но пока лучшие результаты терапия показала в лечении меланомы и рака легких. Определить, какое лечение подойдет в конкретном случае, может только лечащий врач.
А побочные эффекты есть?
Есть. Так же как и у других эффективных методов лечения онкологических заболеваний — но они отличаются от нежелательных явлений при химиотерапии: причина их возникновения не токсическое действие самих препаратов, а сильный иммунный ответ. Нередко пациенты на иммунотерапии могут сталкиваться с усталостью, кашлем и тошнотой, теряют аппетит, а на коже может появиться сыпь. Реже эти лекарства могут вызывать более серьезные проблемы в легких, кишечнике, печени, почках и других органах. Обычно так бывает, если иммунитет начинает атаковать не только опухолевые клетки, но и здоровые. Пациенты, которые проходят лучевую терапию, также нередко испытывают усталость, у них могут быть проблемы с кожей, а люди, которые получают химиотерапию, сталкиваются с потерей волос, анемией, тошнотой и рядом других проблем.
Объясните, как проходит лечение. Обязательно ложиться в больницу?
В России этот метод лечения популярен?
Нет. Некоторые препараты, например пембролизумаб, ниволумаб, ипилимумаб и атезолизумаб, зарегистрированы в России. Но о широком доступе к терапии говорить не приходится. Препараты зарегистрированы не по всем показаниям, и во многих ситуациях назначить их можно только офлейбл (не по инструкции), но тогда лечение нельзя будет получить бесплатно по полису ОМС.

- Что такое метастазы?
- Из-за чего возникают метастазы?
- С какой вероятностью возникают метастазы?
- От чего зависит скорость распространения метастазов по организму?
- Как метастазируют различные виды рака?
- Как проявляются метастазы?
- Как диагностируются метастазы?
- Можно ли вылечить метастазы, и что это дает?
- Где лучше лечить рак с метастазами — в Москве, в Израиле или в Германии?
Что такое метастазы?
Современные концепции развития метастазов основаны на том, что метастазы развиваются практически сразу, как только появляется сама злокачественная опухоль. Отдельные оторвавшиеся от нее клетки сначала проникают в просвет кровеносного (гематогенный путь диссеминирования) или лимфатического (лимфогенный путь диссеминирования) сосуда, а затем переносятся с током крови или лимфы, останавливаются на новом месте, выходят из сосуда и растут, образуя метастазы. Вначале этот процесс идет медленно и незаметно, поскольку раковые клетки из материнского очага подавляют активность вторичных очагов.
С момента, когда возникают вторичные очаги, рак называют метастатическим. Процесс распространения раковых клеток называют метастазированием.
Способность к метастазированию — один из ключевых признаков злокачественных опухолей, который отличает их от доброкачественных новообразований.
Из-за чего возникают метастазы?
Будут ли отдельные клетки отрываться от материнской опухоли и формировать метастазы? Опухолевые клетки отрываются и будут отрываться всегда. Местные факторы иммунной системы очень долгое время защищают организм от быстрого роста опухолевых клеток. Вопрос лишь в вероятности возникновения метастазов, а она зависит от типа опухоли, скорости ее роста, степени дифференцировки клеток (насколько они отличаются от нормальных), стадии, на которой был диагностирован рак, и других факторов.
Распространившись, опухолевые клетки долго, на протяжении ряда лет, могут оставаться неактивными или расти очень медленно. Точные механизмы запуска быстрого роста метастазов в организме не изучены.
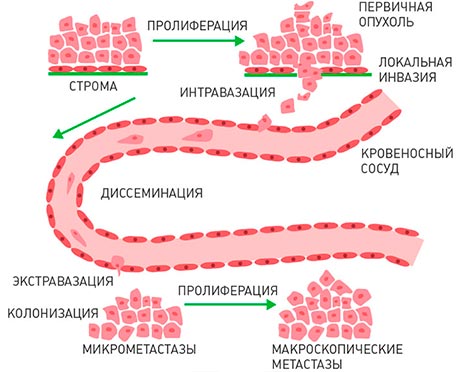
Важен другой факт: по мере увеличения числа клеток в метастазе, они начинают выделять особые вещества - факторы роста. Эти факторы роста стимулируют образование капиллярной сети, что обеспечивает клетки раковой опухоли всеми питательными веществами в ущерб остальным тканям организма.
Можно выделить несколько стадий распространения рака по организму:
- Проникновение опухолевых клеток в ближайший кровеносный или лимфатический сосуд;
- Распространение с током крови или лимфы по различным частям тела;
- Затем раковая клетка останавливается в одном из мелких сосудов и проникает через его стенку в ткани;
- Какое-то время она неактивна или размножается, но очень медленно;
- Бурный рост, разрастание капиллярной сети.
Многие опухолевые клетки погибают на одной из этих стадий. Те, которым удалось выжить, дают начало метастазам.
С какой вероятностью возникают метастазы?

От чего зависит скорость распространения метастазов по организму?
Время, необходимое для клинического проявления первых метастазов, во многом определяется видом опухоли и степенью дифференцировки её тканей.
- Высокодифференцированные опухоли, как правило, метастазируют гораздо реже и позднее, чем низкодифференцированные опухоли.
- В низкодифференцированных опухолях клетки практически утрачивают черты нормальной ткани. Такой рак ведет себя агрессивнее.
Вероятность метастазирования можно снизить при помощи разных методов лечения:
- Химиотерапия. Например, адъювантная химиотерапия проводится после операции и помогает уничтожить раковые клетки, которые, возможно, остались в организме.
- Лучевая терапия.
Существует такое заблуждение, что метастазы возникают из-за проведенных процедуры. Однако, удаление части опухоли или ее биопсия (взятие ткани опухоли на исследование) не повышают частоту развития метастазов.
Как метастазируют различные виды рака?
Наиболее часто метастазы обнаруживаются в лимфатических узлах, печени, легких, существенно реже — в мышце сердца, скелетных мышцах, коже, селезенке, поджелудочной железе. Промежуточное место по частоте обнаружения метастазов при различных видах рака занимают центральная нервная система, костная система, почки, надпочечники.
- Метастаз Крукенберга — в яичники;
- Метастаз сестры Марии Джозеф — в пупок;
- Метастаз Вирхова — в лимфоузлы над левой ключицей.
- Рак молочной железы: легкие, печень, кости.
- Рак яичников: брюшина, печень, легкие.
- Рак желудка: печень, брюшина, легкие.
- Рак кишечника (толстой кишки): печень, брюшина, легкие.
- Рак прямой кишки: печень, легкие, надпочечники.
- Рак предстательной железы: кости, легкие, печень.
- Рак матки: печень, легкие, брюшина.
- Рак почек: легкие, печень, кости.
- Рак легкого: надпочечники, печень, второе легкое.
- Меланома: легкие, кожа/мышечные ткани, печень.
- Рак поджелудочной железы: печень, легкие, брюшина.
- Рак щитовидной железы: легкие, печень, кости.
Метастазирование, как правило, происходит в случаях, когда исчерпаны резервы организма в борьбе с опухолью. Метастазы существенно нарушают функционирование всех жизненно важных органов и систем. В подавляющем большинстве смерть онкологических пациентов обусловлена именно метастазами.
Кроме того, метастазы существенно ухудшают общее состояние, нередко сопровождаясь нестерпимыми болями, требующими постоянного обезболивания.
Как проявляются метастазы?
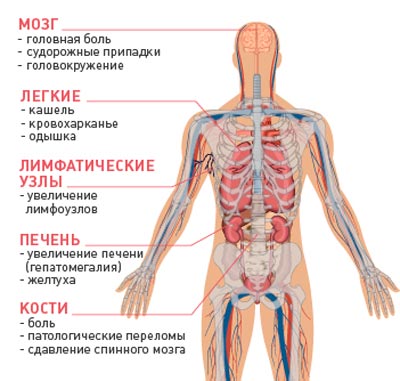
Клиническая картина метастатического рака определяется местом расположения метастазов:
- Поражение брюшины (канцероматоз брюшины) приводит к возникновению асцита, что требует проведения лапароцентеза;
- Поражение плевры (канцероматоз плевры) вызывает развитие экссудативного плеврита, который требует выполнения торакоцентеза;
- Поражение костей и позвоночника ведет к болям в разных частях тела, переломам;
- Поражение легких проявляется в виде одышки;
- Метастазы головного мозга приводят к головным болям, головокружениям, судорогам, нарушению сознания;
- Поражение печени приводит к механической желтухе.
Кроме того, высвобождающиеся в ходе постоянной гибели опухолевых клеток токсины вызывают раковую интоксикацию организма.
Как диагностируются метастазы?
Обзорная рентгенография, ультразвуковое исследование, радиоизотопное исследование, компьютерная томография, магнитно - резонансная томография, позитронно - эмиссионная томография, — все эти методики имеют существенное значение в распознавании метастазов. Эти методики дают возможность уточнить величину, распространенность и характер роста метастазов, их распад, нагноение, прорастание в соседние органы и ткани. Кроме того, эти же методики диагностики позволяют контролировать эффективность лечения по степени регресса метастазов.
Условно можно выделить два этапа диагностики метастазов:
- Первичное обследование, когда только диагностирована основная опухоль;
- Наблюдение у онколога после пройденного лечения. Если изначально метастазы обнаружены не были, а лечение прошло успешно, в будущей все равно придется периодически проходить обследования - есть риск рецидива.
Можно ли вылечить метастазы, и что это дает?
Основной целью активной химиотерапии и лучевой терапии является профилактика возникновения метастазов рака на максимально ранней стадии. Лечение основано на общих принципах лечения опухолей, включая химиотерапию, лучевую терапию, оперативное лечение (при одиночных метастазах).
Лечение метастазов рака имеет определенные сложности. Поэтому в ряде случаев мы проводим лечение метастазов с целью облегчения симптомов и продления жизни. Мы используем системную терапию (химиотерапия, гормонотерапия, таргетная терапия), и местные виды лечения (хирургия, радиотерапия). Лечение тормозит рост опухоли, уменьшает ее размеры, замедляет процесс метастазирования. Это помогает подарить пациенту лишние месяцы, а иногда и годы.
Параллельно проводят поддерживающую терапию, которая помогает справиться с симптомами и побочными эффектами химиотерапии. При болях назначают сильные обезболивающие средства.
За рубежом при метастатических очагах в печени часто используют чрескожную чреспеченочную радиочастотную аблацию. Данная методика доступна нашим пациентам в Европейской клинике.
Как говорилось выше, лечение в таких случаях является средством облегчения состояния пациента. Вероятность достижения ремиссии очень мала.
Мы в Европейской клинике также используем такую методику как эмболизация артерий, питающих крупные метастазы в различных органах.
Узнайте о современных методах лечения метастазов рака в печени, которые применяют врачи Европейской клиники, а также о результатах лечения - историях пациентов Европейской клиники.
Где лучше лечить рак с метастазами — в Москве, в Израиле или в Германии?
Для того чтобы получить наиболее современное и эффективное лечение при раке с метастазами, российскому пациенту не обязательно ехать за границу. В Европейской клинике применяются те же препараты и технологии, что и в ведущих онкологических центрах мира.
Даже если вероятность ремиссии мала, лечение нужно продолжать. Врачи-онкологи Европейской клиники знают, как облегчить страдания пациента, продлить жизнь. Для этого мы используем наиболее современные методики и препараты. Если вы проходите курс лечения в другой клинике, у нас всегда можно получить второе врачебное мнение: иногда подходы разных врачей к лечению метастатического рака сильно различаются.
Выберите врача и запишитесь на приём:

Главный врач Европейской клиники, онколог, к.м.н.
Читайте также:





