Нет мутаций при раке легких
Когда в 1962 году американский ученый обнаружил в экстракте слюнной железы мышей сложное вещество, эпидермальный фактор роста (EGF), состоящий из более чем пяти десятков аминокислот, он и не представлял, что сделал первый шаг к большому открытию, которому будет суждено изменить представление о раке легкого. Но лишь в начале XXI века станет достоверно известно, что мутации рецептора, с которым связывается EGF, могут становиться отправной точкой в развитии одной из самых агрессивных опухолей – рака легкого.
Что такое эпидермальный фактор роста?
Следует отметить, что EGF – белок, необходимый нашему организму. Так, находящийся в слюнных железах эпидермальный фактор роста обеспечивает нормальный рост эпителия пищевода и желудка. Кроме того, EGF содержится в плазме крови, моче, молоке.
Свою работу EGF выполняет, связываясь с рецептором эпидермального фактора роста, EGFR, расположенным на поверхности клеток. Это приводит к активации ферментов тирозинкиназ, которые и передают сигнал о необходимости активной деятельности. В результате происходят несколько последовательных процессов, в том числе увеличение скорости выработки белков и синтез молекулы, которая обеспечивает хранение и реализацию программы развития живых организмов, ДНК. Итогом этого и становится деление клеток.
В 90-х годах прошлого века стала очевидна роль рецептора эпидермального фактора роста как онкогена, играющего одну из ведущих ролей в развитии ряда злокачественных заболеваний.
Эпидермальный фактор роста и рак
В конце XX века было проведено несколько исследований, подтверждающих значение EGF в развитии злокачественных заболеваний. В 1990 году американские ученые доказали, что блокирование связывания эпидермального фактора роста с рецепторами и, как следствие, предотвращение активации фермента тирозинкиназы останавливает рост злокачественных клеток [1].
Есть ли у вас мутация эпидермального фактора роста?
Показательные результаты, отражающие распределение мутаций эпидермального фактора роста среди россиян, были получены в одном крупном отечественном исследовании, в котором были изучены данные более 10 тысяч больных раком легкого [2]. Они показали, что мутации EGFR обнаруживались:
- У 20,2% больных аденокарциномой, 4,2% больных плоскоклеточным раком и 6,7% больных крупноклеточной карциномой легкого
- У 38,2% некурящих женщин и только у 15,5% некурящих мужчин
- У 22% курящих женщин и 6,2% курящих мужчин
Результаты зарубежного исследования, в котором участвовали более 2000 больных аденокарциномой легкого [3], показали, что мутация EGFR была выявлена:
- У 15% больных, которые курили в прошлом
- 6% больных, куривших в настоящем
- 52% больных, которые никогда не курили
Эти данные подтверждают: мутации рецептора эпидермального фактора роста могут быть обнаружены и у тех, кто не представляет жизни без сигареты, просто гораздо реже, чем у приверженцев здорового образа жизни.
Если у вас обнаружена мутация EGFR
Еще каких-то десять лет назад у половины больных раком легкого было гораздо меньше шансов успешно бороться с опухолью. Однако сегодня стали доступны препараты, которые позволили в корне изменить эту ситуацию. Речь идет о таргетной терапии, которая стала доступной в последнее десятилетие.
Наличие мутации эпидермального фактора роста, подтвержденное результатами молекулярно-генетического исследования, предоставляет онкологам возможность ввести в схему лечения таргетные препараты. Создание таргетных лекарственных средств для лечения рака легкого стало прорывом в современной онкологии.
Таргетная терапия рака позволяет значительно отдалить его прогрессирование, в том числе и по сравнению со стандартной химиотерапией. Это – значимое преимущество таргетных лекарств.
Способность таргетных препаратов (ингибиторов тирозинкиназы EGFR) продлевать время до прогрессирования опухоли была доказана в крупном анализе, изучающем результаты 23 исследований, в которых участвовало более 14 тысяч больных немелкоклеточным раком легкого с мутацией рецептора эпидермального фактора роста [6].
Важно отметить, что при наличии мутации EGFR лечение рака, как правило, не исчерпывается только таргетными препаратами. Вы должны быть готовым к сложной, длительной и комплексной терапии, в том числе оперативному вмешательству, лучевой терапии и др.
Если у вас не обнаружена мутация EGFR
- Divgi C.R., et al. Phase I and Imaging Trial of Indium 111-Labeled Anti-Epidermal Growth Factor Receptor Monoclonal Antibody 225 in Patients With Squamous Cell Lung Carcinoma. JNCI J. Natl. Cancer Inst. Oxford University Press, 1991. Vol.83, №2, P. 97-104.
- Imyanitov E.N., et al. Distribution of EGFR Mutations in 10,607 Russian Patients with Lung Cancer. Mol. Diagn. Ther. Springer International Publishing, 2016. Vol.20, №4, P. 40-406.
- D’Angelo S.P., et al. Incidence of EGFR exon 19 deletions and L858R in tumor specimens from men and cigarette smokers with lung adenocarcinomas. J. Clin. Oncol. American Society of Clinical Oncology , 2011. Vol.29, №15, P. 2066-2070.
- Sharma S.V., et al. Epidermal growth factor receptor mutations in lung cancer. Nat. Rev. Cancer. 2007. Vol.7, №3, P. 169-181.
- Lynch T.J., et al. Activating Mutations in the Epidermal Growth Factor Receptor Underlying Responsiveness of Non-Small-Cell Lung Cancer to Gefitinib. N. Engl. J. Med. Massachusetts Medical Society, 2004. Vol.350, №21, P. 2129-2139.
- Lee C.K., et al. Impact of EGFR Inhibitor in Non-Small Cell Lung Cancer on Progression-Free and Overall Survival: A Meta-Analysis. JNCI J. Natl. Cancer Inst. Oxford University Press, 2013. Vol.105, №9, P. 595-605.
При копировании материалов
ссылка на сайт обязательна.

Успехи современной клинической онкологии неоспоримы. Все более сложные операции, новые препараты, эффективные методы обезболивания и устранения мучительных симптомов. Мы в нашем блоге достаточно рассказывали о том, как сегодня можно продлить и облегчить жизнь пациентам даже на последних стадиях болезни.
Но, тем не менее, тысячи онкологических больных во всем мире ежедневно узнают, что опухоль, которая вчера поддавалась определенному лечению – сегодня снова растет или дает метастазы. Врачи регулярно оказываются в тупике: все положенные лекарства и методы лечения перепробованы, и эффективных для данного пациента – не осталось.
Однако даже из этого тупика можно найти выход. С развитием генетики и молекулярной биологии в руках онкологов оказался новый способ изучить опухоль, чтобы найти в ней уязвимые места.
Для этого используют молекулярно-генетическое тестирование – определение особенностей ДНК раковых клеток. Метод сложный технически, дорогой, требует специфических знаний от врача.
Исследование занимает 3 недели, стоит от 250 до 670 т.р. В результате врач получает отчет в 30 страниц сложной информации, которой он еще должен уметь воспользоваться. Но пациентам, которые уже было перестали надеяться, это дает дополнительное время жизни.
Сегодня мы хотим рассказать о том, как делается молекулярно-генетическое тестирование, в каких случаях оно может помочь пациенту и какие знания дает врачу.
Мы все – мутанты, это норма. Но некоторые мутации приводят к раку
Для этого все соматические клетки (те, из которых состоит организм), кроме эритроцитов, беспрестанно делятся.

Деление соматических клеток происходит во всех органах и тканях
Иногда в процессе деления получаются сбои – мутации. То нить ДНК порвется, то скопируется с ошибкой, то участки хромосом перемешаются. Влиять на это может сотня факторов: от стресса и табачного дыма до воздействия радиации.
Мутации можно разделить на 4 вида.
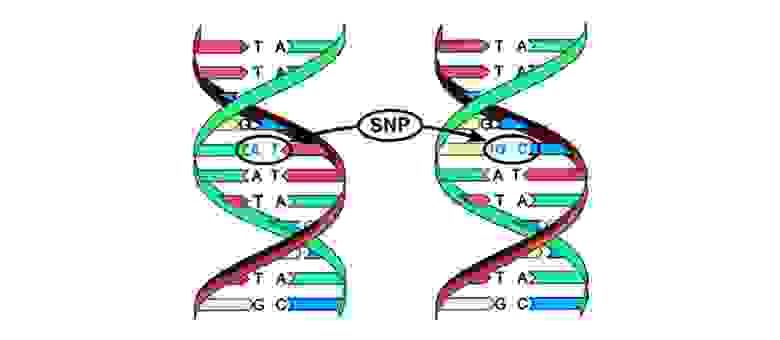
2. Хромосомные аберрации.
Делеция – утрата участка хромосомы. Происходят из-за обрыва концевого участка или разрыва ДНК сразу в двух местах. Всё – этот ген в хромосоме больше не экспрессируется.
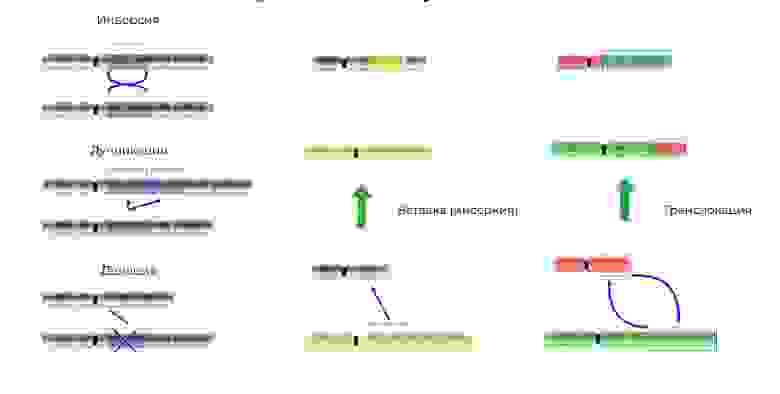
Мутации изменяют не только структуру участка ДНК, но и порядок этих участков
Злокачественную клетку от нормальной отличает нарушение клеточного цикла.
Клеточный цикл (жизнь клетки от деления до деления/гибели) строго регулируется работой специальных белков: киназы, циклины, факторы роста и транскрипционные факторы – в каждой живой клетке их десятки, и у каждого своя узкоспециальная, но важная функция.
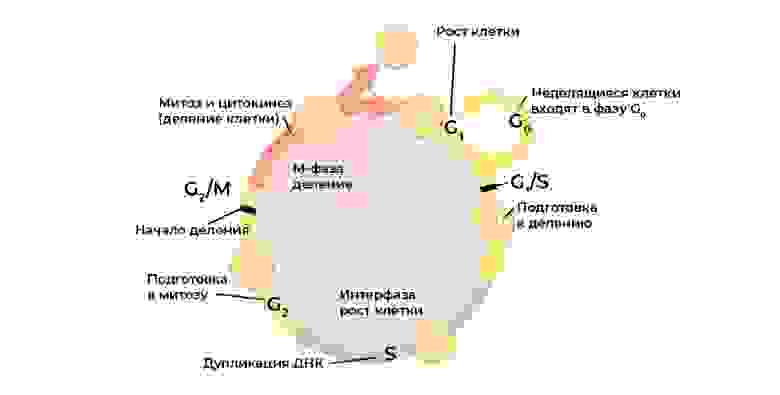
Каждый этап клеточного цикла контролируется белками-регуляторами
Таких значимых генов, изменения в которых могут привести к канцерогенезу (возникновению рака) – две больших группы.
Из тех, что наиболее хорошо изучены и у всех на слуху:
- EGFR, ALK, BRAF – немелкоклеточный рак легкого;
- BRAF – меланома;
- HER2 – рак молочной железы (РМЖ);
- KRAS – колоректальный рак.
Причем, мутации этих генов бывают обнаружены при нескольких видах опухолей. Например, повышенная экспрессия HER2 обнаруживается не только при РМЖ, но и при раке легкого и желудка.
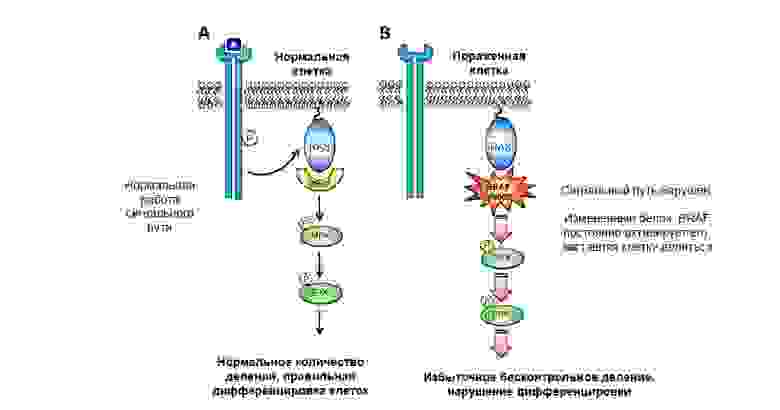
Мутация в протоонкогене белка BRAF приводит к неконтролируемому росту опухоли.
Гены-супрессоры опухоли (антионкогены) – напротив, могут подавить рост опухолевых клеток или участвуют в репарации (починке) поврежденной ДНК. А вот инактивация генов-супрессоров в результате мутации – резко увеличивает вероятность появления злокачественной опухоли.
Всего изучено влияние нескольких десятков протоонкогенов и опухолевых супрессоров на канцерогенез.
Зачем столько сложностей и как они продлевают жизнь пациентам
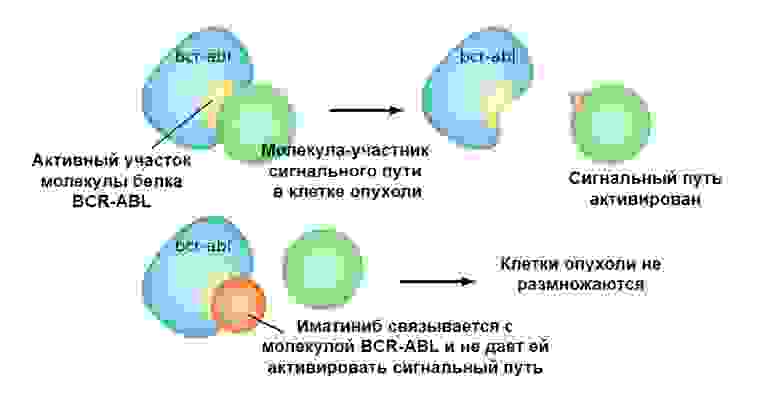
Иматиниб связывается с активным участком молекулы белка BCR-ABL, и блокирует его способность взаимодействовать с остальными молекулами в цепочках сигнальных путей.
Так что таргетные препараты имеют 2 важных преимущества перед классической химиотерапией.
Но и лечение для него должно быть соответствующее – индивидуально подобранное для конкретного пациента – на основе того, что мы определяем мутации в его опухолевых клетках.
В совсем недалеком прошлом злокачественные опухоли можно было классифицировать только по гистологии, то есть в зависимости от того, в каком органе они возникли, и как выглядели раковые клетки под микроскопом.
- узнаем чувствительность опухоли к препаратам;
- выясним, есть ли у опухоли устойчивость к определенным лекарствам;
- обнаружим генетические особенности, которые дают гиперчувствительность к препаратам;
- подберем новое лечение, если опухоль перестала отвечать на стандартную терапию;
обнаружим опухоль/метастаз на очень ранней стадии – по обрывкам ее ДНК в крови; - можем прогнозировать благоприятное или агрессивное течение заболевания.
Образцом выступает чаще всего ткань опухоли, либо взятая во время операции по удалению первичного очага, либо биопсия – микроскопический кусочек опухоли берут специальной тонкой длинной иглой.
Можно поискать ДНК опухолевых клеток в крови – тогда нужна так называемая жидкостная биопсия, две пробирки с кровью по 8,5 мл.
При биопсии мы часто сталкиваемся с тем, что многие пациенты боятся вообще трогать опухоль – опасаются, что ее это спровоцирует на рост. На сегодня не доступны какие-либо исследования, которые бы показали такую взаимосвязь. Конечно, биопсию надо выполнять правильно. У нас чаще всего врачи при заборе биоптата помечают место входа иглы: либо делают маленькую татуировочку (есть и такой инструмент ), либо скобку (хирургическую) ставят. Если потом понадобится операция, они иссекают весь этот ход, где была игла – от кожи до опухоли – так мы делаем шанс распространения раковых клеток за пределы опухоли еще меньше.
Далее образцы отправляются в лабораторию молекулярно-генетически исследований.
Причем применяют сразу несколько методов: секвенирования нового поколения (NGS), секвенирование по Сэнгеру и метод флуоресцентной гибридизации (FISH). Вместе они позволяют прочесть всю последовательность ДНК опухоли, выяснить драйверные мутации – то есть те, которые запустили злокачественный процесс и теперь могут быть мишенью для таргетной терапии – и даже визуализировать весь кариотип (хромосомный набор).
Кроме того, в полном молекулярно-генетическом исследовании обязательно определяют микросателлитную нестабильность (MSI, microsatellite instability) – нарушение в работе механизма репарации ДНК, которые приводят к быстрому накоплению мутаций в клетках. Этот фактор позволяет делать прогноз по поводу дальнейшего течения заболевания.
После получения молекулярно-генетического профиля опухоли – начинается его анализ
Специальные программы обрабатывают полученные результаты и составляют рекомендации автоматически. Но затем эти рекомендации обязательно вручную курируются командой экспертов. В анализе участвуют генетики, биоинформатики, врачи-онкологи, иммунологи и химиотерапевты. На этом этапе обязательно происходят уточнения и дополнения.
В итоге, в первой части отчета прописаны все найденные мутации в опухоли пациента, и таргетные препараты, которые будут наиболее эффективны в данном случае. Указана таргетная терапия, одобренная для данного типа опухолей с обнаруженными мутациями, и таргетная терапия, которая одобрена для лечения других типов рака с теми же мутациями. У нас в практике были случаи, когда назначались препараты именно второго порядка, off-label – и хорошо действовали.
Далее сотрудники лаборатории проводят огромную работу по мониторингу научных исследований, которые могут быть значимы в случае с данным пациентом.
Во второй части отчета находится обзор существующих на тот момент исследований с подробными данными о частоте встречаемости данной мутации, о действии разных препаратов и о возможности использовать тот или иной вид таргетной терапии при выявленных мутациях. Это помогает составить хотя бы приблизительный прогноз для пациента.
В третьей части отчета собраны актуальные клинические исследования, в которых пациент может принять участие, чтобы получить экспериментальное лечение. Это самый последний запасной способ, но знать о нем все подробности – полезно для спокойствия пациента.

Отчет получается довольно увесистым – 30 страниц захватывающего чтения
В этом случае молекулярно-генетическое исследование и дает нам понимание, какой препарат будет эффективен против данной опухоли, именно с этим набором мутаций. Назначение такого препарата позволяет выиграть главный для онкопациента ресурс – время.
Проблемы методики
Опухоли неоднородны. Они состоят из разных клеток, которые могут отличаться весьма значительно. И, например, в 80% клеток опухоли мутация определенного гена присутствует, а 20% клеток поделились с другим распределением хромосом – и остались немутировавшими. Да, мы назначаем препарат по результатам молекулярно-генетического теста, и против 80% опухолевых клеток он сработает эффективно, но для оставшихся 20% нужно будет придумывать другое лечение.
Некоторые виды рака более-менее гетерогенны, например, РМЖ. А некоторые опухоли, такие как саркомы, напоминают по структуре винегрет. Это затрудняет и диагностику, и лечение: нельзя заранее узнать, в какой части опухоли какие клетки, сколько их видов, как сильно они отличаются. И нельзя, грубо говоря, взять 10 образцов из разных мест опухоли – по ним придется сделать 10 отдельных генетических исследований.
До 30% таргетных и иммунопрепаратов в России назначается без соответствующего обоснования – без исследований генетики опухоли. И часть этих лекарств оказывается пустой тратой средств бюджета и денег пациента, потому что назначать таргетное лечение без понимания генетики опухоли – это рулетка: зарегистрировано более 600 препаратов. Например, для рака молочной железы есть пять протоколов лечения, в зависимости от мутации гена HER2/Neu.
В западной медицине определение генетического профиля опухоли уже становится стандартом лечения. Для российских онкопациентов молекулярно-генетические тестирования – все еще редкий случай, к сожалению – для бюджетной медицины это пока дорого. Но есть надежда, что все изменится к лучшему. Если сейчас оно стоит 600 тыс. руб., то 5 лет назад стоило больше миллиона – технология становится все проще и совершеннее, а, значит, популярнее и доступнее. Здесь время работает на нас.
Поэтому мало просо сделать генетический тест, нужно уметь понять результаты и сделать верные выводы. Мы с коллегами чаще всего сначала изучаем отчет сами (бывает, приходится посидеть над ним дома, в тишине после работы) – а потом еще и собираем консилиум, принимаем коллегиальное решение.
Но хорошие истории пациентов, честно говоря, всегда мотивируют лучше всего.
Сейчас у нас есть пациентка, 48 лет, с рецидивирующей глиобластомой (агрессивная опухоль мозга). К нам она попала после того, как прошла две линии терапии в государственном онкоцентре. Там все делали правильно, проводили лучевую терапию и назначали таргетный препарат, но опухоль все равно вернулась. Женщине отвели полгода жизни.
Мы предложили ей полное молекулярно-генетическое тестирование. Да, оно стоит 600 тыс. рублей, сокращенный вариант, за 250, в ее случае не подошел – нужно было расширенное тестирование, с максимально полным набором мутаций.
Но по результатам обследования назначили ей препарат, который предназначен обычно для лечения немелкоклеточного рака легкого. Он эффективен против опухолей с мутацией EGRF – у нашей пациентки глиобластома была именно с этой мутацией.
Женщина ходит к нам лечиться и наблюдаться уже 4 года. Это в 5 раз дольше, чем при стандартной терапии. Причем, она самостоятельна, живет эти 4 года обычной жизнью, ходит на работу и собирается дождаться внуков.

Мутация EGFR
Эта мутация встречается преимущественно у некурящих людей. Обнаружение такой мутации на поздних стадиях рака представляет собой обнадеживающий признак, поскольку предполагает восприимчивость к лечению ингибиторами тирозинкиназы (препараты эрлотиниб и гефитиниб).
Транслокации ALK
По данным исследований, эта мутация при раке легкого более характерна у молодых и некурящих пациентов. Её обнаружение говорит о чувствительности к кризотинибу.
Мутация KRAS
Обычно данная мутация при лаке легкого встречается у курильщиков. Особой роли для прогноза не играет. При анализе статистических данных указано – встречались и случаи ухудшения состояния, и улучшения, что не позволяет сделать однозначный вывод о её влиянии.
Транслокация ROS1
Эта мутация, подобно транслокации ALK, преимущественно встречается у молодых, некурящих пациентов. В ходе клинических испытаний установлена высокая чувствительность таких опухолей к лечению кризотинибом, сейчас ведутся исследования препаратов нового поколения.
Мутация HER2
Обычно изменения представлены точечными мутациями. Опухолевые клетки в своей жизнедеятельности не зависят критическим образом от этой мутации, однако по результатам новых испытаний выявлен частичный положительный эффект у пациентов с комбинированным лечением посредством трастузумаба и цитостатических средств.
Мутация BRAF
Некоторые больные с мутациями этого гена (вариант V600E) поддаются лечению дабрафенибом, ингибитора белка B-RAF, кодируемого геном BRAF.
Мутация МЕТ
Ген МЕТ кодирует тирозинкиназный рецептор фактора роста гепатоцитов. Встречается увеличение числа копий этого гена (амплификация), при этом сам ген редко подвергается мутациям, и их роль изучена недостаточно.
Амплификация FGFR1
С данной амплификацией сталкиваются 13-26% пациентов с плоскоклеточным раком легких. Обычно распространена среди курящих пациентов, на практике предполагает неблагоприятный прогноз. Однако ведется соответствующая работа по разработке препаратов, направленных на это нарушение.
Основные принципы диагностики мутаций рака легкого
Чтобы точно диагностировать рак легких, предусмотрена бронхоскопия с забором биоптата для проведения цитологического и гистологического исследований. После того как из лаборатории поступит заключение о наличии мутации и выявленном типе мутации, будет составляться подходящая тактика медикаментозного лечения, назначаются соответствующие биологические препараты.
Биологическая терапия при злокачественных опухолях легких
Каждая программа терапии индивидуальна. Биологическая терапия предполагает работу с двумя типами лекарств, которые различаются по принципу воздействия на опухоль, но направлены на одинаковый окончательный эффект. Их цель – блокирование мутации клеток на молекулярном уровне, без вредного последствия для здоровых клеток.
За счет стабильного целевого действия исключительно на клетки опухоли удается приостановить рост злокачественных клеток уже спустя несколько недель. Чтобы поддержать достигнутый эффект, требуется продолжение курса приема препаратов. Лечение с помощью препаратов практически не сопровождается побочными эффектами. Но постепенно возникает невосприимчивость клеток к действующим компонентам лекарств, поэтому нужно корректировать лечение по мере необходимости.
Различия в лечении мутаций рака легкого
На долю мутации гена EFGR приходятся порядка 15% всех случаев. В таком случае для лечения может использоваться один из ингибиторов EGFR: эрлотиниб (Тарцева) или гефитиниб (Иресса); созданы и более активные препараты нового поколения. Данные лекарства обычно не вызывают тяжелых побочных эффектов, выпущены в форме капсул либо таблеток.
Транслокация генов ALK/EML4, на долю которой приходятся 4-7% всех случаев, предполагает назначение кризотиниба (Ксалкори); разрабатываются его более активные аналоги.
При опухолевом ангиогенезе для его подавления предполагается терапия с препаратом бевацизумаб (Авастин). Назначается препарат вместе с химиотерапией, значительно повышая эффективность данного лечения.

Что же заставляет живые клетки позабыть об эгоизме и работать на благо всего организма? Это свойство закодировано в их генетическом коде. Существуют определенные молекулы, белки, которые регулируют клеточную жизнь.
Одна из таких молекул — рецептор эпидермального фактора роста, по-английски — epidermal growth factor receptor, сокращенно — EGFR. Еще его обозначают как ErbB-1 и HER1. За открытие этой молекулы в 1986 году получили Нобелевскую премию два ученых — американский биохимик Стэнли Коэн и итальянский биолог Рита Леви-Монтальчини.
Какие функции в организме выполняет рецептор эпидермального фактора роста?
Когда сигнальная молекула (например, эпидермальный фактор роста) достигает клетки и взаимодействует с EGFR, этот белок активируется и запускает внутри клетки каскад биохимических реакций. В итоге клетка начинает размножаться.
Мутации EGFR и рак
Мутации гена EGFR определяются при разных типах рака, включая злокачественные опухоли легких, головы и шеи, толстой кишки, поджелудочной, молочной железы, яичников, мочевого пузыря, почек и др.
Из-за повышенной активности рецептора эпидермального фактора роста опухолевые клетки быстрее размножаются, агрессивнее вторгаются в окружающие ткани, метастазируют. Усиливается ангиогенез — образование новых кровеносных сосудов, питающих опухоль.
В общем наличие мутации EGFR в опухолевых клетках ухудшает прогноз для пациента.
Когда ученые поняли, что рецептор эпидермального фактора роста играет роль в развитии рака, возникла идея создать лекарственные препараты, которые могли бы блокировать этот белок. И сегодня такие препараты существуют.
Но нужно понимать, что молекулярно-генетические характеристики и гистологический тип рака — разные и не всегда связанные между собой вещи. Если взять две одинаковые злокачественные опухоли легких, то в одной активность EGFR может быть повышена, а в другой нет. Рассматривая опухоль под микроскопом, нельзя сказать, есть ли в ней такие мутации, будут ли в данном случае эффективен препараты из группы блокаторов EGFR. Для этого нужны специальные анализы. И они тоже существуют.
Кому показан анализ на EGFR?
В настоящее время показанием к исследованию является немелкоклеточный рак легкого (НМРЛ), в особенности если он представлен аденокарциномой (гистологический тип НМРЛ, который встречается в 40% случаев), в случаях, когда пациенту показано лечение ингибиторами EGFR. Это исследование помогает проверить, будет ли пациент реагировать на терапию.
- Ингибиторы EGFR эффективны у 80% больных, имеющих мутацию в гене рецептора эпидермального фактора роста. Причем, у некоторых из этих пациентов препараты действуют довольно сильно и в течение длительного времени.
- При отсутствии данных мутаций ингибиторы EGFR эффективны лишь у 10% пациентов.
Ингибиторы EGFR помогают в течение некоторого времени, в среднем 8 месяцев. Затем развивается резистентность: в злокачественной опухоли происходят новые мутации, и она перестает реагировать на лечение. В этом случае врач может назначить повторный анализ. Для этого нужно снова взять образец опухоли и отправить в лабораторию.
Не все мутации в гене EGFR делают рак чувствительным к ингибиторам рецептора эпидермального фактора роста. Некоторые, напротив, вызывают резистентность. Одна из таких мутаций обозначается как T790M. Если она обнаружена, применяют препарат, который эффективен в таких случаях — осимертиниб. Именно из-за мутации T790M злокачественные опухоли чаще всего (в 60% случаев) перестают реагировать на ингибиторы EGFR.
Анализ на мутации в гене EGFR может быть выполнен как отдельно, так и в составе панели, которая также включает исследования других мутаций — в частности, в генах KRAS, ALK, ROS1, BRAF. Это поможет врачу подобрать оптимальную терапию.
Избыточная активность гена рецептора эпидермального фактора роста, как мы упомянули, встречается и при других типах рака. Но на данный момент анализ рекомендован только при немелкоклеточном раке легкого.
Методы определения статуса мутаций EGFR
Для того чтобы провести анализ на мутации в гене EGFR, нужно провести биопсию — получить образец опухолевой ткани. При этом образец должен быть достаточно большого размера и содержать достаточное количество опухолевых клеток. Поэтому важно, чтобы забор материала проводил опытный врач, который хорошо владеет этим навыком.
Для того чтобы обнаружить мутантный ген EGFR, обычно применяют полимеразную цепную реакцию (ПЦР): метод предполагает создание множества копий ДНК с помощью ферментов.
Когда анализ завершен, лаборатория выдает одно из двух заключений:
- Результат положительный: обнаружена мутация в гене EGFR, при этом указывают, какая именно.
- Результат отрицательный: мутация не обнаружена.
На основе этих данных врач (онколог, химиотерапевт) определяется с дальнейшей тактикой лечения.
Методы лечения: ингибиторы EGFR и их эффективность
Ингибиторы EGFR относятся к группе таргетных препаратов. В отличие от классических химиопрепаратов, они действуют прицельно, на определенную молекулу, а не поражают все подряд быстро размножающиеся клетки.
Для лечения рака легкого применяют такие ингибиторы EGFR, как гефитиниб (Иресса), эрлотиниб (Тарцева), афатиниб (Гиотриф), бригатиниб (Алунбриг), икотиниб (Конмана). При раке толстой кишки применяют цетуксимаб (Эрбитукс), панитумумаб (Вектибикс).
Ингибиторы EGFR имеют разную химическую структуру, разные механизмы действия, и в зависимости от этого их можно разделить на две большие группы:
При раке легкого ингибиторы EGFR чаще всего используют на поздних стадиях, отдельно или в сочетании с химиопрепаратами.
Таргетные препараты действуют более прицельно по сравнению с классическими химиопрепаратами, тем не менее, они могут приводить к некоторым побочным эффектам. При применении ингибиторов EGFR чаще всего возникают такие проблемы, как сыпь и инфекции кожи, диарея, потеря аппетита. Более серьезные побочные эффекты встречаются редко.
Гефитиниб — таргетный препарат из группы ингибиторов EGFR для лечения немелкоклеточного рака легких в случаях, когда опухоль проросла в окружающие ткани, либо имеются отдаленные метастазы. В 2002 году он был одобрен в Японии, в 2003 году — в США. На данный момент гефитиниб продается более чем в 60 странах мира.
Препарат принимают в виде таблеток, по одной в день. Доказано, что в более высоких дозах гефитиниб не действует более эффективно, но возрастает риск побочных эффектов.
Чем доказана эффективность гефитиниба?
В 2009 году завершилась третья фаза клинического исследования, в котором участвовали пациенты с запущенной аденокарциномой легкого из Восточной Азии. Испытуемых поделили на три группы. В первой группе лечение проводилось гефитинибом, в двух других — химиопрепаратами карбоплатином и паклитакселом. В подгруппе пациентов, имеющих мутацию гена EGFR, эффективность гефитиниба оказалась значительно выше.
В Европейской клинике применяются все таргетные препараты, зарегистрированные на территории России, и у нас есть возможность провести молекулярно-генетические исследования, которые помогут выявить мутации и подобрать оптимальную терапию. Свяжитесь с нами, мы знаем, как помочь.
Читайте также:

