Наука о раковых клетках
Раковые клетки являются аномальными клетками, которые быстро размножаются, сохраняя способность к репликации и росту. Этот неконтролируемый рост клеток приводит к развитию масс ткани или опухолей. Опухоли продолжают расти, а некоторые, известные как злокачественные опухоли, способны распространяться из одного места в другое.
Раковые клетки отличаются от нормальных клеток числом или распространением в организме. Они не испытывают биологического старения, сохраняют свою способность делиться и не реагируют на сигналы саморазрушения. Ниже приведены 10 интересных фактов о раковых клетках, которые могут вас удивить.
1. Существует более 100 видов рака
Существует много разных видов рака, и эти опухолевые образования могут развиваться в различных типах клеток. Виды рака обычно называются в честь органов, тканей или клеток, в которых они развиваются. Наиболее распространенным типом онкологии является карцинома или рак кожи.
Карциномы развиваются в эпителиальной ткани, которая покрывает внешнюю поверхность тела и органов, сосудов и полостей. Саркомы образуются в мышцах, костях и мягких соединительных тканях, включая жировые, кровеносные сосуды, лимфатические сосуды, сухожилия и связки. Лейкемия - это рак, возникающий в клетках костного мозга, которые образуют белые кровяные клетки. Лимфома развивается в лейкоцитах, называемых лимфоцитами. Этот тип рака влияет на В-клетки и Т-клетки.
2. Некоторые вирусы производят раковые клетки
Развитие раковых клеток может быть следствием ряда факторов, включая воздействие химических веществ, радиации, ультрафиолетового света и ошибок репликации хромосом. Кроме того, вирусы также способны вызывать онкологические заболевания, изменяя гены. По оценкам, раковые вирусы приводят к 15-20% всех видов онкологии.
Эти вирусы меняют клетки путем интеграции их генетического материала с ДНК клетки-хозяина. Вирусные гены регулируют развитие клеток, что дает клетке способность к аномальному новому росту. Вирус Эпштейна-Барра связан с лимфомой Беркитта, вирус гепатита В может вызвать рак печени, а вирусы папилломы человека могут вызывать рак шейки матки.
3. Около трети всех случаев рака можно предотвратить
По данным Всемирной организации здравоохранения, около 30% всех случаев рака можно предотвратить. По оценкам, только 5-10% всех видов рака связано с наследственным дефектом гена. Остальные связаны с загрязнением окружающей среды, инфекциями и выбором образа жизни (курение, плохое питание и физическая бездеятельность). Единственным наиболее вероятным фактором риска развития рака во всем мире является курение и употребление табака. Около 70% случаев рака легких относятся к курению.
4. Раковые клетки жаждут сахара
Митохондрии опухолевых клеток обеспечивают энергию, необходимую для развития аномального роста, связанного с раковыми клетками. Митохондрии обеспечивают усиленный источник энергии, который также делает опухолевые клетки более устойчивыми к химиотерапии.
5. Раковые клетки спрятаны в теле
Раковые клетки могут избежать иммунной системы организма, скрываясь среди здоровых клеток. Например, некоторые опухоли выделяют белок, который также секретируется лимфатическими узлами. Белок позволяет опухоли трансформировать свой внешний слой в то, что напоминает лимфатическую ткань.
Эти опухоли проявляют себя как здоровая, а не раковая ткань. В результате иммунные клетки не обнаруживают опухоль как вредное образование, и позволяют ей неконтролируемо расти и распространяться в организме. Другие раковые клетки избегают химиотерапевтических препаратов, скрываясь в отделениях организма. Некоторые клетки лейкемии избегают лечения, прячась в кости.
6. Раковые клетки изменяют форму
Раковые клетки претерпевают изменения во избежание защиты иммунной системы, а также для защиты от радиации и химиотерапии. Раковые эпителиальные клетки, например, могут походить на здоровые клетки с определенными формами, напоминающими свободную соединительную ткань.
Способность изменять форму объясняется инактивацией молекулярных переключателей, называемых микроРНК. Эти небольшие регуляторные молекулы РНК обладают способностью регулировать экспрессию генов. Когда некоторые микроРНК становятся инактивированными, опухолевые клетки приобретают способность изменять форму.
7. Раковые клетки делятся бесконтрольно
Раковые клетки могут иметь мутации генов или хромосом, которые влияют на репродуктивные свойства клеток. Нормальная клетка, делящаяся через митоз, продуцирует две дочерние клетки. Опухолевые клетки, однако, способны делиться на три или более дочерних клеток. Недавно развитые раковые клетки могут быть, как с дополнительными хромосомами, так и вообще без них. Большинство злокачественных опухолей имеют клетки, которые потеряли хромосомы при делении.
8. Раковые клетки нуждаются в сосудах крови для выживания
Одним из контрольных признаков рака является быстрое образование новых кровеносных сосудов, известное как ангиогенез. Опухолям нужны питательные вещества для роста, обеспечиваемые кровеносными сосудами. Эндотелий сосудов крови ответственен как за нормальный ангиогенез, так и за ангиогенез опухоли. Раковые клетки посылают сигналы соседним здоровым клеткам, влияя на них, чтобы образовать кровеносные сосудов, которые будут снабжать опухоль. Исследования показали, что при предотвращении образования новых кровеносных сосудов опухоли перестают расти.
9. Раковые клетки могут распространяться из одной области в другую
Раковые клетки могут метастазировать или распространяться из одного места в другое через кровоток или лимфатическую систему. Они активируют рецепторы в кровеносных сосудах, позволяющие им выйти из кровообращения и распространиться на ткани и органы. Раковые клетки выделяют химические вещества, называемые хемокинами, которые индуцируют иммунный ответ и позволяют им проходить через кровеносные сосуды в окружающие ткани.
10. Раковые клетки избегают запрограммированной гибели клеток
Когда нормальные клетки испытывают повреждение ДНК, высвобождаются белки супрессоров опухолей, вызывающие клеточную реакцию, называемую запрограммированной гибелью клеток или апоптозом. Из-за мутации гена опухолевые клетки теряют способность обнаруживать повреждение ДНК и, следовательно, способность к самоуничтожению.
- Чем раковые клетки отличаются от нормальных?
- Каковы причины появления раковых клеток?
- Какие бывают типы генов рака?
- Основные характеристики и строение раковых клеток
- Как выглядят раковые клетки под микроскопом?
- Как развиваются раковые клетки, какие этапы проходят в своем развитии?
- Ликвидация раковых клеток: что помогает их уничтожить?

Чем раковые клетки отличаются от нормальных?
Для того чтобы организм человека правильно работал как единое целое, каждая клетка в нем должна подчиняться общим правилам и обладать некоторыми основополагающими свойствами:
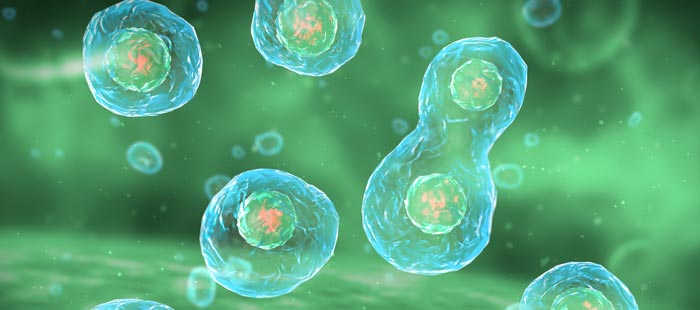
Не перестает размножаться. Сколько бы своих копий ни создала опухолевая клетка, она не останавится. Злокачественная опухоль постоянно растет и распространяется в организме.
Не специализируются. Раковая клетка не становится специализированной и не выполняет полезные для организма функции. Процесс клеточной специализации называется дифференцировкой. Чем ниже степень дифференцировки, тем агрессивнее ведет себя рак.
Каковы причины появления раковых клеток?
Почему в теле конкретного человека возникли раковые клетки — вопрос во многом риторический.
Каждая живая клетка функционирует и размножается в соответствии с заложенной в ней генетической информацией. При возникновении определенных мутаций эти тонкие механизмы регуляции сбиваются, и может произойти злокачественное перерождение.
Сложно сказать, что именно привело к таким мутациям в каждом конкретном случае. Современным врачам и ученым известны лишь факторы риска, которые повышают вероятность злокачественного перерождения и развития заболевания. Вот основные из них:
- Неблагоприятная экологическая ситуация.
- Курение.
- Чрезмерное употребление алкоголя.
- Профессиональные вредности, контакт с канцерогенными веществами и различными излучениями на производстве.
- Ожирение, избыточная масса тела.
- Ультрафиолетовое излучение солнца и соляриев.
- Малоподвижный образ жизни.
- Возраст: со временем мутации накапливаются, поэтому вероятность возникновения в организме раковых клеток повышена у пожилых людей.
- Нездоровое питание: преобладание в рационе животных жиров, красного и обработанного мяса.
Ни один из этих факторов не приводит со стопроцентной вероятностью к развитию злокачественной опухоли.
Какие бывают типы генов рака?
Не все мутации одинаково опасны. К раку приводят те, которые возникают в определенных генах:
Онкогены активируют размножение клеток. Злокачественное перерождение происходит, когда они становятся слишком активны. В качестве примера можно привести ген, который кодирует белок HER2. Этот белок-рецептор находится на поверхности клетки и заставляет ее размножаться.
Мутации, которые приводят к раку, могут быть наследственными (возникают в половых клетках) и соматическими (возникают в клетках тела в течение жизни).

Основные характеристики и строение раковых клеток
Раковые клетки обладают тремя основополагающими характеристиками, за счет которых так опасны онкологические заболевания:
- Способность к бесконтрольному размножению.
- Способность к инвазии — прорастанию в окружающие ткани.
- Способность к метастазированию — распространению в организме и образованию новых очагов в различных органах.
Не всякая опухолевая клетка — раковая. Раком или карциномой называют злокачественные опухоли из эпителиальной ткани, которая выстилает кожу, слизистые оболочки внутренних органов, образует железы. Из соединительной ткани (костной, жировой, мышечной, хрящевой, кровеносных сосудов) развиваются саркомы. Злокачественные заболевания органов кроветворения называют лейкозами. Опухоли из клеток иммунной системы — лимфомы и миеломы.
Как выглядят раковые клетки под микроскопом?
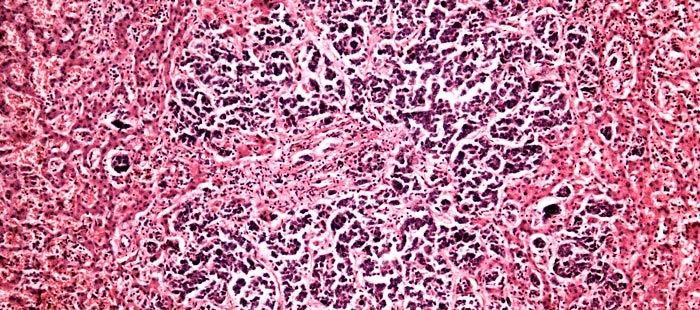
Если коротко, то они сильно отличаются от нормальных, тех, что ожидает увидеть патологоанатом, когда рассматривает под микроскопом фрагмент ткани. Раковые клетки имеют более крупные или мелкие размеры, неправильную форму, аномальное ядро. Если нормальные клетки в одной ткани все примерно одинаковых размеров, то раковые зачастую разные. Ядро содержит очень много ДНК, поэтому оно крупнее (его размеры тоже вариабельны), а при окрашивании специальными веществами выглядит более темным.
Из нормальных клеток образуются определенные структуры, например, железы. Раковые клетки располагаются более хаотично. Например, они образуют железы искаженной, неправильной формы или непонятные массы, которые на железы совсем не похожи.
Как развиваются раковые клетки, какие этапы проходят в своем развитии?
Раковые опухоли растут за счет деления клеток, которые входят в их состав. Во время деления злокачественная клетка образует две своих копии, таким образом, рост происходит в геометрической прогрессии. Например, для того чтобы образовалась опухоль размером 1 см, нужно около 30 удвоений. Через 40 удвоений новообразование достигает веса 1 кг, и этот размер считается критическим, смертельным для пациента.
Согласно современным представлениям, за рост злокачественной опухоли отвечают так называемые стволовые опухолевые клетки. Они активно делятся, в то время как другие опухолевые клетки просто существуют. Современные ученые заняты поиском методов лечения, направленных против этих стволовых клеток.
Время удвоения опухолевых клеток бывает разным. Например, при лейкозе это происходит за 4 дня, а при раковых новообразованиях толстой кишки — за 2 года. Проходит много времени, прежде чем опухоль достигнет настолько больших размеров, что станет проявляться какими-либо симптомами. Например, если у онкологического больного появились некоторые жалобы, и после этого он прожил год, вероятно, опухоль в его организме на момент появления жалоб существовала уже около трех лет, просто он об этом не знал.
Пока раковая опухоль небольшая, ей вполне хватает кислорода. Но по мере роста она все сильнее испытывает кислородное голодание — гипоксию. Чтобы обеспечить свои потребности, опухолевые клетки вырабатывают вещества, которые стимулируют образование кровеносных сосудов — ангиогенез.
По мере роста опухоли происходит инвазия — распространение раковых клеток в окружающие ткани. Они вырабатывают ферменты, которые разрушают нормальные клетки.
Некоторые из них отрываются от материнской опухоли, проникают в кровеносные и лимфатические сосуды, образуют в них вторичные очаги — метастазы. В этом самая главная опасность злокачественных опухолей. Именно метастатические очаги становятся причиной гибели многих онкологических пациентов.
Ликвидация раковых клеток: что помогает их уничтожить?
С раковыми клетками можно бороться разными способами. Например, удалить их из организма хирургическим путем. Но это возможно лишь в случаях, если опухоль не успела сильно распространиться в организме. Даже если можно выполнить радикальную операцию, никогда нет стопроцентной гарантии того, что в организме не остались микроскопические опухолевые очаги, которые в будущем станут причиной рецидива. Поэтому зачастую хирургические вмешательства дополняют адъювантной и неоадьювантной терапией.
Другие методы лечения:
В Европейской клинике применяются наиболее современные оригинальные препараты для борьбы с раком. У нас есть возможность провести молекулярно-генетический анализ опухолевой ткани, разобраться, из-за каких мутаций клетки стали злокачественными, и назначить наиболее эффективную персонализированную терапию. Свяжитесь с нами, мы знаем, как помочь.

Генетическая природа
За более чем 100 лет было доказано, что повреждение генов вызывает перерождение (трансформацию) нормальных клеток человеческого организма в злокачественные, определено, какие именно гены участвуют в этом процессе, открыты наследственные формы рака. Поочередное присоединение мутаций, приводящих к злокачественному перерождению клетки, называют канцерогенезом. И ключевым моментом для новых методов профилактики и терапии онкозаболеваний является именно раскрытие этих механизмов. На сегодняшний день специалисты в области онкологии рассматривают рак как болезнь, вызванную нарушениями в генетическом аппарате клетки, из-за которых она приобретает ряд способностей, приводящих к злокачественной трансформации.

Из-за большого количества происходящих подряд делений опухолевой клетке нужно большое количество энергетических ресурсов и строительных материалов. Ускоренный обмен веществ — это четвертая способность опухолевых клеток. При этом для получения необходимых ей веществ, опухолевая клетка начинает выделять в пространство вокруг себя молекулы, способствующие росту сосудов вокруг опухоли.

Кроме этого, бесконечное деление не дает клетке развиваться и проходить специализацию (функции клетки — прим.ред.). Она оказывается неспособной выполнять какую-либо функцию и поддерживать контакты с другими клетками, из-за чего приобретает способность к инвазии (проникновению вглубь — прим.ред.) и метастазированию.
Своевременное определение
В процесс канцерогенеза вовлечены два класса генов: протоонкогены, мутации в которых превращают их в онкогены, и гены-супрессоры, подавляющие рост опухолевых клеток. В настоящее время известно более 100 онкогенов и онко-супрессоров. Мутации в них могут не только возникать в отдельной клетке организма, но и наследоваться. В этом случае мы говорим о наличии у пациента наследственной предрасположенности к развитию той или иной опухоли. Выявлять таких людей крайне важно. С учетом их генетических особенностей и высоких рисков заболеть раком пока еще здоровым людям можно предложить специальную программу профилактики и наблюдения, которая позволит снизить риски развития злокачественных новообразований или выявить их на ранних стадиях, когда лечение максимально эффективно.
Если у человека уже выявлена опухоль, то, во-первых, необходимо проводить лечение с учетом наследственной природы заболевания, во-вторых, рассчитать риск развития других опухолей. Унаследованная мутация затрагивает все клетки организма человека, а это значит, что опухоль может возникнуть не только в одном органе. Кроме того, человек рискует передать мутацию, унаследованную от родителей, своим детям.
— Пётр Михайлович, не могли бы вы рассказать, в чём заключается суть вашего метода?
— Есть вирусы, которые могут подавлять рак. Они обладают онколитическими свойствами. И они безвредны для здоровья человека. Этот способ лечения практически не даёт побочных эффектов. Возможно только кратковременное повышение температуры, что является положительным признаком, говорящим о том, что вирус в организме прижился и оказывает реакцию. Это легко снимается обычными жаропонижающими средствами.
— Когда метод станет широко применяться в практической медицине?
— Сейчас основная наша задача — сертифицировать те препараты, которые у нас есть. Эта работа поддерживается Минздравом и Минобрнауки. У нас есть несколько грантов, по которым мы испытываем эти препараты. Мы делаем новые варианты онколитических вирусов с усиленными свойствами. Скоро должны начаться доклинические испытания в институте имени Смородинцева в Санкт-Петербурге. Мы уже передали туда препараты. Врачи говорят, что на испытания уйдёт месяцев пять-шесть. Учитывая ситуацию с коронавирусом, я думаю, что в начале 2021 года испытания могут быть закончены и тогда мы уже сможем договариваться с клиниками о проведении клинических испытаний.
— Что собой представляет препарат, который должен пройти испытания?
— Препарат — это живой вирус, который выращивается на культурах клеток. Это лекарство нового типа, которого не нужно много. Важно, чтобы он попал в организме в те клетки, которые чувствительны к нему. А дальше он сам размножается. То есть лекарство само себя воспроизводит уже в том месте, где оно нужно. Это раствор, 100 млн вирусных частиц в 1 мл. Но самая большая проблема в этом лечении — это способ доставки вируса в опухоль, в случае с глиобластомой — в мозг, в ту область, где находится опухоль.
Если препарат ввести просто внутривенно, то очень небольшая часть вируса может попасть в опухоль. В кровотоке есть неспецифические факторы, которые этот вирус быстро инактивируют. Кроме того, в мозгу есть гематоэнцефалический барьер, который препятствует попаданию туда всяких нежелательных агентов, в том числе и вирусов. Поэтому вирусу очень трудно добраться до опухоли.
— Как вы смогли решить эту проблему?
Эти клетки, как торпеды, идут в очаги воспалений, где находится опухоль. Там вирус выходит из них и начинает убивать опухолевые клетки. Этот метод мы уже отработали на нескольких пациентах. Есть хорошие примеры, когда на МРТ или КТ видно, как опухоль уменьшается и исчезает. Но это происходит не у всех.
— Почему же одни и те же вирусы не справляются с одними и теми же видами опухолей?
— Дело в том, что каждый конкретный вирус нашей панели действует только на 15—20% пациентов. Остальные оказываются к вирусу устойчивы. Однако у нас есть много разных вирусов, и мы можем подобрать свой для любого пациента. Но для этого нужно иметь живые клетки пациента.
Сейчас мы разрабатываем такие тесты, которые могут по обычной биопсии быстро показать, к какому вирусу опухоль будет чувствительна. Это очень сложная работа. Возможно, в будущем специальные клинические лаборатории будут получать от пациентов все необходимые материалы и в режиме конвейера проводить тестирование, подбирать препараты и далее — лечение.
Но сейчас к нам обращаются те, кому уже никто не может помочь. Некоторые из них лечатся у нас по полгода и более. Если идёт стабилизация и видно, что опухоль не растёт, мы делаем перерыв до тех пор, пока рост не возобновится. Но есть случаи, когда рост не возобновляется. У нас есть пациент, который живёт уже четыре года, притом что шансов у него не было. Глиобластома — это смертельное заболевание, средняя продолжительность жизни с ним — 12—15 месяцев с момента постановки диагноза.
— Прежде всего должен сказать, что пока это экспериментальное лечение. Когда Макаров доложил об этом методе на совещании у президента, мне кажется, он не рассчитывал на то, что это вызовет такой резонанс. Сейчас меня буквально атакуют письмами десятки больных с просьбой помочь.
Мне кажется, что не стоило рассказывать про Заворотнюк. Я знаю, что родные Анастасии долгое время вообще не комментировали её состояние и не хотели, чтобы в прессе поднимали этот вопрос. Сам я Анастасию ни разу не видел. Ко мне обращались её близкие с просьбой о помощи. Я сказал, что мы могли бы на первом этапе протестировать её клетки.
Дело в том, что во время операции были забраны живые клетки опухоли и переданы в один из институтов, где их удалось вывести в культуру клеток, чтобы они делились в пробирке. Мы взяли их и протестировали на чувствительность к нашим онколитическим вирусам, которые мы рассматриваем как средство лечения глиобластомы. Обнаружилось, что из 30 вирусов 7—8 вполне подходящие. И на этом этапе мы остановились, потому что муж Анастасии Пётр Чернышов сказал, что сейчас ситуация более-менее спокойная, если будет крайняя необходимость, они к нам обратятся. Это всё, что касается Заворотнюк.
Но всё это мы делали и делаем в очень ограниченном масштабе. Сейчас, когда всё выплеснулось в СМИ, мы просто не справимся с таким валом пациентов.
— Можете ли вы прокомментировать связь между ЭКО и появлением глиобластомы? Есть такие исследования?
— Как я понимаю, этот вопрос опять поднят историей Заворотнюк. В данном случае у неё было ЭКО. Но это никак не говорит о том, что есть какая-то связь. Во-первых, ЭКО не так много делают и глиобластомы — это 1% всех опухолей. Глиобластома встречается не только у женщин. Я думаю, что никакой связи нет. Ведь как может воздействовать ЭКО? Повышается уровень половых гормонов. Но тех гормонов, которые достаточно физиологичные, и так всегда есть в организме. Они просто появляются в другое время и в другой дозе. И вряд ли могут оказать влияние именно на глиальные клетки, с тем чтобы они переродились.
— В мире ведутся подобные исследования по лечению глиобластомы? Что вам известно об этом?
— Мы не первые, кто проверяет вирусы на глиобластоме. Сейчас это очень горячая тема во всём мире. И разные вирусы тестируют для лечения разной онкологии во многих странах. Я знаю один случай, который начали лечить в 1996 году вирусом болезни Ньюкасла, это птичий вирус. И больной до сих пор живёт с глиобластомой. Это опубликованные данные. И есть ещё несколько случаев лечения с помощью рекомбинантных вирусов герпеса.
В прошлом году вышла нашумевшая работа о том, что 20% больных глиобластомой могут быть вылечены вакциной рекомбинантного вируса полиомиелита.
Но нейрохирурги — люди консервативные. Они ни за что не согласятся даже в порядке эксперимента проводить такие опыты на людях. Потому что они очень сильно рискуют, если будет осложнение. Поэтому мы должны дождаться доклинических испытаний, с тем чтобы потом убедить их опробовать схему с прямым введением вируса прямо в опухоль.
— А кто и когда впервые заметил действие вируса на раковые клетки?
— Ещё в начале ХХ века учёные заметили, что опухолевые клетки особенно хорошо размножают вирусы. После инфекционных вирусных заболеваний у некоторых больных при разных видах рака наблюдались ремиссии. И уже тогда возникла мысль о том, что в будущем можно будет лечить онкобольных с помощью вирусов.
В 1950-е годы в Америке проводились эксперименты по лечению рака безнадёжных больных с помощью патогенных вирусов. Считалось, что это меньшее зло по сравнению с самим раком. И тогда были получены положительные результаты. Но поскольку многие больные умирали от инфекционных заболеваний, возник очень большой резонанс. Врачи, которые начали это делать, дискредитировали всю эту область на долгие годы. Были введены дополнительные этические правила. Само упоминание о том, что вирусом можно лечить рак, стало табу.
В 1990-е годы уже стало понятно, как устроены вирусы, структура их генома. Учёные научились вносить изменения в геном вирусов, чтобы сделать их безвредными. И тогда во всём мире начался бум разработки препаратов на основе вирусов для лечения рака. Но тут новая беда. Этому стали сопротивляться фармацевтические компании. Потому что это совершенно другой способ лечения, который подрывает базу их благосостояния.
В начале 10-х годов нашего века многие небольшие компании разрабатывали препараты, которые потом проходили какие-то клинические испытания, были показаны какие-то многообещающие свойства. Но фармацевтические компании скупали эти разработки и практически прекращали деятельность этих небольших стартапов.
— Удалось ли кому-нибудь преодолеть фармацевтическое лобби и зарегистрировать препарат?
— Сейчас в мире зарегистрировано три препарата онколитических вирусов. Один препарат разрешён к использованию в США для лечения злокачественных меланом. Ещё один рекомбинантный аденовирус — в Китае, и один энтеровирус — в Латвии. Но, в общем-то, каждый из этих препаратов находит пока очень ограниченное применение, из-за того что все они действуют только на часть пациентов.
— Пётр Михайлович, а как давно вы ведёте свои исследования?
— Всю жизнь, ещё с 1970-х годов. Мне выпало такое время, когда мы вначале практически ничего не знали о вирусах. И по мере того, как мы что-то узнавали, мы вносили какой-то вклад в эту науку и сами учились. И я начинал как раз с вирусов. Потом переключился на проблему рака — фундаментальные механизмы деления клеток: как нормальная клетка превращается в рак. А потом снова вернулся в вирусологию.
Должен сказать, что и мои родители были вирусологами, они занимались противополиомиелитной кампанией. Моя мать в 1970-е годы изучала, как у детей образуются антитела к полиомиелитной вакцине, и она обнаружила, что у многих детей не образуются антитела. Оказалось, что в кишечнике у детей в это время шла бессимптомная инфекция другого безвредного энтеровируса. И он вызывал неспецифическую защиту от вируса полиомиелита. Поэтому вакцинный полиовирус не мог индуцировать антитела у этих детей. Эти безвредные вирусы были выделены из кишечника здоровых детей. И на их основе были созданы живые энтеровирусные вакцины, которые испытывались для того, чтобы предотвращать какие-то ещё неизвестные инфекции.
И вот мы решили возобновить тот подход, который был предложен моей мамой, когда используется панель энтеровирусов. Оказалось, что те больные, которые нечувствительны к одному вирусу, могут быть чувствительны к другому. Возникла идея подбора вируса под пациента. Мы разработали целую панель собственных вирусов, которые могут также обладать усиленными свойствами. Мы продолжаем эту разработку.
— Ваши вирусы могут побеждать рак. А есть вирусы, которые вызывают развитие опухоли?
— Да. Например, рак шейки матки в 95% случаев вызывается вирусом папилломы. Сейчас уже есть даже вакцины против онкогенных папилломовирусов 16—18-го серотипа, которые применяются для девочек, чтобы не заболевали раком шейки матки. Но это самый большой пример. У большинства видов рака сейчас можно полностью исключить вирусную природу.
— Вы используете естественные вирусы или конструируете их?
— У нас разные есть вирусы. Как я говорил, первая панель была выделена из кишечника здоровых детей. Это природные непатогенные вирусы, которые, кстати говоря, хорошо защищают детей от многих вирусных инфекций. Кроме того, мы делаем синтетические и рекомбинантные вирусы, когда мы вводим определённые изменения в их состав, которые усиливают их онколитические свойства.
— На планете есть ещё места, где может быть очень много вирусов, о которых мы ещё и понятия не имеем. Например, те, что живут в океанских глубинах. Как вы считаете, если вдруг кто-то возьмётся за изучение океана именно с точки зрения вирусов, там могут найтись полезные для вас?
— Да, и сейчас это тоже очень горячая тема. Когда разработали метод секвенирования геномов, ДНК, РНК, то возник соблазн: профильтровать сточные воды, океанические воды, из прудов, морей. Уже пробурили скважину в Антарктиде к древнему озеру, чтобы посмотреть, что там, выделить оттуда биологические компоненты и секвенировать их. И оказывается, что нас окружает огромное количество вирусов, которые абсолютно безвредны. И такое впечатление, что наше исходное представление о вирусах как о чём-то вредном и вызывающем только болезни неверно. Болезнетворный вирус — скорее исключение, чем правило.
- Культура
- История
- Религия
- Спорт
- Россия глазами иностранцев
- Фото
- Инфографика
- ИноВидео
- ИноАудио
Раньше рак был смертным приговором. Сегодня семь из десяти пациентов живут не менее десяти лет после постановки диагноза. Журналист SvD встретился с самыми выдающимися исследователями в мире и спросил, насколько мы близко к решению загадки рака
Чудо, что я еще жив, говорит 76-летний Дьюи Стринджер (Dewey Stringer). Он разбогател на черном золоте в американском нефтяном городе Хьюстоне и вел такую жизнь, о какой другие могут только мечтать. Но пять лет назад жизнь ударила по тормозам. Даже деньги не могли его спасти.
Почку ему удалили, и врач местной частной больницы объявил, что операция прошла успешно. Но это было не так. Всего через несколько месяцев были обнаружены метастазы в других органах, прежде всего в легких.
Он похудел на десять килограммов, и даже любимое блюдо, классическая техасская говяжья вырезка, не вызывало у него аппетита. Теперь он по большей части сидел или дремал в теньке у себя в саду. Последние дни он планировал провести в хосписе, чтобы не обременять семью.
Долгое время любой онкологический диагноз означал именно это. Смертный приговор. До прорыва в виде лучевой терапии никто не мог и надеяться побороть такую болезнь. Единичным пациентам удавалось продлить жизнь с помощью хирургии и новейших возможностей в области наркоза. Но с лучевой терапией стало возможно исцелять онкологических больных или хотя бы облегчать их болевые ощущения.
В начале 1950-х годов, когда появилась химиотерапия, примерно 30% пациентов могли прожить еще несколько лет после постановки диагноза. Примерно в то же время ученые впервые связали курение с раком.
С тех пор развитие медицины шло семимильными шагами. Комбинированные схемы лечения и гормональная терапия стали действовать точнее. В 2000-е появилась прецизионные препараты и лекарства целевого действия. Они направлены точно на раковые клетки и не затрагивают здоровые.
Сегодня в области лечения онкологических заболеваний происходит много хорошего. Выживаемость растет, относительная смертность падает.
Мерилом успеха считается десятилетняя выживаемость, то есть количество пациентов, которые живут не менее десяти лет после постановки диагноза. В 1980 году этот показатель был около 30% для мужчин и чуть более 40% для женщин. Последние цифры шведского Государственного управления социальной защиты населения показывают рост до примерно 69% как для мужчин, так и для женщин. В среднем трое из четырех пациентов живут не менее пяти лет, после того как заболели.
Устойчивость рака поражала ученых во все времена. Но, может, скоро рак перестанет быть смертельной болезнью? Другими словами, мы вот-вот разгадаем его загадку?
Дьюи Стринджер услышал об этом совершенно случайно. Онкологический центр Андерсона в Хьюстоне, одна из крупнейших в мире онкологических больниц, которая принимает до 130 тысяч человек в год и проводит одновременно более сотни исследований, в которых задействованы 4 тысячи пациентов, испытывала так называемую иммунную терапию. В центре работал Джим Эллисон (Jim Allison), техасский иммунолог и один из двух разработчиков этого нового метода лечения.
Ему разрешили участвовать — за 60 тысяч долларов в месяц. Он уже был готов продать эксклюзивную виллу в Галвестоне, недалеко от Космического центра НАСА, где находится центр управления пилотируемыми космическими полетами.
Многие метастазы к тому времени выросли из горошин до размера виноградины. Оказались затронуты оба легких, Дьюи Стринджер совсем потерял аппетит и, по сути, уже умирал. После первой инъекции в августе 2015 года лучше ему не стало. Вторая и третья тоже не дали результатов.

В 2018 году, после нескольких лет споров, за иммунную терапию была присуждена Нобелевская премия по медицине. Ее разделили Джеймс Эллисон и Тасуко Хондзё из Японии. Не исключено, что по мере развития технологии этот прорыв станет революцией в лечении рака. Сейчас проводятся исследования применительно к разным типам онкологических заболеваний на поздних стадиях.
Он профессор Каролинского института (один из крупнейших в Европе медицинских университетов, находится в окрестностях Стокгольма — прим. ред.), а также член Нобелевского комитета в области физиологии и медицины и председатель Исследовательской комиссии Онкологического фонда Швеции.
Иммунная терапия применяет иммунную систему организма для борьбы с раком
Иммунная система состоит из органов, тканей, клеток и молекул. Одна из ее задач — избавляться от бактерий, вирусов и аномальных клеток, например, раковых. В иммунной терапии применяются разные техники, заставляющие иммунную систему более успешно находить и ликвидировать опухолевые клетки.
Варианты иммунной терапии
Ингибиторы контрольных точек иммунного ответа (чекпойнт-ингибиторы). Эти препараты блокируют сдерживающие механизмы иммунной защиты. Так называемые контрольные точки — естественная ее часть, и их задача — предотвращать слишком мощный иммунный ответ. Блокируя их, препарат помогает иммунным клеткам сильнее воздействовать на опухоль.
Моноклональные антитела. Это протеины иммунной системы, созданные в лабораторных условиях, они привязываются к конкретным точкам в опухолевых клетках. Моноклональные антитела помечают их, и таким образом иммунной системе проще их обнаруживать и уничтожать.
Открытие Джеймса Эллисона и Тасуко Хондзё помогает сдерживать эти механизмы. Другими словами, лечение усиливает естественную способность иммунной системы атаковать раковые клетки.
После нобелевских торжеств в 2018 году Эллисон неравнодушен к Швеции. На праздничные мероприятия он взял с собой друга — гитариста U2 Эджа. Помимо науки, для Эллисона всегда много значила музыка. Сам он играет на губной гармошке, часто ездит на гастроли с разными блюзовыми коллективами и биг-бэндом The CheckPoints и даже играл вместе с легендой кантри Уилли Нельсоном (Willie Nelson).
По чистой случайности именно в эти октябрьские дни становятся известны имена лауреатов премии по медицине 2019 года. Я спрашиваю, что эта премия значит для Эллисона.
В конце 1990-х годов лечение получил первый пациент-человек. У него был рак простаты. В 2001 году много внимания привлек к себе случай женщины с раком кожи на поздней стадии, когда метастазы уже были в мозгу, печени и обоих легких. Случай был безнадежный, иммунную терапию попробовали как последнее средство. Через четыре месяца почти все раковые клетки исчезли.
Но Джиму Эллисону все равно пришлось прыгать выше головы, чтобы убедить какую-нибудь фармацевтическую компанию вложить деньги в его исследование. В конце концов он нашел одну небольшую фирму в области биотехнологий. По его опыту, крупные фармацевтические предприятия чаще всего не заинтересованы в поддержке пациентов, которые обходятся дорого, а потом все равно умирают. Они предпочитают производить лекарства для людей с больным сердцем или диабетом, то есть для хронических больных, которые долго живут, а значит, успевают окупиться.
Его лекарство одобрили только в 2011 году.

В области лечения онкологических заболеваний ученые добиваются все более значительных результатов, но и людей, страдающих от рака, становится все больше.
Похоже, рак всегда был частью человеческой жизни. По мере того как растет продолжительность жизни, заболевают все больше людей: говорят даже, что каждый из нас умрет от рака, если только не успеет пасть жертвой какого-нибудь другого недуга. Недавно онкологические заболевания возглавили рейтинг самых распространенных причин смерти в Швеции.
Ежегодно примерно у 63 тысяч шведов находят рак. По сравнению с ситуацией 50 лет назад цифра практически удвоилась. По прогнозам, через 25 лет она достигнет 100 тысяч.
Вот еще одна интересная цифра: 340 тысяч. Столько человек в Швеции живут с онкологическими заболеваниями в настоящий момент. Через 25 лет в стране будет 600 тысяч граждан, когда-либо сталкивавшихся с таким диагнозом.
То, что рак встречается все чаще, связано прежде всего с ростом населения и увеличением продолжительности жизни. Чаще всего рак диагностируется в пожилом возрасте, обычно после 70 лет.
Согласно статистике, каждый год от рака умирают 23 тысячи человек — примерно столько же, сколько и 50 лет назад. Учитывая, что население увеличилось с 8 до 10 миллионов, можно сказать, что относительная смертность сократилась на 20%.
Большую роль играет и диагностика. Многие виды рака теперь обнаруживают раньше, иногда даже настолько рано, что опухоль еще совершенно безопасна, пусть ее и регистрируют как рак.
Агнес Вольд (Agnes Wold) — врач и профессор клинической бактериологии в Сальгренской академии при Гётеборгском университете. По ее мнению, статистика выживаемости смысла не имеет. Она дает искаженную картину того, скольким пациентам удается пережить рак.
Примечательно как раз то, что сейчас умирает столько же пациентов, сколько и 50 лет назад, считает она.
Клас Черре согласен, что доля малоопасных опухолей в статистике несколько ее приукрашивает.
Но смертность упала, и шансы выжить сегодня выше, чем 50 лет назад, подчеркивает он.
За четыре года Дьюи Стринджер получил в общей сложности 63 курса иммунной терапии. Они разогнали его собственную иммунную защиту, так что опухоли, эти агрессивные метастазы, которые в противном случае уже давно лишили бы его жизни, или существенно уменьшились, или вовсе исчезли.
Конечно, не обошлось без побочных эффектов. Он ходит в туалет по двадцать раз в день, все время чувствует усталость, его мучают раны и зуд.

Необычайно долгая жара в Хьюстоне идет на спад. Но когда мы располагаемся на скамейке в больничном дворе, температура в тени достигает 35 градусов. Дьюи Стринджер вызвал такси, но я успеваю задать ему последний вопрос: теперь-то он победил рак?
Джим Эллисон всегда бывает очень тронут, когда пациенты рассказывают, как иммунная терапия помогла им побороть рак. Это самая настоящая победа после всех препятствий и злобных нападок со стороны коллег, фармацевтических компаний и американского управления по санитарному надзору за качеством продуктов и медикаментов. Все считали, что он занимается ерундой, и это не наука, а вуду.
А еще рак не миновал и его близких. Джим Эллисон вырос в шахтерском городе Алисе в Техасе. Отец был семейным врачом. Мама умерла от рака легких, а брат рано ушел от меланомы. Второй брат скончался от рака простаты в 2011 — в том же году, когда было одобрено лекарство Джима Эллисона. Но у брата не было возможности получить лечение, которое, вероятно, спасло бы ему жизнь.
У самого Джима Эллисона тоже диагностировали рак простаты, и он выздоровел благодаря собственной иммунной терапии.
Насколько хороша иммунная терапия?
Однако иммунная терапия — это по-прежнему дорого, год такого лечения обойдется примерно в миллион в пересчете на шведские кроны. Медицинская страховка может его покрыть, но далеко не у всех в США есть средства на такую страховку.
Мы входим в большую лабораторию, где 70 человек трудятся, проводя исследования рака на мировом уровне. Джим Эллисон полагает, что следующим большим прорывом станет генная инженерия в комбинации с прочими методами.
Материалы ИноСМИ содержат оценки исключительно зарубежных СМИ и не отражают позицию редакции ИноСМИ.
Читайте также:

