Научные статьи о раке тела матки
ФАКТОРЫ ПРОГНОЗА У БОЛЬНЫХ РАКОМ ТЕЛА МАТКИ.
Прогноз при раке тела матки и выживаемость больных во многом зависят от стадии заболевания, определенной на основании интраоперационных находок и результатов гистологического исследования.
Не маловажное значение имеет и своевременность точного прогноза. Наиболее точная диагностика с визуализацией опухолей выполняется с помощью позитронно-эмиссионной томографии, совмещенной с компьютерной томографией.
Факторами неблагоприятного прогноза, статистически достоверно влияющими на отдаленные результаты лечения больных раком тела матки I-III клинических стадий, являются стадия, возраст, глубина инвазии миометрия, степень дифференцировки и размер опухоли, наличие опухолевых эмболов в кровеносных и лимфатических сосудах миометрия, опухолевых клеток в смывах из брюшной полости, дис-семинации и лимфогенных метастазов. Метастазы в лимфатических узлах - наиболее важный фактор прогноза при раке тела матки ранних стадий.
Результаты лечения опровергают традиционное представление о благоприятном клиническом течении рака тела матки (РТМ). Так, 5-летняя общая выживаемость больных РТМ I и II стадий составляет 82 и 65% соответственно, а прогрессирование возникает у 25% больных, лечившихся по поводу РТМ ранних стадий [5].рак матки
В мире РТМ занимает 4-е место в структуре заболеваемости женщин злокачественными новообразованиями и 7-е место в структуре смертности от них. РТМ чаще встречается у женщин в пре- и постменопаузе (75%), однако в последние годы отмечается тенденция омоложения больных РТМ. Значительные темпы прироста заболеваемости РТМ отмечаются в возрастных группах 40-49 (на 12,3%) и 50-56 лет (на 15,6%) [2].
Прогноз при РТМ и выживаемость больных во многом зависят от стадии рака тела маткия, определенной на основании интраоперационных находок и результатов гистологического исследования [3]. При этом учитываются глубина инвазии миометрия, состояние придатков и шейки матки, результаты ревизии брюшной полости и малого таза, биопсии всех подозрительных объемных образований и увеличенных тазовых и парааортальных лимфатических узлов [1]. Данные предоперационного обследования и установленная на этом основании клиническая стадия не совпадают с операционными находками и результатами гистологического исследования у 51% больных РТМ [4]. Таким образом, при РТМ оптимальным является определение морфологической стадии заболевания.
Риск метастазов РТМ в регионарных лимфатических узлах, а также прогрессирования болезни определяется в
Длительное время ведутся научные споры об объемах хирургических вмешательств при РТМ. Эта проблема имеет два аспекта: целесообразность расширения их объема с учетом особенностей лимфогенного метастази-рования и возможность выполнения расширенных операций у больных, обычно страдающих выраженными эн-докринно-обменными нарушениями и сопутствующими заболеваниями сердечно-сосудистой системы. Существуют разные методики визуальной и морфологической оценки состояния регионарных лимфатических узлов при РТМ: УЗИ, пальпация и биопсия увеличенных лимфатических узлов, биопсия одного увеличенного лимфатического узла, селективная и тотальная лимфаденэкто-мия. К сожалению, до сих пор нет единых рекомендаций FIGO по определению морфологической стадии РТМ.
С учетом изложенного целью проведенного исследования являлось изучение эффективности трех методик комбинированного лечения РТМ, выявление факторов прогноза и разработка научно обоснованных рекомендаций по выполнению расширенных операций при РТМ.
В исследование включены 395 больных РТМ IA- IIIC стадий в возрасте 30-89 лет, которым проведено лечение в ГУ РОНЦ им. Н. Н. Блохина РАМН с 1995 по 2005 г. Диагноз у всех пациенток установлен впервые на основании результатов гистологического исследования.
Средний возраст пациенток составил 60,4±0,5 года:
15 (3,8%) - в возрасте до 40 лет, 37 (9,4%) - в возрасте 40-49 лет, 143 (36,2%) - в возрасте 50-59 лет, 137 (34,7%) - в возрасте 60-69 лет, 63 (15,9%) - в возрасте 70 лет и старше. Таким образом, подавляющее большинство больных РТМ (343 больные, 86,8%) были в возрасте 50 лет и старше.
Все больные наблюдались от 1 до 10 лет. Пятилетняя общая выживаемость больных РТМ I-III стадий составила 75,9±2,6%, 10-летняя - 71,5±3,2%, 5-летняя безрецидивная выживаемость - 71,3±3,1%.
Стадия заболевания статистически достоверно связана с прогнозом больных РТМ (р = 0,00001). Так, при I стадии заболевания в течение 5 лет без признаков про-грессирования болезни наблюдались 81,3% пациенток. Десятилетняя выживаемость больных в этой группе составила 77,1±3,3%. При III стадии болезни 50% больных умерли от рецидивов и отдаленных метастазов в сроки до 42,5 мес, а 25% больных - в сроки до 20,8 мес. Не выявлено статистически достоверных различий в отдаленных результатах лечения больных РТМ IIA и IIB, IIIA, IIIB и IIIC стадий (p > 0,05). Пятилетняя общая выживаемость больных РТМ IIIA-IIIC стадий статистически достоверно ниже, чем больных РТМ IA-IC (p = 0,0001) и IIA-IIB (p = 0,01) стадий. Аналогичные результаты выявлены при изучении безрецидивной выживаемости больных РТМ. Так, 5-летняя безрецидивная выживаемость больных РТМ I стадии составила 80,5±2,1%, II стадии - 69,8±7,9%, III стадии - 41,9±11,3% (p = 0,00001). Медиана безрецидивного периода при РТМ III стадии составила 27,9 мес.
Пятилетняя общая выживаемость при РТМ T1N0M0 статистически достоверно выше, чем при РТМ T1N1M0 (81,3±2,8 и 30,9±17,9% соответственно, р = 0,001). В связи с небольшим количеством пациенток с опухолями Т2а-3bN1 сравнение результатов лечения в этой группе в зависимости от наличия лимфогенных метастазов не проводили. Однако следует отметить, что при наличии регионарных лимфогенных метастазов 5-летняя выживаемость больных была менее 50%. При опухолях Т3а 5-летняя выживаемость больных РТМ с метастазами и без таковых оказалась сопоставимой.
Статистически достоверные различия выявлены при изучении отдаленных результатов лечения больных РТМ разных возрастных групп. Установлено, что 5-летняя выживаемость больных старше 60 лет статистически достоверно ниже, чем в других возрастных группах (p 0,05). Пятилетняя безрецидивная выживаемость больных аденокарциномой эндометрия I-III стадий составила при высокой дифференцировке опухоли 91,4±3,8%, при умеренной - 70,1±5,4%, при низкой - 65,3±10,9%, при смешанной - 65,2±7,9% (р = 0,04).
При анализе 10-летней общей выживаемости в зависимости от глубины инвазии миометрия отмечено, что она была наибольшей при прорастании менее половины толщины миометрия (80,9±3,4%). Результаты лечения больных, у которых опухоль прорастала более половины толщины миометрия, и больных, у которых опухоль прорастала до серозной оболочки, оказались одинаковыми. Обе больные с прорастанием опухолью серозной оболочки матки умерли от прогрессирования заболевания через 9 и 10 мес. У 11 пациенток инвазии миометрия при гистологическом исследовании не выявлено. При этом метастазы в регионарных лимфатических узлах выявлены у 2 больных, а переход опухоли на шейку матки - у 1. В целом выживаемость в этой группе была низкой и составила 18,2±1,3%, что обусловлено сочетанием неблагоприятных факторов прогноза. Пятилетняя безрецидивная выживаемость больных РТМ в зависимости от глубины инвазии миометрия составила 81,3±2,9% при прорастании опухолью менее половины толщины миометрия и 62,8±5,9% при прорастании опухолью более половины толщины миометрия (р = 0,000001).
Отмечена тенденция к ухудшению отдаленных результатов лечения больных РТМ с переходом на строму шейки матки по сравнению с таковыми у больных с переходом опухоли на слизистую цервикального канала (5-летняя общая выживаемость 55,9±10,1 и 74,6±6,6% соответственно, р = 0,08). Пятилетняя безрецидивная выживаемость больных РТМ при переходе опухоли на слизистую шейки матки составила 71,3±9,3%, на стро-му - 52,1±19,8% (р = 0,061).
Статистически достоверно ухудшают отдаленные результаты лечения больных РТМ опухолевые эмболы в кровеносных и лимфатических сосудах миометрия (р = 0,035). Пятилетняя общая выживаемость больных РТМ в зависимости от наличия опухолевых эмболов различалась недостоверно, в то время как 10-летняя имела достоверные различия (р = 0,013). Пятилетняя безрецидивная выживаемость больных РТМ составила 59,3±9,4 и 75,7±3,3% соответственно (р = 0,049).
По результатам нашего исследования выявлена тенденция к снижению выживаемости больных РТМ с метастазами в яичниках. Пятилетняя безрецидивная выживаемость при наличии метастазов в яичниках составила 68,6±16,8%, в отсутствие метастазов - 81,8±2,5% (р = 0,35).
Регионарные лимфогенные метастазы, по нашим данным, являются одним из наиболее значимых факторов неблагоприятного прогноза, статистически достоверно влияющим на выживаемость больных. Четверть больных РТМ с метастазами в регионарных лимфатических узлах умерли от прогрессирования болезни в сроки до 20 мес, половина - в сроки до 44,5 мес. Пятилетняя общая выживаемость больных РТМ с метастазами в регионарных лимфатических узлах и без них составила 47,6±11,7 и 82,0±6,3% (р = 0,0018), 5-летняя безрецидивная выживаемость - 41,3±12,1 и 80,9±6,9% (р = 0,01), медиана безрецидивного периода - 30,8 мес.
Диссеминация по брюшине статистически достоверно снижает отдаленные результаты лечения больных РТМ (р = 0,00005). Четверть больных этой группы умерли от прогрессирования заболевания в сроки до 9,6 мес. Медиана продолжительности жизни больных этой группы составила всего 21,6 мес, тогда как в группе больных без диссеминации по брюшине не была достигнута. Пятилетняя общая выживаемость больных РТМ при наличии опухолевой диссеминации по брюшине и без нее составила 28,7±17,0 и 77,6±2,6% (р = 0,0025), 5-летняя безрецидивная выживаемость - 24,3±16,8 и 75,4±3,2% (р = 0,00016), медиана безрецидивного периода - 12,5 мес.
Выявлены статистически достоверные различия в выживаемости больных РТМ в зависимости от размеров первичной опухоли. При первичных опухолях более 4 см 5-летняя безрецидивная выживаемость больных составила 61,4±5,2%, при опухолях менее 4 см - 78,9±3,8% (р = 0,018).
Установлена тенденция улучшения 10-летней общей выживаемости больных с опухолями, содержащими рецепторы прогестерона, и ухудшения 5-летней общей выживаемости больных с опухолями, не содержащими рецепторы эстрогенов и прогестерона (р = 0,25). Пятилетняя безрецидивная выживаемость больных РТМ в зависимости от рецепторного статуса опухоли не различалась и составила в группе больных с рецептороотри-цательными опухолями 54,3±11,0%, с опухолями, содержащими только рецепторы прогестерона, - 69,8±12,6%, с опухолями, содержащими только рецепторы эстрогенов, - 65,4±12,9%, с рецептороположительными опухолями - 68,5±8,1%.
Проведенный анализ показал статистически достоверные различия в отдаленных результатах лечения больных РТМ в зависимости от наличия опухолевых клеток в смывах из брюшной полости (р = 0,0001). Так, в отсутствие опухолевых клеток в смывах медиана продолжительности жизни больных не достигнута, а при наличии опухолевых клеток составила 26,7 мес. Пятилетняя общая выживаемость оказалась равной 77,4±2,6 и 30,5±15,0% соответственно (р = 0,00001). Пятилетняя безрецидивная выживаемость больных РТМ составила в отсутствие опухолевых клеток в смывах 84,1±2,7%, при наличии опухолевых клеток в смывах - 26,5±15,7% (р = 0,00012), медиана безрецидивного периода - 19,7 мес.
Таким образом, факторами неблагоприятного прогноза, статистически достоверно влияющими на отдаленные результаты лечения больных РТМ I-III клинических стадий, являются стадия, возраст, глубина инвазии ми-ометрия, степень дифференцировки и размер опухоли, наличие опухолевых эмболов в кровеносных и лимфатических сосудах миометрия, опухолевых клеток в смывах из брюшной полости, диссеминации, лимфогенных метастазов.
Источник
Научная статья для специалистов
Вестник РОНЦ им. Н. Н. Блохина РАМН, т. 17, №3, 2006
А. В. Налбандян, В. В. Кузнецов, В. М. Нечушкина
НИИ клинической онкологии ГУ РОНЦ им. Н. Н. Блохина РАМН, Москва
ЛИТЕРАТУРА
1. Бохман Я. В. Руководство по онкогинекологии. - Л.: Медицина, 1989. - С. 275-340.
2. Трапезников Н. Н., Аксель Е. М. Статистика злокачественных новообразований в России и странах СНГ (состояние онкологической помощи, заболеваемость и смертность). - М., 2001. - 296 с.
3. Cohn D. E, Horowitz N. S, Mutch D. G. et al. Should the presence of lymphovascular space involvement be used to assign patients to adjuvant therapy following hysterectomy for unstaged endometrial cancer? // Gynecol. Oncol. - 2002. - Vol. 87. - P. 243-246.
4. Creasman W. T., Morrow C. P., Bundy B. N. Surgical pathologic spread patterns of endometrial cancer // Cancer. - 1987. - Vol. 60, N 8. - P. 2035-2041.
5. Lurain J. R. Uterine cancer / Berek J., Adashi E., Hillard P. (eds.). Novak‘s Gynecology. - 12th ed. - Baltimore: Williams & Wilkins, 1996. - P. 1057-1092.
6. Mizuuchi H., Nasim S., Kudo R. Clinical implications of K-ras mutations in malignant epithelial tumors of the endometrium // Cancer Res. - 1992. - Vol. 52, N 10. - P. 2777-2781.
Похожие темы научных работ по клинической медицине , автор научной работы — Нечушкина В. М., Кузнецов В. В., Лазарева Н. И., Морхов К. Ю.
СОВРЕМЕННЫЕ ПРЕДСТАВЛЕНИЯ О ЛЕЧЕНИИ РАКА ТЕЛА МАТКИ
В.М. Нечушкина, В.В. Кузнецов, Н.И. Лазарева, К.Ю. Морхов
ГУ РОНЦ им. Н.Н. Блохина РАМН, г. Москва
Рак тела матки (РТМ) занимает 1-е место по частоте среди опухолей женских половых органов в развитых странах и 2-е место (после рака шейки матки) в развивающихся. По данным ВОЗ и МАИР, Россия занимает 44-е место по заболеваемости РТМ и 26-е место по смертности от этой злокачественной опухоли в мире. По данным М.И. Давыдова и Е.М. Аксель, в 2004 г. РТМ занял 5-е место в структуре заболеваемости женщин злокачественными опухолями. Заболеваемость в 2004 г. составила 13,3 на 100 000 женщин. За 5 лет (с 1998 по 2003 г.) заболеваемость РТМ в России выросла на 6,4 %. В результате по приросту заболеваемости РТМ занял 1-е место среди опухолей женской репродуктивной сферы.
У 70-80 % больных распространенность опухоли соответствует 1-11 стадиям по классификации FIGO. Этот показатель, неоднократно отмеченный многими авторами, одинаков во всех странах мира и практически не меняется со временем, что связано с ранними клиническими проявлениями заболевания, которые заставляют больных обращаться к врачу. Несмотря на это, прогрессирование возникает примерно у 25 % больных РТМ ранних стадий. Все сказанное выше объясняет важность разработки новых подходов к лечению РТМ. Ограниченность объема статьи не позволяет подробно рассказать обо всех методах лечения этого заболевания, поэтому мы постараемся остановиться на наиболее сложных и дискуссионных вопросах.
Основным путем диссеминации РТМ является лимфогенный. От дна матки лимфа оттекает в поясничные лимфатические узлы, от средней и нижней трети тела матки — в тазовые. Это важная особенность РТМ, в значительной степени определяющая тактику его лечения. Риск лимфогенной диссемина-ции зависит от гистологического типа опухоли, степени дифференцировки, глубины инвазии миометрия, размеров опухоли, перехода опухоли на шейку матки и ее распространения за пределы матки. При I клинической стадии РТМ поражение тазовых лимфатических узлов наблюдается у 10 % больных, поясничных -
у 6 %, при II клинической стадии - у 36 % и 23 % больных соответственно. Частота метастазов в поясничных лимфатических узлах в отсутствие метастазов в тазовых составляет 2 %.
В 1971 г. FIGO приняла широко известную классификацию, согласно которой стадии РТМ определялись на основании клинических признаков. Позже было показано, что у 38 % больных РТМ I клинической стадии во время операции обнаруживаются метастазы в лимфатических узлах, яичниках, маточных трубах, распространение по париетальной и висцеральной брюшине или опухолевые клетки в смывах из брюшной полости. Пред- и послеоперационный гистологический диагнозы не совпадают у 27 % больных, степень дифференцировки - у 34 %, стадия - у 51 % (Creasman W.T. et al., 1987; Cowles TA et al., 1985). Анализ выживаемости позволил сделать вывод, что прогноз при РТМ определяется в основном морфологической, а не клинической стадией (Wolfson A.H. et al., 1992). Так, выживаемость при I клинической стадии ниже, чем при III морфологической, а выживаемость при III клинической стадии приближается к таковой при IV морфологической (FIGO Annual Report, 2001). Стало ясно, что стадию РТМ следует определять на основании данных интраоперационной ревизии и гистологического исследования. Практически сразу же появились противники определения морфологической стадии РТМ. Их аргументами являлись и являются высокая частота сопутствующих заболеваний и пожилой возраст больных, которые препятствуют расширению объема хирургического вмешательства или хирургическому лечению вообще, возможность излечения части больных РТМ с помощью только хирургического лечения в объеме экстирпации матки с придатками, а также высокая информативность современных методов визуализации.
О необходимости определения морфологической стадии FIGO впервые заявила в 1988 г. Федерация дала следующие рекомендации: 1) определять стадию РТМ при хирургическом вмешательстве и последующем морфологическом исследовании; 2) если хирургичес-
кое вмешательство не проводят, определять стадию по классификации FIGO 1971 г., обязательно указывая, что использована эта классификация. Однако FIGO не уточнила вмешательства, необходимые для определения стадии РТМ, прежде всего для оценки состояния лимфатических узлов.
Операция - первый этап лечения большинства больных РТМ. Отказ от операции оправдан только в тех случаях, когда риск летального исхода во время и после нее превышает риск смерти от прогрессирования РТМ. Частота рецидивов после лучевой терапии как самостоятельного метода лечения составляет 1015 %. В ведущих онкогинекологических клиниках не подвергаются хирургическому лечению из-за тяжелых сопутствующих заболеваний Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
По данным целого ряда исследований, адъювантная гормонотерапия при РТМ неэффективш (Lewis G.C. et al., 1974; Kauppila A., 1984; DePalo G. et al., 1985; MacDonald R.R. et al., 1988; Vergote I. et al., 1989). Эффективность гормонотерапии при диссеминированном РТМ и при прогрессировании заболевания зависит от степени дифференцировки, уровней рецепторов стероидных гормонов в опухоли. Частота частичных и полных ремиссий при проведении гормонотерапии составляет 11-19 %, стабилизации - 15-52 % (Piver M.S. et al., 1980; PodratzK.C. et al., 1985; Thigpen T. et al., 1986). Эффективность лечения не зависит ни от используемого препарата, ни от режима его назначения.
Активно изучается адъювантная химиотерапия при РТМ. Наиболее активные препараты - таксаны, антрациклины, производные платины. Предполагаемые показания - папиллярный серозный и светлоклеточный РТМ, РТМ III-IV морфологических стадий, РТМ ранних стадий при наличии по крайней мере двух из следующих факторов риска: низкая степень дифференцировки, глубокая инвазия миометрия, по-
ражение стромы шейки матки, опухолевые эмболы в лимфатических и кровеносных сосудах. К не решенным пока вопросам системного лечения РТМ относятся эффективность адъювантной химиотерапии, выбор системной терапии (гормоно- или химиотерапия) при прогрессировании, возможности сочетания системной и лучевой терапии.
К неблагоприятным прогностическим факторам при РТМ относятся пожилой возраст, плоскоклеточный, светлоклеточный, папиллярный серозный и недифференцированный гистологический типы, низкая степень дифференцировки опухоли, глубокая инвазия миометрия, распространение опухоли на перешеек или шейку матки, опухолевые эмболы в кровеносных и лимфатических сосудах, метастазы в яич-
никах и лимфатических узлах, диссеминация по брюшине, большие размеры опухоли, низкое содержание рецепторов прогестерона и эстрогенов в опухоли, присутствие опухолевых клеток в смывах из брюшной полости, анеуплоидия опухолевых клеток и высокий индекс пролиферации, выраженный ядерный атипизм, высокая экспрессия отдельных онкогенов.
В заключение хотелось бы отметить, что 5-летняя общая выживаемость больных РТМ по стадиям соответствует таковой больных раком яичников, что указывает на необходимость совершенствования лечения этого заболевания и проведения крупных рандомизированных исследований, которые позволят точнее определять показания к нему.
Рак тела матки (рак эндометрия) — это злокачественная опухоль, вызванная ростом патологических клеток эндометрия, оболочки, покрывающей внутреннюю полость матки. Это заболевание также называют раком матки или раком эндометрия. Примерно в 8% случаев, выявляется редкий тип опухоли матки — саркома матки. Она возникает, когда опухоль появляется в миометрии, мышечной ткани органа.
В последнее десятилетие рак тела матки занимает лидирующие позиции среди онкологических заболеваний женских половых органов. Более чем в 80% случаев он диагностируется у пациенток в пери- и постменопаузе, однако встречается и у женщин моложе 40 лет.
Факторы риска рака эндометрия
Большинство пациентов с опухолями тела матки страдает обменными нарушениями, заболеваниями сердечно-сосудистой системы, повышенным артериальным давлением.
- повышенная масса тела (ожирение)
- отсутствие беременностей
- поздняя менопауза
- сахарный диабет
- гормональная заместительная терапия.
Однако, несмотря на сложность патогенетического механизма развития злокачественного процесса, рак тела матки выявляется на ранних стадиях благодаря доступным современным методам исследований.
Симптомы и первые признаки рака тела матки
Одним из основных проявлений рака эндометрия являются выделения из половых путей с примесью крови, тянущие боли внизу живота. При этом большинство пациенток чувствуют себя здоровыми. Важно понимать, что после наступления менопаузы любые кровянистые выделения из половых путей считаются патологией.
До наступления климакса заподозрить заболевание возможно, если менструации стали более обильными или есть кровомазанье в межменструальный период. При появлении данных симптомов необходимо обратиться к врачу гинекологу-онкологу. Только онкогинеколог сможет после квалифицированного осмотра назначить необходимо важные для диагностики рака тела матки методы исследования.
Диагностика рака эндометрия
Во время гинекологического осмотра врач может определить изменение формы, плотности, размера матки и заподозрить заболевание. Более точным методом считается ультразвуковое исследование (УЗИ) органов малого таза. При выявлении патологии полости матки необходимым является выполнение биопсии эндометрия.
После выполненной биопсии полученный материал отправляется на гистологическое исследование. Если выявляются опухолевые клетки, то необходимо проведение дополнительного обследования для постановки стадии рака тела матки и определения индивидуальной тактики лечения.
- Рентгенографии органов грудной полости
- Магнитно-резонансной томографии (МРТ) органов малого таза
- Компьютерной томографии (КТ) органов брюшной полости
Исследование онкологических маркеров в сыворотке крови не является достоверным способом диагностики рака тела матки, хотя уровень маркера CA-125 может повышаться.
На основании проведенного обследования выставляют клиническую стадию заболевания (рисунок 1):
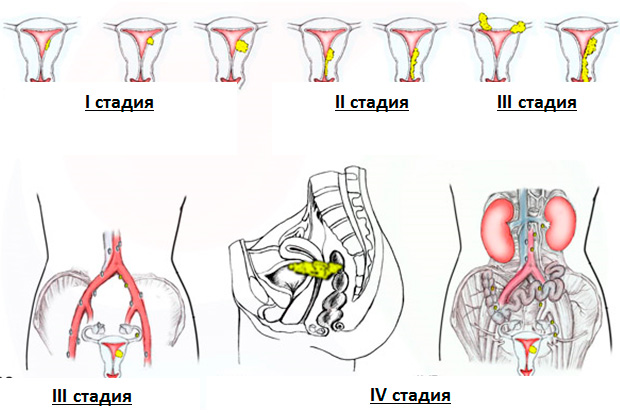
Рис. 1. Стадии рака тела матки (FIGO CANCER REPORT 2012)
Выделяют 4 стадии рака эндометрия:
- I стадия : Опухоль ограничена телом матки.
- II стадия : Опухоль распространяется на шейку матки, но не распространяется за пределы матки.
- III стадия : Опухоль выходит за пределы матки, с поражением придатков матки/ влагалища/ околоматочной клетчатки и/или тазовых лимфатических узлов.
- IV стадия : Опухоль прорастает в близлежащие органы: мочевой пузырь и/или прямую кишку. Или же раковые клетки, образуя метастазы, поражают органы, расположенные вне малого таза — печень, легкие или кости.
Лечение рака тела матки
Ведущим и эффективным методом лечения рака тела матки является хирургический. Объем вмешательства определяется для каждой пациентки индивидуально в соответствии со стадией заболевания. Операция включает в себя удаление матки с придатками (маточные трубы и яичники) и регионарных лимфатических узлов. (рисунок 2).
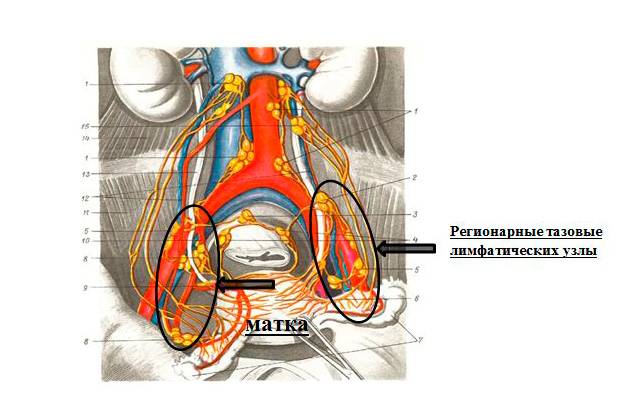
Данный объем хирургического лечения является абсолютно радикальным.
С клинической точки зрения объемы хирургических вмешательств, выполняемых в онкогинекологии, не сопоставимы с операциями при доброкачественных заболеваниях, и требуют очень высокой квалификации и опыта хирурга. Тем не менее, в ведущих онкологических клиниках нашей страны лапароскопические операции не являются редкостью.
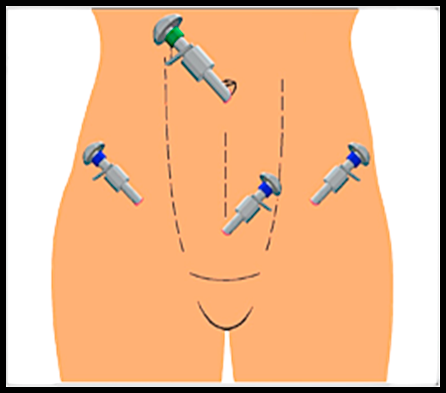
Рис. 3– положение троакаров при выполнении лапаросокпического вмешательства при раке тела матки.
На рисунке 4 представлен вид удаленной матки с придатками и регионарные тазовые лимфоузлы. В матке определяется опухоль, занимающая практически всю ее полость.
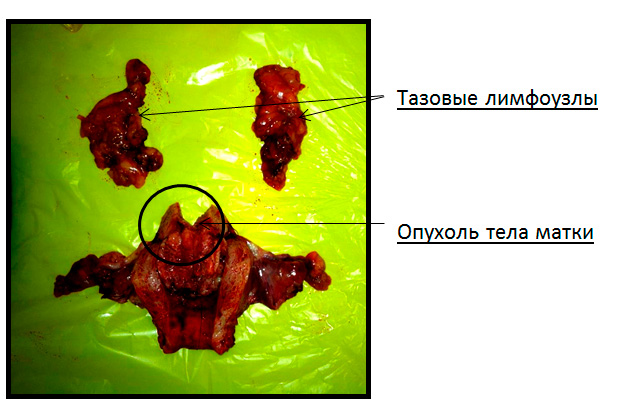
Рис.4 операционный макропрепарат (матка с правыми и левыми придатками, правыми и левыми подвздошными лимфатическими узлами).
Лапароскопические операции могут быть выполнены пациенткам любого возраста и предпочтительны женщинам с повышенной массой тела, так как косметический эффект после видеоэндоскопических вмешательств позволяет избежать множества осложнений со стороны послеоперационной раны.
Лапароскопия характеризуется значительно низкой частотой послеоперационных осложнений, что крайне важно для пациенток с серьезными сопутствующими заболеваниями органов сердечно-сосудистой, дыхательной, эндокринной систем. Благодаря этому сокращаются сроки пребывания пациенток в стационаре. Качество жизни пациенток после лапароскопических вмешательств значительно выше, что обусловлено быстрым восстановлением после операции, хорошим косметическим эффектом.
Выполненные лапароскопические операции у пациенток раком матки не ограничивают показания для проведения необходимого послеоперационного лечения лучевой терапией и способствуют сокращению сроков до ее начала, что крайне важно для эффективного комбинированного лечения данного заболевания.
- Радиотерапевтический метод лечения
- Химиотерапевтический метод лечения
- Гормональная терапия
При проведении лучевого лечения возможны осложнения, связанные с попаданием в зону облучения смежных органов: мочевого пузыря и толстого кишечника.
При проведении химиотерапии не исключены выпадение волос, тошнота, рвота, слабость.
Прогноз заболевания и динамическое наблюдение
Злокачественные опухоли тела матки начальных стадий можно отнести к заболеваниям с относительно благоприятным прогнозом. По данным госпитальных регистров, общая 5-летняя выживаемость больных раком тела матки, получивших лечение в ведущих мировых клиниках, достигает практически 80% (рисунок 5).
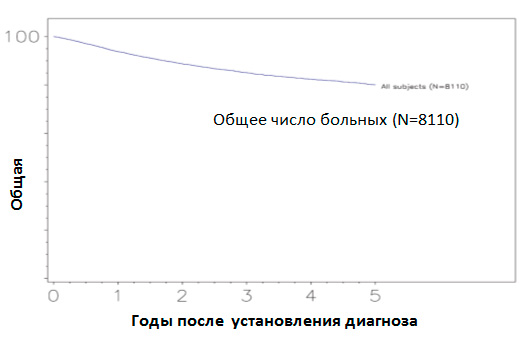
Рис. 5. Общая 5-летняя выживаемость больных раком эндометрия (Annual report on the Results of Treatment in Gynecological Cancer FIGO, 2006)
После завершения лечения пациенту необходимы контрольные визиты к врачу онкологу-гинекологу и регулярные обследования для исключения возврата заболевания.

Авторская публикация:
СМИРНОВА ОЛЬГА АЛЕКСЕЕВНА
врач-онколог, акушер-гинеколог
НИИ онкологии им Н.Н. Петрова

- Как возникает рак матки?
- Факторы риска рака эндометрия
- Онкология матки: симптомы по стадиям
- Диагностика рака эндометрия
- Степень дифференциации опухоли
- Стадии рака эндометрия
- Прогноз выживаемости при раке тела матки
- Цены в Европейской клинике на лечение рака матки
Как возникает рак матки?
Рак всегда начинается с клеток — основы для формирования тканей. Из тканей состоят все органы тела человека, в том числе и матка. Здоровые клетки растут и делятся, чтобы появились новые клетки. Когда здоровые клетки стареют или повреждаются, они умирают, а их место занимают новые клетки. Но иногда этот процесс нарушается. Новые клетки начинают расти даже когда организм в них не нуждается, или же например старые и поврежденные клетки перестают умирать. Когда новых лишних клеток становится слишком много, формируется образование из ткани, которое и называется опухолью.
Доброкачественные опухоли матки, например, миомы, полипы, эндометриоз:
- не представляют угрозу для жизни;
- обычно могут быть удалены и не вырастают снова;
- не врастают в соседние органы и ткани;
- не распространяются в другие части тела
Злокачественные опухоли матки:
- представляют угрозу для жизни;
- обычно могут быть удалены и не вырастают снова;
- могут врастать и повреждать соседние ткани и органы, например, влагалище;
- могут распространяться в другие части тела.
Факторы риска рака эндометрия
Если у вас или ваших близких диагностирован рак эндометрия, совершенно естественно интересоваться и беспокоиться: что могло вызвать такое заболевание? Очень часто врачи просто не могут объяснить, почему у одной женщины появляется рак эндометрия, а у другой нет.

Но врачи знают, что существуют определенные факторы риска, которые могут с большей вероятностью привести к развитию рака матки. Среди них:
- Чрезмерный рост ткани эндометрия (гиперплазия эндометрия: патологическое увеличение числа клеток, которыми выстлана поверхность матки является фактором риска развития рака эндометрия. Гиперплазия сама по себе не является раком, но иногда может перерождаться в злокачественную опухоль. Частыми симптомами этого состояния являются: тяжелые и обильные менструации, кровянистые выделения между менструациями и кровотечения после менопаузы. Гиперплазия эндометрия — нередкое состояние у женщин старше 40 лет.
- Ожирение: Женщины с увеличенной массой тела больше подвержены риску развития рака эндометрия.
- Репродуктивный и менструальный анамнез: женщины, у которых никогда не было детей, женщины, у которых менструации начались до 12 лет, женщины, у которых менструации продолжались после 55 лет.
- Прием ТОЛЬКО эстрогена в анамнезе: риск рака эндометрия выше у женщин, которые принимали только эстроген (без прогестерона) много лет в качестве гормональной заместительной терапии при менопаузе.
- Прием тамоксифена в анамнезе: женщины, которые принимали тамоксифен для лечения или профилактики рака молочное железы.
- Лучевая терапия органов малого таза в анамнезе.
- Семейный анамнез: женщины, у которых у матери, сестры или дочери были случаи рака эндометрия находятся в зоне риска по возникновению этого заболевания, а также женщины с наследственной формой рака толстой кишки (синдром Линча).
Нужно помнить, что не у всех женщин с раком эндометрия присутствуют вышеперечисленные факторы риска. Совершенно не у всех женщин, у которых имеются эти факторы риска, возникнет рак эндометрия.
Онкология матки: симптомы по стадиям
- Первая стадия. Как правило, симптомов нет, либо могут иметься незначительные патологическое отделяемое из влагалища, например, коричневатые выделения, наличие прожилок крови на белье или общее увеличение объема влагалищных выделений.
- Вторая стадия. Симптомы более выражены. У женщин фертильного возраста это может быть увеличение продолжительности менструации, увеличение объема теряемой крови, ациклические кровотечения. У пациенток в менопаузе могут возникать скудные или обильные маточные кровотечения. Также может быть лейкорея — обильные водянистые выделения. Таким образом, распознать рак матки на ранней стадии по симптомам сложно, поскольку признаки сходны с другими заболеваниями, например, с менструальной дисфункцией.
- На третьей стадии, когда в процесс вовлекаются окружающие ткани, может наблюдаться болевой синдром (боли могут носить как постоянный, так и схваткообразный характер), выделения могут быть гнилостные (цвет мясных помоев) с неприятным запахом. При сдавлении опухолевыми массами мочеточников может развиваться гидронефроз, который характеризуется болью в пояснице и развитием азотемии — отравлением организма азотистыми продуктами обмена веществ, которые в норме должны выводиться почками.
- На четвертой стадии усиливается боль. В процесс может вовлекаться толстая кишка, что сопровождается развитием симптомов кишечной непроходимости (запоры, вздутие живота). Если опухоль проросла в стенку мочевого пузыря, в моче могут быть примеси крови. Довольно часто возникает асцит — скопление свободной жидкости в брюшной полости. При наличии отдаленных метастазов симптоматика будет определяться пораженным органом. Чаще всего рак тела матки метастазирует в печень и легкие. Также на 4 стадии отмечается общее воздействие опухоли на организм — кахексия, общая слабость и др.
Диагностика рака эндометрия
Для диагностики рака эндометрия используют следующие методики:
- Физикальное обследование органов малого таза: ваш врач будет исследовать вашу матку, влагалище и близлежащие органы, чтобы исключить наличие образований или изменений в форме и размере.
- Ультразвуковое исследование: аппарат для ультразвукового исследования использует звуковые волны, которые не слышны человеку. Эти волны отражаются от участков разной плотности. Таким образом создается изображение матки и близко расположенных органов. Такая картинка может показать опухоль эндометрия. Для получения более четкого изображения, ультразвуковое исследование может проводиться и трансвагинально (когда ультразвуковой датчик помещается во влагалище).
- Гистероскопия: использование тонкой, гибкой трубки, которая помещается во влагалище. На конце этой трубки располагается камера, которая выводит на экран изображение матки. Таким образом врач может детально рассмотреть состояние матки и эндометрия.
- Биопсия: это удаление ткани и ее дальнейшее исследование в поисках раковых клеток. Обычно используется тонкая трубка, которая помещается в матку через влагалище. Тонкий слой ткани соскабливается со стенки матки, а затем врач-патолог исследует эту ткань под микроскопом. Часто биопсия это единственный способ точной диагностики злокачественной опухоли матки.

Степень дифференциации опухоли
Если обнаружена опухоль, врач исследует образец ткани под микроскопом, чтобы определить тип и степень дифференциации опухоли. Эта степень говорит о том, насколько тип раковых клеток отличается от нормальных клеток эндометрия. По степени дифференциации опухоли можно определить как быстро она будет расти. Высоко дифференцированные опухоли часто растут быстрее и чаще распространяются. Степень дифференциации также помогает определить дальнейший протокол лечения.
При диагностике рака эндометрия очень важно определить стадию заболевания. Это самая важная информация для определения тактики лечения. Стадии заболевания определяются на основании того вросла ли опухоль в соседние органы или распространилась в другие части тела.
Когда опухоль распространяется в другие органы, то она состоит из точно таких же патологических клеток как и первичная опухоль и называется точно также. Например, рак эндометрия может распространяться в легкие; при этом в легком будут присутствовать клетки опухоли эндометрия. Это называется метастатический рак эндометрия, а не рак легкого. Лечится такое осложнение по протоколам лечения рака эндометрия, а не рака легкого.
Чтобы определить распространилась ли опухоль, врач может назначить один из следующих видов исследований:
- Лабораторные анализы. Pap-тест может показать распространился ли опухолевый процесс на шейку матки, а анализы крови могут выявить нарушения функции печени и почек. Также ваш врач может назначить анализ на субстанцию CA-125, которая часто повышается при различных видах рака.
- Рентген грудной клетки: рентген грудной клетки может помочь выявить опухоль в легком.
- Компьютерная томография: Компьютерная томография делает много последовательных рентгеновских снимков-срезов, охватывая большое количество органов, и позволяет получить высоко точную картину, найти опухоль в отдаленных участках тела: лимфоузлах, легких и др. Иногда компьютерная томография проводится с введением контрастного вещества.
- МРТ работает как большой магнит, который подключен к компьютеру и помогает получить очень точные изображения матки, других внутренних органов и лимфоузлов. Иногда МРТ также проводится с введением контрастного вещества.

Часто, чтобы точно определить стадию заболевания, необходима операция. Хирург удаляет матку и берет образцы ткани из органов малого таза и живота. Когда матка удалена, препарат исследуют и оценивают, насколько глубоко вросла опухоль. Хирург также проверяет повреждены ли соседние органы и лимфоузлы.
Стадии рака эндометрия
Стадия 0 — Патологические раковые клетки найдены ТОЛЬКО на слизистой оболочки внутреннего слоя матки такая опухоль называется карцинома матки in situ.
Стадия I — Опухоль проросла через слизистую в эндометрий. Иногда опухоль прорастает и в миометрий.
Стадия II — Опухоль проросла в шейку матки.
Стадия III — Опухоль проросла через все слои матки и внедрилась в соседние органы: влагалище и лимфоузлы.
Стадия IV — Опухоль проросла в мочевой пузырь или кишечник. Или клетки опухоли распространились в отдаленные части тела: печень, легкие или кости.
В лечении рака матки используют хирургию, химиотерапию и гормональную терапию. Часто используют комбинацию этих методов.
Прогноз выживаемости при раке тела матки
Прогноз выживаемости будет определяться стадией заболевания, возрастом пациентки и патогенетическими особенностями опухоли. Наиболее благоприятно протекают гормонально зависимые опухоли без метастазов у пациенток младше 50 лет. У них удается добиться 5-летней выживаемости у 90% пациенток. Наиболее неблагоприятный прогноз у женщин старше 70 лет с автономным типом опухоли. При отсутствии отдаленных метастазов у них удается добиться пятилетней выживаемости в 60% случаев.
Читайте также:

