Моноклональные препараты при раке легкого

Моноклональные антитела и их использование в онкологии
Моноклональные антитела, или МАТ, являются антителами лабораторного производства, которые связываются с конкретными антигенами, выраженных раковых клеток, таких как белок, который присутствует на поверхности раковых клеток, но отсутствуют (или имеют место, но при более низких уровнях) у нормальных клеток.
[important] Принцип разработки
Для создания МАТ исследователи вводят их мышам с антигеном из раковых клеток человека. Затем они собирают клетки, продуцирующие антитело от мышей и индивидуально сливают их с миеломной раковой клеткой (В-клетки), чтобы получить слитую клетку, известную как гибридома. Каждая гибридома (клеточная линия) затем путем деления производит идентичные дочерние клетки или клоны – отсюда термин “моноклональные”.
[/important] А антитела, секретируемые различными клонами, проверяются на способность идентифицировать антитела, которые наиболее сильно связываются с антигеном. С помощью этих бессмертных клеток гибридом могут быть получены большие количества антител. Поскольку антитела мыши могут сами вызывать иммунный ответ у людей, который способен уменьшить их эффективность, мышиные антитела часто “очеловечивают” путем замены большей части мышиного антитела, насколько это возможно, человеческими порциями. Это делается с помощью генной инженерии.
Принцип действия
Некоторые моноклональные антитела стимулируют иммунный ответ, который разрушает раковые клетки. Подобно антителам, полученным естественным путем работы В-клеток, эти моноклональные антитела покрывают “оболочкой” поверхность раковой клетки, вызывая ее разрушение иммунной системой. Уже одобренные медициной МАТ этого типа включают ритуксимаб, который ориентирован на антиген CD20, найденный в клетках неходжкинской лимфомы и алемтузумаб, который ориентирован на антиген CD52, найденный в клетках хронического лимфолейкоза (ХЛЛ). Ритуксимаб может также непосредственно вызывать гибель клеток (апоптоз).
Другая группа МАТ стимулирует противоопухолевый иммунный ответ, связываясь с рецепторами на поверхности клеток иммунной системы и уменьшая сигналы, которые мешают иммунным клеткам нападать на собственные ткани организма, в том числе на раковые клетки. Одним из таких МАТ, Ипилимумаб, был одобрен для лечения метастатической меланомы в 2011 году. Есть и другие, которые находятся в стадии клинических исследований.
Другие моноклональные антитела мешают действию белков, которые необходимы для роста опухоли. Например, целью препарата бевацизумаб является сосудистый эндотелиальный фактор роста (VEGF), белок, секретируемый опухолевыми клетками и другими клетками в микроокружении опухоли, что способствует развитию кровеносных сосудов для питания опухоли. Когда бевацизумаб связывается с VEGF, тот не может взаимодействовать с его клеточными рецепторами, предотвращая передачу сигналов, которые приводят к росту новых кровеносных сосудов.
Аналогичным образом, для препаратов цетуксимаб и панитумумаб целевым является рецептор эпидермального фактора роста (EGFR), а МАТ трастузумаб нацелен на человеческий рецептор эпидермального фактора роста 2 (HER-2). МАТ, которые связываются с клеточной поверхностью фактора роста рецепторов, предотвращают функцию рецептора отправлять свои нормальные стимулирующие рост сигналы. Они также могут запускать апоптоз и активизировать иммунную систему для уничтожения опухолевых клеток.
Другая группа раковых терапевтических моноклональных антител являются иммуноконъюгаты. Эти моноклональные антитела, которые иногда называют иммунотоксины или антитела конъюгаты – лекарственное средство, включающее антитела, такие как бактериальные токсины, химиотерапевтические препараты, или радиоактивные молекулы, прикрепленные к клеточному веществу клеток киллеров.
Антитело прикрепляется к его специфическому антигену на поверхности раковой клетки, и действующее вещество просто растворяет раковые клетки. Утвержденные иммуноконъюгаты, которые работают таким образом, включают ибритумомаб тиуксетан, который ориентирован на антиген CD20, чтобы доставить радиоактивный иттрий -90 до B-клеток для устранения клеток неходжкинской лимфомы; Тозитумомаб, который ориентирован на антиген CD20, чтобы доставить радиоактивное йод-131 к клеткам неходжкинской лимфомы; и шума-трастузумаб эмтансин, который ориентирован на молекулу HER-2 для доставки препарата DM1, который ингибирует пролиферацию клеток, HER-2 принадлежит метастатическим клеткам рака молочной железы.

Моноклональные антитела цена
Сложно все описанное? Достаточно сложно для исследователей, которые работали лет этак тридцать тому назад. Однако наука идет вперед очень быстро. Это я к тому, что моноклональные антитела в силу своих свойств высокой избирательности (они, кстати, имеют низкую токсичность) способны эффективно стимулировать иммунную систему на борьбу с раком.
В связи с важностью работы над разработкой моноклональных антител, в исследовательский процесс включились ведущие фармацевтические компании мира. Получается, что МАТ – одно из ведущих направлений разработок по борьбе с раком. Каковы же цены моноклональных антител на сегодня? Понятно, что сегодняшняя цена еще далека от массового использования по причине дороговизны. Но в ближайшей перспективе в ходе уменьшения себестоимости будет уменьшаться и отпускная цена в аптеках. Что, например уже случилось с препаратом ипилимумаб.
Ипилимумаб
Препарат Ипилимумаб (его рыночное название Ервой — Yervoy) разработан для лечения прогрессирующих форм рака кожи, щитовидной железы, простаты, и некоторых других видов рака. Несмотря на то, что Ипилимумаб появился на рынке совсем недавно – в 2011 году – он уже успел проявить себя как эффективное средство для борьбы с поздними стадиями меланомы. По статистике использование препарата позволило увеличить выживаемость больных почти вдвое. К слову, меланома в стадии прогресса раньше не поддавалась лечению. Конечно, цена препарата пока далека от широкого использования:
YERVOY 5MG/ML в упаковке 10 мл цена вместе с доставкой в Москву из Германии 1 упаковка-4650 евро. YERVOY 5MG/ML в упаковке 40 мл цена вместе с доставкой 1 упаковка-17500 евро. Поставщик обещает доставку в короткие сроки с подтверждением всеми документами покупку в аптеке Германии. Собственно, имеющий возможность, может сам отправиться за препаратом в Германию.
Бевацизумаб
Аптечное название Авастин (действующее вещество бевацизумаб) концентрат для инфузий от 17000 рублей за 25 мл.
Достаточно узкая направленность – метастатический колоректальный рак. Часто его комбинируют с химиотерапией на основе химиотерапевтического агента фторпиримидина и его производных.
Цетуксимаб
Аптечное название Эрбитукс (действующее вещество цетуксимаб). Цена от 8500 рублей в упаковке 5 мг/мл. Направленность – рак в области головы, лица и шеи. К этому добавлен вторичный рак толстого кишечника и некоторых других локализаций, но именно вторичный рак.


Моноклональные антитела — это новейшее достижение медицины, которое применяется при лечении тяжелых заболеваний. Среди них злокачественные новообразования, аутоиммунные, системные, заболевания сердечно-сосудистой системы, некоторые инфекции и многое другое. Помимо этого, моноклональные антитела широко используются в диагностике, например, в иммуногистохимии, иммуноферментном анализе, проточной цитофлуориметрии и др. Таким образом, данная технология используется во многих отраслях современной медицины.
- Способы получения моноклональных антител
- Механизм действия моноклоналных антител
- Препараты с моноклональными антителами
- Проблемы при использовании моноклональных антител
Человечество уже давно открыло для себя действие антител — особых молекул, которые вырабатываются клетками иммунной системы для распознавания чужеродных агентов — антигенов и их уничтожения. Антитела обладают специфичностью. Это значит, что они узнают только свой антиген, причем не просто антиген, а отдельный его фрагмент — детерминантную группу. В одном антигене может быть несколько таких детерминантных групп, и к ним будут образовываться разные антитела. Более того, к одной детерминанте может образовываться сразу несколько видов антител, которые могут отличаться по структуре, степени родства и прочности связывания. Таким образом, при введении антигена в организм образуется большое количество разных видов антител, направленных исключительно на один вид антигена. Это позволяет обеспечить адекватную иммунную защиту.
Антитела образуются специальными антителообразующими клетками. Причем каждый их вид образуется отдельной группой генетически однородных клеток — клонов. Чем больше необходимо видов антител, тем больше образуется клонов. Соответственно, антитела, которые вырабатываются одним клоном клеток называются моноклональными антителами.
Раньше для производства антител применялась иммунизация животных, после которой отбиралась их плазма и использовалась для приготовления отдельных препаратов — иммунных сывороток для борьбы с различными токсинами (дифтерия, столбняк), вирусами, ядами и др. Но бывают ситуации, когда нужно конкретное антитело, направленное на конкретную детерминанту антигена. Здесь уже обычной иммунизацией не обойтись. Требуются более прицельные технологии.
Способы получения моноклональных антител
Получение моноклональных антител — это сложный многоступенчатый процесс, который проходит следующие этапы:
- Иммунизация животных. Обычно используются мыши или крысы. Это нужно для того чтобы увеличить количество лимфобластов — клеток, продуцирующих нужные антитела и перевести эти клетки в активное состояние. После выделения из организма эти клетки не могут долго существовать в лабораторных условиях, они погибнут даже на питательных средах с содержанием ростовых факторов. Чтобы это предотвратить, их скрещивают со злокачественными миеломными клетками.
- Подготовка миеломных клеток. Параллельно с иммунизацией животных проводят подготовку опухолевых миеломных клеток. Они, во-первых, обладают способностью синтезировать моноклональные антитела, а во-вторых, обладают неограниченным жизненным потенциалом (они бессмертны и способны к бесконечному воспроизведению). Для того чтобы миеломные клетки не погибли вне организма, их культивируют на специальных средах с использованием факторов роста.
- Гибридизация (слияние) лимфобластов и миеломных клеток для образования гибридомы. Для этого клетки обрабатывают различными антителами, чтобы изменить строение их мембран и спровоцировать образование цитоплазматических контактов. При этом образуются разные типы клеток, имеющих двойной набор хромосом (дикарионы). Это могут быть дикарионы, образованные только лимфоцитами, или только миеломными клетками. Но для производства моноклональных антител нужны именно дикарионы, образованные лимфоцитом и миеломной клеткой — гибридные клетки.
- Отбор гибридных клеток. Для этого используют специальные растворы, которые позволяют выжить только лимфобластным и гибридомным дикарионам. Первые в скором времени погибают, т. к. не обладают возможностью безграничного деления, а гибридомные клетки остаются жизнеспособными.
- Реклонирование гибридомных клонов.
- Определение и отбор гибридом, продуцирующих моноклональные антитела. Обычно для этого используется иммуноферментный анализ.
- Массовое наращивание антител.
- Очистка полученных антител. Степень очистки будет определяться областью применения препарата. Если это диагностика, достаточно 70-95% степени чистоты. Если препарат предполагается использовать для иммунотерапии, требуется более высокая степень чистоты. Для очистки используется аффинная и ионообменная хроматография.
- Удаление оставшихся примесей и обеззараживание полученного препарата от вирусов и бактерий.
В настоящее время идет тенденция отказа в использовании антител животных для лечебных целей. Во-первых, они являются чужеродными агентами для организма и могут спровоцировать аллергические реакции, вплоть до анафилаксии, что напрямую угрожает жизни пациентов. Во-вторых, иммунная система человека, распознавая такие антитела как чужеродные, будет пытаться их инактивировать, что снизит эффективность противоопухолевого лечения. Получить человеческие моноклональные антитела вышеописанным методом не представляется возможным, ввиду следующих проблем:
- Иммунизация человека различными антигенами неэтична.
- Даже если получить иммунизированные лимфоциты человека, будут проблемы на этапе их слияния с клетками миеломы мыши — полученные гибридомы будут нестабильны.
- Клеточные линии миеломы человека, которые можно было бы эффективно использовать в рамках биотехнологий для получения антител, пока получить не удалось.
В этой связи необходимо было искать новые технологии получения антител. Решением проблемы стали гибридные, гуманизированные и одноцепочечные антитела, производство которых подразумевало применение гибридомной технологии, кратко описанной выше, и технологии рекомбинантной ДНК.
Механизм действия моноклоналных антител
Моноклональные антитела широко используются в лечении заболеваний, у которых в патогенезе замешан иммунный компонент. С их помощью лечат псориаз, аутоиммунные заболевания, ревматоидный артрит, рассеянный склероз. Большие перспективы эти технологии получили и в онкологии в рамках таргетной терапии. При этом, их эффект основан на различных механизмах, которые рассмотрены ниже.

В качестве примера изменения клеточных сигналов можно привести рецепторы факторов роста. Некоторые злокачественные клетки имеют на своей поверхности большое количество рецепторов к факторам роста, активирующим каскад реакций, направленный на усиление размножения клетки. Чем больше таких рецепторов, тем активнее протекает этот процесс. Если блокировать рецептор с помощью моноклонального антитела, он не сможет связаться с лигандом (фактором роста), и соответственно каскад этих реакций не будет запущен. Клетка не будет так активно размножаться и в конце концов погибнет.
Этот механизм реализуется следующим образом. Антитело связывается с антигеном, находящимся на поверхности злокачественной клетки, что приводит к активации многоэтапной системы комплемента (механизма иммунного ответа). Конечным этапом этих реакций является образование особого белка С 9, который перфорирует клеточную мембрану раковой клетки, что в конечном итоге приводит к ее гибели.
Препараты с моноклональными антителами
Препараты на основе моноклональных антител уже два десятилетия входят в протоколы противоопухолевого лечения некоторых злокачественных новообразований. В 2008 году ВОЗ были приняты рекомендации относительно непатентованных названий таких препаратов:
- Их название должно заканчиваться на маб, от английского monoclonal antibody.
- Для указания источника получения моноклонального антитела должны использоваться следующие подосновы:
- -аксо — гибридное антитело.
- -о — мышиное антитело.
- -кси — химерное антитело.
- -у — человеческое антитело.
В настоящее время используется два вида противоопухолевых моноклональных антител:
- Неконъюгированные антитела — они оказывают непосредственное действие на процессы, которые приводят к гибели злокачественной клетки.
- Конъюгированные антитела — они связаны (конъюгированы) с токсинами или изотопами. Токсины и изотопы обладают уничтожающим действием на злокачественные клетки, а антитело обеспечивает их прицельную доставку к клеткам-мишеням.
Эти препараты используются чаще всего. Их целью является определенный рецептор на поверхности злокачественной клетки.
К этому типу препаратов относится ритуксимаб — первое моноклональное антитело, которое было одобрено для применения в клинической практике. Его используют для лечения CD20+ В-клеточных лимфом. Рецептор CD20 есть на В-лимфоцитах, как здоровых, так и опухолевых, но он отсутствует на других тканях и клетках, в том числе на стволовых. Поэтому при воздействии ритуксимаба хоть и погибает популяция В-лимфоцитов, но потом она восстанавливается за счет нетронутых стволовых клеток. Причем восстанавливаются именно здоровые клетки.
Неконъюгированные антитела могут помечать злокачественные клетки и делать их видимыми для иммунной системы. Таким способом работает алемтузумаб, который связывается с CD52+ лимфоцитами и привлекает к ним внимание иммунитета.
Также к неконъюгированным моноклональным антителам относятся ингибиторы рецепторов факторов роста. Факторы роста — это специальные молекулы, которые запускают деление клетки. Для того чтобы запустить этот процесс, фактор должен связаться со специальным рецептором, расположенным на мембране клетки, что приведет к каскаду соответствующих реакций. Такие рецепторы есть и у здоровых клеток, и у злокачественных, но у злокачественных их может быть очень много, что позволяет таким клеткам делиться быстрее. Блокирование рецепторов с помощью антител приводит к нарушению этого процесса деления и клетки уже не могут бесконтрольно размножаться. К таким препаратам относится трастузумаб, цетуксимаб и др.
К неконъюгированным антителам относятся и ингибиторы ангиогенеза — образования кровеносных сосудов. Ангиогенез очень важен для злокачественных опухолей, чтобы получать большее количество кислорода и питательных элементов, поэтому опухоли инциируют его образование с помощью специальных химических сигналов. Моноклональные антитела либо блокируют передачу этих сигналов, либо разрушают уже созданную внутри опухоли сосудистую сеть. Это приводит к нарушению ее питания и остановке роста. К группе этих препаратов относится рамуцирумаб, бевацизумаб и др.
Конъюгированные моноклональные антитела связывают с цитотоксическими или радиотоксическими веществами, что позволяет прицельно воздействовать разрушающим агентом на злокачественные клетки. В качестве примера такого препарата можно привести ибритумомаб (Зевалин), в котором моноклональное антитело против CD20 (как мы помним, это маркер В-лимфоцитов) соединено с радиоактивным изотопом — иттрием-90. Препарат применяется для лечения В-клеточных лимфом. В качестве другого препарата можно привести Кадсилу — препарат, в котором антитело трастузумаб конъюгировано с ингибитором микротрубочек DM1, оказывающим цитотоксический эффект. Применяют его для лечения рака молочной железы.
Проблемы при использовании моноклональных антител
Несмотря на, казалось бы, огромные перспективы в лечении онкологических больных, применение моноклональных антител не является панацеей и тоже имеет ряд проблем:
- Препараты на основе моноклональных антител биологически и биохимически нестабильны. Особенно это касается конъюгированных антител. Это требует особых условий производства, хранения и транспортировки.
- Антитела плохо проникают внутрь опухоли.
- Они могут вызывать иммунный ответ против себя, что блокирует их действие. У 75% пациентов, которым вводились мышиные антитела, наблюдалось образование нейтрализующих антител, что снижало эффективность лечения.
- Препараты на основе моноклональных антител оказывают токсическое действие. Конечно, оно не такое выраженное как у цитостатиков, но в ряде случаев токсичность настолько высокая, что требует отмены препарата.
- Наиболее важным моментом является высокая специфичность моноклональных антител и высокая гетерогенность опухолевых клеток. Не все раковые клетки имеют молекулы мишени, на которые направлено действие препарата. Соответственно, они ускользают от его действия и остаются нетронутыми. Постепенно масса этих клеток накапливается и опухоль становится резистентной к данному методу лечения.
Чтобы улучшить результаты лечения, разрабатываются новые виды моноклональных антител. Одним из вариантов являются биспецифические антитела, которые направлены сразу на две молекулярные мишени, например, блинатумомаб — препарат, направленный сразу на две клеточные мишени В-лимфоцита — CD 19 и CD22. Он повышает узнаваемость злокачественных клеток даже после их трансформации в другие виды лейкоза.
В любом случае моноклональные антитела — это новое и высокоперспективное направление в современной онкологии. Разработка современных, более совершенных технологий помогает решать имеющиеся проблемы и делает лечение пациентов эффективнее и безопаснее.
Одним из перспективных открытий в области медицины являются моноклональные антитела (МКА). Они носят название иммуноглобулинов и представляют собой специфичные белки. Природные антитела вырабатываются клетками иммунной системы, когда в организм проникают природные антигены. Распространяясь по кровеносному руслу, МКА связываются с чужеродными специфическими элементами определенного типа, попавшими в организм, предотвращая тем самым развитие нежелательных процессов.
Как синтезируют моноклональные антитела (МКА)

В лабораторных условиях ученые научились синтезировать данные препараты. Попадая в организм человека, они активизируют действие других элементов иммунной системы с целью уничтожения чужеродных клеток. Действуют целенаправленно, демонстрируя высокий позитивный результат и используются для лечения онкологических заболеваний.
Доказано, что они являются высокоэффективными и безопасными средствами в отличие от иных сильнодействующих, но токсичных препаратов. Как показывает практика, препараты, в состав которых входят МКА, для многих онкобольных являются единственной возможностью получить положительную динамику. После проведенного курса терапии у пациентов со злокачественными опухолями крупных размеров и неутешительными прогнозами наметился прогресс в лечении, а состояние заметно улучшилось. У них появилась надежда вернуться к нормальной жизни.
Достоинства МКА-терапии
Лечение по воздействию сравнимо с лучевой терапией, однако их воздействие оказывает более мягкий щадящий эффект и обладает рядом достоинств:
• Выявив свою мишень, моноклональные антитела блокируют рецепторы, отвечающие за рост опухоли. Это существенно облегчает лечение онкозаболевания.
• Соединяясь с клетками опухоли они выделяют их из общей массы, ослабевая при этом их воздействие. А с ослабленными раковыми клетками организм будет бороться гораздо эффективнее.
• Некоторые препараты имеют в своем составе радиоактивные частицы. Попадая в опухоль, они способствуют ее разрушению.
Современное направление в лечении онкозаболеваний

Все МКА условно делятся на несколько групп, каждая из которых действует по индивидуальной схеме. Одни активизируют элементы, разрушающие клетки опухоли, другие угнетают функциональность белкой защиты раковых клеток, и т.д.
Учитывая важность исследований и создания препаратов данной группы, в работе приняли участие крупные мировые фармацевтические компании. Однако синтезирование иммуноглобулинов осуществляется на клеточных культурах, поэтому их производство считается достаточно дорогостоящим.
По вопросам лечения моноклональными антителами вы можете обратиться к нам через раздел Консультация онколога
Для подбора эффективного метода лечения вы можете обратиться за
- методы инновационной терапии;
- возможности участия в экспериментальной терапии;
- как получить квоту на бесплатное лечение в онкоцентр;
- организационные вопросы.
После консультации пациенту назначается день и время прибытия на лечение, отделение терапии, по возможности назначается лечащий доктор.
Рак легких является самой распространенной болезнью среди прочих онкологических. Смертность от нее превышает 80%.
В зоне риска оказываются активные курильщики, а также люди, страдающие туберкулезом и другими легочными заболеваниями. Чаще болеют мужчины, чем женщины.
Не все, даже инновационные препараты, в состоянии справится с этим страшным недугом. Не зря, онкология считается чумой 21 столетия.
- Препараты при химиотерапии
- Гормональные препараты против рака
- Лекарства, уменьшающие боли
- Противовирусные и противоопухолевые лекарства для лечения рака
Виды лекарственных средств
Несмотря на это, нужно лечить эту патологию и лекарства от рака легких существуют. Множество исследователей и ученых работают над новыми препаратами для полного уничтожения болезни. Выбор метода лечения зависит от расположения и размера опухоли, от состояния пациента, стадии и вида рака. Рассмотрим, какие же виды лечения и медикаментозные препараты для лечения рака легких применимы в наше время.
На первых стадиях обнаружения онкологии легких проводится удаление опухоли, либо ее части, либо всего легкого. Такая операция назначается, когда опухоль небольшая, и она не успела распространиться на другие органы.
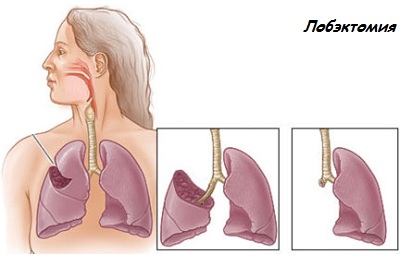
Операция имеет разновидности:
- Пульмонэктомия – удаляется все легкое целиком,
- Лобэктомия – удаляется только часть легкого.
Перед удалением рака нужно сдать необходимые анализы, чтобы удостовериться, что пациент в состояние перенести операцию. Существуют противопоказания, при которых операцию делать не можно. К ним относятся:
- сахарный диабет,
- сердечная, печеночная или почечная недостаточность,
- инфаркт миокарда.
При наличии таких заболеваний проводится другой вид лечения, например химиотерапия.
Химиотерапия является одним из основных и самых эффективных методов лечения этого недуга. Она приостанавливает рост раковых клеток. Но вместе с этим препараты негативно влияют на ряд органов, и организм в целом. Такие лекарства вводятся в кровь человека и могут действовать и распространяться по всему организму.
Доктор выписывают каждому пациенту индивидуальный курс процедур и приема лекарств после сдачи всех необходимых анализов. Перерыв необходим после каждого курса химиотерапии, так как для организма это большой стресс, он должен будет восстановиться через определенное время.
Есть много видов препаратов, которые применяются на практике. Препараты для лечения рака легких, которые используются параллельно с химиотерапией, делятся на два основных вида в зависимости от формы выпуска: таблетки и медикаменты для инъекций, которые вводятся внутривенно.
Среди них чаще всего встречаются следующие названия:
- Карбоплатин,
- Винорелбин,
- Паклитаксел,
- Цисплатин,
- Доцетаксес.
Лекарства также для лучшего эффекта используют в паре по назначению лечащего врача. Схему лечения доктора назначают индивидуально для каждого пациента. Раковые клетки быстро привыкают к препаратам, поэтому через определенное время их чередуют и применяют новые. При возникновении побочных эффектов доктора назначают дополнительные лекарственные препараты.
Химиотерапия может сочетаться с другими видами лечения, например хирургическим или лучевой терапией. Результат напрямую зависит от стадии развития болезни и ее течения.
При плоскоклеточном раке легких химиотерапия имеет ряд особенностей. Такая болезнь возникает при раке кожи и слизистых, при наличии родинок и папиллом, которые быстро растут. Заболевание возникает при раке кожи. Для лечения назначают такие препараты, как:
- Блеомицин,
- Цисплатин,
- Метотрексат.


Часто препараты применяются комплексно. При грамотном подходе к лечению такой способ дает больным людям надежду на полное выздоровление.
Онкологические заболевания могут быть как мужскими, так и женскими. Их развитие зависит от половых гормонов: тестостерона и эстрогена. Главным заданием лекарств является снижение и блокирование их роста. Такой вид терапии изменяет количество гормонов для профилактики и лечения онкологии. Такая терапия будет эффективной, только если рак является гормоночувствительным.
Лечение подразделяется на:
- хирургическое,
- радиационное,
- лекарственное.
При начальной стадии используют хирургический способ, и опухоль удаляется. В случае наличия ряда противопоказаний применяются радиационное и лекарственное лечение.
Выбор зависит от состояния больного, его возраста и уровня гормонов.
При выборе вида лечения стоит обязательно проконсультироваться со специалистом и найти оптимальный вариант. Качество лечения зависит от количества гормонов у женщин и мужчин.
Рак легких отличается сильными болевыми ощущениями. Этот факт заставляет врачей выписывать пациенту обезболивающие препараты. К ним относятся: Трамадол, Ацетаминофен,Омнопон, Морфий и другое обезболивающие лекарство от рака. Одни препараты применяются самостоятельно, иные в комплексе с другими.
Часто практикуется применение блокаторов циклооксигеназы-2, которые не имеют побочных действий, таких как кровотечения, влияние на состояние желудка и прочих. Хотя организм часто привыкает к такому виду лечения. И периодические лекарства нужно чередовать и заменять.
Основной схемой, которая применяется для уменьшения болевого синдрома, есть:
![]()
ненаркотические анальгетики и адъювантные препараты: Напроксен, Аспирин, Пироксикам, Индометацин, Парацетамол, Лорноксикам.- применение слабых опиоидов, адъювантных перпаратов и анальгетиков: Кодеин, Трамадол.
- использование сильных опиоидов, ненаркотических анальгетиков и адьювантных средств: Фентанил, Метадон, Оксикодон, Бупренорфин и прочих лекарств, которые воздействуют на нервную систему.
Если боли не проходят, проводятся дополнительные исследования для выявления их причин и назначения лечения.
Метод иммунотерапии встречается все чаще, так как чем лучше организм борется с вирусами, тем сильнее он становится, тем больше вероятность побороть недуг. Такой вид лечения применяется в тех случаях, когда болезнь возникала под влиянием вирусов и инфекций. Это особенно актуально при легочной онкологии. Организм ослабляется и нуждается в дополнительной поддержке и помощи со стороны.
Для повышения иммунной сопротивляемости организма используют препараты, в которых содержится интерферон. Он помогает увеличить сопротивляемость организма, сдерживать развитие вирусов, а также полностью уничтожает их.
Сегодня существует множество лекарств, которые борются с такой проблемой. Группы препаратов разные, начиная от винкалкалоидов, и заканчивая антрациклинами. Выбор зависит от состояния пациента, его возраста и степени болезни.
Данный вид средств имеет узкий спектр действия, поэтому нужно знать их взаимодействие с другими препаратами, а также механизм действия.
Инновационные препараты для иммунотерапии рака легких
Существуют новейшие препараты для борьбы с недугом. Их суть заключается в стимулировании иммунитета и направлении его против заболевания. Преимущество заключается в том, что их можно использовать на всех стадиях онкологии.
В организм человека вводятся биологические вещества, такие как:
- моноклональные антитела,
- цитокины.
После чего они начинают бороться со злокачественными опухолями. Если опухоль перестает расти – значит препараты подействовали.
Этот вид лечения можно сочетать с другими для достижения лучшего эффекта. Над этим вопросом работаю лучшие врачи современной медицины. Кроме этого, ученые произвели новое средство, которое уничтожает рак. Оно состоит из смеси двух лекарств: Вандетаниба и Селуметиниба.
Исследователи считают, что лекарство должно помогать на всех стадиях протекания болезни, когда обычные уколы и антибиотики бессильны. Несмотря на то, что это новейшие средства, и они пока только тестируются, надежда на полное выздоровление больных есть. Побочные эффекты при употреблении препаратов могут быть следующими:
![]()
тошнота,- аллергия,
- слабость и усталость,
- низкое давление,
- кровотечения и гематомы,
- постоянные атаки со стороны вирусных и инфекционных возбудителей болезней при ослабленности и пониженной сопротивляемости организма,
- воспаление на слизистых.
Для восстановления сил необходимо принимать противовирусные препараты и железо. В ряде некоторых сложных случаев больным проводят переливание крови.
К проблеме нужно относиться серьезно. Лечить онкологию нужно комплексно. Важно подобрать квалифицированного и опытного врача, а также хорошо оборудованную клинику с новыми приспособлениями и компетентным персоналом.
Читайте также:



