Мочегонные при опухолях головного мозга
Данный вид медицинской помощи должен осуществляться в отделениях реанимации и интенсивной терапии и быть построен на нижеприведенных принципах лечения отека головного мозга (Ш. Ш. Шамансуров и др., 1995).
Коррекция нарушения дыхания и сердечной деятельности. В зависимости от степени поражения ЦНС и тяжести состояния больных с тяжелыми формами отека, нарушения дыхания и сердечной деятельности могут быть первичными и вторичными. При их коррекции используются стандартные методики.
Этиологическое лечение основного заболевания. Рациональное лечение отека мозга заключается в устранении самой причины, которая этот отек вызвала. Такое лечение возможно лишь тогда, когда первопричина отека точно известна. Однако даже устранение причины отека не обязательно приводит к его ликвидации. В таких случаях терапевтические воздействия необходимо направить на сам отек мозга. Следует указать, что ни один метод лечения не устранит отек вокруг опухоли, абсцесса или гематомы, если не ликвидирован первичный патологический очаг.
Патогенетическая терапия отека направлена, в первую очередь, на устранение гипоксии как наиболее неблагоприятного фактора, способствующего развитию отека. Эта терапия направлена на нормализацию гемодинамики, ликвородинамики, метаболизма нейронов.
Иными словами, терапия нацелена на коррекцию основных патофизиологических механизмов (циркуляторных, васкуляторных, тканевых), участвующих в развитии отека мозга.
Коррекция гематоциркуляторных нарушений включает:
1. Лечебные мероприятия, направленные на нормализацию показателей системной гемодинамики. Для поддержания адекватной перфузии головного мозга необходимо сконцентрировать усилия на нормализацию системного артериального давления путем рационального назначения вазоактивных (дилататоров или констрикторов) препаратов быстрого действия (клофелин, дибазол или кофеин бензоат натрия и др.).
2. Назначение блокаторов кальциевых каналов. Эти препараты способствуют улучшению мозговой циркуляции, уменьшают накопление тканевых гормонов и тем самым обеспечивают устойчивость мозга к гипоксии. К ним относятся верапамил и его производные (финоптин, изоптин), нимодипин, лидофлазин, нифедипин (коринфар), фендилин (сензид), циннаризин (стугерон).
3. Усиление микроциркуляции мозга путем назначения препаратов, нормализующих тонус сосудов и реологические свойства крови. Здесь целесообразно использовать следующие вазоактивные препараты: кавинтон, ксантинола никотинат (компламин, теоникол, ксарин), эуфиллин, трентал (агапурин), дипиридамол (курантил), галидор, сермион (редергин), реополиглюкин, гепарин, индометацин (вольтарен, ортофен, аспирин).
При коррекции васкулярного (барьерного) фактора назначают следующие препараты:
• глюкокортикоиды (назначается либо преднизолон, либо дексаметазон);
• ингибиторы протеолитических ферментов. Они инактивируют тканевые гормоны воспаления при отеке головного мозга (гистамин, брадикинин, трипсин и др.). Для этой цели в/в вводится контрикал в дозе 1-10 тыс. ЕД/кг, гордокс — 12-15 тыс. ЕД/кг, аминокапроновая кислота — 200—300 мг/кг/24 ч. Курс лечения ингибиторами протеолитических ферментов, как правило, не превышает 5—7 дней;
• препараты, стабилизирующие клеточные мембраны и ангиопротекторы. Назначение последних способствует уменьшению проницаемости стенки сосудов мозга. К этой группе препаратов относятся дицинон, троксевазин, гливенол, венорутон, аскорутин;
• блокаторы кальциевых каналов (о назначении этих препаратов сказано выше);
• иммунокорригирующие препараты. В качестве иммуносупрессоров чаще всего используются стероидные гормоны (кортизон, гидрокортизон, преднизолон).
Иммуностимулирующая терапия включает применение тимозина, Т-активина, В-активина, тимогена, левамизола, пропермила, витаминов группы В.
Коррекция тканевого фактора включает:
• обеспечение адекватной оксигенации крови. Достигается восстановлением и поддержанием проходимости дыхательных путей, проведением постоянной ингаляции увлажненного кислорода, применением в некоторых случаях гипербарической оксигенации и ИВЛ;
• нормализацию метаболических процессов в нейронах головного мозга. Для этой цели используются ноотропы (ноотропил, пирацетам, ами-налон, церебролизин, энцефабол, пантогам, пиридитол и др.).
Коррекция нарушений водно-электролитного обмена и дегидратационная терапия. Важным патогенетическим направлением лечения отека мозга является назначение дегидратационной терапии:
• осмотические диуретики ( глицерин, маннитол, сорбитол и др.);
• салуретики (лазикс, фуросемид и др.);
• кортикостероиды (гидрокортизон, преднизолон). Следует указать, что действие стероидов на отек мозга развивается медленно — эффект обнаруживается не раньше, чем через 24 ч после первого введения препарата. Они более эффективны при локальных отеках мозга; кроме этого необходимо знать, что длительное применение стероидов, особенно в малых дозировках, может вызвать увеличение объема мозга и ВЧД;
• барбитураты (внутримышечно 10% раствор тиопентала натрия в дозе 10 мг/кг каждые 3 ч, суточная доза детям до 80 мг/кг).
Хирургическая коррекция отека мозга. Когда этиологический фактор отека мозга представлен экспансивным процессом (гематома, опухоль, абсцесс и т. д.), он может быть прерван только с помощью нейрохирургического вмешательства.
Для лечения гипертонической болезни широко используются диуретики (чаще в сочетании с другими гипотензивными препаратами). Диуретики (или мочегонные средства) снижают реабсорбцию натрия (также других электролитов) и воды в почечных канальцах, увеличивая выведение жидкости из организма. При лечении гипертонической болезни чаще всего используют тиазидные и тиазидоподобные мочегонные, влияющие на кортикальный отдел петли Генле, петлевые диуретики, действующие на всем протяжении восходящего отдела петли, и калийсберегающие. При гипертонической болезни применяют мочегонные, эффект которых развивается постепенно и носит продолжительный характер.
Механизм гипотензивного действия мочегонных средств в основном связан с выделением ионов натрия и воды из организма и уменьшением объема циркулирующей крови. Кроме того, при длительном применении происходит постепенное вымывание ионов натрия из сосудистой стенки и снижается ее чувствительность к катехоламинам. Тиазидные мочегонные — гидрохлоротиазид (дихлотиазид), циклопентиазид (циклометиазид) и тиазидоподобные — клопамид (бринальдикс) действуют в переходной части кортикального отдела восходящей петли Генле и начального отрезка дистального, а также частично влияют на проксимальный каналец. Они выводят ионы натрия, хлора, калия, магния и НСОз, но увеличивают в плазме крови содержание ионов кальция и мочевой кислоты.
Индапамид (арифон) — диуретик, применяемый в основном при гипертонической болезни. Действует в кортикальном сегменте восходящей петли Генле и дистального канальца, частично в проксимальном. Накапливается в стенке сосудов, уменьшает содержание в ней свободного кальция, расслабляя ее. Арифон снижает чувствительность сосудистой стенки к катехоламинам, увеличивает количество простациклина, который, в свою очередь, способствует дилатации и обладает антиагрегационной активностью; оказывает длительное гипотензивное действие.
Петлевые диуретики — фуросемид (лазикс), кислота этакриновая (урегит) являются наиболее сильными мочегонными средствами. Механизм их действия связан с угнетением реабсорбции ионов на всем протяжении восходящего отдела петли Генле. Фуросемид выводит ионы натрия, хлора, калия, кальция, магния, но снижает экскрецию мочевой кислоты. Он расширяет сосуды и увеличивает почечный кровоток, повышая синтез сосудорасширяющих простагландинов, обладает антиагрегационной активностью (за счет простациклина). Применяется при отеке мозга и легких, сердечной недостаточности, для купирования гипертонических кризов, реже — для терапии гипертонической болезни.
Осложнения: гипокалиемия (необходимо назначать диету, богатую калием); задержка выделения мочевой кислоты (может вызвать обострение подагры); гипергликемия (возможно обострение сахарного диабета); негативное влияние на липидный обмен. Эти эффекты характерны для многих салуретиков. При применении фуросемида может также возникнуть обратимое снижение слуха.
Спиронолактон (верошпирон) — антагонист альдостерона, стероидный калийсберегающий диуретик. Являясь конкурентным антагонистом альдостерона, устраняет его влияние на синтез белков-переносчиков (пермеаз), принимающих участие в реабсорбции натрия в дистальных канальцах. В результате экскреция ионов натрия увеличивается, но уменьшается выделение калия и мочевины. Эффект развивается постепенно через 4-5 дней и проявляется при достаточно высоком уровне альдостерона. Применяют спиронолактон при отеках, связанных с сердечной недостаточностью, при гипокалиемии, циррозе печени, гипертонической болезни. Его часто комбинируют с другими диуретиками (фуросемид, тиазидные мочегонные).
Осложнения: тошнота, сонливость, обратимая форма гинекомастии, иногда — гиперкалиемия.
Назначают внутрь, под кожу, внутримышечно и внутривенно.
Выпускается в таблетках по 0,000075 и 0,00015 г; в ампулах по 1 мл 0,01% раствора.
Выпускается в таблетках по 0,0001 и 0,00025 г.
Назначают внутрь и внутривенно.
Выпускается в таблетках по 0,01 и 0,04 г; в ампулах по 1 мл 0,25% раствора.
Выпускается в таблетках по 0,025 и 0,1 г.
Назначают внутримышечно и внутривенно.
Выпускается в ампулах по 5, 10 и 20 мл 20% и 25% раствора.
Назначают внутрь, внутримышечно и внутривенно.
Выпускается в таблетках по 0,02; 0,002; 0,003 и 0,004 r; в ампулах по 1,2 и 5 мл 0,5% или 1% раствора.
Назначают внутрь. Выпускается в таблетках по 0,025; 0,05 и 0,1 г.
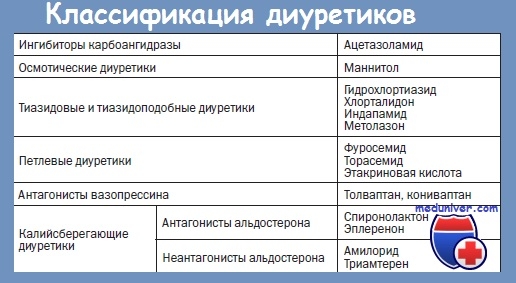
Мочегонные средства (иначе диуретики) – группа различных по структуре веществ, основное действие которых направлено на увеличение объема выводимой жидкости. Мочегонные препараты применяются в комплексной терапии гипертонической болезни и других патологий сердечно-сосудистой системы, заболеваний печени и почек, других нарушений и состояний, сопровождающихся отечностью тканей и органов. Мы поможем разобраться в сложной классификации лекарств и подобрать хорошее мочегонное средство.
По происхождению различают природные средства с диуретическим действием (растительные отвары, некоторые продукты, напитки) и лекарственные мочегонные препараты, которые в зависимости от структуры и механизма действия классифицирую на пять групп: петлевые, тиазидные, калийсберегающие, ингибиторы карбоангидразы и осмотические. Последняя группа препаратов – самые сильные мочегонные средства, которые применяются только в стационарах, вводятся внутривенно при различных острых состояниях, угрожающих жизни пациента.
Петлевые мочегонные средства
- хроническая сердечная недостаточность;
- любая степень хронической почечной недостаточности;
- нефротический синдром;
- цирроз печени, сопровождающийся отечностью, асцитом (скоплением жидкости в брюшной полости).
Петлевые мочегонные средства при отеках лица, ног, рук и других частей тела назначают по 5–20 мг в сутки до устранения отечности (но не дольше 3 дней). Повторный прием при хронических отеках допускается после перерыва, который должен длиться не менее 2–4 недель.
Петлевые мочегонные выпускаются в таблетках и растворах для инъекционного введения, что позволяет выбрать оптимальный для конкретного случая способ применения (внутривенное введение проводится только при тяжелом состоянии пациента). Отличаются быстрым наступлением терапевтического эффекта – действие развивается через 30–90 минут после приема, продолжается от 2 до 6 часов. Препараты уменьшают отеки, снижают объем внеклеточной жидкости, положительно воздействуют на функцию дыхания, уменьшая одышку.
Сильные мочегонные принимаются однократно или короткими курсами, с перерывами, не подходят для продолжительного лечения. При ежедневном применении петлевых диуретиков развивается привыкание и ослабление их терапевтического действия. Петлевые мочегонные средства характеризуются мощным, но коротким по продолжительности действием, поэтому подходят только для купирования гипертонического криза, но не для лечения гипертонической болезни.
Еще один существенный недостаток – выведение вместе с жидкостью ионов натрия и калия, приводящее к нарушению водно-электролитного баланса, развитию тяжелых побочных реакций (сильное снижение давления, судороги, энцефалопатия, аритмия, нарушение слуха вплоть до глухоты при внутривенном введении, прочие).
Мочегонное при отеках мозга — Мочегонные средства, Мочегонные препараты
Отечность — нарушение вывода жидкости из-за неправильной работы органа. Отек мозга является одним из самых опасных и непредсказуемых видов нарушения оттока влаги. Первый шаг в лечении — назначение соответственных диуретических препаратов. Именно от своевременного начала применения мочегонных препаратов при отеке мозга зависит дальнейшее выздоровление.
Причины отека мозга
Для головного мозга характерно увеличенное кровоснабжение. По этой причине нарушить циркуляцию крови может малейшая травма головы или болезнь. К возможным причинам относят:
- новообразования, находящиеся в головном мозге;
- черепно-мозговые травмы;
- воспалительные процессы в мозгу;
- последствия операционных вмешательств;
- отравление тяжелыми веществами;
- гематомы, находящиеся внутри черепа.
Таким образом, привести к отеку мозга способны практически любые заболевания, которые не были своевременно диагностированы. Для туристов и путешественников опасными являются резкие перепады высоты и, соответственно, атмосферного давления. На вероятность получить осложнение в виде отека мозга влияют также пол, возраст и общее состояние организма человека.
Целесообразность использования мочегонных средств для мозга
Отек головного мозга является серьезным осложнением, какой угрожает всему организму. Эффективность лечения напрямую зависит от своевременного снятия отечности. Быстрый результат можно получить, если применять мочегонное средство групп осмодиуретик и салуретик. Лекарства этих категорий препаратов характеризуется быстрым эффектом, поэтому применять их разрешено лишь под контролем лечащего врача. В случае, если при отеке не применять диуретики, возможны негативные последствия для здоровья, вплоть до летальных исходов.
Мочегонные средства при отеках мозга играют важную роль. Так, именно они помогают быстро вывести лишнюю жидкость и предотвратить необратимые последствия для здоровья. На сегодняшний день применяют осмодиуретики и салуретики. Осмотическое мочегонное средство усиливает давление плазмы крови и, тем самым, повышает поступление в кровь жидкости из тканей. Вместе с влагой диуретические препараты выводят соли натрия, при этом полезный калий остается в организме. Салуретики провоцируют образование увеличенного количества мочи, вместе с которой из организма выходят и вредные соли. Данные мочегонные препараты также добавляют результат и длительность действия осмодиуретиков.
Первые признаки опухоли головного мозга легко спутать с симптомами других, менее опасных заболеваний. Поэтому и пропустить начало развития онкологии мозга очень легко. Рассказываем, как этого не допустить.

В России ежегодно выявляют около 34 000 случаев опухоли головного мозга. Как и прочие заболевания, оно молодеет. Дело в том, что первые признаки опухоли головного мозга напоминают усталость, депрессию и тревожные расстройства. А при жалобах на головную боль, бессонницу и потерю внимания обычно советуют взять отпуск, а не сделать МРТ, особенно в молодом возрасте. Именно поэтому так легко пропустить начало болезни.
Первые симптомы новообразований
Первые признаки болезни не дают чёткой картины — очень уж сильно они схожи с симптомами многих других заболеваний:
- тошнота. Она будет присутствовать независимо от того, когда вы последний раз принимали пищу. И, в отличие от отравления, самочувствие после рвоты не улучшится;
- сильная головная боль, усиливающаяся при движении и ослабевающая в вертикальном положении;
- судороги и эпилептические припадки;
- нарушение внимания и ослабление памяти.
О наличии опухоли говорит совокупность этих симптомов. Конечно, есть вероятность, что они появятся по другим причинам независимо друг от друга, но встречается такое достаточно редко.
Именно на этой стадии вылечить опухоль проще всего. Но, к сожалению, редко кто принимает подобные симптомы всерьёз.
Первые общемозговые симптомы опухоли
Когда наступает вторая стадия развития заболевания, возбуждаются мозговые оболочки и повышается внутричерепное давление. В результате наступают общемозговые изменения.
Опухоль давит на мозг, влияя на его работу.
В это время лечение ещё успешно, но проходит дольше и сложнее. Симптомы второй стадии уже не так легко спутать с симптомами других болезней:
- теряется чувствительность на отдельных участках тела;
- случаются внезапные головокружения;
- ослабевают мышцы, чаще на одной стороне тела;
- наваливается сильная усталость и сонливость;
- двоится в глазах.
Вместе с тем, общее самочувствие портиться, продолжается утренняя тошнота. Всё это проявляется у больного независимо от того, в какой части мозга находится новообразование.
Однако, спутать симптомы всё-таки можно — они примерно такие же, как и при эпилепсии, нейропатии или гипотонии. Так что если вы обнаружили у себя эти симптомы, не спешите впадать в панику. Но к врачу обязательно сходите — неизвестность ещё никому не шла на пользу. Да и с такими симптомами не стоит шутить.
Очаговые признаки опухолей на ранних стадиях
Если общемозговые симптомы проявляются из-за поражения всего головного мозга и влияют на самочувствие всего организма, то очаговые зависят от участка поражения. Каждый отдел мозга отвечает за свои функции. В зависимости от местонахождения опухоли поражаются различные отделы. А значит и симптомы болезни могут быть разными:
- нарушение чувствительности и онемение отдельных участков тела;
- частичная или полная потерей слуха или зрения;
- ухудшение памяти, спутанность сознания;
- изменение интеллекта и самосознания;
- спутанность речи;
- нарушение гормонального фона;
- частая смена настроения;
- галлюцинации, раздражительность и агрессия.
Симптомы могут подказать, в какой части мозга располагается опухоль. Так, параличи и судороги характерны для поражения лобных долей, потеря зрения и галлюцинации — затылочных. Поражённый мозжечок приведёт к расстройству мелкой моторики и координации, а опухоль в височной доле приведёт к утрате слуха, потере памяти и эпилепсии.
Диагностика при подозрении на опухоль головного мозга
На наличие опухоли могут косвенно указывать даже общий или биохимический анализ крови. Однако, если есть подозрения на новообразование, назначают более точные анализы и исследования:
- электроэнцефалография покажет наличие опухолей и очагов судорожной активности коры мозга;
- МРТ головного мозга покажет очаги воспаления, состояние сосудов и самые мелкие структурные изменения головного мозга;
- КТ головного мозга, особенно с применением контрастной жидкости, поможет определить границы поражения;
- анализ ликвора — жидкости из желудочков мозга — покажет количество белка, состав клеток и кислотность;
- исследование спинномозговой жидкости на наличие раковых клеток;
- биопсия опухоли поможет понять, доброкачественное это или злокачественное новообразование.
Когда бить тревогу?
Так как первые признаки опухоли головного мозга могут встречаться даже для относительно здоровых людей, следует отнестись к ним разумно: не игнорировать, но и не паниковать раньше времени. К врачу следует обратиться в любом случае, но особенно важно это сделать, если у вас:
- есть все ранние симптомы новообразования (усталость, головная боль и т. д.);
- была черепно-мозговая травма или инсульт;
- отягощённая наследственность: некоторые родственники страдали от онкологических заболеваний.
В ходе осмотра, любой врач может направить вас к неврологу, заподозрив опухоль по косвенным признакам. Офтальмолог, проверяя внутричерепное давление, а эндокринолог — после анализа крови на гормоны. Внимательный врач обратит внимание даже на речь и координацию. Не игнорируйте такие советы: лучше посетить невролога и убедиться, что вы здоровы, чем пропустить развитие заболевания.
Отёк мозга возникает в результате скопления ликвора в мозговых тканях, что повышает внутричерепное давление. Запускается механизм отмирания клеток мозга. Заболевание характеризуется серьёзными последствиями и требует неотложной медицинской помощи.

Отёк головного мозга – болезнь, при которой затрудняется отток цереброспинальной жидкости. Это приводит к повышению внутричерепного давления и затруднению подачи крови к мозговым тканям. Развивается некроз. При отсутствии своевременного лечения патология вызывает смерть.
Характеристика понятия
У здорового человека ликвор циркулирует в межцеребральном мозговом пространстве, питая ткани и защищая их от повреждения. В результате воздействия отрицательных факторов повышается объём спинальной жидкости, что вызывает серьёзные нарушения и осложнения. Проявления отёка головного мозга быстро нарастают, состояние больного резко ухудшается.
Любопытный факт! Впервые болезнь описал Н. Пирогов в 1865 году.
Отёчность нарушает проницаемость сосудистых стенок, блокирует выход крови в окружающие тканевые структуры. В результате развития патологических процессов молекулы воды проникают через мембрану в нервные сплетения. Там клетки взаимодействуют с белками, увеличиваясь в объёмах.
Отёк мозга не может выступать самостоятельным заболеванием, патология развивается вторично в качестве осложнения иных болезней. Заболевание угрожает жизни человека, поскольку церебральные структуры сдавливаются в результате увеличения их объёма. Прогрессирование процесса приводит к защемлению мозговых структур, которые отвечают за терморегуляцию, дыхание, сердечную деятельность.
Классификация
Отёк головного мозга подробно охарактеризован международной классификацией заболеваний. Этот факт облегчает диагностирование патологии, что позволяет начать лечение своевременно.
Обратите внимание! Нужно различать отёки, которые развиваются вследствие различных заболеваний, с перифокальной отёчностью, когда набухание мозга происходит после полученных травм.
Отёки дифференцируют, исходя из этиологии нарушения:
- Вазогенный, вызывается увеличенной сосудистой проницаемостью. Центральная и кровеносная системы разделены анатомическим барьером – гематоэнцефалическим. Отёк развивается при прохождении экссудата через барьер. Это приводит к повышению объёмов белого вещества. Развивается в результате внутреннего кровоизлияния, повреждения центральной нервной системы, возникновения новообразований.
- Гидростатический. Образуется при повышении давления вентикулярного типа. В основном диагностируется у младенцев. У взрослых выявляется изредка, после хирургических вмешательств, черепно-мозговых травм, когда фиксируется вклинивание костных частей в мозговое вещество.
- Цитотоксический. Формируется вследствие интоксикации клеток головного мозга в результате облучения, отравления, а также после инсультов. Нарушается тканевый метаболизм. Остановить гибель клеток можно в первые часы прогрессирования патологии, затем процесс становится необратимым.
- Осмотический. Мозговая жидкость включает мельчайшие растворённые частицы, концентрация которых на килограмм ликвора носит название осмолярности. При нарушениях в соотношении частиц и плазмы мозга развивается отёчность. В результате повышения количества частиц в экссудате ткани пытаются снизить их объём, поглощая влагу из плазмы. Подобный дисбаланс возникает вследствие водного воздействия на мозг, гипергликемии, энцефалопатии.
Отдельно выделяют отёк мозга у новорождённых, который появляется вследствие внутриутробной гипоксии, неправильного развития эмбриона, полученных травм в процессе родоразрешения.
В зависимости от параметров мозгового поражения выделяют локальный, диффузный и генерализованный отёк. Дислокация локального вида фиксируется в очаге поражения, диффузного – в одном полушарии, генерализванного – в обоих полушариях.
Исходя из причины появления, отёк бывает токсическим, травматическим, гипертензивным, ишемическим, послеоперационным, опухолевым, воспалительным.
Отёчность может затрагивать мозговые сосуды, вещество либо ствол мозга. Последнее состояние наиболее опасно, поскольку оно сопровождается нарушением дыхания и кровоснабжения.
Что вызывает мозговую отёчность
Мозговые ткани отекают вследствие воздействия причин инфекционного либо травматического характера.
Травмы, раны с вклинением черепных частей, сотрясения блокируют эвакуацию жидкости, вызывая прогресс некротических процессов. Травматическое набухание осложняется повреждением мягких тканей. Это приводит к проблемам с передвижением, судорожным припадкам, парализации ног.
К этой группе относится отёчность, возникающая вследствие операций, трепанации черепа. После хирургического вмешательства в область головы зачастую образуется рубец, который затрудняет циркуляцию жидкости.
Отёк головного мозга возникает в результате острого воспалительного явления. Патологический симптом развивается на фоне менингита, энцефалита, токсоплазмоза. При образовании гнойных включений состояние человека резко ухудшается.
Раковые опухоли давят на мягкие ткани, вызывая раздражение и отёчность структур. После устранения образования отёк быстро спадает. Пациенту требуется длительное реабилитационное лечение.
Разрыв артериальных стенок происходит в результате наличия атеросклеротических бляшек, аневризмы, травмы головы. Подобное состояние имеет высокий процент летальности.
Ишемическая болезнь сердца возникает в результате образования тромба в артерии. Это провоцирует острую кислородную недостаточность и некроз тканей. Отмирание клеточных структур вызывает отёчность.
Отек мозга – угрожающее жизни состояние, возникающее при травмах головы, гидроцефалии и инсультах. Смещение мозговых тканей приводит к повреждению клеток (цитотоксическому фактору) или нарушению проницаемости мембран головного мозга (вазогенному фактору). Распространенными причинами являются инфаркты мозга, черепно-мозговая травма – бытовая или спортивная, более редкими – опухоли и менингиты.
Общие сведения
Отек головного мозга развивается на фоне ишемического или геморрагического инсульта, черепно-мозговых травм, повышает вероятность летального исхода. Состояния развивается из-за недостаточности мембранных транспортеров и гематоэнцефалического барьера. При развитии отека сочетаются цитотоксические, ионные и вазогенные механизмы. Для лечения используют декомпрессионную краниэктомию и осмотерапию. Но эти методы не влияют на патологический молекулярный каскад, приводящий к отеку.
Причины отека головного мозга
Отек головного мозга возникает на фоне различных неврологических и других патологических состояний:
- Энцефалиты из-за укуса клещей, в качестве осложнений после гриппа.
- Инфекционные факторы нейроцистицеркоз (паразитарное поражение головного мозга), церебральная малярия или менингиты.
- Инсульты ишемические, геморрагические и эмболические.
- Гидроцефалия, как последствие менингита или травм.
- Ишемическая энцефалопатия при родовых травмах, высоком артериальном давлении, атеросклерозе.
- Венозный тромбоз внутричерепных синусов.
- Опухоли головного мозга.
К заболеваниям, провоцирующим отек мозга, относится диабетический кетоацидоз, печеночная недостаточность, нарушения электролитного баланса. Симптомы отека мозга могут проявиться не сразу.
Церебральный отек у детей с гидроцефалией связан с увеличенным внутричерепным давлением.

Кто в группе риска
К группе высокого риска относятся люди с тяжелой формой диабетического кетоацидоза, а также дети, у которых ацидоз произошел впервые. Факторами, повышающими вероятность отека, являются: обезвоживание, воспалительный процесс и сгущение крови.
В результате снижается приток крови к головному мозгу, возникает каскад реакций ишемии и отека. Повышается внутричерепное давление, снижается артериальное давление и частота сердечных сокращений. Грыжа мозга может сжимать жизненно важные структуры в стволе мозга. Пациенты с гиперактивным течением кетоацидоза подвержены большему риску. Высокие уровни аммиака выше 200 мкмоль/л в крови могут быть индикатором риска развития внутричерепной гипертензии.
При гепатической энцефалопатии к церебральному отеку приводит снижение перфузионного давления сосудах мозга, отек клеток астроцитов из-за скопления аммиака и повышения выработки глутамина. На фоне отека растет внутричерепное давление, развивается ишемический ушиб и грыжа мозга.
Зачастую отек мозга развивается у детей, перенесших гипоксию, и имеющих гидроцефалию. Церебральная эдема может осложнять течение инсультов и черепно-мозговых травм.
Патогенез
Набухание головного мозга — это ступенчатый процесс, при котором острое повреждение приводит к образованию цитотоксического, ионного или вазогенного отека. Что такое отек? Это комбинация патогенетических механизмов. Цитотоксический отек характеризуется истощением внутриклеточного аденозинтрифосфата (АТФ), который нарушает активный транспорт осмолитов через клеточные мембраны. В клетках происходит накопление ионов натрия и воды.
На поверхности клеточных мембран нарушается давление и соотношение ионов, что приводит движению жидкости во внеклеточное пространство паренхимы мозга из сосудов. Этот механизм еще называется ионным. При ушибах мозга повышается активность ионного канала Sur1-Trpm4 в эндотелиальных клетках, что приводит к скоплению жидкости.
Отдельная форма цитотоксического отека – вазогенный. Патология развивается из-за повышенной проницаемости гематоэнцефалического барьера головного мозга после ушиба, выброса воспалительных веществ при инфекции и увеличения свободных радикалов. В результате происходит выделение жидкости вне клетки вместе с протеинами плазмы крови.

По мере развития ушиба мозга данные механизмы сменяют и дополняют друг друга, приводя к набуханию. Считается, что отеку предшествует повышение внутричерепного давления из-за фиксированного объема закрытой полости черепа. Одновременно снижается капиллярная перфузия – давление крови в сосудах мозга. Ткани недополучают питательные вещества и кислород, развивается гипоксемия.
Классификация
Отек головного мозга возникает из-за увеличенного содержания мозговой жидкости. В патогенезе развития эдемы условно разделяют три формы: цитотоксическую, вазогенную и интерстициальную или их комбинацию.
Вазогенный отек – наиболее распространенная форма, вызванная нарушением гематоэнцефалического барьера. Белки плазмы проникают за пределы сосудов, из-за чего осмотическое давление нагнетает жидкость в интерстициальное пространство головного мозга. Например, эндотелиальный фактор роста, глутамат и лейкотриены локально повышают проницаемость клеток вокруг опухоли. Именно это, наряду со слабостью сосудистых стенок, приводит к попаданию жидкости с белками в паренхиму белого вещества. Отеки возле опухолей в 65% приводят к когнитивным нарушениям у пациентов из-за смещения мозговых структур.
Вазогенный отек провоцируется нарушением проницаемости сосудов и изменением перфузионного давления на фоне следующих заболеваний и состояний:
- абсцесс мозга;
- инсульт;
- гиперкапния;
- энцефалопатия на фоне гипертонии;
- гепатическая энцефалопатия;
- метаболические нарушения;
- диабетический кетоацидоз;
- отравление свинцом;
- горная болезнь.
Патогенные микроорганизмы при менингитах нарушают проницаемость гематоэнцефалического барьера для белков и ионов натрия. Это приводит к накоплению жидкости в межклеточном пространстве, а также набуханию клеток из-за пассивной гипоксии. Повышенное внутричерепное давление нарушает связи между нейронами.
Клеточный или цитотоксический отек возникает внутри клеток без повреждения гематоэнцефалического барьера. Развивается патология после инсульта или черепно-мозговой травмы с повреждением глиальной ткани, нейронов и эндотелиальных клеток. В клетках нарушается гемостатический механизм, и натрий накапливается в них, нарушается выход ионов за пределы оболочки. Анионы стараются восстановить нейтральность на поверхности мембраны, что приводит к отеку внутри клетки.
Цитотоксический связан с изменением ионного баланса на поверхности клеточных мембран в результате нескольких причин:
- гипоксическая ишемическая травма головного мозга (при утоплении, остановке сердца);
- травма головного мозга;
- метаболические нарушения обмена органических кислот;
- гепатическая энцефалопатия;
- синдром Рея (острая печеночная недостаточность);
- инфекции (энцефалиты и менингиты);
- диабетический кетоацидоз;
- интоксикации (аспирином, этилен гликолем, метанолом);
- гипонатриемия или избыточное потребление воды без электролитов.
Одна из основных причин интерстициального отека – обструктивная гидроцефалия. Интерстициальный отек развивается из-за подтекания спинномозговой жидкости из желудочков мозга в интерстициальное пространство мозга. Пациенты с гидроцефалией или менингитом предрасположены к данной патологии. Увеличенное давление в желудочках приводит к вытеснению содержимого желудочков, что приводит к отеку белого вещества.
Симптомы отека головного мозга
Отек мозга в зависимости от степени изменений может быть бессимптомным или симптоматическим. Тяжесть проявлений зависит от возраста человека. У детей отек компенсируется наличием родничков, и потому симптоматика отличается.
Отек головного мозга имеет различные проявления:
- изменения сознания, в том числе кома;
- головные боли и мигрени;
- эпилепсия;
- интоксикация;
- кишечная непроходимость (заворот кишки, инвагинация)
- неврит зрительного нерва;
- гипертрофический пилоростеноз
- макроцефалия.
Общемозговые симптомы связаны с повышением внутричерепного давления:
- При медленном повышении пациентов беспокоят утренние головные боли, рвота без тошноты, что характерно для опухолей головного мозга. Возникают преходящие головокружения. Медленно меняется поведение: пациенты становятся раздражительными, капризными.
- При быстром повышении боль приступообразная, распирающая, сильная. Рвота не дает облегчения. У пациентов повышаются сухожильные рефлексы, замедляется сердцебиение и двигательные реакции. Меняются движения глаз, наступает сонливость, нарушается речь и мышление.
При декомпенсации повышенного внутричерепного давления развивается кома, а при смещении структур мозга – нарушение дыхания, сердечных сокращений.
Диагностика отека мозга
Ранняя диагностика отека мозга снижает смертность и улучшает функциональные возможности пациентов после ишемического инсульта. При установлении патологии проводят декомпрессионную трепанацию. Нарастание отека мозга можно определить по симптомам увеличения внутричерепного давления: учащения эпизодов потери сознания, тошноты и рвоты, головной боли, нарушению зрения, гемипарезу. Среди перечисленных признаков именно бессознательное состояние, связанное с поражением ретикулярной активирующей системы и таламо-гипоталамической-кортикальной оси, считается самым важным клиническим параметром. Степень поражения сознания измеряется по шкале комы Глазго.
При геморрагическом инсульте существуют другие критерии оценки риска отека мозга. Вероятность увеличения гематомы возрастает при изначальном значительном ее размере, использовании антикоагулянтов, раннем появлении симптомов. Риск развития отека увеличивается при гипергликемии, повышенном артериальном давлении, большом размере гематомы и увеличении перфузионного церебрального давления.

Отек и дислокация головного мозга при ишемии мозга 
КТ картина — отек головного мозга
Лечение отека головного мозга
Задача интенсивной терапии – поддерживать дыхание и нормальные показатели гемодинамики. Голова пациента находится на возвышении на высоте 30 градусов для оттока венозной крови. Начинают раннее энтеральное питание.
Применяются следующие методы терапии:
- искусственная вентиляция легких при симптомах дислокации мозга;
- гипервентиляция при условии мониторинга уровня насыщения кислородом крови;
- введение гиперосмолярных растворов;
- барбитуратовая кома;
- трепанация черепа;
- гипотермия (снижение температуры тела).
Протоколы терапии отека зависят от его причины. При вазоспазме важно увеличение объема плазмы крови, а при гиперемии – диуретики и гипервентиляция.
Осмотерапия – это базовая медикаментозной терапия при отеках головного мозга. Ее редко используют для профилактики из-за ограниченной эффективности из-за раннего применения. Гиперосмолярные средства создают внутрисосудистый осмотический градиент, который облегчает выведение воды. Чаще всего применяют маннитол и гипертонический физиологический раствор. Последний помогает расширить внутрисосудистый объем, увеличить сократимость сердца и внутричерепное давление.
Осмотический диурез с маннитом может вызвать внутрисосудистую дегидратацию и гипотензию, и после него необходимо обеспечить адекватную замену жидкости изотоническими растворами. Длительное повторное применение гипертонического физиологического раствора приведет к развитию гиперхлоремического метаболического ацидоза. Потому средства используют в качестве альтернативы для лечения симптоматического отека мозга.
Хирургическое вмешательство позволяет избежать летальных исходов при обширных полушарных инсультах. Особенно у пациентов в возрасте до 60 лет, если процедура проводится на протяжении 48 часов после появления симптомов. Декомпрессионная хирургия проводится на ранней стадии развития отека, удаляется костный диаметром не менее 12 см. После декомпрессии врачи следят за развитием субдурального кровоизлияния, наружной гидроцефалии, предотвращают инфицирование раны и расхождения кровеносных сосудов.
Хирургия применяется для удаления образования, которое вызывает отек мозга – внутримозговой гематомы, абсцесса или опухоли. Удалению подлежат гематомы в коре размерами более 3 см, а также в области мозжечка – более 2 см.
Лечение цитотоксического отека проводят с помощью маннитола или другого осмодиуретика. Маннитол используют в дозировке 0,5-1 г на килограмм массы тела внутривенно. Эффективность осмотических средств сохраняется первые 48-72 часов. При цитотоксическом отеке стараются не снижать артериальное давление, если сохранены механизмы ауторегуляции. Внутривенно вводят растворы для увеличения объема циркулирующей крови, проводят вазопрессорную терапию. Подход применяют при сохранении гематоэнцефалического барьера. Барбитуровый наркоз уменьшает отечность. Тиопентал натрия вводят для снижения внутричерепного давления ниже 20 мм рт. ст.
Вазогенный отек требует использования ангиопротекторных препаратов. Эсцинулизинат восстанавливает тонус сосудистых стенок, усиливает реабсорбцию и снижает интерстициальный отек. При вазогенных отеках используют глюкокортикоиды для снижения проницаемости гематоэнцефалического барьера. Обычно дексаметазон вводят одновременно с антибиотиками при менингитах. Маннитол при вазогенном отеке наоборот усиливает поступление жидкости в ткани. Для защиты паренхимы мозга применяют антиоксиданты и средства для улучшения метаболизма (актовегин, кортексин).
Прогноз
Отек мозга после инсульта у взрослых развивается под действием ряда факторов. К эпидемиологическим относится история гипертонии или ишемической болезни сердца в анамнезе. Важный клинический критерий — оценка по неврологической шкале NIHSS при инсульте выше 20 в доминирующем полушарии или более 15 в не доминирующем. Развитие тошноты и рвоты первые сутки после инсульта. Систолическое артериальное давление выше 180 мм рт.ст. первые 12 часов после приступа. Снижение реакций на раздражители.
Определить риск отека мозга можно по МРТ:
- окклюзия крупных артерий;
- поражение большого количества сосудов;
- аномалии Виллизиева круга.
- очаг инфаркта более 82 мл спустя 6 часов после появления симптомов;
- очаг более 145 ил спустя 14 часов после первых признаков.
При черепно-мозговых травмах еще до госпитализации важно приступить к нейропротекторной терапии, введению кортикостероиодов и диуретиков, что улучшает прогноз у молодых пациентов.
Какие варианты развития возможны
Зависимо от распространения отека выделяют три синдрома его развития:
- Общемозговой – связан с ростом внутричерепной гипертензии. Головная боль, рвота, нарушения зрения, снижение пульса на фоне роста САД и нарушение мышления.
- Синдром рострокаудального нарастания – распространение отека на кору, подкорковые структуры и ствол мозга. При повреждении коры появляются судороги, подкорковых областей – гиперкинезы, патологические рефлексы. Нарушение сознания означает повреждение гипоталамуса. Стволовые повреждения проявляются угнетением дыхания и сердечно-сосудистой деятельности.
- Синдром дислокации проявляется выпадением функции глазодвигательных нервов, ригидностью мышц затылка, нарушением глотания.
При вклинении ствола мозга в большое затылочное отверстие многие изменения необратимы.
Последствия отека мозга
Осложнения отека мозга связаны с присоединением инфекции в виде пневмонии, пиелонефритов и менингитов. Развиваются трофические нарушения, тромбозы.
Чем опасен отек? При компрессии ствола возможно развитие паралича. Даже после оптимального лечения и восстановления остаются спайки в мозговых оболочках, что приводит к депрессии, головным болями. Последствия отека головного мозга включают психические расстройства, снижение когнитивных функций.
Читайте также:

