Микрочип для выделения раковых клеток из крови

Обычно раковые клетки отделяются от первичного очага и перемещаются по организму через кровь. Обнаружить их порой бывает очень сложно из-за того, что среди миллиарда клеток крови может присутствовать всего одна раковая.
Существующие методы требуют большого количества соответствующих антител, которые связываются с раковыми клетками и помогают изолировать их. Для этого антитела должны быть известными. Другие методы отличаются сложностью. Использование высокоскоростных центрифуг для отделения клеток может также привести к повреждению клеток.
Звуковые волны, в свою очередь, работают быстро и с меньшими затратами. Около пяти часов нужно крошечному устройству, чтобы выделить раковые клетки из образца, взятого у обычного пациента.
Исследовательская команда из Университета штата Пенсильвания, Массачусетского технологического института и Университета Карнеги-Меллон протестировала устройство с образцами крови от трех пациентов с раком молочной железы. Испытания показали высокую эффективность нового метода.

Акустическое выделение клеток не является инвазивным, не изменяет и не повреждает клетки. Производительность системы в 20 раз превзошла все предыдущие достижения.
Поверхностные акустические волны отделяют клетки, затрачивая мизерное количество энергии. Они не оказывают никакого вреда, так как по своим характеристикам схожи с ультразвуковой акустоскопией. Они безопасны даже для ребенка в утробе матери.
Результаты исследования были опубликованы в американском журнале Proceedings of the National Academy of Sciences.
Система работает по принципу двух звуковых волн одинаковой длины, бегущих в противоположных направлениях и компенсирующих друг друга в определенной точке. Наклонные звуковые волны перемещают нужные клетки в точку, где формируется поток, который двигает собранные клетки по отдельному каналу.
В результате исследования было успешно отделено более 83 процентов раковых клеток. Ученые видят большие возможности новой методики в изучении, диагностике и лечении рака.

На сегодняшний день антидепрессанты для многих являются единственным способом борьбы с волнениями и стрессом. Несмотря на то, что разработка этих препаратов началась еще в 50-х годах прошлого века, ученые до сих пор точно не знают, как работают некоторые антидепрессанты. Но тот факт, что для многих людей они являются эффективными, не вызывает сомнений, иначе данные препараты […]

Как думаете, сахар – это наркотик? Этот вопрос обсуждается уже не первое десятилетие. Сахар щекочет наши дофаминовые рецепторы точно так же, как алкоголь, никотин и другие наркотики, вдохновляя систему вознаграждения нашего мозга. Ученым известно, что избыток сахара является виновником целого ряда опасных для жизни заболеваний. Но даже с учетом этого потребление сладкого во всем мире […]

Мы склонны думать, что только негативные изменения причиняют боль. Мы связываем боль с потерями, отказами и неудачами. Тем не менее, в нашей жизни случаются позитивные изменения, которые тоже приходят с долей страданий, что может показаться несколько неожиданным. Часто речь идет о выбранных изменениях, которые, вероятно, сделают нас лучше в долгосрочной перспективе, но они не лишены […]
Весной и итак наступают традиционные обострения психических процессов. А тут еще всемирная эпидемия наложилась, да карантин, так похожий на домашний арест. Общая ситуация, безусловно крайне стрессовая, поэтому не удивительно, что зацвели пышным цветом всевозможные теории заговоров.
А теперь следите за руками, как шла эта спецоперация. Вроде как в китайском Ухане был разработан синтетический адренохром, который был заражен коронавирусом. И если кто-то заражался, это означало, что он состоит в цепочке потребителей этого наркотика. И якобы так отслеживаются все, кто бывали на том тайном острове.
В общем, карантин - это прикрытие для самой масштабной и тайной операции разведки США . При чем тут тогда погибшие старики, врачи, и вообще случайно мимо проходившие люди по всему миру, которые заразились коронавирусом в тяжелой форме, непонятно.
Зато будет героически арестовано 158 тысяч человек, и все плохие люди исчезнут - телезвезды, политики, бизнесмены и прочие, кого верящие в эту теорию сочтут злодеями.
Уже составлен их список, неполный, конечно. Вот ознакомьтесь: Алек Болдуин, Андерсон Купер , Барак Обама , Бен Аффлек, Бейонсе, Билл Клинтон , Билл Мюррей, Чарли Шин, Кортни Лав, Дэми Мур , Гислейн Максвелл, Гвен Стефани , Джеймс Франко , Джеймс Ганн, Джим Керри , Джон Кьюсак, Джон Ледженд , Кэти Перри, Кевин Спейси, Линн Форестер Де Ротшильд , Мадонна Чиконе, Мэрил Стрип, Наоми Кэмпбелл, Опра Уинфри, Фаррел Уильямс, Квентин Тарантино , Роберт Дауни Младший, Сет Грин , Джей Зи, Леди Гага, Стивен Спилберг , Стивен Тайлер, Том Хэнкс, Уилл Смит, Уилл Феррел, Вуди Аллен.
Якобы они все должны быть следующими, кто заразится вирусом. Каждый день эта теория обрастает новыми домыслами, несмотря на многочисленные несуразности и противоречия.
Первая и главная нестыковка, конечно, что адренохром - это продукт окисления адреналина, не обладающий никакими наркотическими свойствами, о чем известно ещё с середины прошлого века.
Эта страшилка родилась еще в 2010 году и бродила тогда только в среде антипрививочников, но в связи с пандемией обрела новое, мощное дыхание.
Что реально движет Биллом Гейтсом, мы конечно, не знаем. Но что-то не тянет он на эко - Гитлера .
Они сразу вообразили, что это некий жидкий и невидимый чип, который будут встраивать в организм пациента во время забора анализа на вирус. И - все, после анализа человек станет чипирован, им можно будет управлять как роботом, запускать любые болезни в его организме по нажатию кнопки и всячески на него воздействовать. Так мир превратится в концлагерь, а карантин - это репетиция.
Надо бы, конечно, пояснить, что ДНК -микрочип - это название технологии, используемой в молекулярной биологии и медицине. Он представляет собой множество небольших одноцепочечных молекул, которые ковалентно пришиты к твёрдому основанию. ДНК-микрочипы давным-давно используются для определения ДНК или РНК при экспресс-анализах.
Одно хорошо в теориях заговоров - они заставляют действительно знающих врачей и ученых выступать в СМИ и объяснять максимально доступным языком сложные научные вещи. И из-за этого в целом мы становимся многократно умнее.
ТЕМ ВРЕМЕНЕМ
"В России нарушителей карантина скармливают львам": Пять самых нелепых фейков про коронавирус
Из-за мировой пандемии коронавируса в соцсетях плодятся тысячи фейковых новостей (подробности)

Американские ученые создали высокочувствительный микрочип для определения в крови так называемых циркулирующих опухолевых клеток (ЦОК) – мельчайших фрагментов, оторвавшихся от первичной раковой опухоли и попавших в кровоток, сообщает журнал Nature.
Новое устройство позволяет выявлять, изолировать и подсчитывать количество этих клеток, а также наблюдать за их динамикой в процессе лечения, утверждают исследователи из Массачусетской больницы (Massachusetts General Hospital) и Гарвардской медицинской школы (Harvard Medical School) в Бостоне.
ЦОК в крови могут приводить к развитию метастазов и выявляются при распространении раковой опухоли за пределы органа. Эти частицы являются хрупкими и редкими, и плохо определяются с помощью существующих методик. Технология, разработанная учеными под руководством Мехмета Тонера (Mehmet Toner), позволила многократно усилить чувствительность метода, сделав его пригодным для практического применения.
Устройство представляет собой силиконовый чип размером с пластиковую карточку, на поверхность которого нанесены антитела. Эти антитела способны распознавать белок, имеющийся в большинстве раковых опухолей. При движении крови вдоль чипа, его поверхность притягивает имеющиеся в ней опухолевые клетки наподобие клея. По словам исследователей, микрочип может обнаруживать тысячу опухолевых клеток в 60 миллиардах клеток крови, содержащихся в 8 мл пробирке с кровью. Ранее ученым удавалось обнаружить не более пяти опухолевых клеток.
Новое устройство было протестировано на образцах крови 68 пациентов с метастазами рака легких, простаты, груди, поджелудочной железы или толстой кишки. По словам ученых, им удалось обнаружить ЦОК в 115 из 116 исследованных образцов. У здоровых людей эти клетки не выявлялись.
Более того, тест оказался достаточно чувствительным для того, чтобы обнаружить изменения уровня ЦОК в процессе лечения. Уменьшение размеров опухоли, по данным компьютерной томографии, сопровождалось снижением уровня ЦОК, сообщил Тонер.
По мнению ученых, новая технология может использоваться для контроля эффективности лечения. Кроме того, она может найти применение в диагностических целях.
NAME] => URL исходной статьи [

Американские ученые создали высокочувствительный микрочип для определения в крови так называемых циркулирующих опухолевых клеток (ЦОК) – мельчайших фрагментов, оторвавшихся от первичной раковой опухоли и попавших в кровоток, сообщает журнал Nature.
Новое устройство позволяет выявлять, изолировать и подсчитывать количество этих клеток, а также наблюдать за их динамикой в процессе лечения, утверждают исследователи из Массачусетской больницы (Massachusetts General Hospital) и Гарвардской медицинской школы (Harvard Medical School) в Бостоне.
ЦОК в крови могут приводить к развитию метастазов и выявляются при распространении раковой опухоли за пределы органа. Эти частицы являются хрупкими и редкими, и плохо определяются с помощью существующих методик. Технология, разработанная учеными под руководством Мехмета Тонера (Mehmet Toner), позволила многократно усилить чувствительность метода, сделав его пригодным для практического применения.
Устройство представляет собой силиконовый чип размером с пластиковую карточку, на поверхность которого нанесены антитела. Эти антитела способны распознавать белок, имеющийся в большинстве раковых опухолей. При движении крови вдоль чипа, его поверхность притягивает имеющиеся в ней опухолевые клетки наподобие клея. По словам исследователей, микрочип может обнаруживать тысячу опухолевых клеток в 60 миллиардах клеток крови, содержащихся в 8 мл пробирке с кровью. Ранее ученым удавалось обнаружить не более пяти опухолевых клеток.
Новое устройство было протестировано на образцах крови 68 пациентов с метастазами рака легких, простаты, груди, поджелудочной железы или толстой кишки. По словам ученых, им удалось обнаружить ЦОК в 115 из 116 исследованных образцов. У здоровых людей эти клетки не выявлялись.
Более того, тест оказался достаточно чувствительным для того, чтобы обнаружить изменения уровня ЦОК в процессе лечения. Уменьшение размеров опухоли, по данным компьютерной томографии, сопровождалось снижением уровня ЦОК, сообщил Тонер.
По мнению ученых, новая технология может использоваться для контроля эффективности лечения. Кроме того, она может найти применение в диагностических целях.
Российские ученые из МФТИ и еще нескольких академических институтов создали чип, который позволяет с высокой точностью определять один из самых распространенных раков - колоректальный (так называют злокачественные опухоли толстой и прямой кишки).
ЧТО АМЕРИКАНЦАМ ЗАПРОСТО.
Крайне важно, что новый тест очень прост, кровь для него берут из вены точно так же, как для обычного так называемого биохимического анализа. Поэтому он будет хорошо подходить для скрининга - быстрого и простого отбора пациентов даже с ранними формами рака. Сейчас в мире для этого рекомендуют колоноскопию, которую после 50 лет нужно проводить не реже одного раза в десятилетие. Это совсем непростая и не очень приятная процедура, при которой гибкий эндоскоп вводят через прямую кишку в толстый кишечник. В США это профилактическое исследование для людей старше пятидесяти поставлено на поток. Каждый эпизодически получает по почте приглашение на такую диагностическую процедуру.
У нас такое исследование проводят по показаниям, когда есть симптомы какого-либо заболевания толстого кишечника. Если же кто-то хочет просто провести такое профилактическое исследование, как это делают в США, чтобы не проморгать болезнь, это можно сделать на платной основе в индивидуальном порядке. Может быть, всем поголовно его и не стоит делать, но тем, у кого есть факторы риска развития колоректального рака, это исследование лишним не будет.
Почему ранняя диагностика рака толстой и прямой кишки так важна? Во-первых, это заболевание одно из самых распространенных - в развитых странах эта злокачественная опухоль стоит на 3-м месте среди всех видов рака. Во-вторых, болезнь весьма тяжелая и тяжело лечится. Несмотря на большие достижения в ее лечении, результаты далеко не самые лучшие: пятилетнее выживание после хорошей терапии бывает примерно у 60-65% пациентов. И в-третьих, если опухоль выловить на ранних стадиях, то результаты будут гораздо лучшими. Для этого и нужен скрининг. И лучше простой и не очень затруднительный, как колоноскопия.
НАУКА - ПРАКТИКЕ
Над поиском такой методики трудится немало ученых в мире. Например, в США недавно появился метод диагностики по сложному анализу стула. Но наши ученые предложили еще более удачное решение. Про-цедура исследования сведена к забору крови из вены, как это делают при биохимическом анализе крови. Российский биочип построен на совсем иных принципах, чем американский набор для диагностики. Хорошо известно, что в крови есть маркеры, которые могут свидетельствовать о наличии опухоли. Они тем или иным образом связаны с обменом веществ в злокачественных клетках и с ответом организма на опухоль. И таких маркеров много. Беда в том, что они весьма капризны: могут быть не только при колоректальном раке, но и при других опухолях и даже при иных состояниях. То есть их специфичность для данного вида рака не всегда достаточна для уверенной постановки диагноза. Наши ученые нашли выход из этой проблемы: они сделали комбинированный чип, который определяет сразу не один маркер, а много. Благодаря этому точность диагностики повысилась многократно.
Не будем приводить названия маркеров, которые определяются при использовании чипа. Для нас гораздо важнее чувствительность предложенного теста - она составляет 88%. То есть он определяет наличие опухоли у 88% больных из 100. Это очень хороший показатель.
Отчет об исследовании отечественного чипа опубликован на днях во влиятельном международном журнале Cancer Medicine, и есть все основания полагать, что скоро такая полезная диагностическая система поступит в практическое здравоохранение. И самое главное, по этому же принципу можно разработать диагностические чипы и для других видов рака.
Материал подготовил Олег Днепров
ФАКТОРЫ РИСКА КОЛОРЕКТАЛЬНОГО РАКА:
- наличие таких болезней, как дивертикулы толстой кишки и неспецифический язвенный колит (болезнь Крона);
- возраст старше 50 лет;
- наличие этой опухоли у кровных родственников;
- большое содержание жиров и мяса в питании;
- пристрастие к алкоголю;
- курение;
- сахарный диабет, ожирение, низкая физическая активность.
Алексей Ржевский с разработанным чипом
Ученые Сеченовского университета совместно с исследователями из Австралии разработали устройство на основе технологии микрофлюидики (микрогидродинамики), с помощью которого можно выделять раковые клетки из мочи пациентов с раком предстательной железы. Результаты исследования, показавшего чувствительность и специфичность этого метода в диагностике рака, были опубликованы в журнале Cancers.
Рак предстательной железы занимает второе место по распространенности среди мужчин, в 2018 году он был диагностирован у 1,27 млн человек, почти 360 тысяч заболевших умерли. Добиться значительного снижения смертности пока не удается из-за того, что не найдено достаточно точного и при этом практически применимого метода диагностики, позволяющего выявлять заболевание на ранней стадии.
Обычно для проверки этого диагноза используется анализ крови на простатический специфический антиген (ПСА, его уровень повышается при раке простаты и некоторых других состояниях) и тканевая биопсия – взятие образца тканей для исследования. Оба эти метода имеют существенные недостатки. Так, анализ крови на ПСА недостаточно специфичен и может давать ложноположительные результаты, в частности, при других заболеваниях предстательной железы. Тканевая биопсия сама по себе является высокоинвазивным вмешательством, которое создает риск развития инфекции, локальных кровотечений и других осложнений. Также, как показали предыдущие исследования, жидкая биопсия крови (выделение из нее раковых клеток) обладает достаточно низкой чувствительностью из-за того, что концентрация таких клеток в крови мала. Альтернативой может стать жидкая биопсия мочи. Наличие клеток рака предстательной железы в моче объясняется тем, что протоки предстательной железы анатомически связаны с уретрой, и раковые клетки пассивно выводятся в процессе мочеиспускания.
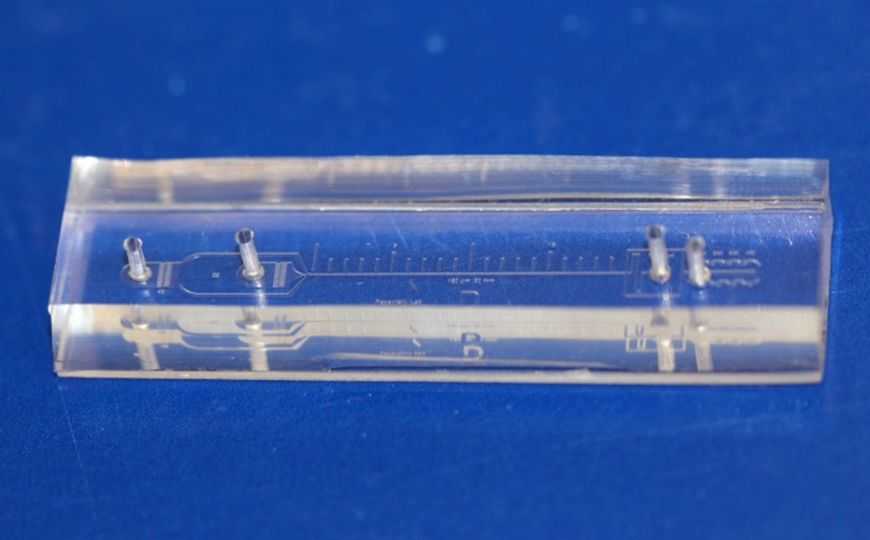
Чтобы выделять клетки из жидкости, ученые предложили использовать разработанный ими микрофлюидный чип. Он представляет собой форму, отлитую из полимера, с тонким раздвоенным на конце каналом в форме спирали и тремя отверстиями: одним для поступления образца мочи и двумя – для сортировки клеток. При этом чип сконструирован таким образом, чтобы при пропускании жидкости через канал крупные – раковые – клетки смещались к внутренней стенке спирали и выходили через внутреннее отверстие, а более мелкие и легкие клетки – к наружной стенке, и выходили через наружное отверстие. Такой эффект обеспечивается одновременным воздействием на клетки нескольких центробежных сил.
Собранные клетки окрашивали с помощью флуоресцирующих антител – молекул, способных присоединяться к определенному типу клеток и светиться при облучении светом определенной длины волны. Клетки опухоли с антителами исследовали с помощью флуоресцентного микроскопа, замеряя интенсивность свечения: если она превышала рассчитанный порог, ученые делали вывод, что клетки являлись онкологическими.
Авторы статьи опробовали работу устройства, используя физраствор с известным заранее количеством клеток (при проведении пилотных экспериментов), а также образцы мочи здоровых людей и пациентов с раком предстательной железы. Чип показал достаточно высокую улавливающую способность и специфичность – в пилотных экспериментах он успешно собирал от 80 до 90% раковых клеток. Положительные результаты дали и тесты с образцами мочи: верно определить наличие заболевания удалось у 12 из 14 пациентов с раком предстательной железы, а его отсутствие – у 11 из 14 здоровых добровольцев.
Разработка микрофлюидных платформ для захвата раковых клеток из кровотока — популярное направление современной диагностики. Изучение циркулирующих в крови опухолевых клеток способно помочь специалистам определить стадию опухоли, выбрать эффективную стратегию лечения и мониторинга пациента. Тем не менее достаточно эффективных устройств для подобного рода анализа до сих пор нет: раковых клеток в крови очень мало по сравнению с нормальными, и их трудно различать. Система CellSearch TM (Menarini Silicon Biosystems, Италия) — пока единственный одобренный FDA коммерческий продукт для подсчета циркулирующих раковых клеток. Однако его широкое применение в клинических условиях сдерживается высокой стоимостью, ручной обработкой данных и высокой частотой ложноположительных и ложноотрицательных результатов. Есть методы, основанные на распознавании поверхностных маркеров клеток, но они также дают много ложноотрицательных результатов.
Новая технология ученых из Университета Иллинойса (США) и Квинслендского технологического университета (Австралия), возможно, изменит ситуацию к лучшему. Принцип работы созданной ими микрофлюидной разделительной системы не требует сложной подготовки образца и основан на инерционной миграции клеток за счет различий в их размерах. В микроканал прибора вводят образец и буфер через два разных отверстия, благодаря чему в центральной части потока создается среда с чистым буферным раствором. Клетки под действием подъемной силы устремляются к боковым стенкам микроканала, а затем более крупные клетки (то есть раковые) перемещаются к центру под действием подъемной силы, создаваемой вращением. Таким образом, циркулирующие раковые клетки отделяют от лейкоцитов крови, выводя из прибора среднюю часть потока через особое отверстие.
Надежность нового метода исследователи сначала проверили на модельной системе — смеси лейкоцитов здоровых пациентов и частиц полистирола более крупного размера, изображающих раковые клетки. Эффективность разделения (отношение отобранных клеток-мишеней, то есть в данном случае частиц, к общему количеству клеток-мишеней) превысила 99,3%, чистота (отношение количества клеток-мишеней к общему количеству отобранных клеток) составила 88,7%, что намного выше, чем у других аналогичных приборов.
Затем прибор проверили на смеси раковых клеток, выращенных в культуре, и суспензии эритроцитов. В опыте с клеточной линией H460 даже для наименьшей клинически значимой концентрации — 10 клеток на 5 мл удалось обнаружить более 83% (для более высоких концентраций результат был еще лучше). Наконец, клиническую пригодность прибора продемонстрировали на образцах крови пациентов с немелкоклеточным раком легких. Микросистема обнаружила раковые клетки у 6 из 8 больных и ни одной — у 5 здоровых добровольцев.
По словам исследователей, полученные результаты уже можно назвать многообещающими, однако необходимы дополнительные тесты на большем количестве образцов. Есть также возможность еще ускорить получение результата. Авторы утверждают, что после некоторых доработок пациенты с онкологическими заболеваниями смогут рассчитывать на быструю, точную и доступную по цене диагностику.
В XXI в. станут известными основные гены-маркеры и белки-маркеры, превращающие нормальную клетку в раковую. По ним будет проводиться ранняя диагностика раковых клеток.
Ранняя диагностика рака – это диагностика его начала. Еще важнее диагностика рака до его начала.
Изменения в генах и эпимутации – это метки или маркеры раковых клеток. По ним отличают раковые клетки от нормальных.
В тканях организма часть раковых клеток погибает от апоптоза или некроза, а их мутантные и эпимутантные гены через лимфу попадают в кровь. За счет мозаичности капилляров опухоли, начиная с узелка раковых клеток в 1-2 мм в диаметре, часть раковых клеток из стенки сосуда легко попадает в кровь. Какие-то из клеток остаются живыми в крови, а другие погибают, но оставляют свой след – фрагменты генов с мутациями и эпимутациями.
Так как ДНК вне клеток в нормальных условиях нет, то обнаружение в плазме крови или других жидкостях от пациента – моча, слюна, слезная жидкость и др. генов-маркеров, равнозначно обнаружению их носителя, т.е. раковых клеток.
Кровь пациента – главный резервуар, куда попадает ДНК из раковых клеток разных тканей организма.
В XXI в. ДНК-чип по генам-маркерам позволит обнаруживать дефектные клетки конкретной болезни, в том числе и рака. За короткое время – часы, а не дни, это устройство позволит найти любые и все изменения в генах раковой клетки или клеток задолго до симптомов рака.
В предыдущем разделе мы обсуждали биочипы, здесь мы выделим цели ДНК-чипа.
Ген – это фрагмент молекулы ДНК из двух цепей нуклеотидов; основной частью нуклеотида является какое-то одно из четырех оснований: А, Т, Г, Ц.
Цепи нуклеотидов гена удерживаются вместе за счет комплементарности пар оснований: А с Т, Г с Ц. Их связывает друг с другом спонтанный процесс образования водородных связей между ними. Это явление – образования пар оснований, называется гибридизацией. На этом явлении основан принцип действия ДНК-чипа.
Для этого молекулы-пробы выделяют из раковой клетки или из образца плазмы крови от пациента. Их метят флуоресцентным красителем и с помощью робота вносят в ячейки чипа.
Молекулы-зонды на чипе способны вылавливать из молекул-проб только комплементарную себе молекулу, т.е. вторую цепь нуклеотидов определенного гена.
Но для обнаружения присутствия в организме раковой клетки или клеток в молекулах-зондах на чипе должны содержаться все возможные эпимутации и мутации определенного гена в дополнение к нормальной копии этого гена на чипе.
Впервые в практике явление гибридизации пар оснований применил Эд.
Для каких основных целей можно использовать ДНК-чип?
2. Для сравнения активности генов в нормальной клетке данного типа с активностью генов в раковой клетке этого типа. Это даст возможность выявить гены-причины раковой клетки.
3. Выяснять, зависят ли изменения генов раковой клетки – дефекты их или изменения их экспрессии, от типа клетка.
4. Определить, изменения каких генов и в чем встречаются в раковой клетке чаще других.
5. Контроль лечения рака и его излечения по исчезновению в плазме крови от пациента генов-маркеров раковой клетки.
1. Замена – это замена одной пары оснований в молекуле гена на другую. Пример: А-Т на Г-Ц.
2. Вставка – это дополнительная пара оснований или даже несколько их в ген. Пример: новая пара оснований А-Т в ген.
3. Делеция – выпадение одной или нескольких пар оснований в гене. Пример: Г-Ц в последовательности оснований где-то отсутствует.
Мутация в гене выразится в его продукте, т.е. в его белках – изменена последовательность аминокислот в белке. Если этот ген в норме регулирует деление клетки, то в случае мутации в этом гене такая клетка может стать раковой.
Раковая клетка может возникать из нормальной клетки не только от эпимутаций и мутаций в ряде генов, но и в результате чрезмерной активности гена. Это приводит к избытку в клетке числа копий этого гена, т.е. иРНК, а значит, нормального по строению, но избытка этого белка.
Пример: ген c-myc во многих типах клетки активирует РНК-полимеразу III типа в 12-15 раз по сравнению с обычной, и этим ведет к превращению нормальной клетки в раковую.
Как найти мутацию гена с помощью ДНК-чипа?
Для выявления в гене какого-либо вида мутации, в молекулы-зонды надо внести все виды мутаций этого гена во время синтеза молекул. После этого их размещают в ячейках ДНК-чипа.
Из клеток или здесь образца плазмы крови пациента готовится смесь ДНК-пробы. Каждую из них молекулу метят флуоресцентным красителем и роботом вносят в ячейки известного гена.
Если в ячейке произойдет гибридизация молекулы-зонда с молекулой- пробой, то лунка начнет светиться. Из этого будет вывод: в гене из образца плазмы есть эпимутация или мутация. А это означает, что в организме пациента есть раковая клетка или клетки.
Зная, какой ген в этой ячейке и какая в нем мутация или эпимутация, а также сравнив его с нормальной копией гена в контрольной ячейке на чипе, мы узнаем какой измененный ген в плазме крови пациента.
Измерение степени свечения в гелевой лунке укажет нам на титр мутантного или с эпимутацией гена в образце плазмы крови: чем меньше титр, тем меньше раковых клеток в организме пациента.
Как определить экспрессию гена с помощью ДНК-чипа?
Геном человека расшифрован и главная задача ученых – как можно скорее выяснить функции каждого гена в клетке каждого типа и для организма в целом.
Для определения активности гена в клетке, в лунках чипа фиксируются одноцепочные молекулы ДНК, т.е.
Известно, что активные гены синтезируют на своей матрице молекулы информационной РНК, т.е. иРНК. Затем эти молекулы используют для синтеза белков.
Роботом в ячейки чипа переносят молекулы-пробы, т.е. кДНК. Если молекула-зонд комплементарна кДНК, то между ними происходит гибридизация с образованием двухцепочного гена. Такая ячейка или ячейки на чипе начнут светиться. Чем больше степень свечения в гелевой ячейке, тем больше титр этого гена в плазме от пациента, а значит, больше раковых клеток.
Обнаружение раковой клетки или клеток в образце плазмы крови от пациента по маркерам: эпимутации и мутации генов или амплификация генов, да- ет возможность выявлять рак у пациента в самом его начале и даже до его начала, т.е. задолго до появления его симптомов. Низкий титр генов-маркеров в плазме крови пациента при анализе на ДНК-чипе должен означать минимальное количество предраковых и/или раковых клеток в его организме.
Превращение нормальной клетки любого типа в раковую после действия на нее какого-либо канцерогена. Но когда, и на какую клетку и где в организме человека подействовал канцероген или продукты окисления кислорода, что, может быть, чаще всего, нам всегда неизвестно.
Но при этом раковые клетки обладают одинаковыми зловещими свойствами вне зависимости от типа клетки и от класса канцерогена, вызвавшего ее образование. Это и заставляет думать, что раковая клетка любого типа может возникать от одних и тех же изменений в генах.
Если это подтвердится, тогда легче создать минимальный набор генов- маркеров, вызывающих превращение нормальной клетки любого типа в раковую клетку. Гены-маркеры разместят в качестве молекул-зондов в ячейках ДНК-чипа и фиксируют в них. В будущем каждый человек может носить на руке такой чип того же крохотного размера. Чип будет дополнен микросхемой для анализа его информации.
Читайте также:

