Миелоидный лейкоз и множественная миелома
Хотя появление острого миелоидного лейкоза (AML) после химиотерапии при множественной миеломе (ММ) распространено в клинических условиях, одновременное появление этих злокачественных новообразований у пациентов без предшествующего воздействия химиотерапии является редким событием. Этиология, управление болезнями и клиническое лечение остаются неясными для этого конкретного случая. Насколько нам известно, это исследование впервые сообщает о одновременном представлении AML и MM после воздействия ультрафиолетового облучения.
Мы сообщили о случае 73-летнего мужчины (этническая принадлежность ханьцев) без предыдущей истории болезни AML и MM. Морфология и иммунология клеток костного мозга подтвердили сосуществование AML и MM. Флуоресцентный анализ гибридизации на месте иммуномагнитно разделенных аномальных плазматических клеток показал аномальную экспрессию амплифицированных RB-1, TP53 и CDKN2C (1p32). Цитогенетический анализ продемонстрировал делецию Y-хромосомы.
После того, как пациент был введен с помощью бортезомиба в сочетании с цитрабином + акларубицином + гранулоцитарным колониестимулирующим фактором (режим CAG) и наблюдались явные лечебные эффекты. Пациент добился и поддерживал полную ремиссию более 6 месяцев. До появления заболевания пациент получил ультрафиолетовое облучение в течение 1 года и был обнаружен с аберрантной экспрессией гена RB-1, TP53 и CDKN2C (1p32). Тем не менее, корреляция этого явления с этиологией одновременного БОД с ММ остается неясной.
В этом исследовании обсуждался случай пациента с диагнозом AML, одновременно с ММ, у которого нет предшествующего воздействия химиотерапии. Этот пациент успешно лечился бортезомибом в сочетании с режимом CAG. Это исследование обеспечивает основу для руководства клинической терапии для этой конкретной группы пациентов и для подтверждения этиологии болезни.
В онлайн-версии этой статьи (doi: 10.1186 / s12885-015-1743-6) содержится дополнительный материал, доступный для авторизованных пользователей.
Связь острого миелоидного лейкоза (AML) с множественной миеломой (ММ) описывается как осложнение химиотерапии, но может также возникать в отсутствие этого лечения. Одновременное появление AML и MM у пациента без предварительного воздействия химиотерапии — редкое событие. В литературе до 2003 года сообщалось о девяти случаях этого явления в соответствии с Лука и Альманасиром [1]. Эти случаи AML, совпадающие с MM с 1989 по 2014 год, были получены из базы данных PUBMED 10.
Три из этих случаев приводили к одновременному появлению AML и MM при первом диагнозе, даже без предварительного воздействия химиотерапии [1, 3, 6]. Здесь мы сообщали случай одновременного появления AML и MM у пациента без предварительного воздействия химиотерапии. Это исследование было одобрено Комитетом по этике госпиталя Цилу университета Шаньдун. Форма информированного согласия была подписана пациентом.
73-летний мужчина без предыдущей медицинской истории купил ультрафиолетовый облучатель и получил ультрафиолетовое облучение на 1-2 часа в день в течение 1 года для поддержания здоровья и повышения иммунитета, поскольку он считал, что этот метод может способствовать местному кровообращению, тем самым принося пользу его физическое здоровье. (Этот метод является нетипичным в Китае.) Пациент не курил и не имел семейной истории рака. Он развил прогрессирующую усталость и головокружение в течение 6 месяцев и представил игольчатое подкожное кровоизлияние на обе нижние конечности в течение 1 недели. Результаты исследования показали бледность, иглообразное подкожное кровоизлияние, петехии, боль в груди и спленомегалия 1,5 см под ребрами. У пациента было количество белых кровяных телец 2,1 × 109 на литр, уровень гемоглобина 57 г / л, количество тромбоцитов 23 × 109 на литр и скорость седиментации эритроцитов 156 мм / ч. Мы провели обнаружение сывороточного М-белка с помощью теста электрофореза, и результат подтвердил наличие моноклонального иммуноглобулина M. Тест иммунофиксации сыворотки выявил моноклональную IgA / λ-полосу. Количественный анализ иммуноглобулина показал следующее содержание: IgG 9,22 г / л (NV 7,0-16 г / л); IgA, 14,4 г / л (NV 0,7-4 г / л); IgM 0,33 г / л (NV 0,4-2,3 г / л); IgE1 124,0 (NV 0-100 г / л), β2-MG, 3,09 мг / л (NV 0,7-1,8 мг / л); λ (лямбда), 4,62 г / л (NV 0,9-2,1 г / л); κ (каппа), 2,14 г / л (NV 1,7-3,1 г / л), без отношения сыворотки κ / λ, 0,46 (NV 1,35-2,65). В мазке аспирационных клеток костного мозга (BM) выявлено 45% клеток миелобласта (неэритроидных клеток, NEC) и около 17% высокоатипичных плазматических клеток (NEC), как показано на рисунках 1a и b соответственно. Рентгенологическое исследование не выявило аномальных изменений в кости пациента. На рентгенограмме не наблюдалось никаких других признаков. 1 Мазок аспирата костного мозга (BM) показал примитивные и незрелые мононуклеарные клетки (a: первоначальное увеличение × 100 под маслом) и аномальная морфология плазматических клеток (b: первоначальное увеличение × 100 под маслом). Биопсия BM trephine показала повышенную активность гиперплазии (70%), широко распространенные наивные клетки, большое клеточное тело, обильную цитоплазму и несколько нерегулярных ядер с видными ядрышками. Процент клеток плазмы увеличивался, и клетки характеризовались рассеянным или скопленным распределением особой формы с положительно окрашенными ретикулярными волокнами (c: первоначальное увеличение × 100 под маслом). d: проточная цитометрическая иммунофенотипирование аномальных плазматических клеток показала положительную экспрессию CD138, CD38, CD56 и λ и отрицательную экспрессию CD19 и CD45. e: Фенотипические характеристики злокачественных миоидных клеток показали сильную положительную экспрессию CD38, положительную экспрессию CD117, CD34, CD33, HLA-DR, CD56, CD13 и MPO и отрицательную экспрессию CD5, CD11, CD64, CD20 и CD70. f: экспрессия гена RB-1, IgH, TP53 и CDKN2C / CKS1B, о чем свидетельствуют результаты анализа FISN на иммуномагнитно разделенных аномальных плазматических клетках. Примечание: A-1, B-1, C-1 и D-1 для нормальных клеток костного мозга; A-2, B-2, C-2 и D-2 для клеток костного мозга пациента. Тестирование RB-1 (13q14) с использованием Vysis и монохромного меченого зонда показало нормальный сигнал 2R (A-1) и положительные характеристики сигнала 1R (A-2) (сигнал слияния, показывающий красный цвет). Тестирование IgH (14q32) с использованием Vysis и двухцветного отдельно помеченного зонда (сигнал: зеленый для 5′-IgH и красный для 3′-IgH) показал сигнал слияния с желтым или зелено-красным цветом, который представлял собой нормальную экспрессию IgH в B-1 и B-2. Тестирование TP53 (17p13) с использованием Vysis и монохромного меченого зонда показало нормальный сигнал 2R (C-1) и положительные характеристики сигнала 1R (C-2) (сигнал слияния, показывающий красный цвет). Тестирование CDKN2C (1p32) / CKS1B (1q21) с использованием Vysis и двухцветного отдельно помеченного зонда CKS1B / CDKN2C (сигнал: зеленый для CDKN2C и красный для CKS1B) показал нормальный сигнал 2R2G и характеристики в D-1 и положительный сигнал для 3R2G 1q21 и 2R1G делеция 1p32 в D-2
Результаты биопсии BM trephine показали повышенную активность гиперплазии (70%), широко распространенные наивные клетки, большое клеточное тело, обильную цитоплазму и несколько нерегулярных ядер с выраженными ядрышками. Процентная доля плазматической клетки увеличивалась, и эти клетки характеризовались рассеянным или скопленным распределением особой формы с положительно окрашенными ретикулярными волокнами (рис.1c).
Анализ флуоресцентной in-situ гибридизации (FISH) иммуномагнитно разделенных аномальных плазматических клеток показал аберрантную экспрессию амплифицированных RB-1, TP53 и CDKN2C (1p32) (фиг.1f). (примечание: В настоящей работе гибридизованные зонды теста FISH включали RB-1, TP53, Bcr / abL, PML / RARA, AML1 / ETO, MLL, FGFR1, CBFB, TET / AML, Bcl-2, MYC, CCND1 / IgH, из тех отрицательных биомаркеров не указали.) Иммунные маркеры миелоидных и плазматических клеток костного мозга или миелоидных клеток определяли проточной цитометрией. Результаты показали положительную экспрессию CD138 в клетках костного мозга, тогда как CD38, CD117, CD33, CD34, LHA-DR, CD15, CD56, CD7, CD17 и MPO были положительно экспрессированы в миелоидных клетках костного мозга.
Как показано на фиг.2, обычный цитогенетический анализ продемонстрировал делецию Y-хромосомы. 2Контроциальный цитогенетический анализ показал 45 ×, -y [6]
Онкозаболевания представляют серьезную угрозу, особенно те виды опухолей, которые имеют высокие показатели заболеваемости у населения. К таким патологиям относится и миеломная болезнь. В медицинской практике существуют другие названия, среди которых миеломатоз, ретикулоплазмоцитоз, генерализованная плазмоцитома.
Эту патологию относят к гемобластозам (рак крови) во время течения которых происходит увеличение концентрации плазмоцитов, вырабатывающих большое количество парапротеинов (патологических белков). Обычно онкопатология диагностируется у пожилых афроамериканцев.
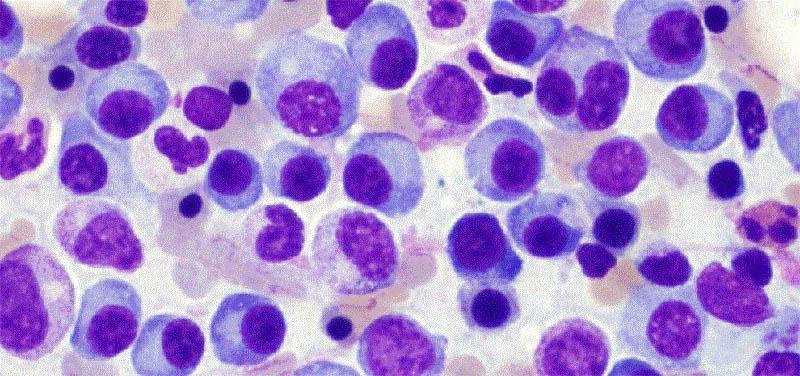
Что такое миеломная болезнь
Эта патология именуется как плазмоцитома или множественная миелома. Онкопатологию относят к хроническим миелобластным лейкозам с невысоким показателем злокачественности. Изначально, B-лимфоцит достигает уровня плазмоциты и обретает способность вырабатывать антитела против инфекций. В нормальном состоянии плазмоциты регулируют в организме иммуноглобулины, защищающие организм от проникновения и распространения вирусов. Патологические клетки не в состоянии обеспечивать защиту организма, что обусловлено внезапным снижением синтеза и стремительным разрушением здоровых антител. Под влиянием определенных факторов у больного начинают формироваться клетки, которые постоянно делятся и мутируют. Во время этого образуется большое количество плазмобластов и плазмоцитов в костном мозгу. Они синтезируют в больших объемах белки иммуноглобулина в крови, имеющие неправильное строение. Такие белковые соединения не утрачивают защитную способность, но всё больше скапливаются в костномозговых структурах.
Онкопатология обычно развивается медленно, разрушая костные структуры, но иногда может распространяться на лимфатические ткани, почки и селезенку. После образования миеломы до возникновения признаков болезни может пройти несколько десятилетий. При диагнозе множественная миелома, без адекватного лечения болезнь может привести к летальному исходу на протяжении двух лет.
Причины заболевания
Досконально изучить причины появления миеломной болезни ученым не удалось, но уже установлены факторы, способные спровоцировать развитие онкологического процесса:
- престарелый возраст,
- хронические заболевания крови,
- частые инфекционные заболевания,
- нефропатия (инфекции мочеполовой системы),
- длительное ионизирующее излучение,
- проживание в плохой экологической среде,
- работа, подразумевающая регулярный контакт с токсинами и химикатами,
- наследственность и генетическая предрасположенность к онкопроцессам,
- наличие вредных привычек, в частности курение и пристрастие к спиртным напиткам,
- регулярные стрессы и эмоциональные всплески.

Главным провоцирующим фактором считается нарушение B-лимфоцитов в плазмоциты во время трансформации по организму. Из-за такого сбоя начинает стремительно увеличивается число аномальных плазмоцитов, образующих миеломные клетки внутри костей. По мере течения болезни патологические клетки замещают нормальные, из-за чего постепенно кровь начинает плохо сворачиваться, а иммунитет ухудшаться.
Разновидности
Исходя из того, какой вид парапротеинов вырабатывают атипичные плазмоциты, миелома крови классифицируется на:
- A-миелома — диагностируется в 25% случаев,
- G-миелома — наиболее распространенная разновидность, выявляемая у 50% пациентов,
- M-миелома — встречается не более чем в 6% случаев патологии,
- E-миелома — данный вид болезни диагностируется у двух пациентов из ста,
- D-миелома — на данную разновидность приходится около 3% больных,
- Миелома Бенс-Джонса — на этот вид болезни приходится до двадцати процентов случаев,
- Несекретирующая опухоль — встречается крайне редко, не чаще чем у 1% пациентов.
Миеломы костного мозга G, A, M, E, и D продуцируют неправильные клетки иммунного глобулина типов IgG, IgA, IgE, IgD. Миелома Бенс-Джонса именуется так из-за выделения белка Бенс-Джонса. По большей части это теоретическое распределение миелом. На практике чаще используются классификации по локализации плазмоцитарных клеток и по их строению, а также особенностям опухоли. Исходя из количества затронутых патологией костей либо органов, выделяют одиночные и множественные миеломы.
Данный вид патологии характеризуется возникновением только одного очага, который способен формироваться в определенном лимфоузле или кости, где есть костный мозг. Часто локализуется в бедренных костях, однако может поражать позвоночник и другие трубчатые кости.
При появлении множественной формы опухолевые очаги появляются в нескольких костях. Поражению одинаково часто подвергается позвоночный ствол, черепные кости, ребра, лопатки и т.д. Кроме костей болезнь способна распространяться на селезенку и лимфоузлы.
Главным отличием такой онкопатологии является отсутствие ограниченных точек роста новообразований. Плазматические клетки стремительно делятся и расходятся по всем костям в теле. Внутри кости расположение плазмоцитов не ограничивается одним очагом, патологические клетки заполняют всю площадь костного мозга.
Болезнь отличается одновременным развитием опухолевых очагов со стремительным развитием плазмоцитов, а еще глобальной деформацией костномозговой структуры. Плазмоциты занимают только определенные участки, а остальные патологические изменения возникают из-за воздействия новообразования. При данной болезни плазмоциты могут находиться внутри костной ткани, поражать селезенку или лимфатические узлы.
Болезнь имеет черты как множественной, так и единичной миеломы. Диффузно-очаговая форма делится на несколько видов:
- плазмоцитарной,
- плазмобластной,
- полиморфноклеточной,
- мелкоклеточной.
Каждый подвид болезни отличается своими особенностями течения.
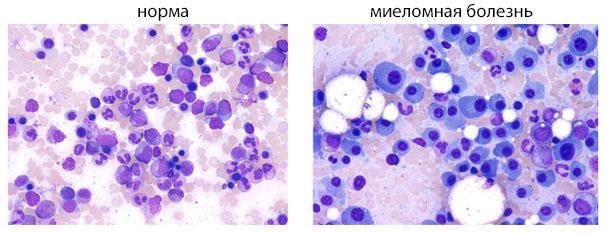
При такой онкопатологии появляется большое количество B-лимфоцитов в очагах роста новообразования, активно продуцирующих парапротеины. Развитие такой миеломы проходит медленно и зачастую вызывает трудности во время терапии. Иногда активная выработка парапротеинов становится причиной поражения важных для жизни органов и систем, которые нечувствительны к терапии.
При наличии злокачественной болезни в кости преобладают плазмобласты, которые синтезируют малое количество парапротеинов, но слишком быстро делятся и размножаются. При своевременном выявлении болезни она хорошо поддается терапии.
Эти виды миелом отличаются наличием в патологических очагах плазмоцитов, находящихся на разных стадиях созревания. Такие миеломы самые агрессивные, ведь очень быстро развиваются и вызывают дисфункцию многих отделов организма.
Стадии заболевания
Тяжесть онкопатологии зависит от этапа, на котором находится заболевание.
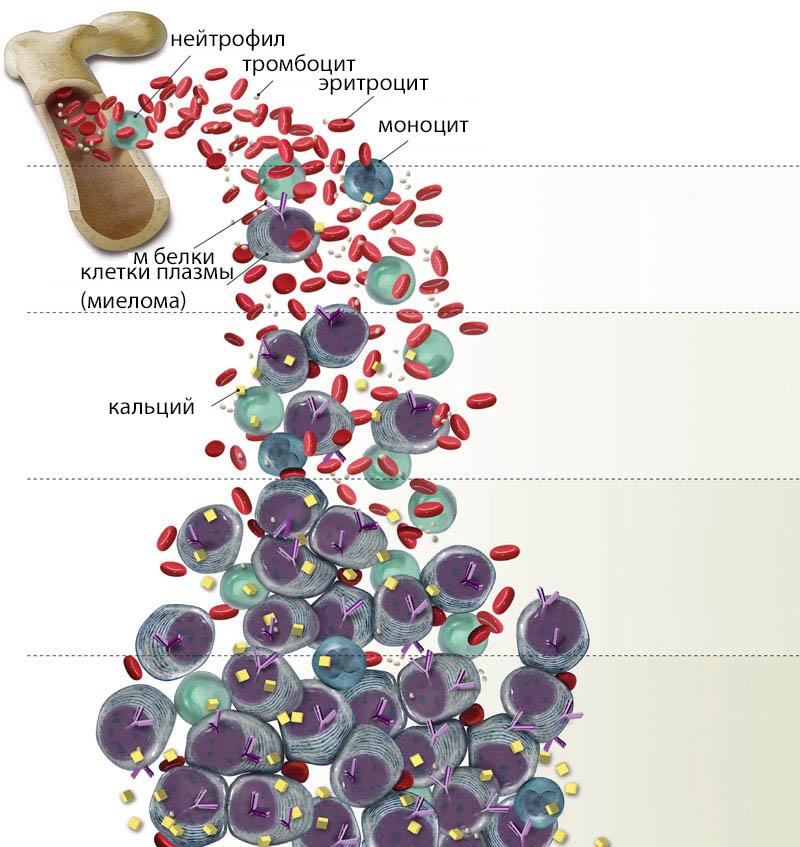
Стадий множественной миеломы всего существует три:
- При первой стадии общая масса опухолевого процесса не достигает одного килограмма, гемоглобин в крови равняется 100 г/л или выше. Данная стадия не вызывает симптомов, поэтому болезнь на этом этапе течения обнаруживают крайне редко.
- Вторая — вес опухолевой массы увеличивается до 1,2 кг. Возникают клинические проявления в виде понижения в организме железа, избытка кальция, почечной недостаточности и болевого синдрома.
- Третья — данная стадия характеризуется увеличением опухолевой массы свыше 1,2 кг и значительным изменением костномозговой структуры. Уровень гемоглобина опускается до 85 г/л, кальций падает до 12 мг/100 мл. Течение множественной миеломы 3 степени обычно заканчивается смертью больного. Основной причиной является инфаркт или почечная недостаточность.
Успех лечения в первую очередь зависит от фазы развития болезни, поэтому рекомендуется регулярно проходить полное медицинское обследование.
Симптомы болезни
При наличии миеломы в первую очередь происходит поражение костей и почек, из-за чего возникают нарушения в кроветворной системе. Симптомы миеломы зависят от стадии ее развития, а также степени поражения. Так как развитие болезни занимает очень много времени, бессимптомное ее течение может продолжаться около пятнадцати лет. В это время больной даже не будет подозревать о наличии серьезной патологии. Выявить миелому возможно посредством лабораторных исследований для профилактического обследования или лечения другой патологии.
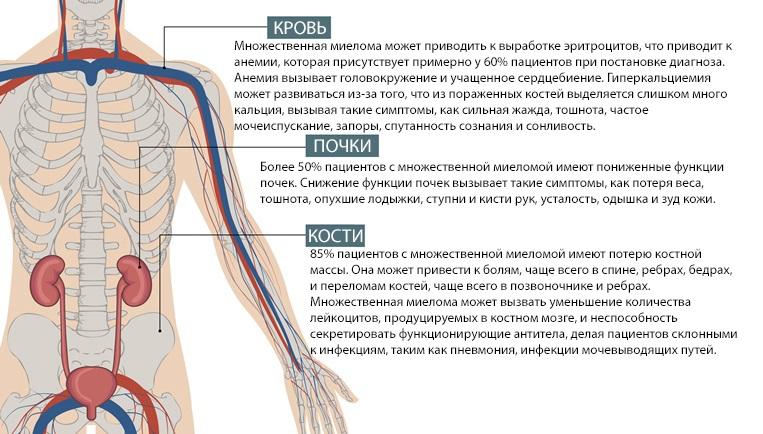
Симптомами миеломной болезни служат такие проявления:
- частые головокружения,
- развивается анемия,
- наличие болей,
- астения,
- стремительное уменьшение веса больного,
- постоянные ОРВИ и ОРЗ.
При появлении этих признаков миеломной болезни, стоит сразу отправиться за консультацией специалиста и пройти дополнительное обследование, для распознания патологии.
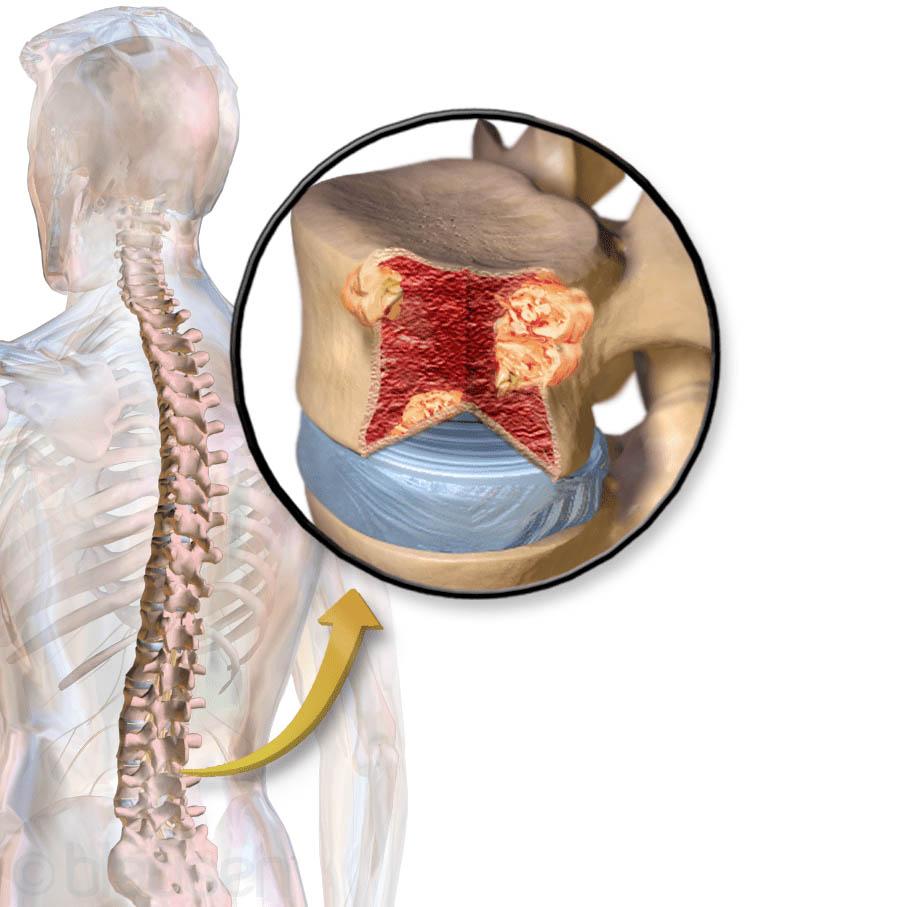
При обильном распространении множественной миеломы у пациентов очень часто наблюдается наличие таких синдромов:
Еще при развитии болезни поражается ЦНС и начинается гиперкальциемия, это только осложняет течение болезни. Когда патология переходит на заключающую стадию, клиническая симптоматика значительно усиливается. В некоторых случаях на четвертой стадии развивается острый лейкоз.
Диагностика
Если возникают подозрения на наличие миеломной болезни, диагностику проводит опытный врач в условиях стационара. В основном к врачу приходят пациенты, у которых анализ крови показал значительное повышение СОЭ, что характерно для миеломы. Во время постановки диагноза больным назначаются определенные лабораторные исследования, которые позволяют распознать болезнь еще на этапе ее формирования. Сначала врач проводит осмотр больного, а также уточняет период возникновения первых клинических признаков болезни, затем назначает анализы.
При миеломе диагностика проводится с помощью следующих исследований:
- общеклинический анализ мочи и крови (определяется повышение белка в моче),
- биохимический анализ крови,
- миелограмма,
- спиральная компьютерная томография,
- рентген костей,
- метод иммуноэлектрофореза.

Курс терапии назначается врачом только после проведения всех диагностических исследований.
Общие принципы терапии
Лечение миеломы не предусматривает применения радикальных методов, так как основной задачей курса терапии является продление и улучшение качества жизни. Вылечить полностью миелому невозможно. Однако в борьбе с опухолевым поражением можно затормозить его развитие и вызвать ремиссию.
После точного диагностирования миеломной болезни, лечение проводится с использованием паллиативных методов, позволяющих затормозить рост новообразования и ослабить признаки. К паллиативным способам лечения миеломы относится химическая терапия, облучение и подбор правильного питания. Проводить лечение народными средствами в домашних условиях не рекомендуется.
Применение химиотерапии — самый результативный метод борьбы с миеломой. Во время проведения курса лечения может использоваться как один препарат (монохимиотерапия), так и несколько медикаментозных средств (полихимиотерапия).
При назначении полихимиотерапии могут использоваться следующие препараты:
- Циклофаосфамид,
- Мелфан,
- Леналидомид,
- Дексаметазон.

Препараты принимают внутрь или внутривенно с помощью внутримышечных инъекций. Когда назначают курс химиотерапии, лечение может проводиться по одной из нескольких схем:
- Схема MP — прием препаратов мелфалан и преднизолон в таблетированном виде.
- Схема M2 — введение внутривенных инъекций винкристина, циклофосфамида и BCNU. Вместе с этим на протяжении двух недель необходимо принимать таблетки преднизолона и мелфалана.
- Схема VAD — терапия проводится в 3 сеанса. Во время первого сеанса лечение проводится лекарствами доксирубицин и винкристин. Во время следующих сеансов необходимо принимать таблетки дексаметазона.
- Схема VBMCP — назначается больным, возраст которых младше 50 лет. В первый день терапии пациентам внутривенно вводят винкристин, циклофосфамид и кармустин. Затем на протяжении недели необходимо пить мелфалан и преднизолон. Через полтора месяца им вновь вводят инъекцию кармустина.
При любой схеме лечения, прием препаратов осуществляется только под строгим наблюдением специалистов.

После лечения химиопрепаратами стойкая ремиссия наблюдается у 40% пациентов.
Применение лучевой терапии назначается обычно при солитарных и крупноочаговых опухолях, когда лечение химиопрепаратами бессильно. В таком случае удается затормозить развитие злокачественного образования и ослабить клинические проявления болезни.
Если облучение и применение химических препаратов не дали эффекта, пациентам проводят пересадку костного мозга. Примерно у 40% пациентов трансплантация стволовых клеток помогает достичь стойкой ремиссии болезни.
Этот способ лечения множественной миеломы предполагает прием назначенных лекарств. Их действие направлено на купирование болей, корректировку концентрации кальция в крови. Препараты нормализуют свертываемость крови и стабилизируют работу почек.
Иногда еще возможно проведение операции по удалению одиночного очага миеломы, над которым потом проводится цитологическое исследование. Если наблюдается тяжелое течение болезни, пациентам может быть назначено применение морфина, бупренорфина и других наркотических препаратов.

Во время лечения болезни обязательно нужно придерживаться правильного питания. Диету при миеломной болезни назначает лечащий специалист. В рационе следует ограничить употребление продуктов с большим содержанием белка. Больному нужно есть меньше мясных блюд, яиц, бобовых и орехов.
Прогноз и профилактика
Обычно при множественной миеломе прогноз неблагоприятный. Почти у всех пациентов удается достичь ремиссии на два или три года, в лучшем случае этот период можно увеличить еще на два года. Без адекватного лечения миеломы, продолжительность жизни пациентов составляет не более двух лет. Полное выздоровление возможно только в случае солитарной формы онкопатологии.
Специфических способов для профилактики образования миеломной опухоли нет. Людям, попадающим в зону риска заболеваемости, рекомендуется регулярно проходить профилактический осмотр, для своевременного обнаружения патологии. Стоит тщательно следить за своим здоровьем, вести активный образ жизни и избавиться от вредных привычек.
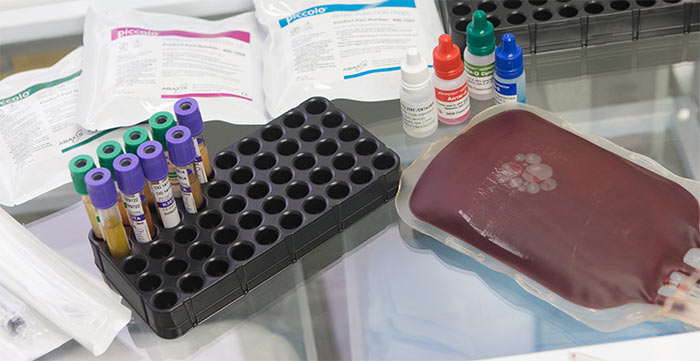
Множественная миелома — это злокачественная опухоль лимфоидной природы, для которой характерна триада признаков:
- Колонизация костного мозга опухолевыми плазматическими клетками.
- Возникновение очагов расплавления костной ткани (деструкция кости).
- Обнаружение в крови и/или моче специфического белка — моноклонального глобулина.
Основу миеломы составляют плазматические клетки (дифференцированные В-лимфоциты, плазмоциты). Они секретируют особый белок — моноклональный иммуноглобулин, он же М-белок, М-компонент, М-протеин, который негативно влияет на организм, приводя к развитию тяжелых симптомов. Кроме того, колонизация плазмоцитами костного мозга приводит к нарушению кроветворения и очаговому расплавлению костной ткани.
- Симптомы множественной миеломы
- Виды множественной миеломы
- Стадии и прогноз при множественной миеломе
- Причины множественной миеломы
- Диагностика множественной миеломы
- Как лечится множественная миелома
- Диета и питание при миеломе
Симптомы множественной миеломы
В начальных стадиях множественная миелома протекает бессимптомно. По мере увеличения количества опухолевых клеток, заболевание прогрессирует и могут развиваться следующие симптомы:

Виды множественной миеломы
Существует несколько классификаций миеломной болезни. По степени распространенности опухолевых поражений выделяют:
- Диффузная форма множественной миеломы. Происходит инфильтрация костного мозга без костных разрушений (остеодеструкции).
- Диффузно-очаговая форма миеломы. Помимо инфильтрации костного мозга имеются очаги деструкции костей.
- Множественно-очаговая форма миеломы. Есть очаги остеодеструкции, но нет диффузного поражения костного мозга. В этом случае при исследовании пунктата возможно получение нормальной миелограммы.
- Редкие формы миеломы — склеротическая, висцеральная и др.
Также множественная миелома классифицируется на основе иммунохимического типа опухоли. Основным фактором здесь является вид патологического иммуноглобулина, определяемого в крови и моче. Выделяют G, A, D, E, M-миелому, миелому Бенс-джонса, биклональную и несекретирующую.
Стадии и прогноз при множественной миеломе
Стадирование множественной миеломы определяется на основании 4-х параметров: количество М-компонента, уровень гемоглобина, уровень кальция, степень поражения костей. Стадии:
- 1 стадия миеломы – легкая анемия (гемоглобин более 100 г/л), кальций в норме, низкий М-белок, менее 5 очагов поражения костей. Средняя продолжительность жизни таких пациентов составляет 6,5 лет.
- 2 стадия миеломы – анемия средней степени тяжести, кальций повышен до 3 ммоль/л, количество очагов остеолизиса не превышает 20, уровень М-компонента: 35 IgG
Причины множественной миеломы
Причиной развития миеломной болезни являются мутации в клетках-предшественницах В-лимфоцитов. Что приводит к этим мутациям, до конца неизвестно. Но выделяют несколько факторов риска, при наличии которых вероятность развития заболевания превышает общепопуляционную:
- Возраст старше 40 лет.
- Мужской пол.
- Принадлежность к негроидной расе.
- Наличие моноклональной гаммапатии — у каждого сотого такого пациента развивается миелома.
- Вторичные иммунодефициты — ВИЧ, прием иммуносупрессивной терапии.
- Наличие миеломы среди близких кровных родственников.
- Наличие в анамнезе радиационного воздействия, в том числе лучевой терапии.
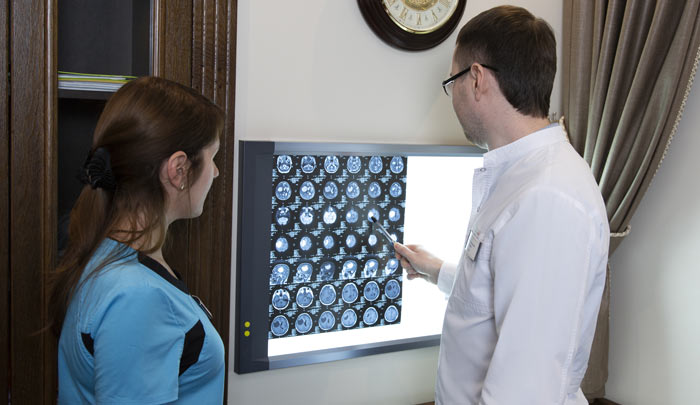
Диагностика множественной миеломы
Диагностика миеломы предполагает оценку жалоб пациента и проведение инструментальных методов диагностики:
- Лабораторные исследования — помимо рутинных анализов выполняется биопсия костного мозга и/или опухолевой ткани, определение β2-микроглобулина и др.
- Рентген костей или компьютерная томография костей для поиска очагов остеодеструкции.
- Иммунофенотипирование и цитогенетическое исследование опухолевых клеток для определения прогноза и составления плана лечения.
Диагноз множественной миеломы выставляется на основании следующих критериев:
- Уровень плазмоцитов в костном мозге или опухолевом биоптате превышает 10%.
- В крови и моче определяется М-белок (кроме несекретирующей формы множественной миеломы).
- Присутствуют признаки поражения внутренних органов миеломными клетками — гиперкальциемия, анемия, поражение костей, почечная недостаточность.
Как лечится множественная миелома
Множественная миелома сегодня считается неизлечимым заболеванием. Усилия медицины направлены на то, чтобы сдержать рост опухоли, продлить и улучшить качество жизни таких больных.
Выделяют следующие виды лечения миеломы:
- Стандартная химиотерапия. Назначается пациентам, которым противопоказана высокодозная полихимиотерапия. Средняя продолжительность жизни после нее 29 месяцев. В стандартную схему первой линии входит мелфалан и преднизолон. Более эффективные схемы включают талидомид, леналидомид или бортезомиб (относительно новые противоопухолевые препараты).
- Высокодозная полихимиотерапия (ВПХТ) с последующей пересадкой кроветворных стволовых клеток ТГСК (как аутологичных, так и донорских). Данное лечение позволяет достичь полной ремиссии у большинства пациентов (до 75%), но к сожалению, в течение 2-5 лет отмечается прогрессирование заболевания. Более эффективным является проведение двойного курса ВПХТ с ТГСК (тандемная ВПХТ). Она позволяет добиться пятилетней безрецидивной выживаемости у 90% пациентов. Но такое тяжелое лечение могут перенести не все пациенты, поэтому показания к нему ограничены.
- Поддерживающая терапия. Даже ВПХ не может предотвратить развитие рецидива, назначается лечение, которое призвано подавлять клон злокачественных клеток. С этой целью используются интерфероны. Они помогают продлить медиану безрецидивной выживаемости до 42 месяцев.
- Борьба с осложнениями. Лечение боли — назначение сильных аналгезирующих препаратов, лучевая терапия. Хирургические операции проводятся при компрессионных переломах позвонков. Коррекция осложнений, вызванных угнетением кроветворения — переливание эритромассы и назначение эритропоэтина, применение антибиотиков при повышении температуры. Проведение гемодиализа, плазмофереза, назначение бисфосфонатов для контроля гиперкальциемии.

Диета и питание при миеломе
Особой диеты при множественной миеломной болезни не требуется, за исключением периода прохождения химиотерапии. Учитывая то, что основным побочным эффектом такого лечения является потеря аппетита, тошнота и рвота, требуется легкое и, вместе с тем, калорийное сбалансированное питание. Более подробные рекомендации пациенту дает лечащий врач.
Читайте также:

