Метаболиты эстрогенов и рак молочной железы
Женщины, у которых диагностирован рак молочной железы (РМЖ), сталкиваются с большим количеством противоречивых рекомендаций, особенно если они находятся в пременопаузе. Их просят детально описать семейный анамнез для выяснения возможного характера генетической предрасположенности к РМЖ, обусловленного экспрессией гена BRCA1 или BRCA2, определяющих риск семейного РМЖ и рака яичников (РЯ).
Затем может быть рекомендовано генетическое консультирование и тестирование с целью более тщательного обследования пациентки и членов ее семьи на предмет возможных положительных эффектов и рисков профилактической мастэктомии и двусторонней аднексэктомии. Это ставит пациенток с выявленным в пременопаузе РМЖ в щепетильное положение, когда им предлагают выполнить двустороннюю овариэктомию с целью предотвращения РЯ, а затем сообщают, что им противопоказана ЗГТ эстрогенами или тестостероном по поводу симптомов постменопаузы, которые у них закономерно возникнут после этой операции. Это мнение высказывают онкологи.
Но его перевешивают личные пожелания пациентки об эмоциональном благополучии в тот момент, когда она сталкивается с угрожающим ее жизни заболеванием, новыми симптомами постменопаузы, нарушением половых функций и потенциальными проблемами с замужеством. Преимущества двусторонней аднексэктомии у носительниц мутаций гена BRCA1 или BRCA2 заключаются в возможности уменьшения риска рецидива РМЖ, а также снижении риска РЯ на 90 %. Если бы после операции возможен был контроль за симптомами постменопаузы, это было бы большим ее преимуществом. Однако недостаточность эстрогенов и андрогенов ведет к снижению либидо, увеличению сухости во влагалище, появлению приливов жара, бессонницы, депрессии.
Поэтому некоторые женщины считают, что положительные эффекты операции не оправдывают ее возможных рисков. Поэтому возраст, в котором следует планировать выполнение профилактической овариэктомии у носительниц генетических мутаций, не установлен и должен определяться индивидуально. Некоторые врачи на ограниченный период времени назначают инъекционный Depo-Lupron® (ТАР Pharmaceuticals Inc.), который вызывает обратимую менопаузу, что помогает пациентке принять решение.
Лечение рака молочной железы (РМЖ) включает тамоксифен, ингибиторы ароматазы, местную лучевую и химиотерапию (XT). Некоторые утверждают, что цель XT заключается в подавлении функции яичников. Овариэктомия могла бы заменить этот положительный эффект XT, но к настоящему времени не проведено адекватного научного сравнения этих двух методов. Кроме того, женщинам в постменопаузе можно назначать терапию ингибиторами ароматазы, о чем свидетельствует снижение частоты рецидивов РМЖ на 43 % через 5 лет применения тамоксифена.
Растет беспокойство в отношении показателей смертности в отдаленный период после проведения стандартной терапии рака молочной железы (РМЖ), которые недостаточно учитываются в клинических исследованиях. После XT у женщин снижаются когнитивные функции, повышается утомляемость, развивается остеопороз, увеличивается масса тела и нарушается половая функция. Требуются дальнейшие исследования для внедрения более эффективной симптоматической терапии, включающей препараты кальция и витаминные добавки, бисфосфонаты; необходимы также мониторинг плотности костной ткани и профилактика когнитивной и половой дисфункций.
Применение тамоксифена с целью профилактики рака молочной железы (РМЖ) сопровождается определенными осложнениями, включая тромбоэмболии, инсульты и рак эндометрия (РЭ). Прогнозируемый ежегодный показатель заболеваемости РЭ среди больных РМЖ составляет 1 случай на 1000 женщин. Для пациенток, принимающих тамоксифен, повышение риска составляет 2 случая на 1000 женщин, или общий риск 3 на 1000 в год. Исследования, целью которых было изучить целесообразность тщательного наблюдения за женщинами, принимающими тамоксифен, показали, что ежегодные трансвагинальное УЗИ и обязательная биопсия эндометрия сами по себе увеличивают риск РЭ.
Исторически укрепилось авторитетное мнение, что женщины с раком молочной железы (РМЖ) в анамнезе ни при каких условиях не должны получать заместительную терапию эстрогенами. Учитывая, что не существует источников литературы, подтверждающих это предостережение, а также положительные эффекты эстрогенов, некоторые специалисты убеждены в необходимости отмены этого запрета. Принимая во внимание отсутствие проспективного исследования влияния ЗГТ на пациенток после лечения РМЖ, Wile и DiSaia в 1989 г. предложили проанализировать ситуации, при которых эти женщины, возможно уже имевшие раковые клетки в молочных железах, подвергались воздействию эстрогенов в крови в высоких концентрациях. К таким ситуациям отнесли беременность в сочетании с РМЖ, беременность, наступившую после лечения РМЖ, случаи заболевания у женщин, получавших пероральные контрацептивы ранее или применяющих их в настоящее время, а также случаи развития РМЖ на фоне ЗГТ.
После тщательного анализа подобных ситуаций выяснилось, что исследуемая взаимосвязь незначительна, если вообще имеет место. В настоящее время в США ежегодно диагностируют 185 000 новых случаев РМЖ. Долгосрочная выживаемость у женщин, завершивших лечение РМЖ, все время растет; по некоторым прогнозам, она может превысить 90 %. В связи с этим увеличится количество женщин, перенесших РМЖ, которые доживут до пожилого возраста. Вот почему нам необходимо обратить внимание на целесообразность ЗГТ у данной категории пациенток.
По данным некоторых авторов, заместительная терапия эстрогенами у больных РМЖ безвредна. Мы должны помнить, что в прошлые времена, до применения цитостатиков, женщины в постменопаузе, страдающие метастатическим или рецидивным РМЖ, получали эстрогены в качестве терапии первой линии. Сейчас мы понимаем, что эффективность гормональной терапии в известной мере зависит от рецепторного статуса опухоли. По крайней мере в 7 проспективных рандомизированных двойных слепых исследованиях сравнивали эффективность эстрогенов и тамоксифена у пациенток с рецидивирующим или метастатическим РМЖ. Частота ответов на эстрогены и тамоксифен оказалась одинаковой. В проспективных рандомизированных исследованиях, сравнивавших эстрогены и тамоксифен в качестве адъювантной терапии, процент рецидивирования заболевания в обеих терапевтических группах не отличался. Однако мы обладаем весьма небольшим объемом клинических данных, посвященных этому вопросу.
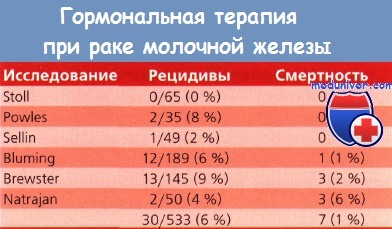
Оценка эффективности заместительной гормональной терапии (ЗГТ) у женщин с раком молочной железы (РМЖ) проводилась как минимум в 6 ретроспективных исследованиях. Перед приемом эстрогенов у пациенток не было признаков рецидива заболевания. ЗГТ была назначена с целью уменьшить вазомоторные симптомы или для профилактики хронических заболеваний сердечно-сосудистой системы, остеопороза и рака ободочной кишки. В данной группе, насчитывающей более 500 пациенток, было выявлено 30 (6 %) случаев рецидива опухоли и всего 7(1%) летальных исходов.
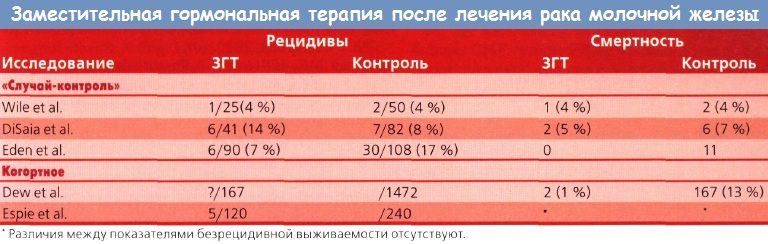
В проведенном авторами этой главы исследовании, включавшем 145 пациенток с раком in situ и I—IV стадии, рецидив заболевания выявлен у 13 (9 %) больных. Терапию эстрогенами получали пациентки и с метастатическими, и интактными лимфоузлами. Из 96 больных с интактными лимфоузлами рецидивы развились у 11, а в группе с пораженными лимфоузлами к настоящему времени рецидив опухоли выявлен только у 1 из 34. В группе пациенток, которым гистологическая оценка лимфоузлов не проводилась, рецидив выявлен у 1 из 15.
Кроме этого обнаружено, что рецепторный статус опухоли у больных, которым его определяли, никаким образом не влиял на частоту возникновения рецидивов в зависимости от приема эстрогенов. Данные о показателях рецидивирования у больных РМЖ, получавших ЗГТ, и летальных исходах представлены в таблице.
Уклонение от обсуждения с больной возможности заместительной терапии можно рассматривать как прямое нарушение ее интересов. В ближайшем будущем в США РМЖ заболеет более 36 000 женщин в возрасте моложе 50 лет. Большинство, если не все, получат цитотоксическую XT, у многих наступит аменорея, несмотря на возраст моложе 35 лет. К сожалению, при возникновении аменореи, обусловленной XT, в подавляющем большинстве случаев разовьется яичниковая недостаточность. Частота последней даже среди очень молодых женщин (моложе 40 лет) составит 86 %. Поэтому мы будем наблюдать увеличение количества молодых женщин с индуцированной XT преждевременной менопаузой.
У многих больных раком молочной железы (РМЖ) наступит выздоровление, но преждевременная менопауза станет причиной вазомоторных нарушений, по интенсивности превышающихтаковые при естественной менопаузе. Поэтому положительные эффекты ЗГТ при преждевременной менопаузе могут быть более выраженными. Для того чтобы принять грамотное решение, женщины должны осознавать смысл этой терапии, т. е. взвесить пользу от лечения и риск. Больные РМЖ — идеальные кандидаты для применения влагалищных колец с медленным высвобождением эстрадиола. Estring® содержит небольшую дозу эстрадиола, но достаточную и эффективную для лечения атрофии слизистой оболочки влагалища. При использовании этого кольца содержание эстрадиола в плазме повышается только на 10 % от той дозы, которая возникает при применении пластыря 0,05 Estraderm®. Если же симптомы, связанные с менопаузой, сохраняются, используют Eemring® с более высокой дозой эстрадиола (0,05 мг/сут), что также позволяет облегчить выраженность вазомоторных проявлений.
- Вернуться в оглавление раздела "Онкология"
Рак молочной железы — это один из самых распространенных видов онкологических заболеваний среди женщин репродуктивного возраста. Примерно в 70-80 % случаях злокачественная опухоль является гормонозависимой. Данный факт вызывает тревогу относительно того, что повышенная подверженность гормону эстроген может способствовать развитию и распространению онкологических образований.
Какие функции выполняет гормон эстроген?
Гормон эстроген обычно ассоциируется с репродуктивными функциями у женщин, однако он играет важную роль в здоровье костной ткани, сердца и кровеносной системы, регулирует эмоциональное состояние и поведение, способствует сжиганию жира и т. д.
Эстроген является жизненно важным гормоном, но его чрезмерное количество в организме может существенно повысить риск развития различных заболеваний, в том числе онкологических.
К группе риска относятся женщины с ранним наступлением первой менструации и поздней менопаузой, забеременевшие первый раз в позднем возрасте, не кормящие грудью. Все они имеют переизбыток данного гормона в организме на протяжении многих лет. У всех этих женщин риск заболеть раком груди значительно выше, чем у остальной части населения женского пола.

Как снизить уровень гормона эстрогена в организме?
Эстроген производится в яичниках на протяжении всего репродуктивного периода, затем, с наступлением менопаузы, источником его секреции становятся жировая ткань и надпочечники. Уменьшить уровень эстрогена можно путем снижения функционирования органов, которые его производят (например, яичников), или блокировки чувствительных к нему рецепторов. По данному принципу построено лечение гормонозависимых опухолей молочной железы, то есть когда опухоль содержит большое количество рецепторов к эстрогену. В таких случаях применяют препараты, препятствующие контакту гормона с данными рецепторами, и таким образом происходит подавление развития новообразования.
Повышению уровня эстрогена могут способствовать прием противозачаточных препаратов, заместительная гормональная терапия (после наступления менопаузы) и лечение бесплодия. Кроме того, гормон может поступать в организм через пищу, чистящие средства и даже косметику — в них могут содержаться молекулы, очень похожие на эстроген, которые выполняют в организме его функции.
В последние годы обнаружен еще один возможный источник повышенного содержания эстрогена, а именно — способ, с помощью которого избыток гормона выводится из организма.
Как выводится эстроген из организма?
После завершения своей функции гормон распадается и выводится из организма. Основную роль здесь играет печень, в которой происходит его метаболизм. Существует три способа метаболизма эстрогена в организме, при каждом из них образуются разные продукты распада.
Первый способ — OH 2 — является самым безопасным, он связан с низкой эстрогенной активностью и канцерогенным действием.
Два других способа — OH 4 и OH 16 — менее желательны, так как при них происходит доминантное действие эстрогена, что повышает риск развития онкологических заболеваний.
Как можно предотвратить или снизить риск развития рака молочной железы?
К счастью, во многих случаях изменение питания и образа жизни, а также употребление лекарственных трав и пищевых добавок может значительно повлиять на путь метаболизма эстрогена. По результатам последних исследований, у женщин, употреблявших в течение всего одного месяца соответствующие лекарственные травы и фитовещества, которые были выделены из брокколи, преобладал первый путь вывода эстрогена из организма!
Какие продукты рекомендуется употреблять для улучшения процесса метаболизма эстрогена?
Продукты, богатые пищевыми волокнами, которые находятся в овощах, фруктах, крупах и цельных бобовых. Они способствуют лучшей работе кишечника, который также играет важную роль в выводе эстрогена.
Овощи из семейства крестоцветных, такие как брокколи, капуста и цветная капуста. Кроме пищевых волокон, они содержат индолы — фитовещества, способствующие лучшему распаду эстрогена. Так как они очень чувствительны к высоким температурам, овощи рекомендуется готовить на пару. С целью достижения лучшего клинического эффекта можно использовать индолы в виде пищевых добавок (I3C и DIM), влияние которых на рак молочной железы научно доказано.
Семена свежего молотого льна. Рекомендуется добавлять 1-2 столовых ложек молотых семян льна в воду, йогурт или другие негорячие блюда. В семенах льна содержится омега-3, которая катализирует энзим, ответственный за лучшую переработку эстрогена.
Зерна сои, тофу и соевые продукты также способствуют правильному выводу эстрогена. Ранее считалось, что данные продукты противопоказаны женщинам, страдающим раком молочной железы из-за фитоэстрогенов — растительных эстрогенов, похожих по своей структуре на эстрогены, содержащиеся в организме человека. Результаты многочисленных исследований последних лет показали, что регулярное употребление сои снижает риск рецидива заболеваний. Обратите внимание, что речь идет о сое, а не о соевых переработанных продуктах, таких как шницели, от потребления которых следует воздержаться.
Лекарственные травы. Розмарин, куркум, чертополох, пожитник также полезны для стимуляции правильного метаболизма эстрогена. Их можно использовать при приготовлении пищи, добавлять в чай или готовить травяные растворы. Однако перед их употреблением следует сначала обратиться за консультацией к специалисту, который объяснит, как, в каких количествах и по какой схеме лучше всего использовать данные лекарственные растения в качестве травяных добавок.
Какие продукты следует ограничить в рационе?
Необходимо избегать избыточного употребления сладкого, продуктов, содержащих животные жиры, а также алкоголь в больших количествах. Малоподвижный образ жизни и избыточный вес признаны факторами, способствующими повышению риска развития рака молочной железы, не исключающими его рецидив.
Таким образом, здоровый образ жизни, полноценное, сбалансированное питание и правильно подобранные пищевые добавки могут значительно снизить риск заболеть раком молочной железы.


Что большинство людей знает о раке молочной железы (РМЖ)?
- Опухоли бывают злокачественными и доброкачественными.
- Для лечения используется химиотерапия и хирургическое вмешательство.
- Рак пугает нас до чертиков.
Что знают о раке молочной железы врачи?
Очень, очень и очень много. И будьте уверены, вышеперечисленными фактами медицинские знания и близко не ограничиваются.
Не существует некого универсального рака, который поражает разные органы нашего тела.
Онкология разнообразна, типов опухлевой активности множество — это относится и к раку молочной железы.
Для того, чтобы успешно бороться с раком и снизить риски рецидивов, онкологи изучают опухоль различными способами, определяя ее особенности, вплоть до молекулярного строения.
Важным аспектом терапии РМЖ является определение, является ли опухоль гормонозависимой или гормоно-негативной.
Это первоочередная задача после биопсии или операции. В зависимости от полученных результатов врачи определятся со стратегией лечения.
Какое отношение к раку имеют гормоны?
Если речь идет о раке молочной железы (и некоторых других органов), то отношение самое прямое. Наша грудь — орган гормонозависимый, на ее работу влияют прогестерон, эстроген и пролактин (и некоторые другие, но о них в другой раз).
Гормоны — активные вещества, они отвечают за эффективную работу различных систем организма, в том числе, за клеточное деление.
В тех случаях, когда опухоль восприимчива к гормонам, ее рост может ускориться или усилиться. Подавление выработки эстрогена и прогестерона позволяет контролировать опухоль и снизить риски ее возвращения после химиотерапии или операции.
Как это работает на клеточном уровне?
Можно представить себе рецепторы как крошечных котят, лапки которых цепко хватают только любимые игрушки, игнорируя все остальные.
Некоторые рецепторы восприимчивы только к эстрогену, другие — только к прогестерону, третьи воспринимают оба гормона, и так далее.
Как это связано с раком молочной железы?
Онкологический процесс подразумевает мутацию клеток.
Когда мы говорим о РМЖ, нужно помнить, что клетки многих опухолей сохраняют рецепторы к половым гормонам, а значит, такой рак более склонен к клеточному делению и формированию метастазов.
Как узнать, есть ли в опухоли рецепторы к эстрогену и прогестерону?
Для этого необходимо иммуногистохимическое исследование.
Кусочек опухоли, полученный при операции или биопсии, тщательно изучают в лаборатории под микроскопом на наличие биомаркеров рецепторов.
Считается, что около 70% опухолей молочной железы являются гормонозависимыми.
Если рецепторы обнаружили, что происходит дальше?
Этого можно достичь двумя способами:
Некоторые опухоли гормонозависимы или гормон-негативны и к эстрогену, и к прогестерону. Другие реагируют только на эстроген.
Логика терапии будет одинаковой в обоих случаях.
Какую терапию используют, и как она работает?
Для лечения гормонозависимого рака молочной железы используется четыре типа препаратов.
Что такое ингибиторы ароматазы? Звучит перспективно
Ароматаза — это фермент, трансформирующий андрогены в эстрогены. Ингибиторы ароматазы можно назвать антиэстрогенами.
Использование ингибиторов имеет свои побочные эффекты. Часть из них относится к искусственной менопаузе, в которую, по сути, препарат погружает организм.
Другие несут осложнения иного рода.
- Приливы жара
- Боли в суставах
- Мышечная боль
- Головная боль
- Ночная потливость
- Потеря волос
- Бессонница
- Тошнота
- Расстройство желудка
- Диарея
- Усталость
- Депрессия
- Отеки
К долговременным побочным эффектам можно отнести повышение риска остеопороза.
Поэтому при гормональной терапии такого плана врачи обычно следят за состоянием костной ткани.
Терапию ингибиторами ароматазы связывают с повышенным риском сердечно-сосудистых заболеваний и диабета.
Существует также крошечная вероятность развития рака эндометрия во время терапии ингибиторами ароматазы.
Побочные эффекты гормональной терапии могут быть очень неприятными, но они но она несопоставимо менее значимы, чем риски рецидива рака молочной железы.
Ингибиторы ароматазы могут взаимодействовать с определенными лекарствам, что снижает их концентрацию и требует корректировки дозы.
Среди таких препаратов некоторые гормональные контрацептивы, антибиотики, антидепрессанты, противогрибковые препараты, антипсихотики, сердечные препараты и препараты для лечения ВИЧ, а также БАДы, содержащие зверобой.
В Курчатовском институте создали новую форму известного лекарства от рака груди. Ученые загрузили действующее вещество в микрочастицы, что позволило сделать действие жизненно важного препарата пролонгированным. В результате, пациенткам нужно будет реже принимать лекарство, что делает его значительно менее токсичным, а эффект будет сильнее. Ученые уверены, что новый препарат сможет снизить частоту рецидивов рака молочной железы.
Снизить эстроген
Большинство женщин с раком молочной железы после удаления опухолей нуждаются в адъювантной (дополнительной) терапии. В случае рака молочной железы часто используется гормонотерапия. Она направлена на то, чтобы увеличить шансы на выживаемость в течение длительного периода. Главная цель такого лечения – не допустить рецидива болезни.

Эффект микрочастиц
В отличие от таблеток, новый препарат будет представлять собой порошок на основе микрочастиц размером 60 мкм, предназначенный для приготовления суспензии для внутримышечного введения.
— Мы создали полимерную форму, предназначенную для терапии рака груди. Активное вещество включено в состав частиц из биоразлагаемого сополимера молочной и гликолевой кислоты. Полимер инертен для человеческого организма, расщепляясь, он обеспечивает необходимую скорость выделения анастрозола. Мы добились того, что вещество выделяется из частиц в течение месяца в достаточном для лечения количестве, то есть мы добились пролонгации эффекта, — пояснил Юрий Полтавец.

— Этот проект носит комплексный характер. Мы вовлекли в коллектив специалистов различных профилей — это и фармакологи, и токсикологи, и клеточные биологи, и генетики, и врачи. Все они работают в стенах Курчатовского института, - подчеркнула Надежда Гукасова.
Как пояснили ученые, препарат уже готов к клиническим испытаниям. Сейчас идет поиск индустриального партнера — крупной фармацевтической компании, которая заинтересована в проведении клинических испытаний и выведении препарата на рынок.
Инъекционная форма препарата действительно усилит терапевтический эффект, уверена руководитель центра персонализированной онкологии, профессор кафедры онкологии Первого МГМУ имени Сеченова Марина Секачева.
- Онкологи знают, что чем реже пациенту нужно принимать препарат, тем это лучше. Это связано и с колебаниями основного действующего вещества, и с тем, что люди, особенно пожилого возраста, попросту пропускают прием таблеток, что в случае рака очень опасно, - отметила специалист.
Рак молочной железы занимает первое место в структуре онкологических заболеваний среди российских женщин. Ежегодно выявляется 54 тысячи больных женщин, при этом 22 тысячи из них умирает. Как отмечают ученые, снижение смертности от рака груди — это крайне актуальная медицинская проблема.
Комплексное исследование, позволяющее определить уровень стероидных гормонов и их метаболитов в суточной моче. Синтез эстрогенов у женщин осуществляется фолликулярным аппаратом яичников. У женщин эстрогены обеспечивают нормальное развитие и функционирование репродуктивной системы. Эстрогены представлены тремя формами: эстроном (фолликулин) – Е1, эстрадиолом – Е2 и эстриолом – Е3, имеющими разную физиологическую активность.
Исследование предназначено только для женщин в возрасте 16 лет и старше. При регистрации заявок для исследования стероидных гормонов у женщин обязательно указывать наличие/отсутствие беременности.
- Эстрадиол
- Эстрон
- Эстриол
- 2-гидроксиэстрон (2-OHE1)
- 4-гидроксиэстрон (4-OHE1)
- 16a-гидроксиэстрон (16a-OHE1)
- 2-метоксиэстрон (2-OMeE1)
- 4-метоксиэстрон (4-OMeE1)
- 2-гидроксиэстрадиол (2-OHE2)
- Соотношение 2-ОНЕ1/16а-ОНЕ1
- Соотношение 2-ОНЕ1/2-OMeE1
- Соотношение 4-OHE1/4-OMeE1
- Прегнандиол
Уровень баланса эстрогенных метаболитов.
Газовая хроматография-масс-спектрометрия (ГХ-МС).
Мкг/сут. (микрограмм в сутки).
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
- День сбора биологического материала определяется лечащим врачом, исходя из имеющихся клинических данных. Женщинам репродуктивного возраста с устоявшимся менструальным циклом рекомендуется сдавать суточную мочу в лютеиновую фазу цикла. Проведение исследования в другие фазы цикла определяет лечащий врач.
Общая информация об исследовании
Эстрогены – стероидные половые гормоны, преобладающие в женском организме. Синтез эстрогенов у женщин осуществляется фолликулярным аппаратом яичников, а у мужчин - в основном яичками (до 20 %). У женщин эстрогены обеспечивают нормальное развитие и функционирование репродуктивной системы, а у мужчин участвуют в регуляции функций простаты и яичек. Эстрогены представлены тремя формами: эстроном (фолликулин) - Е1, эстрадиолом - Е2 и эстриолом - Е3, имеющими разную физиологическую активность: Е2 ˃ Е3 ˃ Е1.
Эстрадиол оказывает мощное феминизирующее влияние на организм, стимулирует развитие влагалища, матки, маточных труб, стромы и протоков молочных желез, формирование вторичных половых признаков по женскому типу, в том числе характерное распределение жировой ткани. Эстрадиол также способствует своевременному отторжению эндометрия и наступлению менструации.
Эстрон (фолликулин) в меньшей степени, чем эстрадиол, участвует в развитии женской репродуктивной системы и регуляции менструального цикла. Вызывает пролиферацию эндометрия, стимулирует развитие матки, фаллопиевых труб, вторичных женских половых признаков, уменьшает климактерические расстройства, влияет на тонус и эластичность урогенитальных структур. В постменопаузальном периоде эстрон преобладает среди эстрогенов, т. к. образуется из андростендиона надпочечников.
Эстриол (16-гидроксиэстрадиол) – гормон беременности, активно синтезируется плацентой с 25-й недели. Выработка эстриола напрямую связана с развитием будущего ребенка и отражает состояние фетоплацентарного комплекса. Предшественники эстриола (ДГЭА и 16α-ОН ДГЭА) вырабатываются надпочечниками и печенью плода, после чего поступают в плаценту, где и преобразуются в эстриол. Вне беременности и у мужчин в следовых количествах эстриол синтезируется корой надпочечников.
Метаболиты эстрогенов
2-гидроксиэстрон (2-OHE1) и 2-гидроксиэстрадиол (2-OHE2) действуют как антиэстрогены, ингибируют митотическую активность клеток и препятствуют развитию неоплазии. Понижение их концентрации может соответствовать гиперэстрогенемии.
16α-гидроксиэстрон (16α-OHE1) и 4-гидроксиэстрон (4-OHE1) – агонисты эстрогенов. Высокие концентрации стимулирует клеточную пролиферацию и ассоциированы с развитием эстрогенозависимых новообразований. Низкий уровень 16α-OHE1 - фактор риска развития остеопороза. Высокие уровни 4-ОНЕ1 обладают прямым генотоксическим действием. Для 4-ОНЕ1 установлена связь с такими новообразованиями, как рак молочной железы у женщин и грудной железы у мужчин, рак тела матки, яичников, поджелудочной железы, саркоматозные опухоли матки, злокачественная меланома, гепатоцеллюлярный рак, карциноидные опухоли, немелкоклеточный рак легкого, злокачественная мезотелиома, рак почки, рак предстательной железы, астроцитомы, миеломная болезнь, десмоиды и кисты. Поэтому эффективное метилирование способствует быстрой элиминации потенциально опасных гидроксиэстрогенов.
2-метоксиэстрон (2-OMeE1) и 4-метоксиэстрон (4-OMeE1) – неактивные и "защитные" формы метаболитов эстрогенов. Значения 2-OMeE1 и 4-OMeE1 не менее 25 % от значений 2-OHE1 и 4-OHE1 соответствуют процессам адекватного метилирования.
Прегнандиол - конечный метаболит прогестерона.
Исследование данных показателей выполняется методом газовая хроматографии-масс-спектрометрии (ГХ-МС), позволяет провести неинвазивную диагностику заболеваний, связанных с гормональными нарушениями; обладает высокой специфичностью – 100 %.
Когда назначается исследование?
- Остеопороз;
- ожирение;
- жировая дистрофия печени;
- бесплодие;
- высокий риск развития эстрогензависимых новообразований либо их наличие;
- дисфункция яичников, нарушения менструального цикла, прием противозачаточных препаратов и антиэстрогенов (тамоксифен и его аналоги: билем, зитазониум, новофен и нолвадекс).
Что означают результаты?
Результаты исследования выдаются в соответствии с референсными диапазонами для женщин детородного возраста 18-40 лет и в постменопаузе.
Читайте также:

