Медиана выживаемости при раке яичников
Необходимость удаления максимально возможного объема опухоли во время первой операции по поводу диссеминированного рака яичника (РЯ) стала аксиомой для многих онкогинекологов. Известно, что значительное снижение опухолевой нагрузки дает выраженный паллиативный эффект. По данным Munnell, 5-летняя выживаемость больных после операций в максимально возможном объеме составляла 28 %, после частичной резекции — 9 %, а после биопсии — 3 %. Для 14 выживших пациенток операция в максимально возможном объеме включала гистерэктомию с двусторонней аднексэктомией и оментэктомию.
Aure и соавт. отметили существенное улучшение выживаемости пациенток с III стадией рака яичника (РЯ) после удаления всей видимой опухоли. Griffiths и соавт. получили аналогичные результаты при использовании линейного уравнения множественной регрессии выживаемости в качестве зависимой переменной для одновременного контроля множества терапевтических и биологических факторов, влияющих на исход заболевания у отдельных пациенток.
Самыми важными факторами были гистологическая степень дифференцировки и наибольший размер остаточной опухоли после первичного хирургического лечения. Операция улучшает выживаемость только в том случае, если максимальный размер остаточной опухоли составляет менее 1,6 см.
Так называемые циторедуктивные операции (debulking operation) получили значительное распространение при лечении рака яичника (РЯ). Цель хирургического вмешательства заключается в уменьшении объема новообразования для оптимальной эффективности адъювантной терапии. Все формы дополнительного лечения наиболее эффективны при минимальном объеме остаточной опухоли. Это особенно касается истинного рака яичника (РЯ) — солидных опухолей, наиболее чувствительных к химиотерапии (XT). Часто аккуратный и терпеливый хирург может удалить крупные опухолевые очаги, которые на первый взгляд казались неоперабельными.
При использовании бессосудистых зон забрюшинного пространства можно выделить воронкотазовую связку, мочеточник и изолировать сосуды, кровоснабжающие яичник. После их перевязки и пересечения ретроградное удаление больших опухолей яичников выполнить проще и безопаснее. Выделение мочеточников проводят с максимальной осторожностью, однако их повреждение бывает даже у самых опытных хирургов. Конгломераты большого сальника при раке яичника (РЯ) удаляют через бессосудистую зону поперечно-ободочной кишки после лигирования правой и левой желудочно-сальниковых артерий. Удаление больших новообразований яичников и метастатически пораженного сальника часто уменьшает общий объем опухоли на 80—99 %.
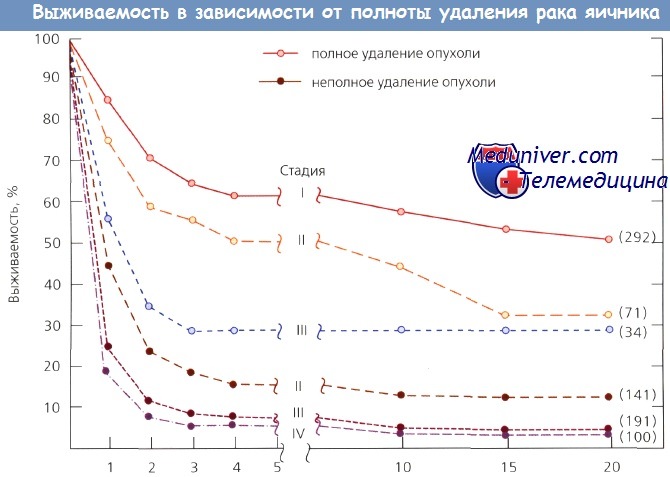
Сравнение выживаемости пациенток при полном и неполном удалении опухоли в зависимости от стадии рака яичников
Теоретическим обоснованием рассматриваемых операций (debulking procedures) служит концепция о повышении эффективности адъювантной терапии после существенного снижения числа опухолевых клеток. Кроме того, при солидных опухолях, к которым относят рак яичника (РЯ), элиминация большой популяции клеток в фазе покоя (G0) может вызывать переход оставшихся клеток в уязвимую для цитостатиков и облучения фазу пролиферации. Несколько скрупулезных ретроспективных исследований продемонстрировало увеличение выживаемости больных, у которых с помощью хирургического метода лечения удалось добиться статуса минимального опухолевого носительства. Большой опыт, накопленный в M.D. Anderson Hospital and Tumor Institute, свидетельствует о существенном повышении эффективности XT второй линии при II и III стадиях рака яичника (РЯ), если после первой операции не оставались макроскопические остаточные новообразования или диаметр единичной остаточной опухоли не превышал 1 ем.
При этом 2-летняя выживаемость пациенток со II стадией без остаточных опухолей составила 70 %, а при отдельных узлах диаметром до 1 см — 50 %.
Эти показатели хорошо согласуются с часто публикуемыми цифрами общей выживаемости при раке яичника (РЯ). GOG проводила детальный анализ результатов хирургического лечения больных с поздними стадиями заболевания для определения концепции первичной циторедуктивной операции. На первом этапе сравнили выживаемость пациенток с III стадией рака яичника (РЯ) с опухолью в брюшной полости до 1 см (1-я группа) и 1 см и более (2-я группа); больным 2-й группы опухоли уменьшили до 1 см и менее.
Если хирургическая операция — единственный важный фактор, как рассуждали исследователи, то выживаемость в обеих группах должна быть одинаковой. Однако на самом деле этого не произошло. Больные с небольшим размером опухоли 1-й группы жили дольше по сравнению с пациентками, у которых благодаря хирургической циторедукции достигнут малый размер опухоли (2-я группа). Этот феномен свидетельствует о том, что биологические свойства новообразования имеют важное прогностическое значение. На следующем этапе исследователи GOG оценили влияние наибольшего диаметра остаточной опухоли на выживаемость пациенток после субоптимальных циторедуктивных операций. Они обнаружили, что циторедукция до 2 см и менее значительно увеличивала выживаемость, но при любых остаточных опухолях диаметром более 2 см этот показатель был одинаковым. Следовательно, если остаточную опухоль нельзя уменьшить до 2 см и менее, то выживаемость не зависит от величины диаметра остаточной опухоли.
При исследовании оптимальной и субоптимальной циторедукции эксперты GOG выделили три группы: микроскопическая остаточная опухоль, диаметр остаточной опухоли менее 2 см или более 2 см. В 1-й группе 4-летняя выживаемость составила примерно 60 %, во 2-й — 35 % и в 3-й — менее 20 %. Самое удивительное — это неспособность циторедуктивной операции оказать хотя бы минимальное влияние на выживаемость, если не удалосьуменьшитьдиаметр остаточной опухоли до 2 см и менее.
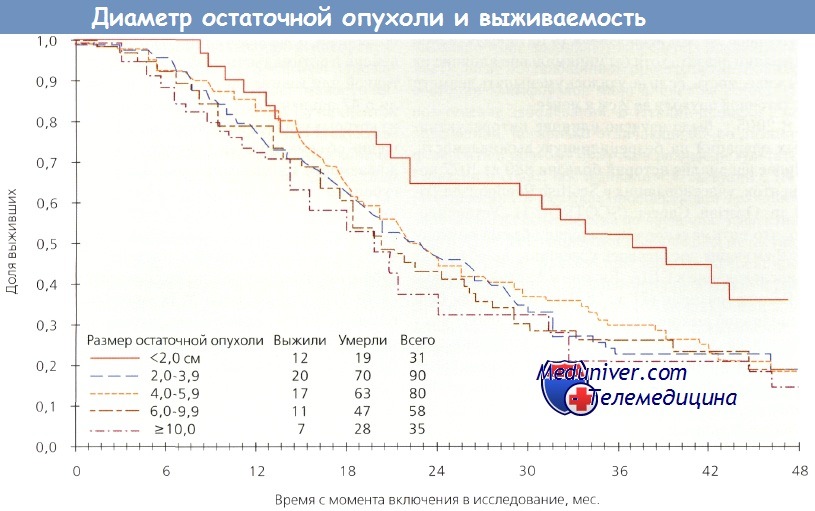
Выживаемость в зависимости от максимального диаметра остаточной опухоли
В 2005 г. было изучено влияние циторедуктивных операций на безрецидивную выживаемость. Проведен анализ историй болезни 889 из 1077 пациенток, участвовавших в Scottish Randomised Trial in Ovarian Cancer (SCOTROC-1). Установлено, что оптимальное уменьшение объема опухоли ( 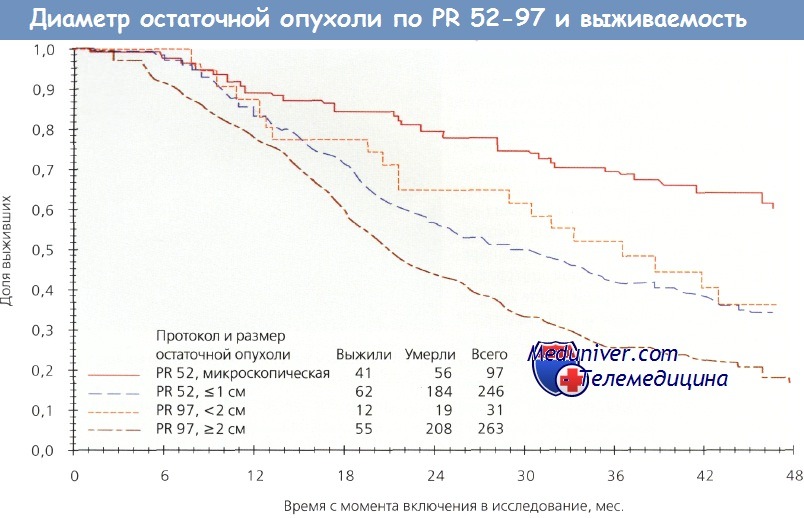
Выживаемость в зависимости от максимального диаметра остаточной опухоли, согласно 52-му и 97-му протоколам (PR) Gynecologic Oncology Group
Эксперты Southwest Oncology Group и GOG исследовали эффективность интраперитонеальной и внутривенной ХТ у пациенток с III стадией РЯ после оптимальных циторедуктивных операций и установили, что при микроскопической остаточной опухоли, остаточном поражении до 0,5 или 0,5—2,0 см медиана выживаемости составила 76, 42 и 32 мес. соответственно. Eisenkop и соавт. сообщили о 163 пациентках с IIIс и IV стадиями РЯ; полную циторедукцию можно было выполнить в 86 % случаев. Медиана выживаемости для всей группы составила 54 мес, а для больных с оптимальной циторедукцией — 62 мес.
Целесообразность выполнения лимфаденэктомии при поздних стадиях рака яичника (РЯ) продолжает оставаться предметом обсуждения. Во всех исследованиях обнаружено обширное поражение лимфоузлов при поздних стадиях заболевания (> 50 %). Вопрос заключается в том, влияет ли лимфаденэктомия на выживаемость. Burghardt один из первых высказал мнение о ее терапевтической пользе. По его данным, даже при наличии метастазов в лимфоузлах, выживаемость пациенток с поздними стадиями РЯ, которым выполнили хирургическое стадирование, а следовательно, и лимфаденэктомию, выше, чем без такого вмешательства. Некоторые авторы считают, что метастазы в лимфоузлах в отличие от интраперитонеальных не так хорошо поддаются XT, поэтому их необходимо удалять. Противники утверждают, что рецидивы значительно чаще возникают в пределах брюшной полости, но не в забрюшинном пространстве, поэтому состояние лимфоузлов мало влияет на естественное течение заболевания.
В Италии провели 2 исследования, несколько отличающихся по дизайну, и, вероятно, поэтому получили разные результаты. Parazzini и соавт. обследовали 456 женщин с III и IV стадиями РЯ в рамках проспективного рандомизированного исследования по изучению эффективности XT. У 161 пациентки обнаружены метастазы в лимфоузлах, причем при низкодифференцированных опухолях (G3) чаще, чем при высоко- и умереннодифференцированных (G1 и G2). Авторы не выявили отличий в показателях выживаемости между больными с метастатическими и интактными лимфоузлами. Следовательно, положительное влияние удаления метастатических лимфоузлов на выживаемость не установлено. Scarabelli и соавт. выполнили лимфаденэктомию 98 больным РЯ IIIс—IV стадии, у которых не было макроскопических остаточных опухолей; в группу контроля вошло 44 пациентки, которым лимфаденэктомия не проводилась. Выживаемость больных, которым выполнили лимфаденэктомию, была значительно лучше (анализ Кокса). Результаты этого исследования показали, что лимфаденэктомия обеспечивает потенциальный терапевтический эффект, но в определенной группе пациенток. Ранее обсуждались аналогичные выводы клинического испытания SCOTROC-1.
Мы обязательно выполняем стандартную тазовую и парааортальную лимфаденэктомию, но при условии оптимального уменьшения объема опухоли. Эффективность лимфаденэктомии при большом объеме остаточной опухоли, по нашему мнению, сомнительна. При поздних стадиях РЯ показано удаление всей опухоли, если это технически возможно. Для этого разработано много способов. Некоторые врачи используют хирургический УЗ-аспиратор, другие предлагают электрохирургическую резекцию с помощью электрокоагулятора с аргоновой приставкой, третьи все еще убеждены, что резекция диафрагмальной брюшины или мышцы играет важную роль в циторедукции. Влияние всех этих методов на выживаемость окончательно не определено. Следует с осторожностью относиться к успешному применению той или иной методики в руках отдельных энтузиастов и подождать весомого подтверждения в публикациях.
Растет число сторонников проведения лапароскопии вместо лапаротомии. Технически это возможно, но целесообразность удаления больших объемных образований придатков матки с помощью лапароскопа сомнительна. В публикациях описаны случаи возникновения метастазов в местах введения троакаров. Феномен рецидива рака в области послеоперационного рубца хорошо известен, однако удивительно, что даже при большой интраабдоминальной опухоли это редкость. Wang и соавт. провели обзор литературы для определения факторов риска ранних рецидивов в местах установки портов. Из всех злокачественных опухолей женских половых органов метастазы в местах введения троакаров чаще всего возникают при раке яичника (РЯ), независимо от того, имеется асцит или нет, стадии заболевания (ранней или поздней), появления после диагностических или паллиативных операций.
Такие метастазы обнаруживали и при опухолях низкой степени злокачественности. Чаще они возникают при асците и канцероматозе брюшины. Наименьший промежуток времени между лапароскопией и появлением метастаза в месте установки порта составил 8 дней. По этому поводу предложили несколько теорий: имплантация раковых клеток при травматической диссеминации во время удаления первичной опухоли, прямая имплантация инструментами, создание градиента давления при пневмоперитонеуме с последующим выходом газа (через порты), который привел опухолевые клетки во флотирующее состояние. Лапароскопия больше подходит для удаления доброкачественных образований придатков матки. При подозрении на РЯ мы предпочитаем лапаротомный доступ. Если во время лапароскопии обнаруживают РЯ, необходимо немедленно перейти на лапаротомию.
Группа EORTC сообщила о собственном опыте циторедуктивных операций при поздней стадии рака яичника (РЯ). Пациентки получили 3 курса цисплатина и циклофосфамида, и затем их разделили случайным образом на две группы: одним выполнили циторедуктивную операцию, другим — нет. Все женщины получили 6 курсов XT. Среди 278 пациенток медиана выживаемости составила 26 и 20 % (операция и без операции; р = 0,012). Многофакторный анализ показал, что циторедуктивная операция была независимым прогностическим фактором. После учета всех факторов прогноза оказалось, что хирургическое вмешательство снизило риск смерти на 33 % (р = 0,008).
В 2004 г. GOG сообщила о проведении аналогичного исследования, в которое было включено 550 больных. При неоптимальной первичной цито-редуктивной операции (остаточная опухоль более 1 см) назначали 3 цикла паклитаксела с цисплатином. После этого пациенток рандомизировали на две группы: одним продолжили XT, а другим выполнили вторую циторедуктивную операцию и продолжили XT. Промежуточная (дополнительная) между курсами XT операция не привела ни к улучшению безрецидивной выживаемости, ни к снижению относительного риска смерти. Авторы предполагают, что разница в результатах может быть обусловлена более агрессивным выполнением хирургических вмешательств у пациенток в исследовании GOG по сравнению с EORTC. Если суммировать оба исследования, можно сделать следующее заключение: пациенткам с поздними стадиями рака яичника (РЯ) показана хотя бы одна циторедуктивная операция, но с максимально возможным уменьшением объема опухоли, лучше, если се проведет онкогинеколог.
Нет сомнений, что тщательно выполненная первичная циторедуктивная операция — основной фактор, определяющий отдаленную выживаемость. Выбор времени для проведения хирургического вмешательства, целью которого служит удаление максимально возможного объема опухоли, остается предметом обсуждения. При относительных противопоказаниях (возраст, сопутствующие заболевания, плевральный или перикардиальный выпот) и распространенном злокачественном процессе в брюшной полости успешную циторедуктивную операцию осуществить невозможно, поэтому настоятельно рекомендуется рассмотреть вопрос о назначении неоадъювантной XT. Хороший клинический ответ после 2—4 циклов XT часто дает возможность выполнить эффективную циторедуктивную операцию с небольшой частотой осложнений. До начала XT нужно точно установить локализацию рака (яичник, маточная труба или брюшина), используя для этого цитологическое исследование или малоинвазивное хирургическое вмешательство. На сегодня неоадъювантная XT с последующей циторедуктивной операцией представлена в нескольких небольших ретроспективных исследованиях, включающих от 20 до 90 пациенток. Результаты указанной терапии аналогичны таковым при первичном хирургическом вмешательстве с последующей XT.
В текущем клиническом исследовании, проводимом EORTC и Национальным институтом рака (NCI) в Канаде, принимает участие более 700 больных, набор которых закончен в 2006 г. Ожидают, что это исследование даст подробную информацию о показаниях к неоадъювантной XT с последующей операцией и результатах такого комбинированного лечения.
У пациенток после обширного хирургического вмешательства увеличен риск расхождения краев раны, поэтому нужно использовать методики ушивания передней брюшной стенки через все слои. Однако в ситуациях выпячивания отечных петель кишечника из брюшной полости во избежание прорезания фасции и снижения риска несостоятельности рубца лучше наложить узловые швы с отсроченным их затягиванием.

Статистика рака яичников
В странах Западной Европы заболеваемость раком яичников составляет 18000 на 1000 представительниц женского пола. В РФ ежегодно диагностируют рак яичников у 11000 женщин, в Беларуси – в 80000. Эта патология составляет 5% в структуре заболеваемости онкологическими заболеваниями. В Великобритании заболеваемость раком яичников составила в 2012 году 7000 человек. В день выявляли 19 новых случаев заболевания. Это 2% от всех новых случаев рака. Во всём мире в 2012 году зарегистрировано 239000 новых случаев рака яичников.
Он находится на третьем месте среди злокачественных новообразований женских репродуктивных органов после рака шейки и тела матки. Средний возраст пациенток, страдающих раком яичников, составляет 63-64 года. 28% рака яичника выявляют у женщин старше 75 лет. Подростков и женщин молодого возраста поражают преимущественно гермиогенные опухоли.
Средний возраст женщин, у которых выявляют эти новообразования, составляет 20лет. Их доля в структуре онкологической заболеваемости такова: 81% злокачественных новообразований яичников у подростков и 6% всех опухолей яичников. Негермиогенные опухоли яичников встречаются у женщин после 50 лет. У них в 66% случаев выявляют аденокарциномы.
Заболеваемость раком яичников в мире увеличилась с конца семидесятых годов прошлого столетия на 1/3. За последнее десятилетие благодаря новым методам исследования она снизилась на 14%. К сожалению, растёт и показатель смертности от этого новообразования. Так, ежегодно во всём мире умирает от рака придатков матки около 152000 женщин.
Скорее всего, это происходит из-за того, что от этого новообразования умирают в основном пожилые люди, у которых есть тяжёлая сопутствующая соматическая патология. Так, процент смертности женщин, страдающих раком яичников, после 65 лет составил 37,5, а после семидесяти лет – 65. Наиболее высокая смертность женщин в возрасте после 85 лет.
Это связано с проблемами герниопатологии. Смертность от рака яичников составляет 4% женской смертности и 2% от общего показателя. Она наиболее высокая в странах Восточной Азии и Малайзии.
Причины рака яичников
До сих пор не установлены точные причины рака яичников. Считается, что в 70% случаев развитию новообразования способствуют нарушения гормонального гомеостаза. 30% группы риска составляют женщины, которые никогда не рожали, или имеют в анамнезе много беременностей.
Классификация рака яичников
Для того чтобы знать, каков прогноз заболеваемости при раке яичников, следует уточнить, какие бывают формы и варианты течения заболевания. По гистологической структуре различают несколько типов опухолей придатков матки. Прежде всего, следует отметить, что в большинстве случаев рак яичника представлен аденокарциномой.
В 66,7% случаев встречается серозная аденокарцинома, в 11,2% пациенток определяют муцинозный тип опухоли, в 11,2% - эндометриоидный. Светлоклеточный морфологический вариант аденокарциномы определяют у 5,4% женщин, а недифференцированные клетки находят в 5,4% исследуемого материала.
Стадия рака яичников самым непосредственным образом влияет на возможность радикального лечения опухоли и определяет прогноз выживаемости. Рак яичников первой стадии характерен тем, что злокачественное новообразование находится в пределах одного или обоих яичников. Опухоль не распространяется за пределы органа. Её определяют в 33,7% случаях. При стадии IA опухоль развивается только в одном яичнике и находится внутри него. На поверхности органа нет атипичных клеток. Если же злокачественное новообразование находят в обоих яичниках, то говорят о IB стадии. На стадии IC раковая опухоль определяется в обоих яичниках, но, кроме этого, есть один из следующих признаков заболевания:
в случае кистозного новообразования случается разрыв его капсулы;
в смывах из брюшной полости находят атипичные клетки;
опухолевые клетки находят на поверхности яичника.
В 8,7% случаев определяют вторую стадию рака яичников. В случае выявления опухоли на стадии II А стадии она распространяется матку или же фаллопиевы трубы. При IIВ стадии опухоль распространяется на органы малого таза и кишечник, но в смывах из брюшной полости отсутствуют раковые клетки. На стадии IIC в 100% случаев раковые клетки находят в смывах из брюшной полости.
При III опухоль поражает яичники и метастазирует в лимфатические узлы, за пределы малого таза или в полость брюшины. Её диагностируют в 40,9% случаев. У 16,7 % женщин выявляют рак яичников на четвёртой стадии. Прогноз в этом случае неблагоприятный, поскольку метастазы находят в отдалённых органах или определяют атипичные клетки в полостях организма.
Рак яичников - симптомы и прогноз
Рак яичников относится к чрезвычайно коварным заболеваниям, поскольку на ранних стадиях болезни выявить какие-то симптомы не представляется возможным. Женщина думает о какой угодно патологии, но только не о раке яичников. Знание симптомов болезни позволяет своевременно обратиться к специалисту, что может значительно улучшить прогноз выживаемости.
Основные симптомы заболевания следующие:
I. Болезненные тянущие ощущение в нижней части живота, которые отдают отдающие в ноги или же пояснично-крестцовый отдел. Они возникают преимущественно после поднятия тяжести занятия спортом (98%).
II. Дискомфорт во время полового акта (65%).
III. Дисменорея (89%).
IV. Быстрая насыщаемость и неприятные ощущения во время еды (15%).
V. Изжога, вздутие и увеличение в объеме живота (43%).
VI. Выделение крови из влагалища (59%).
VII. Быстрый набор и потеря массы тела (54%).
VIII. Плохое самочувствие по утрам, вялость, сонливость и быстрая утомляемость (96%).
IX. Плохой аппетит, тошнот и рвота (43%).
X. Ощущение давления на органы малого таза и учащённые позывы к дефекации (38%).
В случае метастазирования рака яичников в другие органы появляются иные симптомы. Так, 65% пациенток беспокоит кашель с прожилками крови, одышка и кровохарканье, что говорит о наличие метастазов в лёгкие. У 65% женщин, страдающих раком яичников, появляется желтуха. В таких случаях следует подумать о метастазах в печень или головку поджелудочной железы.
При болях в костях, которые беспокоят 88% пациенток на поздних стадиях рака придатков, следует исключить наличие метастазов в костные ткани. В 67% случаях пациенток начинают беспокоить головные боли, которые не купируются анальгетиками, нарушается координация движений, возникают судороги. Это может быть признаком метастазов в головной мозг.
Онкологи выделяют неспецифичные признаки рака придатков матки:
анемия (в 99% случаев);
высокая СОЭ (в 100%);
синдром хронической усталости (в (97);
признаки хронической интоксикации (в 76% пациенток).
Дополнительные методы исследования мало помогают в постановке диагноза на ранней стадии заболевания. Так, врачи функциональной диагностики при проведении ультразвукового исследования не видят опухоли яичников малых размеров. Её не замечают в 44% случаев лапароскопии, да и это исследование проводится не так часто.
Поставить точный диагноз в 100% случаев можно только с помощью компьютерной и резонансной томографии. Современным методом исследования, который помогает заподозрить рак яичников, является определение в крови онкомаркеров. При этой патологии следует проверить следующие онкомаркеры:
A. НЕ4, который синтезируется раковыми клетками яичников. Повышение его уровня выше граничной нормы в 67% случаев говорит о раке яичника.
B.Β-хорионический гонадотропин человека в норме вырабатывается плацентой беременной женщины. Если его уровень повышается в крови небеременной женщины, то это в 87% случаев свидетельствует о наличии рака яичников.
C.Онкомаркер АФП (α-фетопротеин) не является специфичным маркером. Он в норме синтезируется печенью взрослых людей и детей. С помощью этого онкомаркера оценивают эффективность лечения рака яичников.
D. Эстрадиол – это эстрогенный гормон, который определяется в крови женщин. Повышение уровня эстрадиола может говорить о раке яичников.
Влияние методов лечения на прогноз выживаемости
При операбельных опухолях методом выбора является оперативный метод лечения. Он в 75% случаев дополняется адъювантной полихимиотерапией. Проводится несколько курсов лечения с интервалами в 3-4 недели. 36% пациенткам вначале проводят лечение химиотерапевтическими препаратами, а затем оперативное вмешательство.
Характер операции определяется степенью распространения ракового процесса и зависит от общего состояния пациентки. В 54% случаев выполняют экстирпацию матки, яичников и резекцию большого сальника. При запущенности опухоли хирургическую тактику приходится менять на операционном столе.
В 39% случаев выполняют аднексэктомию, которую дополняют резекцией сальника. Полная циторедукция выполняется в 41% пациенток, оптимальная в 22% случаев, а в 37% случаев приходится ограничиться субоптимальной операцией. У 0,7% пациенток пожилого возраста, у которых имеется 4 стадия рака яичников, возникает необходимость уменьшить объём оперативного вмешательства до минимума: лапаротомии и оменэктомии.
Рак яичников, симптомы и признаки, которого мы обсудили, имеет прогноз, который зависит от многих факторов. На таблице №1 представлены интересные данные.
Таблица №1. Показатели прогноза выживаемости в зависимости от возраста
Как видим, наиболее высокий процент выживаемости у молодых женщин. После шестидесяти пяти летпрогноз становится менее оптимистичным.
Выбор метода операции, как и прогноз выживаемости, зависят от размеров опухоли. Так, при небольших раковых узлах при условии полного комплексного лечения, выживает в течение одного года 93,5% пациенток. Трёхлетняя и пятилетняя выживаемость у этой категории лиц составляет 85%.
При более крупных раковых новообразованиях, которые соответствуют Т2, выживаемость в течение одного года составляет 92%. Показатель трёхлетней выживаемости составляет 71%, а пятилетней – 55%. При объёмных новообразованиях выживаемость в течение одного года равна 76%, трёхлетняя – 33%, а после пяти лет остаются живыми 21% пациенток.
Рассмотрим показатели выживаемости в зависимости от гистологической структуры опухоли. Так, в течение одного года выживает 87% с серозной аденокарциномой, 86,5% с муцинозной, 77% с эндометриоидной, 80% СС светлоклеточной формой рака и 60% пациенток с недифференцированной опухолью. Их трёхлетняя выживаемость, соответственно, выглядит таким образом: 54%, 68%, 46%, 60%, 33%.
В течение пяти лет выживает 41% пациенток, которым диагностирован серозный рак яичников, 68% с муцинозной формой рака, 41% с эндометриоидной, 60% со светлоклеточной опухолью. В случае не дифференцированной формы рака яичников процент выживаемости наиболее низкий: он составляет 33%. На графике №1 показаны показатели пятилетней выживаемости пациенток, у которых выявлены разные стадии рака яичников.
График №1. Зависимость пятилетней выживаемости при раке яичников в зависимости от стадии процесса

Из этого графика можно сделать вывод, что при первой стадии заболевания наилучший показатель выживаемости. Это связано с тем, что, во-первых, опухоль ограничена одним органом, нет метастазов, а, во-вторых, у лиц молодого возраста значительно меньше сопутствующих заболеваний, которые могли бы повлиять на результаты лечения.
Когда заболевание находится в четвёртой стадии, поражаются другие органы и системы организма, появляются симптомы интоксикации, под воздействием которых обостряются хронические болезни. Это усугубляет течение рака яичников. Распространённость опухоли не позволяет применить полный комплекс лечения, что также влияет на выживаемость пациенток.
Также можно проследить зависимость выживаемости от степени дифференциации раковых клеток. ПриG1 степени дифференциации клеток однолетняя выживаемость составляет 88%, при G2 86%, при G3 – 82%, а при G4 60%. Пятилетняя выживаемость при разной степени дифференциации клеток выглядит таким образом: соответственно 58%, 32%, 43% и 33%.
На прогноз выживаемости пациенток при наличии рака яичников непосредственным образом влияет адекватность и полнота применяемого лечения. Так, в случае выполнения радикального оперативного вмешательства и полихимиотерапии при первой стадии рака яичников показатель однолетней выживаемости составляет 79,8%, при комбинации полихимиотерапия+оперативное вмешательство – 89,6%, а после одной только операции выживает 34% пациенток. Важным для прогноза выживаемости является и то, завершена ли была в процессе лечения адъювантная химиотерапия. Так, при завершённом лечении химиопрепарами пятилетняя выживаемость составила 50%, при прерванном лечении – 33,6%.
Как влияет уровень циторедукции на показатель выживаемости можно оценить, исходя из приведенных ниже наблюдений. При полной циторедукции однолетняя выживаемость составила 94,6%, трёхлетняя и пятилетняя – 83,9%. В случае оптимальной циторедукции этот показатель был несколько иным. В течение одного года выжило 89,7% пациенток, в течение трёх лет 52,3%, а в течение пяти лет – 32,2%. Когда же выполнялась субоптимальная циторедукция, то показатель однолетней выживаемости был равен 70%, трёхлетней – 23%, а пятилетней – 12,4%.
Таким образом, рак яичников относится к заболеваниям, которые диагностируются сложно, выявляются поздно и лечатся трудно. Только своевременное обращение к специалисту при появлении первых признаков патологии репродуктивной системы может уберечь женщину от рака яичников.
Рак яичников является одной из наиболее частых злокачественных гинекологических опухолей и составляет 4-ю причину смертности от рака у женщин. Половина всех случаев заболевания приходится на возраст старше 65 лет. Приблизительно 5-10% рака яичников является семейным заболеванием в 3-х наиболее частых вариантах: только рак яичников, рак яичников и молочной железы, рак яичников и толстой кишки. В первую очередь прослеживается наследственность у родственников по 1-й степени (мать, дочь, сестра). Меньший риск существует для женщин 2-й степени родства (бабушка, тетя). При генетических исследованиях обнаруживаются мутации связей в локусе BRCA-1 хромосомы 17g21.
BRCA -2, также отвечающий за возникновение семейного рака яичников и рака молочной железы, расположен в хромосоме 13g12.
Для женщин, имеющих повышенный риск заболевания, старше 35 лет, имеющих детей, может рассматриваться вопрос о профилактической овариэктомии, однако ее значимость до сих пор окончательно не установлена. Описаны случаи заболевания после профилактической операции, первоначально начинающиеся с перитонеальных опухолевых разрастаний, подобных раку яичников.
Особенностью рака яичников являются распространение в брюшную полость путем имплантации клеток и локальная инвазия в мочевой пузырь и кишечник. Частота поражения лимфоузлов составляет 24% при стадии I, 50% — при II, 74% — при III и 73% — при IV стадии. Тазовые лимфоузлы вовлекаются так же часто, как и парааортальные. Опухоль путем трансдиафрагмального распространения может блокировать диафрагмальный лимфоотток, что является причиной асцита и плеврита.
Для больных с I стадией наиболее важна степень морфологической дифференцировки опухоли. Проточный цитометрический анализ ДНК при I и IIA стадиях может выявить группу повышенного риска.
Поскольку в ранних стадиях рак яичников является бессимптомной болезнью, он диагностируется главным образом в поздних стадиях, результатом чего является ранняя смертность примерно у 65% заболевших. При субоптимально операбельной III и IV стадиях 5-летняя выживаемость составляет менее 10% даже при использовании цисплатинсодержащих режимов химиотерапии.
После оптимальных операций при III стадии медиана выживаемости составляет 52-63 мес.
Классификация рака яичников (по FIGO)
I Опухоль ограничена яичниками
IA Опухоль ограничена одним яичником, асцита нет. Нет опухолевых проявлений на внешней поверхности яичника, капсула интактна.
IB Опухоль ограничена двумя яичниками, нет асцита. Нет опухоли на внешней поверхности, капсулы интактны.
IC Опухоль такая же, как в стадиях IA и IB, но с наличием опухоли на поверхности одного или обоих яичников, или нарушением капсулы, или имеется асцит, и/или обнаруживаются опухолевые клетки в перитонеальном смыве.
II Опухоль вовлекает один или оба яичника и распространяется в полость малого таза.
IIA Опухоль характеризуется распространением в матку и/или маточные трубы.
IIB Распространение на другие ткани малого таза.
IIC Опухоль такая же, как в стадиях IIA и IIB, но имеется опухоль на поверхности одного или обоих яичников, или отмечается разрыв капсулы, или асцит, и/или обнаруживаются опухолевые клетки в перитонеальном смыве.
IV Опухоль одного или обоих яичников с отдаленными метастазами. Плеврит с цитологически обнаруживаемыми опухолевыми клетками, паренхиматозные метастазы в печени.
Для диагностики и контроля над эффективностью лечения при эпителиальных опухолях используются такие опухолевые маркеры, как раково-эмбриональный антиген и опухолево-специфический антиген СА-125. Имеется высокая корреляция уровня СА-125 через месяц после 3 курса химиотерапии при III и IV стадиях и выживаемости. В случаях нормализации этого маркера в процессе лечения, повторное повышение маркера определяет активизацию процесса, хотя и не означает необходимость незамедлительного лечения.
Повышенный уровень СА-125 указывает на высокую вероятность рака яичников, в то же время отрицательный ответ не исключает наличие остаточной опухоли. Уровень СА-125 может быть повышен как при других злокачественных опухолях, так и при разных заболеваниях половых органов, например при эндометриозе.
Методы лечения зависят от стадии процесса. Ключевым моментом в лечении является операция. В отличие от других опухолей женских половых органов, стадия процесса при раке яичников устанавливается после хирургического вмешательства. Несмотря на то, что лишь незначительное число больных может быть излечено одной операцией, успех терапии определяется объемом первоначального вмешательства. Возможность достижения в последующем полной ремиссии, подтвержденной морфологически, зависит от размеров остаточных опухолей. Радикальной операцией при раке яичников считается двусторонняя овариосальпингэктомия с экстирпацией матки и удалением большого сальника. У молодых женщин, настаивающих на сохранении репродуктивной функции, при I стадии и 1-й степени злокачественности (G1) возможна односторонняя овариэктомия. Во время операции для уточнения стадии и морфологического варианта берут биопсию из латеральных каналов, тазовой брюшины и диафрагмы, связки, подвешивающей яичник, парааортальных, общих подвздошных, наружных и внутренних подвздошных лимфатических узлов, серозы прямой кишки и мочевого пузыря.
Тактика лечения
Больным с опухолями в IA-IB стадии с высокой или средней степенью дифференцировки (т.е. I-II степенью злокачественности G1 и G2) после операции не требуется дополнительного лечения.
При 3-й степени злокачественности (G3) IC стадии высока вероятность рецидива (до 20%), что требует дополнительных методов лечения.
Возможна системная химиотерапия; внутрибрюшинное введение радиоактивного фосфора 32Р или облучение брюшной полости малого таза. Однако введение 32Р оказалось более токсичным при одинаковой эффективности при сравнении с проведением 6 курсов цисплатина.
Экстирпация или надвлагалищная ампутация матки с придатками с резекцией большого сальника и удалением всех или большинства опухолей. При отсутствии видимых опухолей производят множественные биопсии и смывы из брюшной полости. Дальнейшее лечение включает:
-
При минимальных остаточных опухолях (
Читайте также:

