Лучевой ректит после рака шейки матки
Острые и хронические побочные эффекты возникают после облучения таза, как правило, по поводу рака предстательной железы или женских половых органов. Обычные дозы: рак простаты - 64-74 Гр, рак шейки матки - 45 Гр, рак эндометрия - 45-50 Гр, рак прямой кишки - 25-50,4 Гр, рак мочевого пузыря - 64 Гр.
Очаговое поражение прямой кишки может являться результатом брахитерапии: имплантации радиактивных зерен или внутриполостного облучения. Лучевое поражение может возникать в областях, располагающихся за пределами полей облучения: например, рассеянное облучение может привести к диффузному лучевому энтериту!
Повреждения зависят от общей дозы (обычно > 40 Гр), энергии пучка и очаговой дозы, размера фракции и поля, времени подведения, пролиферации и оксигенации тканей.
В развитии лучевых повреждений выделяют две фазы:
1. Острая: обычно самоограничивающаяся цитотоксичность радикалов и индуцированных повреждений ДНК быстро обновляющихся клеточных популяций (эпителий кишечника, костный мозг, придатки кожи и т.д.).
2. Хроническая: постоянные и необратимые повреждения, связанные с микроишемией в результате облитерирующего эндартериита, дегенерации эндотелия, неоваскуляризации, интерстициального фиброза, разрушения эпителия.
Роль превентивных препаратов (балсалазид, мизопростол, сукральфат и т.д.) при назначении лучевой терапии остается спорной.

а) Эпидемиология:
• Ранние повреждения: 30-70% больных, подвергнутых облучению таза в сроки 
Прямокишечно-влагалищный свищ после лучевой терапии по поводу рака шейки матки
г) Патоморфология лучевого проктита и энтерита
Макроскопическое исследование:
• Гиперемированная/отечная слизистая, некрозы, изъязвления/свищевые отверстия, телеангиэктазии, стриктуры, укорочение кишки.
Микроскопическое исследование:
• Острое повреждение: изъязвление эпителия, мегануклеоз, воспаление собственной пластинки, отсутствие митотической активности.
• Хроническое повреждение: фиброз субинтимы артериол (облитерирующий эндартериит), дегенеративные изменения эндотелия, фиброз собственной пластинки, повреждение крипт, гипертрофия Ауэрбаховского сплетения мышечного слоя кишки.
д) Обследование при воспалении кишки после лучевой терапии
Необходимый минимальный стандарт:
• Ригидная или фибросигмоидоскопия: обычно достаточна для установления диагноза, полный осмотр кишки выполняется по общим показаниям.
• Внимание: биопсия патологических образований/язвы передней локализации противопоказана в связи с риском образования ятрогенного ректовагинального/ректовезикального свища!
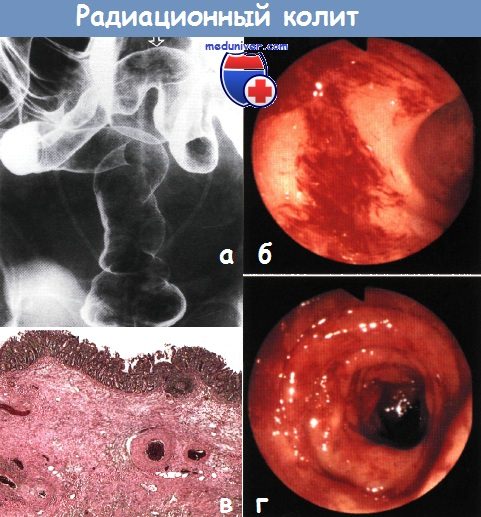
а - Лучевой проктосигмоидит. Ректосигмоидный отдел толстой кишки сужен, трубчатой формы, с потерей клапанов Хьюстона.
Слизистая оболочка ректосигмоидного соединения и дистальной части сигмовидной кишки (показано стрелкой) мелкозернистая. Стенты мочеточников в правильном положении. Клизма с барием, двойное контрастирование.
б,г - Эндоскопическая картина радиационного колита. Диагноз подтвержден наличием множественных телеангиэктазий.
в - Гистологическая картина лучевого энтерита. Наблюдаются подслизистый фиброз и утолщение стенки сосудов без признаков воспаления.
е) Классификация:
• Лучевой проктит: острый или хронический, локализованный или диффузный.
• Лучевой энтерит: острый или хронический, локализованный или диффузный.
• Вторичные осложнения, связанные с облучением (стриктура, свищ и т.д.).
ж) Лечение без операции воспаления кишки после лучевой терапии:
- Острый лучевой проктит: временные меры (регуляция стула, антидиарейные препараты, уход за перианальной кожей) и терпение; местные лекарственные препараты (сукральфат, стероиды или клизмы с ацетилсалициловой кислотой), отключение кишки при тяжелом, плохо переносимом заболевании.
- Хронические лучевые повреждения: лечение отсутствует, плохое состояние тканей => симптоматическая терапия:
• Антидиарейные препараты и спазмолитики.
• Местные противовоспалительные препараты: свечи/клизмы со стероидами, ацетилсалициловой кислотой, сукральфат, мизопростол.
• Пероральные антибиотики: метронидазол.
• Витаминные добавки: витамины С и Е.
• Потенциальные преимущества полного парентерального питания в домашних условиях.
• Восстановление целостности слизистой толстой кишки: клизма с жирными кислотами с короткой цепью (химически нестабильные соединения, малоприменимые на практике).
• Лазерная аблация: необходимость множественных сеансов.
• Инстилляция формалином: нанесение 50 мл 4% раствора формалина на 2-3 минуты на область поражения с последующим обильным промыванием физраствором. Обычно дает быстрые результаты, могут потребоваться повторные сеансы.
з) Операция при лучевом проктите и энтерите
Показания:
• Выраженные и устойчивые к лечению симптомы: кровотечение, тенезмы, отделяемое, инконтиненция.
• Обструкция: формирование стриктуры.
• Формирование свища.
• Невозможность исключения вероятного рецидива опухоли.
Хирургический подход:
• Иссечение области лучевых повреждений с реконструкцией или без (может быть очень сложным).
• Облегчение симптомов без резекции пораженных тканей: отключение пассажа кала/мочи.
и) Результаты лечения воспаления кишки после лучевой терапии:
• Острые лучевые реакции: самокупирующиеся обычно в течение 6-12 недель.
• Хронические лучевые повреждения: часто можно добиться ответа на консервативное лечение, требуются повторные сеансы лечения. В будущем ожидается снижение тяжелых повреждений (более совершенная техника облучения).
• Анастомозы в области облучения: повышенный риск несостоятельности => рекомендуется формирование временной отключающей стомы.
• Отключение кишки: некоторые симптомы (выделение слизи, крови, болевой синдром) могут сохраняться.
к) Наблюдение. Частые визиты до тех пор, пока сохраняется симптоматика. В дальнейшем - обычное наблюдение.
1. Предоперационная ЛТ - применяется у пациенток, когда есть шанс перевода неоперабельной опухоли в операбельную (используется внутриполостное облучение).
2. Послеоперационная ЛТ - выполняется в случаях обнаружения метастазов в регионарных лимфатических узлах или разрастания опухоли за пределы шейки матки (используется дистанционное облучение).
К сожалению, у 20-30% больных РШМ после ЛТ вследствие различных причин формируются лучевые повреждения (ЛП) прямой кишки и мочевого пузыря. Они могут возникать сразу непосредственно после лучевой терапии или в сроки свыше 3-х месяцев после окончания курса (поздние лучевые поражения).
По клиническим проявлениям ЛП прямой кишки и мочевого пузыря различаются на легкие (катаральные, эрозивные) и тяжелые (язвенные и свищевые).
К числу основных факторов, которые определяют вероятность возникновения и степень тяжести ЛП, относятся:
- величина суммарной поглощенной дозы;
- режим фракционирования дозы;
- объем облучаемых тканей;
- сопутствующие заболевания, прежде всего органов, входящих в зону облучения;
- индивидуальная радиочувствительность тканей у конкретной пациентки.
Профилактика
Первым шагом в данном направлении было использование локальной радиомодификации (Г.М. Жаринов, 1993). В клинике Центрального научно-исследовательского рентгенорадиологического института МЗ РФ (ЦНИИРИ МЗ РФ) была разработана система мероприятий по активной профилактике поздних ЛП прямой кишки и мочевого пузыря. Она включает в себя:
- коррекцию общесоматического статуса больных;
- общеукрепляющую терапию, направленную на активизацию иммунозащитных систем организма;
- симптоматическую терапию сопутствующих заболеваний;
- нормализацию функций желудочно-кишечного тракта;
- диагностику и лечение воспалительных процессов урогенитальных органов;
- лечебную физкультуру;
- психотерапию, социальную адаптацию;
- местное применение (внутрипузырное и/или интраректальное) лечебных препаратов (дибунол, смеси витаминов, гидрокортизон, антибиотики, аналгетики, диметилсульфоксид и пр.).
Подобные результаты свидетельствуют о том, что осуществление относительно несложных и недорогостоящих мероприятий у больных РШМ с высоким риском возникновения ЛП, начатое сразу после курса ЛТ, позволяет значительно снизить частоту и степень тяжести поздних ректитов и циститов.
Новые подходы к лечению
Лечение сформировавшихся ЛП прямой кишки и мочевого пузыря представляет серьезную проблему и требует комплексного подхода. Общепринятой для лечения подобных осложнений является методика, разработанная в ЦНИРРИ МЭ РФ (А.А. Габелов, 1970). Она включает в себя коррекцию соматического состояния больной, нормализацию функций кишечника, санацию мочевыводящих путей, а также местного (внутрипузырного и/или интраректального) применения лечебных препаратов. Стандартный курс лечения продолжается 3-4 недели.
Известно, что при проведении лучевой терапии ослабляются репаративные процессы в окружающих опухоль тканях и органах. У онкологических больных значительно снижаются процессы адаптации. В последние десятилетия в клинической практике достаточно широко применяется низкоинтенсивное лазерное излучение. Оно обладает метаболическим, противовоспалительным, анальгетическим, иммуномодулирующим, денсенсибилизирующим и бактерицидным действием. На фоне лазерного воздействия более выражена пролиферация элементов соединительной ткани и эпителия, усиление фибринолитической активности крови, более интенсивное заживление ран (Kleinkort, Foley, 1984; В.П. Арсютов,1989; Гуща с соавт., 1989; А.К. Полонский, 1995). Эффект лазерного воздействия опосредуется сложной гаммой процессов, в числе которых доминируют реакции организма, ответственные за клеточную адаптацию и повышение регенераторного потенциала. Низкоинтенсивный лазер использовался нами для лечения поздних лучевых повреждений прямой кишки и мочевого пузыря у больных раком шейки матки, подвергшихся сочетанной лучевой терапии в различных клиниках Санкт-Петербурга в период с 1979 по 1996 годы. Лазеротерапия применялась у пациенток с катаральными и эрозивно-десквамативными ректитами и циститами. Такой выбор определялся тем, что эффективность лечения ЛП легкой и средней степени тяжести может быть оценена количественно по срокам достижения клинического результата, а также по частоте последующих обострений.
Рак шейки матки является одной из наиболее распространенных опухолей у женщин. На земном шаре ежегодно выявляется около 500 тыс. новых случаев этого заболевания. В 90-95% случаев опухоль имеет гистологическое строение плоско-клеточного рака, в 3-5% - аденокарциномы.
В зависимости от метода лечения все больные были разделены на три группы. Каждая группа состояла из 20 пациенток (10 с катаральными и 10 с эрозивными ректитами и циститами), выбор методики лечения осуществлялся методом "слепого" отбора.
Первой группе пациенток проводилось лечение по стандартной методике. Во второй группе, помимо стандартной терапии, осуществлялось локальное воздействие низкоинтенсивным лазером "Узор-Янис" с длиной волны 890 нм. Использование матричного излучателя с 16 световодами позволило увеличить площадь лазерного воздействия и сместить в глубину область энергетического максимума (Л.Г. Малышева с соавт., 1998). Зонами лазерного воздействия являлись надлобковая и крестцово-ягодичная области. Сеанс лазеротерапии на каждую область продолжался 10 минут, всего за курс лечения проводилось 12-15 лазерных воздействий.
В третьей группе пациенток стандартная - "базовая" - терапия и локальная лазеротерапия сочетались с системным лазерным воздействием, зонами которого были область грудины, шейный, грудной и поясничный отделы позвоночника, подвздошные и седалищные кости, а также кубитальная вена. Продолжительность лазеротерапии на каждую зону составляла 10 минут, курс лечения также состоял из 12-15 сеансов.
В качестве критериев эффекта оценивались сроки исчезновения клинических симптомов лучевых повреждений. Момент полного прекращения болей, макрогематурии и выделения крови из прямой кишки считался началом ремиссии. Все больные после завершения лечения наблюдались не менее двух лет с контрольными осмотрами через 2-3 месяца. Частота обострений, а также время их наступления также являлись количественными характеристиками эффективности проведенного лечения. Среди 20 больных первой группы у 18 (90%) в результате проведенного лечения удалось полностью ликвидировать клинические проявления лучевых повреждений. Средний срок наступления полной ремиссии составил 25+/-4 сут.
Во второй и третьей группах у всех больных удалось добиться наступления полной клинической ремиссии в сроки соответственно 16+/-2 и 10+/-2 сут. По частоте полных ремиссий различий между группами не было. Средние сроки наступления ремиссии достоверно (р
Редким последствием лучевой терапии злокачественных новообразований в районе тазовых органов является постлучевой ректит. Болезнь характеризуется воспалением слизистой оболочки прямой кишки, появлением гнойных, слизистых или кровяных выделений из ануса и болезненными ощущениями перед опорожнением кишечника. Такая патология опасна, т. к. способствует формированию постлучевых стриктур кишечника и вызывает его сужение.
В чем особенность постлучевого ректита?
Патология относится к распространенным формам поражения кишечника при радиационной терапии раковых образований прямой кишки или шейки матки. Лучевые повреждения слизистой кишечника появляются к концу лечебной процедуры и выражаются равномерной или ограниченной гиперемией, отеком и развитием радиоэпителиита. Особенностью постлучевого ректита являются болезненные ложные позывы к опорожнению кишечника при полном отсутствии кала.
Развитие постлучевого ректита диагностируется у 12% онкобольных, получивших лучевую терапию тазовых органов.
Существует две формы течения постлучевого ректита:
- острая;
- хроническая.
Острая форма недуга характеризуется сильной болью в районе тазовых органов и появлением слизисто-гнойных, серозных выделений из ануса. Хроническая форма патологии протекает с периодическими болями в левом передне-боковом отделе брюшной стенки и присутствием слизи в каловых массах. Виды заболевания зависят от стадии развития патологического процесса. Стадия, вид и их характерный признак представлены в таблице:
| Стадия | Вид | Характерный признак |
|---|---|---|
| Начальная | Легкий катаральный | Покраснение и отек слизистой |
| Средняя | Эрозивно-десквамативный | Образование эрозий на слизистой оболочки |
| Тяжелая | Язвенный | Формирование язв и закупорка кишечника |
Влияние радиационной терапии в борьбе с раком тазовых органов является главной причиной развития постлучевого ректита. Спровоцировать развитие такого заболевания способны:
- гамма-терапия онкологии шейки или тела матки;
- рентгенотерапия тазовых органов;
- радиационная терапия онкологических новообразований мочеполовой системы или смежных органов.
Основными признаками постлучевого повреждения прямой кишки являются:
- чувство давления и спазматические боли перед испражнением;
- учащение стула, но чаще чередование диареи и запоров;
- появление в каловых массах слизистых сгустков и крови;
- свербеж и жжение в анальном канале;
- выделение кровяных и слизистых сгустков из ануса;
- кровотечение из анального прохода;
- ложные позывы к дефекации.
На фоне заболевания развивается общая слабость, повышается температура тела, появляется тошнота и рвота. Возникновение такой патологии приводит к полному истощению организма, формированию ректальных свищей, сужению кишечных просветов. Язвенная форма постлучевого ректита приводит к перфорации ректовагинальной перегородки.
При появлении любых симптомов постлучевого ректита необходимо незамедлительно обратиться к специалисту-проктологу.
Какие способы лечения постлучевого ректита?
Лучевой ректит лечится медикаментозно. Лечебная терапия включает:
- применение антибактериальных и антигистаминных лекарственных средств;
- проведение местных противовоспалительных мероприятий;
- употребление витаминных комплексов.
В таблице представлены эффективные фармацевтические средства и их действие на организм больного:
Местные противовоспалительные процедуры являются важной составляющей комплексной терапии постлучевого ректита. Они предусматривают очищение кишечника и ликвидацию воспалительных проявлений. Эффективное лечебное действие оказывают:
Терапию дополняют местным препаратом – свечами с облепиховым маслом.
- клизмы с ромашковым настоем или раствором колларгола;
- микроклизмы с рыбьим жиром;
- ректальные свечи с облепиховым маслом;
- сидячие ванные с применением перманганата калия;
- теплый душ на область промежности;
- питье травяного отвара донника;
- кишечные промывания с раствором серебра или щелочных минеральных вод.
При лечении постлучевого ректита рекомендуется правильно питаться. Необходимо избегать острую, соленую пищу, алкогольные напитки, сладости и увеличить питьевой режим. Если на фоне лучевого ректита формируются свищи, происходит рубцовое сужение кишечника, используются хирургические способы ликвидации патологии. Прогноз на выздоровление преимущественно благоприятный. Профилактика заболевания заключается в применении методик ликвидации онкологических новообразований, оказывающих меньшее негативное влияние на кишечные ткани.
Лучевой проктит — это воспаление прямой кишки, которое возникает на фоне лучевой терапии опухолей органов малого таза. Сопровождается данное состояние болью в прямой кишке и в области заднего прохода, болезненными позывами на дефекацию, диареей, выделением из прямой кишки слизи и крови.
Вероятность лучевого повреждения стенки кишки и развития проктита напрямую связано с суммарной очаговой дозой, полученной при ЛТ. Оптимальная переносимая суммарная очаговая доза в области малого таза составляет 40-50Гр. В этом случае вероятность развития осложнений составляет около 3-5%. При повышении СОД до 65 Гр, лучевой проктит развивается уже у половины пациентов.
- Причины воспаления кишки после лучевой терапии
- Фазы лучевых повреждений
- Классификация лучевого проктита
- Симптомы лучевого проктита
- Как диагностируют лучевой проктит
- Как лечат лучевой проктит
- Прогноз и профилактика лучевого проктита
Причины воспаления кишки после лучевой терапии
Основе лучевых поражений кишки лежат следующие механизмы:
- Повреждение кишечного эпителия, которое развивается под действием ионизирующего излучения. Это приводит к его очаговому некрозу, десквамации (отшелушиванию) и атрофии.
- Развитие неспецифического воспаления слизистой оболочки и подслизистой основы. Ткани инфильтрируются нейтрофилами, наблюдается гиперемия, отечность, кровоточивость.
- Из-за трофических нарушений (повреждаются артериолы) ухудшается кровоснабжение пораженных участков слизистой кишки, что еще больше усугубляет ишемию и некроз. В результате прогрессируют атрофические изменения с развитием фиброза подслизистого слоя.
- На этом фоне начинает присоединяться патогенная флора, которая вызывает инфекционные осложнения, вплоть до сепсиса.
Конечным результатом длительных трофических нарушений стенки кишки и некрозов становится формирование стриктур (сужение просвета), образование свищевых ходов, формирование телеангиоэктазий и развитие кровотечения из них.
Фазы лучевых повреждений
В зависимости от сроков появления, выделяют ранние и поздние лучевые повреждения. Ранние дают о себе знать непосредственно во время проведения лучевой терапии, либо в течение 100 дней с момента ее окончания. Этот период (100 дней, или три месяца) является крайним сроком восстановления эпителия, находящимся в сублетальном повреждении. На этом этапе этиологическим фактором выступает повреждение эпителия кишки с развитием воспалительных реакций. Если доза облучения невелика, эпителий довольно быстро восстанавливается, и, соответственно, слизистая оболочка приходит в норму. В среднем на это уходит около 2-4 недель с момента последнего сеанса облучения.
Поздние лучевые поражения развиваются через 100 дней после окончания ЛТ. В этот период на первое место выходят сосудистые нарушения из-за повреждения эндотелия. Его клетки некротизируются, и чтобы их восстановить, начинают активно пролиферировать оставшиеся эндотелиоциты. Это приводит к облитерации просвета сосудов, развитию тромбозов, ишемии и трофических нарушений. В результате развиваются лучевые васкулиты с кровотечениями, атрофические процессы, фиброзные изменения, разрастание рубцовой ткани.
Классификация лучевого проктита
В зависимости от степени тяжести, выделяют следующие виды лучевых проктитов:
- Катаральный проктит. Во время осмотра обнаруживается гиперемированная рыхлая отечная стенка кишки. Может быть повышенное выделение слизи. Эта форма проктита считается легкой.
- Эрозивно-десквамативный проктит. Эта форма проявляется очагами деструкции эпителия с образованием эрозии — дефекта ткани в пределах эпителиального слоя.
- Язвенный проктит — деструкция распространяется на более глубокие слои ткани и вовлекает в процесс слизистую оболочку с подслизистой основой.
- Свищевой проктит. Образуется сквозная перфорация стенки кишки с выходом в полость малого таза или с вовлечением в процесс рядом расположенных органов, например, мочевого пузыря или влагалища.
Существует классификация лучевого проктита, основанная на ректоскопической картине:
- Имеется локальное покраснение и рыхлость слизистой оболочки кишки, отмечаются телеангиоэктазии расширенные кровеносные сосуды).
- На фоне гиперемии и отечной слизистой кишки обнаруживаются язвы, покрытые серым струпом.
- На фоне воспалительных поражений обнаруживаются стриктуры кишечной стенки.
- На фоне язвенного поражения обнаруживаются стриктуры и свищи или кишечная перфорация.
Симптомы лучевого проктита
Симптомы острого лучевого проктита развиваются в течение 1-2 недель после начала облучения. Это могут быть:
- Диарея.
- Боли в области прямой кишки или внизу живота.
- Болезненные позывы на дефекацию.
- Выделение слизи из анального канала или ее примесь в стуле.
- Анальная инконтиненция.
- Кровотечение. У ряда пациентов кровотечения бывают обильными и приводят к острой геморрагической анемии, которая требует гемотрансфузии.
Если симптомы острого лучевого проктита отсутствуют, это не значит, что не возникнут отдаленные последствия. Частота поздних постлучевых проктитов составляет около 10% от общего числа случаев. При этом присутствует латентный период, который длится несколько месяцев или даже лет. Клиническая картина характеризуется следующими симптомами:
- Боли в правой подвздошной области или в прямой кишке.
- Частый стул, тенезмы.
- Наличие примесей крови в кале.
- При образовании стриктур могут отмечаться запоры и явления частичной кишечной непроходимости.
- При форсировании свищей, отмечаются патологические влагалищные выделения мутного цвета, пневматурия (примеси воздуха в моче), жидкий стул с примесями непереваренной пищи.
В зависимости от тяжести течения, выделяют несколько степеней заболевания:
1 степень — проктит с легким течением. Сопровождается слабо выраженной диареей, менее 5 раз в сутки, может присутствовать выделение небольшого количества слизи и крови.
2 степень — проктит с управляемым течением. Диарея умеренно выраженная, более 5 раз в сутки. Выделяется большое количество слизи, имеются кровотечения.
3 степень — проктит с тяжелым течением. Имеются стриктуры и кровотечения из прямой кишки, требующие хирургического вмешательства.
4 степень это жизнеугрожающее течение, которое требует немедленного вмешательства. Оно сопровождается кишечной непроходимостью, свищами, обильными кровотечениями.
Как диагностируют лучевой проктит
Диагностика заболеваний не представляет труда. Ключевым моментом здесь является наличие в анамнезе лучевой терапии и ее влияние на органы малого таза, учащение стула, и наличие в нем патологических примесей.
При затяжном течении рекомендуется проводить осмотр прямой кишки с помощью ректоскопа или эндоскопа. Это позволит обнаружить множественные эрозии, рубцовую деформацию, атрофические изменения и телеангиоэктазии и решить вопрос о необходимости эндокопического или хирургического лечения.
Как лечат лучевой проктит
При развитии симптомов лучевого проктита во время лучевой терапии, требуется пересмотр схемы облучения. При легком поражении достаточно увеличить интервалы между сеансами. В более тяжелых случаях встает вопрос об уменьшении суммарной очаговой дозы или даже отмене лучевой терапии. Помимо этого, требуется лечение, которое включает в себя несколько направлений:
- Диетическое питание. Важную часть лечения постлучевого проктита занимает диетическое питание. Пища должна содержать повышенное количество белка, достаточное количество макро и микронутриентов. Также она должна быть химически и физически щадящей, т. е. следует отказаться от острых, маринованных, консервированных продуктов. Кроме того, следует избегать грубой растительной клетчатки, чтобы она не травмировала и без того поврежденную стенку кишки.
- Консервативные методы — это медикаментозная терапия, лечебные клизмы, свечи и др. В рамках самостоятельного лечения используется только при легкой и умеренной патологии, в остальных случаях применяется в рамках комплексного лечения совместно с другими методами лечения.
- Эндоскопические методы — радиочастотная аблация, коагуляция аргоновой плазмой и др. В настоящее время эти методы являются золотым стандартом лечения хронических форм заболевания и в основном применяются для устранения кровотечений.
- Хирургические методы — удаление прямой кишки с выведением стомы или наложением колоанального анастомоза. Применяются в тяжелых случаях, когда имеется угроза жизни пациента. Хирургические операции применяются для устранения стриктур, свищей и перфораций стенки кишки.
Для лекарственной терапии используются следующие группы препаратов:
- Глюкокортикостероиды — это основная группа препаратов, применяемых при среднетяжелом и тяжелом течении проктита. ГКС оказывают мощное противовоспалительное действие.
- Анальгетики. Используются разные группы препаратов, в том числе наркотические.
- 5-аминосалициловая кислота (месалазин) — оказывает противовоспалительное и протективное действие, тем самым защищая пораженную слизистую и стимулируя ее восстановление.
- Антидиарейные препараты. Применяются обволакивающие и вяжущие средства, спазмолитики.
- Антибактериальные препараты. Их назначают для лечения или профилактики бактериальных осложнений проктитов.
Учитывая то, что прямая кишка является терминальным отделом пищеварительного тракта, многие препараты местного действия оказываются недостаточно эффективными при применении в формах, предназначенных для перорального приема. Поэтому отдается предпочтение формам для локального применения — свечи, клизмы, порошки и т. д. Они действуют непосредственно на стенку кишки и оказывают эффект в кратчайшие сроки.
Хирургическое лечение направлено на устранение конкретных симптомов или осложнений постлучевого проктита. Это могут быть непрекращающиеся кровотечения, свищи и перфорации кишечной стенки, стрикруты. Очень редко хирургия применяется для устранения неконтролируемой боли.
Перед планированием операции важно учитывать, что радиационные повреждения снижают регенеративные возможности ткани, поэтому есть высокие риски развития осложнений, в том числе кровотечений, плохого заживления раны, присоединения инфекций и ее генерализация, а также долгосрочные отрицательные эффекты типа грубого рубцевания или несостоятельности анального сфинктера.
Таким образом, классические хирургические вмешательства в остром периоде являются рискованными, они не позволяют полностью контролировать кровотечение и могут привести к тяжелым, жизнеугрожающим осложнениям. Поэтому их в основном применяют для устранения отдаленных последствий лучевых проктитов.
Более безопасными являются эндоскопические методы лечения. В их основе лежит деструкция пораженного отдела слизистой кишки с последующим ее некрозом и замещением здоровым эпителием. С этой целью используется в частности используется радиочастотная аблация. В основе метода лежит локальное контролируемое нагревание тканей с целью получения термального ожога. Источником энергии здесь выступают волны радиочастотного диапазона.
Преимуществом эндоскопического лечения является его бескровность, высокая степень контроля при выполнении вмешательства, быстрый результат. Наибольшую эффективность оно оказывает при кровотечениях. Уже с помощью одной процедуры можно коагулировать все патологические кровеносные сосуды и остановить даже обильное кровотечение. Как правило, для максимального результата процедуру проводят 2-3 раза с интервалом в несколько месяцев.
Прогноз и профилактика лучевого проктита
Профилактика лучевого проктита сводится к усовершенствованию технологий проведения лучевой терапии:
В подавляющем большинстве случаев при лучевом проктите прогноз благоприятный — при адекватном лечении заболевание проходит и не сказывается на дальнейшей жизни человека. У 10% пациентов могут развиться тяжелые осложнения в виде свищей, перфораций, некупируемого болевого синдрома, требующие хирургического вмешательства. В ряде случаев необходима экстирпация прямой кишки с наложением анастомоза или выведением колостомы. Последний вариант приводит к инвалидности. Но даже в этом случае есть возможность в отдаленном периоде провести реконструктивную операцию по восстановлению непрерывности кишечника.
Необходимо учитывать, что лучевой проктит может стать препятствием для прохождения полного курса лучевой терапии. В этом случае необходим подбор других методов противоопухолевого лечения.
Читайте также:

