Лимфом на ходжкин трансплантация
Лимфома Ходжкина (лимфогранулематоз) относится к группе злокачественных заболеваний, при которых у большинства больных (детей и взрослых) удается добиться полного излечения с помощью современных программ химио- и лучевой терапии. Наибольшие сложности составляет лечение группы больных с первичной резистентностью (5—10 %) и рецидивами заболевания, особенно ранними (в пределах года с момента достижения ремиссии). Рецидивы наблюдаются у 10—15 % больных лимфомой Ходжкина, из которых приблизительно у половины удается достичь состояния повторной ремиссии даже при использовании резервных схем цитостатической терапии.
В настоящее время стандартом в лечении взрослых больных лимфомой Ходжкина является комбинированная химио- и лучевая терапия. С помощью современных протоколов около 95 % больных с I—II стадией и 70—80 % с III—IV стадией лимфомы Ходжкина могут быть излечены.
В целом эффективность терапии при лимфоме Ходжкина зависит от стадии болезни в момент постановки диагноза и IPI. К неблагоприятным факторам относятся возраст больного 45 лет и старше, мужской пол, IV стадия, содержание гемоглобина менее 105 г/л, альбумина менее 4 г/л, лимфоцитов менее 0,6 • 109/л, количество лейкоцитов в момент постановки диагноза 15- 109/л или более. Другими прогностическими факторами, имеющими значение, являются индекс Карновского, невозможность достижения ПР при использовании стандартных доз химиотерапии. До сих пор не установлено статистически достоверного влияния гистологического варианта лимфомы Ходжкина на отделенные результаты лечения.
С увеличением длительности жизни больных с лимфомой Ходжкина возрастает значение адекватности доз при проведении цитостатической и лучевой терапии, поскольку вероятность развития вторичных опухолей, наиболее часто возникающих в областях рядом с местом лучевого воздействия, зависит от интенсивности цитостатической и лучевой нагрузки. Проблемой отдаленного периода может быть развитие сердечной и легочной недостаточности.
Таким образом, высокодозная цитостатическая терапия с последующей трансплантации гемопоэтических стволовых клеток представляется оправданной только при следующих вариантах течения лимфомы Ходжкина: наличии прогностически неблагоприятных значений IPI, отсутствии ремиссии при проведении стандартной химиотерапии, развитии рецидива лимфомы Ходжкина или первичной резистентности. В подобных случаях терапия иногда бывает безуспешной и не зависящей от дозы применяемых препаратов.
К прогностически неблагоприятным вариантам течения лимфомы Ходжкина относятся III—IV стадии заболевания.
До последнего времени основным вариантом трансплантации гемопоэтических стволовых клеток, используемым у больных с лимфомой Ходжкина, являлась ауто-трансплантации гемопоэтических стволовых клеток (преимущественно ауто-ТПСКК).
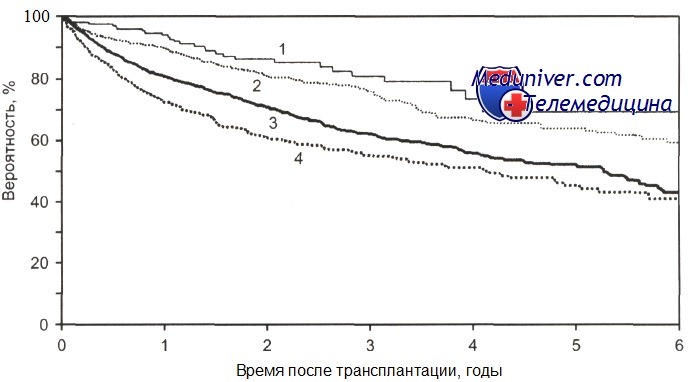
Общая выживаемость после ауто-ТГСК больных с лимфомой Ходжкина в зависимости от стадии болезни.
1-ПР1 (n = 184); 2-ПР2+ (n = 734); 3 - рецидив (n = 1806); 4 — ремиссия не достигнута (n = 632); р = 0,0001.
Проведение ауто-трансплантации гемопоэтических стволовых клеток больным лимфомой Ходжкина I—II стадии возможно только при наличии признаков рецидива, особенно раннего, или первичной резистентности заболевания.
У части больных использование высокодозной химиотерапии с трансплантацией гемопоэтических стволовых клеток ограничено быстрой прогрессией заболевания, возрастом, низким индексом Кар-новского, а также невозможностью получения ауто-логичного трансплантата вследствие значительного снижения клеточности КМ и изменения функционального состояния гемопоэтических стволовых клеток после многочисленных курсов химиотерапии. Наиболее часто это связано с тем, что значительному большинству больных с лимфомой Ходжкина ранее проводилась лучевая терапия, что затрудняет получение аутотрансплантата из костного мозга (КМ). В связи с этим трансплантация гемопоэтических стволовых клеток, выделенных из крови (ауто-ТПСКК), стала при лимфоме Ходжкина методом выбора.
| Автор | Количество больных | Результаты |
| Sweetenham J. et al. | 290 | 30 % 5-летняя БРВ, 34 % 5-летняя ОВ |
| Chopra R. et al. | 46 | 33 % 5-летняя БРВ |
| Reece D. et al. | 30 | 42 % 5-летняя БРВ, 60 % 5-летняя ОВ |
| Yahalom J. et al. | 28 | 33 % 5-летняя БРВ |
| Moreau P. et al. | 28 | 31 % 3-летняя БСВ, 50 % 5-летняя ОВ |
| Gianni A. et al. | 7 | 31 % 6-летняя БРВ, 42 % 6-летняя ОВ |
Наряду с указанным установлено отрицательное влияние следующих прогностических факторов на общую выживаемость больных с лимфомой Ходжкина при ауто-трансплантации гемопоэтических стволовых клеток: наличие В-симптомов, признаки экстранодального поражения, длительность полной ремиссии менее 1 года, низкий индекс Карновского (менее 80 %), отсутствие химиочувствительности и эффекта от двух-трех предшествующих курсов химиотерапии.
По данным CIBMTR, у больных лимфомой Ходжкина без учета стадии заболевания 3-летняя общая выживаемость после ауто-трансплантации гемопоэтических стволовых клеток в ПР1 была 81 %, во второй и последующих ремиссиях —76 %, при рецидиве — 63 %, при первичной резистентности — 55 %.
Факт рецидива отрицательно влияет на общую и безрецидивную выживаемость больных лимфомой Ходжкина. Несмотря на это, по данным различных исследований, у пациентов с рецидивом лимфомы Ходжкина 5-летняя общая выживаемость после ауто-трансплантации гемопоэтических стволовых клеток колеблется в пределах 65—85 % и зависит от интенсивности примененной перед ауто-трансплантации гемопоэтических стволовых клеток химиотерапии. Сохранение химочувстви-тельности опухоли имеет принципиальное значение. В случае отсутствия химиочувствительности лимфомы Ходжкина 5-летняя общая выживаемость после ауто-трансплантации гемопоэтических стволовых клеток составила 26,1 %, при сохранении химиочувствительности — 73,7 %.
| Автор | Количество больных | рецидив менее чем через 12 мес | рецидив более чем через 12 мес |
| Chopra R. et al. | 52 | 41 % | 57 % |
| Bierman P. et al. | 85 | 32% | 47% |
| Reece D. et al. | 58 | 48 % | 85 % |
Эффективность ауто-трансплантации гемопоэтических стволовых клеток при лимфоме Ходжкина исследовали многократно. Изучено прогностическое значение многих факторов. Так, установлено, что отдаленные результаты зависят от стадии болезни и места рецидива в момент проведения трансплантации. При выполнении ауто-трансплантации гемопоэтических стволовых клеток в первом рецидиве 10-летняя безрецидивная выживаемость составила 60 %, при рецидиве в первично-вовлеченной области — 38 %, при IIIВ—IV стадии лимфомы Ходжкина —21 %. По данным другого исследования, при первично-резистентном варианте лимфомы Ходжкина 10-летняя общая выживаемость и безрецидивная выживаемость после ауто-ТГСК составили 55 и 36 % соответственно. Общие результаты ауто-трансплантации гемопоэтических стволовых клеток при неблагоприятных вариантах течения лимфомы Ходжкина представлены в таблицах
Наиболее часто при лимфоме Ходжкина используются режимы кондиционирования: CBV (цикло-фосфан, BCNU, этопозид) и BEAM (BCNU, этопо-зид, цитозар, мелфалан), возможно применение VIP (этопозид, ифосфамид, цисплатин). При режиме кондиционирования CBV 5-летняя общая выживаемость больных с первичной рефрактерностью или рецидивом лимфомы Ходжкина достигает 67 %, при использовании BEAM она составляет 47—70 %.
Таким образом, показанием к трансплантации гемопоэтических стволовых клеток у больных лимфомой Ходжкина являются прогностически неблагоприятные варианты течения болезни. Эффективность трансплантации гемопоэтических стволовых клеток при лимфоме Ходжкина колеблется в среднем от 25 до 80 %, что зависит от индекса IPJ, стадии болезни, места рецидива и сохранения химиочувствительности опухоли.
Пересадка костного мозга при лимфоме является одним из способов лечения. Она позволяет восстановить функции системы кроветворения, избавляет от опасного заболевания. Но процедура отличается высокой степенью сложности, имеет ряд противопоказаний, что сказывается на стоимости трансплантации.
Эффективность пересадки костного мозга при лимфоме

Лимфома – это группа онкологических заболеваний, поражающих лимфатическую систему больного. Развитие злокачественных опухолей наблюдается в любом органе, через который проходит лимфа. Последние годы показали высокую эффективность химиотерапии при лечении этого заболевания. Но для ряда больных единственным шансом остается пересадка костного мозга.
Основные причины гибели костного вещества при лимфоме:
- Поражение при метастазировании на 2–4 стадии. Чаще развивается при неходжкинских лимфомах В-типа.
- Развитие рецидива, при котором клетки новой опухоли не реагирует на применяемые протоколы, уничтожает иммунную систему.
- Клетки костного мозга могут погибнуть при лечении высокодозной химией, превышении допустимой дозы при лучевой терапии.
В этой ситуации костный мозг больного перестает производить кровяные клетки и тельца, полностью отсутствует иммунная защита. Больной может погибнуть от любой инфекции в течение нескольких суток. С помощью трансплантации врачам удается победить аплазию костного мозга, добиться его восстановления и эффективного функционирования.
Трансплантация костного мозга при лимфоме применяется нечасто. Этот метод лечения используется только в ситуациях, когда более простые и доступные терапевтические способы не дают результата. Его эффективность зависит от многих факторов и достигает 80% при лимфоме разного типа. Последние исследования, проводимые онкологическими центрами Беларуси и России, показали уровень стойкой ремиссии у 88,1% людей, перенесших пересадку. Более 51% пациентов живут после процедуры без дополнительной поддерживающей терапии свыше 5 лет.
Виды пересадок костного мозга
В медицинской практике выделяют несколько видов трансплантации:
- пересадка костного мозга;
- введение препарата на основе стволовых клеток;
- переливание пуповинной крови.
При лечении лимфомы пересадка осуществляется разными способами:
- Аутологичным.
- Аллогенным (аллотрансплантация).
Некоторые врачи относят аутологичную пересадку к поддерживающей терапии, которую применяют на 2–3 стадии лимфогранулематоза или лимфомы Ходжкина. Стволовые клетки вводят только при стойкой ремиссии или на стадии, когда метастазы еще не поразили костный мозг больного. В качестве донора выступает сам пациент, что снижает риск отторжения до минимального.
Аллотрансплантация делится на несколько видов:
- Сингенная – забор материала производится от близнеца-донора, генетические данные которого совпадают максимально.
- Гаплоидентичная – успешность операции во многом зависит от уровня совместимости. Поэтому кандидат подбирается из числа близких родственников-доноров с совместимостью 50% и выше (родители, братья, сестры).
- Пересадка от совместимого неродственного донора – при отсутствии других вариантов больному подбирается кандидат из числа людей, генетический материал которых совпадает минимум на 35%.
При аллогенной трансплантации значительно повышен риск отторжения и осложнений после проведения операции.
Пересадка при болезни Ходжкина
Лимфома Ходжкина в большинстве случаев хорошо реагирует на химиотерапию, достигая стойкой ремиссии. Но остается определенный процент больных, которым не помогают традиционные методики лечения. На 2–3 стадии может возникнуть поражение костного мозга, требующее принятия срочных мер. Для данного типа лимфом рекомендуется аутологичный вид трансплантации.
Пересадка костного мозга при лимфоме Ходжкина чаще производится путем переливания специального раствора. Его заранее изготовляют из стволовых клеток больного, которые получают путем фильтрации костного мозга и периферической крови. Перед проведением процедуры больному проводится курс полихимиотерапии, которая помогает остановить развитие онкологии.
Первые результаты появляются через 4–6 недель, когда начинается активная выработка собственных кровяных клеток. Если проведена пересадка костного мозга при лимфоме Ходжкина, прогноз зависит от многих факторов: возраст, наличие хронических болезней, острые инфекции во время реабилитации. Но при отсутствии отторжения длительная ремиссия возникает у 60–80% заболевших, против 0,8–3% без проведения уникальной процедуры.
Трансплантация при неходжкинских лимфомах
При неходжкинских лимфомах поражение костного мозга встречается гораздо чаще, протекает более агрессивно. Оно является результатом распространения метастазов или первичного поражения органа кроветворения.
Основные задачи трансплантации:
- Если наблюдается опухоль с низкой реакцией на химиотерапию, больной может погибнуть при проведении агрессивного лечения. После пересадки костного мозга организм быстрее восстанавливается, вырабатывает здоровые стволовые клетки, выдерживает усиленную терапию, побеждая смертельное заболевание. Методика сочетания аутологической пересадки и интенсивной химиотерапии уже активно применяется в клиниках Израиля и США, показывает хорошие результаты.
- При поражении и гибели костного мозга пересадка остается единственным способом его восстановления: без эффективной работы системы кроветворения больной не выживет даже при устойчивой ремиссии.
Дабы уменьшить риск рецидива после проведения трансплантации, применяется инфузия тромбомассы и лимфоцитов, защищающая от инфекций.
Показания и противопоказания для пациента
Трансплантация костного мозга при лимфоме требуется при лечении наиболее тяжелых видов онкологии:
- неходжкинские лимфомы;
- лимфома Ходжкина;
- миелоидный лейкоз;
- лимфобластная лимфома;
- миелодиспластический синдром.
В европейских онкологических центрах 30% всех пересадок костного мозга приходится на неходжкинские формы, 11% на лимфому Ходжкина.
Но процедура имеет ряд противопоказаний, которые делают трансплантацию невозможной:
- наличие хронических инфекций (мононуклеоза, сифилиса, грибковых патологий);
- опухоль не восприимчива к препаратам химиотерапии, поэтому невозможно провести процесс подготовки к переливанию стволовых клеток от донора;
- иммунная деструкция тромбоцитов, при которой риск отторжения максимальный;
- дисфункция почек или печени, серьезные патологии сердца, способные привести к летальному исходу.
Перед процедурой проводится ряд обследований и анализов, помогающих оценить общее состояния пациента.
Что должен знать донор?
Подавляющее большинство пересадок приходится на костный мозг и стволовые клетки, полученные от неродственного донора. В европейских странах и США существует огромный реестр добровольных кандидатов, который используется для лечения больных лейкемией и лимфомами.
Донорство является добровольной процедурой, поэтому кандидат всегда может отказаться от его проведения. Учитывая высокую стоимость забора и обработки биоматериала, донор должен со всей ответственностью подойти к процедуре, заботиться о своем здоровье.
Он обязан предупредить врачей о любых изменениях, способных повлиять на качество костного мозга:
- перенесенные недавно грипп, ОРВИ;
- менструация;
- последний день приема алкогольных напитков.
После процедуры забора костного мозга донору можно покинуть лечебное учреждение уже на следующий день. Иногда в течение 2–5 суток сохраняется болезненный синдром, который легко снимается обезболивающими препаратами, не требует лечения. На полное восстановление мозгового вещества требуется 14–20 дней. В это время рекомендуется уменьшить физические нагрузки, наполнить рацион полезными продуктами, обогащенными витаминами и минералами.
Показания и противопоказания для донора
Среди потенциальных доноров биоматериала проводится тщательный отбор. Поэтому к забору и допускаются только здоровые люди возрастом от 18 до 45 лет. После донорства костный мозг таких кандидатов восстанавливается быстро без осложнений для здоровья. Как правило, они легко переносят процедуру, понимая всю ответственность и важность решения.
Даже при самой тщательной фильтрации и подготовке остается риск загрязнения инфицированными донорскими клетками. Поэтому при пересадке к потенциальному донору предъявляются строгие требования.
Противопоказаниями являются следующие болезни и патологии:
- аутоиммунные заболевания;
- ВИЧ;
- перенесенный ранее туберкулез, сыпной тиф;
- гепатит С;
- хронические инфекции;
- психические заболевания.
Донором костного мозга при пересадке не может стать человек, имеющий хронические заболевания:
- печени (цирроз, холецистит);
- почек (мочекаменная болезнь, дисфункция);
- гиперплазию щитовидной железы;
- язву желудка или кишечника;
- бронхиальную астму;
- сахарный диабет.
Временными противопоказаниями к включению в донорский реестр становятся переливание крови, поездки в экзотические страны, контакт с носителями вирусного гепатита. Такие кандидаты могут приступить к сдаче анализов только через полгода после события.
Забор донорской кроветворной ткани

Забор материала для последующей трансплантации производится разными способами. Наибольшая концентрация клеток костного мозга у взрослого человека наблюдается в бедренной или подвздошной тазовой кости. Перед процедурой донора госпитализируют, проводят ряд анализов, чтобы убедиться в отсутствии воспалений и инфекций. Все манипуляции проводятся под общей или эпидуральной анестезией.
Для забора ткани хирург делает несколько проколов в кости донора специальной иглой. Через них производится пункция. В среднем за один прием врачам необходимо получить от 15 до 20 мл костного вещества. После выхода из наркоза и оценки общего состояния донор может возвращаться к привычному образу жизни. При таком способе удается получить максимальное количество материала и стволовых клеток всего за 30–40 минут.
Гораздо реже используется методика забора венозной крови. За 2–3 недели потенциальный донор начинает принимать специальные препараты, стимулирующие выброс стволовых клеток. Это повышает ценность биоматериала. После очищения и выделения ценных элементов кровь возвращают донору, что ускоряет процесс восстановления. Среди недостатков метода – на процедуру забора уходит несколько часов, могут наблюдаться головокружения, тошнота, дискомфорт. Кроме того, для получения необходимого объема забор повторяют до 6 раз.
Подготовка и процедура пересадки КМ при лимфоме
Чтобы трансплантация прошла успешно для больного, проводится специальная подготовка. Обязательная часть – проведение нескольких курсов полихимиотерапии в сочетании с облучением.
Предназначение иммуносупрессивной терапии (конденсирования):
- Такое интенсивное лечение позволяет добиться временной ремиссии, во время которой производится трансплантация.
- Необходимо разрушить собственный костный мозг пациента, чтобы освободить пространство для донорского.
- Происходит полное подавление иммунной системы больного, которая может стать причиной быстрого отторжения костного мозга.
Пациента перед трансплантацией помещают в асептическую (стирильную) палату, чтобы не допустить контакта с носителями вирусных или бактериальных заболеваний, попадания в кровь патогенных возбудителей. В этот период проводится процедура подготовки донорской ткани, последние контрольные исследования.
Трансплантация мало напоминает хирургическую операцию: во время процедуры материал из стволовых клеток переливается с помощью капельницы. Он смешивается с кровью пациента, равномерно распределяется по всему организму. Трансплантат оседает в трубчатых костях, запуская процесс формирования здорового костного мозга. Для поддержки организма в этот ответственный период времени проводится вливание тромбоцитов донора, которые уменьшают риск отторжения.
Что происходит после трансплантации КМ?
Ежедневно больному следует сдавать анализы крови: врачи контролируют показатели, отслеживают динамику. Ему проводится поддерживающая терапия с применением антибиотиков, витаминов и антисептиков. Пациент остается в полной изоляции, чтобы исключить заражение инфекцией. В этот период человек испытывает не только физические, но и психологические проблемы, опасаясь осложнений и рецидива лимфомы.
Осложнения и побочные эффекты
Наиболее опасные осложнения, с которыми может столкнуться пациент после пересадки:
- у каждого второго больного через несколько дней начинается отторжение, способное привести к летальному исходу;
- анафилактический шок при аллергии на донорские клетки или тромбоциты;
- инфицирование различными заболевания при отсутствии иммунной защиты;
- происходит отказ почек из-за интоксикации.
В первые 2 недели после процедуры реципиент может столкнуться с побочными эффектами, осложняющими процесс приживления:
- болезненное воспаление слизистой желудка и кишечника;
- сильная слабость, постоянная сонливость;
- головные боли;
- сердечная аритмия;
- проблемы с мочеиспусканием;
- полное отсутствие аппетита.
Для снижения неприятных ощущений реципиенту дают специальные питательные растворы, содержащие необходимые организму вещества и микроэлементы. Они вводятся в кровь, чтобы уменьшить нагрузку на пищеварительную систему.
Питание и диеты до и после проведения процедуры

До трансплантации костного мозга больному рекомендуется легкое питание без большого количества ограничений. Как правило, в этот период проходит химиотерапия, поэтому аппетит практически отсутствует Лучше исключить жареные и жирные блюда, мясо, заменив животные белки творогом.
После пересадки необходимо придерживаться определенных рекомендаций:
- отказ от алкоголя, тонизирующих напитков;
- употребление большого количества овощей, фруктов;
- включение в пищу продуктов, улучшающих состояние крови (свекла, печень, гранатовый сок);
- ежедневное употребление свежих соков, морсов, компотов;
- снижение в рационе сахара, сдобы и сладостей.
До восстановления пищеварения некоторым пациентам рекомендуется употребление детских пюре. Они имеют гомогенизированную структуру, не содержат искусственных добавок и специй.
Прогноз жизни
Пересадка костного мозга при лимфоме или других заболеваниях кроветворной системы проводится с 1990 года.
Многочисленные наблюдения и исследования доказали, что прогноз выживаемости зависит от некоторых факторов:
- возраст (наилучшие результаты фиксируются у детей и молодых людей до 25 лет);
- половая принадлежность (гормональный фон женщины является дополнительной защитой от отторжения);
- степень поражения лимфатической системы при лимфоме.
При онкологии сложно составить прогноз жизни после пересадки костного мозга. Но последние данные показали, что после трансплантации до 80% пациентов прожили от 5 до 8 лет. Свыше 10 лет живет каждый второй пациент, не имевший шанса на выздоровление без трансплантации.
Где можно пройти процедуру в России, какая ее стоимость?
Донорство костного мозга только развивается в России, а реестр доноров насчитывает не более 10 000 кандидатов (против 7 млн. в Германии).
Но существует ряд клиник, которые проводят пересадку при лимфоме на высоком уровне:
Стоимость процедуры складывается из затрат на многочисленные анализы, подготовительный период, реагентов для приготовления препарата из стволовых клеток и многих других факторов. В зависимости от ситуации трансплантация стоит от 1 до 3 млн. рублей.
Если вы нашли ошибку просто выделите ее и нажмите Shift + Enter или нажмите здесь. Большое спасибо!
Спасибо за ваше сообщение. В ближайшее время мы исправим ошибку

Неходжкинская лимфома – большая группа злокачественных заболеваний системы кроветворения, возникающих в результате мутаций ее лимфоидного ростка. Если патологической трансформации подвергаются B-лимфоциты, развивается B-клеточная лимфома, если трансформируются T-лимфоциты, возникает T-клеточная лимфома, а если натуральные киллер-клетки – NK-лимфома. Неходжкинские лимфомы составляют четыре пятых всех лимфом. В девяти случаях из десяти заболевают взрослые люди пожилого возраста.
В каждой из этих групп существует множество подвидов. Например, в группе B-лимфом – наиболее распространенных, составляющих 85% неходжкинских лимфом, различают более 10 различных вариантов. То же относится и к другим видам неходжкинских лимфом.
Столь же разнообразна и клиническая картина заболевания. Лимфома может протекать бурно и агрессивно (при этом она часто хорошо поддается лечению), а может – вяло (индолентно), долго не прогрессируя и даже не требуя лечения, но в то же время эти формы в большинстве своем неизлечимы.
Увеличение лимфоузлов, в первую очередь, подмышечных, паховых, шейных, безболезненное, не исчезающее на фоне антибиотикотерапии и нередко бессимптомное – постоянный признак лимфомы. По расположению и количеству лимфоузлов, вовлеченных в патологический процесс, определяют стадию заболевания.
Симптомы
Среди частых, но необязательных симптомов:
- выраженная общая слабость;
- обильная ночная потливость;
- быстрое и значительное похудение;
- стойкое повышение температуры, иногда более 38 градусов;
- локальные симптомы со стороны органов грудной клетки, брюшной полости, костей как отражение развившихся в них локальных опухолевых очагов.
Таким образом, симптомы неходжкинских лимфом неспецифичны, а формы многочисленны. Поэтому диагностика направлена не только на подтверждение лимфомы как таковой, но и на уточнение ее клинического варианта и стадии, так как от этого зависит тактика ведения пациента. Проводятся:
- клинические анализы крови с микроскопией мазков;
- биохимические анализы крови;
- трепанобиопсия грудины и подвздошных костей для получения образцов костного мозга. Иммунологические, гистохимические и цитогенетические исследования позволяют детально определить все особенности лимфомы у конкретного пациента. Например, мутация B-лимфоцитарного антигена CD-20, ответственного за пролиферацию лимфоцитов, приводит к их неконтролируемому размножению. Если такая мутация выявляется, могут быть назначены таргетные препараты, блокирующие этот ген;
- биопсия лимфоузлов с последующим лабораторным исследованием биоптата;
- компьютерная и магнитно-резонансная томография для первичной диагностики и динамического наблюдения очагов лимфомы в лимфатических узлах и внутренних органах;
- позитронно-эмиссионая компьютерная томография – для раннего выявления метастазов по вновь возникшим очагам аномального метаболизма.
К лечению агрессивных лимфом приступают немедленно по их выявлении, индолентные иногда наблюдают до первых признаков прогрессирования. Современная терапия неходжкинских лимфом включает в разных комбинациях:
- химиотерапию;
- лучевую терапию;
- иммунную терапию;
- трансплантацию костного мозга;
- хирургические методы.
Основу лечения составляет химиотерапия. Как правило, применяются протоколы из нескольких препаратов – полихимиотерапия. Лишь в отдельных случаях у пациентов преклонного возраста с тяжелыми сопутствующими заболеваниями и высокодифференцированными, относительно доброкачественно протекающими лимфомами, может быть проведено лечение единственным средством. Чаще всего применяются схемы из препаратов:
- циклофосфамид, доксорубицин, онковин, преднизолон;
- циклофосфамид, онковин, прокарбазин, преднизолон;
- блеомицин, адриабластин, циклофосфамид, онковин, преднизолон.
Закрепляющая, противорецидивная химиотерапия продолжается после полной нормализации анализов крови и ликвидации клинических проявлений на протяжении двух лет с интервалом в 3 месяца.
Лучевая терапия неходжкинских лимфом назначается ограниченно, в основном для воздействия на крупные локализованные очаги, а также в качестве паллиативной помощи при метастазах в костях.
Хирургические методы применяются индивидуально, в зависимости от локализации очагов лимфомы во внутренних органах и вызванных ими осложнений. Спленэктомия (удаление селезенки) выполняется очень часто, а при первичном ее поражении – практически всегда.
Трансплантация стволовых клеток (пересадка костного мозга) – сложная, но систематически выполняющаяся в иностранных гематологических клиниках процедура. Именно с помощью донорской (а при непораженном костном мозге пациента – и аутогенной) трансплантации там справляются с устойчивыми к химиотерапии, рецидивирующими и особо злокачественными вариантами неходжкинских лимфом. Перед трансплантацией проводится агрессивный курс высокодозной химиотерапии, позволяющий уничтожить практически все злокачественные лимфоидные клетки. Функция крови в дальнейшем восстанавливается благодаря трансплантированному и прижившемуся здоровому костному мозгу.
Трансплантация костного мозга – вмешательство с потенциально высоким риском. В ведущих гематологических центрах мира эти риски удается минимизировать за счет большого опыта и высокой квалификации персонала, регулярно проводящего подобные манипуляции, совершенной методики ее выполнения, а также обеспечения идеальной внешней среды для пациента в критические периоды терапии.
Квалификация специалистов, оснащение гематологических центров и доступность наиболее прогрессивных методов лечения в развитых зарубежных странах позволяют успешно решать наиболее сложные проблемы в лечении неходжкинских лимфом. Это лечение рецидивирующих, распространенных и прогностически неблагоприятных клинических вариантов. Для их преодоления в зарубежных клиниках широко используются иммунотерапия и трансплантация костного мозга, традиционная химиотерапия проводится только оригинальными препаратами. Поэтому полной длительной ремиссии достигают 70-80% пациентов, а 5-летняя выживаемость превышает 90%.
Читайте также:

