Лимфаденопатия при остром лейкозе
Лимфаденопатия (новолат. lymphadenopathia; лимфа + др.-греч. ἀδήν — железа + -патия) — состояние, проявляющееся увеличением лимфатических узлов лимфатической системы. Лимфаденопатия является либо рабочим предварительным диагнозом, требующим уточнения при дальнейшем клиническом обследовании, либо ведущим симптомом заболевания.
По природе увеличения лимфоузлов:
• опухолевые формы;
• неопухолевые формы.
По распространенности процесса:
• локальная лимфаденопатия – это увеличение строго одной группы лимфатических узлов или нескольких групп, расположенных в одной или двух смежных анатомических областях (наличие первичного очага не обязательно);
• генерализованная лимфаденопатия – увеличение лимфатических узлов в двух или более несмежных зонах.
По длительности:
• непродолжительная лимфаденопатия – длящаяся менее 2 мес;
• затяжная лимфаденопатия – длящаяся более 2 мес.
По характеру течения:
• острая;
• хроническая;
• рецидивирующая.
Увеличение лимфатических узлов не всегда является признаком заболевания. У многих людей можно прощупать подчелюстные лимфатические узлы, что обычно связано с наличием заболеваний зубов. Очень часто у здоровых лиц можно пропальпировать небольшие паховые или подмышечные лимфатические узлы.
Каждый такой случай, естественно, должен рассматриваться индивидуально, в контексте всей клинической информации, полученной при работе с пациентом.
Увеличенные лимфатические узлы необходимо отличать от нелимфоидных образований.
Очень часто за увеличенный лимфатический узел принимают кисту – полое опухолевидное образование на передней или боковой поверхности шеи. Не всегда легко диагностируются фибромы – доброкачественные опухоли из соединительной ткани, которые могут иметь различную локализацию и консистенцию. Напоминать увеличенный лимфатический узел может жировая доброкачественная опухоль липома.
У женщин увеличенный лимфоузел могут имитировать добавочные дольки молочной железы.
При болезненности увеличенных подкожных образований и общих признаках интоксикации всегда необходимо исключать гидраденит (гнойное воспаление потовых желез) и панникулит (воспаление подкожной жировой клетчатки).
Основными этиологическими факторами, вызывающими лимфаденопатию, являются:
• инфекции;
• опухолевые поражения (первичные и метастатические);
• иммунопролиферативные заболевания;
• дисметаболические заболевания.
1. Инфекционная лимфаденопатия
Может быть обусловлена как прямым инфекционным поражением лимфатических узлов (инфекционные лимфадениты), так и реактивным воспалением (реактивные лимфадениты).
Во многих случаях лимфаденопатия носит смешанный характер, например, при туберкулезе лимфатических узлов.
2. Реактивные лимфадениты
Возникают на фоне инфекционного очага (при панариции на руках – подмышечный лимфаденит, при рожистом воспалении нижних конечностей – паховый лимфаденит, при ротоглоточной инфекции – подчелюстной лимфаденит). Лечение таких пациентов осуществляется в хирургическом стационаре, при ротоглоточной инфекции – в отделении челюстнолицевой хирургии.
3. Инфекционные лимфадениты
Могут быть:
• бактериальными (гнойный лимфаденит);
• вирусными (инфекционный мононуклеоз, краснуха, гепатит, ЦМВ, ВИЧинфекция, болезнь кошачьих царапин);
• грибковыми (актиномикоз, кокцидиомикоз, гистоплазмоз);
• паразитарными (токсоплазмоз);
• микобактериальными (туберкулез, лепра).
Гнойный лимфаденит проявляется увеличением лимфатических узлов, местной болезненностью, признаками интоксикации, повышением температуры тела. Чаще поражаются подчелюстные, шейные и подмышечные лимфатические узлы, однако возможно поражение лимфоузлов и других локализации. Процесс может быстро распространяться – с развитием аденофлегмоны и даже сепсиса, поэтому лечение должно начинаться максимально рано. Необходима срочная консультация хирурга. Лечение хирургическое – вскрытие, дренирование и санация, проводятся антибиотикотерапия и дезинтоксикационная терапия.
ВИЧ-инфекция – одна из частых причин лимфаденопатии. Заболевание имеет огромное социальное значение. В России каждый четвертый инфицированный ВИЧ не знает о своем заболевании. Обследование на ВИЧ является одним из самых важных элементов в диагностическом процессе у пациентов с лимфаденопатией. Проводится исследование крови на ВИЧ методами ИФА и полимеразной цепной реакции (ПЦР), иммунный блоттинг.
Цитомегаловирусная инфекция (ЦМВ) широко распространена, антитела к ЦМВ выявляются не меннее чем у половины всех взрослых людей планеты. Заболевание часто протекает бессимптомно, может иметь неспецифические проявления (слабость, недомогание и т. д.).
Для выявления ЦМВ проводится ИФА крови на IgM и IgGспецифические антитела к ЦМВ, определяется ДНК ЦМВ методом ПЦР, оценивается индекс авидности (индекс авидности дает возможность определить стадию и вид заболевания).
Токсоплазмоз – хроническая паразитарная инвазия, вызываемая простейшими – токсоплазмами. Инфицированность населения очень высока, в Европе – до 50 %. У большинства заболевание протекает в виде латентной инфекции; существуют также острая и хроническая формы. Проявления зачастую неспецифичны.
Для выявления токсоплазмоза проводится ИФА крови на IgM и IgGспецифические антитела к Toxoplasma gondii, выявляется ДНК Toxoplasma gondii методом ПЦР, определяется индекс авидности.
Инфекционный мононуклеоз – острая вирусная инфекция, вызываемая вирусом Эпштейна – Барр. Проявляется ангиной, увеличением лимфатических узлов, гепатоспленомегалией, возможна пятнистопапулезная сыпь. В общем анализе крови – лейкоцитоз с преобладанием лимфоцитов, моноцитов. Характерным признаком заболевания является появление в крови атипичных мононуклеаров, однако появляются в крови эти клетки зачастую с большим опозданием – до 2–3 нед. Проводится ИФА крови на IgM и IgGспецифические антитела к вирусу Эпштейна – Барр, выявляется ДНК вируса методом ПЦР, определяется индекс авидности.
Туберкулез лимфатических узлов в некоторых случаях возникает без поражения легких и бронхов. Процесс развивается медленно, обычно в течение нескольких месяцев, на фоне общего ухудшения самочувствия.
Выделяют 4 стадии развития: пролиферативная, казеозная, абсцедирующая, свищевая. Может поражаться сразу несколько димфоузлов, формируются так называемые пакеты. Основные локализации туберкулезного лимфаденита: шейный, внутригрудной, внутрибрюшной. Важное значение в диагностике имеет биопсия пораженного лимфоузла (если это возможно). Современная диагностика туберкулеза включает в себя большое количество методов: диаскинтест, проба Манту, МСКТ органов грудной полости, бронхоскопия под местной анестезией, бронхоальвеолярный лаваж с посевом лаважной жидкости на микобактерии туберкулеза (МБТ), микробиологическое исследование мокроты на МБТ с определением лекарственной чувствительности, выявление ДНК МБТ в крови методом ПЦР, трансторакальная биопсия легкого под контролем МСКТ, микробиологическое исследование мочи и ПЦР мочи на МБТ.
4. Опухолевое поражение лимфатических узлов
Опухолевое поражение лимфатических узлов может быть первичным (гемобластозы) или вторичным (метастатическим).
Гемобластозы
Включают:
• лимфопролиферативные опухоли (лимфогранулематоз, неходжкинские лимфомы);
• лейкозы (хронический лимфолейкоз, макроглобулинемия Вальденстрема, острый лейкоз, лимфобластный и нелимфобластный лейкозы).
Лимфогранулематоз (болезнь Ходжкина) – это онкологическое заболевание лимфатической системы, при котором в лимфоидной ткани при микроскопическомо исследовании находят клетки Березовского – Штернберга – Рида.
Проявляется увеличением лимфатических узлов, интоксикацией, лихорадкой, похудением и др.
По локализационному признаку выделяется периферическая, медиастинальная, легочная, абдоминальная, желудочнокишечная, кожная, костная, нервная формы заболевания. Процесс может быть острым и хроническим. Выделяют 4 стадии заболевания: локальную, регионарную, генерализованную, диссеминированную. Подтверждает диагноз биопсия лимфатического узла. Диагностикой и лечением лимфогранулематоза занимаются онкологи.
Неходжинские лимфомы – злокачественные лимфопролиферативные опухоли, отличные от лимфомы Ходжкина. Проявляются увеличением лимфатических узлов, интоксикацией, лихорадкой, похудением и др. Подтверждает диагноз биопсия лимфатического узла. Диагностикой и лечением заболевания занимаются онкологи.
Лейкоз – клональное злокачественное (неопластическое) заболевание костного мозга, проявляющееся значительным увеличением количества кроветворных клеток: низкодифференцированных – при острых лейкозах, созревающих или зрелых – при хронических лейкозах. Бластные незрелые клетки вытесняют нормальные гемопоэтические ростки.
Подтверждает диагноз биопсия костного мозга.
Диагностикой и лечением лейкозов занимаются гематологи.
К этой группе относятся лимфаденопатии:
• при системных заболеваниях (ревматоидный артрит, СКВ, болезнь Стилла, аутоиммунный гепатит и др.);
• при саркоидозе;
• лекарственные (фенитоин, препараты золота и др.);
• поствакцинальные;
• при иммунодефицитных состояниях.
6. Дисметаболические лимфаденопатии
Развиваются при амилоидозе, болезнях накопления (болезнь Гоше, болезнь Ниманна – Пика).
Болезнь Гоше – глюкозилцерамидный липидоз – наследственное заболевание, самая распространенная из лизосомных болезней накопления. Проявляется хронической активацией макрофагальной системы, увеличением количества макрофагов и нарушением их регуляторных функций. Основные клинические проявления: спленомегалия, гепатомегалия, цитопения, поражение костей. Цитопенический синдром проявляется тромбоцитопенией со спонтанными геморрагиями, анемией, лейкопенией. Поражение костей варьирует от бессимптомного до тяжелого остеопороза и ишемических некрозов.
Нейронопатические типы болезни Гоше проявляются нарушением глазодвигательных функций, атаксией, нарушением чувствительности, потерей интеллекта. Диагностикой заболевания занимаются врачигенетики. Возможна эффективная заместительная терапия рекомбинантной глюкоцереброзидазой.
При физикальном обследовании пациента с лимфаденопатией необходимо обратить особое внимание на следующие моменты:
• состояние лимфатических узлов (пальпация периферических лимфатических узлов с оценкой локализации, размера, плотности, спаянности с окружающими тканями, болезненности, цвета кожи над лимфоузлами);
• состояние кожных покровов и видимых слизистых оболочек (цвет, патологические высыпания и образования, следы от кошачьих царапин и укусов насекомых, наличие имплантов и татуировок, воспалительные изменения слизистых оболочек);
• наличие суставного синдрома;
• наличие гепато и/или спленомегалии;
• наличие лихорадки;
• наличие признаков заболеваний системы дыхания, лорорганов, мочеполовой системы и др.
Вопрос нормальных размеров лимфатических узлов является неоднозначным и условным.
Принято считать, что в большинстве случаев у взрослых размеры лимфатических узлов до 1–1,5 см являются нормальными.
Болезненность обычно вызвана воспалением, нагноением, может быть связана с кровоизлиянием и некрозом тканей лимфатического узла. Каменная плотность лимфатического узла обычно является признаком метастатического поражения при раке. Плотные лимфатические узлы встречаются при лимфатических опухолях.
Мягкие лимфатические узлы определяются при воспалении.
Спаянность лимфатических узлов может быть обусловлена неопухолевыми процессами (туберкулез, саркоидоз, паховая лимфогранулема) и опухолями.
При локальной лимфаденопатии необходимо прежде всего исключить местный воспалительный процесс (острый тонзиллит; средний отит; стоматит; экземы; конъюнктивит; острый тромбофлебит; рожистое воспаление; фурункулы, карбункулы; панариции; царапины, укусы и др.). Определение локализации и распространенности лимфаденопатии позволяет предварительно обозначить круг возможных заболеваний и наметить направления диагностического поиска.
За генерализованную лимфаденопатию можно принять увеличение лимфатических узлов, обусловленное несколькими заболеваниями (обычно это одновременное увеличение шейных и паховых лимфатических узлов). При весомых подозрениях на опухоль необходимо сразу же делать биопсию.
Если причину генерализованной лимфаденопатии не удалось установить после полного обследования, она называется необъяснимой и может быть последствием перенесенных инфекционных заболеваний, тяжелых травм, операций. В таких случаях необходимо регулярное наблюдение, при прогрессировании лимфаденопатии в ближайшие месяцы проводится биопсия.
Учитывая сложность и междисциплинарный характер проблемы, необходимо максимально рано, сразу же при выявлении лимфаденопатии, проконсультировать пациента с узкими специалистами:
• хирургом (исключить гнойный лимфангит, реактивный лимфаденит при местном воспалительном процессе);
• стоматологом (исключить заболевание полости рта как причину подчелюстного лимфаденита);
• лорврачом (исключить патологию лорорганов как причину шейного лимфаденита);
• инфекционистом (исключить ВИЧ, бактериальные, вирусные, грибковые и паразитарные заболевания; сепсис и др.);
• фтизиатром (исключить туберкулез);
• онкологом (исключить злокачественное новообразование, лимфогранулематоз, лимфомы);
• гематологом (исключить лейкоз);
• ревматологом (исключить ревматоидный артрит, СКВ и др.).
С диагностикой при лимфаденопатии нельзя медлить! Пациентов с необъяснимой лимфаденопатией, особенно при наличии признаков интоксикации (если исключено инфекционное заболевание), увеличении печени и селезенки, с изменениями показателей периферической крови необходимо сразу отправлять в специализированное гематологическое учреждение (в большинстве случаев это областная клиническая больница).
Лабораторноинструментальное обследование пациента с лимфаденопатией начинается с основных и общедоступных методов исследования:
• общий анализ крови с подсчетом лейкоцитарной формулы;
• общий анализ мочи;
• развернутый биохимический анализ крови (общий белок, альбумины, электрофорез глобулинов, билирубин общий и его фракции, активность аминотрансфераз, щелочной фосфатазы, гаммаглютамилтранспептидазы, мочевина, креатинин, холестерин, триглицериды, глюкоза);
• анализ крови на ВИЧ, сифилис, маркеры вирусных гепатитов В и С;
• рентгенография, а лучше МСКТ грудной клетки;
• УЗИ органов брюшной полости;
• УЗИ лимфатических узлов.
Спектр дальнейших исследований, в общем‑то, неограничен. Наиболее часто используются:
• серологическая и молекулярная диагностика герпесвирусной инфекции (цитомегаловируса, вируса Эпштейна – Барр, вируса простого герпеса 1го, 2го типов);
• серологическая диагностика токсоплазмоза, бартонеллеза (болезнь кошачьей царапины), бруцеллеза, риккетсиозов, боррелиоза и др. инфекционных заболеваний;
• диагностика ревматоидного артрита (ревматоидный фактор класса IgA, IgM, IgG; антитела к циклическому цитруллинированному пептиду (АЦЦП);
• диагностика СКВ (LEклетки, антитела к ДНК, антинуклеарный фактор и др.);
• диагностика туберкулеза (смотри ранее) и т. д.
Особое значение при лимфаденопатии имеет биопсия лимфатического узла с гистологическим, цитологическим, иммуногистохимическим и молекулярнобиологическим исследованиями.
Биопсия лимфатического узла целесообразна, если после проведения неинвазивных исследований диагноз остается неясным.
Нет единого мнения по вопросу размеров лимфатического узла, который подлежит обязательной биопсии. Тем не менее у взрослых при исключении инфекции размер лимфатического узла 3 см обычно рассматривается как показание к биопсии.
Эксцизионная биопсия (то есть удаление лимфатического узла с его последующим всесторонним исследованием) проводится в следующих случаях:
• при высокой вероятности опухолевого поражения по результатам неинвазивного обследования;
• при отсутствии диагноза после выполнения всех неинвазивных исследований и сохраняющейся лимфаденопатии;
• при подозрении на опухолевый генез лимфаденопатии у пациентов с реактивными лимфатическими узлами, прилежащими к опухоли, или реактивными изменениями, предшествующими выявлению лимфатических опухолей;
• при некрозе лимфатического узла по данным морфологического исследования.
Рекомендуется проводить выбор лимфатического узла и биопсию с соблюдением следующих правил:
• для биопсии выбирают максимально увеличенный и измененный лимфатический узел, появившийся первым;
• в случаях наличия конгломерата предпочтительнее частичная резекция опухолевого конгломерата, чем прилежащих отдельных лимфатических узлов;
• при наличии нескольких групп лимфатических узлов порядок выбора следующий:
• надключичный – шейный – подмышечный – паховый;
• перед выполнением биопсии необходимо сформулировать предварительные варианты диагноза, поскольку от этого зависит объем исследований биопсийного материала.
Пункция лимфатического узла может использоваться исключительно как ориентировочный метод диагностики в онкогематологической практике, при выборе лимфатического узла для последующей биопсии. Постановка диагноза лимфопролиферативного заболевания по пункции лимфатического узла принципиально невозможна. Если вопрос касается первичной диагностики, следует выполнять биопсию.
Пункция лимфатического узла используется при следующих показаниях:
• солитарное увеличение лимфатического узла без образования конгломератов (метастатическое поражение лимфатического узлов, как правило, не сопровождается образованием конгломератов) при отсутствии косвенных данных за лимфопролиферативный процесс;
• жидкостный характер образования по ультразвуковым данным или наличие флюктуации
при пальпации.
Лечение зависит от окончательного диагноза, установленного после обследования, единого стандарта лечения лимфаденопатии не существует.
У большинства пациентов симптомы острого лейкоза неспецифичны, однако установление диагноза обычно не вызывает затруднений при изучении анамнеза заболевания, физикальных данных, исследовании периферической крови и миелограммы.
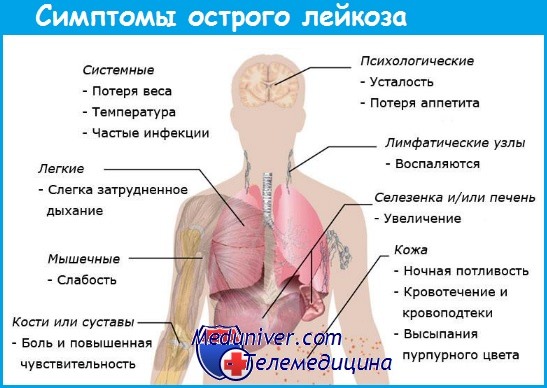
I. Симптомы острого лейкоза:
Слабость, недомогание, одышка; геморрагические проявления от минимальных воздействий и травм;
снижение массы тела;
оссалгии;
боли в животе (редко);
неврологическая симптоматика (редко).
II. Клинические признаки острого лейкоза:
Анемический синдром (слабость, бледность, тахикардия);
геморрагический синдром (экхимозы, петехии, внутренние и наружные кровотечения);
лихорадка и инфекции (пневмония, сепсис, параректальный абсцесс);
лимфоаденопатия, гепатоспленомегалия, расширение средостения;
инфильтрация десен и кожи (редко);
увеличение почек и развитие почечной недостаточности (редко);
поражение мозговых оболочек и черепных нервов (редко).
III. Важные лабораторные и диагностигеские тесты при остром лейкозе
Клинический анализ крови с подсчетом лейкоцитарной формулы;
коагулограмма с определением уровня фибриногена;
биохимические показатели (трансаминазы, креатинин, мочевая кислота, кальций, фосфор, электролиты);
исследование аспирата и трепанобиоптата (не во всех случаях) костного мозга;
определение фенотипа бластных клеток, цитогенетические (по показаниям — молекулярно-генетические) исследования;
анализ спинномозговой жидкости;
рентгенография органов грудной клетки, УЗИ органов брюшной полости, компьютерная томография грудной клетки и брюшной полости (по показаниям — при остром лимфобластном лейкозе);
HLA-типирование (у молодых пациентов).
Дебют острого лейкоза не имеет характерных клинических проявлений. Для детей и молодых людей более типично острое начало, при котором пациентов беспокоят прогрессирующая общая слабость, недомогание, головная боль, одышка, миалгии, оссалгии, реже — боли в животе, лихорадка. В зрелом и пожилом возрасте заболевание обычно развивается медленнее и характеризуется преобладанием симптомов анемии и интоксикации.
Реже первым проявлением острого лейкоза (ОЛ) являются кровоизлияния в кожу, носовые кровотечения, примесь крови при дефекации, кровоточивость слизистых оболочек, гипертрофический гингивит, язвенно-некротический стоматит. Наконец, у 5% больных диагноз устанавливается при исследовании периферической крови по поводу других заболеваний.
При осмотре у большинства больных определяется бледность кожи и слизистых оболочек, обусловленная анемией, и проявления геморрагического синдрома (петехии и/или экхимозы на слизистых оболочках полости рта и на коже, возможны признаки внутреннего кровотечения). Реже отмечается увеличение печени и селезенки, лимфоаденопатия.
При развернутой клинической картине острого лейкоза (ОЛ) в той или иной степени выражены следующие синдромы:
1) синдром опухолевой интоксикации (слабость, утомляемость, снижение массы тела, не связанное с инфекцией повышение температуры тела);
2) анемический синдром (одышка при обычной физической нагрузке, головокружения, бледность кожи и слизистых оболочек);
3) геморрагический синдром (кровоизлияния, кровоточивость слизистых, в тяжелых случаях — профузные кровотечения различной локализации, кровоизлияния в головной мозг);
4) синдром лейкемической пролиферации (оссалгии, увеличение лимфатических узлов, печени, селезенки, гипертрофический гингивит, нейролейкоз);
5) синдром инфекционных осложнений (локальные или генерализованные инфекции).
Инфекционные осложнения (респираторные инфекции, бактериальный сепсис) редко развиваются в дебюте заболевания, но имеют важное практическое и прогностическое значение. Осложнения различной этиологии (бактериальные, вирусные, грибковые) обычно возникают на фоне лечения, наиболее часто при развитии агранулоцитоза и являются одной из основных причин летальных исходов.
Нейролейкоз в большинстве случаев манифестирует менингеальным симптомокомплексом или картиной внутримозговой опухоли (тошнота, рвота, головная боль), значительно реже отмечается изолированное поражение черепных нервов (nn oculomotorius, facialis).
Клинические признаки не позволяют достоверно дифференцировать острый миелобластный лейкоз (ОМЛ) и острый лимфобластный лейкоз (ОЛЛ) без проведения цитохимического и иммунологического исследования бластных клеток. Тем не менее, некоторые симптомы с большей частотой встречаются при определенных вариантах острого лейкоза (ОЛ).
Острые миелоидные лейкозы характеризуются более яркой симптоматикой: у больных обычно выражены интоксикационный, анемический и геморрагический синдромы, чаще развиваются тяжелые инфекционные осложнения. У 90% больных ОПЛ развивается синдром ДВС. Острый моноцитарный, реже миеломоноцитарный лейкоз чаще других вариантов ОМЛ сопровождаются гипертрофическим гингивитом, лимфоаденопатией, появлением лейкемидов на коже и высоким лейкоцитозом.
При остром эритромиелозе ведущим является анемический синдром, макроцитоз и нормоцитоз периферической крови. Острый мегакариобластный лейкоз обычно характеризуется выраженным миелофиброзом, что затрудняет получение аспирата костного мозга и служит основанием для выполнения трепанобиопсии костного мозга с целью верификации диагноза.
Острые лимфобластные лейкозы характеризуются более скудными клиническими проявлениями: в меньшей степени выражены интоксикационный, анемический и геморрагический синдромы, реже возникают инфекционные осложнения. В то же время у больных острым лимфобластным лейкозом (ОЛЛ) значительно чаще отмечаются оссалгии, лимфоаденопатия (в том числе увеличение средостения), гепатоспленомегалия и нейролейкоз.
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
Основная проблема дифференциальной диагностики при ЛДП заключается прежде всего в сходстве клинической картины опухолевых и неопухолевых ЛДП. Лимфадениты и реактивные гиперплазии ЛУ являются важной составляющей синдрома ЛДП. По данным исследования в Гематологическом научном центре Минздравсоцразвития России, неопухолевые ЛДП составляют 30% среди причин первичных обращений к гематологу по поводу увеличенных ЛУ. Нозологический диагноз устанавливается лишь в 50% случаев у больных с неопухолевыми ЛДП.
Основными патологическими процессами, вызывающими увеличение ЛУ, являются инфекции, опухолевые поражения (первичные или метастатические), иммунопролиферативные и дисметаболические процессы (рис. 1).
ЛДП инфекционного происхождения могут быть обусловлены непосредственным инфекционным поражением ЛУ с внедрением инфекционного агента гематогенным или лимфогенным путем в ткань ЛУ (туберкулез, актиномикоз, гнойные лимфадениты, вирусные инфекции) или реактивным воспалением в ответ на инфекционный очаг в соответствующей зоне (подмышечный лимфаденит при панариции, паховый лимфаденит при рожистом воспалении нижней конечности или генитальной инфекции, подчелюстной лимфаденит при ротоглоточной инфекции и т. д.). Четкое разграничение этих 2-х форм в известной степени условно и связано с уровнем диагностического обследования (морфологический, иммунологический, использование ПЦР и др.). При одной и той же инфекции ЛДП может носить как инфекционный, так и реактивный характер (первичный туберкулезный аффект, туберкулез ЛУ).
Опухолевое поражение ЛУ может быть первичным (лимфопролиферативные опухоли) либо вторичным – при лейкозах или раке (метастатический процесс). Опухолевые ЛДП составляют около 70% всех обращений больных в специализированные отделения по поводу увеличения ЛУ.
Иммунопролиферативные ЛДП. Этот термин не является общепринятым и может употребляться в тех случаях, когда увеличение ЛУ не связано ни с инфекцией, ни с опухолевым процессом. При этом в ЛУ происходит пролиферация иммунокомпетентных клеток или гранулематозное воспаление вследствие различных нарушений в системе клеточного, гуморального и неспецифического иммунитета.
Дисметаболические ЛДП обусловлены пролиферацией фагоцитирующих мононуклеаров в ЛУ или отложением амилоида при соответствующих заболеваниях.
Направление диагностического поиска при ЛДП определяется прежде всего клинической ситуаций, т. е. информацией, полученной при первичном осмотре больного (анамнез, физикальное обследование), данными рутинного лабораторного исследования – главным образом показателями периферической крови. При дифференциальной диагностике ЛДП основными ориентирами являются:
- возраст больных;
- анамнестические сведения;
- характер ЛДП (локализация, распространенность, размеры, консистенция, болезненность, подвижность ЛУ);
- наличие других клинических признаков (увеличение селезенки, лихорадка, кожные высыпания, суставной синдром, поражение легких и др.);
- показатели периферической крови.
Каждый из вышеназванных признаков имеет различное и неоднозначное диагностическое значение. Так, лихорадка или анемия у больного с ЛДП могут быть проявлением не только инфекционного и опухолевого процесса, но и некоторых системных васкулитов (системная красная волчанка (СКВ), болезнь Стилла и др.). В то же время выявление в периферической крови бластных клеток практически однозначно свидетельствует о наличии у больного острого лейкоза и требует лишь уточнения его морфологического варианта. Диагностический поиск при ЛДП условно может включать несколько этапов, на каждом из которых решаются конкретные задачи для реализации конечной цели – нозологической диагностики у больного с наличием синдрома ЛДП.
I этап диагностического поиска. Выявление
увеличенного ЛУ и отличие его
от нелимфоидных образований
II этап диагностического поиска.
После верификации выявленного образования увеличенного ЛУ необходимо определить различную локализацию и оценить распространенность ЛДП. Это может иметь значение в определении направления дальнейшего диагностического поиска.
Локализация увеличенных ЛУ позволяет заподозрить круг заболеваний с целью проведения дальнейшего целенаправленного исследования. Так, заднешейные ЛУ обычно увеличиваются при инфекциях волосистой части головы, токсоплазмозе и краснухе, в то время как увеличение передних (околоушных) ЛУ предполагает инфекцию век и конъюнктивальной оболочки. Часто выявляемое местное увеличение шейных ЛУ является следствием инфекций верхних дыхательных путей, носоглотки, инфекционного мононуклеоза, однако при этом необходимо также исключать как лимфопролиферативные опухоли (лимфогранулематоз), так и метастазы в ЛУ опухолей различной локализации (голова и шея, легкие, молочная и щитовидная железы). В то же время увеличение надключичных и предлестничных ЛУ практически никогда не бывает реактивным, а чаще связано с лимфопролиферативными опухолями (лимфогранулематоз), метастатическим опухолевым процессом (опухоли желудка, яичников, легких, молочных желез).
В зависимости от распространенности следует различать следующие варианты ЛДП:
- локальная – увеличение одного ЛУ в одной из областей (единичные шейные, надключичные ЛУ);
- региональная – увеличение нескольких ЛУ одной или двух смежных областей (надключичные и подмышечные, надключичные и шейные, затылочные и подчелюстные ЛУ и т. д.);
- генерализованная – увеличение ЛУ трех и более областей (шейные, надключичные, подмышечные, паховые и др.).
При всей относительности такого разделения распространенность ЛДП может иметь значение при выдвижении предварительной диагностической гипотезы после первичного осмотра больного.
Анатомическое положение ЛУ при локализованной ЛДП позволяет во многих случаях сузить дифференциально-диагностический поиск. Так, например, для болезни кошачьих царапин характерно поражение шейных и подмышечных, а при инфекциях, передающихся половым путем, – паховых ЛУ. Увеличение одного ЛУ чаще требует исключения первичного или метастатического опухолевого процесса; может являться реактивным ответом на местный инфекционно-воспалительный процесс в соответствующей области (реактивный паховый лимфаденит при генитальных инфекциях, увеличение подчелюстных ЛУ при остром тонзиллите и т. д.). Регионарная ЛДП с преимущественным увеличением затылочных и заднешейных ЛУ более характерна для инфекционного мононуклеоза. Генерализованная ЛДП выявляется при различных заболеваниях: инфекционных (вирусные инфекции, токсоплазмоз), системных (СКВ), лимфопролиферативных опухолях (хронический лимфолейкоз).
Наряду с распространенностью ЛДП необходимо оценить размеры и консистенцию ЛУ. Это не является определяющими признаками, однако может служить обоснованием при выдвижении предварительной диагностической гипотезы (подозрение на опухолевый процесс при наличии плотного ЛУ размером более 1 см, болезненность при воспалении, флуктуация при абсцедировании и т. д.).
III этап диагностического поиска.
При определении направления диагностического поиска важным является наличие у больного дополнительных клинических признаков, выявляемых при первичном осмотре (анамнестические, клинические) и проведении рутинного лабораторно-инструментального исследования (рентгенография грудной клетки, общий анализ крови).
Анамнестические сведения (травма конечностей, оперативные вмешательства, наличие имплантата, путешествия, контакт с некоторыми больными и т. д.) позволяют определить направление диагностического поиска, а в ряде случаев могут приобретать решающее значение при дифференциальной диагностике ЛДП (наличие у больного заболевания, проявляющегося увеличением ЛУ, прием некоторых медикаментов).
Клинические признаки. Необходимо тщательное клиническое обследование пациента с ЛДП с целью выявления различных дополнительных симптомов, среди которых диагностически наиболее важными являются:
- поражения кожи и слизистых (макулезно-папулезные высыпания, геморрагии, царапины, укусы, язвы и др.);
- увеличение печени;
- спленомегалия;
- суставной синдром;
- лихорадка;
- респираторная симптоматика;
- изменения со стороны ЛОР-органов;
- урогенитальные симптомы.
Выявление увеличенной селезенки у больного ЛДП более характерно для вирусных инфекций (инфекционный мононуклеоз), острого и хронического лимфолейкоза, системных заболеваний (СКВ, болезнь Стилла у взрослых). Суставной синдром чаще ассоциируется с системными заболеваниями (ревматоидный артрит, СКВ, болезнь Стилла). Наличие кожных высыпаний в первую очередь требует исключения вирусных инфекций, СКВ, болезни Стилла.
IV этап диагностического поиска.
Исследование периферической крови
Среди рутинных лабораторных методов дифференциальной диагностики у больных ЛДП обязательным является исследование показателей периферической крови. При трактовке выявленных изменений периферической крови необходимо учитывать их неодинаковую специфичность. Так, стойкий абсолютный лимфоцитоз с наличием клеток Гумпрехта является патогномоничным лабораторным признаком хронического лимфолейкоза, а наличие бластных клеток в крови может свидетельствовать либо о лимфобластном лейкозе, либо о лейкемизации лимфом. Такие признаки, как нейтрофильный лейкоцитоз, лейкопения (нейтропения), тромбоцитопения не являются специфичными, поскольку могут встречаться при более широком круге заболеваний, сопровождающихся ЛДП (табл. 1).
Наряду с общим анализом периферической крови при первичном обращении больного с ЛДП обязательными исследованиями являются: рентгенологическое исследование грудной клетки, УЗИ органов брюшной полости, иммуно-серологические исследования (сифилис, ВИЧ-инфекция, гепатит В и С). На рисунках 2 и 3 представлены алгоритмы диагностического поиска при локальных (регионарных) и генерализованных ЛДП.
Трудности дифференциальной диагностики при локальной или регионарной ЛДП заключаются прежде всего в умении выявлять местный воспалительный процесс инфекционного (чаще) или неинфекционного характера и ассоциировать выявленную местную патологию с увеличением ЛУ соответствующей области. Наиболее частыми местными воспалительными процессами, сопровождающимися увеличением регионарных ЛУ, на выявление которых необходимо ориентироваться, являются следующие:
- острый тонзиллит (тонзиллофарингит);
- стоматит;
- средние отиты;
- экземы лица, конечностей;
- конъюнктивит;
- острые тромбофлебиты конечностей;
- рожистое воспаление (лицо, конечности);
- фурункулы, карбункулы;
- панариции;
- царапины, укусы;
- воспалительный процесс наружных гениталий.
При выявлении местного воспалительного процесса у больных с увеличением регионарных ЛУ ситуация расценивается как реактивный лимфаденит. Методы цитологической и гистологической диагностики в острой фазе заболевания малоинформативны из-за трудностей трактовки морфологической картины на фоне реактивной гиперплазии лимфоидной ткани. Для окончательной верификации природы ЛДП необходима оценка динамики локального воспаления и регионарной ЛДП на фоне проводимой терапии (антибиотики, хирургическое лечение) или спонтанного обратного развития. В случаях сохраняющегося увеличения ЛУ, несмотря на регрессию местного воспалительного процесса, особенно при наличии ЛУ плотной консистенции, показана биопсия ЛУ для гистологического исследования. На рисунке 4 представлено диагностическое значение дополнительных клинических признаков, выявляемых при первичном осмотре у больных ЛДП.
Дополнительные методы обследования следует применять с учетом предварительной диагностической гипотезы, выдвинутой на основании характера ЛДП, наличия дополнительных признаков (анамнестических, клинических, лабораторных). Назначение антибиотиков больным с ЛДП показано только в случаях доказанной бактериальной инфекции. Применение глюкокортикоидов при неясных ЛДП нецелесообразно.
Литература
Только для зарегистрированных пользователей
Читайте также:

