Амелобластическая карцинома что это
Амелобластическая карцинома – редкая злокачественная (раковая) опухоль, которая, как правило, начинает развиваться в костях челюсти. Эта опухоль является одонтогенной, это означает, что она возникает из эпителия, который формирует эмаль зубов. Особенности этого типа рака могут включать в себя прогрессивную боль и отек челюсти. Амелобластические карциномы могут метастазировать.
Амелобластическая карцинома. Эпидемиология
Амелобластическая карцинома развивается у лиц обоих полов и в равном соотношении. Они могут развиваться у лиц любого возраста, включая детей, но средний возраст, в котором чаще всего отмечается развитие этого рака – 30 лет.
Амелобластическая карцинома. Причины
Точная причина развития амелобластических карцином неизвестна. В большинстве случаев они возникают спонтанно. Исследователи предполагают, что генетические и иммунологические нарушения, факторы окружающей среды (например, воздействие ультрафиолетовых лучей, некоторых химических веществ, ионизирующего излучения), диета, стресс и / или другие факторы могут играть роль в содействии развития определенных типов рака.
Чаще всего, амелобластические карциномы развиваются из эпителиальной ткани, которая остается после развития зубов и из связанных с ними структур. В некоторых случаях, эти карциномы появляются по ходу злокачественной трансформации адамантином или доброкачественной одонтогенной кисты.
Амелобластическая карцинома. Похожие расстройства
- Адамантинома – редкое расстройство, оно характеризуется разрастанием ткани в области челюсти. Эти опухоли не злокачественные, но рост этой ткани может быть агрессивным. В некоторых случаях, эти опухоли могут проникнуть в область вокруг пазух и в глазницы.
Амелобластическая карцинома. Фото

Предоперационная фотография. Отек в области верхней челюсти справа.


Удаленная опухоль (максиллэктомия)

Послеоперационный фотография (спустя 6 месяцев)
Амелобластическая карцинома. Симптомы и проявления
Некоторые лица не испытывают никаких симптомов. Но другие (их большинство), испытывают прогрессивную боль, отек челюсти, кровотечения и головные боли. Редкие особенности этого типа рака включают: неспособность открыть рот (тризм) или дисфония, голосовые расстройства, слабость, покалывание или онемение (парестезии) и, в редких случаях, потеря голоса, закупорка носовых проходов (если опухоль проникнет в пазухи верхней челюсти).
Чаще всего, амелобластические карциномы развиваются в нижней челюсти. В одном известном случае, пациент развил эту опухоль в основании черепа. Амелобластические карциномы часто агрессивны и могут распространяться (метастазировать) в другие участки тела, особенно в легкие, что может привести к развитию угрожающих жизни осложнений. Кости, печень и мозг являются самыми распространенными местами, в которые метастазирует этот рак. Наиболее распространенным течением заболевания является стойкость рецидивов с местным распространением.
Амелобластическая карцинома. Фото




Это фото было сделано через 8 месяцев. У пациента развился рецидив с распространением опухоли в область шеи
Амелобластическая карцинома. Диагностика
В большинстве случаев амелобластичекая карцинома диагностируется случайно. Для подтверждения этого диагноза чаще всего проводят пункционную биопсию. В дополнение к биопсии, врачи могут использовать различные визуализационные методы, которыми можно оценить размер, локализацию и расширение опухоли. Такие методы визуализации включают: компьютерная томография (КТ), магнитно-резонансная томография (МРТ), рентгенография.
Амелобластическая карцинома. Лечение
Конкретные терапевтические процедуры и меры могут изменяться в зависимости от многих факторов (местоположение основной опухоли, степень первичной опухоли, степень злокачественности, метастазы и / или другие факторы). Первым шагом в лечении пациентов всегда является широкое хирургическое иссечение. После того как операция будет проведена, врачи могут применить лучевую терапию для уничтожения оставшихся раковых клеток. Лучевую терапию также можно выполнить и перед операцией, для уменьшения размера опухоли.
К сожалению, рецидив амелобластической карциномы является относительно частым событием и в таких ситуациях может произойти быстрое метастазирование рака. Чаще всего, рецидивы наблюдаются в той же области в которой удалялась первоначальная опухоль. Рецидив может произойти как через год так и спустя несколько лет (с момента хирургического удаления). Из-за высокого риска рецидива, пациенты должны пожизненно проходить медицинские осмотры.
Что касается химиотерапии, то она неэффективна в лечении людей с амелобластическими карциномами.
Амелобластома – доброкачественная опухоль челюстно-лицевой области, сопровождающаяся разрушением костной ткани. Это одна из самых распространенных в хирургической стоматологии опухолей. Более чем в 80% случаев амелобластома локализуется в нижней челюсти.
Заболевание с одинаковой частотой поражает как мужчин, так и женщин в возрасте от 20 до 60 лет, изредка встречается у детей и подростков.
Причины
Точные причины появления амелобластомы на сегодняшний день не установлены. Многие специалисты считают, что ее возникновение связано с нарушением развития зубных зачатков.
При ранней диагностике и своевременном хирургическом лечении прогноз амелобластомы благоприятный.
Формы заболевания
В зависимости от особенностей клинического течения выделяются две формы заболевания:
- Кистозная амелобластома. Диагностируется наиболее часто. Характерны частично соединенные между собой или полностью изолированные друг от друга кистозные образования, изнутри выстланные эпителиальной тканью.
- Массивная (солидная) амелобластома. Особенность данной разновидности – губчатое строение ткани.
Симптомы
Амелобластома развивается медленно. По мере роста опухоли происходит деформация челюсти, которая проявляется припухлостью лица со стороны поражения, прогрессирующим нарушением симметрии.
Более чем в 80% случаев амелобластома локализуется в нижней челюсти.
Визуальные изменения при верхнечелюстной локализации амелобластомы малозаметны, так как опухоль растет не наружу, а внутрь гайморовой пазухи. При этом наблюдается деформация твердого неба и альвеолярного отростка. Опухоль может распространяться в глазницу и (или) полость носа.
Прорастая внутрь костной ткани, амелобластома повреждает ее и сдавливает нервные окончания, что приводит к появлению болевого синдрома. Пациенты ошибочно связывают болевые ощущения с заболеваниями зубов (кариесом, пульпитом). Разрушение костной ткани становится причиной расшатывания, а затем и смещения зубов, деформации челюсти в области поражения.
Кожные покровы, покрывающие амелобластому, продолжительное время остаются подвижными и не имеют видимых изменений, легко собираются в складку.
Диагностика
Диагностика амелобластомы проводится стоматологом на основании характерных клинических проявлений, а также данных инструментально-лабораторного обследования. Для диагностики применяются следующие методы:
- компьютерная томография;
- рентгенография;
- цитологический анализ материала, полученного при проведении диагностической пункции образования (биопсия).
Амелобластома требует дифференциальной диагностики с плоскоклеточным раком челюстно-лицевой области, цистаденоидной карциномой слюнной железы, дентальными кистами, вызванными воспалительным процессом.
Амелобластома может перерождаться в злокачественную опухоль. Малигнизация наблюдается в 4–5% случаев.
Лечение
Лечение амелобластомы хирургическое. В ходе операции производится резекция пораженного опухолью участка челюсти. При ранней диагностике объем оперативного вмешательства минимален, после операции функции челюсти сохраняются, обезображивания лица не происходит. Если же опухоль достигла значительных размеров, то клинические и эстетические результаты хирургического лечения снижаются.
Амелобластома склонна к рецидивам. Для предотвращения повторного роста опухоли после ее удаления операционная полость тщательно обрабатывается концентрированным раствором фенола, что позволяет добиться гибели эпителиальных элементов амелобластомы, которые могут оставаться после резекции.
При значительной резекции челюсти и обезображивании лица в дальнейшем возникает необходимость в костной пластике или постоянном ношении ортопедических конструкций.
Возможные осложнения и последствия
Амелобластома нередко осложняется воспалительным процессом, приводящим к образованию свищей с серозно-гнойным отделяемым, открывающихся в ротовую полость.
Амелобластома может перерождаться в злокачественную опухоль. Малигнизация наблюдается в 4–5% случаев и обычно возникает у пациентов, которые не получали лечения.
Прогноз
При ранней диагностике и своевременном хирургическом лечении прогноз в целом благоприятный.
При удалении значительных по своему объему амелобластом многие пациенты в послеоперационном периоде испытывают психологический шок от изменившейся внешности и нуждаются в психотерапевтической помощи.
Профилактика
Специфической профилактики амелобластом не существует. С целью раннего выявления опухоли необходимо раз в полгода посещать стоматолога для профилактического осмотра.

Образование: окончила Ташкентский государственный медицинский институт по специальности лечебное дело в 1991 году. Неоднократно проходила курсы повышения квалификации.
Опыт работы: врач анестезиолог-реаниматолог городского родильного комплекса, врач реаниматолог отделения гемодиализа.
Информация является обобщенной и предоставляется в ознакомительных целях. При первых признаках болезни обратитесь к врачу. Самолечение опасно для здоровья!
У 5% пациентов антидепрессант Кломипрамин вызывает оргазм.
В Великобритании есть закон, согласно которому хирург может отказаться делать пациенту операцию, если он курит или имеет избыточный вес. Человек должен отказаться от вредных привычек, и тогда, возможно, ему не потребуется оперативное вмешательство.
Наши почки способны очистить за одну минуту три литра крови.
Многие наркотики изначально продвигались на рынке, как лекарства. Героин, например, изначально был выведен на рынок как лекарство от детского кашля. А кокаин рекомендовался врачами в качестве анестезии и как средство повышающее выносливость.
Желудок человека неплохо справляется с посторонними предметами и без врачебного вмешательства. Известно, что желудочный сок способен растворять даже монеты.
Люди, которые привыкли регулярно завтракать, гораздо реже страдают ожирением.
Самое редкое заболевание – болезнь Куру. Болеют ей только представители племени фор в Новой Гвинее. Больной умирает от смеха. Считается, что причиной возникновения болезни является поедание человеческого мозга.
Человеческие кости крепче бетона в четыре раза.
Согласно исследованиям, женщины, выпивающие несколько стаканов пива или вина в неделю, имеют повышенный риск заболеть раком груди.
Ученые из Оксфордского университета провели ряд исследований, в ходе которых пришли к выводу, что вегетарианство может быть вредно для человеческого мозга, так как приводит к снижению его массы. Поэтому ученые рекомендуют не исключать полностью из своего рациона рыбу и мясо.
В течение жизни среднестатистический человек вырабатывает ни много ни мало два больших бассейна слюны.
Даже если сердце человека не бьется, то он все равно может жить в течение долгого промежутка времени, что и продемонстрировал нам норвежский рыбак Ян Ревсдал. Его "мотор" остановился на 4 часа после того как рыбак заблудился и заснул в снегу.
Большинство женщин способно получать больше удовольствия от созерцания своего красивого тела в зеркале, чем от секса. Так что, женщины, стремитесь к стройности.
Согласно мнению многих ученых, витаминные комплексы практически бесполезны для человека.
Для того чтобы сказать даже самые короткие и простые слова, мы задействуем 72 мышцы.
Любой чай подразумевает натуральный продукт, который состоит из различных трав, цветов, измельченных плодов и специй. Сегодня выпускаются специальные виды напит.
Амелобластома (адамантинома) относится к самой часто встречаемой форме одонтогенной опухоли, которая формируется в нижней челюсти и поражает моляры и премоляры.
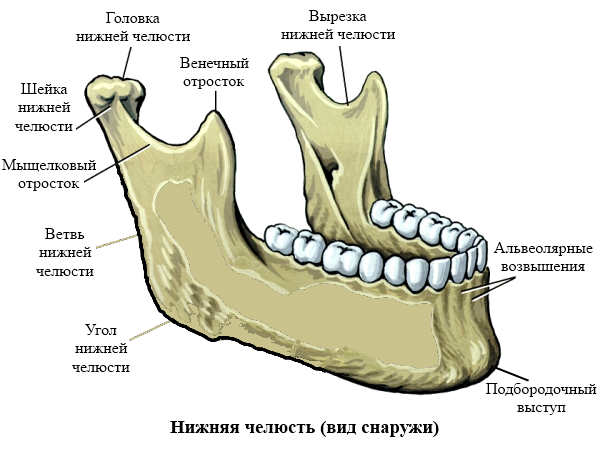
- Что такое амелобластома
- Этиология амелобластомы
- Классификация новообразования
- Симптомы патологии
- Диагностика заболевания
- Лечение
- Прогноз заболевания
- Профилактика болезни
Что такое амелобластома
Амелобластома (код по МКБ 10 – D16.4) относится к доброкачественным опухолям челюстно-лицевой локализации, которые вызывают деструкцию костной ткани. При развитии опухоли наблюдается асимметрия лица, постепенная деформация челюсти, смещение и расшатывание зубного ряда, нарушение функции жевания. Чаще всего, — более чем в 80% случаев, — встречается амелобластома нижней челюсти, амелобластома верхней челюсти – значительно реже.
Данная патология встречается одинаково часто у женщин и у мужчин в возрасте 20–60 лет. Но не исключается развитие патологии у детей и подростков – у них такая патология встречается в 6-7% случаев от числа всех доброкачественных образований подобной локализации.
У большинства пациентов амелобластома диагностируется на начальных этапах (1–6 месяцев), что считается важным условием успешного лечения. Часто патологию обнаруживают при проведении рентгенографии по поводу другого заболевания стоматологического течения.
Но бывают случаи, когда амелобластома диагностируется на поздних сроках, когда новообразованию – год и более. Это новообразование часто дает рецидивы, а при неблагоприятном течении и запущенной форме возможно перерождение данной опухоли в злокачественную.
Ведущие клиники в Израиле



Этиология амелобластомы
Точные причины начала развития амелобластомы не установлены. Существует несколько предположений о причинах появления такой опухоли. Одна из версий появления заболевания связана с патологией формирования зубного зачатка. Этот орган напоминает своей структурой колпачок, внутри которого развивается зачаток зуба. Постепенно эпителиальный внутренний слой становится толще, а клетки образуют твердую эмаль. Как только зуб прорезается — эмалевый орган исчезает. Но иногда часть клеток органа остается, и из них начинает формироваться амелобластома.
Другая версия говорит о том, что амелобластома появляется из одонтогенных остатков эпителия (так называемых островков Малассе).
Факторами, которые дополнительно способствуют появлению опухоли, считаются:
- инфекционное поражение зубов, десен;
- травмы ротовой полости или челюсти;
- различные вирусные заболевания.
Классификация новообразования
Определяют две формы патологии – кистозную (поликистозную) и массивную (солидную).
Кистозная форма встречается чаще, для нее характерно наличие одиночных или частично соединенных кист (полостей), внутренняя поверхность которых выстлана тонким эпителием. В сообщающихся камерах есть прослойки мягких тканей, коллоидоподобное вещество или буроватая жидкость.
Массивная форма характеризуется присутствием губчатой ткани и иногда неопределяемых рентгенологически кист разной величины, которые при продолжительном развитии патологии могут сливаться в несколько крупных или одну полость.
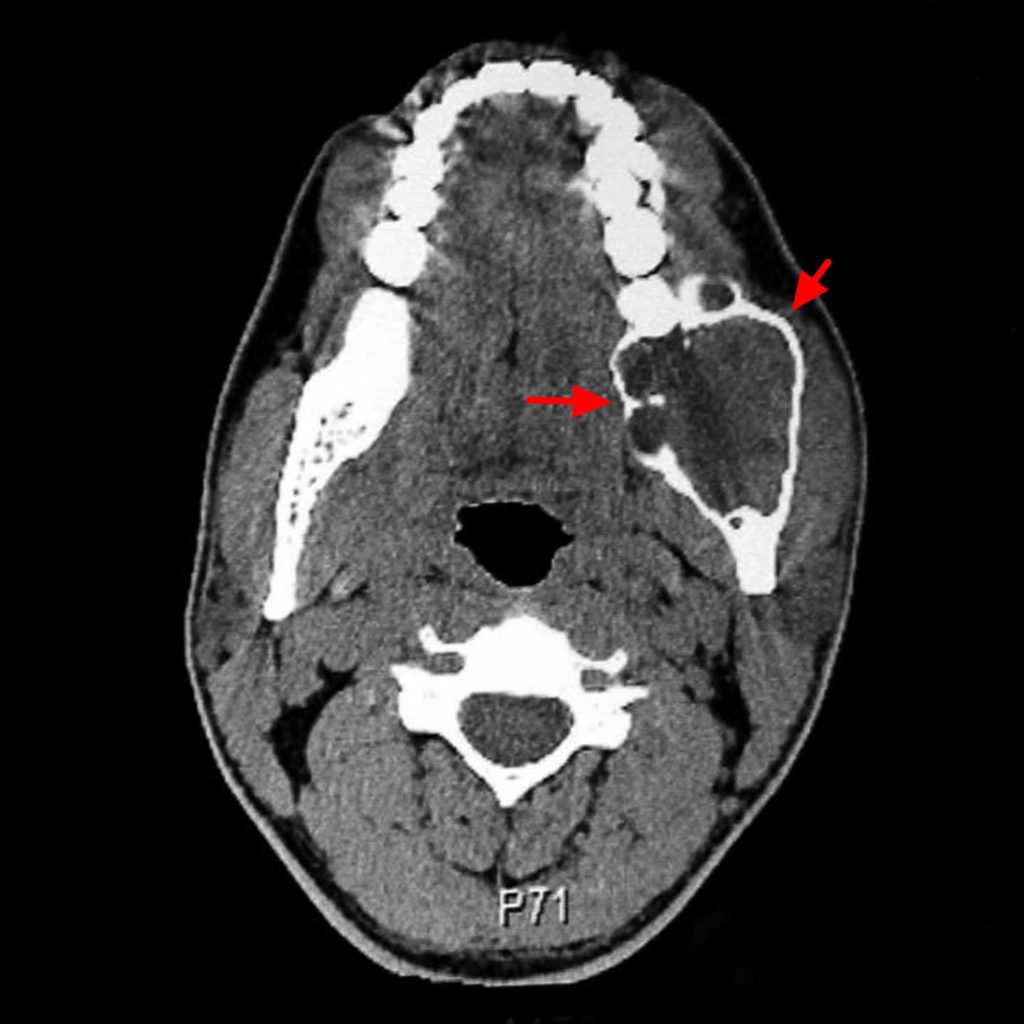
Микроскопически можно различить несколько типов опухоли:
- плеоморфная. Этот тип являет собой разветвленную сеть одонтогенных эпителиальных тяжей;
- фолликулярная. Для нее характерно присутствие изолированных островков (фолликулов) из клеток эпителия, находящихся в строме из соединительной ткани;
- акантоматозная. При данном виде патологии наблюдается четкая плоскоклеточная метаплазия с формированием кератина в опухолевых клетках;
- базальнолеточная. Этот тип амелобластомы имеет с базальноклеточным раком большую схожесть;
- гранулярно-клеточная. Этот тип характеризуется большим количеством ацидофильных гранул в эпителии.
Первые два типа патологии встречаются более часто, но обычно в пределах одной опухоли бывают различные типы гистологического строения.
* Только при условии получения данных о заболевании пациента, представитель клиники сможет рассчитать точную цену на лечение.
Симптомы патологии
Развитие амелобластомы идет очень медленно, и больной продолжительное время может не обращать внимания на незначительные симптомы. Но по мере развития заболевания челюсть начинает деформироваться. Первым видимым проявлением патологии является нарушение симметричности лица, незначительная припухлость со стороны поражения.
Когда опухоль повреждает структуру костной ткани, у больного возникают болевые ощущения, которые напоминают зубную боль. Начинает происходить расшатывание и смещение зубов. Челюсть в зоне поражения медленно деформируется, а при дальнейшем развитии – происходит истончение кортикальной пластинки — возникает специфический пергаментный хруст. При пальпации можно почувствовать гладкую или бугристую веретенообразно вздутую часть кости, при истончении ткань кости легко прогибается и пружинит. Со стороны полости рта видна трансформация альвеолярного отростка.
Кожа над пораженной областью продолжительное время остается неизмененная, подвижная, легко собирается в складку. При формировании опухоли твердое небо и альвеолярный отросток на верхней челюсти трансформируются, есть высокий риск проникновения опухоли в глазницу и полость носа.
Протекание патологии бывает осложнено воспалениями — в полости рта могут обнаруживаться свищи с выделениями серозно-гнойного характера.
Прочие симптомы амелобластомы:
- затруднение при процессе глотания, зевания;
- нарушение подвижности челюсти;
- хруст при закрывании и открывании рта (причина — истончение кортикальной пластины);
- кровотечения из изъязвленной слизистой над опухолью.
Диагностика заболевания
Диагностирование патологии происходит на основании анамнеза, клинической симптоматики и данных, полученных в итоге различных лабораторных и инструментальных обследований, таких как:
- рентгенография (боковая, внутриротовая, панорамная, аксиальная);
- КТ;
- цитологическое исследование.
Обязательно проводят дифференциальное диагностирование с такими заболеваниями, как: дентальные кисты воспалительной этиологии, цистаденоидные карциномы слюнной железы, плоскоклеточный рак.
* Только при условии получения данных о заболевании пациента, представитель клиники сможет рассчитать точную смету на лечение.
Лечение
Лечение патологии заключается в хирургическом удалении амелобластомы. Объем иссеченной костной ткани зависит от величины, места расположения и запущенности опухоли.
При ранней диагностике хирургические методы дают возможность удалить ее без резекции или частичной экзартикуляции челюсти. Подобные операции не ведут к нарушению непрерывности челюсти, позволяют сохранить ее работоспособность и избежать обезображивания лица больного. Для предотвращения появления рецидива патологии, стенки полости подвергают обработке раствором фенола для того, чтобы элементы эпителия амелобластомы подверглись некрозу.
При значительном развитии опухоли, делается резекция челюсти или ее частичная экзартикуляция (с нарушением непрерывности).
При нагноении выполняется одновременная хирургическая ликвидация опухоли и воспалительного процесса.
Послеоперационное лечение состоит из антибактериальной, симптоматической и корригирующей терапии. При утрате больным большого объема кости для восстановления работоспособности челюсти используют костную пластику и формируют ортопедические конструкции.
В рационе пациента после удаления опухоли не должно быть твердых и грубых продуктов, после употребления пищи нужно обязательно промывать полость рта.
Прогноз заболевания
Большое значение для эффективной терапии амелобластомы имеет раннее диагностирование патологии. При своевременном диагностировании и правильном хирургическом лечении прогноз обнадеживающий. У опухоли есть склонность к рецидивам. Когда происходит позднее обнаружение опухоли, то после хирургического вмешательства есть большой риск, что будут нарушения двигательной активности нижней челюсти и возможно обезображивание лица.
Малигнизация доброкачественной опухоли встречается в запущенных случаях и при неправильном лечении. Лимфогенное метастазирование встречается редко.
Профилактика болезни
Во избежание тяжелых последствий следует при первых подозрительных признаках пройти обследование. Также рекомендуется регулярно посещать врача для профилактического осмотра.
- Педиатрический рак
- Рак головы и шеи
- Рак легких
- Рак печени
- Рак кости
- Побочные эффекты
Авторы: Франческо Диониси 1 , Маурицио Амичетти 1 , Карло Алгранати 2 , Ирене Джиагомелли 1 , Маттиа Барбарески 3 , Мауро Рекла 4 , Цезаре Гранди 5
1 Отдел протонной терапии, отделение онкологии, Больница Тренто, Тренто, Италия
2 Отдел протонной терапии, отделение медицинской физики, Больница Тренто, Тренто, Италия
3 Отделение патологии, Больница Тренто, Тренто, Италия
4 Отделение радиологии, Больница Тренто, Тренто, Италия
5 Отделение отоларингологии, Больница Тренто, Тренто, Италия
КРАТКОЕ СОДЕРЖАНИЕ
Мы сообщаем о случае 87-летнего мужчины, страдающего от неоперабельной амелобластомы правой челюсти, которая была успешно вылечена протонной терапией как основным методом лечения дозами до 66 Гр в 33 фракциях. Лечение хорошо переносилось, прерываний из-за токсичности не было. При последующих посещениях у пациента наблюдался полный клинический ответ на лечение без признаков заболевания и полное восстановление после острых побочных эффектов. В этом отчете мы обсудим потенциальные и возможные подводные камни протонной терапии при лечении конкретных клинических ситуаций.
ВВЕДЕНИЕ
Амелобластома - редкая доброкачественная одонтогенная опухоль, возникающая на нижней и верхней челюстях с потенциальным местным агрессивным поведением. Злокачественная амелобластома (то есть, метастазирующая амелобластома и амелобластическая карцинома) встречается редко. Рост этого вида рака обычно медленный; однако значительное ухудшение состояния пациента может возникнуть из-за местной инвазивности. Хирургия является основным методом лечения. Когда ее применение возможно, она обеспечивает локальный контроль в пределах от 69% (если выполняется только энуклеация) до 96% при резекции[1]. Роль лучевой терапии (ЛТ) неясна из-за недостатка данных, представленных в литературе относительно ее эффективности при лечении этого заболевания[2].
Протонная терапия (ПТ) представляет собой уникальный метод для проведения ЛТ, который использует физические свойства частиц, теряющих энергию в конечной точке пробега, что обеспечивает низкую входную дозу и почти нулевую дозу за пределами их пути [3]. Эти особенности делают лечение протонами особенно эффективным в определенных клинических ситуациях; позволяют улучшить результаты лечения, уменьшить побочные эффекты и повысить качество жизни пациента[4,5].
В работе сообщается о случае неоперабельной амелобластомы, пролеченной ПТ как основным методом лечения. Пациент дал письменное согласие на использование своих данных для научного отчета.
ИСТОРИЯ БОЛЕЗНИ
В мае 2013 года 85-летний мужчина с раком прямой кишки в анамнезе был госпитализирован в отделение неотложной помощи в Больницу Тренто с неконтролируемым носовым кровотечением. Рентгенологические обследования выявили сложное многоступенчатое новообразование, возникшее на правой челюсти с локальной инвазивностью в полости носа, а также в пазухах решетчатой кости и верхней челюсти (рис. 1).
Рис. 1 Осевые, сагиттальные и фронтальные МРТ изображения с контрастом, показывающие увеличение амелобластомы в мае 2013 года.
Был проведен гистологический диагноз плексиформной амелобластомы (рис. 2).
Рис. 2 Типичный плексиформный рост опухоли, расположенный в анастомозирующих двойных колонках кубических клеток, с минимальным свидетельством центрального звездчатого ретикулума. С подкрашиванием гематоксилин-эозином, 200 ×.
Команда специалистов по лечению уха, носа и горла предложила операцию, но пациент отказался. Было начато медицинское лечение симптомов. Во время последующего наблюдения отмечалось медленное и непрерывное увеличение очага поражения начиная с октября 2015 года. Когда состояние ухудшилось, пациент был госпитализирован в отделение неотложной помощи с оро-назальным кровотечением, правым лагофтальмом и затруднением дыхания. Магнитный резонанс (МР) показал увеличение объема опухоли (соответственно 97, 62 и 70 мм в переднезаднем, поперечном и краниокаудальном диаметрах) и новое поражение носоглотки, орбиты (дна и медиальной стенки) и мышц нижней прямой кишки (рисунок 3).
Рис. 3 (А) Аксиальные, сагиттальные и фронтальные МРТ изображения с контрастом, сделанные в октябре 2015 года. (B) Области внутри красных линий представляют собой увеличение расширения опухоли и инвазивности по сравнению с исходными изображениями.
Данный клинический случай обсуждался на совещании многопрофильной коллегии врачей, где патология была признана неоперабельной из-за возраста пациента, сопутствующей патологии и отказа от хирургического вмешательства. Коллегия рекомендовала ПТ, которая действовала в Тренто с октября 2014 года, как местное лечение с радикальным намерением, учитывая увеличение опухоли и ее непосредственную близость к оптическим структурам.
ЛЕЧЕНИЕ ПРОТОННОЙ ТЕРАПИЕЙ
Процедуры подготовки включали иммобилизацию пациента с использованием головной рамки с индивидуальной 3-точечной термопластичной маской. Был предложен загубник, чтобы отжать язык и полость рта от подвергаемого лечению объема. Однако он не использовался из-за индивидуальных особенностей пациента.
Снимок для планирования моделирования (толщина среза 2 мм) был получен с помощью диагностических МРТ и КТ для разграничения объема мишени и органов в зоне риска (ОЗР).
Клинический объем мишени определялся путем добавления 3-миллиметровой границы вокруг общего объема опухоли. Планируемый объем мишени состоял из 4-миллиметрового увеличения изотропной клинической мишени. Для создания планируемого объема, подверженного риску, была добавлена изотропная граница 1,5 мм вокруг оптических нервов и хиазм. Назначенная доза для планируемого объема мишени составила 66 Гр (ОБЭ) в 33 суточных фракциях с максимальной допустимой дозой на 1% оптических структур ≤54 Гр (ОБЭ) (рисунок 4).
Рис. 4 Гистограмма объема-дозы, на которой желтые, оранжевые и красные изолинии представляют собой линии изодоз 54, 60 и 62,7 Гр соответственно.
Протонный план был создан при помощи системы планирования XIO (Xio Proton, Elekta AB, Стокгольм, Швеция) с использованием активных сканируемых протонов (диапазон энергий от 70 до 230 МЭВ, сигма пятна при 32 г / см2
2,65 мм), ускоренных циклотроном и излучаемая поворотным гентри (Приложения Ионного Пучка, IBA, Лувэн-ля-Нев, Бельгия). Для данного случая применялся метод однополевой оптимизации, в котором индивидуально оптимизированные ПТ поля доставляют гомогенную дозу к мишени. Была выбрана трехкомпонентная копланарная и некопланарная схема луча (250 ° стол 0 °, 110 ° стол 0 °, 340 ° стол 90 °, 0 °, 280 ° стол 90 °, 240 ° стол 90 °). Для поверхностных слоев некомпланарного пучка использовался энергетический адсорбер. Межточечный интервал был установлен на 0,3 см.
Лечение было проведено между ноябрем 2015 года и январем 2016 года с ежедневными онлайн проверками настроек. Еженедельное КТ сканирование выполнялось для проверки постоянного охвата целей и защиты от воздействия на ОЗР во время лечения. Перепланирование не потребовалось (рисунок 5).
Рис. 5 Сравнение гистограммы планируемого объема - дозы и гистограммы объема - дозы, полученной при еженедельном КТ сканировании, которое показывает стабильность охвата мишени и защиты от воздействия на ОЗР.
Что касается токсичности, у пациента наблюдался острый G3 радиационный дерматит и мукозит. Были прописаны кремы для наружного применения и краткий курс опиоидных анальгетиков. Делать перерывы в лечении не понадобилось. Полное восстановление после кожной и слизистой токсичности произошло по истечении одного и двух месяцев соответственно.
Первый МР после ПТ был проведен через 3 месяца после лечения и показал полную реакцию без признаков опухоли. На консультациях врачей ЛОР в течение следующих 18 месяцев не было обнаружено никаких признаков заболевания. Через 18 месяцев после окончания ПТ у пациента сохранялось очень хорошее качество жизни. Рисунок 6 иллюстрирует консолидированные МР изображения после ПТ. До настоящего времени токсичность визуально не наблюдалась. Недавно пациент обновил свои водительские права.
Рис. 6 Объединенные снимки после протонной терапии, показывающие полный клинический ответ, полученный (а) через 3 месяца после окончания протонной терапии и (б) через 1 год после окончания протонной терапии.
ОБСУЖДЕНИЕ
В данном отчете сообщается о случае крупной амелобастомы, успешно вылеченной ПТ как основным методом лечения при амелобластоме или амелобластической карциноме.
В исследовании Кеннеди и коллег[2] сообщалось о местном контроле 67% со средней дозой облучения 66,2 Гр (диапазон от 63 до 74,4 Гр) у 6 пациентов, получавших лечение с целебными намерениями одной только РТ (n = 2) или после операции (n = 4) в период с 1973 по 2007 гг. при среднем сроке наблюдения 7,8 лет.
Аналогичные дозы облучения были зарегистрированы в исследовании Филипса и др[6]. Между 1973 и 2004 годами дозы от 63 до 72 гр традиционным фракционированием давались 5 пациентам, страдающим амелобластической карциномой или амелобластомой. При 2,1-летнем наблюдении 4 пациента были живы и имели явную болезнь; 1 пациент умер от других причин. Одному пациенту РТ давалась отдельно; 4 пациента получали РТ после операции с близкими или микроскопически положительными границами.
Кока и др. [7] недавно сообщали о частичном ответе с использованием томотерапии дозой до 60 Гр 30 фракциями для рецидивной амелобластической карциномы. Размер опухоли был 57 × 56 × 63 мм, что составляло примерно половину от размера опухоли, описанной в настоящем исследовании. Мендерхалл и др. [8] несколько существующих сообщений относительно РТ при лечении амелобластомы. Локальный контроль был достигнут у 7 из 9 пациентов, облученных по поводу явного заболевания, и 3 из 3 пациентов, получавших лечение после операции. В своем обзоре авторы предложили использовать ПТ для обширных верхнечелюстных амелобластом для адекватного лечения опухоли и уменьшения дозы на ОЗР (например, центральной нервной системы и оптических структур).
Насколько нам известно, это первый зарегистрированный случай ПТ в лечении амелобластомы. Что касается более тяжелых частиц, Дженсен и др. [9] описали случай локально рекуррентной амелобластической карциномы, положительно пролеченной углеродной ионной терапией в Гейдельберге с дозой 60 Гр (ОБЭ) в 20 фракциях.
В обоих случаях наблюдался быстрый и полный ответ. Учитывая относительно вялую естественную историю этих опухолей, такого быстрого ответа не ожидалось. Наоборот, в опубликованном исследовании рентгеновской лучевой терапии Кокой и др. [7] сообщалось только о частичном ответе во время однолетнего последующего наблюдения. Возможное объяснение противоречащих результатов этих исследований может заключаться в более высоких дозах облучения и использовании заряженных частиц с их своеобразной радиобиологией, которые могли повлиять на быстроту и полноту ответа опухоли.
Использование заряженных частиц, действительно, может быть целесообразным при лечении рака головы и шеи, в частности при параназальных раках пазух, где обычно требуются высокие дозы для лечения больших и сложных объемов мишеней, окруженных критическими ОЗР, такими как зрительный аппарат или ствол мозга. Несколько дозиметрических исследований, а в последнее время - клинические исследования, показали многообещающие результаты и потенциальные преимущества ПТ по сравнению с рентгеновской терапией при лечении рака головы и шеи[11–14]. Более того, недавний мета-анализ Пател и др. [15] продемонстрировал значительно лучшие результаты с точки зрения безрецидивной выживаемости и локально-регионального контроля над раком параназальных пазух и раком носовой полости, пролеченных заряженными частицами, по сравнению с пациентами, получавшими фотонную терапию.
В данном случае мы четко описали потенциал активного сканирования ПТ для успешной доставки радикальных доз на большие объемы, подвергаемые лечению, вблизи критических ОЗР, и для снижения риска токсичности. В настоящем докладе показан еще одно потенциальное показание для ПТ: использование метода для радикального лечения заболеваний головы и шеи у пожилых и ослабленных пациентов [15] , которые имеют ограниченную способность компенсировать побочные эффекты лечения [16]. Потенциал ПТ для уменьшения острых и поздних осложнений по сравнению с обычным РТ следует рассматривать многодисциплинарными коллегиями перед вынесением заключений о назначении лучевого лечения.
Потенциальный подводный камень этого метода при лечении синоназального рака - это сложная взаимозависимость между ошибками при подготовке к лечению и анатомическими неопределенностями (т. е., изменениями заполнения носовой полости и заполнения носовых пазух носа), которые могут возникать во время лечения с потенциальными соответствующими различиями между номинальным распределением дозы (рассчитанным по КТ планированию) и фактически доставляемой дозой[17]. В свете этого рекомендуется ввести еженедельные контрольные КТ сканирования с использованием трехмерных протоколов в протонной терапии с визуальным контролем[18], чтобы выявить необходимость перепланирования. Кроме того, разработка инструментов надежности для обеспечения реализации высококачественных планов имеет важное значение, особенно когда используются нестандартные неоднородные поля, как при многоуровневой оптимизации (т. е. многоуровневая оптимизация или модулированная по интенсивности ПТ) планирования[19].
ВЫВОДЫ
Мы сообщили о положительном результате ПТ как основного метода при лечении крупной неоперабельной амелобластомы у пожилого пациента, подтверждая и поддерживая роль ПТ для конкретных сложных клинических сценариев (например, синоназальный рак, большие объемы мишеней, радикальные методы лечения и излечимые пожилые люди и ослабленные пациенты).
References
| 1. | Lau SL, Samman N. Recurrence related to treatment modalities of unicystic ameloblastoma: a systematic review. Int J Oral Maxillofac Surg. 2006;35:681–90. |
| 2. | Kennedy WR, Werning JW, Kaye FJ, Mendenhall WM. Treatment of ameloblastoma and ameloblastic carcinoma with radiotherapy. Eur Arch Otorhinolaryngol. 2016;273:3293–7. |
| 3. | Wilson RR. Radiological use of fast protons. Radiology. 1946;47:487–91. |
| 4. | Mishra MV, Aggarwal S, Bentzen SM, Knight N, Mehta MP, Regine WF. Establishing evidence-based indications for proton therapy: an overview of current clinical trials. Int J Radiat Oncol Biol Phys. 2017;97:228–35. |
| 5. | Langendijk JA, Lambin P, De Ruysscher D, Widder J, Bos M, Verheij M. Selection of patients for radiotherapy with protons aiming at reduction of side effects: the model-based approach. Radiother Oncol. 2013;107:267–73. |
| 6. | Philip M, Morris CG, Werning JW, Mendenhall WM. Radiotherapy in the treatment of ameloblastoma and ameloblastic carcinoma. Hong Kong J Radiol. 2005;8:157–61. |
| 7. | Koca T, Basaran H, Arslan D, Sezen D, Cerkesli ZA, Kilinc O, Karaca S, Bassorgun CI, Okay HO, Demirci M. Prominent response with helical tomotherapy in recurrent ameloblastic carcinoma of maxillary sinus: a case report. Radiat Oncol. 2014;9:157. |
| 8. | Mendenhall WM, Werning JW, Fernandes R, Malyapa RS, Mendenhall NP. Ameloblastoma. Am J Clin Oncol. 2007;30:645–8. |
| 9. | Jensen AD, Ecker S, Ellerbrock M, Nikoghosyan A, Debus J, Munter MW. Carbon ion therapy for ameloblastic carcinoma. Radiat Oncol. 2011;6:13. |
| 10. | Durante M. New challenges in high-energy particle radiobiology. Br J Radiol. 2014;87:20130626. |
| 11. | McDonald MW, Liu Y, Moore MG, Johnstone PA. Acute toxicity in comprehensive head and neck radiation for nasopharynx and paranasal sinus cancers: cohort comparison of 3D conformal proton therapy and intensity modulated radiation therapy. Radiat Oncol. 2016;11:32. |
| 12. | Ruggieri R, Dionisi F, Mazzola R, Fellin F, Fiorentino A, Schwarz M, Ricchetti F, Amichetti M, Alongi F. Nasal cavity reirradiation: a challenging case for comparison between proton therapy and volumetric modulated arc therapy. Tumori. 2016;102(suppl 2):12–5. |
| 13. | Romesser PB, Cahlon O, Scher E, Zhou Y, Berry SL, Rybkin A, Sine KM, Tang S, Sherman EJ, Wong R, Lee NY. Proton beam radiation therapy results in significantly reduced toxicity compared with intensity-modulated radiation therapy for head and neck tumors that require ipsilateral radiation. Radiother Oncol. 2016;118:286–92. |
| 14. | McDonald MW, Zolali-Meybodi O, Lehnert SJ, Estabrook NC, Liu Y, Cohen-Gadol AA, Moore MG. Reirradiation of recurrent and second primary head and neck cancer with proton therapy. Int J Radiat Oncol Biol Phys. 2016;96:808–19. |
| 15. | Patel SH, Wang Z, Wong WW, Murad MH, Buckey CR, Mohammed K, Alahdab F, Altayar O, Nabhan M, Schild SE, Foote RL. Charged particle therapy versus photon therapy for paranasal sinus and nasal cavity malignant diseases: a systematic review and meta-analysis. Lancet Oncol. 2014;15:1027–38. |
| 16. | Daly ME, Lau DH, Farwell DG, Luu Q, Donald PJ, Chen AM. Feasibility and toxicity of concurrent chemoradiation for elderly patients with head and neck cancer. Am J Otolaryngol. 2013;34:631–5. |
| 17. | Fukumitsu N, Ishikawa H, Ohnishi K, Terunuma T, Mizumoto M, Numajiri H, Aihara T, Okumura T, Tsuboi K, Sakae T, Sakurai H. Dose distribution resulting from changes in aeration of nasal cavity or paranasal sinus cancer in the proton therapy. Radiother Oncol. 2014;113:72–6. |
| 18. | Veiga C, Janssens G, Teng CL, Baudier T, Hotoiu L, McClelland JR, Royle G, Lin L, Yin L, Metz J, Solberg TD, Tochner Z, Simone CB II, McDonough J, Teo BK. First clinical investigation of cone beam computed tomography and deformable registration for adaptive proton therapy for lung cancer. Int J Radiat Oncol Biol Phys. 2016;95:549–59. |
| 19. | Liu W, Frank SJ, Li X, Li Y, Park PC, Dong L, Ronald Zhu X, Mohan R. Effectiveness of robust optimization in intensity-modulated proton therapy planning for head and neck cancers. Med Phys. 2013;40:051711. |
Источник: International Journal of Particle Therapy, оригинальный текст статьи можно прочитать здесь.
Читайте также:

