Клинические испытания лекарственных препаратов от рака
Исследователи из онкологического центра Рогеля Университета Мичигана провели клинические испытания нового препарата, предназначенного для лечения рака поджелудочной железы, и первые результаты являются многообещающими.
Рак поджелудочной железы является одним из смертельных видов рака
При этом средняя пятилетняя выживаемость составляет мрачные 9%. Общеизвестно, что он распространяется на отдаленные области организма и обычно устойчив к химио- и лучевой терапии.
В течение последних двух десятилетий исследователи этого института изучали различные способы борьбы с раком поджелудочной железы.
По данным Центра профилактики и контроля заболеваний (CDC), люди старше 65 лет более подвержены риску рака поджелудочной железы. CDC говорит, что мужчины:
- потребители табака,
- люди, страдающие ожирением и избыточным весом,
- диабетики,
- люди с хроническим панкреатитом,
- имеющие семейный анамнез рака поджелудочной железы, подвергаются наибольшему риску возникновения этого вида онкологии.
Фаза 1-го клинического испытания проводилась с использованием молекулы, названной AZD1775. Препарат работает путем ингибирования фермента киназы Wee1. Было показано, что киназа Wee1 играет значительную роль в восстановлении поврежденной ДНК. Раковые клетки особенно чувствительны к фатальному повреждению ДНК, поскольку их геномы нестабильны по сравнению со здоровыми клетками.
Исследователи объяснили, что химиотерапия с использованием гемцитабина, стандартного химиотерапевтического препарата, и лучевая терапия, применяемая при раке поджелудочной железы, может привести к повреждению ДНК. Раковые клетки поджелудочной железы могут восстанавливать поврежденную ДНК и, таким образом, снижать эффективность лечения.
Руководитель исследования Мередит Морган, доктор философии, объяснила, что новая молекула была в состоянии предотвратить раковые клетки поджелудочной железы от защиты от повреждения ДНК, вызванного химиотерапией. Это повысило эффективность гемцитабина и лучевой терапии. Доктор объяснила, что лечение оказало минимальное влияние на нормальные клетки.

В исследовании приняли участие 34 пациента с местнораспространенным раком поджелудочной железы.
Пациенты получали:
- радиацию,
- гемцитабин,
- AZD1775.
Доза AZD 1775 была повышена с использованием "метода непрерывной переоценки по времени". Это означало, что доза была увеличена на основании токсичности, наблюдаемой в течение первых 15 недель лечения.
Общая выживаемость улучшилась у пациентов после этого режима лечения, по сравнению с теми, кто получал химиотерапию и только радиацию. Средняя продолжительность жизни без нового препарата составляла от 12 до 14 месяцев. С добавлением нового лекарственного средства выживаемость увеличилась в среднем до 22 месяцев, и безболезненное состояние наблюдалось в течение 9 месяцев с новым лекарственным средством.
Кунео сказал: "Добавление AZD 1775 к радиации и гемцитабину относительно хорошо переносилось, что дало хорошие результаты выживания. Необходимы дальнейшие исследования с этой многообещающей комбинацией".
Эксперты добавили, что этот новый препарат также тестируется на другие виды онкозаболеваний, такие как рак молочной железы и яичников, в качестве дополнения к стандартной химиотерапии и лучевой терапии.
Встройте "Правду.Ру" в свой информационный поток, если хотите получать оперативные комментарии и новости:
Подпишитесь на наш канал в Яндекс.Дзен или в Яндекс.Чат
Добавьте "Правду.Ру" в свои источники в Яндекс.Новости или News.Google
Также будем рады вам в наших сообществах во ВКонтакте, Фейсбуке, Твиттере, Одноклассниках.

вместе создадим единую базу клинических исследований в онкологии
- Руководства ESMO
- Помощь пациентам в период пандемии COVID-19
- Руководства RUSSCO
- Школа жизни онкологического пациента во время коронавируса (интервью члена Правления RUSSCO, проф. Н.В. Жукова)
Клинические исследования, которые проходят в данный момент
Многоцентровое, рандомизированное, открытое клиническое исследование фазы 3 в трех группах применения препаратов энкорафениб, цетуксимаб совместно с биниметинибом или без него, по сравнению с применением препаратов иринотекан/цетуксимаб или инфузионной терапии с применением 5-фторурацила (5-ФУ)/ фолиновой кислоты (ФК)/ иринотекана (FOLFIRI)/ цетуксимаба с определением безопасной дозы введения комбинации препаратов энкорафениб, бениметиниб, цетуксимаб для лечения пациентов с метастатическим коларектальным раком с мутацией BRAF V600E
Рандомизированное двойное слепое плацебо-контролируемое исследование для сравнения двух гуманизированных моноклональных антител направленного специфического действия против фактора роста эндотелия сосудов, применяемых в сочетании с химиотерапией по модифицированной схеме FOLFOX6 у пациентов с нерезектабельной метастатической колоректальной опухолью
TASCO1
Открытое рандомизированное исследование II фазы по оценке эффективности комбинации препарата TAS-102 с бевацизумабом и комбинации капецитабина с бевацизумабом у пациентов с метастатическим колоректальным раком, ранее не получавших лечение по поводу распространенного опухолевого процесса и которым не показано проведение интенсивной химиотерапии
Двойное слепое рандомизированное плацебо-контролируемое исследование III фазы препарата нинтеданиб в комбинации с оптимальной поддерживающий терапией (ОПТ), по сравнению с плацебо в комбинации с ОПТ, у пациентов с колоректальным раком, устойчивым к стандартному лечению
Рандомизированное двойное слепое плацебо-контролируемое многоцентровое международное исследование III фазы дурвалумаба или комбинации дурвалумаба с тремелимумабом в качестве консолидирующей терапии у пациентов с локализованным мелкоклеточным раком легкого I-III стадии, у которых не произошло прогрессирование после одновременной химиолучевой терапии (ADRIATIC)
Рандомизированное двойное слепое плацебо-контролируемое многоцентровое международное исследование III фазы дурвалумаба или комбинации дурвалумаба с тремелимумабом в качестве консолидирующей терапии у пациентов с локализованным мелкоклеточным раком легкого I-III стадии, у которых не произошло прогрессирование после одновременной химиолучевой терапии (ADRIATIC)
База, на которой проводится исследование:
Международное, рандомизированное, открытое исследование 3 фазы препарата REGN2810 (анти-PD 1 антитело) по сравнению с химиотерапией препаратами платины в качестве первой линии терапии у пациентов с распространенным или метастатическим PD-L1-положительным немелкоклеточным раком легких
Рандомизированное, открытое исследование 3 фазы комбинации препарата REGN2810 (анти-PD 1 антитело), ипилимумаба и двухкомпонентной схемы химиотерапии производными платины в терапии первой линии пациентам с распространенным или метастатическим немелкоклеточным раком легкого и уровнем экспрессии в опухоли PD-L1 менее или равно 50%
Открытое многоцентровое исследование III фазы, проводимое для сравнения действия препарата авелумаб с действием двухкомпонентной химиотерапией препаратами платины при их применением в качестве первой линией терапии рецидивирующего или PD-L1-положительного немелкоклеточного рака легкого IV стадии
Протокол № EMR 100070-005
Многоцентровое исследование 2 фазы с целью изучения пероральной терапии ингибитором cMET, препаратом INC280 у взрослых пациентов с распространенным немелкоклеточным раком легкого при немутантном статусе EGFR (WT)
2) Аболмасов Александр Евгеньевич
+7 (925) 928-51-59
Открытое многоцентровое рандомизированное исследование 3 фазы по изучению эффективности и безопасности препарата BGB-A317 (анти-PD1 антитела) по сравнению с доцетакселом у пациентов с немелкоклеточным раком легкого и прогрессированием заболевания после курса платиносодержащей химиотерапии
Рандомизированное открытое исследование фазы 3 применения Бригатиниба (Алунбриг™) в сравнении с Алектинибом (Алеценса ® ) у пациентов с распространенным ALK-позитивным немелкоклеточным раком легких, у которых возникла прогрессия заболевания на фоне применения Кризотиниба (Ксалкори ® )
Многоцентровое рандомизированное, двойное слепое, плацебо-контролируемое исследование III фазы, проводимое с целью оценки эффективности и безопасности анаморелина гидрохлорида, применяемого для восполнения дефицита массы тела и лечения анорексии, развившихся на фоне распространенного немелкоклеточного рака легкого у взрослых пациентов
Двойное слепое, рандомизированное, проводимое в параллельных группах исследование 3-й фазы с использованием активного препарата в качестве контроля с целью сравнения эффективности и безопасности препарата CT-P16 и разрешенного в ЕС препарата Авастин, применяемых в качестве первой линии терапии метастатического или рецидивирующего неплоскоклеточного немелкоклеточного рака легкого
Протокол № CT-P16 3.1
Рандомизированное, двойное слепое, многоцентровое исследование III фазы для оценки эффективности, безопасности, фармакокинетики и иммуногенности исследуемого препарата SB8 (предлагаемого биоаналога бевацизумаба) в сравнении с препаратом Авастин ® у пациентов с метастатическим или рецидивирующим неплоскоклеточным немелкоклеточным раком легкого
2) Козлов Вадим Викторович
+7 (913) 463-828-6
2) Бабина Ксения Геннадьевна
+7 (968) 267-77-76
Открытое исследование препарата афатиниб у пациентов с местнораспространенным или метастатическим немелкоклеточным раком легкого с мутацией рецептора эпидермального фактора роста, ранее не получавших лечение или предварительно получавших химиотерапию
Рандомизированное, двойное-слепое, плацебо-контролируемое исследование III фазы по изучению ARQ 197 плюс эрлотиниб vs эрлотиниб у ранее леченых пациентов с местно-распространенным или метастатическим неплоскоклеточным немелкоклеточным раком легкого
Программа расширенного доступа к ИПИЛИМУМАБУ для больных глиобластомой и глиомой
Mногоцентровое, рандомизированное, открытое исследование III фазы Атезолизумаба (антитело к PD-L1) в комбинации с адъювантной химиотерапией на основе антрациклина/таксана в сравнении только с химиотерапией у пациентов с операбельным трижды негативным раком молочной железы
Двойное слепое рандомизированное исследование III фазы, проводимое в параллельных группах, по сравнению эффективности, безопасности и иммуногенности TX05 и препарата Герцептин ® у пациентов с ранней стадией HER2-положительного рака молочной железы
Двойное слепое продолженное исследование для проведения адъювантной монотерапии препаратом Герцептин ® или препаратом TX05 для продолжения оценки безопасности и иммуногенности у пациентов с ранней стадией HER2-положительного рака молочной железы после проведения неоадъювантной терапии и хирургической резекции в рамках протокола TX05-03
Рандомизированное открытое исследование 3 фазы по оценке препарата абемациклиб в комбинации со стандартной адъювантной эндокринной терапией по сравнению с применением только стандартной адъювантной эндокринной терапии у больных раком молочной железы на ранней стадии, с высоким риском развития рецидива, поражением регионарных лимфатических узлов, с положительным статусом гормональных рецепторов и отрицательным статусом рецептора эпидермального фактора роста человека 2-го типа
Рандомизированное, многоцентровое, открытое, III фазы исследование лапатиниба плюс капецитабин или трастузумаб плюс капецитабин упациенток с Her2/neu позитивным метастатическим раком молочной железы ранее получавших антрациклины и таксаны
Международное проспективное открытое многоцентровое неинтервенционное исследование OPTIMIS.
Изучение результатов лечения больных гепатоцеллюлярным раком, получавших или не получавших сорафениб после трансартериальной химиоэмболизации (ТАХЭ), и влияние времени начала терапии сорафенибом
Многоцентровое открытое исследование 1b фазы с эскалацией дозы по изучению безопасности и переносимости препарата квинакрин у пациентов с опухолевыми заболеваниями печени различного происхождения
Многоцентровое рандомизированное открытое исследование (3 фаза) эффективности и безопасности Ленватиниба (E7080) в сравнении с Сорафенибом в первой линии лечения больных неоперабельным печеночно-клеточным раком
Рандомизированное многоцентровое двойное слепое исследование III фазы препарата регорафениб у больных ГЦР, ранее получавших сорафениб
Рандомизированное, двойное-слепое исследование II фазы по сравнительной оценке режимов рамуцирумаба в комбинации с цисплатином и гемцитабином; мерестиниба в комбинации с цисплатином и гемцитабином или плацебо в комбинации с цисплатином и гемцитабином в качестве первой линии терапии у пациентов с распространенным или метастатическим раком желчевыводящих путей
JAVELIN BLADDER 100
Многоцентровое, международное, открытое, рандомизированное, проводимое в параллельных группах исследование 3-й фазы, в котором Авелумаб (MSB0010718C) в комбинации с наилучшей симптоматической терапией сравнивается с наилучшей симптоматической терапией в качестве поддерживающего лечения у пациентов с местно-распространённым или метастатическим уротелиальным раком, который не прогрессировал после завершения первой линии химиотерапии на основе препаратов платины
2) Аболмасов Александр Евгеньевич
+7 (925) 928-51-59
Многоцентровое, рандомизированное, двойное слепое исследование III фазы для оценки эффективности и безопасности препарата BIBIF 1120 в комбинации с карбоплатином и паклитакселом в сравнении сплацебо в комбинации с карбопалином и паклитакселом у пациентов с распространенным раком яичников
Многоцентровое, двойное слепое, плацебо-контролируемое, рандомизированное исследование II фазы по изучению омрабулина у больных с чувствительным к препаратом платины рецидивирующим раком яичников, получающих карбоплатин/паклитаксел
MK1775 в сочетании с карбоплатином и паклитакселом при платиночувствительном раке яичников
Эффективность и безопасность Пембролизумаба у пациентов с прогрессией распространенного рака яичников (KEYNOTE 100)
Рандомизированное двойное слепое плацебо-контролируемое исследование III фазы эффективности и безопасности копанлесиба в комбинации с ритуксимабом у пациентов с рецедивами индолетных В-клеточных лимфом (иНХЛ) – CHRONOS-3
Исследование II/III фазы по оценке продолжительности тяжелой нейтропении при лечении плинабулином в сравнении с пэгфилграстимом у пациентов с солидными опухолями, получающих миелосупрессивную химиотерапию доцетакселом
Мультинозологичное исследование: анализ предиктивных биомаркеров для применения пембролизумаба при распространенных солидных опухолях (KEYNOTE 158)
* Критерии включения и исключения представлены не в полном объёме

Причиной смерти пациента-испытателя назвали неожиданную реакцию организма на экспериментальный препарат производства "Биокад". Ранее фармзавод удостоился похвалы Минздрава за "фантастические результаты" в лечении опухолей. Лекарство должно было появиться на рынке ещё год назад. Не остановит ли смерть добровольца исследования и когда ждать отечественное лекарство от рака — в расследовании Лайфа.
Одна из самых секретных разработок российской медицины попала в неприятную историю, которая могла бы так и остаться в стенах петербургской лаборатории. Рассказываем, как российские учёные изобретали молекулу для лечения меланомы и рака лёгких и с какими трудностями столкнулись.
1. Экспериментальный препарат стал главной темой онкологического конгресса
В ноябре 2018 года состоялся XXII Российский онкологический конгресс. Представители фармзавода "Биокад" и врачи рассказали об успешных испытаниях на людях новейшего отечественного лекарства от рака. Он заставляет иммунные клетки атаковать опухоль.
Речь о препарате под кодовым названием BCD-100. Это одна из самых засекреченных разработок отечественной фармацевтики — не разглашают даже имена учёных, разработавших молекулу (основное действующее вещество).
Препарат показал ошеломляющие результаты в лечении неоперабельной меланомы. Когда опухоль даёт метастазы, зловредные клетки проникают в окружающие органы и там формируют вторичные очаги болезни. Справиться с метастазирующей меланомой гораздо труднее. Однако BCD-100 сумел полностью убрать подобные опухоли у 7% пациентов. Ещё у 29% пациентов размер опухоли уменьшился не меньше чем на треть. В исследовании участвовало 126 онкобольных с неоперабельной меланомой. Испытания финансировал сам "Биокад".
Меланома (рак кожи)
Не самый частый, но один из самых агрессивных видов рака (≈74 тысяч больных в РФ). С 1950-х мировая заболеваемость выросла на 600%
Однако пациентов ждут серьёзные побочные эффекты, которые стали сюрпризом и для врачей — препарат-то новый.
"Внедрение [иммунотерапии], по-русски сказать, взорвало химиотерапевтам мозг. Мы столкнулись со спектром сложных и не понятных для нас [побочных] реакций. Может поражаться любой орган: начиная от щитовидной железы и заканчивая воспалением сосудов".
онколог центра им. Блохина Михаил Федянин
Но в декабре 2018 года НИИ онкологии им. Н.Н.Петрова (Санкт-Петербург) презентовал новые данные о результатах того же исследования.
У пациентов, принимавших BCD-100, чаще воспалялась щитовидная железа, чем у пациентов, принимающих аналогичные зарубежные препараты. Об этом заявил на конференции Федянин, то же впоследствии подтвердил и химиотерапевт из НИИ онкологии им. Н.Н. Петрова Алексей Новик. Его выступление находится в открытом доступе. Однако другие показатели побочных явлений не сильно отличались от уже выпущенных на рынок аналогов, так что Новик осторожно назвал BCD-100 "не менее безопасным", чем ему подобные.
2. Летальный исход, о котором умолчали
В ноябрьском выступлении доктор Федянин коротко обмолвился: были описаны смертельные случаи после приёма подобных препаратов. Одна из причин летальности — воспаление сердечной мышцы (миокардит).
Ни Федянин, ни Новик подолгу не останавливались на опасностях подобного рода препаратов. Врачи не упомянули и о смертельном случае с одним из пациентов-добровольцев. А самое главное, этого не сделала медицинский директор фармзавода "Биокад" Юлия Линькова.
Представители завода "Биокад" вовремя не проинформировали государственные службы о смерти пациента из-за приёма BCD-100. Об этом говорится в материалах проверки Росздравнадзора, которые попали в Лайф из прокуратуры.
"В ходе клинического исследования препарата BCD-100 по протоколу Miraculum уполномоченное лицо ЗАО "Биокад" Юлия Линькова [не сообщила] в Росздравнадзор о летальной непредвиденной нежелательной реакции на данный препарат".
Материалы проверки Росздравнадзора от 26.11.18
Линькова обязана была уведомить о произошедшем либо через защищённую информационную систему Росздравнадзора, либо просто по электронной почте.
В том же предписании Росздравнадзор отмечает, что ни в 2017-м, ни в 2018-м в адрес ведомства вообще не поступало данных о безопасности трёх других препаратов, которые разрабатывает "Биокад".
Недавние исследования показали — больше половины российских медиков не сообщают в Росздравнадзор о побочных эффектах на препараты, с которыми столкнулись их пациенты. Ещё 8% вообще считают, что рассказывать о нежелательных реакциях нецелесообразно.
3. В надежде на "чудо"
Ещё в 2016 году министр здравоохранения Вероника Скворцова назвала результаты использования BCD-100 фантастическими. Протоколу, по которому исследовали лекарство, даже придумали соответствующее метафорическое название. С латыни "miraculum" переводится как " чудо". И действительно, с некоторыми пациентами BCD-100 сотворил чудо.
У 64-летней пациентки из Питера был опухолевый очаг в лёгком
Через несколько месяцев после приёма BCD-100 опухоль заметно уменьшилась в объемах. Это видно на снимках НМИЦ им. Н.Н.Петрова.
Но для других пациентов чудо обернулось проблемами или трагедией. Побочные эффекты от BCD-100 испытывали 80% пациентов, заявил на ноябрьской конференции доктор Федянин.
Чтобы разобраться, как работает BCD-100, важно понимать принцип работы иммунной системы человека.
Очень упрощённо иммунитет можно описать как систему "свой-чужой". Некоторые клетки крови умеют распознавать чужеродные бактерии и опасные тела и уничтожать их. Такой тип иммунных клеток называют Т-лимфоцитами. Получается эдакий "иммунный спецназ", который способен проникать через стенки сосудов в окружающие ткани и проводить там боевые действия против чужаков.
На поверхности Т-лимфоцита живёт белок PD-1, который отвечает за восприятие чужеродных клеток. Раковые же клетки "прячутся" от лимфоцитов, обманывая белок PD-1. Лимфоциты начинают думать, что раковая клетка — "своя", и не трогают смертельную опухоль.
Учёные по всему миру ломают головы над тем, как взломать маскировку и обучить лимфоциты распознавать в раковой клетке врага. Как уверяют создатели Miraculum, именно это им и удалось.

Создатели препарата рассчитывают, что его можно будет использовать не только для лечения меланомы и рака лёгких, но и других видов онкологии.
Поначалу на заводе "Биокад" рассчитывали выпустить лекарство на рынок в 2018 году. Сейчас сроки отодвинулись до 2022 года. Причин может быть множество: от недостаточного финансирования до неожиданно вскрывшихся проблем при использовании препарата.
В одном из интервью представители завода сравнивали цены на зарубежные аналогичные препараты. Выходило, что лечиться израильскими либо японскими средствами стоит примерно 9 миллионов рублей за курс. Отечественные разработчики обещали существенно меньшую цену за курс BCD-100. Возможно, в разы.
Хронология разработки препарата
4. Человечество писало кровью правила исследований препаратов
Лайф попросил эксперта, который много лет занимается клиническими исследованиями, рассказать о морально-этической стороне испытаний препаратов на людях. Вот что рассказала исполнительный директор Ассоциации организаций по клиническим исследованиям Светлана Завидова.
"Человечество двигалось к системе регулирования через лекарственные трагедии. Где-то, конечно, своим умом доходили, но в основном двигателем послужил негативный опыт, который и приводил к разработке тех или иных правил. Правила писали "на крови".
Светлана Завидова, Ассоциация по клиническим исследованиям
Один из первых мировых законодательных актов на тему регулирования исследований препаратов появился в США в 1938 году. Взяться за его разработку пришлось после того, как из-за неподтверждённого по критериям безопасности препарата сульфаниламида погибло 107 человек, большинство из которых — дети. Именно после этой трагедии фармпроизводителей обязали подтверждать безопасность лекарств. В том числе и на пациентах.
Исследования на людях идут в три фазы и длятся годами. В первую, как правило, включают только здоровых добровольцев. Вторая фаза — это испытания на пациентах, страдающих от конкретного заболевания. Обычно в них участвует несколько сотен человек. Третья фаза — самая масштабная: здесь в выборку могут включить несколько тысяч больных. Именно на третьей фазе появляется большинство данных о побочных реакциях и их частоте. Все добровольцы подписывают информированное согласие, соглашаясь на все риски (вплоть до летального исхода). Для многих пациентов участие в испытаниях — последний шанс.
Только при успешном завершении третьей стадии препарат регистрируют в госорганах и завозят в аптеки.
Второй случай изучают в медвузах как пример халатного отношения к безопасности препарата в угоду его продаваемости. Препарат талидомид в середине ХХ века был одним из самых продаваемых успокоительных и снотворных. Особенно его рекомендовали беременным и кормящим матерям, чтобы справляться с ночной бессонницей, утренней тошнотой и беспокойством. При этом никакие тесты влияния таблеток на плод не проводились. Препарат активно продавался в Европе. Через несколько лет стали чаще рождаться дети с патологиями: у новорожденных не было рук, ног либо ушей.
Ещё год потребовался властям нескольких стран, чтобы увязать страшную статистику с популярностью талидомида. Всё это время компания-производитель не признавала связи между этими событиями и продолжала рекламировать лекарство как безопасное.
5. Биокад: мы ничего не пытались скрыть!
Действия петербургской фармацевтической компании, которая не сообщила в Росздравнадзор о смерти пациента, на первый взгляд выглядят попыткой скрыть негатив во избежание репутационных и иных потерь. Однако в "Биокаде" заявляют, что специально ничего не утаивали.
"Первично полученные данные не соответствовали определению "Серьёзная непредвиденная нежелательная реакция". После получения дополнительных сведений информация была передана в Росздравнадзор".
Юридический департамент ЗАО "Биокад"
— Предположение о том, что ЗАО "Биокад" пыталось скрыть летальный случай, не соответствует действительности, поскольку данная информация сообщалась в ряд компетентных органов и учреждений, — добавили представители фармзавода. — Компания провела внутреннюю проверку, по результатам которой были детализированы внутренние процедуры.
Один из корпусов завода "Биокад" в Петербурге.
Компания "Биокад" создана в 2001 году. Это одна из крупнейших биотехнологических компаний России, где разрабатывают, изучают и производят новые типы лекарств. В штате трудятся более 1800 человек. Компания фокусируется на препаратах для терапии онкологических и аутоиммунных заболеваний, также ведёт разработки в области терапии других социально значимых заболеваний.
19 апреля 2019 года Национальный медицинский исследовательский центр радиологии Минздрава сообщил об увеличении числа онкобольных в стране. На первом месте в России рак лёгких. Каждый год онкологией заболевают около 600 тысяч человек. Всего в России на онкологическом учёте стоят 3,6 миллиона человек.
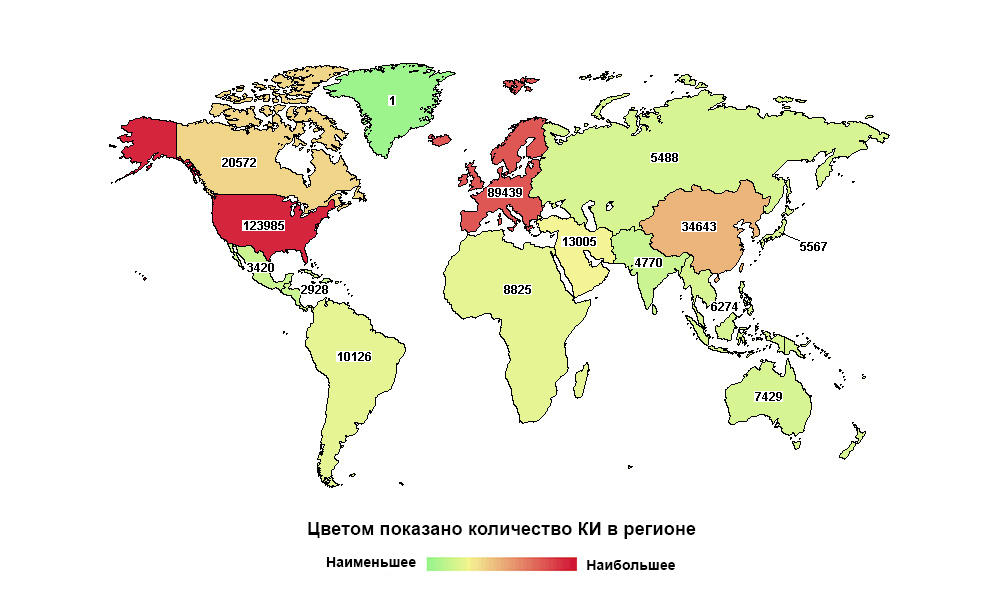
Россия далеко не на первом месте в мире, но первая по количеству исследований в своем макрорегионе
Для частных клиник практика необычная: минимум коммерческой выгоды, слишком много сложностей в организации процесса и строгие требования к лечебному учреждению. Обычно только крупным федеральным центрам удается им соответствовать.
А ведь для многих пациентов в России клиническое испытание препарата – единственный шанс получить бесплатное лечение от смертельной болезни. Но среди российских онкопациентов 30% просто не знают, что такое клиническое исследование, и лишь немногие принимали в них участие.
Поэтому мы хотим, чтобы как можно больше людей узнали и проверили: возможно, у них есть шанс получить препарат, который может спасти им жизнь.
В этой статье мы расскажем, зачем нужны и как устроены клинические исследования, кто и как может туда попасть.
Клиническое исследование/испытание (далее – КИ)– научное исследование с участием людей в качестве испытуемых, которое проводится с целью оценки эффективности и безопасности нового лекарственного препарата или расширения показаний к применению уже известного. Кроме лекарств, КИ могут также изучать эффективность и безопасность новых методов лечения и диагностики.
Медицина эволюционирует и превращается в точную науку, которая не обходится без статистики.
Когда медицина стала массовой, у врачей возникла необходимость вырабатывать действительно безошибочные тактики лечения. Определенные лекарства должны были помогать в заданных условиях большинству пациентов.
И именно клинические исследования – основа доказательной медицины.
До середины XX (!) века не было никакого регулирования исследований новых препаратов. Чтобы навести порядок, как часто бывает, понадобилась пара трагедий.

Мамы этих детей пили снотворное, не проверенное на людях
С тех пор лекарства перед регистрацией очень тщательно изучают. Регулируется это Международными гармонизированными трехсторонними правилами Надлежащей клинической практики (ICH Harmonized Tripartite Guideline for Good Clinical Practice, сокращённо — ICH GCP). С 1996-97 г. они действуют в США, Японии и ЕС, а с 2003 года введены и в России.
Весь процесс создания препарата можно поделить на 3 крупных фазы.
1. Поиск идеи и доклинические исследования – в пробирках и на животных.
2. Если на этом все не закончилось – то начинаются клинические исследования, с людьми: сначала осторожные, потом более массовые.
3. Затем препарат регистрируется в регуляторных органах, чтобы стать привычным наименованием в медицинских справочниках.
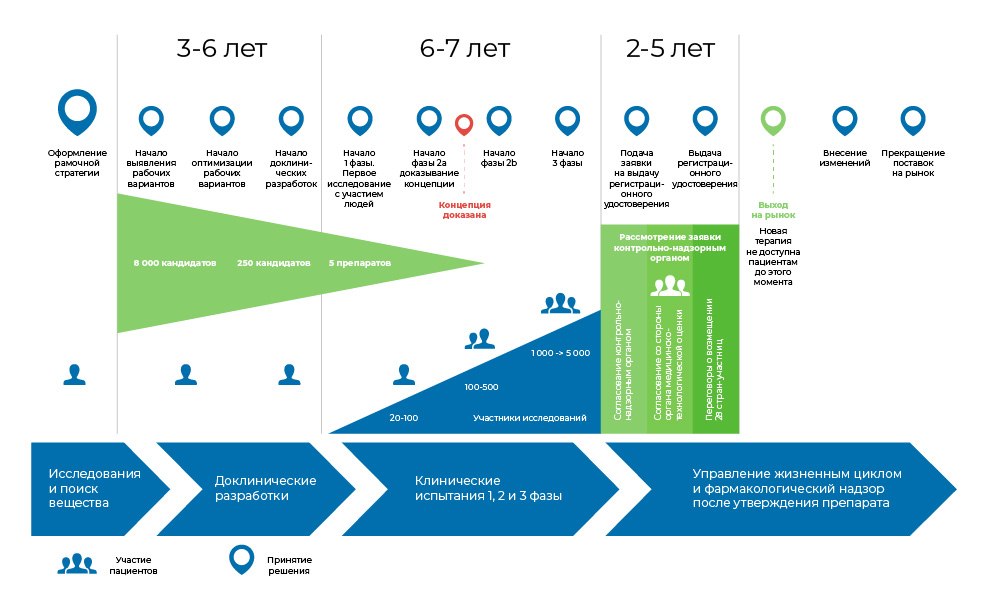
Процесс разработки медицинского препарата. С момента создания молекулы до момента начала продажи лекарства проходит от 8 до 20 лет.
Значит, это кому-нибудь нужно? Онкология — одна из самых вопиющих сфер медицины в плане неудовлетворенной потребности в лекарствах. По данным Всемирной организации здравоохранения, в 2018 году онкологические заболевания убили 9,6 миллиона человек. Часто опухоли обнаруживают на поздних стадиях, когда остается лишь паллиативное лечение.
При этом открытия в сфере молекулярной биологии и генетики позволили понять механизмы, которые способствуют развитию и прогрессированию рака, улучшилось понимание работы противоопухолевого иммунитета.
И сегодня разработка противоопухолевых препаратов – одно из самых наукоемких и востребованных направлений медицины.
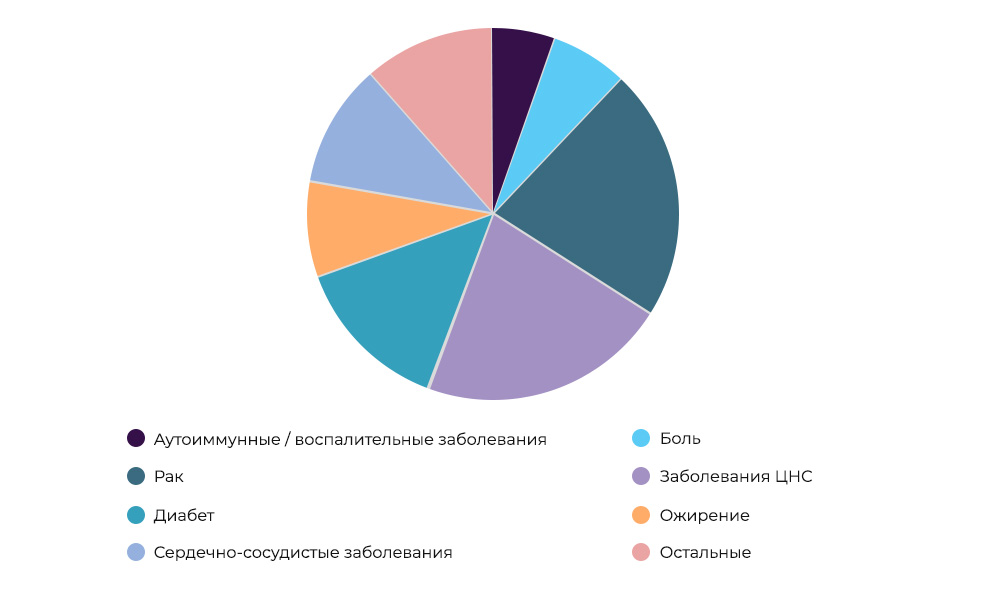
Исследования противораковых препаратов – 23% всех КИ в мире
Раньше многие фармкомпании проводили исследования самостоятельно, силами своего штата ученых. Сейчас медицинское учреждение, которое прошло аккредитацию и соответствует определенным требованиям, может стать площадкой и исполнителем для эксперимента.

Механизм работы таргетных препаратов при колоректальном раке. Раковые клетки прекращают делиться, либо приращивать к опухоли дополнительные кровеносные сосуды, либо препарат предохраняет соседние клетки от превращения в злокачественные
Чтобы найти такие вещества, а потом выбрать из кандидатов подходящие, требуется много ресурсов и времени на исследования in vitro и in silicio – то есть в пробирке или с помощью компьютерного моделирования.
Выбранное вещество запасают в нужном количестве – производят по специальным правилам (в России это ГОСТ Р 52249-2009), без примесей и нарушения технологии. И с этими пробирками ученые отправляются тестировать препарат на животных.
Мышь – двигатель прогресса. После проверки идей в пробирке ученый с запасом своего потенциального препарата идет в виварий – нужно проверить, как поведет себя прототип в теле млекопитающего (in vivo).
И до сих пор в медицине без опытов на животных – не обойтись. Львов и коней, правда, оставили в покое. Доклинические исследования во всем мире происходят, в основном, на мышах, морских свинках и кроликах.

Лабораторным мышкам даже поставили памятник в Новосибирском Академгородке
На этом этапе проверяют, насколько вреден/безопасен препарат:
- вызывает ли аллергию,
- оказывает ли токсичное влияние на ткани и органы,
- как влияет на способность животных к размножению и нормальному развитию плода и т.п.
Кроме того, наблюдают, как кандидат в лекарства ведет себя внутри организма зверька (фармакокинетика):
- скорость всасывания и нарастание концентрации в крови,
- каковы максимальная и минимальная доза,
- как быстро выводится из организма, и т.п.
Все эти данные нужны, чтобы решить: можно ли применять исследуемое вещество для людей. И если да – то сколько его нужно.
Неизбежное зло. Бюрократия. За правильным ходом КИ следят Департамент гос. регулирования обращения лекарственных средств Минздрава и Федеральная служба по надзору в сфере здравоохранения (Росздравнадзор).
Если ученый пришел к моменту, когда нужно переходить к клиническим исследованиям на людях – пора готовить заявку на проведение КИ. Для этого ему нужно несколько документов.
- Досье исследуемого лекарственного препарата. Все, что уже выяснили о препарате: данные о фармакокинетике, эффективности, токсичности и т.п.
- Протокол исследования. В нем подробно описан план будущего исследования и методики оценки результатов;
- Брошюра исследователя. Краткая шпаргалка, чтобы понятно объяснить суть исследования волонтерам и пациентам и получить их информированное согласие.
Этический комитет. Следующий этап квеста – получить оценку и заключение комитета по этике.
Комитет по этике – это независимая группа врачей, ученых, медицинского персонала и неспециалистов (представителей общественности). Они изучают протокол исследования и информированное согласие, чтобы до старта исследования удостовериться, что между пациентом, исследователями, фармкомпанией и национальным компетентным органом регулирования достигнуто согласие, ничьи права не нарушены, никто не подвергается принуждению и никому не прищемили свободу воли.
После проверки всех документов и одобрения этического комитета потенциальный препарат переходит в стадию клинических испытаний – на людях.
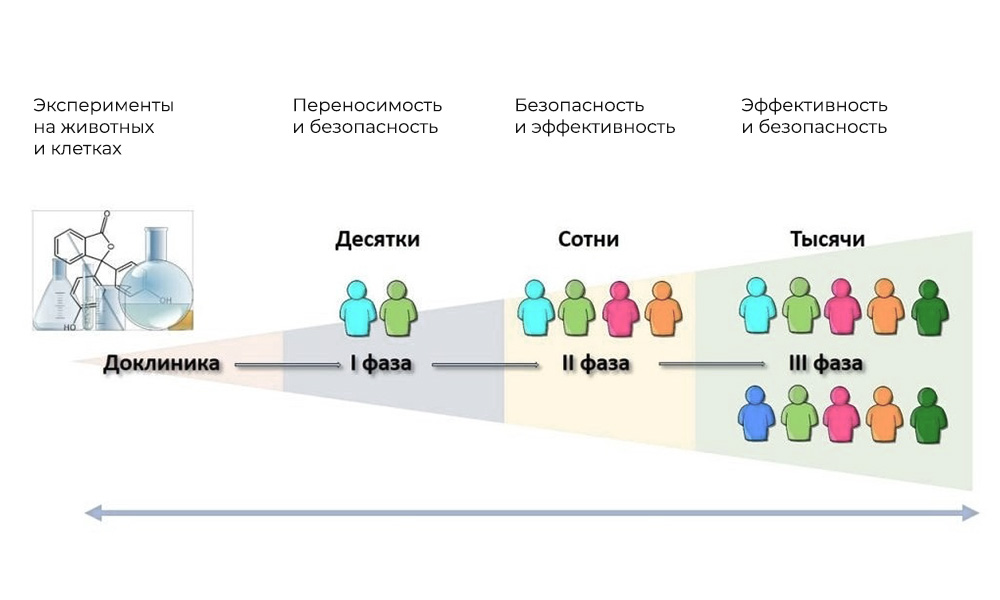
Основные фазы клинических исследований – на людях
Участники: 20 – 100 человек.
Длительность: от нескольких месяцев до 1 года.
Цель: изучить переносимость, фармакодинамику и фармакокинетику.
Проверяется, действует ли вещество на людей так же, как на животных, безопасно ли оно.
В первой фазе клинического исследования должны, теоретически, участвовать здоровые добровольцы, но в онкологии тестирование сильнодействующих веществ на здоровом организме нельзя назвать этичным. Поэтому участвуют люди с соответствующим заболеванием, против которого может быть эффективен будущий препарат.
Участникам постепенно вводят все бОльшие дозы препарата, начиная с минимальной и до максимально допустимой. После каждого введения отслеживается состояние пациента.
Оценивают фармакокинетику: скорость всасывания и экскреция (выделение неизменённого вещества), распределение по тканям и органам. Также оценивается фармакодинамика: действие препарата на клетки опухоли, на другие такни и органы, побочные эффекты. Выясняется предпочтительный вариант применения и уровень дозировки.
Кроме исследований с нарастающими дозами, в фазе I проверяют:
- действие пищи на препарат;
- взаимодействие с другими препаратами;
- влияние прочих заболеваний, которые могут повлиять на нужные дозы препарата (например, у пациента с почечной недостаточностью).
По данным FDA, первую фазу КИ успешно проходят 70% препаратов.
Участники: 100 – 500 пациентов.
Длительность: от нескольких месяцев до 2 лет.
Цель: проверка эффективности при определенных показаниях
Необходимо изучить, насколько новый препарат эффективнее по сравнению с плацебо или уже существующим лечением. Плюс, большее количество участников позволяет обнаружить более редкие побочные эффекты, которые не выявлены в фазе I.
Обычно на этой стадии исследования проводятся как двойные слепые рандомизированные плацебо-контролируемые.
Двойное ослепление: ни врач, ни пациент не знают, кто получает активное вещество, а кто – плацебо или оптимальное существующее на данный момент лечение.
Рандомизация подразумевает, что пациенты делятся на группы случайным образом – с помощью генератора случайных чисел. Повлиять на этот процесс не может ни врач, ни участник КИ.
Плацебо-контроль означает, что участники одной группы будут получать плацебо в таких же условиях, что и участники другой группы, которым дают активное вещество.

Всем – одинаковые на вид, вкус и запах лекарства.
Согласно данным FDA, лишь 33% препаратов, дошедших до фазы II, успешно проходят КИ и переходят в следующую фазу.
Количество участников: 300 – 3 000 и более.
Продолжительность: от года до нескольких лет.
Цель: подтверждение эффективности и безопасности исследуемого вещества на больших выборках.
Это самая крупномасштабная, сложная и дорогостоящая часть процесса разработки препарата. Цель таких исследований — подтвердить эффективность и безопасность исследуемого вещества при применении большим количеством пациентов.
По результатам этой фазы производители препарата получают разрешение для вывода его на рынок.
В фазе III могут принимать участие тысячи пациентов из разных стран. Все должно быть спланировано до мелочей, чтобы во всех местах проведения исследования его дизайн и значимые условия были абсолютно одинаковыми.
Дизайн исследования настолько узкий, что в него может попасть не только умирающий, но и пациент с прогнозом на стойкую ремиссию. Препарат должен быть настолько безопасным, чтобы его можно было давать практически здоровому человеку – и качество жизни не снижалось.
Перед началом фазы III проводится множество консилиумов и обсуждений между исследователями и сторонними экспертами: очень важно продумать дизайн экспериментов так, чтобы не упустить важное и получить все нужные данные.
В ходе фазы III окончательно подтверждается эффективность и безопасность нового лекарства, зависимость эффекта от дозы.
Анализируется соотношение преимуществ и рисков. По результатам контролирующий орган принимает решение о том, можно ли выводить препарат на рынок. Для этого нужно, чтобы соблюдались условия:
- препарат более эффективен, чем ранее известные аналоги,
- дает меньше побочных эффектов/лучше переносится,
- эффективен, когда не работают ранее известные препараты,
- более выгоден экономически,
- проще в применении.
Процесс рассмотрения заявки надзорным органом занимает 12-18 месяцев.
По данным FDA, третья фаза клинических исследований заканчивается положительным результатом лишь в 25-30% случаев от всех, что были на старте третьей фазы.
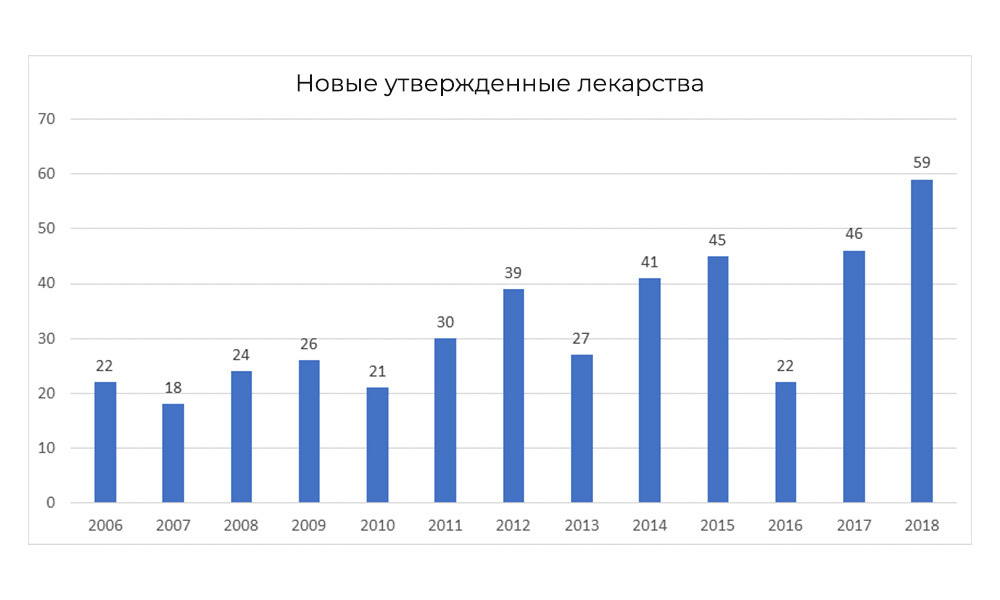
Тем не менее, в 2018 FDA побила собственный рекорд по числу одобренных препаратов
У контроля за новыми препаратами в России есть свои баги (или фичи, как посмотреть). По закону, одобренные зарубежные препараты должны пройти дополнительные клинические испытания в России: якобы, это повысит качество зарубежных препаратов.
Когда препарат уже прошел 3 фазы, вышел в продажу на мировой рынок, в нашей стране он еще может быть не зарегистрирован. Мы знаем, что он работает, в его инструкции на иностранных языках есть показания, подтвержденные 3 фазами исследований в США, или Канаде, или Европе.
Скажем, 12 показаний – 12 диагнозов, при которых препарат будет эффективен. Но в России еще не все эти показания подтвердили официально, только 6 из 12. И если у пациента именно тот вид рака, для лечения которого препарат еще пока официально не зарегистрирован в РФ, такой препарат бесплатно, в рамках ОМС, он не получит.
Это на 2-3 года замедляет пациентам доступ к новым лекарствам.
К сожалению, нас таких мало. Не всякая клиника может принимать у себя КИ.
Во-первых, у клиники должен быть сертификат GCP, Good Clinical Practice.
Во-вторых, исследователей должно быть минимум двое. У них тоже сертификаты, и не так-то просто их добыть: выдаются контролирующим органом страны-производителя препарата. В нашем случае это США и Франция. Проверяли двух врачей полгода.
В-третьих, сама клиника. Обязательно отделение реанимации, своя лаборатория, сертифицированные медсестры, правильная калибровка нужных автоматов, определенные помещения для хранения препаратов и документов, анонимные помещения, где нет камер – для пациентов. Чтобы запуститься в первый раз – пришлось переоборудовать некоторые кабинеты и палаты: вплоть до новых кроватей, все по дизайну КИ.

Для разных препаратов – разные холодильники
Словом, те клиники и врачи, которые хотят этим заниматься, должны еще постараться, чтобы создать определенные условия.
Набираем 2 или 3 группы пациентов, подписываем с ними информированное согласие.
Обычно на участие в клинических исследованиях люди соглашаются по 2 причинам:
- отсутствие эффективных методов лечения их болезни,
- желание сделать вклад в развитие науки.
В любом случае это исключительно добровольное решение. Исследователи обязаны в письменном виде предоставить пациенту информацию о цели КИ, о том, как оно будет проводиться, какое лекарство будет применяться, и т.п. Все это отражено в особом документе —информированном согласии. Каждый участник исследования застрахован от причинения вреда жизни и здоровью.
Наши пациенты пока ни разу не отказывались – для них это невероятный шанс получить лечение, причем бесплатное, когда остальные методы терапии уже исчерпали себя.
Но онкологических пациентов у нас много. Если клиент признается, что денег на лечение нет – мы обязательно проверяем требования к участникам исследования. Вполне возможно, что ему найдется место.
В данный момент открыт набор в 18 крупномасштабных исследований.
Конечно, масштабы в частной клинике – совсем не то, что в большом НИИ, но обычно 3-4 пациента в неделю попадают в протокол исследования. Это немало: не менее 10 человек в месяц, которые получают самое продвинутое передовое лечение – бесплатно.
И у них самих появляется дополнительный шанс, и будущие пациенты скорее смогут получить этот препарат, когда закончится КИ.
Пациенты вовсе не обязательно постоянно находятся в клинике – если это не запрещено дизайном КИ и пациент чувствует себя хорошо – он участвует амбулаторно. Приходит, получает свою капельницу и уходит. Есть и такие, кому лучше остаться в клинике, под присмотром.
В результате долгих месяцев скрупулезного выполнения длинного списка требований, постоянного мониторинга состояния пациента, консолидации данных по десяткам параметров мы делаем исследования, которые будут опубликованы, а пользоваться результатами – расширенной возможностью применения новых препаратов – будут все врачи из всех онкоцентров страны. И несколько десятков человек получают шанс на лечение прямо сейчас.
Надеемся, этот текст был для вас просто интересным чтением.
Читайте также:

