Как заставить раковые клетки самоуничтожится
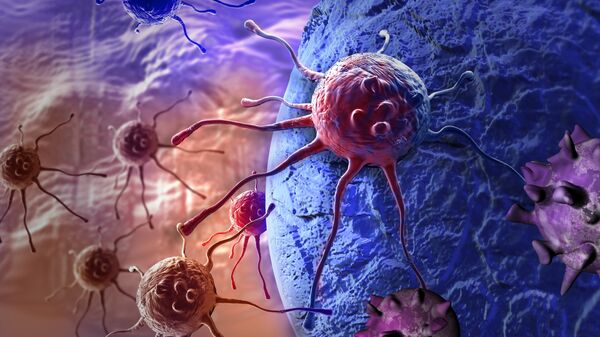
МОСКВА, 30 ноя — РИА Новости. Биологи из МГУ и их шведские коллеги выяснили, что раковые клетки можно заставить самоуничтожаться при делении, если ввести в них вещества, связанные с так называемой митотической катастрофой. Об этом говорится в статье, опубликованной в журнале Scientific Reports.
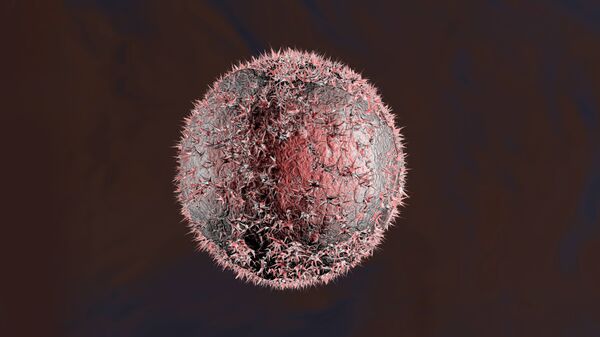
Значительная часть раковых опухолей возникает из-за поломки в гене p53. Он отвечает за синтез белка, который обеспечивает целостность генетической информации, а при серьезных повреждениях ДНК включает механизм самоуничтожения — апоптоз. Поэтому культуры клеток с поврежденным геном p53 крайне сложно уничтожить — в их геноме просто нет программы самоуничтожения.
Существуют и другие механизмы самоуничтожения клеток, например энтоз и митотическая катастрофа. Под последней биологи понимают сложный процесс, который приводит к резкому увеличению размеров клетки, появлению в ней лишних ядер и гибели в тот момент, когда она начинает делиться и при этом имеет серьезные повреждения в ДНК.
Ученые считают митотическую катастрофу одним из защитных механизмов организма, который убивает клетки до того, как они превращаются в раковые новообразования и становятся угрозой для жизни.
Животовский и его коллеги решили выяснить, какую роль играют в этом процессе митохондрии — своеобразные "энергостанции" клетки. Они не только вырабатывают молекулы "энерговалюты" АТФ, но и участвуют в запуске апоптоза. Это натолкнуло биологов на мысль, что митохондрии могут быть задействованы и в митотической катастрофе.
Для проверки этой идеи ученые вырастили культуру раковых клеток прямой кишки и попытались вызвать митотическую катастрофу при помощи двух противораковых лекарств — антибиотика доксирубицина, который продуцируют микробы-стрептомицеты, и алкалоида колцемида, получаемого из цветов-осенников. Оба препарата нарушают работу двух ключевых этапов цикла деления клетки.
Как показали опыты, комбинация этих веществ заставляет примерно 80% раковых клеток самоуничтожиться во время деления. Это позволило биологам детально изучить роль митохондрий в данном процессе, а также то, какие изменения в работе клеток запускают его.
Во-первых, ученые обнаружили, что наступление митотической катастрофы само по себе не приводит к смерти клетки — она самоуничтожается потому, что в ней активируются цепочки генов, связанные с двумя другими типами клеточной смерти, — апоптозом и аутофагией.

Во-вторых, оказалось, что для запуска митотической катастрофы необходимо лишь прекратить доступ кислорода к митохондриям и заставить их выделять два "белка смерти" — Mcl-1 и Bcl-xL. Сейчас Животовский и его команда проверяют несколько соединений, способных вызывать подобную реакцию в раковых клетках и не затрагивать их здоровых соседей.
Если эти эксперименты закончатся удачно, то ученым, вероятно, удастся создать новый класс противораковых препаратов с куда более щадящим эффектом, чем радиация или химиотерапия.
Сколько в человеческом организме клеток, не знает никто. Публикуемые в научных работах шести-, семи-, а то и восьмизначные цифры обозначают лишь приблизительную вероятность, но не реальное количество. Гораздо точнее наука установила разницу между ними - клетки сердца, легких, печени, почек, любых тканей отличаются друг от друга белками, из которых состоят, ферментами, участвующими в их функционировании, генами в их ДНК. И в "чужом" органе они работать не будут. Исключение составляют так называемые стволовые клетки, но не о них сейчас речь.
Но есть одно свойство, присущее всем клеткам, - свойство, за которое ученый с мировым именем академик РАН Владимир Скулачев образно назвал их камикадзе, - готовность в любой момент прибегнуть к "самоубийству" - запрограммированной клеточной смерти, называемой апоптозом. Название придумал древнеримский врач Гален, наблюдая осенний сброс листвы деревьями, - тоже своего рода суицид. К апоптозу клетка прибегает тогда, когда что-то в ней непоправимо сломалось и ее дальнейшее существование может навредить организму. Подчеркиваю: только может навредить, до настоящего вреда дело не доходит, поскольку тут же поступает приказ на уничтожение и запускается система умерщвления. Вот так клетки бросаются на амбразуру - все, кроме раковых.
Раковые будто пришли с другой планеты. В отличие от остальных они безудержно размножаются, пожирая ткани вокруг себя и образуя опухоль, растущую как лавина. И обладают поразительной способностью к выживанию, вот почему так трудно остановить их рост, а еще труднее вообще уничтожить. В отличие от остальных клеток, срок жизни которых исчисляется днями или неделями, раковые умирают вместе с "хозяином", в теле которого поселились и которого сами же убили. В некоторых лабораториях мира они живут в колбах уже более ста лет и чувствуют себя превосходно. И до недавнего времени считалось, что к добровольному уходу из жизни они неспособны. Российские и американские исследователи доказали, что это мнение ошибочно.
- Апоптоз, самоубийство клеток происходит по сложной, четко отработанной технологии, - рассказывает руководитель российской группы исследователей, лауреат Ленинской премии Михаил Ханин, профессор Центра теоретических проблем физико-химической фармакологии РАН. - В каждой клетке затаились и ждут своего часа особые ферменты, их называют каспазами. Это - палачи, непосредственные исполнители смертной казни. А сигнал к исполнению дают специальные рецепторы на клеточной мембране, зорко следящие за состоянием своей клетки, за ее взаимодействием с окружающими тканями и точно отмечающие момент, когда она может стать опасной для организма. Специалисты называют их жутковато - "рецепторы смерти". Отданный ими сигнал запускает длинную цепь биохимических реакций, в результате которых мирно "спящие" каспазы превращаются вдруг в бешеных убийц, уничтожающих цитоплазму, ядро и наконец сам геном клетки. Она сморщивается, уменьшает объем, после чего ее съедают окружающие здоровые клетки, используя ее ткани в своем развитии. Так сказать, своего рода безотходная технология.
Уже 30 лет биологи интенсивно изучают механизм апоптоза. И довольно далеко продвинулись в этой работе. Главное, выяснили, как запускается в действие огромная, многоэтапная цепочка биохимических реакций, несущая роковой приказ клетке на самоуничтожение, где одни белки и ферменты передают эстафету другим, на определенных этапах к ним примыкают третьи, четвертые, пятые и еще другие, которые вроде бы и не имеют прямого отношения к поставленной задаче, но без их присутствия приказ до цели не дойдет. Более того, исследователи научились сами запускать цепную реакцию апоптоза, провоцируя "рецепторы смерти" давать сигнал на уничтожение, и вполне работоспособные клетки послушно кончают самоубийством. Теперь остался последний шаг: от обычных клеток перейти к раковым.
Заставить раковую клетку покончить с собой. На первый взгляд - задача из области фантастики. Ведь цель этих клеток не оберегать организм, в котором они живут, а, наоборот, уничтожать окружающие ткани, пожирая их и перерабатывая в собственные белки, чтобы питать ими постоянно растущую опухоль. Так что, логически рассуждая с позиций здравого смысла, у раковых клеток вовсе не должно быть механизма апоптоза, а если он почему-то есть, то должен быть просто неработоспособным. Вот таким предположением поделился я со своим собеседником, чем вызвал у него откровенную усмешку.
- Неблагодарное это занятие - пытаться разгадать загадки природы, опираясь на обывательскую логику здравого смысла, - сказал Михаил Ханин. - Природа мыслит другими категориями, учитывая в своих решениях множество факторов, которые, на наш взгляд, никакого отношения к данной проблеме не имеют. Вот так и с раковыми клетками. Казалось бы, зачем им апоптоз, если их предназначение разрушать организм, а не оберегать его? Тем не менее в каждой раковой клетке, как и в любой другой, есть механизм самоуничтожения. И он безотказно срабатывает, если суметь его запустить.
В последней фразе - суть проблемы. Раковые клетки - отнюдь не сестры-близнецы, у каждого вида рака они свои. И по-разному противостоят попыткам запустить механизм апоптоза. Большинство клеток бешено сопротивляются, другие поддаются команде на уничтожение так же, как и обычные клетки, а третьи даже легче. Вот почему медицина достигла определенных успехов в лечении онкологических заболеваний. Некоторые болезни подчас излечиваются полностью, развитие других сильно замедляется. Сегодня медики считают, что все виды рака можно излечить апоптозом, тем более что механизмы его запуска давно освоены. Это, в частности, всем известные - радиационное облучение и химические токсичные вещества, которые не просто сами разрушают раковые клетки, как считалось раньше, а заставляют "рецепторы смерти" дать роковой сигнал. И чем раньше обнаружены скопления раковых клеток, начавших превращаться в опухоль, тем меньше их живучесть, тем слабее сопротивление сигналу на смерть. Есть и другие способы запуска апоптоза, только вот беда: ни один из них не дает стопроцентного эффекта. Один и тот же рак на одной и той же стадии у одного больного иногда излечивается полностью, у второго просто прекращается рост опухоли, а у третьего он лишь слегка замедляется. К тому же при одном запуске апоптоза результаты одни, при другом у того же вида рака бывают совсем другие. Поэтому не всегда можно предсказать заранее, что лучше поможет данному больному: облучение или химиотерапия? Почему же так происходит? А дело в том, что для науки до сих пор остается "черной дырой" средний этап апоптоза - процессы, происходящие между подачей сигнала на смерть и до разрушения клетки.
- Задача медицины - подавить сопротивление раковых клеток сигналу саморазрушения,- говорит Михаил Александрович,- добиться его неукоснительного выполнения. На это и направлена наша работа совместно с американскими коллегами из клиники Мейо в городе Рочестер (штат Миннесота), которой руководит выдающийся исследователь апоптоза, доктор философии и медицины, профессор Скотт Гарольд Кауфманн. И решаем мы эту проблему с двух разных сторон, соединив, казалось бы, далекие друг от друга вещи - биохимию и математику.
Надо думать, природе пришлось немало потрудиться, чтобы решить головоломную задачу - как изменить главное свойство обычной клетки при перерождении ее в раковую, не изменяя ее строения. Ведь механизм апоптоза никуда не выбросишь, он остается в клетке, задачи которой теперь кардинально меняются: не оберегать организм, а разрушать его. И апоптоз должен не мешать этому процессу, но тем не менее быть готовым и к разрушению самой клетки на случай, так сказать, непредвиденных ситуаций. Природа решила эту задачу, сделав раковый апоптоз сложнейшей нелинейной системой, в которой участвует огромное количество белков, где одни способствуют самоубийству клеток, другие не мешают, а третьи препятствуют. И во всей этой запутанной паутине различных биохимических процессов скрывается некий единственный процесс, который и приводит к окончательному результату - смерти клетки. Природе он известен, и она им иногда пользуется: иначе чем объяснить редкие случаи самоизлечения рака, ставящие медиков в тупик? Науке же пока известно, что этот процесс существует и у каждого вида рака он свой. Его и необходимо вычленить, выявить участвующие в нем белки, определить влияние каждого из них на общую динамику системы. Более того, необходимо определить скорость каждой из десятков и сотен биохимических реакций, входящих в систему апоптоза данного вида рака, без чего невозможно научиться управлять этим процессом. По сравнению со всей этой работой поиски пресловутой иголки в стоге сена - задачка для первоклассников. И исследования американских биохимиков грозили затянуться на десятки лет, если бы к ним не пришли на помощь российские математики.
- В последние годы математические и компьютерные модели занимают все большее место в биологических лабораториях, показав себя весьма эффективным методом исследования динамики сложных биохимических систем, - отмечает профессор Ханин. - А если говорить просто, то все, что биохимики создают в своих колбах и на что у них уходят недели и месяцы, а бывает, и годы, мы воспроизводим на экране компьютера, за считаные минуты проигрывая вариант за вариантом.
Конечно, это сказано слишком просто. На деле же идет сложнейшая работа - скрупулезный перебор на компьютерных моделях всех биохимических реакций, входящих в систему апоптоза, и их сочетаний. Определение их скоростей и других параметров, сверка полученных данных с теми, что успели получить коллеги за океаном - если сошлось, значит, правильно. Вот так белок за белком определяется одна из возможных цепочек от "рецепторов смерти" до раковых клеток. Но как определить, та ли это цепочка, по которой приказ на смерть дойдет до адресата, не потеряв силы, и разбудит "спящих" каспаз, заставив их приступить к своей палаческой работе? Или в нее попали белки лишние, не поддерживающие приказа, а то и препятствующие ему? Поэтому полученные варианты тестируются великим принципом оптимальности, которым руководствуется природа, создавая все свои творения. Он гласит, что все, что делается, должно происходить с минимальными затратами времени и энергии. Поэтому исследователи четко знают, что им надо искать, - цепочку биохимических реакций, содержащую минимальное количество белков, по которой сигнал на смерть доходит до палачей-каспаз за минимальное время и с минимальными потерями энергии. А вот получение этих данных позволит медикам создать систему управления механизмом апоптоза, действующую при лечении больных с максимальной эффективностью.
Рак остается одним из самых сложных для лечения заболеваний, от которого не существует одного эффективного лекарства. При этом в многочисленных исследованиях, посвященных поиску эффективных средств от недуга, не раз упоминаются определенные продукты питания, которые разными исследователями считаются эффективными для уничтожения раковых стволовых клеток.

Это очень важно, потому что именно тот факт, что химиотерапия не уничтожает раковые стволовые клетки, считается причиной того, что у онкологических пациентов случаются рецидивы и появляются метастазы. Эти клетки, иногда называемые "материнскими клетками", составляют лишь небольшую часть всех клеток опухоли, но они имеют способность самовосстанавливаться и сопротивляются химиотерапии. Они также могут отделяться и создавать новые колонии опухолей, поэтому их уничтожение является ключом к эффективному лечению рака в долгосрочной перспективе.
Лекарств, нацеленных конкретно на эти клетки, нет, но исследователи обнаружили множество природных веществ, способных бороться с этими клетками. Naturalnews. com перечислил продукты, которые являются лучшими "убийцами" раковых клеток.
Зеленый чай
Зеленый чай уже давно используется в китайской медицине для лечения множества недугов, но только недавно исследователи раскрыли его невероятный потенциал для лечения рака. Исследователи из медицинского центра Бэйлорского университета обнаружили, что активный ингредиент зеленого чая, EGCG (epigallocatechin-3-gallate), убивает раковые стволовые клетки и, следовательно, может помочь в случаях, когда образование не поддается химиотерапии. Хотя EGCG присутствует также в черном чае, в зеленом чае его концентрация выше.
Имбирь
Доклиническое исследование показывает, что один из компонентов имбиря дает в 10 000 раз большую эффективность в борьбе со стволовыми клетками при раке молочной железы, чем популярный препарат Таксол. Компонент, который известен как 6-Shogaol, выделяется, когда корень имбиря сварен или высушен, и его концентрация, необходимая для умерщвления раковых клеток, для клеток здоровых не опасна, в отличие от традиционных препаратов, применяемых в таких случаях.
Куркума
Куркумин, компонент древней индийской специи куркума, может выборочно влиять на стволовые раковые клетки без риска воздействия на здоровые стволовые клетки, необходимые для регенерации ткани. Это вещество эффективно при раке молочной железы, раке поджелудочной железы, колоректальном раке и раке головного мозга.
Ягоды винограда
Вещество resveratrol, которое находится в коже и семенах ягод винограда, наносит "смертельный" удар по стволовым клеткам рака толстой кишки. Таковы выводы ученых из Пенсильванского университета. Они верят, что в будущем это открытие поможет научиться предотвращать рак толстой кишки, который является одним из самых распространенных ныне типов рака. Когда во время эксперимента resveratrol и выдержка из семени винограда принимались одновременно, их воздействие было чрезвычайно мощно, и при этом они не повредили здоровым клеткам.
Другие продукты, которые убивают раковые стволовые клетки
Хотя вышеозначенные продукты — одни из самых мощных противораковых природных лекарств, есть и много других со сходным эффектом. Среди них — черника, морковь, кофе, грейпфрут, мята, вишня, лук, черный перец и тимьян.
Обилие продуктов, которые могут иметь большое влияние на рак, напоминает нам, насколько эффективно и безопасно природа может помочь справиться с серьезными недугами нашего времени. Многие врачи не очень хорошо разбираются в теме, у иных же есть финансовые мотивы, чтобы продолжать настаивать на дорогих и часто опасных лекарствах. По этой причине есть большой смысл расширять свой кругозор и узнавать, что, помимо лекарственной помощи, доступно нам в борьбе с серьезными заболеваниями.
Злокачественную опухоль можно усыпить, не вмешиваясь в клеточную ДНК – можно просто отключить белки, которые помогают клеткам делиться.
Обычные методы противораковой терапии нацелены на то, чтобы повредить ДНК раковых клеток. Это может быть жесткое ионизирующее излучение, как при радиотерапии, или какое-нибудь вещество-мутаген, как в химиотерапии; в любом случае в ДНК возникают множественные разрывы, с которыми клетка не может размножаться – у нее просто не получится правильно скопировать свою ДНК для дочерних клеток, да и вообще гены с повреждениями работать не могут.
Конечно, есть специальные ремонтные системы, но у раковых клеток такие системы часто изначально повреждены – ведь и сами злокачественные опухоли возникают из-за неотремонтированных дефектов в геноме. Лекарства и облучение портят ДНК еще сильнее, чтобы даже раковая клетка не смогла выжить.
Однако такие средства повреждают не только раковые, но и здоровые клетки – побочные эффекты от радиотерапии и химиотерапии бывают весьма и весьма тяжелыми. Здесь можно, с одной стороны, попытаться организовать адресную доставку: сделать прибор для облучения, который можно было бы настроить строго на область опухоли, или сделать какие-нибудь частицы с лекарственной начинкой, которые накапливались бы только в злокачественных клетках, высвобождая в них лекарство. С другой стороны, можно пойти иной дорогой и действовать на рак, не разрушая ДНК.
Часто клетки перерождаются в опухолевые оттого, что в них из-за мутаций становятся слишком активны определенные белки – обычно те, что помогают клетке делиться. Одни из самых известных таких белков – KAT6A и KAT6B. Про KAT6A обычно говорят в связи с острым миелоидным лейкозом, KAT6B связан с целым рядом различных опухолей.
Не вдаваясь в подробности, напомним, что ДНК в клетках всегда находится в комплексе с особыми белками – гистонами. Некоторые участки ДНК сильно упакованы с помощью гистонов и недоступны для молекулярных машин, считывающих генетическую информацию; другие участки ДНК, наоборот, открыты для работы. Есть специальные ферменты, которые химически модифицируют гистоны-упаковщики, так что они то открывают ДНК ко всеобщему доступу, то закрывают. И вот KAT6A и KAT6B как раз открывают для работы те гены, от которых зависит размножение клетки.
Сотрудники Института медицинских исследований Уолтера и Элизы Холл вместе с коллегами из Мельбурнского университета, Университета Монаша и других научных центров в прошлом пытались выключать сам ген KAT6A, и оказалось, что с выключенным KAT6A больные животные живут в четыре раза дольше.
Но если все-таки не вмешиваться в ДНК? В новой статье, опубликованной в Nature, исследователи описывают два вещества, которые избирательно подавляют активность белков KAT6A и KAT6B – оба вещества испытывали на клеточных культурах и на животных: на рыбах с карциномой печени и на мышах с лимфомой.
Во всех случаях злокачественные клетки переставали делиться, как бы засыпая, однако сон этот оказывался вечным. Раковая клетка, в общем-то, ничего другого не умеет, кроме как размножаться, и все у нее нацелено на деление. Если им запретить делиться, они начинают стареть: они синтезируют меньше белков, у них снижается энергообмен, в них накапливается биохимический мусор. В стареющих клетках может включиться программа клеточного самоубийства – чтобы клетка погибла аккуратно, не мешая окружающим; если же такая программа не включается, их уничтожает иммунитет.
Пока что авторы работы увидели, как раковые опухоли останавливаются в росте и как их клетки начинают стареть. И стоит еще раз отметить, что это удалось сделать, не портя им ДНК.
Конечно, возникает вопрос, как к таким веществам, которые запрещают делиться, отнесутся другие, здоровые клетки, которые тоже сохраняют способность к размножению, вроде стволовых.
Источник: Наука и жизнь (nkj.ru)
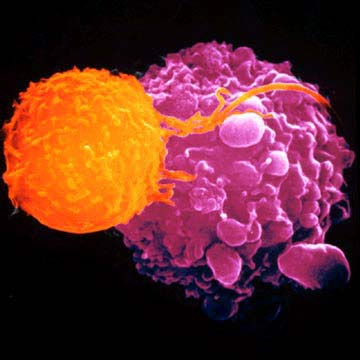
Если разбудить Т-лимфоциты, сидящие внутри опухоли, они не только уничтожат ее саму, но и найдут другие очаги болезни, рассеянные по организму.

Эксперименты на человеческих клетках рака толстой кишки и лимфомы, внедренных в организм грызунов, обнаружили, что подавление специфического белка, который питает опухоли, убивает рак.
В настоящее время ученые располагают готовыми лекарственными препаратами, блокирующими данную субстанцию под названием ATF4.
Результаты нового исследования позволяют надеяться на скорое появление революционной противоопухолевой терапии, избирательно действующей на раковые клетки.
Миллион клеток нашего организма каждый день совершают самоубийство, чтобы защитить человеческий организм от появления потенциально опасных единиц. Клетки рака, с другой стороны, игнорируют контроль со стороны иммунной системы.
Ученые годами пытались подавить активность гена MYC, который в случае онкогенных мутаций стимулирует пролиферацию опухолевых клеток и отвечает за распространение болезни.
Профессор Куменис и его коллеги из Пенсильванского университета (США) обнаружили, что ATF4 контролирует особый химический путь, работающий в тандеме с геном. Они утверждают, что если он остановится, раковые клетки вырабатывают много белка и погибают.
Результаты, опубликованные в журнале Nature Cell Biology, могут открыть путь к новому подходу в лечении рака. Препараты-ингибиторы, которые останавливают биосинтез ATF4 (активирующий фактор транскрипции 4), уже существуют на фармацевтическом рынке. Они изучаются при множестве заболеваний, включая болезнь Паркинсона и Альцгеймера.
Как запустить самоуничтожение рака?
Нормальные варианты MYC контролируют рост здоровых клеток и выполняют физиологическую функцию. Однако мутантные гены MYC становятся проблемой – они вызывают цепную реакцию, которая помогает опухолям развиваться и распространяться.
В настоящее время не существует конкретного способа нацеливания на этот ген, поэтому все больше внимания уделяется альтернативным способам косвенного влияния на процесс. Команда профессора Кумениса установила, что в некоторых опухолях ATF4 активируется особым ферментом, известным как трансмембранная протеинкиназа PERK.

Однако блокировать этот белок не всегда удается, потому что MYC фактически контролирует второй фермент GCN2, который может действовать параллельно, что делает PERK ненужным.
Альтернативный подход ученых заключается в том, чтобы воздействовать на сам ATF4 – единственную точку, где сходятся оба этих сигнальных пути. По словам Кумениса, это дает опухолевым клеткам минимальные шансы на выживание и процветание.
Ученые также выяснили, что белок ATF4 активирует гены, используемые MYC для клеточного роста, а также контролирует скорость продукции специфических белков под названием 4E-BP.
В опухолях человека, связанных с мутацией MYC, экспрессия ATF4 и 4E-BP также была повышена. Профессор Куменис называет это свидетельством того, что уникальный подход окажется успешным в клинической практике.
По оценкам Международного агентства по исследованию рака, 18 миллионов человек в год заболевают раком, а около 10 миллионов человек ежегодно умирает от онкологии.
Исследователи по всему миру постоянно ищут лучшее лечение рака, но полная победа ещё далека.
Константин Моканов: магистр фармации и профессиональный медицинский переводчик
Ученые из Северо-Западного университета (штат Иллинойс, США) разработали способ запуска древнего "аварийного выключателя" рака, который спрятан в наших генах. Результаты исследования опубликованы в OncoTarget.
Рак – один из самых злейших и постоянных врагов человечества. Но если на сегодняшний день у человека имеется развитая иммунная система для борьбы, то как же ранняя многоклеточная жизнь справилась с этим? Скорее всего, существовала некая генетическая "аварийная кнопка", которая и была любимым оружием организма против заболевания. Сделав такое предположение, ученые Северо-Западного университета инициировали свое исследование и теперь сделали заявление, что обнаружили способ запуска этого древнего механизма. Полученные результаты потенциально могут способствовать разработке новой терапии, когда раковые клетки начнут самоуничтожаться и не смогут выработать адаптационные схемы.
Рак начинает формироваться, когда обычные клетки ломают привычную упорядоченность, начиная расти и размножаться быстрее, чем они должны. В конце концов, лишние клетки образуют опухоль. Конечно, в скором времени такое отклонение от нормы привлекает особое внимание иммунной системы, функцией которой как раз и является уничтожение опасных клеток. К сожалению, иммунная система далеко не всегда вовремя реагирует, а рак в свою очередь имеет некоторые хитроумные козыри в рукаве, чтобы избежать обнаружения.

"Можно сказать, что уже более чем 2 миллиарда лет живым организмам приходится заниматься профилактикой или уже непосредственно борьбой с раком", – рассказывает ведущий автор исследования Маркус Питер. "Таким образом, организм должен был каким-то образом разработать действенный механизм безопасности, предотвращающий рак, или помогающий реагировать на него в тот момент, когда он образуется. Если бы такого механизма не существовало, то и нас с вами не было бы сейчас здесь", – добавляет биолог.
Поэтому команда ученых начала поиск именно такой "аварийной кнопки", скрытой в нашем геноме. Это был трудоемкий и сложный процесс, так как любой вид подобной защиты появляется там, где она нужна в данный конкретный момент. То есть механизм активизируется в отдельной ячейке тогда, когда она станет раковой. В конце концов, команде удалось обнаружить молекулярное оружие, которое они искали.
Определенные нуклеотидные последовательности гена, имеющиеся во всем геноме человека, могут быть преобразованы в молекулы, называемые siRNAs – малыми интерферирующими РНК. Когда они вводятся в клетки, то подавляют активность генов, из которых они были первоначально созданы. Поэтому команда разработала siRNAs, которые нацелены на три гена, на которые опирается рак, эффективно заставляя клетки убивать себя.
Так как это влияет одновременно на 3 различных "гена выживания", молекулы запускают ни один, а несколько путей смерти клеток сразу. То есть рак не может разработать устойчивость к лечению. Исследователи назвали механизм DISE – Death Induced by Survival gene Elimination.
"Надеемся, что это станет по-настоящему серьезным прорывом", – отмечает Маркус Питер. "Мы полагаем, что именно таким образом многоклеточные организмы устраняли рак до того, как была развита адаптивная иммунная система. А появилась она всего около 500 миллионов лет назад. Это может быть именно та "аварийная кнопка", которая вынуждает клетки-изгои "совершать самоубийство". Мы считаем, что данный защитный механизм имеется в каждой клетке".
Как отмечают авторы New Atlas, немного беспокоит именно тот факт, что механизм DISE может применяться практически к любой клетке. Но команда Питера утверждает: опыты показывают, что он предпочитает раковые клетки. Исследователи уже опробовали новое лечение на мышах, больных раком яичников. И первые результаты не могут не радовать: что рост опухоли был значительно снижен, при этом не было выявлено ни каких-то побочных токсических эффектов, ни признаков резистентности рака к молекулам. Сейчас ученые Северо-Западного университета продолжают свое исследование в надежде, что DISE может стать эффективным вариантом лечения рака.

Сигналом для этих белков служит неправильная работа так называемых протоонкогенных белков — именно они в большинстве случаев запускают развитие рака. Часто эти белки, регулирующие деление клетки, являются клеточными рецепторами; кроме того, они сами по себе важны для нормальной жизнедеятельности клетки, но мутации в генах этих белков нередко фатальны. Мутировавший протоонкогенный белок становится просто онкогенным и начинает непрерывно слать в клеточное ядро сигнал к размножению, что и влечёт за собой образование опухоли.
К подобного рода белкам-рецепторам-протоонкогенам относится один из белков семейства Ras, представители которого виновны в возникновении 30% онкозаболеваний у человека. Лаборатория Шемуса Мартина при Дублинском университете обнаружила в гене Ras мутацию, которая провоцирует аутофагию новообразованных раковых клеток. Белок Ras с этой мутацией способен стимулировать синтез другого белка, Noxa, который в свою очередь является спусковым крючком в программе саморазрушения клетки.
В то же время исследователи отметили роль другого белка — Bcl2 — в торможении процесса клеточного самоубийства. Он является регулятором апоптоза, препятствуя бесконтрольной и ненужной смерти здоровых клеток. Однако белок может действовать и во вред, тормозя уничтожение раковых клеток. Работой Bcl2 можно легко объяснить то, почему не происходит полной ликвидации раковых клеток в организме.

Так происходит со всеми неполноценными клетками, но только не с раковыми. Раковые вместо самоуничтожения безудержно размножаются, пожирая ткани вокруг себя и образуя опухоль, растущую со скоростью лавины. Клетки эти обладают поразительной способностью к выживанию, поэтому так трудно остановить их рост, еще труднее уничтожить.
Неужели заставить раковую клетку покончить с собой-задача из области фантастики? Оказалось, что в каждой раковой клетке, как и в любой другой, есть механизм самоуничтожения. И он безотказно срабатывает, если суметь его запустить . Заставить раковые клетки подчиниться приказу на саморазрушение — главная задача медиков.
Есть и другие способы запуска апоптоза, но ни один из них не дает стопроцентного эффекта излечения. Кроме того, лечение одного и того же вида рака на одной и той же стадии у разных людей проходит чрезвычайно индивидуально. Кто-то вылечивается полностью, а у кого-то только замедляется рост опухоли. Для науки до сих пор остается непознанным средний этап апоптоза — процессы, которые происходят между подачей сигнала на уничтожение клетки и началом ее разрушения.
Читайте также:

