Как составлять электронные уравнения с хлором
Спецификой многих ОВР является то, что при составлении их уравнений подбор коэффициентов вызывает затруднение. Для облегчения подбора коэффициентов чаще всего используют метод электронного баланса и ионно-электронный метод (метод полуреакций). Рассмотрим применение каждого из этих методов на примерах.
Метод электронного баланса
В его основе лежит следующее правило: общее число электронов, отдаваемое атомами-восстановителями, должно совпадать с общим числом электронов, которые принимают атомы-окислители .
В качестве примера составления ОВР рассмотрим процесс взаимодействия сульфита натрия с перманганатом калия в кислой среде.
- Сначала необходимо составить схему реакции: записать вещества в начале и конце реакции, учитывая, что в кислой среде MnO4 — восстанавливается до Mn 2+ (см. схему):
- Далее определим какие из соединений являются окислителем и восстановителем; найдем их степень окисления в начале и конце реакции:
Из приведенной схемы понятно, что в процессе реакции происходит увеличение степени окисления серы с +4 до +6, таким образом, S +4 отдает 2 электрона и является восстановителем. Степень окисления марганца уменьшилась от +7 до +2, т.е. Mn +7 принимает 5 электронов и является окислителем.
- Составим электронные уравнения и найдем коэффициенты при окислителе и восстановителе.
S +4 – 2e — = S +6 ¦ 5 восстановитель, процесс окисления
Mn +7 +5e — = Mn +2 ¦ 2 окислитель, процесс восстановления
Чтобы число электронов, отданных восстановителем, было равно числу электронов, принятых восстановителем, необходимо:
- Число электронов, отданных восстановителем, поставить коэффициентом перед окислителем.
- Число электронов, принятых окислителем, поставить коэффициентом перед восстановителем.
Таким образом, 5 электронов, принимаемых окислителем Mn +7 , ставим коэффициентом перед восстановителем, а 2 электрона, отдаваемых восстановителем S +4 коэффициентом перед окислителем:
- Далее надо уравнять количества атомов элементов, не изменяющих степень окисления, в такой последовательности: число атомов металлов, кислотных остатков, количество молекул среды (кислоты или щелочи). В последнюю очередь подсчитывают количество молекул образовавшейся воды.
Итак, в нашем случае число атомов металлов в правой и левой частях совпадают.
По числу кислотных остатков в правой части уравнения найдем коэффициент для кислоты.
В результате реакции образуется 8 кислотных остатков SO4 2- , из которых 5 – за счет превращения 5SO3 2- → 5SO4 2- , а 3 – за счет молекул серной кислоты 8SO4 2- — 5SO4 2- = 3SO4 2- .
Таким образом, серной кислоты надо взять 3 молекулы:
- Аналогично, находим коэффициент для воды по числу ионов водорода, во взятом количестве кислоты
Окончательный вид уравнения следующий:
Признаком того, что коэффициенты расставлены правильно является равное количество атомов каждого из элементов в обеих частях уравнения.
Ионно-электронный метод (метод полуреакций)
Реакции окисления-восстановления, также как и реакции обмена, в растворах электролитов происходят с участием ионов. Именно поэтому ионно-молекулярные уравнения ОВР более наглядно отражают сущность реакций окисления-восстановления. При написании ионно-молекулярных уравнений, сильные электролиты записывают в виде ионов, а слабые электролиты, осадки и газы записывают в виде молекул (в недиссоциированном виде). В ионной схеме указывают частицы, подвергающиеся изменению их степеней окисления, а также характеризующие среду, частицы: H + — кислая среда, OH — — щелочная среда и H2O – нейтральная среда.
Рассмотрим пример составления уравнения реакции между сульфитом натрия и перманганатом калия в кислой среде.
- Сначала необходимо составить схему реакции: записать вещества в начале и конце реакции:
- Запишем уравнение в ионном виде, сократив те ионы, которые не принимают участие в процессе окисления-восстановления:
- Далее определим окислитель и восстановитель и составим полуреакции процессов восстановления и окисления.
В приведенной реакции окислитель — MnO4 — принимает 5 электронов восстанавливаясь в кислой среде до Mn 2+ . При этом освобождается кислород, входящий в состав MnO4 — , который, соединяясь с H + , образует воду:
MnO4 — + 8H + + 5e — = Mn 2+ + 4H2O
Восстановитель SO3 2- — окисляется до SO4 2- , отдав 2 электрона. Как видно образовавшийся ион SO4 2- содержит больше кислорода, чем исходный SO3 2- . Недостаток кислорода восполняется за счет молекул воды и в результате этого происходит выделение 2H + :
- Находим коэффициент для окислителя и восстановителя, учитывая, что окислитель присоединяет столько электронов, сколько отдает восстановитель в процессе окисления-восстановления:
MnO4 — + 8H + + 5e — = Mn 2+ + 4H2O ¦2 окислитель, процесс восстановления
SO3 2- + H2O — 2e — = SO4 2- + 2H + ¦5 восстановитель, процесс окисления
- Затем необходимо просуммировать обе полуреакции, предварительно умножая на найденные коэффициенты, получаем:
Сократив подобные члены, находим ионное уравнение:
- Запишем молекулярное уравнение, которое имеет следующий вид:
Далее рассмотрим пример составления уравнения реакции между сульфитом натрия и перманганатом калия в нейтральной среде.
В ионном виде уравнение принимает вид:
Также, как и предыдущем примере, окислителем является MnO4 — , а восстановителем SO3 2- .
В нейтральной и слабощелочной среде MnO4 — принимает 3 электрона и восстанавливается до MnО2. SO3 2- — окисляется до SO4 2- , отдав 2 электрона.
Полуреакции имеют следующий вид:
MnO4 — + 2H2O + 3e — = MnО2 + 4OH — ¦2 окислитель, процесс восстановления
SO3 2- + 2OH — — 2e — = SO4 2- + H2O ¦3 восстановитель, процесс окисления
Запишем ионное и молекулярное уравнения, учитывая коэффициенты при окислителе и восстановителе:
И еще один пример — составление уравнения реакции между сульфитом натрия и перманганатом калия в щелочной среде.
В ионном виде уравнение принимает вид:
В щелочной среде окислитель MnO4 — принимает 1 электрон и восстанавливается до MnО4 2- . Восстановитель SO3 2- — окисляется до SO4 2- , отдав 2 электрона.
Полуреакции имеют следующий вид:
MnO4 — + e — = MnО2 ¦2 окислитель, процесс восстановления
SO3 2- + 2OH — — 2e — = SO4 2- + H2O ¦1 восстановитель, процесс окисления
Запишем ионное и молекулярное уравнения, учитывая коэффициенты при окислителе и восстановителе:
Необходимо отметить, что не всегда при наличии окислителя и восстановителя, возможно самопроизвольное протекание ОВР. Поэтому для количественной характеристики силы окислителя и восстановителя и для определения направления реакции пользуются значениями окислительно-восстановительных потенциалов.
Подробно решение уравнений окислительно-восстановительных реакций (ОВР) методом электронного баланса разобраны на странице "Метод электронного баланса".
Ниже приведены примеры решения уравнений окислительно-восстановительных реакций соединений хлора:
Если в окислительно-восстановительной реакции принимают участие простые вещества, молекулы которых состоят из двух или более атомов элементов, то в электронном балансе кол-во отданных и полученных электронов определяют с учётом кол-ва атомов в молекуле: H2 0 -2e - → 2H +1 .
Уравнения окислительно-восстановительных реакций соединений хлора
1. Уравнение реакции соляной кислоты с кислородом (HCl+O2):
2. Уравнение реакции соляной кислоты с перманганатом калия (HCl+KMnO4):
Следует обратить внимание, что часть хлорид-ионов соляной кислоты окисляется до хлора, а другая часть переходит в состав молекул хлорида калия и хлорида магния без изменения своей степени окисления, поэтому, коэффициенты в первую очередь ставятся перед Cl2, KCl, MnCl2 и только потом, перед HCl.
3. Уравнение реакции соляной кислоты с хромом на воздухе (HCl+Cr):
4. Уравнение реакции соляной кислоты с манганатом калия (HCl+K2MnO4):
5. Уравнение реакции разбавленной соляной кислоты с кальцием (HCl+Ca):
6. Уравнение реакции разбавленной соляной кислоты с гидридом кальция с образованием хлорида кальция и водорода:
7. Уравнение реакции хлорида кальция с водородом с образованием гидрида кальция и соляной кислоты:
8. Уравнение реакции хлорида железа (II) с водородом с образованием железа и соляной кислоты:
9. Уравнение реакции хлорида железа с хлором в нейтральной среде с образованием метагидроксида железа и соляной кислоты:
10. Уравнение реакции окисления на воздухе хлорида железа (III):
11. Уравнение реакции хлорида железа (III) с водородом с образованием хлорида железа (II) и соляной кислоты:
12. Уравнение реакции хлорида меди с алюминием с образованием хлорида алюминия и меди:
13. Уравнение реакции хлорида аммония с нитратом калия с образованием оксида азота, хлорида калия и воды:
14. Уравнение реакции хлорида аммония с магнием с образованием хлорида магния, аммиака и водорода:
15. Уравнение реакции разложения гипохлорита натрия с образованием хлората и хлорида натрия:
16. Уравнение реакции разложения хлората калия с образованием хлорида калия и кислорода:
17. Уравнение реакции хлората калия с алюминием:
18. Уравнение реакции хлората калия с концентрированной соляной кислотой:
19. Уравнение реакции хлората калия с концентрированной серной кислотой:
20. Уравнение реакции хлората калия с серой:
21. Уравнение реакции хлората калия с красным фосфором:
22. Уравнение реакции хлората калия с гидридом кальция:
23. Уравнение реакции разложения хлорной кислоты:
24. Уравнение реакции разложения перхлората калия:
25. Уравнение реакции разложения хлорита натрия:
26. Уравнение реакции гипохлорита кальция с пероксидом водорода:
27. Уравнение реакции хлорноватистой кислоты с иодоводородом:
28. Уравнение реакции разложения оксида хлора (I):
29. Уравнение реакции разложения диоксида хлора при нагревании (сопровождается большим выделением тепла - взрывом):
30. Уравнение реакции диоксида хлора с гидроксидом калия:
31. Уравнение реакции диоксида хлора с озоном:
32. Уравнение реакции диоксида хлора с пероксидом водорода:
33. Уравнение реакции дихлоргексаоксида с гидроксидом калия:
34. Уравнение реакции разложения оксида хлора (VII):
Если вам понравился сайт, будем благодарны за его популяризацию :) Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Задание 236.
Реакции выражаются схемами:
HCl + CrO3 ⇔ Cl2 + CrCl3 + H2O;
Cd + KMnO 4 + H2SO 4 ⇔ CdSO 4 + MnSO 4 + K 2 SO 4 + H 2 O
Составьте электронные уравнения. Расставьте коэффициенты в уравнениях реакций. Для каждой реакции укажите, какое вещество является окислителем, какое - восстановителем; какое вещество окисляется, какое - восстанавливается.
Решение:
Если в условии задачи даны как исходные вещества, так и продукты их взаимодействия, то написание уравнения реакции сводится, как правило, к нахождению и расстановке коэффициентов. Коэффициенты определяют методом электронного баланса с помощью электронных уравнений. Вычисляем, как изменяют степень окисления восстановитель и окислитель, и отражаем это в электронных уравнениях. Коэффициенты для восстановителя и окислителя идентичны для продуктов окисления и восстановления. . Коэффициент перед веществами, атомы которых не меняют свою степень окисления, находят подбором.
а) HCl + CrO 3 ⇔ Cl2 + CrCl 3 + H 2 O
уравнения электронного баланса:
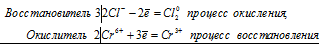
2Cr 6+ + 6Cl - = 2Cr 3+ + 3Cl2 0
Общее число электронов, отданных восстановителем, должно быть равно числу электронов, которые присоединяет окислитель. Общее наименьшее кратное для отданных и принятых электронов шесть. Разделив это число на 3, получаем коэффициент 2 для окислителя и продукта его восстановления, а при делении 6 на 2 получаем коэффициент 3 для восстановителя и продукта его окисления. Молекулярное уравнение реакции:
В данной реакции: HCl – восстановитель, CrO3 – окислитель; HCl окисляется до Сl2, CrO3 – восстанавливается до CrCl3.
Уравнения электронного баланса:
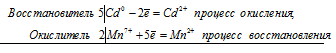
5Сd 0 + 2Mn 7+ = Cd 2+ + 2Mn 2+
Общее число электронов, отданных восстановителем, должно быть равно числу электронов, которые присоединяет окислитель. Общее наименьшее кратное для отданных и принятых электронов десять. Разделив это число на 5, получаем коэффициент 2 для окислителя и продукта его восстановления, а при делении 10 на 2 получаем коэффициент 5 для восстановителя и продукта его окисления. Молекулярное уравнение реакции:
В данной реакции: Cd – восстановитель, KMnO 4 – окислитель; Cd окисляется до CdSO 4, KMnO 4 – восстанавливается до MnSO 4.
Задание 237.
Реакции выражаются схемами:
Cr2O3 + KClO3 + KOH ⇔ K2CrO4 + KCl + H2O;
MnSO4 + PbO2 + HNO3 ⇔ HMnO4 + Pb(NO3)2 + PbSO4 + H2O
Составьте электронные уравнения. Расставьте коэффициенты в уравнениях реакций. Для каждой реакции укажите, какое вещество является окислителем, какое - восстановителем; какое вещество окисляется, какое - восстанавливается.
Решение:
Если в условии задачи даны как исходные вещества, так и продукты их взаимодействия, то написание уравнения реакции сводится, как правило, к нахождению и расстановке коэффициентов. Коэффициенты определяют методом электронного баланса с помощью электронных уравнений. Вычисляем, как изменяют степень окисления восстановитель и окислитель, и отражаем это в электронных уравнениях. Коэффициенты для восстановителя и окислителя идентичны для продуктов окисления и восстановления. . Коэффициент перед веществами, атомы которых не меняют свою степень окисления, находят подбором.
уравнения электронного баланса:
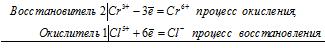
2Cr 3+ + Cl 5+ = 2Cr 6+ + Cl -
Общее число электронов, отданных восстановителем, должно быть равно числу электронов, которые присоединяет окислитель. Общее наименьшее кратное для отданных и принятых электронов шесть. Разделив это число на 6, получаем коэффициент 1 для окислителя и продукта его восстановления, а при делении 6 на 3 получаем коэффициент 2 для восстановителя и продукта его окисления. Молекулярное уравнение реакции:
В данной реакции: Cr2O3 – восстановитель, KClO3 – окислитель; Cr2O3 окисляется до K2CrO4, KClO3 – восстанавливается до KCl.
Уравнения электронного баланса:
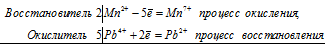
5Pb 4+ + 2Mn 2+ = 5Pb 2+ + 2Mn 7+
Общее число электронов, отданных восстановителем, должно быть равно числу электронов, которые присоединяет окислитель. Общее наименьшее кратное для отданных и принятых электронов десять. Разделив это число на 2, получаем коэффициент 5 для окислителя и продукта его восстановления, а при делении 10 на 5 получаем коэффициент 2 для восстановителя и продукта его окисления. Молекулярное уравнение реакции:
В данной реакции: PbO2 – восстановитель, MnSO4 – окислитель; PbO2 окисляется до Pb(NO3)2, MnSO4 – восстанавливается до HMnO4.
Задание 238.
Реакции выражаются схемами:
H 2 SO 3 + HClO 3 ⇔ H 2 SO 4 + HCl;
FeSO4 + K 2 Cr 2 O 7 + H 2 SO 4 ⇔ Fe 2 (SO 4 ) 3 + Cr 2 (SO 4 ) 3 + K 2 SO 4 + H 2 O
Составьте электронные уравнения. Расставьте коэффициенты в уравнениях реакций. Для каждой реакции укажите, какое вещество является окислителем, какое - восстановителем; какое вещество окисляется, какое - восстанавливается.
Решение:
Если в условии задачи даны как исходные вещества, так и продукты их взаимодействия, то написание уравнения реакции сводится, как правило, к нахождению и расстановке коэффициентов. Коэффициенты определяют методом электронного баланса с помощью электронных уравнений. Вычисляем, как изменяют степень окисления восстановитель и окислитель, и отражаем это в электронных уравнениях. Коэффициенты для восстановителя и окислителя идентичны для продуктов окисления и восстановления. . Коэффициент перед веществами, атомы которых не меняют свою степень окисления, находят подбором.
уравнения электронного баланса:
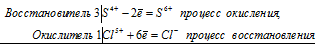
3S 4+ + Cl 5+ = 3S 6+ + Cl -
Общее число электронов, отданных восстановителем, должно быть равно числу электронов, которые присоединяет окислитель. Общее наименьшее кратное для отданных и принятых электронов шесть. Разделив это число на 6, получаем коэффициент 1 для окислителя и продукта его восстановления, а при делении 6 на 2 получаем коэффициент 3 для восстановителя и продукта его окисления. Молекулярное уравнение реакции:
В данной реакции: H2SO3 – восстановитель, HClO3 – окислитель; H2SO3 окисляется до H2SO4, HClO3 – восстанавливается до HCl.
Уравнения электронного баланса:
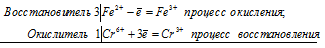
3Fe 2+ + Cr 6+ = 3Fe 3+ + Cr 3+
Общее число электронов, отданных восстановителем, должно быть равно числу электронов, которые присоединяет окислитель. Общее наименьшее кратное для отданных и принятых электронов три. Разделив это число на 3, получаем коэффициент 1 для окислителя и продукта его восстановления, а при делении 3 на 1 получаем коэффициент 3 для восстановителя и продукта его окисления. Учитывая, что в схеме реакции указаны вещества, содержащие железо и хром с двумя атомами в молекулах Fe 2 (SO 4 ) 3 и Cr 2 (SO 4 ) 3], умножим коэффициенты при окислителе и восстановителе на 2, получим молекулярное уравнение реакции:
Задание 239.
Реакции выражаются схемами:
I2 + Cl2 + H2O ⇔ HClO3 + HCl;
K2Cr2O7 + H3PO3 + H2SO4 ⇔ Cr2(SO4)3 + H3PO4 + K2SO4 + H2O
Составьте электронные уравнения. Расставьте коэффициенты в уравнениях реакций. Для каждой реакции укажите, какое вещество является окислителем, какое - восстановителем; какое вещество окисляется, какое - восстанавливается.
Решение:
Если в условии задачи даны как исходные вещества, так и продукты их взаимодействия, то написание уравнения реакции сводится, как правило, к нахождению и расстановке коэффициентов. Коэффициенты определяют методом электронного баланса с помощью электронных уравнений. Вычисляем, как изменяют степень окисления восстановитель и окислитель, и отражаем это в электронных уравнениях. Коэффициенты для восстановителя и окислителя идентичны для продуктов окисления и восстановления. . Коэффициент перед веществами, атомы которых не меняют свою степень окисления, находят подбором.
уравнения электронного баланса:
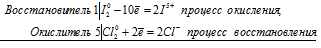
I 2 0 + 5Cl2 0 = 2I - + 10Cl -
Общее число электронов, отданных восстановителем, должно быть равно числу электронов, которые присоединяет окислитель. Общее наименьшее кратное для отданных и принятых электронов десять. Разделив это число на 2, получаем коэффициент 5 для окислителя и продукта его восстановления, а при делении 10 на 10 получаем коэффициент 1 для восстановителя и продукта его окисления. Молекулярное уравнение реакции:
В данной реакции: I2 – восстановитель, Cl2 – окислитель; I2 окисляется до HIO3, Cl2 – восстанавливается до HCl.
Уравнения электронного баланса:
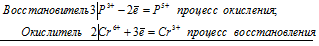
3P 3+ + 2Cr 6+ = 3P 5+ + 2Cr 3+
Общее число электронов, отданных восстановителем, должно быть равно числу электронов, которые присоединяет окислитель. Общее наименьшее кратное для отданных и принятых электронов шесть. Разделив это число на 3, получаем коэффициент 2 для окислителя и продукта его восстановления, а при делении 6 на 2 получаем коэффициент 3 для восстановителя и продукта его окисления. Молекулярное уравнение реакции:
В данной реакции: H 3 PO 3 – восстановитель, K 2 Cr 2 O 7 – окислитель; H 3 PO 3 окисляется до H 3 PO 4, K 2 Cr 2 O 7 – восстанавливается до Cr 2 (SO 4 ) 3.
Задание 240.
Могут ли происходить окислительно-восстановительные реакции между веществами: а) РН3 и НВг; б) K2Cr2O7 и Н3PO3; в) HNO3 и Н2S? Почему? На основании электронных уравнений расставьте коэффициенты в уравнении реакции, идущей по схеме:
АsH3 + НNO3 Н3AsO4 + NO2 + Н2O
Решение:
а) Степень окисления в РH3 n(Р) = -3 (низшая), в HBr n(Br) = -1 (низшая). Так как и фосфор, и бром находятся в своей низшей степени окисления, то оба вещества проявляют только восстановительные свойства и взаимодействовать друг с другом не могут;
б) в K2Cr2O7 n(Сr) = +6 (высшая); в Н3PO3 n(Р) = +5 (высшая). Так как и хром, и фосфор находятся в своей высшей степени окисления, то оба вещества проявляют только окислительные свойства и взаимодействовать друг с другом не могут;
в) в HNO3 n(N) = +5 (высшая); в H2S n(S) = -2 (низшая). Следовательно, взаимодействие этих веществ возможно, причём HNO3 является окислителем, а H2S – восстановителем.
Если в условии задачи даны как исходные вещества, так и продукты их взаимодействия, то написание уравнения реакции сводится, как правило, к нахождению и расстановке коэффициентов. Коэффициенты определяют методом электронного баланса с помощью электронных уравнений. Вычисляем, как изменяют степень окисления восстановитель и окислитель, и отражаем это в электронных уравнениях. Коэффициенты для восстановителя и окислителя идентичны для продуктов окисления и восстановления. . Коэффициент перед веществами, атомы которых не меняют свою степень окисления, находят подбором.
Уравнения электронного баланса:
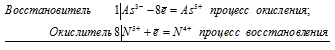
As 3- + 8N 5+ = As 5+ + 8N 4+
Общее число электронов, отданных восстановителем, должно быть равно числу электронов, которые присоединяет окислитель. Общее наименьшее кратное для отданных и принятых электронов восемь. Разделив это число на 1, получаем коэффициент 8 для окислителя и продукта его восстановления, а при делении 8 на 8 получаем коэффициент 1 для восстановителя и продукта его окисления. Молекулярное уравнение реакции:
.jpg)

Если мы замерли, или хотим приготовить еду, то зажигаем огонь. Реакция горения это тоже окислительно – восстановительная реакция.
А знаете, что можно согреться и без огня, с помощью химических грелок. Например такой: совершенно сухую смесь железной (Fe) или алюминиевой (Al) стружки с солями меди (например, CuCl2) можно хранить довольно долго, а при добавлении воды температура сразу же повышается почти до 100 о С за счет реакции:
Fe + CuCl2 = FeCl2 + Cu
При этом грелка, в которой хлорид меди CuCl2 превращается в хлорид железа FeCl2, сохраняет тепло около десяти часов.

I. Сущность окисления и восстановления
Если через раствор хлорида меди (II) пропускать электрический ток, то на катоде выделится медь, а на аноде образуется хлор.

Рис. 1. Электролиз раствора хлорида меди (II)
Изобразим схемы протекающих на электродах процессов:
НА КАТОДЕ: Cu 2+ → Cu 0
НА АНОДЕ: 2Cl - → Сl2 0
Чтобы катион меди Cu 2+ превратился в электонейтральный атом меди, он должен принять от катода 2 электрона. Чтобы из двух анионов хлора Cl - образовалась молекула хлора, они должны отдать 2 электрона:
НА КАТОДЕ: Cu 2+ + 2е → Cu 0 (восстановление меди)
НА АНОДЕ: 2Cl - - 2е → Сl2 0 (окисление хлора)
Таким образом, можно сделать вывод:
Вещество, отдающее электроны, называется восстановителем . Вещество, принимающее электроны, называется окислителем.

Рис. 2. Переход электронов от восстановителя к окислителю
Окислитель, принимая электроны, сам при этом восстанавливается. Восстановитель, отдавая электроны, сам окисляется.
Процессы окисления и восстановления не могут протекать раздельно друг от друга, поэтому говорят об окислительно-восстановительной реакции.

Восстановителем может быть атом элемента, а восстановление - это процесс принятия электронов.

Есть ряд мнемонических правил, которые позволяют лучше запомнить разницу между этими понятиями:
-
По первым буквам слов можно составить следующие сокращения:
ОВВ: окислитель - взял e¯ - восстановился
ВОО: восстановитель - отдал - окислился

2. Или использовать словосочетание "окислитель-грабитель".
Восстановитель — это тот, кто электроны отдает.
Сам отдает грабителю, злодею-окислителю.
Отдает — окисляется, сам восстановителем является.
II. Электронный баланс
В окислительно-восстановительной реакции число принятых электронов должно быть равно числу отданных электронов. В рассматриваемом процессе электронный баланс можно изобразить следующей схемой:
Cu 2+ + 2Cl - = Cu 0 + Cl2 0
Если рассмотреть сущность еще одного окислительно-восстановительного процесса (между железом и сульфатом меди (II)), то мы увидим, что катионы меди в этой реакции выполняют роль окислителя. В результате происходит восстановление меди:
Роль восстановителя играет простое вещество железо:
При этом железо окисляется до двухзарядного катиона.
В этом методе сравнивают степени окисления атомов в исходных веществах и в продуктах реакции, при этом руководствуемся правилом: число электронов, отданных восстановителем, должно равняться числу электронов, присоединённых окислителем.
Для составления уравнения надо знать формулы реагирующих веществ и продуктов реакции.
Вы уже знаете, что окислительно-восстановительные реакции могут протекать под действием электрического тока. Такие реакции называют электролизом . Этот процесс был подробно изучен Майклом Фарадеем. Сегодня электролиз широко применяется в промышленности. С помощью него делают копии различных деталей, наносят на стальные детали автомобилей защитный слой другого металла.
Рассмотрим реакцию магния с кислородом. Запишем уравнение этой реакции и расставим значения степеней окисления атомов элементов:

Как видно, атомы магния и кислорода в составе исходных веществ и продуктов реакции имеют различные значения степеней окисления. Запишем схемы процессов окисления и восстановления, происходящих с атомами магния и кислорода.
До реакции атомы магния имели степень окисления, равную нулю, после реакции - +2. Таким образом, атом магния потерял 2 электрона:

Магний отдает электроны и сам при этом окисляется, значит, он является восстановителем.
До реакции степень окисления кислорода была равна нулю, а после реакции стала -2. Таким образом, атом кислорода присоединил к себе 2 электрона:

Кислород принимает электроны и сам при этом восстанавливается, значит, он является окислителем.
Запишем общую схему окисления и восстановления:

Число отданных электронов равно числу принятых. Электронный баланс соблюдается.
В окислительно-восстановительных реакциях происходят процессы окисления и восстановления, а значит, меняются степени окисления химических элементов. Это отличительный признак окислительно-восстановительных реакций.
Окислительно-восстановительными называют реакции, в которых химические элементы изменяют свою степень окисления.
Рассмотрим на конкретных примерах, как отличить окислительно-восстановительную реакцию от прочих реакций.
1. NaOH + HCl = NaCl + H2O
Для того чтобы сказать, является ли реакция окислительно-восстановительной, необходимо расставить значения степеней окисления атомов химических элементов.
1. Na +1 O -2 H +1 + H +1 Cl -1 = Na +1 Cl -1 + H2 +1 O -2
Обратите внимание, степени окисления всех химических элементов слева и справа от знака равенства остались неизменными. Значит, эта реакция не является окислительно-восстановительной.
В результате данной реакции степени окисления углерода и кислорода поменялись. Причем углерод повысил свою степень окисления, а кислород понизил. Запишем схемы окисления и восстановления:
С -4 -8е =С +4 - процесс окисления
О2 0 +4е = 2О -2 - процесс восстановления
Чтобы число отданных электронов было равно числу принятых, т.е. соблюдался электронный баланс, необходимо домножить вторую полуреакцию на коэффициент 2:
С -4 -8е =С +4 - восстановитель, окисляется
2О2 0 +8е = 4О -2 - окислитель, восстанавливается
Окислитель в ходе реакции принимает электроны, понижая свою степень окисления, он восстанавливается.
Восстановитель в ходе реакции отдает электроны, повышая свою степень окисления, он окисляется.
V. Алгоритм составления ОВР
Расставить коэффициенты в реакции, схема которой:
Алгоритм расстановки коэффициентов
1. Указываем степени окисления химических элементов.
Подчёркнуты химические элементы, в которых изменились степени окисления.
2. Составляем электронные уравнения, в которых указываем число отданных и принятых электронов.
За вертикальной чертой ставим число электронов, перешедших при окислительном и восстановительном процессах. Находим наименьшее общее кратное (взято в красный кружок). Делим это число на число перемещённых электронов и получаем коэффициенты (взяты в синий кружок). Значит, перед марганцем будет стоять коэффициент-1, который мы не пишем, и перед Cl2 тоже -1.
Перед HCl коэффициент 2 не ставим, а считаем число атомов хлора в продуктах реакции. Оно равно - 4.Следовательно, и перед HCl ставим - 4,уравниваем число атомов водорода и кислорода справа, поставив перед H2O коэффициент - 2. В результате получится химическое уравнение:
Рассмотрим более сложное уравнение:
Расставляем степени окисления химических элементов:
Электронные уравнения примут следующий вид
Перед серой со степенями окисления -2 и 0 ставим коэффициент 5, перед соединениями марганца -2, уравниваем число атомов других химических элементов и получаем окончательное уравнение реакции
Читайте также:

