Как проходит химиотерапия при опухоли головного мозга
Многие годы считалось наиболее целесообразной стандартная химиотерапия рака мозга на основе концепции лечения ACNU+VM26, при которой в случае рецидива следовали протоколу на основе Темозоломида (Темодала). Что это за протокол? Согласно этому протоколу Темозоломид применяется отдельно в качестве моновещества (но моно использование его применяется в крайних случаях), чаще всего его вводят вместе с другими активными ингредиентами, например, с доксорубицином. Если этот терапевтический подход срабатывает и результаты удовлетворяют онкологов, считается, что врачиприменяют стандартную химиотерапию и не прибегают к экспериментальному подходу. Стандартная схема используется при лечении злокачественных и доброкачественных опухолей головного и спинного мозга, очень часто совместно с радиотерапией.
Если из-за степени воздействия или из-за того, что организм более не переносит токсичность процедуры (скажем, из-за побочных действий), химиотерапия перестает быть эффективной, тогда онкологи прибегают к новым, экспериментальным, менее инвазивнымметодам лечения или к методам, имеющим меньше побочных эффектов, например, метод с применением мелатонина. За основу берется американское исследование, которое показало лучший результат лечения пациентов с применением мелатонина. Поскольку мелатонин в диапазоне от 10 до 20 мг почти или вообще не имеет побочных эффектов, в Германии считается целесообразным его использование.
Эффективность основной терапии с применением ACNU+VM26 либо с тамоксифеном, либо без него, в случае пациентов, которые до сих пор еще не проходили лечения химиотерапией в Германии, оценивается, по мнению разных немецких авторов, от 25 до 40%.
То есть в случае четырех из десяти пациентов с глиобластомой можно рассчитывать на то, что химиотерапия даст благоприятный эффект. Благоприятный эффект означает, что опухоль не продолжает расти, а регрессирует. Уровень частичных ремиссий оценивается примерно в 12%, уровень полной ремиссии, а значит, в перспективе более не обнаруживаемой опухоли, примерно в 4-5% (по данным врача-онколога, немецкого доктора ГрегораДреземанна).
Преимущества амбулаторных условий при химиотерапии головного мозга очевидны: данная терапия, как правило, субъективно хорошо переносится и имеет немного побочных эффектов. При проведении ACNU+VM26 надо учитывать, что в течение двух-четырех недель после химиотерапии могут наблюдаться самые сильные побочные эффекты в связи с параметрами крови. В этот период времени необходимо, чтобы лечащий в амбулаторных условиях врач тщательно делал анализ крови и был на связи с онкологами клиники.
Однако ситуация та же и при проведении химиотерапии в стационарных условиях, потому что стационарное лечение не перекрывает действительно опасный период времени. Через две-четыре недели после прохождения химиотерапии такие пациенты уже тоже выписываются из больницы. Вывод: химиотерапия рака мозга в амбулаторных условиях эффективно действует только в случае надежного медицинского ухода на месте.
Осложнения при стандартной химиотерапии ACNU+VM26
В прошлом, когда не было тесной связи с лечащим врачом и онкологом стационара, во время лечения амбулаторно возникали чрезвычайные проблемы и серьезные осложнения. Если врач стационара знает все нюансы проведения амбулаторной химиотерапии, реакцию пациента на нее, последние анализы в динамике, ситуация резко меняется. Как правило, именно родственники или сами пациенты заботятся о том, чтобы все анализы и данные были собраны и переданы непосредственно в онкоклинику. Онколог анализирует последние обследования и анализы, дает свои консультации и рекомендации, которые нужно учитывать пациентам и их близким друзьям.
Показания к химиотерапии при опухоли головного мозга
- Химиотерапия опухолей головного мозга целесообразна при лечении анапластической олигодендроглиомы и астроцитомы III степени по классификации Всемирной организации здравоохранения. Значимость химиотерапии в этих случаях неоспорима и в данный момент, в соответствии с исследованиями NOA-04, сравнима с предыдущим стандартным лечением, лучевой терапией.
- Кроме того, сегодня химиотерапия является стандартным методом лечения первичных мозговых лимфом. В случае лечения опухолей более низкой II степени, химиотерапию, как правило, назначают уже тогда, когда все другие альтернативы ― операция или лучевая терапия ― больше не дают желаемых результатов.
- Уже не один год оспаривается эффективность химиотерапии в рамках первичного лечения при глиобластоме. Результаты большинства анализов показывают, что есть определенная польза в назначении дополнительной химиотерапии. Документально лучше подтверждена действенность химиотерапии при рецидиве глиобластомы. В этом случае можно рассчитывать на 30%-ю эффективность терапии.
Обширное тестирование на химиочувствительность проводилась в Германии еще в 1980 году. Цель этих тестов заключалась в том, чтобы культивировать опухолевые клетки пациентов и тестировать в клеточной культуре их реакцию на то или иное цитостатическое средство. Таким образом, стремились разрабатывать курсы химиотерапии для конкретных пациентов. Уже тогда данные попытки оказались неудачными в случае опухолей головного мозга, а также большинства других опухолей. Так что в настоящий момент при взвешивании методов лечения, онкологи, как правило, не используют анализы на химиочувствительность.
Причина проблемы в таких тестах состоит, вероятно, в том, что ко времени, когда отдельные опухолевые клетки переносят в клеточную культуру, специфические клоны опухоли очень быстро превосходят в развитии другие клетки. В конечном счете, это приводит к тому, что произрастающая в клеточной культуре опухоль через несколько недель больше не соответствует характеристикам гетерогенных клеточных популяций опухоли у пациента.
В связи с тем, что не все больные с опухолью головного мозга хорошо переносят химиотерапию на основе Темозоламида, с одной стороны, с другой – исследования показали, что половина клеток глиобластомычерез некоторое время начинают блокировать данный препарат, врачи все чаще прибегают к химиотерапии новыми препаратами и другими способами введения лекарственных средств.
Что выбрать сначала – лучевую терапию или химиотерапию при раке мозга? Это в большой степени зависит от опухоли. Вне контролируемого исследования, например, в лечении глиобластомы, не представляется возможным первоначально опробовать химиотерапию, потому что ситуация с имеющимися данными по лучевой терапии значительно лучше, чем по химиотерапии. В клинических исследованиях при лечении глиобластомы можно проверить, лучше ли было бы назначить химиотерапию перед облучением или нет. Как правило, исходят из того, что пациентам легче переносить химиотерапию перед лучевой терапией, чем наоборот. Этот научный вывод связан, главным образом, с опытом лечения первичных мозговых лимфом и лечения опухолей в детском возрасте. Назначение химиотерапии перед лучевой терапией представляет собой стандарт лечения мозговыхлимфом. Этот важный вопрос необходимо также рассматривать в свете последующей нейротоксичности при долгосрочной выживаемости.Сейчас проходит исследование, цель которого посредством изменения порядка трех хорошо известных терапевтических методов, а именно лучевой терапии, PCV и метода с применением Темозоломида, выяснить, какие последовательности наиболее совместимы и наиболее эффективны.
(495) 506 61 01
Химиотерапия является одним из трех основных методов лечения злокачественных опухолей. Принцип химиотерапии заключается в том, что пациенту назначаются особые цитотоксические препараты, которые губительно действуют на быстроразмножающиеся клетки, к которым и относятся опухолевые клетки. К химиопрепаратам относится много групп химических веществ, каждая из которых обладает своим механизмом действия, конечной целью которого является разрушение клеток опухоли.
Такая особенность опухолевых клеток, как усиленный метаболизм и размножение ввиду генетических мутаций в них, играет важную роль в применении цитостатиков. Это делает их чувствительными к химиопрепаратам. Однако, кроме опухолевых клеток в организме имеются и другие здоровые клетки, которые также характеризуются повышенным метаболизмом и усиленным размножением. Это клетки эпителия, а также клетки костного мозга, которые отвечают за кроветворение и иммунную систему. Химиопрепараты влияют, таким образом, не только на опухоль, но и на здоровые ткани, что приводит к известным побочным реакциям.
Обычно, химиотерапия при опухолях мозга проводится курсами, которые чередуются перерывами. Эти перерывы нужны для организма как передышка, чтобы он мог восстановиться. Следует отметить, что химиопрепараты применяются каждый для определенных типов опухолей и поэтому химиотерапия назначается обычно после оперативного вмешательства, которое позволяет определить гистологический тип опухоли мозга. Если же химиотерапия проводится без предварительной операции на мозге, то для определения гистологического типа опухоли делается т.н. стереотаксическая биопсия мозга. При этом химиотерапия может проводиться различными способами, который выбирает лечащий врач.

При системном введении химиопрепарата пациент получает лекарство внутривенно или перорально в виде таблеток. Такой способ характеризуется наибольшим риском побочных эффектов. При регионарном введении химиопрепаратов лекарственное средство вводится непосредственно в артерии, которые кровоснабжают область расположения опухоли.
При интратекальном способе химиопрепарат вводится путем люмбальной пункции в цереброспинальный ликвор. Таким образом, цитостатик действует непосредственно на ткань мозга. Этот способ используется при данном расположении опухолей. В случае, когда химиопрепарат вводится непосредственно в ткань опухоли, говорят об интерстициальном методе химиотерапии.
В химиотерапии опухолей мозга также применяется т.н. конвекционный методе доставки препарата в опухоль. При этом в саму ткань опухоли или окружающие мягкие ткани имплантируется тонкий пластиковый катетер, через который постоянно медленно вводятся необходимые химиопрепараты, обычно в течение нескольких дней.
Обычно при химиотерапии используется схема, в которой применяется несколько цитостатических препаратов в определенной дозе в течение определенного времени.
Среди химиопрепаратов, которые применяются в лечении опухолей мозга, широкое применение на сегодня нашли такие средства, как Темозоломид и Кармустин, а также препараты на основе платины цисплатин (Платинол) и карбоплатин (Параплатин). Кроме указанных средств, исследователи сегодня изучают возможность применения и других цитостатиков для лечения опухолей мозга.
Среди побочных эффектов химиотерапии опухолей мозга можно отметить все те эффекты, которые встречаются при химиотерапии других видов злокачественных опухолей.
Как уже было сказано, химиопрепараты губительно действуют на клетки с усиленным метаболизмом и быстрым ростом. К таким клеткам относятся не только опухолевые клетки, но и клетки здоровых тканей: клетки эпителия ЖКТ и волосяных луковиц, а также клетки костного мозга, который относится к кроветворной системе. Дело в том, что эпителий в организме у нас постоянно обновляется, а клетки костного мозга так же постоянно обновляют состав форменных элементов крови. С этим-то и связаны все побочные эффекты химиотерапии.
В костном мозге происходит созревание форменных элементов крови: эритроцитов, лейкоцитов и тромбоцитов. Эти клетки характеризуются интенсивным развитием, в результате чего их созревание во время химиотерапии страдает. Возникает анемия, лейкоцитопения и тромбоцитопения. Это проявляется слабостью, быстрой утомляемостью, плохим аппетитом, шумом в ушах. Кожа становится бледной.
Лейкоцитопения ведет к снижению защитных сил организма и иммунитета. Могут легко присоединяться всякие инфекции. Профилактика инфекционных осложнений химиотерапии заключается в соблюдении пациентом личной гигиены и контакта с инфекционными больными. При развитии инфекции у таких больных в обязательном порядке используются антибиотики. В случае возникновения апластической анемии применяются т.н. эритропоэтины, которые стимулируют созревание эритроцитов в костном мозге. Для стимуляции роста белых клеток крови используются т.н. колониестимулирующие факторы, среди которых известен такой препарат, как филграстим.
При снижении уровня тромбоцитов отмечается повышенная кровоточивость. На коже возникают т.н. петехии в виде мелкоточечной сыпи. При выраженной тромбоцитопении проводятся трансфузии тромбоцитарной массы.
Кроме влияния на указанные ткани и клетки, цитостатики влияют на эпителий органов ЖКТ, что проявляется тошнотой, рвотой, чувством дискомфорта в животе, вздутием и диареей.
Химиопрепараты негативно влияют и на репродуктивную систему как женщин, так и мужчин, приводя к вторичному бесплодию. У женщин химиотерапия может привести к появлению симптомов менопаузы в виде приливов жара, сухости во влагалище и нарушений менструального цикла.
Химиотерапия оказывает неблагоприятное воздействие и на функцию почек, а также печени. Для снижения негативных эффектов на эти органы при химиотерапии рекомендуется пить больше жидкости, чтобы быстрее вывести токсические вещества из организма.
(495) 506-61-01 - где лучше оперировать головной мозг
Кибер-нож - современная инновационная технология применения лучевой терапии, позволяющая воздействовать на опухоль мозга и служит альтернативной оперативным методам лечения. Кибер-нож относится к методам так называемой радиохирургии, как и гамма-нож. Подробнее

На базе нейрохирургической клиники Аахенского Университета с 1998 года применяется специальная методика гамма-кобальтового облучения для лечения опухолей и сосудистых новообразований головного мозга. Подробнее
Национальный Онкоцентр Им. Сураски является интегральной частью крупнейшей муниципальной мед. клиники Сураски и предоставляет передовое лечение опухолей мозга всех видов.Подробнее
- Почему возникает химио мозга?
- Какие химиопрепараты вызывают самые тяжелые побочные эффекты со стороны головного мозга?
- Основные симптомы
- Как бороться с химио мозга?
- Что можете сделать вы?
- Сможет ли нервная система восстановиться полностью?
- Химио мозга: результаты недавних исследований
Химио мозга — не менее неприятный и мучительный побочный эффект, чем выпадение волос, проблемы с приемом пищи, анемия или снижение иммунитета. Эффективных средств его профилактики не существует. Лечить данное состояние сложно, у некоторых пациентов проблемы с памятью, вниманием и мышлением сохраняются в течение многих лет.

Почему возникает химио мозга?
Позже оказалось, что все намного сложнее.
Химио мозга развивается под действием многих факторов. Это могут быть побочные эффекты противоопухолевых средств, препаратов от тошноты и обезболивающих, анемия, последствия хирургического вмешательства и применения наркоза, хронический стресс, нарушение сна, подавленность, страх, депрессия, плохое питание, боли. Раковые клетки выделяют вещества, некоторые из которых способны влиять на работу нервной системы.
Считается, что далеко не последнюю роль в развитии химио мозга играет наследственность и индивидуальные особенности организма. Видимо, в группе повышенного риска находятся люди, у которых хуже происходит репарация ДНК, медленнее восстанавливаются нервные клетки, слабее работают нейротрансмиттеры — вещества, которые передают сигналы между нейронами.
Были проведены исследования, посвященные химио мозга, они помогли установить некоторые факты:
- Нарушения не всегда возникают после курса химиотерапии. Известны случаи, когда серьезные симптомы появлялись у больных, которые вообще не получали химиопрепаратов. Иногда ухудшения начинаются после операции или применения гормонов.
- Исследование, проведенное на лабораторных животных, показало, что после применения химиопрепаратов в головном мозге замедляется высвобождение медиаторов дофамина и серотонина.
- Однажды ученые измерили объем головного мозга у женщин, которые 21 год назад проходили курсы химиотерапии по поводу рака молочной железы, и сравнили результаты с показателями здоровых женщин. Оказалось, что после применения химиопрепаратов в мозге уменьшается количество серого вещества, в котором находятся нейроны.
- В другом исследовании ученые обнаружили, что белое вещество головного мозга у женщин, прошедших курсы химиотерапии 9 лет назад, тоже пострадало. У них отмечалась дегенерация (разрушение) аксонов (длинных отростков нервных клеток) и демиелинизация — разрушение оболочки нервных волокон, необходимой для нормального проведения импульсов.
Риски химио мозга повышены у людей старшего возраста, при сопутствующих заболеваниях (сахарный диабет, атеросклероз и др.), применении больших доз химиопрепаратов и лучевой терапии, облучении области головы, локализации основной опухоли или метастазов в головном мозге.
Какие химиопрепараты вызывают самые тяжелые побочные эффекты со стороны головного мозга?
Ученые впервые задались этим вопросом в 2015 году. Было проведено исследование с участием женщин, которые ранее получали лечение разными химиопрепаратами по поводу рака молочной железы.
Участницы, которые лечились химиопрепаратами из группы антрациклинов, хуже справлялись с тестами, и у них в мозге были выявлены более значительные изменения по данным функциональной МРТ.
Основные симптомы
Сами пациенты зачастую описывают свои симптомы так:
Многие онкологические пациенты с умеренными нарушениями памяти, внимания и мышления испытывают депрессию, повышенную тревожность, быстро устают. Сложно сказать, что является первопричиной, а что — следствием.
Как бороться с химио мозга?
Не существует препаратов, которые могли бы повлиять на причину химио мозга и устранить это состояние, потому что сама причина до конца не известна. Однако, врач может помочь. Существуют препараты для симптоматической терапии. Нужно проводить противоопухолевое лечение, бороться с состояниями, которые могут ухудшить работу мозга: анемией, мучительными болями, нарушением сна, ранней менопаузой на фоне гормональной терапии.

В Европейской клинике с пациентами работает психоонколог, он помогает привыкнуть к новому состоянию, вернуться к максимально полноценной жизни.
Что можете сделать вы?
Большое значение в борьбе с побочными эффектами химиотерапии в отношении головного мозга имеет образ жизни. Основные рекомендации:
Сможет ли нервная система восстановиться полностью?
Это индивидуально. Зачастую симптомы химио мозга сохраняются около года, а затем сильно уменьшаются или исчезают. У некоторых больных они довольно сильны в течение многих лет. Из-за проблем с памятью, вниманием и мышлением может потребоваться смена места работы. Некоторые больные получают группу инвалидности.
Обычно симптомы химио мозга становятся более заметными в следующих ситуациях:
- после выхода на работу;
- когда человек одновременно пытается выполнять несколько дел;
- при утомлении.
Химио мозга: результаты недавних исследований
Хотя полная картина механизмов развития химио мозга пока неясна, проведены многие исследования, которые попытались объяснить, что происходит под действием химиопрепаратов в нервной системе на клеточном и молекулярном уровне. Так, согласно одной из теорий, химиопрепараты усиливают выработку цитокинов — сигнальных молекул, которые активируют работу иммунной системы и усиливают воспаление в нервной ткани. Согласно другому предположению, виновниками являются свободные радикалы и окислительный стресс.
В 2018 году ученые из Стэнфордского университета в Калифорнии в экспериментах на мышах показали, что в результате применения химиопрепарата метотрексата в головном мозге повышается активность микроглии — клеток, которые обеспечивают защиту от чужеродных агентов. В итоге нарушается созревание олигодендроцитов (клеток, которые формируют миелиновую оболочку, необходимую для нормального проведения нервных импульсов) и функция астроцитов (клеток, которые обеспечивают питание нейронов и передачу нервных импульсов). Уже существует препарат, который может это исправить, и он проходит испытания на животных.
Современные ученые пока еще пытаются ответить на ряд вопросов:
- Какие препараты сильнее всего нарушают работу головного мозга?
- Можно ли как-то предотвратить это осложнение?
- Как разновидность и доза химиопрепарата, генетические особенности пациента влияют на вероятность развития и степень выраженности химио мозга?
- Какие лекарства помогут бороться с этим состоянием?
а) Общие рекомендации по химиотерапии опухоли головного мозга:
• Перед началом лечения должны быть проверены гематологические показатели, а также функция печени и печек.
• При наличии инфекции химиотерапия не проводится.
• Для женщин: исключить беременность; для мужчин и женщин: консультации в отношении контрацепции.
• Пациент должен лечиться у специалиста с опытом работы в химиотерапии.
• При расчете токсичности обращаться к общим критериям побочных эффектов, в таблице ниже приведены данные о гематологической токсичности.
• Доза определяется с учетом площади поверхности тела (ППТ). У пациентов с расчетной поверхностью тела >2,1 ППТ следует воспринимать как 2,1.
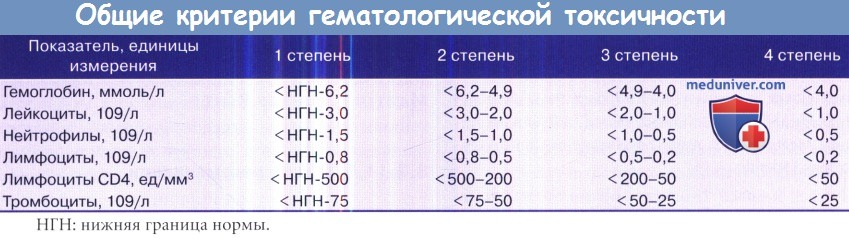
б) Темозоламид:
1. Протокол лучевого лечения с адъювантной и сопутствующей терапией темозоламидом глиом высокой степени злокачественности (протокол EORTC 26981). Лечение состоит из двух этапов: сопутствующей лучевой и химиотерапии темозоломидом, затем шесть циклов классического режима химиотерапии темозоломидом по 1-5 раз в день в течение четырех недель.
I. Темозоламид в сопутствующей фазе. Лучевая терапия (ЛТ) 60 Гр (30x2 Гр) в сочетании с темозоломидом (ежедневно в дозе 75 мг/м 2 ). Предполагаемая продолжительность: шесть недель; сопутствующий прием темозоломида не должен превышать семи недель.
• Прием темозоломида за один час до начала сеанса ЛТ в будние дни. В выходные дни и другие дни без ЛТ прием темозоломида продолжается и проводится в первой половине дня.
• Рекомендуется за час до первой и второй дозы темозоломида прием противорвотного средства (например, 8 мг ондансетрона, 1 мг гранисетрона). При сопутствующей химиолучевой терапии с низкими дозами ТМЗ противорвотная профилактика необходима лишь изредка.
• Профилактика пневмоцистной пневмонии (ПЦП) (960 мг котримоксазола три раза в неделю) показана пациентам, принимающим стероиды в течение сопутствующего этапа, или при CD4 3 . Профилактика должна продолжаться до полного нивелирования лимфоцитопении (ОКПЭ класса 2 /день на 1-5 дни, с однократным повышением дозы до 200 мг/м 2 /день с первого по пятый дни в последующих циклах в случае отсутствия существенной токсичности в первом цикле (все ОКПЭ без гематологической токсичности 100 х 10 9 /л и нейтрофилов > 1,5 х 10 9 /л).
— Для лечения рецидивирующих заболеваний:
После предшествовавшей химиотерапии в начале следующего цикла стартовая доза для первого цикла составляет 150 мг/м 2 в день на 1-5 дней, с одним повышением дозы до 200 мг/м 2 /день в последующих циклах в случае отсутствия существенной токсичности. Не получавшим химиотерапии пациенты дают начальную дозу 200 мг/м 2 /день и темозоламид с первого по пятый дни.
— Используют три уровня дозировок: 200 мг/м 2 , 150 мг/м 2 и 100 мг/м 2 ежедневно с первого по пятый день.
• Продолжительность лечения:
— При впервые диагностированной глиоме после сопутствующей химиолучевой терапии не более шести циклов адъювантной терапии.
— При рецидиве заболевания до прогрессирования заболевания или 12 циклов.
• С первого по пятый день стандартного лечения темозоломидом рекомендуется прием противорвотных средств, так как тошнота и рвота могут быть очень серьезными, особенно в первый и второй дни. Так как 5-НТ 3-антагонисты могут вызвать запор, рекомендуется давать ондансетрон (8 мг) или гранисетрон (1 мг) один или два раза в день 1-3 дня, только при необходимости и с приемом за один час до темозоломида.
• Перед каждым циклом лечения темозоломидом должен быть получен общий анализ крови (ОАК) (за 72 ч). Контроль проводится на 21 день первого цикла или после увеличения дозы.
• Снижение дозы на один уровень (обычно примерно на 21-й день) в случае гематологической токсичности 3 или 4 класса или в начале следующего цикла при задержке более трех недель из-за токсичности.
• Лечение прекращают в случае 3-й степени кардиотоксичности, 4-й степени гематологической токсичности или 3-й степени негематологической токсичности в дозе 100 мг/м 2 в день (500 мг/м 2 за цикл), или негематологической токсичности 4-го класса (за исключением тошноты и рвоты).
• Следующий цикл может начаться, если уровень нейтрофилов > 1,5 х 10 9 /л и/или тромбоцитов >100х 10 9 /л в 29 день = 1-й день следующего цикла, и при отсутствии негематологической токсичности (за исключением алопеции):
— В противном случае — задержка следующего цикла до возникновения указанного состояния.
— Если вопрос не решен в течение трех недель, следует прекратить лечение.
IV. Альтернативные режимы дозирования темозоламида:
• Используются и некоторые другие схемы темозоломида с более плотной дозировкой в течение нескольких дней каждые четыре недели. Наиболее часто используются:
— Неделя через неделю: чередуется одна неделя ежедневного приема и одна неделя отдыха.
• Уровни дозировки: 100 мг/м 2 ежедневно, 125 мг/м 2 ежедневно, 150 мг/м 2 ежедневно.
— Три недели через неделю: три недели ежедневного приема, затем одна неделя отдыха.
• Используется дозировка: 75 мг/м 2 ежедневно, 100 мг/м 2 ежедневно.
• Тошнота и рвота часто менее выражены, чем при стандартном режиме дозирования.
• Усталость, недомогание и т. д., могут быть более выраженными, усиливаясь после новых циклов.
• Лимфопения является побочным эффектом всех таких режимов. Рекомендуется мониторинг CD4+, с профилактикой ПЦП если CD4+ ниже 200/мм 3 (и продолжение до восстановления уровня > 200/мм 3 ).
• Начать с низкой дозы, если перед этим проводилась химиотерапия.
• Уменьшить дозировку и начать новый цикл в соответствии с приведенными рекомендациями в течение 1-5 дней 4 раза в неделю.
• Рассмотреть возможность перехода на стандартное лечение в случае изнурительных общих симптомов.
• Рекомендуемая продолжительность лечения при рецидивирующих опухолях: до одного года.

в) PCV химиотерапия опухоли головного мозга:
• Каждый курс стандартной химиотерапии PCV состоит из:
— CCNU (ломустин), 110 мг/м 2 перорально в первый день с противорвотными средствами (метоклопрамид или домперидон, в случае необходимости ондансетрон или аналогичные средства).
— Прокарбазин (натулан), 60 мг/м 2 внутрь в течение 14 дней каждого цикла на 8-21 дни.
— Винкристин, 1,4 мг/м 2 на 8 и 29 день каждого цикла (максимум 2 мг).
• Полный курс терапии повторяется каждые шесть недель (42 дня), максимум шесть циклов.
• Эффективность винкристина была поставлена под сомнение, и многими врачами этот препарат не включается в схему.
• Токсичность проявляется в основном кумулятивной миелосупрессией, тошнотой, алопецией, повышенной утомляемостью, потерей аппетита, нарушением функции печени и полинейропатией (винкристин).
— Прокарбазин может вызвать аллергическую реакцию кожи.
— Прием тирамин-содержащих продуктов, таких как красное вино, сыр, бананы во время лечения прокарбазином, может вызвать гипертонический криз (эффект моноаминоксидазы). Пациенты должны быть предупреждены о дисульфирам-эффекте после приема алкоголя (головная боль, слабость и потливость).
• Тошнота и рвота, вызванные схемой PCV, как правило, контролируются обычными противорвотными средствами, такими как домперидон или метоклопрамид.
• Контроль показателей:
— Гематологические параметры на 1, 8 и 43 сутки (= 1-й день следующего цикла).
— Биохимический анализ перед началом каждого цикла.
• Модификации дозировки:
— Если схема используется после предыдущей химиотерапии темозоломидом в сочетании с облучением: уменьшить дозу CCNU и прокарбазина на 25%.
— При снижении лейкоцитов 9 /л или тромбоцитов 9 /л в первый день:
• CCNU задерживается на одну неделю.
В случае последующей лейкопении 9 или тромбоцитопении 9 лечение откладывается еще на неделю. Если лейкопения или тромбопения сохраняются после этого, необходимо прекратить химиотерапию.
• В случае задержки цикла на две недели из-за токсичности снизить дозировку CCNU и прокарбазина на 25%.
— Уменьшить дозу CCNU и прокарбазина на 25% в случае 3/4 класса лейко- или гранулоцитопении, или в случае 3/4 класса тромбоцитопении.
— В случае уровня лейкоцитов 9 /л или тромбоцитов 9 /л на 8-й день:
• Винкристин и прокарбазин откладывают на одну неделю. В случае стойкой лейкопении ( 9 ) или тромбоцитопении ( 9 ) лечение откладывается еще на неделю. Если гематологические нарушения сохраняются и далее, лечение прекращается.
— Уменьшить дозу CCNU и прокарбазин на 25% в случае 3 степени гематологической токсичности и 2 или 3 степени негематологической токсичности.
— Прекращение лечения в случае:
• 3 степени кардиотоксичности.
• 4 степени гематологической токсичности или 3 степени негематологической токсичности, несмотря на снижение дозы.
• Любой негематологической токсичности 3 степени (за исключением тошноты и рвоты).
— В случае аллергической реакции кожи прием прокарбазина должен быть прекращен.
— Винкристин отменяется в случае 2 степени нейротоксичности.
— В связи с кумулятивной миелосупрессией CCNU продолжение лечения при маргинальных гематологических нарушениях приведет к более высокой токсичности в последующих циклах.
— Как правило, печеночные нарушения постепенно уменьшаются.
г) BCNU (кармустин) для химиотерапии опухоли головного мозга. 60 мг/м 2 в 1-3 дни каждые 8 недель:
• Наиболее распространенной схемой для BCNU (кармустина) является 130-200 мг/м 2 каждые 6 недель, но 8-недельный прием в дозе 80 мг/м 2 оказался эффективным в исследовании на 40 пациентах с глиомами высокой степени злокачественности. Исследование пациентов с мультиформной глиобластомой с предварительным лечением темозоломидом (в комбинации химиолучевой терапии) показало значительную гематологическую токсичность при такой дозировке и снижении дозировки до 60 мг/м 2 в 1-3 день восьминедельного цикла.
• Основные побочные эффекты: гематологическая токсичность, токсическое поражение печени, тошнота и легочная токсичность.
• BCNU вводят внутривенно с первого по третий день в дозе 60 мг/м 2 /день (доза на цикл 180 мг/м 2 ) каждые 8 недель. Назначают противорвотные средства (метоклопрамид, домперидон).
• Противопоказания: заболевания легких в анамнезе, так как возможно действие на функцию легких; необходимо оценить функцию по диффузионной емкости оксида углерода, которая должна быть выше 60% прогнозируемого значения.
• Контроль показателей:
— Гематологические параметры на 21, 28, 35, 42, 65 сутки (= первый день следующего цикла).
— Биохимический анализ перед началом каждого цикла.
• Модификации дозировки:
— В случае количества лейкоцитов 9 /л или тромбоцитов 9 /л в первый день—задержка до восстановления.
• Если гематологическая токсичность не регрессирует в течение двух недель или повторяется токсичность 2 степени в ходе последующего цикла, следует прекратить лечение.
— В случае гематологической токсичности 3-й степени дозировка для следующего цикла снижается на 25%.
— В случае гематологической токсичности 4 степени дозировка для следующего цикла снижается на 50%.
— При негематологической токсичности:
• Не начинать следующий цикл, пока вся токсичность (за исключением алопеции) не регрессирует до 1 степени или менее.
• При печеночной токсичности 2 степени дозировка следующего цикла снижается на 25% после возвращения к нормальным показателям.
• При печеночной токсичности 3 степени дозировка следующего цикла снижается на 50% после возвращения к нормальным показателям.
• В случае легочной токсичности 3 или 4 степени лечение следует прекратить.
• В случае любой негематологической токсичности 4 степени или непеченочной токсичности 3 степени (за исключением тошноты, рвоты и алопеции) лечение необходимо прекратить.
• Если негематологическая токсичность не восстанавливается в течение первого месяца или если негематологическая токсичность повторяется в последующем цикле до степени >2, следует прекратить лечение.
Читайте также:

