Как часто рецидив при саркоме

Методы исследования. Под рецидивной саркомой мы понимаем развитие опухоли после проведенного лечения, считающегося радикальным, т.е. повторное появление опухоли в области первичного очага или зонах регионарного метастазирования в период более 6 месяцев после оперативного вмешательства (от 6 месяцев до 3 лет - ранние рецидивы, позднее 3 лет - поздние рецидивы СМТ). Выявление отдаленных метастазов саркомы мягких тканей в период времени до 6 месяцев нами определено как первично-генерализованная саркома мягких тканей.
Основным симптомом локального рецидива саркомы мягких тканей явился определяемый визуально, реже - пальпаторно, опухолевый узел или несколько узлов (при мультицентричном росте). У 73 (76,8%) из 95 больных локальный рецидив саркомы мягких тканей выявлен при профилактическом осмотре. В 22 (23,2%) случаях больной самостоятельно выявил наличие опухолевого узла, что и явилось причиной явки на осмотр. Рентгенологическое исследование позволило выявить отдаленные метастазы в легкие у 15 (15,8%) из 95 пациентов, а также наличие или отсутствие рентгенологических признаков вторичного вовлечения подлежащих костных структур. Анатомо-топографическая локализация СМТ определялась с помощью компьютерной томографии или ядерно-магнитного резонанса - у 27 больных. Эти методы являются наиболее достоверными и позволяют планировать объем оперативного вмешательства. Для морфологической диагностики опухоли мягких тканей использовалась закрытая пункционная аспирационная или трепан-биопсия, открытая инцизионная биопсия.
Результаты исследования. По полученным нами данным, наибольшее количество случаев возобновления местного опухолевого роста после хирургического лечения наблюдалось в течение первых 6 месяцев после лечения - 22 (27,8±5,0%) при размере опухоли не более 5 см и в 17 (21,5±4,6%) случаях - при размере опухоли более 5 см. К началу третьего года частота локальных рецидивов была одинакова независимо от размера первичной опухоли. Сроки появления локального рецидива сарком мягких тканей в зависимости от размера первичной опухоли после хирургического лечения представлены на рис. 1.
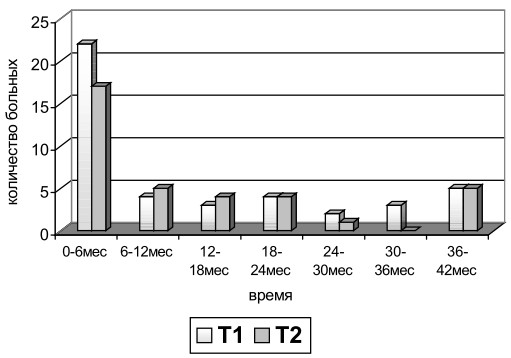
Рис. 1. Сроки появления локального опухолевого роста после хирургического лечения в зависимости от размера саркомы мягких тканей.
Наиболее высокая частота локальных рецидивов при размере первичной опухоли более 5 см наблюдалась нами к концу второго года после хирургического лечения. Эти данные свидетельствуют о том, что опасность появления местного рецидива опухоли у больных саркомами мягких тканей возрастает после хирургического лечения с интервалом в 1 год. Неадекватность хирургического лечения явилась основной причиной высокой частоты локальных рецидивов при размере опухоли до 5 см. Снижение же абсолютного количества локальных рецидивов опухоли при ее диаметре более 5 см к концу третьего года после хирургического лечения было обусловлено гибелью части больных.
Нами также был проведен анализ периодичности возобновления местного роста саркомы мягких тканей в зависимости от размера опухоли после хирургического лечения (табл. 1).
Таблица 1 - Сроки появления локального опухолевого роста после хирургического лечения в зависимости от размера опухоли
Рецидив саркомы
Онкологические заболевания не всегда удается вылечить даже при обнаружении на ранних стадиях. Современные методы хирургического и терапевтического лечения несовершенны, а злокачественные опухоли могут начать вновь формироваться даже после длительной ремиссии. Так, рецидив саркомы диагностируют у пациентов после удаления новообразования и химиотерапии. Предотвратить повторный рост опухоли можно при постоянных обследованиях. Консультация онколога поможет пациенту узнать больше о таком патологическом состоянии, как саркома мягких тканей: рецидив, риски, негативные последствия, рецидив хондросаркомы и других типов.
В медицинской литературе саркомами называют группу злокачественных новообразований, происходящих из клеток соединительнотканного происхождения. Это могут быть опухоли мягких тканей, вроде жира, мышц и сосудов, или новообразования твердых тканей, включая кости и хрящи. Такие заболевания менее распространены, чем раковые опухоли, сформированные из эпителиальных тканей. Клиническая картина разнообразна и зависит от конкретного типа патологии. Некоторые саркомы быстро растут и распространяются в организме, а другие, напротив, долго развиваются и редко метастазируют. Рецидив саркомы также может быть достаточно характерным для отдельных типов новообразований.
Гистологическое происхождение опухолевой ткани говорит о многом, поэтому важнейшим методом диагностики онкологии является биопсия. Изучение новообразования под микроскопом помогает специалисту оценить агрессивность саркомы, определить стадию болезни и даже назначить лечение. Первоначально онкологу нужно уточнить, из каких конкретно клеток происходит опухоль, поскольку от этого зависит клиническая картина патологии. Как показывает практика, рецидив саркомы в большей степени характерен для новообразований из кроветворных клеток.
Типы заболевания по локализации и происхождению:
- Недифференцированная плеоморфная саркома – это опухоль, чаще всего образующаяся в области верхних или нижних конечностей, а также в задней части живота.
- Желудочно-кишечная стромальная опухоль – новообразование, происхождение которого связано с нервно-мышечными тканями органов пищеварительной трубки.
- Саркома костной ткани – патология остеобластов или других клеток. Рецидив остеосаркомы встречается достаточно часто.
- Липосаркома – опухоль белой жировой ткани, отличающаяся относительно благоприятным течением.
- Лейомиосаркома – патология, поражающая гладкие мышцы в стенках органов.
- Синовиальные саркомы, развивающиеся в области суставов рук и ног.
- Злокачественная опухоль периферической нервной оболочки, также известная как нейрофибросаркома. Новообразование негативно влияет на защитную оболочку нервов.
- Рабдомиосаркома – форма заболевания, поражающая поперечнополосатую мышечную ткань. Патология чаще всего встречается у детей.
- Ангиосаркомы, развивающиеся из клеток кровеносных или лимфатических сосудов.
- Фибросаркомы – основные новообразования соединительной ткани, развивающиеся из фибробластов.
Рецидив саркомы очень важно обнаружить вовремя, поскольку повторный рост патологии может занимать меньше времени. Зачастую онкологические больные поздно проходят обследование из-за отсутствия симптомов, однако нормальное самочувствие не свидетельствует об отсутствии злокачественного процесса. Пациентам с предрасположенностью к таким новообразованиям следует также проходить скрининговые обследования для раннего обнаружения саркомы.
Злокачественные новообразования соединительнотканного происхождения изучены не так хорошо, как эпителиальные опухоли, однако современные молекулярно-генетические исследования помогают ученым обнаруживать все новые этиологические факторы. Механизмы развития саркомы многообразны и зависят от конкретного типа патологии. На сегодняшний день онкологам известные некоторые внутренние и внешние негативные влияния, способствующие канцерогенезу. В первую очередь это генетика, образ жизни пациента, вредные привычки и заболевания внутренних органов.
Рецидив саркомы мягких тканей и первичное новообразование формируются по-разному. Начальные процессы онкогенеза обусловлены изменениями клеток соединительной ткани под воздействием негативных факторов. Главным пусковым фактором является нарушение внутренней регуляции клеток. Чаще всего речь идет о нарушении структуры молекул ДНК, поскольку именно эти химические соединения контролируют метаболизм и клеточный цикл. В результате в ткани формируются клетки, способные быстро расти и делиться. Постепенно образуется опухолевый процесс, распространяющийся на другие анатомические области. Противоопухолевой защиты иммунитета редко бывает достаточно для предотвращения канцерогенеза.
Обобщенные факторы риска:
- Воспалительные и аутоиммунные патологии соединительных тканей. Атака клеток иммунной системы собственных тканей часто может приводить к предраковым изменениям.
- Радиационное воздействие на мягкие и твердые ткани. Этот негативный фактор обычно обусловлен лучевой терапией онкологических заболеваний. Ионизирующее излучение воздействует на ДНК клеток и провоцирует образование аномальные компонентов.
- Курение. В табачном дыме содержатся смолы и другие вредные соединения, негативно воздействующие на соединительные ткани.
- Алкоголизм. Этиловый спирт в первую очередь повреждает эпителий слизистой оболочки желудочно-кишечного тракта и печень, однако возможны и другие негативные эффекты.
- Вредная диета. Этот этиологический фактор в большей степени связан с онкологическими патологиями органов пищеварения. Регулярное употребление красного мяса и жирных продуктов приводит к изменениям во внутренней оболочке органов ЖКТ. Диетологи рекомендуют пациентам с предрасположенностью к онкологии есть больше овощей и фруктов.
- Наследственные этиологические факторы. Обнаруженный рецидив саркомы у близких родственников пациента свидетельствуют о повышенном индивидуальном риске канцерогенеза. Зачастую детям от родителей передаются специфические генные мутации, ассоциированные с ростом новообразований.
- Медикаментозная терапия некоторых заболеваний.
- Доброкачественные опухоли органов. Такие заболевания могут постепенно переходить в злокачественный процесс.
- Малоподвижный образ жизни и избыточная масса тела.
- Воздействие токсичных химических веществ.
Предполагается, что генетические факторы играют большую роль в этиологии соединительнотканных опухолей, чем в случае эпителиальных новообразований. Тем не менее профилактика некоторых сарком не лишена смысла, поэтому следует проконсультироваться с врачом при наличии предрасположенности к онкологии.
Онкологические заболевания известны своим прогрессирующим течением, обусловленным постоянным распространением злокачественной ткани. На определенном этапе опухолевые клетки проникают в кровоток и лимфатическую систему, что обуславливает рост новых патологических очагов в отдаленных органах. Наиболее удобной для лечения является именно локализованная стадия саркомы, при которой новообразование расположено в пределах одного органа. Распространенный процесс сложнее остановить. Онкологическим пациентам с терминальной стадией саркомы часто назначают только терапевтические процедуры для облегчения состояния.
Рецидив саркомы может являться результатом естественного развития болезни или недостатками лечения. Одним из вариантов повторного роста новообразования может быть некачественная хирургия, во время которой врачу не удается удалить все злокачественные ткани. Кроме того, опухолевые клетки могут задерживаться в лимфатической системе. Пациент должен понимать, что ни один метод терапии или хирургии не гарантирует полного излечения, поэтому после прохождения лечения важно регулярно проходить обследования. Чем раньше врач обнаружит рецидив новообразования, тем больше шансов провести эффективную терапию.
При подозрении на повторное развитие опухоли следует обратиться к онкологу. Врач спросит о жалобах, изучит историю болезней и проведет осмотр. Для постановки диагностика специалисту понадобятся результаты инструментальных и лабораторных исследований.
Назначаемые диагностические процедуры:
- Анализ крови на онкологические маркеры и общие показатели.
- Биопсия пораженных тканей с последующим излучением материала в лаборатории и определением гистологического типа саркомы.
- Ультразвуковое исследование мягких тканей.
- Рентгенография, компьютерная и магнитно-резонансная томография – методы получения изображения органов, позволяющие обнаружить рецидив болезни и метастазы.
- Эндоскопическое исследование органов.
Лечение рецидива обычно не отличается от лечения первичной болезни. Если новообразование можно удалить, врач проводит хирургическую операцию. Обычно требуется резекция части органа с удалением близлежащих лимфатических узлов. После операции назначаются терапевтические процедуры для предупреждения нового рецидива.
- Введение цитотоксических и цитостатических противоопухолевых средств для уменьшения размера патологического очага, удаления отдельных злокачественных клеток или замедления роста саркомы.
- Радиационная терапия саркомы, позволяющая замедлить развитие болезни и уменьшить опухоль.
- Введение высокоселективных медикаментов.
- Паллиативная помощь.
Таким образом, чем раньше пациент пройдет обследование у врача, тем выше шансы на выздоровление.

Саркомы — это общее название злокачественных опухолей, которые образуются из разных типов соединительной ткани. Зачастую они характеризуются прогрессивным, очень быстрым ростом и частыми рецидивами, особенно у детей. Такое поведение сарком объясняется ускоренным развитием в молодом возрасте клеток соединительной и мышечной тканей.
- Причины сарком и факторы риска
- Развитие саркомы
- Распространенность саркомы
- Симптомы
- Диагностика
- Выберите врача и запишитесь на приём
- Лечение саркомы
Саркомы подразделяют на две большие группы: мягких тканей и костей.
В отличие от рака, который представляет собой злокачественное новообразование из эпителия, саркомы произрастают из соединительной ткани и не привязаны к какому-либо конкретному органу, а могут возникать в любом месте организма. В быту все злокачественные новообразования принято называть раком, однако это некорректно.
Саркомы костей могут развиваться как непосредственно из костной ткани (параостальная саркома, хондросаркома), так и из тканей некостного происхождения (саркома Юинга — из мезенхимальных стволовых клеток, ангиосаркома — из клеток кровеносных сосудов и др.). Они могут поражать внутренние органы, кожу, лимфоидную ткань, центральную и периферическую нервную систему. Классификация, основанная на типе ткани, из которой сформировалась опухоль, включает следующие ее разновидности:
- остеосаркомы произрастают из костной ткани;
- мезенхимомы — из эмбриональной;
- липосаркомы — из жировой;
- миосаркомы — из мышечной ткани;
- ангиосаркомы — из кровеносных и лимфатических сосудов и т.д.
Всего известно около 100 различных вариантов сарком, каждая из которых имеет свои особенности развития, лечения и, соответственно, свой прогноз.
По степени зрелости ткани, их разделяют на низко-, средне- и высокодифференцированные. От данной особенности зависит степень злокачественности опухоли, а также тактика ее лечения: чем менее дифференцированы опухолевые клетки, тем агрессивнее новообразование и серьезнее прогноз.
Причины сарком и факторы риска
На сегодняшний день существуют научные работы, доказывающие роль ионизирующего излучения, ультрафиолета, химических веществ, а также некоторых вирусов в развитии сарком. Все эти факторы вызывают генетические мутации, которые в результате ведут к бесконтрольному росту и размножению клеток.
В возникновении саркомы Юинга большую роль играет скорость роста костей и гормональный фон. Также к факторам риска можно отнести курение, работу в сфере химической промышленности, наследственную отягощенность, сбои в работе иммунной системы.

Кроме того, среди причин, способствующих образованию сарком, можно отнести следующие: наличие доброкачественных новообразований (они могут озлокачествляться), механические травмы, наследственная предрасположенность и др.
Развитие саркомы
Произошедшие генетические нарушения ведут к бесконтрольному делению клеток соединительной ткани. Опухоль начинает расти, проникая в соседние органы и разрушая их. Как правило, чем менее дифференцированы клетки, тем более злокачественное течение имеет заболевание.
По мере развития новообразования, опухолевые клетки разносятся по организму с током крови или лимфы, они оседают далеко от расположения первичной опухоли и образуют вторичные очаги — метастазы. В связи с этим, даже после радикального лечения саркомы, зачастую возникают рецидивы.
По мере развития опухоли, происходит ее врастание в окружающие ткани и органы с нарушением их функционирования, развитием болевого синдрома (при врастании в нервные стволы), нарушением глотания (при поражении пищевода), нарушением дыхания (при поражении трахеи).
Чаще на разрезе ткань саркомы бело-розового цвета и напоминает рыбу, по консистенции мягкая или эластичная. Она не имеет четких границ и плавно переходит в здоровую ткань.
Поскольку саркомы включают в себя большое множество вариантов, все же стоит отметить, что некоторые виды характеризуются крайне медленным прогрессированием (паростальная саркома костей), для других характерно молниеносное течение (рабдомиосаркома), а, например, для липосаркомы характерно одновременное или последовательное появление сразу нескольких очагов в разных местах.
Распространенность саркомы
Саркомы встречаются довольно редко — они составляют около 1% от всех злокачественных опухолей человека. В России среди мужчин показатель заболеваемости составляет 2,13 и 1,83 случая на 100 тысяч населения среди мужчин и женщин соответственно.
Данный тип новообразований обнаруживают и у детей, и у взрослых людей. Выделяют формы, которые встречаются в основном у детей (саркома Юинга) или преимущественно у взрослых (лейомиосаркома, хондросаркома, стромальные опухоли ЖКТ).
Каждый второй случай костной саркомы и каждый пятый случай мягкотканной саркомы выявляется у пациентов в возрасте до 35 лет. Треть случаев выявляют у пациентов в возрасте до 30 лет, но большая их часть обнаруживается в промежутке от 33 до 60 лет.
Симптомы
Проявления саркомы могут быть самыми разными в зависимости от места ее возникновения, размеров и направления их роста. В большинстве случаев сначала обнаруживается новообразование, которое постепенно увеличивается в размерах. По мере его роста, вовлекаются соседние ткани, прорастая в которые, саркома повреждает в них нервы и сосуды. Это проявляется болевым синдромом, который плохо купируется анальгетиками.

- при саркоме Юинга — боли по ночам в ногах;
- при лейомиосаркоме кишечника — прогрессирующие признаки кишечной непроходимости;
- при саркоме матки — межменструальные кровотечения;
- при внебрюшинной саркоме — лимфостаз и слоновость нижних конечностей;
- при саркоме средостения — отек шеи, расширение подкожных вен на груди, одышка;
- при саркомах лица и шеи — асимметрия, деформация головы, нарушения в работе жевательных и мимических мышц лица и др.
По мере развития саркомы конечностей, над ней появляются изменения кожи в виде покраснения, расширения вен, тромбофлебита и местного повышения температуры. Подвижность рук и ног становится ограниченной, нарушение функций сопровождается постоянной болью.
Диагностика
Постановка диагноза основана на типичных ее проявлениях, данных рентгенологического, лабораторного и гистологического исследования. В молодом возрасте боли в костях должны вызывать повышенную онкологическую настороженность. Методы, использующиеся для выявления сарком, следующие:
- рентгенография костей в 2 проекциях;
- рентгенография грудной клетки (для выявления метастазов в легких);
- компьютерная томография;
- магнитно-резонансная томография;
- УЗИ брюшной полости;
- допплерография и ангиография;
- радионуклидная диагностика;
- биопсия опухоли с последующим гистологическим, цитологическим и цитохимическим исследованием материала.
Полное обследование позволяет точно определить расположение и размеры саркомы, ее метастазов, их строение, особенности кровоснабжения и роста, степень зрелости клеток. Важно еще до начала лечения как можно точнее установить диагноз, поскольку от него зависит тактика лечения.
Лечение опухолей и опухолеподобных поражений костно-суставной системы зависит от характера, локализации и распространенности процесса.
Методом выбора является хирургическое удаление патологического образования.
Из доброкачественных опухолей чаще других рецидивируют гигантоклеточная опухоль (остеокластома) и хрящевые опухоли, главным образом, после нерадикального оперативного их удаления или злокачественного перерождения.
Из злокачественных опухолей оперативному лечению подлежат малочувствительные или нечувствительные к ионизирующему излучению хондросаркомы, злокачественные хордомы и остеокластомы, саркомы мягких тканей. При остеогенной саркоме, саркоме Юинга, злокачественных лимфомах (ретикулосаркоме, лимфосаркоме), сосудистых опухолях применяется комбинированное лечение с использованием хирургического метода, лучевой терапии, химиотерапии и гормонотерапии.
Рецидивы доброкачественных опухолей и опухолеподобных поражений костей
После применения костных и костно-пластических операций рецидивы опухолей возникают в сроки от 2 месяцев до нескольких лет. Рецидивы остеокластомы, хондромиксоидной фибромы, хондромы и хондробластомы могут локализоваться в местах оперативного вмешательства на кости, а также изолироваливанно в мягких тканях пораженного сегмента конечности.
Рецидивы аневризмальной костной кисты, солитарной костной кисты, остеоидной остеомы, десмопластической фибромы, фиброзной дисплазии возникают только в пределах оперированной кости, без поражения окружающих мягких тканей. Повторные рецидивы встречаются значительно реже (при остеокластоме или злокачественной хрящевой опухоли) и локализуются обычно в мягких тканях. Однако, повторные рецидивы могут наблюдаться и в оперированной кости после нерадикального удаления опухолевой ткани первого рецидива. Фиброзная дисплазия рецидивирует многократно в пределах пораженного участка кости.
Клиника рецидивирующей опухоли менее выражена, чем первичной, и долгое время после операции может отсутстствовать. Рецидив хондробластомы имеет свои особенности. Первые несколько месяцев он протекает бессимптомно, а затем появляется болевой симптом, который во времени постепенно усиливается и становится мучительным для больного. Появляется и субфебрильная температура. В области рубца пальпация болезненна, окружающая кожа гиперемирована, отечна, с местным повышением температуры. Только радикальное хирургическое вмешательство избавляет больного от боли.
Рентгенологически в ранние сроки после операций рецидивы доброкачественных опухолей проявляются деструкциями по краям опила кости. В последующем возникают множественные мелкие очаги деструкции с нечеткими контурами. В подобных наблюдениях эффективно применение традиционной томографии и компьютерной томографии, а в случаях после костно-пластических операций с резекциями суставного конца — рентгенография с прямым увеличением изображении.
При динамическом рентгенологическом наблюдении отмечается слияние мелких и средних очагов с образованием крупных участков деструкции, занимающих, как правило, весь поперечник кости. При этом констатируется истончение и разрушение коркового слоя. В последнем случае опухоль прорастает в параостальные мягкие ткани. Наблюдается и вздутие. Выраженность вздутия зависит от длительности рецидивного процесса. Вначале очаги деструкции имеют однородный характер, а затем появляется неоднородная ячеистая структура. Следует особо подчеркнуть, что деструкция при рецидиве опухоли имеет тенденцию к распространению и на трансплантат.
Выше было сказано, что рецидив некоторых доброкачественных опухолей костей (остеокластомы — гигантоклеточной опухоли, остеобластомы, хондробластомы, хондромиксоидной фибромы, эк- и энходромы) может локализоваться в мягких тканях. В подобных случаях в мягких тканях рентгенологически начинают определяться добавочные образования округлой формы, разной величины, интенсивности и структуры. Они могут располагаться в мышечном массиве, изолированно в подкожной жировой клетчатке либо одномоментно в них. Структура рецидивирующей опухоли обычно однородная.
Патогномоничных рентгенологических признаков озлокачествления доброкачественной опухоли кости при ее рецидиве нет.
Злокачественные перерождения характеризуются теми же рентгенологическими признаками, что и рецидив доброкачественной опухоли. Вначале появляются мелкие очаги деструкции, а затем истончение коркового слоя, его разрушение и прорастание опухоли в мягкие ткани с формированием внекостного компонента. Трансплантат, как правило, разрушается. Однако, прогрессирование процесса происходит более быстро, чем при рецидиве доброкачественной опухоли.
Обращает на себя внимание, что рентгенологические проявления рецидива доброкачественной опухоли и опухолеподобных поражений заметно (от нескольких месяцев до нескольких лет) опережают появление клинических симптомов. Поэтому для своевременного их выявления необходимо регулярное контрольное рентгенологическое обследование больных.
Рекомендуется проводить контрольное рентгенологическое обследование подобных больных по следующей схеме: в течение первого года после операции проводить рентгенографию каждые три месяца; в течение второго года — каждые шесть месяцев и в течение третьего и последующих лет — один раз в год. Контрольное лучевое исследование должно включать помимо традиционной рентгенографии и компьютерную томографию. При рецидиве остеокластомы для уточнения мягкотканного компонента следует применить ангиографию.
При этом следует помнить, что интенсивное и неравномерное контрастирование опухоли наступает быстро и к началу венозной фазы усиливается. Усиливается и венозный отток. По периферии опухоли определяются патологические сосуды. При злокачественном перерождении остеокластомы ангиографически определяется наличие на всем протяжении опухоли множества патологических сосудов в сочетании с ранним усиленным контрастированием и ранним венозным оттоком.
Анализируя рентгенограммы и ангиограммы, следует помнить и о рентгенологических проявлениях послеоперационных осложнений (вторичный остеомиелит, остеолиз трансплантата, патологическая перестройка трансплантата), а также о различных фазах восстановительного процесса.
В диагностике рецидива опухолей возможно использование радионуклидного исследования.
В случаях, когда клинико-рентгено-радиологическое исследование не разрешит диагностическую задачу, рекомендуется повторное исследование через 2-3 недели или выполнение биопсии.
Рецидивы злокачественных опухолей костей
Рецидивы хондросаркомы, остеогенной саркомы, саркомы Юинга, злокачественных лимфом и других опухолей наблюдаются часто после сберегательных операций, иногда сочетающихся с химиотерапией и лучевым лечением. Рецидивы опухолей после радикальных хирургических вмешательств наблюдаются реже.
Повторные рецидивы характерны для злокачественной хордомы и хондросаркомы. Последние рецидивируют обычно в первом полугодии после операции. При других злокачественных опухолях рецидивы возникают в сроки от 3 месяцев до 3-х лет. Остеогенная саркома и злокачественная остеокластома, как правило, рецидивируют в первый месяц после операции.
Клинически рецидив опухоли проявляется болевым симптомом, который быстро прогрессирует. Особенно он нарастает, когда появляется опухоль в области послеоперационного рубца. Повышается общая температура тела, а в анализах крови умеренно увеличивается скорость оседания эритроцитов (СОЭ). В далеко зашедшем случае кожа над опухолью изъязвляется и начинает кровоточить.
Рентгенологически рецидив характеризуется прогрессирующей деструкцией кости и трансплантата, а также инфильтрацией мягких тканей. При этом появляются разнообразные периостозы (линейные, козырьковые, лучистые, многослойные). Рецидив хондросаркомы сопровождается образованием безструктурных обызвествлений в кости или мягких тканях.
В тех случаях, когда известна природа первичной опухоли диагностика рецидива не представляет трудности. Если форма первичной опухоли неизвестна, то традиционная рентгенография лишь подтверждает факт рецидива, т.к. рентгенологическая семиотика рецидивов злокачественных опухолей не имеет специфики для различных нозологических форм.
Ангиография также позволяет подтвердить злокачественную природу рецидива, т.к. дает возможность установить степень распространения опухоли в мягкие ткани, характер васкуляризации и вовлечение в процесс магистральных сосудов. При рецидивах остеогенной саркомы, хондросаркомы, ретикулярной саркомы, лимфосаркомы и злокачественной остеокластомы наблюдается выраженный атипизм сосудов. Радионуклидное исследование позволяет провести дифференциальную диагностику организовавшейся гематомы и рецидивирующей опухоли.
Рецидивы опухолей мягких тканей
Рецидивы доброкачественных и злокачественных опухолей мягких тканей возникают после первой операции в сроки от нескольких месяцев до 5 лет.
Клинически подобные рецидивы проявляются появлением уплотнения в послеоперационном рубце или вблизи его и болевым симптомом. При возникновении рецидивов опухолей мягких тканей малого таза первыми симптомами являются иррадирующие боли, запоры или дизурические явления.
Рентгенодиагностика рецидива основывается на традиционной рентгенографии, пневмографии, ангиографии, а также компьютерной томографии. На обзорных рентгенограммах пораженной области в большинстве случаев рецидив удается распознать по наличию участков затемнения неопределенной или округлой формы, интенсивностью равной или выше интенсивности мышечного массива.
Структура фокуса затемнения однородная, реже встречаются известковые включения. Возможны и вторичные изменения прилежащей кости (атрофия от давления, краевая деструкция, периостоз или гиперостоз). В случаях, когда на традиционных рентгенограммах не удается определить признаки рецидива опухоли мягких тканей, следует прибегнуть к пневмографии, ангиографии или компьютерной томографии.
Ангиоархитектоника рецидивной доброкачественной опухоли мягких тканей не отличается от таковой в нормальной ткани. Однако, может наблюдаться смещение магистральных сосудов. Ангиографическая картина рецидивной злокачественной опухоли мягких тканей характеризуется атипичными сосудами, усиленным продолженным контрастированием, "ампутацией" питающих артерий, лакунами, ранним венозным оттоком и нечеткостью контуров магистральных сосудов.
Характер кровоснабжения рецидивных образований не отличается от архитектоники первичной опухоли той же структуры. Но в отличие от первичных опухолей при рецидивах отмечается более частое вовлечение в процесс магистральных сосудов. При использовании радионуклидного метода следует помнить, что рецидивная доброкачественная опухоль мягких не имеет тенденции к высокому уровню накопления радиофармацевтического препарата (РФП). Исключение составляют фибромы и нейрофибромы.
При рецидивах злокачественных опухолей мягких тканей уровень накопления РФП довольно высокий, что позволяет рекомендовать этот метод в практику. Контрольное исследование больных для диагностики рецидива опухоли мягких тканей следует проводить также часто, как и после удаления опухолей костей, особенно в течение первого года после операции.
Читайте также:

