Iv российская конференция по раку молочной железы

30-31 января 2020, Москва
Место проведения: Москва, Отель Ренессанс Москва Монарх Центр
(Ленинградский пр., д.31А, стр.1).
Участники, прослушавшие всю конференцию, получат 6 кредитов за каждый день
по программе непрерывного медицинского образования Министерства здравоохранения РФ.
Коды для начисления баллов будут направлены по электронной почте, указанной при регистрации.
Дополнительную информацию можно получить на стенде RUSSCO.
Актуальные вопросы морфологической диагностики при РМЖ
10:20-10:40 – Вопросы, дискуссия
RUSSCO-Junior
Дискуссия: Хирургическое вмешательство после неполного ответа на неоадъювантную химиотерапию при первично неоперабельном раке молочной железы
Дискуссия: Пришло ли время PARP ингибиторов при РМЖ
Да
д-р Гречухина Катерина Сергеевна, ГБУЗ Московский клинический научный центр им. А.С. Логинова ДЗМ, Москва
Сателлитный симпозиум компании Эйсай
О чем молчат клинические рекомендации?
* Доклады не входят в программу для НМО
Сателлитный симпозиум компании Novartis
PIK3CA-мутированный рак молочной железы: что мы о нем знаем сейчас
* Доклады не входят в программу для НМО
Сателлитный симпозиум компании Roche
По следам SABCS: что еще мы можем сделать
для пациента с раком молочной железы?
* Доклады не входят в программу для НМО
Сложные вопросы комплексного лечения рака молочной железы
14:50-15:10 – Дискуссия
Новые морфологические маркеры
Объединенная пациентская сессия
Современные стандарты системного лечения метастатического гормоночувствительного рака молочной железы
* Доклады не входят в программу для НМО
15:20-15:50 – Регистрация участников
15:50-16:20 – Современный взгляд на лечение рака молочной железы
проф. Жукова Людмила Григорьевна, ГБУЗ Московский клинический научный центр им. А.С. Логинова ДЗМ, Москва
16:50-17:20 – Реабилитация женщин, больных раком молочной железы
д.м.н. Грушина Татьяна Ивановна, ФГБУ "НМИЦ реабилитации и курортологии" МЗ РФ, Москва
17:20-17:30 – Вопросы и ответы
* Доклады не входят в программу для НМО
Актуальные вопросы хирургического лечения рака молочной железы
17:40-17:50 – Обсуждение
Нейроэндокринные опухоли молочной железы
17:40-17:50 – Дискуссия
Сателлитный симпозиум компании Pfizer
Люминальный мРМЖ – чего на самом деле стоит бояться?
* Доклады не входят в программу для НМО
Сателлитный симпозиум компании Р-Фарм
Возможности поздних линий химиотерапии
диссеминированного рака молочной железы
18:00-18:30 – Современные возможности лечения диссеминированного рака молочной железы после прогрессирования на первой линии терапии
проф. Жукова Людмила Григорьевна, ГБУЗ Московский клинический научный центр им. А.С. Логинова ДЗМ, Москва
* Доклады не входят в программу для НМО
Сателлитный симпозиум компании Pierre-Fabre
* Доклады не входят в программу для НМО
Сложные вопросы лекарственного лечения метастатического РМЖ
Разбор клинических случаев с интерактивным голосованием
Сложные вопросы скрининга рака молочной железы
09:20-09:40 – Скрининг и ранняя диагностика рака молочной железы после аугментационной маммопластики
д-р Пучкова Ольга Сергеевна, МНОЦ МГУ им. М.В. Ломоносова, Москва
10:20-10:40 – Дискуссия
Реабилитация
Сателлитный симпозиум компании Besins
Терапия мастопатии и снижение риска РМЖ. Есть ли связь?
12:30-12:50 – Алгоритм выбора консервативного лечения мастопатии в свете задачи снижения заболеваемости РМЖ
проф. Протасова Анна Эдуардовна, Санкт-Петербургский государственный университет, Санкт-Петербург
* Доклады не входят в программу для НМО
Сателлитный симпозиум компании Novartis
Оптимальный выбор первой линии терапии HR+ HER2- рРМЖ
на основе новых данных доказательной медицины
13:00-13:10 – Дискуссия. Подведение итогов
* Доклады не входят в программу для НМО
Сателлитный симпозиум компании Lilly
Оптимальное время назначения ингибитора CDK4 и 6 в терапии гормонозависимого HER2-отрицательного рака молочной железы поздних стадий
12:50-13:10 – Дополнительные терапевтические возможности при назначении абемациклиба у интенсивно предлеченных пациенток с гормонозависимым HER2-отрицательным метастатическим раком молочной железы
проф. Жукова Людмила Григорьевна, ГБУЗ Московский клинический научный центр им. А.С. Логинова ДЗМ, Москва
* Доклады не входят в программу для НМО
Сессия по лучевой терапии
15:50-16:00 – Вопросы, дискуссия
Осложнения противоопухолевых препаратов с новым механизмом действия
15:50-16:00 – Вопросы, обсуждение
Исследования, инициированные исследователем (IIT).
Как это работает в России
- Правовое регулирование IIT. Что необходимо знать врачу
- Как правильно запланировать и организовать IIT в России
Бутылин Алексей Александрович, Крокус Медикал БВ, Москва
Регистрация на мероприятие
Российский онкологический научный центр им. Н.Н. Блохина РАМН
Европейское общество медицинской онкологии (ESMO)
21-23 ноября 2000 года
Российская академия государственной службы при Президенте Российской Федерации
С.М. Портной, К.П. Лактионов, А.И. Барканов, К.Л. Чимишкян, В.В. Птушкин, В.Б. Ларионова, Н.В. Жуков, М.Г. Мистакопуло, М.Ш. Ахметов.
ОПЫТ ЛЕЧЕНИЯ БОЛЬНЫХ ПРОГНОСТИЧЕСКИ ОТЯГОЩЁННЫМ МЕСТНО-РАСПРОСТРАНЁННЫМ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ.
IV ежегодная российская онкологическая конференция 21-23 ноября 2000 года, Москва, 2000, с.57-59
Российский онкологический научный центр им. Н.Н. Блохина РАМН, Москва
РМЖ — рак молочной железы
МРРМЖ — местно-распространённый рак молочной железы
ВДХТ — высокодозная химиотерапия
Отдалённые результаты лечения больных отёчно-инфильтративной формой рака молочной железы остаются неудовлетворительными. Отёчно-инфильтративная форма рака молочной железы (inflammatory breast cancer) клинико-рентгенологически характеризуется диффузным распределением опухолевой ткани в молочной железе по типу инфильтрата (без выявляемого опухолевого узла) и отёком кожи, отличается особой агрессивностью течения, выражающейся в быстром местно-регионарном распространении опухоли по лимфатической системе с быстрым развитием отдалённых метастазов.
Местное лечение (оперативное, лучевое, сочетание лучевого с оперативным) отёчно-инфильтративной формы РМЖ даёт 0-4 % 5-летней выживаемости при средней длительности жизни от 18 до 22 месяцев (1).
После эффективной предоперационной химиотерапии и радикальной операции, несмотря на проведение профилактической ХТ по схеме CMF и профилактической ЭТ, уже на первом году наблюдений рецидивы и метастазы развиваются в 50% случаев, 3-летняя безрецидивная выживаемость составляет 24%, 5-летняя — 19% (2). Сходным плохим прогнозом отличается также узловая форма рака с вторичным выраженным отёком кожи (3).
Целью настоящего исследования было изучение возможности повышения эффективности лечения путём последовательного применения химиотерапии, химиолучевой терапии, операции и адъювантной системной терапии, одним из компонентов которой является высокодозная ХТ с аутотрансплантацией клеток-предшественников периферической крови или костного мозга.
Таблица 1
Характеристика больных
Степень распространённости по системе TNM
Материалы и методы. В исследование включена 51 больная. Критериями включения были: отёчно-инфильтративная форма рака (T4d — 13), узловая форма с отёком кожи, занимающим более половины поверхности железы (31), либо наличие метастатического поражения надключичных лимфатических узлов на стороне поражения (7). Исключались больные, имевшие отдалённые метастазы других локализаций.
Сокращения в схеме:
CAF — химиотерапия циклофосфаном, доксорубицином и 5-фторурацилом;
CMF — химиотерапия циклофосфаном, метотрексатом и 5-фторурацилом,
40 Гр, 20-30 Гр — лучевая терапия в соответствующих суммарных дозах,
ВДХТ — высокодозная химиотерапия с аутотрансплантацией стволовых клеток.
Через 3 недели после химиотерапии начиналось химиолучевое лечение, включавшее лучевую терапию на молочную железу и зоны регионарного метастазирования расщепленным курсом: первый этап — 40 Гр за 4 недели, второй этап — 20-30 Гр на молочную железу и 10-20 Гр на зоны регионарного метастазирования за 2-3 недели. На протяжении последних недель облучения первого и второго этапов больным проводились 2 курса химиотерапии по схеме CMF. Интервал между этапами химиолучевого лечения составлял 2-3 недели.
Еще через 3-4 недели, в случае перевода в операбельное состояние, больным выполнялась радикальная мастэктомия в одном из её вариантов. Оперированы 46 больных. Радикальная мастэктомия по Halsted выполнена 4 больным в связи с врастанием опухоли в большую грудную мышцу, модифицированная радикальная мастэктомия (по Patey-Madden) — 40 пациенткам, модифицированная радикальная мастэктомия с одномоментной реконструкцией молочной железы поперечным ректоабдоминальным лоскутом — 2 больным.
Адъювантное лечение проводилось по одному из двух вариантов:
a) 6 курсов однодневной ХТ по схеме CAF (500/50/500 мг/м 2 ) ± эндокринная терапия (39 больных);
b) 2-3 курса однодневной ХТ по схеме CAF (500/50/500 мг/м 2 ) + высокодозная ХТ (тиофосфамид 500-600 мг/м 2 , циклофосфан 6000 мг/м 2 , карбоплатин 1200-1500 мг/м 2 ) с аутотрансплантацией клеток предшественников кроветворения ± эндокринная терапия (6 больных).
Эндокринная терапия проводилась больным с рецепторопозитивными по рецепторам эстрогенов и/или рецепторам прогестерона опухолями и состояла в выключении функции яичников (у больных репродуктивного периода) и назначении тамоксифена по 20 мг в сутки на протяжении 5 лет. Общая выживаемость вычислялась актуариальным методом от начала лечения, безрецидивная выживаемость — с момента операции.
План лучевой терапии по разным причинам выполнен не полностью у 7 больных, суммарная очаговая доза в этой группе составляла 40 Гр.
Российский онкологический научный центр им. Н.Н. Блохина РАМН
Европейское общество медицинской онкологии (ESMO)
21-23 ноября 2000 года
Российская академия государственной службы при Президенте Российской Федерации
С.М. Портной, К.П. Лактионов, А.И. Барканов, К.Л. Чимишкян, В.В. Птушкин, В.Б. Ларионова, Н.В. Жуков, М.Г. Мистакопуло, М.Ш. Ахметов.
ОПЫТ ЛЕЧЕНИЯ БОЛЬНЫХ ПРОГНОСТИЧЕСКИ ОТЯГОЩЁННЫМ МЕСТНО-РАСПРОСТРАНЁННЫМ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ.
IV ежегодная российская онкологическая конференция 21-23 ноября 2000 года, Москва, 2000, с.57-59
Российский онкологический научный центр им. Н.Н. Блохина РАМН, Москва
РМЖ — рак молочной железы
МРРМЖ — местно-распространённый рак молочной железы
ВДХТ — высокодозная химиотерапия
Отдалённые результаты лечения больных отёчно-инфильтративной формой рака молочной железы остаются неудовлетворительными. Отёчно-инфильтративная форма рака молочной железы (inflammatory breast cancer) клинико-рентгенологически характеризуется диффузным распределением опухолевой ткани в молочной железе по типу инфильтрата (без выявляемого опухолевого узла) и отёком кожи, отличается особой агрессивностью течения, выражающейся в быстром местно-регионарном распространении опухоли по лимфатической системе с быстрым развитием отдалённых метастазов.
Местное лечение (оперативное, лучевое, сочетание лучевого с оперативным) отёчно-инфильтративной формы РМЖ даёт 0-4 % 5-летней выживаемости при средней длительности жизни от 18 до 22 месяцев (1).
После эффективной предоперационной химиотерапии и радикальной операции, несмотря на проведение профилактической ХТ по схеме CMF и профилактической ЭТ, уже на первом году наблюдений рецидивы и метастазы развиваются в 50% случаев, 3-летняя безрецидивная выживаемость составляет 24%, 5-летняя — 19% (2). Сходным плохим прогнозом отличается также узловая форма рака с вторичным выраженным отёком кожи (3).
Целью настоящего исследования было изучение возможности повышения эффективности лечения путём последовательного применения химиотерапии, химиолучевой терапии, операции и адъювантной системной терапии, одним из компонентов которой является высокодозная ХТ с аутотрансплантацией клеток-предшественников периферической крови или костного мозга.
Таблица 1
Характеристика больных
Степень распространённости по системе TNM
Число больных
Материалы и методы. В исследование включена 51 больная. Критериями включения были: отёчно-инфильтративная форма рака (T4d — 13), узловая форма с отёком кожи, занимающим более половины поверхности железы (31), либо наличие метастатического поражения надключичных лимфатических узлов на стороне поражения (7). Исключались больные, имевшие отдалённые метастазы других локализаций.

Сокращения в схеме:
CAF — химиотерапия циклофосфаном, доксорубицином и 5-фторурацилом;
CMF — химиотерапия циклофосфаном, метотрексатом и 5-фторурацилом,
40 Гр, 20-30 Гр — лучевая терапия в соответствующих суммарных дозах,
ВДХТ — высокодозная химиотерапия с аутотрансплантацией стволовых клеток.
Через 3 недели после химиотерапии начиналось химиолучевое лечение, включавшее лучевую терапию на молочную железу и зоны регионарного метастазирования расщепленным курсом: первый этап — 40 Гр за 4 недели, второй этап — 20-30 Гр на молочную железу и 10-20 Гр на зоны регионарного метастазирования за 2-3 недели. На протяжении последних недель облучения первого и второго этапов больным проводились 2 курса химиотерапии по схеме CMF. Интервал между этапами химиолучевого лечения составлял 2-3 недели.
Еще через 3-4 недели, в случае перевода в операбельное состояние, больным выполнялась радикальная мастэктомия в одном из её вариантов. Оперированы 46 больных. Радикальная мастэктомия по Halsted выполнена 4 больным в связи с врастанием опухоли в большую грудную мышцу, модифицированная радикальная мастэктомия (по Patey-Madden) — 40 пациенткам, модифицированная радикальная мастэктомия с одномоментной реконструкцией молочной железы поперечным ректоабдоминальным лоскутом — 2 больным.
Адъювантное лечение проводилось по одному из двух вариантов:
a) 6 курсов однодневной ХТ по схеме CAF (500/50/500 мг/м 2 ) ± эндокринная терапия (39 больных);
b) 2-3 курса однодневной ХТ по схеме CAF (500/50/500 мг/м 2 ) + высокодозная ХТ (тиофосфамид 500-600 мг/м 2 , циклофосфан 6000 мг/м 2 , карбоплатин 1200-1500 мг/м 2 ) с аутотрансплантацией клеток предшественников кроветворения ± эндокринная терапия (6 больных).
Эндокринная терапия проводилась больным с рецепторопозитивными по рецепторам эстрогенов и/или рецепторам прогестерона опухолями и состояла в выключении функции яичников (у больных репродуктивного периода) и назначении тамоксифена по 20 мг в сутки на протяжении 5 лет. Общая выживаемость вычислялась актуариальным методом от начала лечения, безрецидивная выживаемость — с момента операции.
План лучевой терапии по разным причинам выполнен не полностью у 7 больных, суммарная очаговая доза в этой группе составляла 40 Гр.
ЯДЕРНАЯ МЕДИЦИНА ДЛЯ ПРОДЛЕНИЯ ЖИЗНИ
С помощью такой технологии удается остановить рост опухоли почти у 90% больных раком печени. Продолжительность жизни пациентов увеличивается в 2 - 3 раза по сравнению с другими стандартными методами лечения, когда радикальную операцию выполнить невозможно (радикальная операция возможна только у 20% больных). Внедрение радиоэмболизации печени в клиническую практику, как и выпуск отечественного радиофармпрепарата , позволяют существенно снизить затраты и включить этот метод в программу бесплатной медицинской помощи, подчеркивают в НМИЦ радиологии.

УБИТЬ ОПУХОЛЕВЫЕ КЛЕТКИ И АКТИВИРОВАТЬ ИММУНИТЕТ
Этот метод лечения - так называемая альфа-эммитерная брахитерапия - открывает новую страницу в борьбе со злокачественными новообразованиями, считают международные эксперты. Речь идет о разновидности лучевой терапии, при которой источник излучения вводится в опухоль и высокоточно уничтожает раковые клетки, не повреждая окружающие ткани. Уникальность альфа-частиц заключается в том, что в отличие от других известных излучений они не только разрушают клетки опухоли, но и способствуют выработке защитных свойств иммунной системы, говорит академик Каприн.
Операция длилась четыре часа. Спустя две недели пациентке удалили интродьюсеры (специальные катетеры), через которые альфа-частицы были доставлены к опухоли. Остальное должен сделать сам организм: выработать защитные механизмы для борьбы с удаленными метастазами.
- Мы надеемся, что этот метод позволит не только спасать жизнь пациенток с запущенными формами рака молочной железы, но и добраться до таких грозных заболеваний, как рак поджелудочной железы, - отметил профессор Кейсари .
ВЫРАСТИТЬ КОЖУ НА МЕСТЕ ТЯЖЕЛЫХ РАН

- Безусловно, онкология будет одной из первых областей медицины, где эта технология будет востребована, - говорит академик Каприн. - Современный уровень хирургических вмешательств, огромный арсенал прецизионных (высокоточных. - Ред.) методов облучения и спектр химиотерапевтических и таргетных препаратов позволяет сегодня добиться излечения большого количества онкологических больных. Однако качество жизни после такого агрессивного лечения может серьезно страдать из-за потери или нарушения функций органов. Мы возлагаем большие надежды на 3D-биопринтинг как на технологию создания фрагментов органов из живых элементов.
ОНКОПАТРУЛЬ ШАГАЕТ ПО СТРАНЕ
ЦИФРЫ
16 случаев онкологических заболеваний и еще 100 других патологий были выявлены на ранних стадиях, когда высоки шансы на успешное лечение болезни.
В ТЕМУ
В России появятся первый центр ионной терапии и биобанк
Одним из важных достижений прошлого года академик Каприн называет подписание российско-японского соглашения о создании первого в России центра ионной терапии. Он будет построен в Обнинске и предназначен для передовых методов лечения тяжелыми ионами углерода.

- Как возникает рак молочной железы?
- Типы рака молочной железы
- Причины и факторы риска
- Симптомы рака молочной железы
- Самостоятельная диагностика рака груди
- Диагностика
- Стадии рака молочной железы
- Лечение рака молочной железы
- Прогноз при раке молочной железы
Как возникает рак молочной железы?
Рак груди развивается так же, как и любая другая злокачественная опухоль в организме. Одна или несколько клеток железистой ткани в результате произошедшей в них мутации начинают аномально быстро делиться. Из них образуется опухоль, способная прорастать в соседние ткани и создавать вторичные опухолевые очаги — метастазы.
Мутации, которые приводят к РМЖ, бывают наследственными и приобретенными .
Распространенными наследственными генетическими причинами рака молочной железы становятся мутации в генах BRCA1 и BRCA2. Носительницы мутации BRCA1 имеют риск заболеть раком молочной железы 55–65%, а носительницы BRCA2 — 45%. Такие генетические дефекты передаются по наследству от родителей детям, они становятся причиной рака молочной железы примерно в 15% случаев.
Намного чаще опухоль возникает из-за приобретенных мутаций: они возникают в клетках молочной железы и не передаются по наследству. Например, в 20% случаев увеличено количество копий гена, кодирующего HER2 — белок-рецептор, который находится на поверхности клеток и стимулирует их размножение.
Типы рака молочной железы
Злокачественные опухоли груди делятся на два типа: протоковые и железистые. Протоковый рак молочной железы встречается чаще. Он может быть внутриэпителиальным (in situ) и инвазивным. У внутриклеточного протокового рака молочной железы более благоприятный прогноз, он редко дает метастазы и излечивается в 98% случаев. Инвазивный же вариант опухоли склонен к бесконтрольному росту и генерализации процесса.
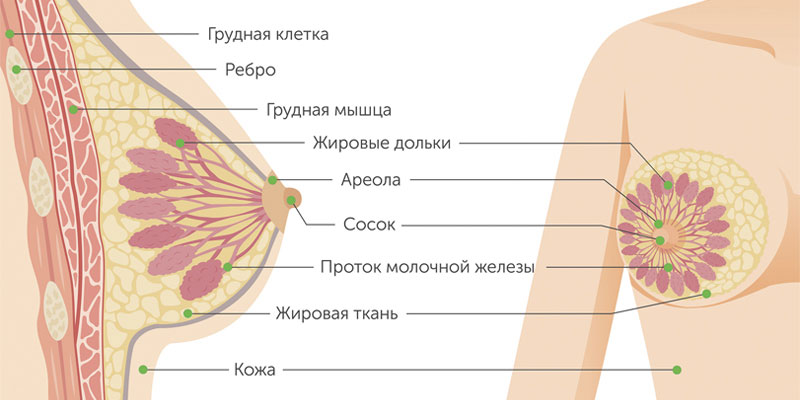
Железистый рак молочной железы может быть дольковым (инвазивная лобулярная карцинома) или произрастать из других клеток железистой ткани. Для долькового рака нередко характерен мультицентричный рост. Скорость увеличения в размерах и сроки метастазирования форм узлового рака груди зависят от степени дифференцировки опухоли.
Причины и факторы риска
К сожалению, полной информации о причинах возникновения рака молочной железы у ученых пока нет. Существует список факторов риска, влияющих на вероятность появления опухоли, однако у некоторых болезнь диагностируют при отсутствии этих факторов, другие же остаются здоровыми при наличии сразу многих из них. Тем не менее, ученые все же связывают развитие рака груди с определенными обстоятельствами, наиболее часто предваряющими его появление. К ним относятся:
- Возраст. Большинство случаев РМЖ приходятся на женщин в возрасте 55 лет и старше.
- Наследственность. Если РМЖ диагностирован у кого-то из близких родственников, риск повышается вдвое.
- Рак молочной железы в анамнезе.
- Повышенная плотность ткани молочной железы по результатам маммографии.
- Некоторые доброкачественные новообразования в молочной железе.
- Раннее начало менструаций — до 12 лет.
- Поздняя менопауза — после 55 лет.
- Отсутствие детей или поздние (после 35 лет) первые роды.
- Воздействие радиации, например, в ходе лучевой терапии, проводимой для лечения другого типа рака.
- Курение и злоупотребление алкоголем. Если женщина ежедневно потребляет 28–42 г этилового спирта, ее риски повышаются на 20%.
- Лишний вес и низкая физическая активность.
- Использование гормональных препаратов: оральные контрацептивы, заместительная гормональная терапия в постменопаузе.
- Травмы молочных желез.
- Сахарный диабет.
- Работа по графику с ночными сменами.
Симптомы рака молочной железы
На ранних стадиях рак молочной железы, как правило, никак клинически не проявляется. Чаще всего опухоль обнаруживается самими больными или выявляется случайно при проведении профилактических исследований.
Пациентки обычно жалуются на наличие пальпируемого образования, выделения из соска. Боль является редким симптомом рака грудной железы, однако болевой синдром может выйти на первый план на этапе генерализации процесса, в особенности при распространении метастазов в кости.
Довольно часто выявляются такие признаки рака груди, как появление асимметрии вследствие изменения размеров пораженной железы. Уменьшение, смещение кверху, деформация и сморщивание молочной железы может наблюдаться при скиррозной (фиброзной) форме опухоли. Напротив, увеличивается грудь на стороне поражения при быстром росте образования или из-за отека, который формируется по причине нарушенного оттока лимфы.
При распространении новообразования в подкожную клетчатку могут наблюдаться изменения кожи. При этом выявляются следующие симптомы рака молочной железы:
Иногда, при распространении опухоли на поверхность кожи могут наблюдаться такие признаки рака груди, как покраснение и изъязвление. Наличие этих симптомов говорит о запущенности процесса.
Изменения соска тоже могут определяться, но только на поздних стадиях. При этом имеют место такие симптомы рака грудной железы, как:
- Симптом Форга — на стороне поражения сосок находится выше, чем на здоровой стороне.
- Симптом Краузе — сосок утолщен, складки ареолы заметно выражены.
Такой признак рака молочной железы, как патологические выделения, является довольно редким, но в ряде случаев может быть единственным симптомом, который выявляется при осмотре. Часто выделения носят кровянистый характер, реже встречаются серозные и гнойные.
Также были выделены особые формы рака груди, которые проявляются типичной симптоматикой. К ним относятся:
- Отечно-инфильтративная форма, для которой характерно увеличение и отечность железы, мраморный цвет кожи, выраженная гиперемия.
- Маститоподобная. Данный вид рака груди проявляется уплотнением пораженной груди, повышением температуры тела.
- Рожистоподобная форма, при которой на коже выявляются очаги (иногда появляются изъязвления), которые внешне напоминают рожистое воспаление.
- Панцирная форма характеризуется наличием множественных узлов, за счет которых происходит сморщивание и деформация железы.
- Рак Педжета — поражает сосок и ареолу. При данной разновидности наблюдают утолщение соска, изменение кожи в виде покраснения и уплотнения, образование корок и чешуек.
Иногда люди, интересуясь по каким признакам можно распознать наличие опухоли молочной железы, по ошибке ищут симптомы рака грудины. Данное название является неверным, так как грудина является центральной плоской костью грудной клетки и даже при метастазировании злокачественного образования груди практически никогда не поражается.
Самостоятельная диагностика рака груди
Самостоятельно проверять грудь на наличие узелков или каких-либо других изменений стоит раз в месяц после менструации. Домашнюю диагностику удобнее всего проводить, принимая ванну или находясь под душем. О любых изменениях, которые удалось обнаружить, стоит как можно быстрее рассказать врачу.
Порядок проведения самообследования молочных желез:
- Разденьтесь выше пояса и встаньте перед зеркалом.
- Поднимите руки вверх и заведите их за голову. Внимательно осмотрите грудь. Повернитесь правым, левым боком.
- Ощупайте молочные железы в положении стоя сложенными указательным, средним и безымянным пальцем. Начинайте с верхней наружной части груди и двигайтесь по часовой стрелке.
- Сожмите сосок двумя пальцами. Проверьте, выделяется ли из него что-нибудь.
- Снова ощупайте молочные железы — теперь в положении лежа.
70% случаев рака молочной железы выявляются пациентами самостоятельно в результате самообследования груди.
Диагностика
Диагностика рака молочной железы начинается с беседы. На этом этапе для врача важно оценить жалобы женщины и выяснить, встречались ли случаи рака молочной железы в её семье, если да — насколько часто. Это помогает заподозрить наследственную форму рака, связанную с мутациями в генах BRCA1, BRCA2, NBS1, CHECK, TP53.
Далее врач осматривает, ощупывает молочные железы, проверяет, нет ли в них узлов и уплотнений, не увеличены ли лимфатические узлы в подмышечной, надключичной и подключичной областях.
После осмотра врач может направить женщину на маммографию — рентгенографию молочной железы. Показаниями к этому исследованию являются: уплотнения в молочной железе, изменения со стороны кожи, выделение крови из соска, а также любые другие симптомы, которые могут указывать на злокачественную опухоль. Также для диагностики рака молочной железы назначают ультразвуковое исследование. Маммография и УЗИ являются взаимодополняющими методами, каждый из них имеет свои преимущества:
Маммография
УЗИ молочных желез
Позволяет обнаружить патологические изменения за 1,5–2 года до появления симптомов.
При кровянистых выделениях из соска можно провести дуктографию — рентгенографию с контрастированием молочных протоков. Это помогает получить дополнительную полезную информацию.
Высокая чувствительность — точная диагностика до 90% случаев рака.
Возможность обнаружить микрокальцинаты до 0,5 мм.
Безопасность — нет воздействия на организм рентгеновскими лучами.
Хорошо подходит при высокой плотности ткани молочной железы, у молодых женщин (до 35–45 лет).
Позволяет отличать кисты (полости с жидкостью) от плотных опухолей.
Позволяет оценить состояние регионарных лимфатических узлов.
Хорошо подходит для контроля положения иглы во время биопсии.
Магнитно-резонансная томография — высокоинформативный метод диагностики злокачественных опухолей молочной железы. Ее применяют при лобулярном раке, когда неинформативны маммография и УЗИ, а также для оценки размеров и расположения опухоли, что помогает определиться с тактикой хирургического лечения. МРТ может применяться для скрининга у женщин-носительниц аномальных генов, связанных с повышенным риском рака молочной железы, при отягощенном семейном анамнезе.
О роли биопсии в диагностике рака молочной железы рассказывает врач Европейской клиники Портной С.М.:

В лаборатории проводят цитологическое и гистологическое исследование, то есть оценивают строение отдельных клеток и ткани. В настоящее время доступны молекулярно-генетические исследования: они помогают выявить мутации, за счет которых произошло злокачественное перерождение, и подобрать оптимальную противоопухолевую терапию.
Биопсия позволяет выяснить, является ли опухоль злокачественной, а также определить ее тип и стадию. Кроме того, исследование биопсийного материала дает ответ на вопрос, является ли опухоль гормонозависимой , что также влияет на схему лечения.
После того как рак диагностирован, важно определить его стадию и понять, насколько сильно он распространился в организме. Для этого применяют следующие исследования:

Стадии рака молочной железы
Стадирование при раке молочной железы опирается на общепринятую систему TNM. Буква T в этой аббревиатуре обозначает размер первичной опухоли:
Буквой N обозначают наличие метастазов в регионарных лимфатических узлах. N0 — очаги в лимфатических узлах отсутствуют. N1, N2 и N3 — поражение разного количества лимфатических узлов.
Буква M обозначает наличие отдаленных метастазов. Рядом с ней может быть указана одна из двух цифр: M0 — нет отдаленных метастазов, M1 — отдаленные метастазы имеются.
В зависимости от значений T, N и M, выделяют пять основных стадий рака молочной железы (внутри некоторых из них есть подстадии):
- Стадия 0: рак на месте.
- Стадия I: опухоль в молочной железе диаметром до 2 см.
- Стадия II: опухоль в молочной железе диаметром до 5 см и более, могут быть метастазы в подмышечных лимфоузлах на стороне поражения.
- Стадия III: опухоль в молочной железе до 5 см и более, может прорастать в грудную стенку или в кожу, имеются очаги в регионарных лимфатических узлах.
- Стадия IV: опухоль может быть любых размеров, не имеет значения, поражены ли регионарные лимфоузлы. Если обнаруживают отдаленные метастазы, всегда диагностируют рак четвертой стадии.
Лечение рака молочной железы
Стратегия лечения рака молочной железы должна подбираться индивидуально для каждой пациентки с учетом таких факторов, как тип опухоли, стадия, чувствительность новообразования к гормональной терапии. Берется во внимание и общее состояние больной. Если опухоль обнаружена на ранних стадиях и выбрана правильная тактика ведения пациентки, то шанс полностью вылечить рак груди является весьма высоким.
Выберите врача-онколога и запишитесь на приём:

Пластический хирург, онколог-маммолог, доктор медицинских наук
Читайте также:

