Химиотерапия при раке поперечной ободочной кишки
Здравствуйте! Маме 49 лет 1960 года рождения поставили диагноз аденокарцинома.Весит 66 килограмм при росте 1,65 метров.
Диагноз основной Са поперечной ободочной кишки T4N1M0 IIIB ст., Dukes'C
23.01.09 проведена операция расишренная правосторонняя гемиколэктомия. Послеоперационный
период протекал без осложнений.
Гистологическое заключение. Умеренно/низкодифференцированная аденомокарционма толстой кишки
с выраженным воспалением высокой митотической активностью, прорастает все слои стенки.
Края резекции: Полнокровие сосудов. В прилежащей клетчатке из 20 л.у. в 1 - MTS а
аденокарцинома аналогичного строения; в остальных - отек, реактивная гиперплазия лимфоидной
ткани. Тонкая кишка - без особенностей; червеобразный отросток: фиброз,
липоматоз подслизистого слоя. В резецированном большом сальнике полнокровие сосудов,
очаговые кровоизлияния.
Кл. ан. крови: Hb - 126г/л; Er-4.81x10^12/л; ЦП-0,78; L-6,9x10^9/л; п-3; с-62; э-4;м-3;
б-1; л-27.
Общий ан. мочи: желт., прозр, сл. мутн., 1001, б-0, лей.-6-8 в п/зр., эр-0 в п/зр., слизь-,
бактерии -.
Б/х ан. крови: билирубин-26-16-10; глюкоза-4,8; остаточный азот-27,0; мочевина-9,0;
АСТ-0,7; АЛТ-0,9; общий белок-68,0 г/л; креатинин-94,0; К(верхний индекс +)-5,3; Na(верхний индекс +)-154,0;
Сl (верхнйи индекс - )-100,0, альбумин - 34,2.
УЗИ органов брюшной полости: без особенностей.
ФГДС: При исследовании пищевдоа, желудка и 12 п.к. патологических изменений не выявлено.
ЭКГ: Синусовая тахикардия, 100 в минуту. Вариант нормы.
Rg органов грудной клетки: в пределах возрастных изменений.
Консультация химиотерапевта: С учетом стадии заболевания, возраста больной показано проведение
химиотерапевтического лечения по схеме de Gramount.
Потом отправили на повторную гистологию. реузльтаты исследования. Низкодифференцированная аденокарцинома толстой кишки,
прорастающая мышечную оболочку, с участком солидного строения, розеткоподобными структурами, клетками среднего размера,
небольшими ядрами с дисперстным хроматитом, невыраженной эозонфильной цитоплазмой. В краях резекции опухоли не обнаружено.
Метастаз в 1 из 16 лимфоузлов. Для исключения нейроэндокринного компонента рекомендуется иммунгистохимическое исследование.
2 фрагмента жировой клетчатки без опухоли. аппендикс обычного строения.
Далее отправили на Компьютерную томографию.
КТ установка "COMATOM-APT" Область исследования: грудная клетка, живот таз.
Дата обследования 5.02.09
Очаговые и инфильтративные изменения в легких не определяются. Сердце аорты возрастные изменения.
Печень неувеличена. плотность ткани + 54+62едН (N+50+70). Желчный пузырь небольших размеров, однородной структуры.
Поджелудочная железа неувеличена. Холедох, вирсунгов, внутрипеченочные желчные протоки
не расширены. Селезенка 10,2х3,1 см. обычного строения. Надпочечники - N. Почки - соотшношение
паренхимы и полостной системы не нарушено, несколько опещены, Мочевой пузырь без особенностей.
Матка 5,5х5 см. Увеличенние Х лимфатических узлов патологических образований не выявлено.
Над, под печенью, селезенкой, в полости м. таза незначительное количество жидкости.
Постинъекционные объевестлвления в легких тканях ягодиц.
ПОчерк немного непонятный, поэтому некоторые слова разобрал,наверное, неправильно.
Сдали анализ на РЭА на 21 день после операции. РЭА - 1,95 нг/мл.
1)Оптимальная ли подобрана схема химиотерапии (de Gramount)?
2)Как Вы можете прокомментировать нашу ситуацию?
3)Думаем еще о подкожном порте, чтобы не сжечь вены. Какие могут быть осложнения с этим портом?
4)Еще мы слышали о такой схеме как FOLFOX, в которую входит Элоксатин. Где его можно купить? Вообще, реально ли это?
5)Может быть, у вас есть какая-то информация по поводу того, появится ли он в ближайшее время
В Санкт-Петербурге в виде бесплатного обеспечения гражданам?
6)И что это за иммунгистохимическое исследование?
Толстая кишка – это конечная часть пищеварительного тракта. В ней выделяют два отдела: ободочную (colon) и прямую кишку (rectum). Все злокачественные опухоли толстой кишки называют еще колоректальным раком (КР).
Карцинома толстой кишки уверенно выходит на лидирующие позиции в структуре онкологической заболеваемости. За десять лет частота выявления выросла на 20% и в настоящий момент данная патология занимает третье место среди всех злокачественных новообразований.
Основным методом лечения рака кишечника остается операция. Однако более половины впервые выявленных опухолей толстой кишки – это злокачественные новообразования 3-й или 4-й стадии, при которых одна операция неэффективна. Необходимо еще воздействие на опухолевые клетки, которые уже успели распространиться по организму.
Химиотерапия – важный компонент комбинированного лечения КР. Статистика убедительно показывает, что применение химиопрепаратов увеличивает пятилетнюю выживаемость на 5-10%. Кажется, что цифры небольшие, однако в абсолютных значениях это выливается в сотни и тысячи человеческих жизней.
Химиотерапия — цели и точки приложения
Раковая опухоль представляет собой автономную колонию клеток, утратившие все свои функции кроме размножения и не подчиняющиеся регуляторным сигналам организма. В результате мутации клетка начинает бесконтрольно делиться. Опухоль растет, увеличиваясь в размерах. Но основное ее коварство в том, что раковые клетки способны распространяться по лимфатическим, кровеносным сосудам далеко за пределы первичной локализации и формировать новые колонии.

Задачи химиотерапии – уничтожить или хотя бы замедлить рост новообразования, предотвратить распространение оставшихся после операции злокачественных клеток, уменьшить или стабилизировать опухолевые очаги для их дальнейшего удаления.
Для этих целей применяются препараты цитотоксины и цитостатики. Первые вызывают непосредственно некроз клеток, воздействуя токсически на их мембрану и ядро. Вторые – блокируют механизм деления.
Химиопрепараты действуют негативно на все клетки, но в первую очередь на те, которые обладают высоким метаболизмом и способностью к быстрому делению. Поэтому при химиотерапии токсические эффекты препаратов неизбежны. Задача онкологов – подобрать такой режим, при котором польза от лечения будет превалировать над вредом. Задача пациента – настроиться на длительную борьбу и иметь мотивацию перетерпеть все возможные побочные эффекты.
Химиотерапия назначается курсами, между которыми должно пройти время для восстановления поврежденных клеток. Перерыв между циклами обычно составляет 2-3 недели.
Необходимый объём обследований
Лекарственное лечение планирует и назначает врач-химиотерапевт. Для принятия решения он должен иметь перед собой полную информацию о самой опухоли, и о состоянии пациента:
- данные колоноскопии;
- КТ легких, органов брюшной полости, МРТ малого таза;
- заключение о гистологической структуре опухоли (данные нативной биопсии или уже удаленного в ходе хирургического вмешательства макропрепарата);
- протокол операции;
- общий анализ крови и мочи;
- биохимические показатели;
- коагулограмма;
- ЭКГ;
- данные молекулярно-генетического исследования биоптата (7 мутаций в гене KRAS);
- уровень онкологических маркеров КР (РЭА, СА19.9);
- заключения врачей-специалистов при наличии у больного сопутствующих заболеваний.
При необходимости могут быть назначены дополнительные обследования: ПЭТ-КТ, сцинтиграфия костей скелета, МРТ головного мозга и др.
Противопоказания к химиотерапии
- Нейтропения (снижение количества лейкоцитов в крови).
- Текущие инфекционные заболевания.
- Выраженная кахексия.
- Печеночная или почечная недостаточность.
- Тяжелая нейропатия.
- Возраст старше 75 лет (относительное противопоказание).
Показания
Химиотерапия при раке кишечника назначается в случае 3-й стадии (с наличием злокачественных клеток в регионарных лимфоузлах), 4-й стадии (с отдаленными метастазами), а также 2-й ст. при наличии некоторых неблагоприятных факторов прогноза, а именно:
- прорастание опухолью серозной оболочки кишки (Т4);
- низкая дифференцировка по данным гистологического исследования;
- поражение краев резекции, сомнения в радикальности хирургического вмешательства;
- экстрамуральное прорастание сосудов;
- операция, выполненная в условиях осложнения (кишечная непроходимость, перитонит, перфорация кишки);
- повышение уровня РЭА (раково-эмбрионального антигена) через 4 недели после оперативного лечения;
- при высоких показателях микросателлитной нестабильности (MSI).
Виды химиотерапии при колоректальном раке
- Адъювантная (послеоперационная).
- Неоадъювантная (предоперационная).
- Паллиативная.
При 2-й и 3-й стадиях КР дополнительное лечение должно быть назначено как можно раньше после хирургического (оптимально – в течение 4-х недель).
Основные препараты, применяемые при лечении рака кишечника уже достаточно длительное время – это фторпиримидины Фторурацил(5-ФУ) (с его усилителем Лейковорином (ЛВ) — вводится инфузионно; а также капецитабин — принимается внутрь в виде таблеток.
Фторпиримидины применяются или самостоятельно, или в сочетании с другими цитостатиками:
- 5-ФУ+ЛВ+Оксалиплатин (схемы FLOX, FOLFOX).
- Схема XELOX (Оксалиплатин + Капецитабин).
- Схема FOLFIRI (5-ФУ+ЛВ+иринотекан).
Комбинации введения, продолжительность курса, дозы препаратов подбираются индивидуально. Они зависят от опыта применяемых схем в каждой конкретной клинике, а также от наличия тех или других препаратов. Наиболее распространенные режимы: 5 дней подряд каждого месяца или 1-2 дня каждые 2 недели.
Обычная длительность химиотерапии – 6 месяцев, имеются данные исследований, что 3-х месячный курс по схеме XELOX обладает не меньшей эффективностью.
По поводу продолжительности поддерживающего лечения после основного курса ХТ у онкологов пока нет единого мнения.
Наблюдение при проведении адъювантной химиотерапии:
- Перед каждым курсом ХТ сдаются анализы крови, мочи, биохимические показатели.
- 1 раз в 2-3 месяца – УЗИ брюшной полости.
- Через 6 месяцев –КТ органов брюшной полости и грудной клетки.
- Исследование на онкомаркеры – 1 раз в 3 месяца. Во время проведения курса лечения значения показателей могут повышаться, важна оценка их концентрации в динамике. Существенный критерий эффективности – снижение онкомаркеров после окончания курса.
Наиболее часто такое лечение в комбинации с лучевым (химиолучевая терапия) проводится при местнораспространенном раке прямой кишки 2-3 стадии, расположенном в нижнеампулярном отделе. Применяются фторпиримидины одновременно с лучевым воздействием. Курс – около 4-х недель.
Следующим этапом выполняется контрольное обследование, обязательно включающее в себе МРТ малого таза и, если это возможно, хирургическое вмешательство , затем после небольшого перерыва химиолучевое лечение продолжается.
4 стадия КР характеризуется метастазированием в другие органы. Наиболее часто отсевы идут в печень, легкие, а также распространяются по брюшине, реже – в другие органы (кости, головной мозг).
При раке кишечника 4 стадии химиотерапия – основной метод лечения. Выделяют следующие группы таких пациентов:
- Имеются изолированные резектабельные метастазы в печени или легкое. Удаляется первичная опухоль и одновременно или несколько отсрочено резецируются метастазы. После операции проводится химиотерапия схемами FOLFOX или XELOX.
- Потенциально резектабельные метастазы. Применяются схемы FOLFOX, XELOX, FOLFIRI 4-6 курсов, затем – операция и продолжение ХТ после вмешательства.
- Множественные нерезектабельные метастазы. Проводится паллиативная химиотерапия фторпиримидинами или вышеуказанными схемами в зависимости от переносимости. Паллиативная ХТ призвана замедлить рост опухоли и метастазов, увеличить продолжительность и улучшить качество жизни пациента.
Проводится она непрерывно до конца жизни, или же в течение полугода с последующим наблюдением (четких рекомендаций по этому поводу нет). При прогрессировании процесса или выраженном токсическом эффекте ХТ прекращается.
Таргетная терапия при колоректальном раке
Химиотерапию рекомендуется дополнять таргетными препаратами. Это различные биологические вещества, которые блокируют сложную схему митотической активности опухолевых клеток. Они направлены против конкретных молекул, которые стимулируют бесконтрольное их деление. Этот механизм связан с определенными генными мутациями, которые выявляются не у всех опухолей даже одинакового гистологического типа

Поэтому для назначения таргетных препаратов необходим сложный молекулярно-генетический анализ карциномы.
- Антитела к EGFR – Цетуксимаб и Панитумумаб.
- Моноклональное антитело к VEGF- Бевацизумаб.
Исследования показали, что монотерапия только МКА при аденокарциноме кишечника неэффективна. Такие препараты добавляются к стандартным схемам ПХТ у пациентов с 4-й стадией колоректального рака. Комбинация ХТ с моноклональными антителами достоверно увеличивает период безрецидивного течения на 10-15%.
Для определения прогноза и отбора пациентов на лечение таргетными препаратами анализируют патологические изменения в генах KRAS(7 мутаций) и BRAF. Опухоли с мутациями в гене KRAS плохо отвечают на терапию анти- EGFR-антителами, но при этом не исключается применение Бевацизумаба.
Осложнения и методы их предотвращения
Химиотерапия при аденокарциноме кишечника так же, как и любое лечение, сопряжена с неизбежными побочными эффектами.
- Угнетение костного мозга, снижение количества лейкоцитов, тромбоцитов в крови.
- Поражение слизистой полости рта – образование язв, стоматит.
- Тошнота, диарея.
- Выраженная слабость, утомляемость.
- Выпадение волос.
- Носовые кровотечения.
- Сухость кожи и различные высыпания, эритема ладоней и подошв.
- Нарушение чувствительности конечностей.
- Повышение температуры.
- Инфекционные осложнения вследствие снижения иммунитета.
Чтобы несколько нивелировать неприятные последствия ХТ рекомендуется питание с повышенным содержанием белковосодержащих продуктов и овощей, применение гепатопротекторов, противорвотных препаратов. Пищу следует принимать небольшими порциями, питье не ограничивать.
При выраженных симптомах рекомендуется снизить дозу химиопрепарата на 50% или временно отменить один из них.
Критерии эффективности химиотерапии
- положительным ответом опухоли на лекарственную терапию является уменьшение суммы всех наибольших диаметров оцениваемых очагов новообразования на 30% и более;
- прогрессией считается увеличение этого показателя на 20% и выше;
- стабилизация — все промежуточные значения.
Заключение
Более половины пациентов с колоректальным раком нуждаются в проведении химиотерапии.
Такое лечение достоверно увеличивает продолжительность жизни, уменьшает вероятность рецидивов, иногда может привести к полному регрессу заболевания.
Препараты, применяемые при ХТ – токсичны. Лечение неизбежно сопряжено с побочными эффектами.
Неблагоприятное действие цитостатиков на организм – не повод для отказа от лечения. Почти все эффекты можно облегчить с помощью нелекарственных и лекарственных методов.

По частоте рак ободочной кишки занимает 2-3 место среди злокачественных новообразований желудочно-кишечного тракта. В последние годы отмечается рост заболеваемости раком ободочной кишки в России, странах Европы и США. Преимущественно заболевают лица в возрасте 40-60 лет. Среди эпителиальных злокачественных опухолей на аденокарциному приходится 60-70%, солидный рак — 10-12%, слизистый рак — 12-15%. Наиболее часто (до 70%) опухолью поражаются сигмовидная и слепая кишки.
Прогноз заболевания и выживаемость больных напрямую связан со стадией процесса в момент установления диагноза.
Основным методом лечения рака ободочной кишки является хирургический. Характер и объем вмешательства зависят от локализации и распространения опухоли, осложнений опухолевого процесса и общего состояния больного. 5-летняя выживаемость после радикальных операций — около 70%.
Паллиативные резекции ободочной кишки, произведенные с целью ликвидации непроходимости и ее профилактики, а также обходные анастомозы, колостомы при отдаленных метастазах продлевают жизнь больных и улучшают ее качество. В последние годы все чаще проводится хирургическое удаление единичных метастазов в легкие и яичники, печень.
При метастазах рака ободочной кишки в печень хирургическое вмешательство является предпочтительным методом лечения. Только активная хирургическая тактика может значительно продлить жизнь больных, 5-летняя выживаемость у таких пациентов составляет 20-40%. При невозможности выполнить хирургическое удаление метастазов в печени используют метод эмболизации и химиоэмболизации воротной вены и печеночной артерии. Кроме того, используется криодеструкция метастазов под контролем интраоперационного УЗИ. Показатели выживаемости после применения этих методов выше, чем после системной или регионарной химиотерапии.
Лучевая терапия малоэффективна, однако проводится с паллиативной целью, в частности при поражении забрюшинных или периферических лимфоузлов.
Рак ободочной кишки является относительно резистентной к воздействию цитостатиков опухолью. В течение длительного времени единственным препаратом, активным при этом заболевании, был антиметаболит из группы фторпроизводных пиримидина — фторурацил (5-ФУ), вошедший в клиническую практику еще в 1960-е годы. Эффективность его не превышает 10-15%, причем чаще удается достигнуть лишь частичных регрессий продолжительностью 4-6 мес. Позже был создан препарат для перорального применения — тегафур (Фторафур), который по существу является транспортной формой 5-ФУ. Биохимическая модуляция 5-ФУ и тегафура с помощью фолината кальция (Лейковорин) позволила увеличить их противоопухолевую активность до 20-30%.
В последнее десятилетие в клиническую практику вошли новые цитостатики из группы антиметаболитов — УФТ (тегафур/урацил), так же как и тегафур, создающий постоянный уровень 5-ФУ в сыворотке крови, и капецитабин (Кселода), трансформирующийся в 5-ФУ в опухоли, а также прямой ингибитор тимидилатсинтетазы — ралтитрексид (Томудекс). Рак ободочной кишки оказался чувствителен к цитостатикам с оригинальным механизмом действия — к ингибитору топоизомеразы 1 иринотекан (Кампто) и производному платины 3 поколения оксалиплатину (Элоксатин). Использование этих препаратов в монорежиме и в составе лекарственных комбинаций расширило возможности химиотерапии рака ободочной кишки, увеличив ее эффективность. Однако 5-ФУ не потерял своего значения, оставаясь основой лекарственной терапии рака ободочной кишки. В современных терапевтических режимах чаще всего используют длительные (22-48 ч) инфузии 5-ФУ с фолинатом кальция (Лейковорин), вводимые еженедельно или раз в 2 нед. Такой режим имеет преимущества как по непосредственной эффективности, так и по выживаемости больных. Как правило, все режимы комбинированной химиотерапии с использованием новых цитостатиков строятся на основе 5-ФУ. В ряде случаев они оказываются эффективны при резистентности к 5-ФУ с фолинатом кальция.
Изучается целесообразность использования таргетных препаратов бевацизумаба и цетуксимаба в комбинированной химиотерапии метастатического колоректального рака, показана эффективность комбинации FL + бевацизумаб. Химиотерапия у больных с 4 стадией или рецидивом заболевания используется с паллиативной целью. Последовательное использование наиболее эффективных терапевтических режимов увеличивает выживаемость больных (медиана 20 мес.). Помимо системной, при изолированном метастатическом поражении печени, применяется регионарная внутриартериальная химиотерапия. Давая больший непосредственный эффект, она не приводит к увеличению выживаемости.
В результате многочисленных исследований установлено, что применение комбинации фторурацил + фолинат кальция (Лейковорин) в течение 6 мес. после радикальных операций при 3 стадии рака ободочной кишки на 15-20% увеличивает 5-летнюю выживаемость. Этот режим используется в качестве стандартного адъювантного лечения для данной группы пациентов.
РЕЖИМЫ ХИМИОТЕРАПИИ
Монохимиотерапия
Фторурацил — 2600мг\м2 24-часовая в\в инфузия еженедельно до токсичности.
Тегафур (Фторафур) -800-1000мг\м2 внутрь ежедневно (доза делится на 2 приема) до суммарной дозы 30г. Повторный курс через 3-4 нед.
УФТ (тегафур\урацил) — 400 мг\м2 внутрь (доза делится на 2-3 приема) ежедневно в течение 3-4 нед. Повторные курсы через 1-2 нед.
Капецитабин — 2500 мг\м2 внутрь (доза делится на 2 приема) ежедневно в течение 2 нед. Повторные курсы через 1-2 нед.
Ралтитрексид (Томудекс) — 3,0-4,5мг\м2 в\в 15-минутная инфузия. Повторные курсы через 3 нед.
Иринотекан (Кампто) — 350 мг\м2 в\в 1-часовая инфузия. Повторные курсы через 3 нед. Или иринотекан (Кампто) — 125 мг\м2 90-минутная в\в инфузия еженедельно в течение 4 нед. Повторный курс через 2 нед.
Комбинированная химиотерапия
Фторурацил -500 мг\м2 в\в в 1,8,15,22,29,36-й день.
Фолинат кальция (Лейковорин) — 500 мг\м2 в\в в виде 2-часовой инфузии за час до введения фторурацила в 1, 8, 15, 22, 29, 36-день.
Интервал между циклами 2 нед.
Фторурацил — 425 мг\м2 в\в в1, 2, 3, 4, 5-й день.
Фолинат кальция (Лейковорин) — 20-30 мг\м2 струйно или 2-часовая в\в инфузия перед введением фторурацила в 1, 2, 3, 4, 5-й день.
Повторные курсы через 3 нед.
Митомицин — 8-10 мг\м2 в\в в 1-й день.
Фторурацил — 425 мг\м2 в 1, 8, 15, 22, 29, 36-й день, в\в в 2, 3, 4, 5-й день.
Повторные курсы через 3-4 нед.
FOLFOX
Иринотекан (Кампто) — 100 мг\м2 в\в капельно в 1-й день.
Фолинат кальция (Лейковорин) — 200 мг\м2 + фторурацил 400 мг\м2 в\в струйно 1, 8, 15, 22 дни каждые 6 нед.
Повторный курс через 1 нед.
FOLFIRI
Иринотекан (Кампто) — 180 мг\м2 в\в капельно в 1-й день.
Фолинат кальция (Лейковорин) — 200 мг\м2 в\в в 1-й день.
Фторурацил — 400 мг\м2 в\в струйно в 1-й день, затем
Фторурацил — 2,4-3,0 г\м2 24-часовая в\в инфузия.
Повторные курсы через 2 нед.
XELOX
Оксалиплатин 130 мг\м2 в\в -1 день.
Капецитабин 2000 мг\м2 \сутки (разделив на 2 приема) 1-14 дни.
В качестве адъювантной послеоперационной химиотерапии при 3 стадии заболевания используется следующий режим:
Фторурацил ( 425 мг\м2 в\в 5 дней) + фолинат кальция (Лейковорин) (20 мг\м2 в\в 5 дней).
Повторные курсы каждые 4-5 недель. Лечение в течение 6 мес.
Фолинат кальция (Лейковорин) — 500 мг\м2 2-часовая в\в инфузия.
Фторурацил — 500 мг\м2 в 1, 8, 15, 22, 29, 36-день в\в струйно через час после начала инфузии фолината кальция.
Повторные курсы через 2 нед. Всего проводится 4 курса.
FOLFOX (см. выше).
Повторение курса каждые 2 недели, в течение 6 мес.

Ободочная кишка составляет примерно 4/5 от общей длины толстой кишки. В ней выделяют четыре отдела: восходящую, поперечную, нисходящую и сигмовидную ободочную кишку. Последняя переходит в прямую кишку.
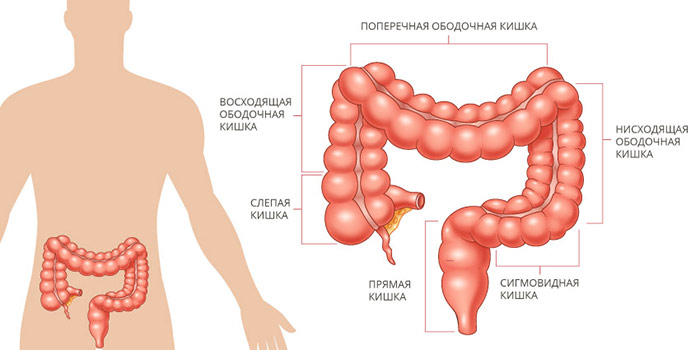
Обычно возникновению злокачественной опухоли ободочной кишки предшествует возникновение доброкачественного новообразования — полипа. Существуют разные типы полипов, они обладают различным потенциалом к озлокачествлению. Риски повышаются с возрастом, поэтому всем, кому 50 лет и больше, рекомендуется проходить скрининговое эндоскопическое исследование — колоноскопию.
В зависимости от того, в каком анатомическом отделе возникла опухоль, выделяют рак в поперечной ободочной кишке, восходящей и нисходящей, сигмовидной.
- Причины развития рака ободочной кишки
- Классификация
- Стадии рака ободочной кишки
- Как происходит метастазирование рака из ободочной кишки?
- Симптомы
- Осложнения рака ободочной кишки
- Методы диагностики
- Методы лечения
- Прогноз
Причины развития рака ободочной кишки
Нельзя точно сказать, почему у конкретного человека в ободочной кишке возникла злокачественная опухоль. Рак всегда является результатом определенного набора мутаций в клетке, но что к этим мутациям привело — вопрос, на который сложно ответить.
Выделяют некоторые факторы риска, которые повышают вероятность развития колоректального рака:
Ни один из этих факторов не вызовет рак ободочной кишки со стопроцентной вероятностью. Каждый из них лишь в определенной степени повышает риски. На некоторые из этих факторов можно повлиять, например, начать правильно питаться, отказаться от алкоголя и сигарет, заняться спортом.
Классификация
Самая распространенная разновидность рака ободочной кишки и вообще колоректального рака — аденокарцинома. Она развивается из железистых клеток, которые находятся в слизистой оболочке. Аденокарциномами представлено более 96% злокачественных новообразований толстой кишки. В этой группе опухолей выделяют ряд подгрупп. Наиболее агрессивные из них — муцинозный и перстневидноклеточный рак. Такие пациенты имеют самый неблагоприятный прогноз.
Стадии рака ободочной кишки
Рак ободочной кишки классифицируют по стадиям, в зависимости от размеров и глубины прорастания первичной опухоли (T), наличия очагов в регионарных лимфатических узлах (N) и отдаленных метастазов (M). Выделяют пять основных стадий:
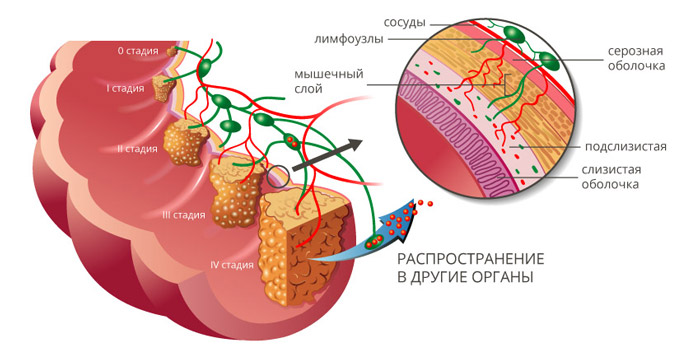
Как происходит метастазирование рака из ободочной кишки?
Рак ободочной кишки может распространяться в другие органы разными способами:
Чаще всего метастазы при раке толстой кишки обнаруживаются в легких и печени, реже — в костях, головном мозге.
Симптомы
Рак толстой ободочной кишки зачастую существует длительное время, не вызывая каких-либо симптомов. Но даже когда симптомы возникают, они неспецифичны и напоминают признаки многих других заболеваний. Если вас беспокоят расстройства из этого списка, скорее всего, у вас не рак, но нужно обязательно посетить врача и пройти обследование:
- запоры или диарея, которые сохраняются в течение нескольких дней;
- изменение внешнего вида стула: если он стал темным, как деготь, или тонким, как карандаш;
- примеси крови в стуле;
- после посещения туалета возникает ощущение, что кишка опорожнилась не полностью;
- боли, спазмы в животе;
- беспричинная слабость, чувство усталости, необъяснимая потеря веса.
Осложнения рака ободочной кишки
Если опухоль блокирует просвет ободочной кишки, у больного развивается кишечная непроходимость. Это состояние проявляется в виде отсутствия стула, сильных болей в животе, тошноты, рвоты, сильного ухудшения общего состояния. Больному немедленно требуется медицинская помощь, иначе может произойти некроз (гибель) участка кишки, разовьется перитонит.
Если опухоль приводит к постоянным кровотечениям, развивается анемия. Пациент становится бледным, постоянно испытывает слабость, его беспокоят головные боли, головокружения. В тяжелых случаях требуется переливание крови.
Метастазирование рака кишки в печень грозит нарушением оттока желчи и развитием механической желтухи — состояния, при котором кожа и слизистые оболочки приобретают желтоватый оттенок, беспокоит кожный зуд, боли в животе, ухудшается общее состояние. Пока не восстановлен отток желчи, становится невозможным проведение активного противоопухолевого лечения.
Состояние, при котором раковые клетки распространяются по поверхности брюшины, называется канцероматозом, при этом развивается асцит — скопление жидкости в животе. Это осложнение развивается при раке ободочной кишки стадии IVC. Асцит ухудшает состояние пациента, затрудняет лечение и резко негативно сказывается на прогнозе.
В Европейской клинике есть всё необходимое для эффективной борьбы с осложнениями злокачественных опухолей ободочной кишки. При неотложных состояниях пациенты получают лечение в полном объеме в отделении интенсивной терапии. Наши хирурги выполняют паллиативные операции, устанавливают стенты при кишечной непроходимости. При механической желтухе мы проводим дренирование, стентирование желчевыводящих путей. При асците наши доктора выполняют лапароцентез (эвакуацию жидкости через прокол), устанавливают перитонеальные катетеры, проводят системную и внутрибрюшинную химиотерапию.
При IVC стадии рака ободочной кишки, когда развивается канцероматоз брюшины, хирурги в Европейской клинике применяют инновационный метод лечения — гипертермическую интраперитонеальную химиотерапию (HIPEC). Удаляют все крупные опухоли, затем брюшную полость промывают раствором химиопрепарата, подогретым до определенной температуры — это помогает уничтожить мелкие очаги. Согласно результатам мировой практики, HIPEC может продлить жизнь онкологического больного до нескольких лет.
Методы диагностики
Если пациента беспокоят симптомы, которые могут указывать на рак ободочной кишки, врач первым делам назначит УЗИ органов брюшной полости и колоноскопию. Эти исследования помогут обнаружить опухоль, а во время колоноскопии можно провести биопсию — получить фрагмент патологически измененной ткани и отправить в лабораторию. Биопсия — самый точный метод диагностики рака.
После того, как рак диагностирован, нужно установить его стадию. Для этого применяют КТ, МРТ, ПЭТ-сканирование. Метастазы в легких выявляют с помощью рентгенографии грудной клетки. Если имеются метастазы в печени, применяют ангиографию — рентгенологическое исследование, во время которого в кровеносные сосуды вводят контрастный раствор.
Дополнительно врач может назначить анализ стула на скрытую кровь, общий и биохимический анализ крови, чтобы выявить анемию, оценить функции печени. Анализы крови на онкомаркеры обычно проводят в процессе лечения, чтобы проконтролировать его эффективность.
Симптомы, возникающие при раке ободочной кишки, могут беспокоить при многих других патологиях. Чаще всего злокачественную опухоль приходится дифференцировать с такими заболеваниями, как кишечные инфекции, хронические воспалительные процессы, геморрой, синдром раздраженного кишечника.
Методы лечения
При раке ободочной кишки возможны разные варианты лечения. Врач выбирает оптимальную тактику, в зависимости от стадии злокачественной опухоли, ее локализации, общего состояния пациента, наличия у него тех или иных осложнений, сопутствующих заболеваний. Выполняют хирургические вмешательства, применяют разные типы противоопухолевых препаратов, проводят курсы лучевой терапии.
Химиотерапия при злокачественных опухолях ободочной кишки может преследовать разные цели:
- Неоадъювантную химиотерапию назначают до хирургического вмешательства, чтобы сократить размеры опухоли и упростить ее удаление.
- Адъювантная химиотерапия проводится после хирургического вмешательства, чтобы уничтожить оставшиеся раковые клетки и снизить риск рецидива.
- В качестве основного метода лечения химиотерапию применяют при поздних стадиях рака, в паллиативных целях.
При злокачественных новообразованиях толстой кишки применяют разные типы химиопрепаратов: капецитабин, 5-фторурацил, оксалиплатин, иринотекан, трифлуридин/типирацил (комбинированный препарат). Чаще всего одновременно используют два или более препаратов, это помогает повысить эффективность лечения.

Таргетные препараты воздействуют более прицельно по сравнению с классическими химиопрепаратами: они направлены на определенные молекулы-мишени, которые помогают раковым клеткам бесконтрольно размножаться и поддерживать свою жизнедеятельность. Чаще всего при злокачественных опухолях кишки применяют две группы таргетных препаратов:
- Ингибиторы VEGF — вещества, с помощью которого раковые клетки стимулируют ангиогенез (образование новых кровеносных сосудов). К этой группе относятся: Зив-афлиберцепт (Залтрап), Рамуцирумаб (Цирамза), Бевацизумаб (Авастин). Их применяют при прогрессирующем раке ободочной кишки, вводят внутривенно раз в 2 или 3 недели, обычно сочетают с химиотерапией.
- Ингибиторы EGFR — белка-рецептора, который находится на поверхности раковых клеток и заставляет их бесконтрольно размножаться. В эту группу входят такие препараты, как Цетуксимаб (Эрбитукс), Панитумумаб (Вектибикс). Ингибиторы EGFR вводят внутривенно раз в неделю или через неделю.
В некоторых случаях применяют препараты из группы ингибиторов контрольных точек. Они блокируют молекулы, которые мешают иммунной системе распознавать и атаковать раковые клетки. К этой группе препаратов относятся: Пембролизумаб (Кейтруда), Ниволумаб (Опдиво), Ипилимумаб (Ервой). Обычно их применяют при неоперабельном, метастатическом раке, когда неэффективна химиотерапия, если произошел рецидив.
Колэктомия может быть выполнена открытым способом (через разрез) или лапароскопически (через проколы в брюшной стенке).
Иногда анастомоз не получается наложить сразу. В таких случаях накладывают временную колостому или илеостому — участок ободочной или подвздошной кишки подшивают к коже и формируют отверстие для отхождение стула. В дальнейшем стому закрывают.
Если опухоль блокирует просвет кишечника, и ее нельзя удалить, накладывают постоянную колостому. Проходимость кишечника можно восстановить с помощью стента — металлического каркаса в виде полого цилиндра с сетчатой стенкой. Такие операции называются паллиативными: они направлены не на удаление рака, а на борьбу с симптомами, улучшение состояния пациента.
Лучевая терапия может быть назначена до (неоадъювантная), после (адъювантная) операции на кишке или в качестве основного метода лечения при метастатическом раке, для борьбы с симптомами.
Если лучевую терапию сочетают с химиотерапией, то такое лечение называется химиолучевой терапией.
Прогноз
Основной показатель, с помощью которого определяют прогноз при онкологических заболеваниях ободочной кишки и других органов — пятилетняя выживаемость. Он показывает процентную долю пациентов, которые остались живы спустя пять лет после того, как им был установлен диагноз.
Пятилетняя выживаемость при колоректальном раке зависит от стадии:
- При локализованном раке (не распространился за пределы кишечной стенки — стадии I, IIA и IIB) — 90%.
- При раке, распространившемся на соседние органы и регионарные лимфатические узлы (стадия III) — 71%.
- При метастатическом раке (стадия IV) — 14%.
Как видно из этих цифр, наиболее успешно лечатся злокачественные опухоли ободочной кишки на ранних стадиях, а при возникновении метастазов прогноз резко ухудшается. Однако, данные показатели носят лишь ориентировочный характер. Они рассчитаны на основе статистики среди пациентов, у которых рак в толстой кишке был диагностирован пять лет назад и ранее. За это время в онкологии произошли некоторые изменения, появились новые технологии, препараты.
Никогда нельзя опускать руки. Даже при запущенном раке с метастазами больному можно помочь, продлить его жизнь, избавить от мучительных симптомов. Врачи Европейской клиники берутся за лечение любых пациентов. Мы знаем, как помочь.
Читайте также:

