Гистологической верификации опухоли что это такое
Предположить характер новообразования в организме можно благодаря клиническим и рентгенологическим симптомам, а вот определить его гистогенетическую принадлежность можно только благодаря морфологической верификации диагноза. Основной задачей такой диагностики является перепроверка онкологического диагноза для его подтверждения и подбора эффективного курса химиотерапии.
Морфологическая верификация
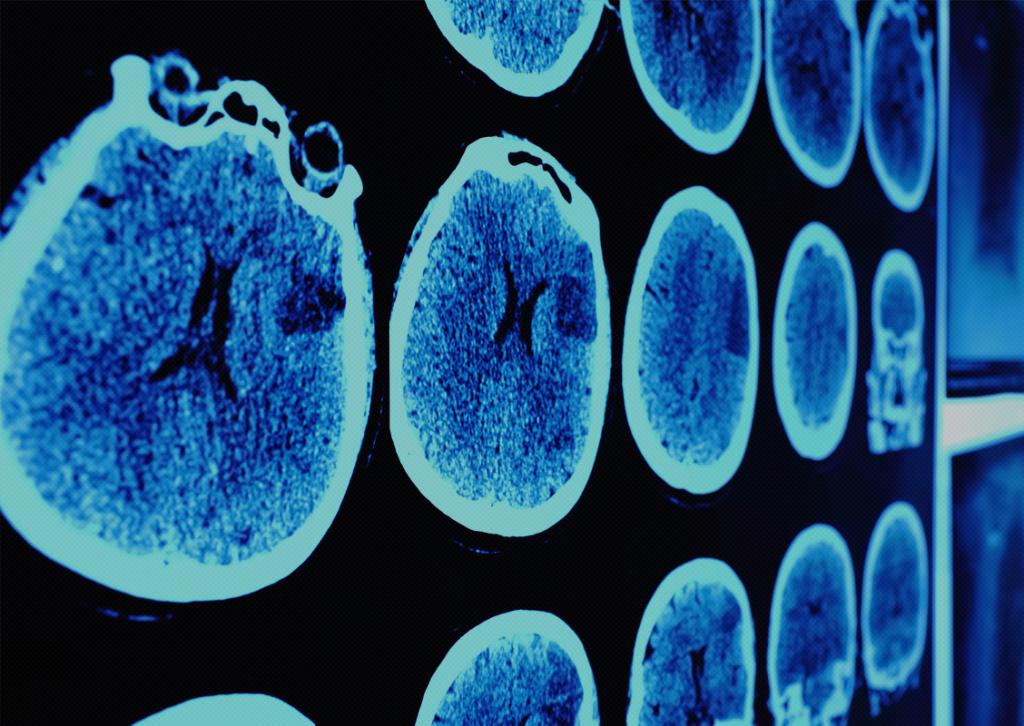
Услышав впервые от доктора о необходимости проведения морфологической диагностики, многие не имеют представления, что это и для чего проводится.
Верификация является важным исследованием, без которого невозможно принять решение о дальнейших действиях. Морфологическая верификация - это медицинская процедура, которая помогает подтвердить или опровергнуть онкологический диагноз. Чтобы провести исследование, необходимо получить материал. Его выбор в основном зависит от локализации образования. После проведения исследования специалист в зависимости от результата определяет дальнейшую тактику лечения, которая может быть консервативной или хирургической. Только после морфологического подтверждения может планироваться адекватное лечение. Показанием для проведения верификации являются объемные образования или диффузные изменения органа или его структур. Для проведения морфологического исследования забор ткани осуществляется следующим образом:
- при поверхностных изъявленных опухолях берется соскоб и мазки-отпечатки;
- при неглубоко размещенных узловых образованиях проводится пункция;
- при невозможности взятия пункции проводится биопсия с забором участка ткани;
- после неудачных попыток верификации всеми перечисленными выше методами проводится открытая биопсия.
Морфологическая верификация диагноза практически ничем не отличается от цитологической пункции. Чтобы взять материал на исследование, сначала человеку проводят анестезию мягких тканей и кожного покрова, после этого выполняется незначительный разрез кожи, через который внедряется специальный инструмент в мягкие ткани и непосредственно в ткань опухоли. Все последующие действия напрямую зависят от используемого прибора.
Методы верификации
Стандартным вариантом гистологической верификации диагноза является забор тончайших срезов биопсийных тканей для последующего микроскопического исследования. Благодаря им получается полезная информация о составе опухоли.
Морфологическая верификация опухоли проводится следующими способами:
- гистохимией;
- иммуногистохимией;
- иммунофлюоресценцией;
- иммуноферментным анализом.
Независимо от того, какая методика для проведения исследования будет выбрана, целью верификации является не только определение разновидности опухоли, но и оценка клеточных модификаций. По результатам исследования появляется возможность безошибочно принять решение и выбрать тактику лечения.
Гистохимическое исследование

С помощью гистохимической методики можно получить ценную информацию о функциональной активности образования, его типе и гистогенезе. Данный метод позволяет точно поставить диагноз и решить вопрос его дифференциальности.
В расположении гистохимии находятся многочисленные реакции, которые оказывают содействие выявлению разных классов веществ.
Иммуногистохимия
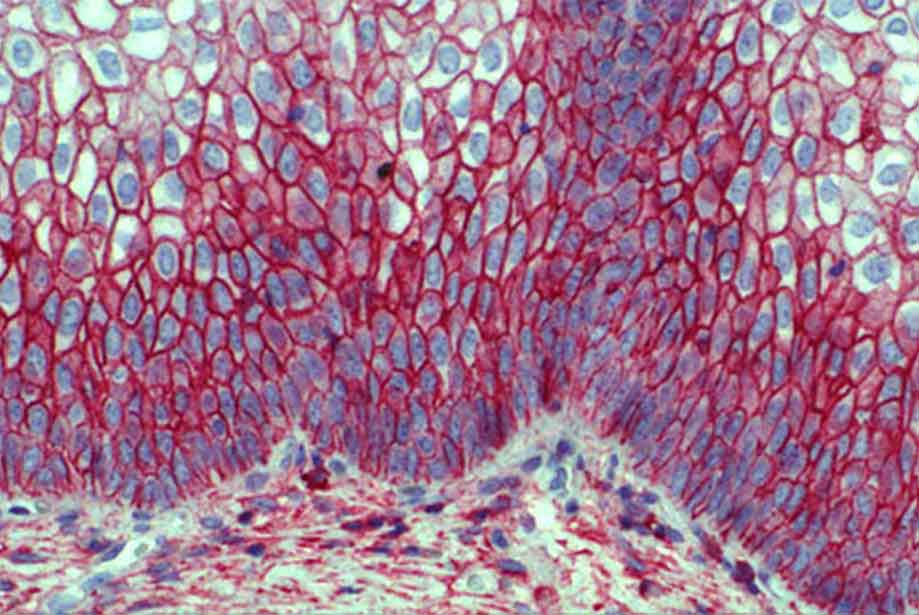
ИГХ является методом визуализации, который помогает определить локализацию веществ в препаратах тканевых срезов. В основе данного метода лежит принцип характерного взаимодействия антигенов с антителами, полученными особенным методом.
Иммунофлуоресценция
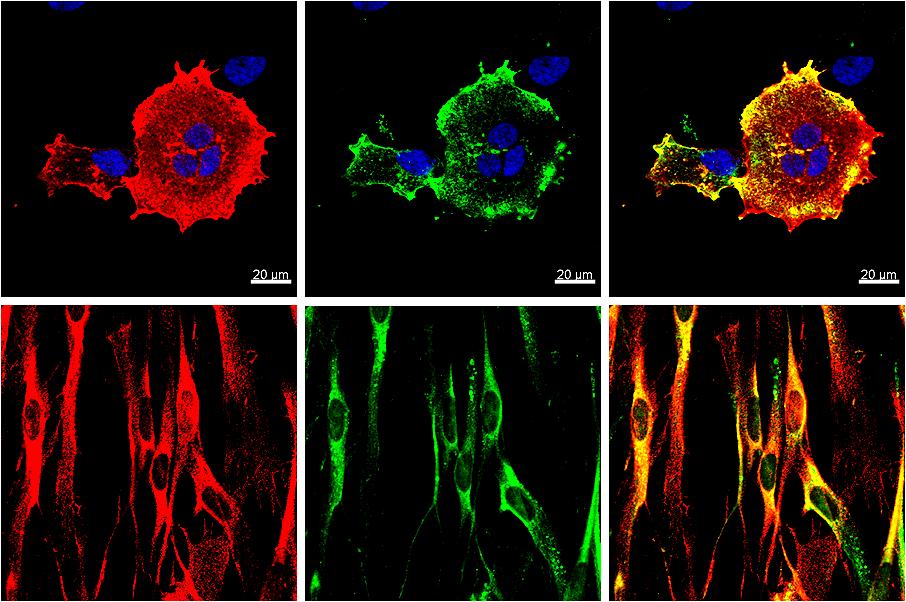
Метод исследования основан на чувствительности флюоресцентной микроскопии и специфичности иммунологической реакции. В процессе его проведения опухолевая ткань метится специальным красителем, который помогает доктору точно определить диагноз. Особенностью этого метода является простота и необходимость использования минимального количества изучаемого материала.
Иммуноферментный анализ
Метод диагностики обладает высокой восприимчивостью и позволяет устанавливать минимальные количества вещества. В современных методах диагностики именно с помощью этого способа определяется локализация антигена. Для проведения анализа используются специальные ферменты для обнаружения рака.
Независимо от выбранной методики целью любого морфологического исследования считается точное определение типа опухоли и оценки изменений на клеточном уровне. Можно сказать простыми словами, что морфологическая верификация - это определение разновидности опухоли и ее запущенности для правильного выбора тактики лечения.
Методы получения материала для морфологического исследования
Для морфологической верификации диагноза необходимо получить материал. Сделать это можно следующими способами:
- Трепан-биопсия – считается одной из самых результативных процедур, несмотря на то что имеет определенные недостатки. Для взятия материала используются специальные иглы с внутренними режущими механизмами. С их помощью получается столбик ткани из опухоли. Этот метод позволяет провести морфологическую верификацию молочных желез, предстательной железы, легкого, печени, позвоночника и лимфатических узлов.
- Инцизионная биопсия – самый популярный метод, который выполняется с помощью скальпеля, которым берется материал из центра подозрительных участков, по периферии опухоли. При этом обязательно нужно делать это вне зон отека, некроза и кровоизлияния грануляционной ткани.
- Эксцизионная биопсия – суть такого метода заключается в полном радикальном удалении опухоли. Этот способ применим только если новообразование имеет небольшие размеры. В таком случае этот способ наиболее предпочтителен, так как имеет как диагностическое, так и терапевтическое значение.
Выбор способа морфологической верификации определяет лечащий врач в зависимости от особенностей сложившейся ситуации.
Последовательность морфологических изменений
Что это такое морфологическая верификация диагноза, и в какой последовательности происходят изменения в процессе развития рака, знают не многие. К сожалению, в основном люди начинают интересоваться подобной информацией, только когда сталкиваются с проблемой.
Онкология в процессе развития проходит определенные стадии, и в результате проведения морфологической верификации доктор может наблюдать разные нюансы развития. При верификации могут обнаруживаться следующие изменения в тканях:
- диффузная и очаговая гиперплазия – процесс не опасный и обратимый;
- метаплазия – доброкачественное новообразование;
- дисплазия – предраковое образование;
- рак in situ – преинвазивное раковое поражение;
- микроинвазия;
- прогрессирующий рак с метастазированием.
Промежутки времени между перечисленными этапами индивидуальны и в каждом отдельном случае могут варьироваться от нескольких месяцев до десятилетий.
Главной задачей морфологической диагностики является установление тканевой принадлежности опухоли. При этом выявляется не только ее наличие и разновидность, но и скрупулезно оценивается степень атипии клетки и нарушение тканевых структур. Чаще всего проводится морфологическая верификация щитовидной железы, молочной, предстательной, печени, почек и позвоночника. Метод проведения исследования в каждом отдельном случае определяется персонально.
Важный этап диагностики рака – определение гистологического типа злокачественного новообразования. Верификация опухоли – это оценка морфологического (клеточно-тканевого) варианта карциномы, предполагающая проведение исследований с биопсийным материалом. Нельзя начинать лечение, не зная гистотип (тканевой состав) и клеточную дифференцировку раковой опухоли.
Выяснив клеточно-тканевой состав опухоли, можно начинать терапию
Верификация опухоли
До момента применения комбинированной терапии надо точно выяснить морфологическую структуру новообразования. Вражеская армия может состоять из агрессивных молодых и необученных бойцов, с которыми легко справится иммунная система. Или противоопухолевой защите придется столкнуться с живучим, хитрым и коварным противником, способным быстро изменяться и приспосабливаться.
Зная состав вражеского войска, можно предвидеть исход битвы.
Верификация опухоли – это микроскопическая оценка взятых при биопсии тканей, на основе которых врач-лаборант точно определит цитоморфологический состав злокачественного новообразования: важен не только факт обнаружения рака, но и гистологический вариант опухолевого роста с отличием от исходных здоровых клеток. Зная состав вражеского войска, можно предвидеть исход битвы.
Варианты биопсийного материала
Врач-лаборант, выполняющий морфологические исследования, будет работать со следующими видами биопсийного материала:
- Кусочки тканей, удаленных при проведении диагностической или лечебной операции;
- Соскоб из полых органов;
- Пунктат из опухоли;
- Мазок-отпечаток с поверхности злокачественного новообразования;
- Жидкость, удаленная из кистозной полости;
- Собранная в первичном очаге секреторная или экссудативная жидкость.
Любая ткань может стать основой для проведения качественной морфологической диагностики, но при одном важном условии – во время выполнения биопсии опухоли надо взять неповрежденный участок из карциномы. Чем сохраннее биоптат, тем качественнее диагностика.
Последовательность морфологических изменений
Рак в своем развитии проходит несколько стадий, поэтому врач-гистолог при проведении микроскопического исследования может увидеть разнообразные картины опухолевого роста – от предраковых изменений до выявления признаков распада злокачественного узла. Верификация опухоли – это обнаружение при исследовании одного из вариантов типичной последовательности онкологических изменений в тканях:
- Гиперплазия (диффузная и очаговая) – обратимый и не опасный процесс;
- Метаплазия (доброкачественное изменение);
- Дисплазия (предрак);
- Рак in situ (преинвазивное раковое поражение);
- Микроинвазия;
- Прогрессирующий рак с метастазированием.
Временные промежутки между этапами формирования опухоли относительны – иногда проходят десятилетия от первичных доброкачественных процессов к инвазии, в худших случаях от дисплазии к раку – за месяцы.

Врач-гистолог по срезам тканей поставит морфологический диагноз
Методы морфологии
Стандартный вариант проведения гистологического исследования – приготовление тончайших срезов биопсийных тканей с последующей микроскопией материала. Эта методика позволяет получить массу полезной информации о клеточно-тканевом составе опухоли. Кроме этого, верификация опухоли – это следующие диагностические методы:
- Гистохимия (использование химических реакций для определения разных вариантов биологически активных веществ опухоли);
- Иммуногистохимия (применение иммунных реакций взаимодействия опухолевых антигенов со специально созданными антителами);
- Иммунофлюоресценция (специальный краситель метит опухолевую ткань, позволяя врачу поставить точный диагноз);
- Иммуноферментный анализ (использование фермента для обнаружения рака).
Вне зависимости от методики, основная цель гистологического исследования – определение типа опухоли и оценка клеточных изменений: зная состав наступающей армии, можно выбрать тактику защиты или принять решение о контрнаступлении.
Влияние лечебных факторов на опухоль
Далеко не всегда с момента начала комбинированной терапии можно получить желаемый положительный результат. Ни хирургическая операция, ни химиотерапия, ни курсы облучения не гарантируют полного излечения, что объясняется способностью опухоли приспосабливаться и видоизменяться. Значительная часть вражеского войска погибнет, но те бойцы, которые смогли выжить, дадут новые генерации солдат, способных противостоять лечебным воздействиям. Лекарственные препараты и облучение способны разрушить опухолевую ткань, что приведет к некрозу и воспалению, но даже единичный метастаз, сохранившийся в лимфоузле, может стать основой для рецидива опухоли. Это вовсе не означает, что рак непобедим: зная, что враг коварен и хитер, нельзя расслабляться и успокаиваться после локальной победы. Длительное наблюдение у врача, поддержка противоопухолевого иммунитета и регулярные контрольные обследования помогут избавиться от болезни.
В сомнительных случаях диагноз аденокарциномы ПЖ можно подтвердить после выполнения чрескожной тонкоигольной биопсии под контролем УЗИ с последующим гистологическим исследованием биоптата. Однако у больных с резектабельными опухолями биопсия, осуществляемая под контролем ЭУЗИ, более предпочтительна, чем чрескожная пункционная биопсия под контролем УЗИ или КТ. Это обстоятельство обусловлено отсутствием риска возникновения имплантационных метастазов в передней брюшной стенке при выполнении диагностической манипуляции через просвет полого органа [33]. Тонкоигольная биопсия под контролем ЭУЗИ является наиболее достоверной в дифференциальной диагностике опухолевых кистозных поражений и псевдокист ПЖ [34].
При отрицательном результате гистологического исследования биоптата показано проведение повторной биопсии под контролем ЭУЗИ [30].
Рекомендации:
1). Если диагноз веско аргументирован данными комплексного обследования, то гистологическая верификация диагноза рака ПЖ до операции не требуется, чтобы не приводить к задержке хирургического лечения.
2). При трудностях дифференциальной диагностики рака и хронического панкреатита необходимо производить тонкоигольную биопсию под контролем ЭУЗИ.
3). Выполнение чрескожной тонкоигольной биопсии под контролем УЗИ показано при наличии метастатического поражения печени и отдаленных лимфогенных метастазов, которая является обязательной для морфологической характеристики нерезектабельной опухоли и выбора патогенетически обоснованной адъювантной и неоадъювантной терапии.
Опухолевые маркеры
Диагностическая значимость опухоле-ассоциированных антигенов (CEA, CA125) в ряде случаев невысока. Большую диагностическую ценность имеет уровень карбогидратного антигена (CA) 19-9 в крови. Но CA 19-9 обычно повышается при заболеваниях ПЖ, печени и желчных протоков, а также при многих злокачественных опухолях и, таким образом, не является специфичным для рака ПЖ. Однако степень увеличения CA 19-9 имеет значение при дифференцировании аденокарциномы и воспалительных заболеваний железы [35], уменьшение уровня CA 19-9 в динамике коррелирует с лучшей выживаемостью больных раком ПЖ после операции [36] или химиотерапии [37, 38].
Рекомендации:
1). Уровень СА 19-9 сыворотки крови необходимо определять до операции и в различные сроки после удаления резектабельной опухоли ПЖ для своевременной диагностики возможного рецидива заболевания (категория 2B).
Лапароскопическая диагностика
Лапароскопия является ценным способом диагностики при определении мелких имплантационных метастазов на брюшине или в печени, которые могут быть не визуализированы при УЗИ, КТ и МРТ [39].
Рекомендации:
1). При стадировании для исключения метастазов возможно использование диагностической лапароскопии, как до операции, так и перед выполнением химио- и лучевой терапии (категория 2B).
2). У больных с высоким риском распространенности онкологического процесса (сомнительная резектабельность опухоли, повышенный уровень CA19-9, первичная опухоль больших размеров) диагностическая лапароскопия обязательна (категория 2В).
2). Положительный результат цитологического исследования смывов из брюшной полости, полученных при лапароскопии или лапаротомии, следует расценивать как M1. Если при этом выполнена резекция ПЖ, то отдаленные результаты надо трактовать как у больных с отдаленными метастазами (IV стадии).
Хирургическое лечение
Хирургическое удаление опухоли остается единственным методом, способным избавить от заболевания. Однако достичь стойкого эффекта в большинстве случаев рака ПЖ можно только при мультимодальном подходе с использованием химио-, лучевой и таргетной терапией.
При раке ПЖ с органными, перитонеальными и плевральными метастазами резекция ПЖ нецелесообразна. Однако при локорегиональной распространенности заболевания подходы к хирургическому лечению различны.
Используя только резекционный подход у более 80% больных раком железы нельзя излечить от заболевания [40]. В специализированных центрах удалось добиться снижения ранней послеоперационной летальности (менее 5% случаев) после различных по объему резекционных вмешательств на ПЖ [41]. Но даже при самых оптимальных условиях показатели 5-летней выживаемости оперированных больных невысоки (около 20%) с медианой выживаемостью 15-19 месяцев [42].
Достоверными прогностическими факторами, определяющими отдаленную выживаемость больных протоковой аденокарциномой, является R0-резекция, содержание ДНК в опухолевых клетках, размеры опухоли и отсутствие лимфогенных метастазов [43, 44].
Радикальные операции
Только полное удаление первичной опухоли и ее метастазов (R0-резекции) характеризуется хорошими отдаленными результатами [45, 46]. Чтобы избежать оставления опухолевых клеток по линии резекции, при ПДР необходима тщательная диссекция периваскулярных тканей вдоль верхнебрыжеечных сосудов: деликатное отделение крючковидного отростка от мезентерикопортального венозного ствола (при отсутствии признаков его инвазии опухолью); резекция и протезирование вены (при малейших сомнениях); скелетизация ВБА по всей ее окружности, вплоть до адвентиции, в пределах ширины крючковидного отростка [47, 48, 49]. Достоверных данных, подтверждающих целесообразность расширения показаний к выполнению резекций магистральных артерий, нет [50].
Рекомендации:
1). Операции должны выполняться в учреждениях, обладающих опытом выполнения значительного числа резекций ПЖ (не менее 20 операций ежегодно).
2). В большинстве случаев – при отсутствии инвазии в стенку луковицы ДПК – показано выполнение ПДР с сохранением привратника.
3). Окончательное стадирование протоковой аденокарциномы головки ПЖ должно осуществляться только после тщательного патоморфологического и иммуногистохимического изучения опухолевой ткани, а также удаленных операционных препаратов с оценкой возможности опухолевой инвазии по линии резекции железы (крючковидного отростка, перешейка), желчного протока и кишки; ретроперитонеальной поверхности головки железы (в проекции верхнебрыжеечной вены и артерии), лимфогенного метастазирования.
Последнее изменение этой страницы: 2017-01-18; Нарушение авторского права страницы
СПОСОБЫ МОРФОЛОГИЧЕСКОЙ ВЕРИФИКАЦИИ ОПУХОЛЕЙ
Для морфологического исследования используются различные методы забора материала. Соскобы и мазки-отпечатки с поверхностных изъязвленных опухолей являются очень распространенным способом диагностики в практике обследования больных с опухолями головы и шеи. При поверхностно расположенных узловых образованиях выполняется их пункция. При малых размерах подозрительных в отношении опухолевого роста образований возможно выполнение пункции под контролем УЗИ. Тканевую принадлежность опухоли установить тем легче, чем доброкачественнее опухоль, так как в структуре доброкачественной опухоли сохраняется много черт исходной ткани. Отрицательные результаты цитологического исследования не редкость в практике отделений опухолей головы и шеи. Это бывает связано либо с солидным характером опухолей и трудностями фрагментации клеток (саркомы, невриномы), либо с затруднением трактовки полученного материала, так как в виду множественности закладок жаберных дуг бывает сложно установить тканевую принадлежность опухолевых клеток. В неясных случаях прибегают к проведению иммуногистохимических, электронно-микроскопических исследований, иногда выявляющих дополнительные морфологические признаки, позволяющие сопоставить опухоль с исходной тканью.
В настоящее время при обнаружении опухоли внутренних органов возможно осуществить морфологическое исследование практи- чески в любой части тела. Во многих случаях доступ осуществляется с помощью эндоскопической техники. Медиастиноскопия - метод визуального инструментального исследования переднего средостения. Можно проникнуть в плевральную полость и выполнить биопсию плевры и легочной ткани (медиастиноплевроскопия) при соче- танном поражении легких и лимфатических узлов средостения. Во время медиастиноскопии возможно удаление паратрахеальных кист, кистоподобных образований и небольших опухолей вилочковой железы. Ретроперитонеоскопия позволяет осуществить забор материала из этой области. В тех случаях, когда непосредственный визуальный доступ невозможен или сопряжен с большим риском (при патологии сосудов), пункция или трепанобиопсия осуществляются под контролем УЗИ или КТ. Таким образом, становятся доступными для обследования опухоли щитовидной железы, средостения, пери-
ферических отделов легких, печени, почек, поджелудочной железы, внеорганные забрюшинные опухоли и др. Если пункцию выполнить невозможно, используют эндоскопические методы исследования: фаринго- и ларингоскопию, эзофагогастродуоденоскопию, торакоскопию, бронхоскопию, колоноскопию и др., в ходе которых под визуальным контролем обычно забирают участок ткани (биоптат или браш-биоптат - соскоб специальной щеточкой, смывы с поверхности образования и т.д.) для морфологического исследования. Эти способы обычно дают достаточно материала для морфологической верификации диагноза. Наиболее информативный материал получают из участков опухоли на границе со здоровой тканью.
Открытая биопсия опухоли выполняется, как правило, после неудачных попыток верифицировать диагноз вышеуказанными методами или из-за необходимости получить больше ткани для выполнения некоторых специфических исследований, например для определения рецепторов гормонов при опухолях молочной железы, иммуногистохимического исследования при гематосаркомах. Биопсия инцизионная предполагает получение участка ткани непо- средственно из патологического очага, выполняется под местной анестезией (из опухоли молочной железы, мягких тканей) или под наркозом (из костных опухолей). Биопсия эксцизионная выполняется как хирургическое вмешательство с удалением опухоли в пределах здоровых тканей. Трепанобиопсия в основном используется для исследования новообразований молочной железы, костей, мягкотканных опухолей. При невозможности верифицировать злокачественность опухоли на диагностическом этапе планируют срочное гистологическое исследование во время операции.
Гистологическая верификация может быть получена при использовании специальной иглы или трепана, при этом изымается столбик измененной ткани, пригодный для гистологического исследования. Особенно важным в плане адекватной диагностики распространен-
ности опухолей бывает исследование сомнительных по клиническим данным образований в зонах регионарного метастазирования. В большинстве же случаев сопоставление клинических проявлений опухоли с ее симптомами вне основного очага не требует верификации всех обнаруженных метастазов. Производят морфологическое исследование наиболее доступных вторичных опухолей, что само по себе делает ясным представление об истинной распространенности заболевания. Верификация диагноза осуществляется путем чрезкожной пункции метастаза или забора материала при лапароили торакоскопии.
Основная задача морфологической диагностики - установить тканевую принадлежность опухоли (гистогенез), при этом тщательно оценивается степень атипии самой клетки и нарушение тканевых структур. В большинстве случаев диагноз устанавливается по традиционно приготовленным препаратам, изучаемым при световой микроскопии.
Общепринятая классификация злокачественных опухолей Международного противоракового союза - TNM - описывает 3 основных параметрараспространения опухоли:
T - первичная опухоль;
N - регионарные лимфатические узлы;
M - отдаленные метастазы.
Для создания полного представления о распространенности новообразования необходимо получить сведения по каждой из указанных категорий.
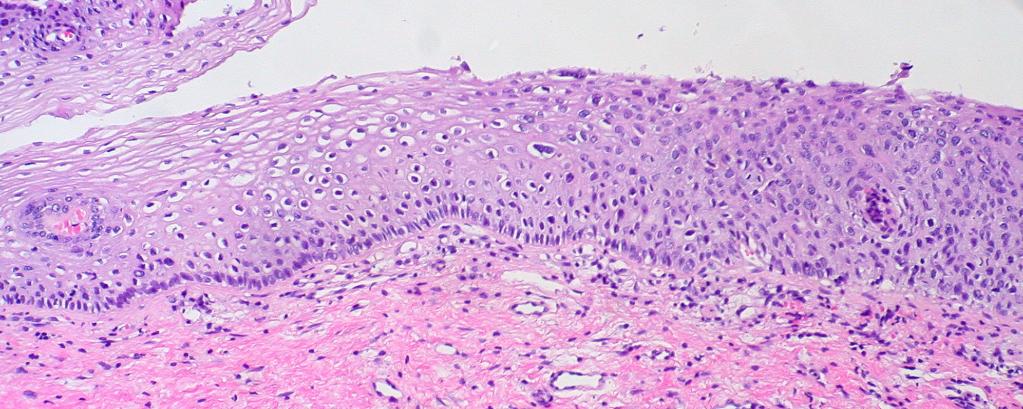
Диагноз злокачественного или иного новообразования приобретает абсолютную точность и считается полностью доказанным только после морфологического подтверждения (верификации) с определением гистологического типа опухоли. При получении биопсийного материала в виде отпечатка или соскоба осуществляется цитологическое исследование - изучение клеток, которые могут иметь только отдельные черты злокачественности или полностью идентифицироваться по гистологическому типу опухоли (рис. 6.4 и 6.5). При получении кусочков тканей производится гистологическое исследование - изучение тканевых структур с идентификацией опухоли по ее внутреннему клеточному строению.
34. Способы забора материала для верификации диагноза злокачественного новообразования.(+вопрос 33)
МЕТОДИКА ЗАБОРА МАТЕРИАЛА ДЛЯ ЦИТОЛОГИЧЕСКОГО ОБСЛЕДОВАНИЯ
Для цитологического исследования используют клеточный материал, взятый из опухоли. Для этого используют отпечатки с поверхности изъязвленной опухоли, пункцию опухолей, жидкостное содержимое опухолей и кистозных полостей. Исследуются любые естественные выделения: моча, мокрота, пунктат и жидкостное содержимое верхнечелюстных или лобных пазух. Жидкости подвергают центрифугированию, осадок исследуется. В ряде случаев цитологическому исследованию подвергается мазок с биоптата или с операционного препарата, когда требуется срочное морфологическое заключение.
Учитывая, что от контакта с водой и слюной клетки опухоли разрушаются, следует избегать контакта исследуемого материала с ними. Для забора материала используют только стерильный сухой инструмент: скальпель, игла, шприц, предметное стекло. Обилие элементов крови в пунктате затрудняет его изучение.
Техника забора материала с язвы состоит в следующем. Поверхность изъязвленных опухолей освобождают от струпов, при обильном кровоснабжении в исследуемой области пережимают приводящие сосуды и производят отпечаток с поверхности опухолевой
язвы. Можно скальпелем царапающими движениями аккуратно снять поверхностные слои с поверхности язвы и распределить их тонким слоем по предметному стеклу. С опухолей, выявляемых при эндоскопическом исследовании, материал для цитологического исследования забирают специальной щеточкой-скарификатором (браш-биоптат). Биопсийный материал при эндоскопии берут специальными цапками, затем с поверхности биопсированного кусочка ткани производится цитологический мазок.
Методика аспирационной биопсии при всей своей простоте требует определенного навыка. Аспирационная биопсия - манипуляция хирургическая. От техники забора материала, обработки и окраски препарата зависит результативность изучения цитологического мазка врачом-цитологом и нередко достоверность результатов. У взрослых пункция выполняется, как правило, без дополнительной анестезии. У детей исследование поверхностных образований проводят с обезболиванием, а пункцию опухолей грудной клетки, малого таза, забрюшинного пространства - с применением масочного наркоза и использованием релаксантов.
Аспирационная биопсия позволяет получить цитологический материал более чем в 90% случаев и решить вопрос о наличии опухолевого процесса. Опухоли малого размера пунктируют под контролем УЗИ. Диагностическое значение имеют только положительные результаты пункции, а отрицательные данные часто не исключают наличие опухоли. В таких случаях, решая вопрос о дальнейших шагах для исключения опухоли, руководствуются клиническими данными. Повторять пункционное обследование больше трех раз обычно нецелесообразно. При отсутствии убедительных данных о морфологической природе опухоли планируют биопсию.
Диагностические операции являются частым диагностическим приемом в онкологии. К ним прибегают, когда исчерпаны все другие возможности уточнить диагноз. Она необходима также, когда требуется более подробное, чем при цитологическом исследовании, изу-
чение структуры опухолей, исследование некоторых биохимических свойств ее - рецепторы, иммуногистохимия и др.
Выполнение пункции не дает гарантии повреждения соседних органов или крупных сосудов с последующими осложнениями. В труднодоступных областях (опухоль печени под куполом диафрагмы) исследование крайне затруднено.
Распознавание локализации одного или нескольких лимфатических узлов, через которые осуществляется преимущественный отток лимфы из определенного органа или участка тела, активно разрабатывается в настоящее время в клинической онкологии. Для большинства локализаций опухолей по клиническим наблюдениям установлены пути преимущественного первичного лимфооттока. Для органов головы и шеи это также достаточно ясно. Например, при локализации рака в передних отделах полости рта и языка первые метастазы развиваются в лимфатических узлах подбородочного и подчелюстных треугольников. Для рака задних отделов полости рта, нёбных миндалин регионарным лимфатическим узлом первого порядка является подчелюстной лимфоузел гомолатеральной сто- роны, рак гортани и гортаноглотки в первую очередь метастазирует в лимфоузел у места впадения лицевой вены во внутреннюю яремную. При раке носоглотки первые метастазы реализуются в верхней группе яремной цепочки лимфатических узлов. Эти данные позволили разработать некоторые варианты фасциально-футлярного иссечения клетчатки шеи в зависимости от локализации первичной опухоли. Выявление микрометастаза в сторожевом лимфатическом узле свидетельствует о реализации метастатического процесса и необходимости активных лечебных мероприятий для эрадикации метастазов.
процессе наблюдения за больным, через 5-10 лет, при этом оценка стадии заболевания изменяться не может.
Остаточная опухоль - элементы злокачественной опухоли, определяемые макроскопически (в операционной ране) или микроскопически (по краю резекции в операционном препарате). Условные сроки проявления остаточной опухоли или рецидива различны для разных опухолей. В среднем считается, что возникновение роста опухоли в зоне операции до 1 года - результат нерадикальной операции, а после этого срока - истинный рецидив. В отношении химиолучевого лечения о радикальном лечении можно говорить, если достигнута полная ремиссия (исчезновение опухоли и всех ее проявлений) на условный срок не менее чем 4 недели.
Общее состояние больного является определяющим в подборе планируемых диагностических мероприятий. Пациенту в тяжелом состоянии не имеет смысла проводить обследование в полном объеме, так как лечение онкологической патологии всегда достаточно агрессивно и тяжесть состояния, обусловленная распространенностью процесса, не позволит провести лечение с удовлетворяющим результатом. В особо тяжелых случаях консилиум обсуждает вопрос о симптоматической терапии без обследования.
Читайте также:

