Гиперкальциемии при злокачественных опухолях
14. ГИПЕРКАЛЬЦИЕМИЯ ПРИ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЯХ
1. На какие две главные категории делится гиперкальциемия при злокачественных новообразованиях?
- Гуморальная гиперкальциемия при злокачественных новообразованиях
- Локальная остеолитическая гиперкальциемия
2. Какие виды злокачественных новообразований связаны с гиперкальциемией?
Наиболее часто ассоциируется рак легких, особенно плоскоклеточная карцинома. Прочие опухоли, ассоциированные с гиперкальциемией - плоскоклеточные карциномы головы, шеи, пищевода и аденокарциномы почек, мочевого пузыря, поджелудочной железы, молочных желез и яичников.
3. Какова причина гуморальной гиперкальциемии при злокачественных новообразованиях?
Гуморальная гиперкальциемия при злокачественных новообразованиях является результатом секреции опухолью (как первичной, так и метастатической) в кровоток продуктов, вызывающих гиперкальциемию. Более, чем в 90% случаев гуморальным медиатором является паратгормон-родственный протеин (ПТГрП). Прочими гуморальными продуктами, редко секретируемыми и способствующими развитию гиперкальциемии, являются трансформирующий фактор роста альфа (ТФРа), фактор некроза опухоли (ФНО), различные интерлейкины и цитокины.
4. Что такое ПТГрП?
ПТГрП - белок, который имеет последовательность аминокислот, сходную с первыми 13 аминокислотами паратиреоидного гормона (ПТГ). ПТГ и ПТГрП связываются с общим рецептором (ПТГ/ПТГрП рецептор), в результате чего происходит стимуляция костной резорбции и ингибирование экскреции кальция почками. ПТГрП находится в высоких концентрациях в грудном молоке и амниотической жидкости, но продуцируется почти всеми тканями организма; в течение беременности его концентрация в кровотоке возрастает. Его физиологическая эндокринная функция заключается в регулировании перехода кальция из материнского скелета и кро-вотока в развивающийся плод и грудное молоко. Как паракринный фактор, он регулирует рост и развитие многих тканей, преимущественно скелета и молочных желез.
5. Каким образом ПТГрП способствует развитию гиперкальциемии у пациентов со злокачественными опухолями?
При снижении дифференцировки некоторые злокачественные опухоли продуцируют большое количество необычных белков, таких, как ПТГрП. Повышенные концентрации ПТГрП стимулируют в целом костную резорбцию, наполняя кровоток избыточным количеством кальция; ПТГрП также действует на почки, предотвращая увеличение экскреции кальция в ответ на его повышение в крови. В результате совместного действия этих факторов увеличивается концентрация в плазме кальция. Гиперкальциемия индуцирует полиурию, следствием чего является дегидратация с повреждением почечных функций, что в свою очередь ведет к снижению экскреции кальция, замыкая патологический круг, и, в конечном счете, приводя к угрожающей жизни гиперкальциемии.
6. Как вы диагностируете гуморальную гиперкальциемию при злокачественных новообразованиях?
Гиперкальциемия у пациентов с установленной опухолью сама по себе заставляет заподозрить диагноз ее малигнизации. Изредка, однако, повышенное содержание кальция в крови - первое звено в диагностике являющейся причиной гиперкальциемии опухоли. Рутинные лабораторные анализы обычно выявляют гиперкальциемию, часто связанную с низким уровнем альбумина. Ключом к диагнозу является сниженный уровень интактиого ПТГ; эта находка надежно исключает гиперпарати-реоз и прочие причины гиперкальциемии, при которых интактный ПТГ повышенный, нормальный или очевидно высокий. Уровень ПТГрП почти всегда высокий, но этот дорогостоящий анализ в большинстве случаев не является необходимым. Если у пациента с выявленным этим диагностическим критерием ранее не была обнаружена какая-либо опухоль, необходимо провести тщательный поиск скрытой онкологической патологии.
7. Какие типы злокачественных опухолей ассоциированы с локальной осте-олитической гиперкальциемией?
Рак молочной железы с метастазами в кости, множественная миелома, лимфома и, редко, лейкемия.
8. Какова причина локальной остеолитической гиперкальциемии?
Локальная остеолитическая Гиперкальциемия обычно возникает при наличии раковых клеток во многих местах скелета. Патогенез включает выработку злокачественными клетками остеокласт-стимулирующих факторов прямо на поверхности кости. Подобные факторы включают ПТГрП, лимфотоксин, интелейкины, трансформирующие ростовые факторы, простагландины и прокатепсин D.
9. Как вы диагностируете локальную остеолитическую гиперкальциемию?
Диагноз достаточно прост, когда у пациента с каким-либо из описанных выше онкологических заболеваний развивается Гиперкальциемия. Дополнительно к гиперкальциемии у пациентов часто отмечаются нормальные показатели фосфора, низкий плазменный альбумин и повышенный уровень щелочной фосфатазы. Опять же, ключом к диагнозу является определение сниженного уровня интактного ПТГ, указывающего на то, что гиперпаратиреоз в данном случае не имеет места. Пациентам с ранее невыявленными опухолями необходимо провести общий анализ крови, электрофорез белков в плазме и моче, сцинтиграфию костей; если эти исследования не окажутся информативными, необходимо сделать биопсию костного мозга.
10. Могут ли лимфомы обусловить гиперкальциемию посредством других механизмов?
Уникальным механизмом, идентифицированным при некоторых лимфомах, является экспрессия злокачественными клетками 1-альфа гидроксилазной активности, в результате чего происходит массивная конверсия 25-гидроксивитамина D в 1,25-ди-гидроксивитамин D. Это вызывает повышение всасывания кальция в кишечнике и в конечном счете ведет к гиперкальциемии, особенно при наличии сниженной экскреции кальция почками, что может возникать при дегидратации или повреждении соответствующей почечной функции.
11. Каков прогноз для пациентов с гаперкальциемией при злокачественных новообразованиях?
Поскольку гиперкальциемия обычно связана с поздними стадиями болезни, общий прогноз достаточно пессимистичен. В одном исследовании средняя продолжительность жизни пациентов с развившейся гиперкальциемией составила только 30 дней. Прогноз для ликвидации гиперкальциемии лучше, поскольку существует эффективное лечение.
12. Каково лечение гиперкальциемии при злокачественных новообразованиях?
Наиболее эффективные отдаленные результаты дает насколько возможно успешное лечение лежащей опухоли, обусловившей гиперкальциемию. Для пациентов с выраженной симптоматикой гиперкальциемии, однако, показано быстрое снижение уровня кальция. Начальной мерой почти у всех пациентов должно быть внутривенное введение физиологического раствора, с петлевыми диуретиками или без них для повышения почечной экскреции кальция. Одновременно проводится лечение для снижения костной резорбции. Наиболее эффективными являются памидронат (60-90 мг внутривенно (в/в) в течение нескольких часов - первый день и повторять каждые две недели в качестве поддерживающей терапии) и этидронат (7,5 мг/кг/день в/в ежедневно в течение 4-7 дней с последующим пероральным приемом 20 мг/кг/день в качестве поддерживающей терапии). В качестве альтернативы предлагается менее эффективный, но более быстро действующий кальцитонин (100-200 ЕД подкожно дважды в день ежедневно) вместе с преднизолоном (30-60 мг/день). При резистент-ной гиперкальциемии может потребоваться лечение пликамицином (25 мкг/кг в/в с повторением, при необходимости, через 48 часов), нитратом галлия (200 мг/м2/день в/в в течение 5 дней) или гемодиализ.
Гиперкальциемия является наиболее частым из опасных для жизни метаболических нарушений при злокачественных новообразованиях. Чаще всего гиперкальциемией осложняются миеломная болезнь и метастатический рак молочной железы (до 40 % больных), однако она может развиться и у пациентов с лимфогранулематозом, лимфомами, лейкозами и т. д.. Несмотря на то что к гиперкальциемии могут приводить многие заболевания, чаще всего ее развитие обусловлено гиперфункцией паращитовидных желез или различными злокачественными опухолями.
На долю других причин приходится менее 10 % случаев гиперкальциемии. Нормальный уровень паратиреоидного гормона исключает гиперпаратиреоидизм с большой степенью вероятности.
Гиперкальциемия, обусловленная злокачественной опухолью, наиболее часто имеет острое начало и выраженную клиническую симптоматику, требующую госпитализации и экстренной помощи. Наоборот, бессимптомная хроническая гиперкальциемия чаще обусловлена гиперфункцией паращитовидных желез.
При злокачественных новообразованиях за развитие гиперкальциемии отвечают два основных механизма. При одном из них (гуморальном) опухолевые клетки выделяют в системный кровоток биологически активные вещества, вызывающие повышенный остеолиз как в зонах метастатического поражения костей, так и за его пределами. Развитие гуморально обусловленной гиперкальциемии может наблюдаться и при отсутствии метастатического поражения костей. Наиболее часто за развитие такого типа гиперкальциемии у онкологических больных отвечает паратиреоидподобная субстанция (протеин) и активная форма витамина D3.
При остеолитическом типе гиперкальциемии разрушение костной ткани происходит только в области метастатического поражения. В данном случае резорбция кости обусловлена паракринной (местной) стимуляцией остеокластов различными цитокинами, выделяемыми опухолевыми клетками. Возможно и сочетание обоих механизмов.
Паратиреоидподобная субстанция (белок, частично гомологичный нормальному паратиреоидному гормону, но отличный от него при иммунологическом определении) отвечает за развитие гиперкальциемии при многих солидных опухолях, однако в онкогематологической практике имеет клиническое значение только у пациентов с Т-клеточной лимфомой/лейкемией. При лимфогранулематозе, неходжкинских лимфомах, миеломной болезни развитие гуморально обусловленной гиперкальциемии чаще связано с избыточным образованием активной формы витамина D3 (1,25 ОН2-витамин D3) под воздействием специфических ферментов, содержащихся в опухолевых клетках.
Выявление цитокинов, отвечающих за остеолитический тип гиперкальциемии, затруднительно в связи с невозможностью их определения в системном кровотоке. Считается, что в развитии остеолитической гиперкальциемии при различных злокачественных новообразованиях задействованы ИЛ-1, ИЛ-6, фактор некроза опухоли, PgE и т. д. Однако наиболее вероятно, что в большинстве случаев развитие гиперкальциемии у пациентов со злокачественными опухолями обусловлено комплексом биологически активных субстанций. Кроме того, необходимо помнить, что наличие у больного злокачественной опухоли не исключает наличия других причин гиперкальциемии (хроническая почечная недостаточность, передозировка витаминов групп D и А, гипертиреоз и т. д.).
Уровень общего кальция сыворотки (рутинно определяемый в большинстве лабораторий) обычно адекватно отражает выраженность гиперкальциемии.
Однако только 40 % кальция сыворотки присутствует в физиологически активной ионизированной форме, в то время как 50 % связано с белками крови (в основном с альбумином) и до 10 % образует комплексы с анионами (бикарбонатом, фосфатом, цитратом и др.). Биологические (и патологические) эффекты повышения уровня кальция зависят именно от величины ионизированной фракции. Доля ионизированного кальция увеличивается при гипоальбуминемии и, соответственно, снижается при гиперпротеинемии (например, при миеломной болезни). Когда изменения затрагивают только уровень альбумина, для более точной характеристики выраженности гиперкальциемии может быть использована следующая формула:
корригированный кальций (ммоль/л) = общий кальций (моль/л) + 0,8 х [4 —альбумин (г/дл)].
Если у пациента имеется выраженная гиперпротеинемия, необходимо прямое определение ионизированного кальция в лаборатории.
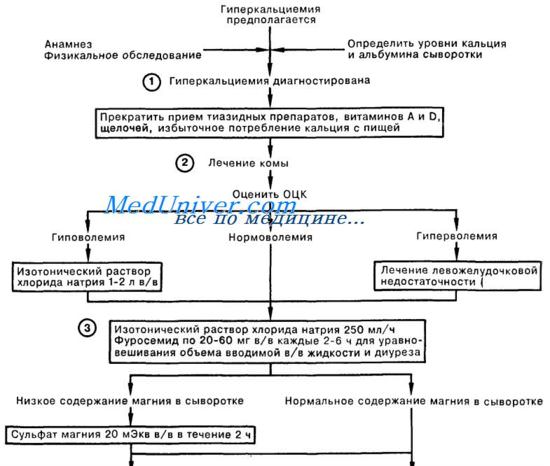
Разумеется, наилучшим лечением гиперкальциемии, обусловленной опухолевым ростом, является лечение основного заболевания, однако данное осложнение наиболее часто наблюдается у пациентов с распространенными опухолями, резистентными к противоопухолевой терапии. В связи с этим, а также учитывая, что гиперкальциемия представляет непосредственную угрозу для жизни больного, основным методом экстренной терапии являются симптоматические мероприятия, направленные на снижение уровня кальция в крови (за счет повышения экскреции кальция с мочой и уменьшения резорбции костной ткани).
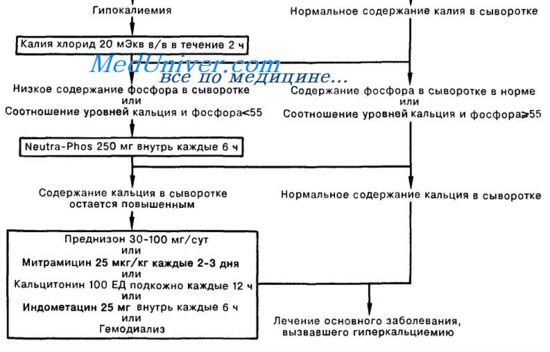
Попытки уменьшить поступление кальция в организм (диета со сниженным содержанием кальция) при гиперкальциемии, вызванной опухолью, неэффективны.
Должен быть приостановлен прием препаратов, снижающих экскрецию кальция (тиазидные диуретики), уменьшающих почечный кровоток (нестероидные противовоспалительные средства, Н2-блокаторы), и, разумеется, препаратов, напрямую вызывающих гиперкальциемию (препараты кальция, витамин D, ретиноиды).
Более того, фуросемид потенциально способен увеличить явления гиповолемии и реабсорбцию кальция в почках. Гидратация, однако, остается необходимым начальным компонентом терапии больных с гиперкальциемией, так как необходима для коррекции гиповолемии (представляющей наибольшую опасность для жизни) и позволяет сохранить адекватную функцию почек, препятствуя кристаллизации солей кальция в канальцах.
Первой линией терапии, направленной на снижение резорбции костной ткани, в настоящий момент признаны бисфосфонаты (синтетические аналоги пирофосфата, устойчивые к воздействию пирофосфатазы). Данные препараты, связываясь с молекулами костного матрикса (кристаллические гидроксиапатиты), подавляют метаболическую активность остеокластов, что приводит к уменьшению резорбции костной ткани и соответственно снижению экстракции из нее кальция. Преимуществами бисфос-фонатов, определяющими их широкое использование, являются высокая эффективность (гиперкальциемия купируется у 80—100 % больных) при малой токсичности (у 20 % больных может развиваться повышение температуры тела, гриппоподобный синдром или умеренно выраженные местные реакции в области введения). Эффект бисфосфонатов развивается достаточно быстро (в течение нескольких дней) и длительно сохраняется.
В настоящий момент для использования доступны следующие препараты, показавшие свою клиническую эффективность: аредиа (памидронат), бондронат (ибандронат), зомета (золендронат). Кальцитонин (миакальцик) также обладает способностью снижать уровень кальция за счет увеличения его почечной экскреции и снижения резорбции костной ткани. Данный препарат является наиболее быстродействующим (начало действия через 2—4 ч). Основным недостатком кальцитонина является кратковременность действия. Пик терапевтического действия приходится на 24—48 ч лечения с последующим быстрым снижением эффекта. Кортикостероиды также способны тормозить резорбцию костной ткани остеокластами, однако из-за меньшей активности и большего количества побочных эффектов их используют только у пациентов с опухолями, чувствительными к данному виду терапии. Пликамицин (митрамицин) и нитрат галлия, используемые в зарубежной практике при резистентности к терапии бисфосфанатами, в России недоступны.
При выборе тактики ведения больного с гиперкальциемией необходимо оценить тяжесть состояния больного и уровень кальция в крови. Уровень общего кальция более 3 ммоль/л и/или наличие симптомов гиперкальциемии (особенно дегидратации, нарушений ЦНС) является абсолютным показанием для госпитализации. В случае гиперкальциемии пациенту немедленно должна быть начата гидратация. Скорость регидратации зависит от выраженности дефицита воды и наличия у пациента сопутствующих сердечно-сосудистых и почечных заболеваний. При выраженной дегидратации и отсутствии сопутствующей патологии оптимальным можно считать введение физиологического раствора со скоростью 300— 400 мл/ч в течение 3—4 ч. Более медленная гидратация необходима при наличии кардиальной патологии, особенно застойной сердечной недостаточности.
Строгий контроль за диурезом (с поправкой на исходную дегидратацию), уровнем электролитов (калия, магния, натрия, хлора) и креатинина является необходимым при проведении такой терапии. Использование фуросемида допустимо только в случае задержки жидкости после адекватной регидратации. Сразу же после того, как будет налажен адекватный диурез (обычно через 2—3 ч после начала гидратации почасовой диурез становится равным объему вводимой жидкости), необходимо начать введение бисфосфонатов в рекомендованной дозе (аредиа 90 мг, бондронат 2—6 мг или зомета 4 мг). В связи с риском развития нефротоксичности необходимо строго соблюдать рекомендованную скорость введения (длительность инфузии: аредиа и бондронат — не менее 2 ч, зомета не менее 15 мин). Для пациентов, находящихся в критическом состоянии и/или при уровне кальция более 3,8 ммоль/л, рекомендуется использовать комбинацию бисфосфоната с кальцитонином (8 ME каждые 6 ч, внутримышечно 2— 3 дня), что позволяет добиться более быстрого эффекта.
При наличии у пациента опухоли, чувствительной к терапии кортикостероидами, эти препараты должны быть добавлены к терапии. В случае отсутствия эффекта от первой дозы бисфосфонатов их введение может быть осуществлено повторно через 5—7 дней. Необходимо помнить, что без эффективной противоопухолевой терапии достигнутая после введения бисфосфонатов нормокальциемия обычно длится от 15 до 40 сут, после чего вновь отмечается повышение уровня кальция, требующее повторного введения бисфосфонатов. При почечной недостаточности пациентам с гиперкальциемией рекомендован гемодиализ.

Гиперкальциемия — повышение концентрации кальция в сыворотке > 2,75 ммоль/л. Состояние сочетается с гипофосфатемией, обычно менее 0,7 ммоль/л. Гиперкальциемия — ситуация, которая является весьма серьезной, порой требующая ургентной помощи. Это достаточно редко регистрируемое состояние, наиболее часто встречается при почечной и онкологической патологии.
Постоянная усталость и потеря аппетита могут быть следствием повышенного уровня кальция, что довольно часто своевременно не распознаётся. Постоянная гиперкальциемия, очень высокие уровни кальция могут повлиять на ваши мышцы и частоту сердечных сокращений.
Уровень кальция в крови определяется с помощью несложного биохимического анализа. Лечение зависит от причины и степени превышения нормы. Избежать опасные последствия гиперкальциемии вам поможет регулярный контроль уровнять электролита в крови.
Симптомы гиперкальциемии
Гиперкальциемия часто протекает без четкой клинической картины, возможно отсутствие каких-либо симптомов. Симптоматика хронической гиперкальциемии отличается от клиническая картина внезапного повышения уровня кальция. Помимо этого, клинические эффекты, вызываемые гиперкальциемией, отличаются при незначительным повышение уровня кальция и очень высоким.
Симптомы гиперкальциемии легкой степени тяжести:
- тошнота,
- рвота,
- болевые ощущения в животе,
- мышечная слабость,
- запор.
Симптомы очень высокого уровня кальция:
- жажда вследствие обезвоживания
- снижение частоты мочеиспусканий
- мышечные спазмы
- аритмия сердца (нарушение частоты, ритмичности и последовательности возбуждения и сокращения сердца),
- умственные нарушения, галлюцинации, заторможенность,
- кома (в тяжелых случаях).
Клинические проявления хронической гиперкальциемии:
- мочекаменная болезнь,
- боль в мышцах и суставах.
Пациентам, у которых заболевание почек или онкология, следует знать о симптомах гипокальциемии. Возможен вариант, когда гиперкальциемия развивается очень стремительно, кроме того, встречаются случаи бессимптомного течения патологии.
Причины гиперкальциемии
Причины гиперкальциемии многообразны. Разрушение костей, заболевание почек, гиперпаратиреоидизм — наиболее распространённые причины.
- Гемобластозы: лимфома и лейкемия могут вмешиваться в процессы разрушения и формирования костной ткани, что приводит к повышению концентрация кальция в крови.
- Почечная недостаточность: через почки фильтруется кровь, в результате чего из неё удаляется излишек веществ, в том числе и кальция. Нарушение функций почек, приводит к расстройству водного-электролитного и других видов обмена. Это может привести к избытку кальция в крови.
- Гиперпаратиреоидизм: паратгормон (ПТГ) вырабатывается четырьмя околощитовидными железами, которые расположены на задней поверхности щитовидной железы. Воздействие на почки, паратгормон предотвращает избыточное выделение кальция с мочой. Уровень паратгормона выше нормы (гиперпаратиреоидизм) становится причиной гиперкальциемии. Высокий уровень ПТГ встречается при гиперплазии или аденоме околощитовидной железы.
- Метастатическое поражение костей. При метастазах в кости разрушается костная ткань, что сопровождается высвобождением кальций и поступлением его в кровь. Метастатическое поражение костей часто встречается при раке грудной железы и простаты.
Съев большое количество молочных продуктов, заполучить гиперкальциемию невозможно, если метаболизм кальция в норме. Кальцитонин — гормон, который синтезируется в С-клетках щитовидной железы, его действие направлено на снижение уровня кальция крови.
Кальций — наиболее распространенный минерал в теле человека. Ключевая роль в регуляции мышечного сокращения принадлежит ионам кальция. Избыток микроэлемент может приводить к появлению мышечных судорог. Более опасное последствие гиперкальциемии — это расстройство ритмичности, последовательности и силы сокращений сердечной мышцы.
Диагностика гиперкальциемии
Гиперкальциемия подтверждается на основании результатов биохимического анализа крови. Чтобы выяснить причину, врач будет рекомендовать пройти дополнительное обследование.
План обследования может включать анализы крови и мочи, методы лучевой диагностики, биопсию.
- Общий клинический анализ крови (ОАК): с его помощью выявляются изменения, характерные для лимфомы и лейкоза
- Электролиты сыворотки: возможны и другие нарушения электролитного баланса, например, такие как изменение концентрации натрия, магния, калия и фосфора. Их уровни в крови также регулируются паратгормоном. Результаты анализа на электролиты помогает врача выявить проблемы, связанные околощитовидная железа и почками.
- Анализ мочи: если предполагается почечная недостаточность, анализ мочи помогает выявить функциональные отклонения со стороны почек.
- Анализ крови на паратгормон.
- Компьютерная томография мочевыводящейсистемы (включает КТ почек, надпочечников и мочеточников) или ультразвуковое исследование почек.
- Паратиреосцинтиграфия (радионуклидная визуализация патологически измененных околощитовидных желез).
- Остеосцинтиграфия, или сцинтиграфия скелета (методика сканирования кости может помочь выявить метастатические поражения)
- Биопсия костного мозга необходима, чтобы подтвердить или опровергнуть диагноз гематобластоза (лимфомы или лейкемии)
Как правило, периодически назначается электрокардиограмма (ЭКГ), даже если отсутствует нарушение сердечного ритма.
Лечение гиперкальциемии
Выбор лечебной тактики зависит от уровня кальция в крови и причины гиперкальциемии. Терапевтические подходы могут включать использование медикаментов, форсированный диурез и гемодиализ.
Стратегии лечения гиперкальциемии:
- Большое количество жидкости. Жидкость стимулирует почки к выведению кальция и предотвращает обезвоживание.
- Внутривенное (в/в) жидкости и фуросемид (форсированный диурез), чтобы снизить концентрацию кальций крови и быстро вывести излишек его из организма
Ниже перечислен список медикаментов, которые используют для лечения гиперкальциемии:
- Бисфосфонаты представляют собой класс препаратов, предотвращающих потерю костной массы
- Кальцимакс, Миакальцик (кальцитонин) применяется в качестве средства, снижающего повышенную концентрацию кальция
- Нитрат галлия применяется для лечения гиперкальциемии при онкологии
- Сенсипар (цинакалцет) снижает концентрацию кальция в крови
- Кортикостероиды также могут снижать уровень кальция в крови
- Гемодиализ — метод внепочечного очищения крови, во время процедуры происходит удаление из организма токсических продуктов, нормализуется водно-электролитный баланс.
Несколько слово от OncoInfo
Гиперкальциемия — это редко встречающиеся состояние, так как организм обеспечен множеством механизмов поддержания нормальной концентрации кальция в крови. Тем не менее, некоторые заболевания могут привести к разбалансировки этих механизмов, что приводит к эксцессам высокой концентрации кальция.
Если вы предрасположены к гиперкальциемии, соблюдение диетических рекомендаций, умеренная гидратация организма и постоянный контроль уровней кальция — всё это поможет вам предотвратить развитие этого состояния.
Список использованных источников:
- Feldenzer KL, Sarno J. Hypercalcemia of Malignancy. J Adv Pract Oncol. 2018 Jul — Aug
- Turner. Hypercalcaemia—presentation and management. Clin Med (Lond). 2017 Jun
![]()
Кальций – ключевой катион, который участвует в клеточном транспорте, функции мембран и метаболизме костной ткани. Гиперкальциемия, или системный избыток кальция, пагубна для функциональной способности мембран к возбуждению, и приводит к слабости скелетных мышц и гладких мышц желудочно-кишечного тракта (ЖКТ).
Со стороны сердечной мышцы наблюдается уменьшение интервала QT и повышенный риск остановки сердца при чрезвычайно высоком уровне кальция. Со стороны нервной системы наблюдаются такие нарушения, как депрессия, раздражительность и, при высоких уровнях, кома.
При гиперкальциемии быстро исчерпываются функциональные резервы почек для реабсорбции кальция, за чем следует его выделение в мочу, где происходит образование комплексов кальция с фосфатами, что приводит к возникновению мочекаменной болезни.
При высоких уровнях кальция в крови может наблюдаться его оседание в мягких тканях, например почках, что может приводить к серьезному нарушению их функции. Гиперкальциемия также вызывает дегидратацию, индуцируя резистентность почек к вазопрессину, что приводит к нефрогенному несахарному диабету. Дегидратация, в свою очередь, вызывает дальнейшее повышение уровня кальция в сыворотке.
Растворимость фосфатов тесно связана с уровнем кальция. Любая причина, которая вызывает повышение уровня фосфатов, например, почечная недостаточность, приводит к снижению уровня ионизированного кальция. Биодоступность кальция составляет примерно 10 % и зависит от витамина D. Витамин D₃ может поступать с пищей, а также синтезироваться в коже из предшественников холестерина под воздействием солнечного света.
Витамин D₃ синтезируется в коже путем реакции предшественников холестерина с ультрафиолетовыми лучами спектра В; реакция происходит при контакте кожи с солнечным светом. Поступление витамина с пищей обычно несущественно, исключение составляют жители Арктики, которые потребляют большое количество витамина D₃ из жирных сортов рыбы и млекопитающих.
Витамин D₃ превращается в 25-гидрокси-метаболит в печени, а второе гидроксилирование, при котором он превращается в кальцитриол или 1,25-дигидроксивитамин D₃, происходит в паренхиме почек. Лишь около 1% от общего содержания кальция в организме находится во внеклеточной жидкости, тогда как все остальное количество сосредоточено в костях и внутриклеточном пространстве.
Примерно половина циркулирующего кальция связана с белками, а остальная часть находится в ионизированном виде и составляет физиологически активную фракцию. Уровень кальция строго контролирован паратиреоидным гормоном (ПТГ), который при снижении уровня ионизированного кальция высвобождается из паращитовидных желез. Когда уровень кальция повышается, паращитовидные железы перестают вырабатывать ПТГ.
Гиперкальциемия может протекать легко, и в таком случае быть бессимптомной. При сборе анамнеза можно также выявить симптомы гиперкальциемии, такие как наличие камней в почках, что характерно для гиперпаратиреоза, или летаргию, повышенную утомляемость, спутанность сознания, депрессию, раздражительность, запоры, а также полиурию и полидипсию.
Хронический характер симптомов обычно свидетельствует о гиперпаратиреозе, тогда как острота жалоб более характерна для злокачественных процессов. В случае легкой гиперкальциемии может отсутствовать потребность в проведении какихлибо вмешательств, за исключением мониторинга за осложнениями.
Повышенный уровень кальция может требовать проведения мер по предупреждению осложнений, таких как остеопороз. Симптомы или последствия тяжелой гиперкальциемии могут приводить к катастрофическому неотложному состоянию, связанному с дисбалансом электролитов, и требовать быстрой диагностики и немедленного лечения с целью предотвращения смерти.
Гиперкальциемия развивается либо вследствие первичного гиперпаратиреоза, либо опухолевого процесса в 90% случаев. Остальные случаи являются казуистическими и редкостью.
Первичный гиперпаратиреоз – состояние, характеризующееся патологическим и нерегулируемым повышением продукции ПТГ, что приводит к повышению уровня кальция. Наиболее частой причиной гиперкальциемии, которая требует госпитализации, является злокачественный процесс.
Другие, более редкие, причины – заболевания костей, гранулематозные состояния, а также погрешности в диете. При злокачественном новообразовании либо гранулематозном заболевании определение причины такого состояния может быть даже важнее чем само электролитное расстройство.
Наиболее частой причиной гиперкальциемии является первичный гиперпаратиреоз, который встречается с частотой 1:2000 среди пожилых женщин. В 85% случаев причиной такого состояния является аденома одной из паращитовидных желез, в остальных 15% случаев патологический процесс затрагивает все четыре железы. Всего 1% случаев вызван раком паращитовидной железы. Первичный гиперпаратиреоз может протекать по-разному – от легкой и асимптоматичной до тяжелой формы, которые осложняются утратой костной ткани, включая переломы костей и паратиреоидную остеодистрофию (болезнь Реклингхаузена).
Гиперкальциемия может сопровождать злокачественные опухоли в двух случаях:
-
Вовлечение кости в онкологический процесс может приводить к массивной активизации остеокластов (вызывать остеолиз), и в таком случае темпы высвобождения кальция просто превышают возможности механизмов, направленных на поддержание гомеостаза. Некоторые опухоли высвобождают ПТГ-подобные пептиды, которые активируют рецепторы к ПТГ.
За весь период заболевания у 25–30% больных раком пациентов возникают эпизоды гиперкальциемии. Обычно к злокачественным новообразованиям, которые приводят к гиперкальциемии, относят множественную миелому, лейкемию, рак легких и молочной железы. Если опухоль приводит к гиперкальциемии, в большинстве случаев можно говорить о поздних стадиях заболевания.
Злокачественные заболевания, вызывающие гиперкальциемию, – это множественная эндокринная неоплазия (МЭН) типа 1 (Вермера) и МЭН типа 2а (Сиппла), либо изолированный семейный гиперпаратиреоз. Также существует связь гиперпаратиреоза с нейрофиброматозом и болезнью Гиппеля–Ландау. В редких случаях причиной такого состояния может быть карцинома паращитовидной железы.
-
Метаболические
-
Витамин D – жирорастворимый витамин, который при длительном употреблении в больших количествах может быть токсичен. Обычно это возникает при самостоятельном назначении витамина. Передозировка 1,альфа-гидроксилированными метаболитами витамина D (альфакальцидолом или кальцитриолом) может легко вызывать гиперкальциемию, поэтому необходимо либо избегать хронического применения препарата, либо он должен проводиться под тщательным контролем. Гипертиреоз может приводить к гиперкальциемии, и, почти всегда, к гиперкальцийурии как следствию быстрой резорбции костной ткани. При синдроме пищевой гиперкальциемии, то-есть при значительном увеличении потребления кальция с пищей, может наблюдаться аномальное всасывание кальция. Синдром пищевой гиперкальциемии возникает при избыточном потреблении в пищу молока или щелочей (например, при диспепсии) или излишнем приеме кальция в качестве пищевой добавки (например, у женщин в постменопаузе). Избыточное поступление кальция с пищей или пищевыми добавками также может легко и часто приводить к гиперкальциемии. Уровень витамина D также повышается при гранулематозе, например, при саркоидозе. Это происходит за счет усиленной конверсии витамина D макрофагами. При иммобилизации подростков и молодых может иметь место массивная деминерализация костей с последующей гиперкальциемией. Подобные проблемы могут встречаться и у пациентов старшего возраста, но высокая степень минерализации костей у молодых значит намного больший пул мобильного кальция, который может поддерживать гиперкальциемию. Повышение метаболизма костной ткани любой этиологии может вызывать гиперкальциемию. Болезнь Педжета. Излишняя деминерализация костей с гиперкальциемией и угнетением синтеза ПТГ может также наблюдаться при излишнем употреблении витамина А.
-
На биодоступность кальция влияет литий, а тиазидные диуретики влияют на почечные механизмы и метаболизм костной ткани; таким образом, оба механизма могут вызывать гиперкальциемию, которая минует при отмене подобных препаратов.
-
Клиническая картина семейной гипокальциурической гиперкальциемии может напоминать гиперкальциемию вследствие гиперпаратиреоза, поскольку при этом заболевании нарушается сенсорная функция паращитовидных желез и почек, что приводит к незначительному повышению уровня ПТГ и снижению экскреции кальция.
В неотложных состояниях уровень кальция в сыворотке крови можно использовать как маркер, указывающий на необходимость коррекции гиперкальциемии. Уровень кальция ниже 3,0 ммоль/ л (12 мг/дл) обычно не проявляется симптомами и редко требует срочной коррекции. Пациенты с уровнем кальция 3,0–3,5 ммоль/л (12 и 14 мг/дл) могут хорошо переносить повышение кальция, если он поднимался медленно, но обычно это сопровождается симптомами и требует коррекции. При уровне кальция выше 3,5 ммоль/л (14 мг/дл) повышен риск аритмии и комы. При уровне кальция менее 3,25 ммоль/л (13 мг/дл) выраженные симптомы и кома маловероятны.
Гиперкальциемия может проявляться агрессивными нарушениями метаболизма костной ткани с переломами и болью в костях. Необходимо измерить уровень кальция и ПТГ с целью постановки предварительного диагноза.
Может проявляться в виде глубокой летаргии или комы в отделении неотложной помощи. Измерение уровня кальция и проведение ЭКГ должна быть частью исследования каждого пациента с нарушениями сознания. В случае выраженного повышения уровня кальция, а также при укорочении интервала QT необходимо проводить экстренные лечебные меры, после чего можно дальше проводить диагностику электролитных нарушений. У пациентов со злокачественными опухолями, скорее всего, при стационарном лечении будет диагностирована гиперкальциемия.
-
В случае комы, необходимо измерить уровень электролитов, включая кальций, глюкозу, мочевину, гематокрит, а также провести ЭКГ. Кальций может быть причиной комы только при уровне, намного превышающем 3,25 ммоль/л (13мг/дл). Гиперкальциемия может быть следствием дегидратации, а не прямой и непосредственной причиной понижения уровня сознания.
-
Регидратация с целью снижения уровня кальция. Петлевые диуретики с параллельным введением натрия хлорида с целью увеличения экскреции кальция. Бисфосфонаты с целью ингибирования деятельности остеокластов. Кальцитонин с целью ингибирования деятельности остеокластов и улучшения экскреции кальция с мочой.
Обычно, оценка пациента с гиперкальциемией начинается с первоначального результата анализа крови, с последующей диагностикой возможных причин такого нарушения.
Во-первых, врач должен собрать анамнез, расспросить о любых болях в костях, что может указывать на злокачественный процесс в костях или на метастазирование в длинные кости. Если пациент упоминает о снижении веса, это скорее говорит о злокачественном процессе, а не о гиперпаратиреозе.
В ходе сбора анамнеза можно выявить симптомы, которые свидетельствуют о высоком уровне кальция, например, камни в почках, которые характерны при гиперпаратиреозе, сонливость, легкая утомляемость, спутанность сознания, депрессия, раздражительность, запор и полиурия/полидипсия.
Могут наблюдаться классические симптомы со стороны ЖКТ (тошнота, рвота, боль в животе, язвенная болезнь, панкреатит). Собирают подробный анамнез применения лекарственных препаратов, включая добавки и патентованные лекарства, если таковые имеются. Хронический характер симптомов обычно свидетельствует о гиперпаратиреозе, тогда как острота жалоб более характерна для злокачественных процессов. Физический осмотр обычно не дает возможности подтвердить диагноз.
Наиболее распространенными причинами гиперкальциемии являются первичный гиперпаратиреоз и злокачественные новообразования, которые вместе составляют до 90% причин случаев заболевания.
Их можно дифференцировать, измерив уровень ПТГ, и одновременно повторно определить уровень кальция. Общий уровень кальция в сыворотке обычно достаточен для диагностики, однако если у пациента увеличена либо снижена концентрация белков плазмы, необходимо определить физиологически важную ионизированную фракцию кальция. Референтные значения общего кальция сыворотки: 2,13–2,63 ммоль/л (8,5 –10,5 мг/дл), ионизированного: 1,15– 1,27 ммоль/л (4,6–5,1 мг/дл).
При первичном гиперпаратиреозе повышен уровень ПТГ, несмотря на повышенный уровень кальция, свидетельствующий о нарушении обратной связи между уровнем электролита и гормоном, регулирующим его. При злокачественных процессах уровень кальция повышается вследствие нарушения эндокринной регуляции ПТГ-подобными пептидами, либо вследствие деструкции кости метастазами. При опухолевом процессе уровень ПТГ может быть очень низким или вообще не определяться, поскольку повышение уровня кальция ингибирует синтез ПТГ.
-
Случайно обнаруженная гиперкальциемия
-
Необходимо собрать анамнез, а также провести анализ крови на уровень кальция и ПТГ. Если повышены оба, причиной такого состояния является первичный гиперпаратиреоз, а если уровень ПТГ нормальный или низкий, то, скорее всего, причиной является злокачественное новообразование.
-
Исследования костей (включая сбор опрос по опорно-двигательной системе и рентгеновские исследования болезненных мест). При проведении исследования на уровень кальция необходимо одновременно проверить уровень ПТГ. Остеоденситометрия.
-
Необходимо измерить уровень электролитов, включая кальций, глюкозу, мочевину, гематокрит, а также провести ЭКГ. Кальций может быть причиной комы только при уровне, намного превышающем 3,25 ммоль/л (13мг/дл). Гиперкальциемия может быть следствием дегидратации, а не прямой и непосредственной причиной понижения уровня сознания.
Другие исследования, которые можно назначить в зависимости от вероятного диагноза: измерение суточной экскреции кальция с мочой при первичном гиперпаратиреозе, это может помочь дифференцировать семейную гипокальциурическую гиперкальциемию и первичный гиперпаратиреоз. Дополнительные исследования: уровень витамина D при подозрении на интоксикацию витамином D, измерение уровня креатинина и ультразвуковое исследование почек при подозрении на хроническую почечную недостаточность и вторичный гиперпаратиреоз, а также рентген органов грудной клетки для исключения саркоидоза (при наличии симптомов со стороны легких, например, кашля и одышки).
Читайте также:

