Гены при раке прямой кишки
Рак толстой кишки занимает 2-е место по смертности от злокачественных новообразований. По мере старения общества показатель летальности от рака этой локализации будет увеличиваться. Это неудивительно, если вспомнить об этиологии заболевания и особенностях патоморфологических изменений толстой кишки: ее слизистая оболочка представлена одноклеточным эпителием с быстрым периодом полного обновления и постоянной экспозицией к воздействию канцерогенных факторов.
Следовательно, ДНК этих клеток постоянно и быстро делится и реплицируется. В результате вероятность накопления ошибок и злокачественной трансформации со временем увеличивается. Модель рака толстой кишки, разработанная Vogelstein и соавт., иллюстрирует эти механизмы. Мутации гена-супрессора аденоматозного полипоза толстой кишки (adenomatous polyposis coli, АРС) ведут к разрастанию полипов толстой кишки в раннем возрасте. Для уточнения характера любого заболевания толстой кишки можно легко получить образец ткани путем биопсии. По мере роста полипа он становится доступен для обследования гастроэнтерологом с использованием ряда исследований. Рак толстой кишки хорошо изучен также потому, что существуют семьи, члены которых подвержены редкому заболеванию — семейному аденоматозному полипозу толстой кишки. У этих больных толстая кишка покрывается сотнями и тысячами полипов, один или несколько из которых, как правило, малигнизируются в зрелом возрасте.
Именно у этой категории больных впервые был обнаружен ген АРС. В большинстве спорадических опухолей толстой кишки выявляют соматические мутации гена АРС. В более редких семейных случаях отмечается мутация гена АРС, передающаяся по наследству и в связи с этим присутствующая во всех эпителиальных клетках кишечника, что и предрасполагает к развитию полипов. Соматическая мутация ведет к активации онкогена ras и ускорению роста полипа, который, тем не менее, еще остается доброкачественным. Однако с годами полип может приобрести мутации генов-супрессоров DCC и ТР53, которые ведут к автономному неконтролируемому росту злокачественных клеток рака толстой кишки.
Семейная предрасположенность к раку толстой кишки достаточно широко распространена и делится на две группы: с образованием полипов и без них. Полипозы включают семейный аденоматозный полипоз толстой кишки, синдром Пейтца— Егерса, семейный ювенильный полипоз и гиперпластический полипоз. Риск рака толстой кишки у всех больных с названными синдромами повышен. Например, медиана возраста появления рака толстой кишки при семейном аденоматозном полипозе составляет 40 лет.
К синдромам без полипоза относится наследственный неполипозный колоректальный рак (ННПКРР). У этих пациентов злокачественную опухоль толстой или прямой кишки выявляют в возрасте около 40 лет. У большинства больных ННПКРР идентифицируют генетические дефекты в системе репарации ДНК. Мутации происходят в основном в гене MLH1, однако результаты последних исследований свидетельствуют о частом поражении таких генов, как MSH2 и MSH6. ННПКРР сопровождается и другими онкологическими заболеваниями: раком эндометрия (РЭ), раком яичника (РЯ), раком молочной железы (РМЖ) и опухолями нервной системы.
Семейный рак толстой кишки составляет примерно 3—5 % всех случаев рака этой локализации. Однако риск рака толстой кишки также повышен у родственников больных любой формой этого заболевания. Поэтому в большинстве случаев рака толстой кишки можно наблюдать, по крайней мере отчасти, наследственный компонент. Факторы окружающей среды играют важную роль в развитии заболевания; полученные данные указывают, что диета с высоким содержанием клетчатки может снижать вероятность развития рака толстой кишки. Фактор риска — рацион питания с высоким содержанием жира и красного мяса.
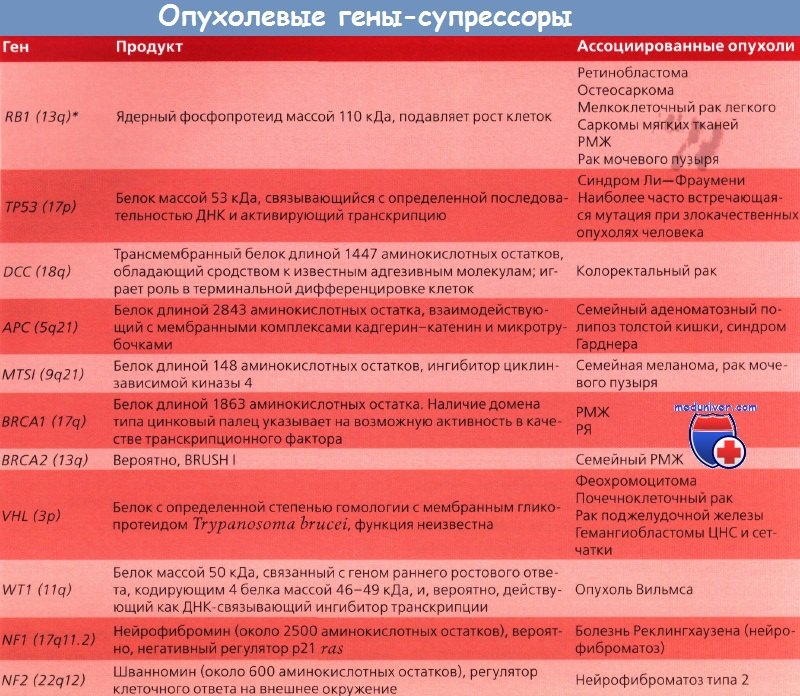
*Локализация на хромосоме
Молекулярные изменения, происходящие при раке толстой кишки, хорошо исследованы Vogelstein и соавт., подробно описавшими прогрессию нормального эпителия в рак. Первыми генами, для которых была установлена связь с раком толстой кишки, стали гены семейства ras, изначально выявленные в вирусах саркомы крыс. Эти гены наиболее часто обнаруживают в промежуточных полипах толстой кишки без дисплазии. В аденомах на ранних стадиях мутации ras встречаются редко, но в промежуточных полипах — регулярно, что свидетельствует о важной роли этих генов в раннем развитии рака толстой кишки.
Опухолевый ген-супрессор АРС принимает участие на самых первых этапах канцерогенеза при раке толстой кишки и был выявлен в исследованиях по изучению утраты гетерозиготности, показавших часто встречающуюся утрату длинного плеча хромосомы 5 (5q). Еще один ген, связанный с развитием рака толстой кишки, — ген-супрессор ТР53, расположенный на коротком плече хромосомы 17 (17р). Мутация этого гена — относительно позднее событие при раке толстой кишки. ТР53 — важный ген в контроле клеточного цикла и апоптоза. Утрата гена-супрессора DCC на длинном плече хромосомы 18 (18q) происходит на промежуточных и поздних этапах канцерогенеза при раке толстой кишки. Этот ген кодирует белок, ответственный за клеточную адгезию.
Ген DPC4, также расположенный на длинном плече хромосомы 18, вовлечен в сигнальную систему, связанную с трансформирующим фактором роста b.
При развитии рака толстой кишки происходит последовательное приобретение ряда мутаций. Для развития злокачественной опухоли обязательного прохождения всех этапов не требуется, однако предполагается, что необходимо по меньшей мере 6 или 7 генетических событий. У больных наследственным неполипозным колоректальным раком (ННПКРР) эти мутации развиваются вследствие неспособности эпителиальных клеток слизистой оболочки кишечника выявлять и устранять ошибки, происходящие во время нормального клеточного деления. Исследования Vogelstein и соавт. продемонстрировали модель, которая может быть применена и к другим опухолям.
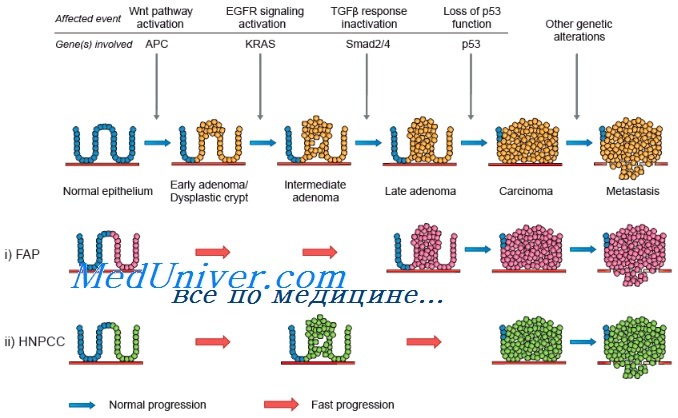
Генетика семейного рака кишечника
Когда говорят о генетически наследуемых видах рака, чаще всего упоминают рак кишечника, и не только потому, что данное заболевание входит в первую тройку наиболее распространенных видов раковых заболеваний. Известно, что, примерно, 25 процентов из всех людей, страдающих от рака кишечника, вполне могли приобрести данное заболевание наследственным путем, если эта болезнь встречалась и у их более ранних поколений в семье. Эта внушительная цифра послужила причиной многочисленных исследований генетической составляющей данного заболевания. В результате, ученые выделили два основных вида наследуемого рака толстого кишечника.
-- Полипозный синдром.
-- Неполипозный синдром.
Полипозный синдром.
Данный вид заболевания, который называют еще семейным полипозом толстой кишки, является крайне редким явлением. У тех, у кого развилось данное состояние, появляется буквально тысячи полипов – маленьких наростов ткани на стенках толстой кишки. Эти полипы образованы редчайшим типом клеток, которые называют аденоматозными клетками. Само заболевание передается по наследству посредством доминантного гена, хотя встречаются еще более редкие, приобретенные случаи данного вида рака прямой кишки, которые являются результатом мутировавшего (изменившегося) гена.
Считается, что семейный полипоз толстой кишки обусловлен потерей генетического материала одной из хромосом. Этот утраченный генетический материал может содержать гены, выполнявшие функцию так называемых супрессоров рака, благодаря чему, большинство людей застраховано от развития данного заболевания. В случае же наличия данного заболевания, полипы, большей частью, обнаруживаются, примерно, в возрасте 25-ти лет. В более редких случаях они появляются еще до наступления пубертатного периода. На самом деле, полипы считаются предраковым состоянием, которое, если его не лечить, приводит к развитию рака прямой кишки практически у всех пациентов, примерно, к сорокалетнему возрасту.
Неполипозный синдром.
Существуют люди с наследственной предрасположенностью к развитию рака кишечника, у которых отсутствуют полипы в толстой кишке. Фактически, речь идет о внушительной группе людей, риск развития рака кишечника у которых составляет 50 процентов. В их случае болезнь возникает в определенной части кишечника, развиваясь крайне быстро. Как правило, в таких семьях можно встретить достаточно много случаев различных раковых заболеваний среди многих предыдущих поколений. Ученым удалось обнаружить особенно явную связь между колоректальным раком и раком матки (рак эндометрия) у женщин. И снова причиной появления данного заболевания у индивидуума является доминантный ген, полученный по наследству. Средний возраст пациентов, у которых обнаруживает рак кишечника, в этом случае не превышает пятидесяти лет, что на 10-15 лет меньше, чем у всей остальной мужской популяции планеты, страдающей от рака толстой кишки.
Генетический скрининг и рак кишечника.
Генетический скрининг рака кишечника действительно дает возможность выявить потенциальный риск развития данного заболевания. Однако, специалисты уверены, что людям, у которых кто-то из предыдущих поколений страдал от полипозного или неполипозного колоректального рака, имеет смысл проходить регулярное и тщательное визуальное обследование на предмет выявления данного заболевания. Рекомендуется начинать обследования с двадцатилетнего возраста и делать их регулярно, сообразно рекомендациям специалистов. Визуальное обследование с помощью метода эндоскопии считается гораздо более надежным и эффективным мероприятием для обнаружения заболевания, нежели чем другие тесты по выявлению опухоли толстой кишки.
Рак часто наблюдается у членов одной семьи, объективно подтверждена наследственная природа некоторых злокачественных опухолей. Есть точка зрения, что наследственная предрасположенность — самая вероятная причина всех онкологических заболеваний, и только дело времени, чтобы наука точно установила, мутация какого гена за какой конкретный рак отвечает. Но уже сейчас наследственную передачу рака можно прервать.
Если у человека возникло онкологическое заболевание, очень важно выяснить, есть ли в его роду другие случаи злокачественных новообразований. Семьям, в которых имеется более одного такого случая, нужно пройти консультацию врача-генетика, чтобы понять, есть ли в семейной истории основания для подозрений на наследственный характер патологии. Особенно настораживающим признаком будет онкологическое заболевание в нескольких поколениях семьи. Одним из основных методов работы врача-генетика является составление родословных. Другая важная часть медико-генетической консультации — осмотр и опрос пациента: наследственные заболевания нередко проявляются специфическими признаками.
Принципиальным отличием наследственного рака является возможность его прогнозировать путем выявления патогенных мутаций. На первом этапе семьям, в которых имеется более одного случая развития рака, рекомендуется пройти консультацию врача-генетика, по результатам которого можно будет понять, есть ли в семейной истории основания для подозрения на наследственный характер патологии.
Если в процессе консультации возникают подозрения на наследственную природу заболевания, то следующий этап — целенаправленное генетическое тестирование, поиск мутаций, которые могут вызывать конкретное заболевание. Одни исследования позволяют обнаружить изменения в самом гене, другие — в белке, который кодируется измененным геном. Один ген может претерпеть до 300 мутаций.
В последние годы найдены мутации, ответственные за возникновение и развитие рака молочной железы, яичников, толстой кишки и др. Цель генетического тестирования, или скрининга,— выявить риск возникновения заболевания до появления симптомов. Это дает возможность в одних случаях провести своевременное лечение, в других — рекомендовать меры, позволяющие избежать передачи наследственного заболевания потомству. Мутации генов найдены для нескольких видов рака, тесты на некоторые из них уже используют в клинике — например, тесты на рак груди и кишечника.
От предков или не от предков
Все онкологические заболевания имеют генетическую природу, поскольку при раке гены, отвечающие за правильное деление клетки, повреждены. Но в одних случаях имеют место наследственные мутации, а в других — приобретенные. Результатом повреждения (мутации) гена во всех случаях является бесконтрольное неограниченное деление клеток, что и является сутью ракового процесса.
Несмотря на то что онкологические заболевания имеют генетическую природу, только 10–15% из них передаются по наследству. Почему важно знать, наследственный или ненаследственный рак? Потому что если установлена его наследственная природа, то есть выявлена мутация, вызвавшая его, то известен прогноз и понятна тактика в отношении самого больного и его родственников. Особенно отчетливо наследование мутации прослеживается в случаях так называемого семейного рака молочной железы и яичников, при семейном аденоматозном полипозе и различных опухолевых синдромах (Линча — рак толстой кишки, Ли-Фраумени — разнообразные саркомы и др.). Многие люди, сами будучи здоровыми, являются носителями мутаций, приводящих к наследственным заболеваниям. Если носители одной и той же мутации — оба родителя, заболевание становится неизбежным. Генетическое тестирование позволяет это выявить.
Следует подчеркнуть, что наличие мутации не означает заболевания. Мутация может сидеть в гене много лет до того, как начнет развиваться опухоль. Но, зная про мутацию, врачи могут назначить рациональный режим обследования и профилактического лечения.
Например, у женщин—носительниц гена BRCA1 в 95% случаев в течение жизни разовьется рак груди и в 65% — рак яичников, причем часто рак развивается в молодом возрасте, до 50 лет. Это означает, что носительница должна все время находиться под наблюдением, а в некоторых случаях целесообразно ставить вопрос о профилактическом удалении груди и (или) яичников. У всех на слуху история Анджелины Джоли, которая настояла на удалении обеих молочных желез, поскольку у нее обнаружили мутацию гена BRCA1.
Специалисты знают результаты исследования ткани удаленных молочных желез у 54 шведских женщин—носительниц этого гена в возрасте до 51 года. Ни у одной из них обследование не показывало опухоли груди до операции, но гистологическое изучение удаленной ткани выявило наличие раковых клеток у пяти (10%!) из них.
К профилактической хирургии прибегают и при семейном аденоматозном полипозе, при котором вероятность развития рака толстой кишки после 40 лет достигает 100%, и при других онкологических заболеваниях, если установлена онкогенная мутация.
Понятно, что женщины с отрицательным результатом теста на мутации генов BRCA1 и BRCA2 не застрахованы от спорадического рака груди и яичников. Однако вероятность его возникновения несопоставимо ниже, чем у женщин с положительным тестом.
Женщине следует заподозрить у себя предрасположенность к наследственному раку груди, пройти консультацию врача и генетика и генетическое тестирование, если в семье:
— было более одного случая рака груди или яичников по женской линии (у матери, бабушки, тетки, сестер и т. д.);
— заболевание было диагностировано в молодом возрасте (до наступления климакса);
— были случаи рака груди у мужчины;
— были больные c множественными опухолями (например, у одного человека — рак груди, толстой кишки, матки, рак поджелудочной железы и т. д.);
— были случаи двустороннего рака обеих молочных желез или обоих яичников.
Тестирование и его последствия
Генетическое тестирование имеет несколько преимуществ. Отрицательный результат может принести человеку облегчение, избавить от страха ожидания тяжелой болезни, от которой, возможно, погибли его близкие, а также от регулярных обследований, которые должны быть обязательны в семьях с высоким онкологическим риском. Положительный результат дает человеку возможность принимать обдуманные решения о будущем своем и своего потомства.
Сегодня возможна профилактика наследственного рака, то есть возможность не передать от родителей потомству ген, несущий опасную мутацию. Метод, который позволяет это сделать, называется преимплантационная генетическая диагностика (ПГД). Он заключается в следующем: для пары выполняют ЭКО, проводят генетическую диагностику полученных эмбрионов и переносят в матку женщины только те из них, в которых нет онкогенных мутаций. У родившегося ребенка их не будет, а значит, не будет и наследственного рака.
Открытое письмо Анджелины Джоли, New York Times, 14 мая 2013 года
ПГД проводится не на всем эмбрионе, а на нескольких клетках, которые получают путем его биопсии. Доказано, что биопсия не оказывает влияния на здоровье и состояние ребенка. Другими словами, ПГД не снижает частоту наступления беременности и безопасна для будущего ребенка.
Кроме мутаций, отвечающих за развитие рака груди и яичников, установлены мутации, несущие предрасположенность к меланоме, раку желудка, матки, предстательной, поджелудочной и щитовидной железы, толстой и прямой кишки. Если мутация определена и в семье есть люди, которые хотят иметь ребенка, важно, чтобы они знали о возможности предотвратить передачу следующим поколениям этой мутации и связанного с ней рака с помощью ЭКО и ПГД.
У четверти людей с онкологическими заболеваниями кишечника обнаруживается отягощенный семейный анамнез. Примерно 10 % эпизодов рака толстой кишки связаны с наследственным фактором. Риск развития опухоли высок при наличии у пациента аденоматозного полипоза и синдрома Линча.
Причины наследственного рака толстой кишки
Перерождение нормального эпителия в раковые образования связано с определенными мутациями в генах, которые могут быть врожденными (в гене АРС) и приобретенными (амплификация гена MYC, точечные мутации гена KRAS, делеции определенных участков хромосом 5, 8, 17, 18).
В 50 % случаев наследственного рака и крупных аденоматозных образований толстой кишки выявляют точечные мутации гена KRAS. В 75 % случаев аденокарционом обнаруживается делеция 17р (в гене TP53), при 30 % крупных аденоматозных полипов и аденокарцином — делеция длинного плеча 5q (в гене APC).
Наследственный аденоматозный полипоз, связанный с мутацией гена-супрессора опухолевого роста APC (в локусе 5q21), грозит развитием рака толстой кишки к 55 годам. Синдром Линча, обусловленный мутациями в генах MSH2 , MLH1 и MSH6 (хромосомы 2 и 3) или гена PMS2 (хромосома 7), характеризуется ранним развитием новообразований (20 лет) и менее агрессивным течением болезни.
Диагностирование наследственного рака толстой кишки
Симптомы заболевания включают в себя: кровь в кале, признаки анемии, кишечной непроходимости, болевой синдром. Больной теряет вес, ухудшается аппетит, появляется слабость, повышается температура тела.
Опухоль обнаруживается во время колоноскопии с биопсией. О присутствии опухолевого процесса могут рассказать исследование кала на скрытую кровь, анализы крови на онкомаркеры, а также гастроскопия, УЗИ, рентгенография, сцинтиграфия.
- возраст пациента на момент обнаружения новообразования — не старше 50 лет;
- множественные раковые образования в кишечнике или других органах, которые характерны для наследственного неполипозного рака толстой кишки;
- наличие у больного признаков генетической нестабильности — Microsatellite Instability (MSI);
- в семье пациента имеется минимум 2 случая опухолей кишечника родственников младше 50 лет;
- минимум 3 случая онкообразований кишечника в семье, вне зависимости от возраста обнаружения патологии.
Опухоль, удаленная во время операции, подлежит обследованию на предмет:
- генетической нестабильности MSI;
- иммуногистохимического анализа белков Mismatch Repair (MR).
Если результаты одного из этих анализов указывают на наследственный рак толстой кишки, назначают генетическое тестирование (анализ крови на мутации в генах DNA Mismatch Repair Genes). Если тест подтверждает присутствие патологии, то такое исследование рекомендуется и родственникам больного.
Лечение наследственного рака толстой кишки
Проктоколэктомия — предпочтительный метод терапии заболевания. При поражении лимфоузлов показана лимфаденэктомия, в случае отдаленных метастазов — паллиативные вмешательства.
Профилактика
Носители мутации находятся в группе риска по наследственному раку толстой кишки и нуждаются в регулярных скрининговых обследованиях для раннего выявления онкопатологии (колоноскопия, анализы на онкомаркеры СА125, СА19-9, карциноэмбриональный антиген и др.).

- Группа особого риска: причины рака прямой кишки
- Полипы кишечника
- Стадии рака прямой кишки
- Чем может проявляться рак прямой кишки?
- Метастазы при раке прямой кишки
- Симптомы рака прямой кишки
- Диагностика рака прямой кишки
- Лечится ли рак прямой кишки?
- Варианты лечения рака прямой кишки на разных стадиях
- Профилактика рака прямой кишки
- Продолжительность жизни
- Цены на лечение рака прямой кишки
Группа особого риска: причины рака прямой кишки
В большинстве экономически развитых стран, за исключением Японии, рак прямой кишки — один из самых частых типов рака, встречающийся и у мужчин, и у женщин. Статистически достоверна взаимосвязь частоты развития рака прямой кишки и большого количества употребляемых в пищу мяса и животных жиров, дефицита в рационе питания грубой клетчатки и пищевых волокон, а также малоподвижного образа жизни. Рак прямой кишки занимает стабильное 3-е место в структуре заболеваемости злокачественными новообразованиями органов желудочно-кишечного тракта, составляет 45-55% среди новообразований кишечника.
К предраковым заболеваниям прямой кишки относят хронические воспалительные заболевания толстого кишечника: хронический проктит, хронический неспецифический язвенный проктосигмоидит, болезнь Крона.
Полипы кишечника
К заболеваниям с наиболее высокой онкогенностью относят полипоз кишечника из-за высокой частоты малигнизации (озлокачествления). Трансформация в рак происходит как при одиночных полипах в прямой кишке, так и при наличии множественных очагов. Особенно это касается случаев наследственного полипоза в семье.
В соответствии с классификацией Всемирной Организации Здравоохранения, аденомы кишки делятся на три разновидности: тубулярные, ворсинчато-тубулярные и ворсинчатые. Важную роль имеет первичная гистологическая диагностика биопсии полипов, полученной в ходе колоноскопии: например, ворсинчатые аденомы малигнизируются в 35-40% случаев, а в случае трубчатых аденом риск озлокачествления ниже - до 2-6%. Риск озлокачествления увеличивается в зависимости от размеров аденомы, особенно если ее диаметр более 1 см.

Когда опухоль прорастает в подслизистую основу, такой рак уже считается инвазивным, он может распространяться в лимфатические узлы и давать отдаленные метастазы.
Стадии рака прямой кишки
Опухоли прямой кишки классифицируются в соответствии с общепринятой системой TNM, в которой учитываются характеристики первичной опухоли (T), наличие очагов поражения в регионарных лимфатических узлах (N) и отдаленных метастазов (M).
Буква T может иметь индексы is, 1, 2, 3 и 4. Tis – опухоль, которая находится в пределах поверхностного слоя слизистой оболочки, не распространяется в лимфатические узлы и не метастазирует. T4 – рак, который пророс через всю толщу стенки прямой кишки и распространился в соседние органы.
Буква N может иметь индексы 0, 1 и 2. N0 – опухолевых очагов в регионарных лимфоузлах нет. N1 – очаги в 1–3 регионарных лимфоузлах или поражение брыжейки. N2 – очаги более чем в трех регионарных лимфатических узлах.
Буква M может иметь индексы 0 или 1. M0 – отдаленные метастазы отсутствуют. M1a – отдаленные метастазы в одном органе. M1b – отдаленные метастазы в двух и более органах, либо опухолевое поражение брюшины .
В зависимости от этих характеристик, выделяют пять стадий:
Чем может проявляться рак прямой кишки?
Прямая кишка (лат. rectum) — это конечный участок толстого кишечника длиной около 14-18 см, в котором заканчиваются пищеварительные процессы и происходит формирование каловых масс. Прямая кишка состоит из нескольких анатомических участков, имеющих различное эмбриональное происхождение и гистологическое строение , что обуславливает существенные различия в характере течения рака прямой кишки в зависимости от уровня её поражения.
Прямая кишка делится на 3 части:
- анальную (промежностную), длиной 2,5 – 3,0 см, в которой расположены мышцы-сфинктеры, управляющие процессом дефекации,
- среднюю – ампулярную, длиной 8,0-9,0 см, в которой происходит всасывание жидкой части пищевого комка и формируются каловые массы,
- надампулярную, покрытую брюшиной, длиною около 4,0-5,0 см.
Злокачественные новообразования прямой кишки чаще всего локализуются в ампулярном отделе (до 80 % случаев), реже всего - в аноректальном отделе (5-8 %).
В ампулярном и надампулярном отделах прямой кишки, покрытом однослойным железистым эпителием, чаще наблюдается железистый рак - аденокарцинома, солидный рак, перстневидно-клеточный, смешанный, скирр. В целом аденокарцинома составляет 96% от всех случаев колоректального рака. Эта опухоль развивается из железистых клеток слизистой оболочки, которые продуцируют слизь. Чаще всего, употребляя термин "колоректальный рак", врачи имеют в виду именно аденокарциному.
Аноректальный отдел прямой кишки, выстланный многослойным плоским неороговевающим эпителием, чаще поражает плоскоклеточный рак и меланома. Плоскоклеточный рак составляет около 90% злокачественных опухолей аноректального отдела.
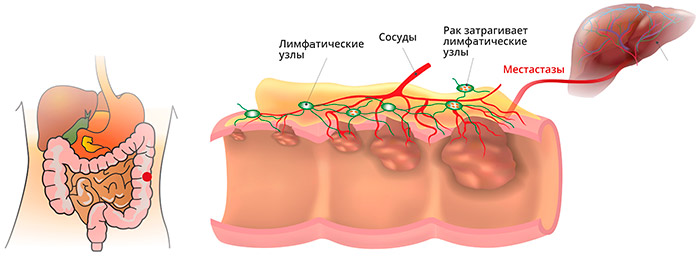
Метастазы при раке прямой кишки
Анатомические особенности прямой кишки, ее кровоснабжения и лимфооттока, определяют и характер преимущественного распространения метастазов:

Симптомы рака прямой кишки
- Первыми признаками рака прямой кишки при большинстве локализаций являются нарушения стула в виде хронических запоров и поносов, ощущения неполноценной дефекации, ложные позывы к ней (тенезмы), выделения из анального канала (слизь, кровь, гной).
- Кроме того, у большинства пациентов рано появляется болезненность при дефекации, обусловленная прорастанием опухолью стенок кишки и нарушением функции соответствующих нервов.
- При поражении мышц, формирующих анальные сфинктеры , развивается недержание кала и газов.
- Боли являются первым признаком рака прямой кишки только при раке аноректальной зоны c вовлечением в опухолевый процесс сфинктера прямой кишки. Характер боли при раке прямой кишки на ранних стадиях эпизодический, далее она может стать постоянной.
- При растущих в просвет кишки (экзофитных) и блюдцеобразных опухолях, опухолях-язвах первыми проявлениями онкологического заболевания может стать кровотечение или воспалительный процесс. Кровотечение отмечается у 75-90 % больных раком прямой кишки чаще всего в виде примеси крови в кале.
- Вместе с кровью на поздних стадиях рака могут выделяться слизь и гной.
- Ухудшение общего самочувствия (общая слабость, быстрая утомляемость, анемия, похудение, бледность кожных покровов), обусловленное длительной хронической кровопотерей и опухолевой интоксикацией, характерно для поздних стадий злокачественных образований прямой кишки.
Диагностика рака прямой кишки
Основу диагностики рака прямой кишки составляют эндоскопические методики и биопсия. Опухоль можно выявить с помощью проктоскопа – специального инструмента с миниатюрной видеокамерой, который вводят в прямую кишку. При этом врач может увидеть новообразование, определить его размеры, положение, оценить, насколько близко оно расположено по отношению к сфинктеру.
Колоноскопия позволяет оценить состояние не только прямой, но и всей толстой кишки. При этом через задний проход вводят колоноскоп – инструмент в виде тонкой длинной гибкой трубки с видеокамерой. Его проводят через всю толстую кишку, осматривая ее слизистую оболочку. Колоноскопия – безболезненная процедура, во время нее пациент находится в состоянии медикаментозного сна.
Во время эндоскопии проводят биопсию: врач получает фрагмент патологически измененного участка слизистой оболочки и отправляет в лабораторию для цитологического, гистологического исследования.
Для оценки стадии рака прямой кишки и поиска метастазов применяют УЗИ брюшной полости, рентгенографию грудной клетки, МРТ, компьютерную томографию, ПЭТ-сканирование. Трансректальное УЗИ проводят с помощью специального ультразвукового датчика, который вводят в прямую кишку. Исследование помогает оценить, насколько опухоль распространилась в окружающие ткани за пределами кишки.
Лечится ли рак прямой кишки?
В соответствии с международными протоколами по результатам диагностического обследования определяется распространенность рака прямой кишки. При этом в дополнение к международной классификации TNM, часто применяют разделение рака на 1-4-ю стадии, а также классификацию Дюка, учитывается гистологическое строение опухоли, степень дифференцировки и особенности метастазирования в зависимости от расположения в прямой кишке, наличие осложнений.
Правильно поставленный диагноз стадии опухолевого процесса при раке прямой кишки позволяет выбрать наиболее рациональную схему лечения с учетом международных руководств, включив в нее хирургическую операцию, лучевую терапию, химиотерапию и терапию таргетными препаратами.
Варианты лечения рака прямой кишки на разных стадиях
На выбор тактики лечения при раке прямой кишки влияют разные факторы, но ведущее значение имеет стадия опухоли.
На 0 и I стадии обычно показано только хирургическое вмешательство. Иногда можно ограничиться удалением полипа – полипэктомией. В других случаях выполняют трансанальную резекцию прямой кишки, низкую переднюю резекцию, проктэктомию с коло-анальным анастомозом, абдоминально-промежностную резекцию. Если операция не может быть проведена из-за слабого здоровья пациента, применяют лучевую терапию,
На II стадии хирургическое лечение сочетают с химиотерапией и лучевой терапией. Наиболее распространенная схема выглядит следующим образом:
- На начальном этапе пациент получает курс химиотерапии (обычно 5-фторурацил или капецитабин) в сочетании с лучевой терапией. Это помогает уменьшить размеры опухоли и облегчить ее удаление.>
- Затем выполняется хирургическое вмешательство. Обычно это низкая передняя резекция, проктэктомия с коло-анальным анастомозом или абдоминально-промежностная резекция – в зависимости от локализации опухоли.
- После операции снова проводится курс химиотерапии, как правило, в течение 6 месяцев. Применяют разные комбинации препаратов: FOLFOX, CAPEOx, 5-фторурацил + лейковорин или только капецитабин.
На III стадии схема лечения будет выглядеть аналогичным образом, но объем хирургического вмешательства будет больше, так как в процесс вовлечены регионарные лимфатические узлы.
На IV стадии тактика зависит от количества метастазов. Иногда они единичные, и их можно удалить, как и первичную опухоль. Операцию дополняют химиотерапией и лучевой терапией. Для борьбы с очагами в печени может быть применена внутриартериальная химиотерапия, когда раствор лекарственного препарата вводят непосредственно в артерию, питающую опухоль.
Если метастазов много, удалить их хирургическим путем невозможно. В таких случаях бывают показаны лишь паллиативные операции, например, для восстановления проходимости кишки, если ее просвет заблокирован опухолью. Основным же методом лечения является применение химиопрепаратов и таргетных препаратов. Врачи в Европейской клиники подбирают лечение в соответствии с международными протоколами и особенностями злокачественной опухоли у конкретного больного.
Профилактика рака прямой кишки
Хотя защититься от рака прямой кишки, как и от других онкологических заболеваний, на 100% невозможно, некоторые меры помогают снизить риски:
- Ешьте больше овощей и фруктов, сократите в рационе количество жирного мяса.
- Откажитесь от алкоголя и курения.
- Регулярно занимайтесь спортом.
- Некоторые исследования показали, что защититься от колоректального рака помогает витамин D. Но прежде чем принимать его, нужно проконсультироваться с врачом.
- Если в вашей семье часто были случаи рака прямой кишки, вам стоит проконсультироваться с клиническим генетиком.
- Если у вас диагностировали наследственное заболевание, которое приводит к образованию полипов и злокачественных опухолей кишечника, вам нужно регулярно проходить колоноскопию. Запись на консультацию круглосуточно
Читайте также:

