Ген р53 его роль в формировании опухолей
Ген р53 — страж генома. Ген р53 расположен на хромосоме 17р13.1 и является наиболее частой мишенью генетических повреждений в опухолях человека. Официальное название гена ТР53, а его белкового продукта — р53; с целью упрощения изложения материала далее оба будем называть р53. Около 50% опухолей человека ассоциированы с мутацией в этом гене.
Гомозиготная утрата р53 происходит практически во всех видах злокачественных опухолей, включая карциномы легкого, толстой кишки и молочной железы — три лидирующие онкологические причины летального исхода. В большинстве случаев инактивирующая мутация затрагивает оба аллеля р53 и развивается в соматических клетках (не в половых клетках). Реже некоторые лица наследуют мутантный аллель р53.
Как в случае с геном RB, наследование одного мутантного аллеля предрасполагает к развитию злокачественных опухолей, поскольку достаточно только одного дополнительного удара для инактивации второго, нормального аллеля. Эту болезнь называют синдромом Ли-Фраумени. При его наличии у пациента в 25 раз повышается риск развития злокачественной опухоли до 50 лет по сравнению с общей популяцией.
В отличие от пациентов, которые наследуют мутантный аллель RB, спектр опухолей у пациентов с синдромом Ли-Фраумени включает самые распространенные новообразования — саркомы, рак молочной железы, лейкемии, опухоли головного мозга и карциномы коры надпочечников. По сравнению со спорадическими опухолями злокачественные новообразования у пациентов с синдромом Ли-Фраумени манифестируют в более молодом возрасте, у таких пациентов также могут развиваться первично-множественные опухоли.
Многие стороны активности белка р53 связаны с его деятельностью как фактора транскрипции. Было установлено: несколько сотен генов, отвечающих за множество разнообразных процессов, регулируются р53. Но какой из них является ключевым для р53, остается неясным. Около 80% точечных мутаций, обнаруженных в злокачественных опухолях человека, располагаются в домене р53, связывающем ДНК.
В то же время эффект разных точечных мутаций чрезвычайно разнообразен: в некоторых случаях это полная утрата транскрипционной способности, в других — связывание и активация подмножества генов. Функционирование р53 может быть инактивировано не только приобретенными соматическими и наследственными мутациями, но и с помощью других механизмов. Как и с белком RB, нормальный р53 также может быть инактивирован трансформирующими белками определенных ДНК-вирусов (например, белком Е6 HPV), которые могут связываться с р53 и деградировать его. Предполагают, что в подавляющем большинстве опухолей без идентификации мутаций р53 все равно присутствует блокада сигнального пути р53 другими генами, регулирующими функционирование р53. Так, MDM2 и MDMX стимулируют деградацию р53; в злокачественных опухолях без мутаций р53 часто отмечается повышение экспрессии этих генов. Действительно, MDM2 амплифицирован в 33% сарком, что ассоциировано с утратой функциональной активности р53 в данных опухолях.
р53 препятствует злокачественной трансформации клеток тремя взаимосвязанными механизмами: путем активации временной остановки клеточного цикла и вывода клетки из него (это называется состоянием покоя), индукции постоянной остановки цикла и вывода клетки из него (это называется состоянием старения) или индукции запрограммированной смерти клетки (апоптоза).
При этом остается непонятным, почему р53 подвергается репрессии, в то время как в большинстве случаев он активирует транскрипцию. В связи с этим обратимся к получившим не так давно известность микроРНК. Установлено, что р53 активирует транскрипцию семейства mir34 микроРНК (mir34a, mir34b, mir34c). МикроРНК (см. главу 5) присоединяется к родственным последовательностям в 3'-нетранслируемых участках мРНК, предотвращая их трансляцию. Интересно, что блокирование mir34 значительно нарушает ответ р53, в то время как индуцированной извне экспрессии mir34, не сопровождающейся активацией р53, достаточно для остановки роста и апоптоза. Следовательно, mir34 микроРНК способна повторять многие функции р53 и необходима для их выполнения. Мишенями для mir34 являются пролиферативные гены, например циклины, и антиапоптозные гены — Bcl-2 и другие. Регулирование р53 посредством mir34 отчасти объясняет, как р53 репрессирует экспрессию генов, а также то, что микроРНК играет критическую роль в ответе р53.
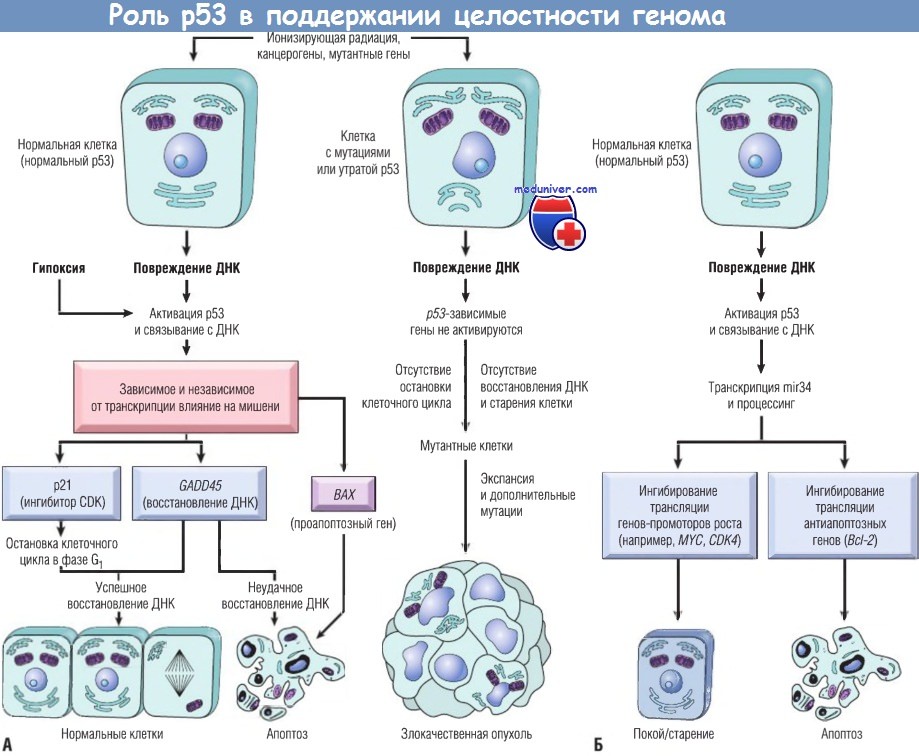
(А) Роль р53 в поддержании целостности генома.
Активация нормального р53 агентами, повреждающими ДНК, а также гипоксией приводит к остановке клеточного цикла в фазе G1 и индукции восстановления ДНК путем повышения транскрипции р21 (CDKN1A) и гена GADD45.
Успешное восстановление ДНК позволяет клеткам вновь входить в митотический цикл; если восстановление ДНК неудачно, р53 инициирует апоптоз или старение клетки.
В клетках с утратой или мутациями р53 остановки клеточного цикла или восстановления ДНК при ее повреждении не происходит, генетически поврежденные клетки пролиферируют и подвергаются в конечном счете злокачественной трансформации.
(Б) р53-индуцированная репрессия генов путем активации микроРНК. р53 активирует транскрипцию mir34 семейства микроРНК.
mir34 подавляет транскрипцию как пролиферативных генов, например циклинов, так и антиапоптозных генов, например Всl-2.
Подавление этих генов может усиливать как вхождение клеток в состояние покоя или старения, так и апоптоз.
CDK — циклин-зависимые киназы; ДНК — дезоксирибонуклеиновая кислота.
Как р53 удается определить повреждение ДНК и адекватность ее восстановления, остается непонятным. Ключевыми инициаторами повреждения ДНК являются две взаимосвязанные протеинкиназы: мутантная атаксии-телеангиэктазии (ATM) и атаксии-телеангиэктазии и Rad3 (ATR). В название гена ATM отражена первоначальная идентификация его мутации в половых клетках у пациентов с синдромом атаксиителеангиэктазии. Организм пациентов с этой болезнью не способен устранить определенные виды повреждений ДНК, больные часто страдают от злокачественных опухолей. Типы повреждений, определяемых ATM и ATR, различны, но регуляторные пути, которые они активируют, сходны.
После активации ATM и ATR фосфорилируют многие молекулы, включая р53 и белки восстановления ДНК. Фосфорилирование этих двух молекул приводит к паузе в клеточном цикле и восстановлении ДНК соответственно.
р53 также вызывает экспрессию определенных белков, участвующих в восстановлении ДНК, например GADD45, что помогает процессу восстановления ДНК. Помимо этого р53 может стимулировать регуляторные пути восстановления ДНК, независимые от механизмов транскрипции. Если повреждения ДНК успешно устранены, то р53 стимулирует транскрипцию MDM2 и соединяется с ним, что приводит к разрушению р53 и снятию блокады клеточного цикла. Если повреждения устранить невозможно, то клетка может подвергнуться р53-индуцированному старению или р53-опосредованному апоптозу.
р53-индуцированное старение — постоянная остановка клеточного цикла, характеризующаяся определенными изменениями в морфологии и экспрессии генов, отличающимися от таковых в состоянии покоя или временной остановки клеточного цикла. Для старения клеток необходима активация р53 и/или RB и экспрессия их посредников, например CDKI. Механизмы старения неясны, но, вероятно, сопряжены с глобальными изменениями хроматина, которые существенно и надолго нарушают экспрессию генов.
Локусы гетерохроматина, ассоциированные со старением клеток, содержат пролиферативные гены, регулируемые E2F. Подобные изменения вызывают выраженное и необратимое нарушение экспрессии мишеней E2F. Старение, как и другие р53-опосредованные эффекты, может быть обусловлено разнообразными стрессорными факторами, такими как беспрепятственная экспрессия онкогенов, гипоксия и укорочение теломер.
р53-индуцированный апоптоз клеток с необратимым повреждением ДНК — наивысшая точка антибластомной резистентности клетки. р53 запускает транскрипцию с помощью нескольких проапоптозных генов, например ВАХ и PUMA (общепринятое название ВВС3). Точно не установлено, каким образом клетка принимает решение, восстанавливать ли ей поврежденную ДНК или погибнуть путем апоптоза. Как оказалось, способность р53 стимулировать и поддерживать гены восстановления ДНК намного выше, чем сродство к проапоптозным генам. Следовательно, сигнальный путь восстановления ДНК запускается первым, а р53 продолжает накапливаться в клетке. В результате к моменту, когда становится очевидной невозможность устранить повреждение ДНК, в клетке уже присутствует достаточное количество р53, позволяющее запустить апоптоз, и клетка погибает. Хотя данная схема в целом верна, но, вероятно, существуют специфические ответы клеток, когда одни гораздо раньше подвергаются апоптозу, а другие — старению.
Подобные различия в ответных реакциях могут быть связаны с функционированием других членов семейства р53, которые экспрессируются в различных клетках.
Способность р53 индуцировать апоптоз в ответ на повреждение ДНК имеет важное значение для лечения опухолей. Облучение и химиотерапия, два основных метода лечения злокачественных опухолей, основаны на индукции повреждения ДНК и последующего апоптоза клеток. Опухоли с нормальным р53 лучше отвечают на эту терапию, чем содержащие мутантные аллели гена, как, например, в случаях тератокарциномы яичка и острой лимфобластной лейкемии у детей. Напротив, опухоли при раке легкого и колоректальном раке, имеющие часто мутантный р53, являются относительно резистентными к химиотерапии и облучению. Различные методы терапии направлены на поддержание и усиление активности нормального р53, а также на поиск способов селективного киллинга клеток с нарушением функции р53.
- Рекомендуем ознакомиться со следующей статьей "Ген APC и его значение в развитии опухоли"

В течение многих лет наши родители, а также бабушки с дедушками, говорили нам, что наше здоровье основывается на наследственности (генетических характеристик), которую мы получаем от своих родителей. Наша генетика, действительно, играет важную роль в нашей физиологии, поэтому ранее, с широкой точки зрения, медицинская наука утверждала, что генетический материал - это самый важный фактор в нашем здоровье.
Сегодня мы понимаем, что многие аспекты нашей генетики контролируется факторами окружающей среды, с которыми мы взаимодействуем каждый день. Такое воздействие внешней среды называется - эпигенетикой, или генетической адаптацией через стимулы среды. Эпигенетика - это область генетики, в которой вариации, обусловленные экологическими раздражителями, включают и выключают гены и влияют на клетки через активность специфических генов.
Давайте внимательнее посмотрим на разницу между генетическими и эпигенетическими выражениями, когда речь идет о нашем здоровье.
Генетический полиморфизм - это изменения в последовательности ДНК, в частности генотипа. Примером может быть синдром Дауна, при котором обнаруживается тройная хромосома. Эта третья хромосома (мы должны иметь только 2) приводит к росту аномалий и умственной отсталости, которые происходят при в период развития в утробе матери.
Эпигенетическая адаптация - это изменение генетической экспрессии (активности) без каких либо модификаций в последовательности ДНК. Определенные гены включаются и выключаются, реагируя на стимулы внешней среды, которое действует на них. Такие изменения происходят уже после рождения, когда организм человека подвергается воздействию различных экологических факторов и гены адаптируются к этим событиям.

В частности, цвет глаз и кожи вы получаете на основе секвенирования ДНК в клетках организма, а развитие хронического заболевания - это результат эпигенетики, когда внешняя среда, в которой вы подвергались воздействию, смогла серьезно изменить выражения ваших генов. И это хорошая новость, потому что если мы можем изменить наше генетическое выражение в зависимости от образа жизни и окружающей среды, это также означает, что мы можем улучшить нашу генетическую экспрессию (активность генов) с помощью позитивных привычек образа жизни. Снижение стресса, потребление хорошей здоровой пищи, отсутствие токсинов, периодическое очищение организма, спокойная психологическая обстановка и адекватный отдых - все это поможет защитить нашу генетическую стабильность и уменьшить риск развития хронических заболеваний.
Одним из генетических белков, роль которого в развитии раковых клеток детально изучают ученые, называется – ген p53. Этот белок действует как хранитель ДНК, выступая в качестве контрольных точек в клеточном цикле. Когда он чувствует аномалии в цикле роста, то активирует ген р21, который привязывается к процессу деления клетки-стимулирующего белка (cdk2) для того, чтобы остановить клеточный цикл. Во время нормального клеточного цикла клеточные ферменты инициируют процесс репарации ДНК. Если ДНК находится в состоянии ремонта, то ген р53 позволяет клетке вернуться в нормальный цикл роста и размножения, а если ДНК не может быть отремонтировано, то белок р53 отдает сигналы для начала клеточного апоптоза (программированной клеточной смерти).

В некотором смысле, р53 действует как охранник, который отслеживает, чтобы анормальный рост не возникал. Для того, чтобы выполнять свою работу, белок р53 регулирует экспрессию сотен генов. Его действие очень похоже на работу охрану президента. Если охрана чувствует угрозу, то одним телефонным звонком она могут мгновенно выключить связь во всем городе.
Если этот ген не чувствует, что клетка является достаточно сильной или достаточно здоровой, чтобы удовлетворять потребностям человеческого тела, то р53 будет стимулировать большее повреждение клеток, ведущих к клеточной смерти. Эти функции белка р53 препятствует прохождению повреждения ДНК в дочерних клетках (передача по наследству) и таким образом поддерживается геномная стабильность.
Различные исследования показали, что эпигенетические мутации, возникающие от хронического окислительного стресса, повреждают белковую матрицу в гене р53 и являются основным фактором в развитии рака. Эта мутация приводит к невозможности гену р53 блокировать анормальный рост. Некоторые формы мутации производят мутированный р53 белок, который стимулирует деление клеток и способствует развитию высоко инвазивных раков, которые более склонны к метастазированию и чаще приводят к к смерти.

Хронический окислительный стресс может вызвать повреждение гена p53, что делает его бесполезным и приводит к неспособности защитить геномную стабильность. Для того, чтобы быть активным, белок р53 должен связывать цинк, в то время как другие металлы, такие как медь, могут вытеснять цинк, что приводит к повреждению гена р53. Низкий уровень потребления цинка или избыточное количество меди и других тяжелых металлов, таких как свинец, алюминий, кадмий и ртуть, может привести к повреждению белка р53. Также многие другие экологические токсины могут привести к повреждению р53 и повышенной активности роста злокачественных опухолей.
К таким токсинам относятся:
- Пестициды
- Гербициды
- Хлор
- Фторид
- Загрязнение воздуха (PCAH)
- Радиационное облучение
Многие факторы, связанные с неправильным питанием и образом жизни увеличивают окислительный стресс, приводящий к мутации гена р53 и повышению риска рака.
К подобным факторам относятся:
- Высокий уровень сахара в крови
- Жареная пища (ГКА и акриламид)
- Транс-жиры в продуктах питания
Многие природные соединения действуют как мощные антиоксиданты и защищают организм от высоких уровней окислительного стресса. Эти соединения защищают ген p53 и позволяют ему оставаться устойчивым, поэтому он может адекватно выполнять свою роль в защите генома от ненормального развития клеток.
Некоторые из этих соединений, которые могут быть найдены в природных источниках пищи:
- Глутатион – из продуктов, содержащих серу, таких как лук, чеснок, молочный чертополох, крестоцветные овощи
- Сульфорафан - из крестоцветных овощей и проростков
- Куркумин – из растения ы
- Антоцианы - из ягод, красной капусты и красного лука
- Катехины – из зеленого чая, сырого какао, яблока и ореха пекан
- Ресвератрол – из кожуры винограда и ягод
- Каротиноиды – из фруктов и овощей, а также мяса животных, пасущихся на естественных пастбищах
Избегая воздействия экологических токсинов и потребляя продукты, богатые веществами, оказывающими положительные генетические воздействия, человек может управлять своими генами. Каждый день Вы выбираете продукты, которые затем употребляете в пищу и ежедневно ведете такой образ жизни, что в совокупности вносит свою лепту в развитие мутаций или укрепление активности вашего гена р53.

Мутации ТР53 — одно из самых частых событий в клетках злокачественных новообразований. По различным данным, от 50 до 80% солидных опухолей имеют различные повреждения ДНК в данном гене, около 90% из которых — миссенс мутации, то есть ведут к изменению структуры белка.
Апоптоз и злокачественные опухоли
Образование любой злокачественной опухоли сопряжено с нарушением механизмов апоптоза (программируемой клеточной гибели), которые контролируются белком р53. Его нормальное функционирование препятствует бесконтрольному делению неполноценных клеток. Если в результате какого-либо воздействия (облучения, химических веществ), в клетке возникают повреждения молекулы ДНК, белок р53 остановит ее деление до устранения повреждения, либо активирует ее программируемую гибель до того, как она успеет поделиться.
Данный механизм работает до тех пор, пока ген ТР53 имеет нормальную структуру. Когда в нем возникают мутации, в клетке накапливается мутантный белок, который не может выполнять свою основную функцию. Это нарушает механизмы включения апоптоза, что проявляется развитием новообразований, а при их существовании — способствует возникновению резистентности опухолевых клеток к проводимой химиотерапии.
Методы диагностики
На сегодняшний день существует несколько основных методов, позволяющих выявить наличие повреждений ДНК в гене ТР53:
- Секвенирование. В результате анализа происходит расшифровка последовательности целого гена, что позволяет найти все существующие в нем мутации. Они могут возникать как в нормальных клетках, увеличивая вероятность злокачественной трансформации, так и в опухолевых, что предопределяет дальнейшее прогрессирование новообразования. Данный метод применяется при подозрении на наследственные синдромы, когда мутации в гене являются инициирующим событием. В остальных случаях существуют значительные сложности с интерпретацией выявленных повреждений ДНК.
- Иммуногистохимический анализ (ИГХ). Данный метод исследования является основным в клинической практике. Он позволяет оценить экспрессию в исследуемой ткани белка р53, увеличение концентрации которого говорит о нарушении в работе соответствующего гена и, как правило, сопряжено с высокой пролиферативной активностью клеток (что позволяет дифференцировать дисплазии и злокачественные опухоли) и чаще всего является признаком неблагоприятного прогноза.
Метод ПЦР (полимеразная цепная реакция) для поиска повреждений ДНК в гене ТР53 является несколько устаревшим. В настоящее время используется он очень редко, когда необходимо подтвердить наличие или отсутствие конкретной мутации. Однако в связи с большим их разнообразием, в диагностическом процессе при наличии такой необходимости, в настоящее время предпочтение отдается полногеномному секвенированию.
Иммуногистохимический метод позволяет косвенно оценить состояние гена ТР53 по концентрации белка р53, которая для разных тканей в норме может значительно отличаться. Поэтому заключение о наличии нарушения делает морфолог.
Для проведения ИГХ, на первом этапе выполняется биопсия. Затем полученная ткань фиксируется на стекле, к ней добавляются специфические антитела, меченные красителем. Результаты могут быть оценены при помощи обычного светового микроскопа.
Таким образом, по количеству связанного красителя в ткани можно визуально оценить содержание белка. Система оценки двумерная:
- Оценивается интенсивность окраски от 0 до 3 баллов. При этом 0 баллов — окраска отсутствует, а 3 — сильное окрашивание.
- Оценивается доля окрашенных клеток, которая в зависимости от числового значения переводится в баллы.
В заключение отметим, что поскольку организм — сложная система, то мутации в одном гене лишь повышают вероятность, но не гарантируют развитие опухоли в организме. Поэтому любое исследование, показавшее то или иное нарушение в работе гена ТР53 должно быть интерпретировано доктором в комплексе с учетом клинической картины и использованного метода.

Раковые опухоли развиваются в организме не сами по себе. Они постоянно взаимодействуют с окружающими клетками, влияя на них при помощи поверхностных и секретируемых сигнальных молекул. Совокупность здоровых клеток разных типов, которые находятся в непосредственной близости от опухоли и контактируют с ней, называют микроокружением (см. Tumor microenvironment). Можно сказать, что опухоли эксплуатируют клетки микроокружения в своих интересах: фибробласты помогают им расти, кровеносные сосуды прорастают внутрь опухоли, чтобы доносить туда кислород и питательные вещества, а активность иммунных клеток микроокружения, наоборот, подавляется опухолью, лишая организм части защиты.
В микроокружении есть и нервные клетки, причем нервные волокна прорастают внутрь опухоли уже на самых ранних стадиях ее развития и продолжают прорастать по мере развития опухоли. Уже довольно давно известно, что чем гуще сеть нервных волокон внутри опухоли, тем хуже для пациента прогноз течения и исхода заболевания (см., например, C. Magnon et al., 2013. Autonomic Nerve Development Contributes to Prostate Cancer Progression). Судя по всему, сигналы от нервных волокон играют важную роль в стимулировании роста опухоли, формировании в ней сети кровеносных сосудов, прорастании опухоли в окружающие ткани и образовании метастазов. Но о молекулярных механизмах взаимоотношений нервов и раковой опухоли не было известно практически ничего. Недавно большой коллектив ученых под руководством Морана Амита (Moran Amit) из Онкологического центро имени М. Д. Андерсона, относящегося к Техасскому университету, предпринял попытку в них разобраться.
Анализ клинических данных пациентов с карциномой ротовой полости показал, что густая сеть нервных волокон в раковой опухоли положительно коррелирует с наличием в клетках мутаций гена TP53 и со значительным снижением выживаемости больных (рис. 2).

Рис. 2. Слева — выживаемость пациентов с карциномой ротовой полости. Хорошо видно, что у пациентов, у которых наблюдалась высокая плотность нервных волокон в опухоли (красный график), выживаемость сильно ниже. Справа — количество нервных волокон на единицу площади среза опухоли у пациентов, в клетках которых были найдены мутации в гене TP53 (красный столбик), и у пациентов без таких мутаций. Здесь хорошо видно, что густота сети нервных волокон положительно коррелирует с наличием мутаций в этом гене. Графики из обсуждаемой статьи в Nature
Поэтому ученые сосредоточились на исследовании взаимодействия между нервами и эпителиальными клетками (с нормальной или нарушенной функцией гена TP53). Эксперименты проводились на генно-модифицированных мышах, у которых можно было избирательно выключить ген TP53 в клетках эпителия (в качестве контроля использовались обычные лабораторные мыши). С помощью сильного канцерогена 4-нитрохинолин-1-оксида у мышей вызывали сначала предраковые изменения тканей ротовой полости, которые затем прогрессировали в раковые опухоли плоскоклеточной карциномы ротовой полости (oral cavity squamous cell carcinoma, OCSCC). И на ранних, и на более поздних стадиях развития рака в опухолях мышей с нарушенной функцией гена TP53 сеть нервных волокон была гораздо гуще, чем опухолях с нормально функционирующим этим геном.
Чтобы детальнее разобраться с нейрогенезом, из мышей извлекали нервные ганглии, которые затем культивировали in vitro совместно с нормальными кератиноцитами ротовой полости или с раковыми клетками, несущими различные мутации гена TP53. Отслеживая прорастание нервных волокон из ганглиев, ученые установили, что клетки с мутациями p53 null , p53 R273H (приводит к полной утрате функции белка) и p53 C238F (нарушает третичную структуру белковой молекулы) наиболее активно стимулировали рост нервных волокон. В то же время клетки с мутацией p53 G245D (нарушает связь р53 с ДНК) стимулировали рост не так активно.
Чтобы определить, каким путем передается к ганглиям фактор, влияющий на рост нервных волокон, ганглии инкубировали либо с очищенными внеклеточными везикулами (которые секретировались в культуральную среду раковыми клетками с нормальным или с мутантным TP53), либо с культуральной средой без везикул. Оказалось, что именно везикулы транспортируют этот фактор.
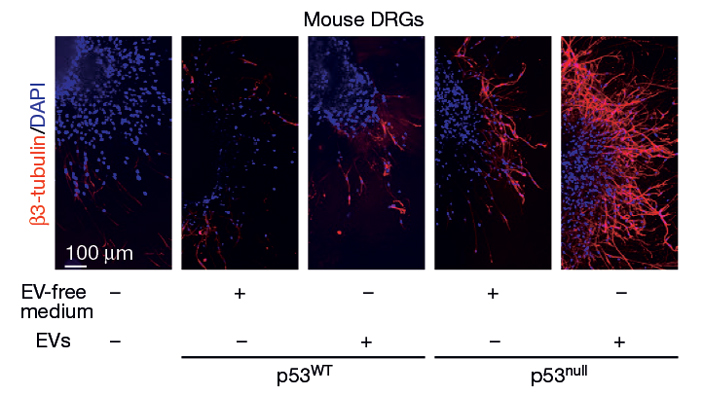
Рис. 3. Результаты культивирования нервных ганглиев мышей в среде, в которой либо совсем отсутствовали внеклеточные везикулы (слева), либо присутствовали везикулы, секретируемые раковыми клетками с нормальным или с мутантным геном TP53. Хорошо видно интенсивное прорастание нервных волокон в случае доступа к ганглию везикул из клеток с мутантным TP53. Рисунок из обсуждаемой статьи в Nature
Везикулы — главные переносчики РНК между клетками. В том числе они транспортируют так называемые микроРНК — малые некодирующие молекулы РНК длиной 18–25 нуклеотидов, которые участвуют в регуляции экспрессии генов на уровне транскрипции и трансляции. Сравнение наборов микроРНК из везикул раковых клеток с нормальным и мутантным р53 выявило существенное обогащение первых двумя конкретными видами микроРНК, которые обозначаются miR-34а и miR-141. Блокирование этих микроРНК с помощью специфических антагонистов показало, что рост нервных волокон ганглиев in vitro стимулировался только при блокировании miR-34а. При блокировании синтеза miR-34а в опухолях мышей in vivo наблюдалось увеличение количества нервных волокон, хотя ген TP53 не был нарушен. То же самое наблюдалось в опухолях мышей с нормальным геном TP53 при инъекции везикул из клеток, дефектных по этому гену.
В чем же разница между нервами, прорастающими в опухоли с нормальным и дефектным белком р53? Авторы сравнили наборы мРНК в нейронах. В нейронах ганглиев, обработанных везикулами дефектных по TP53 клеток, по сравнению с везикулами от клеток с нормальным TP53, наблюдалось угнетение транскрипции 1760 генов и усиление транскрипции 2495 генов. Активированные гены были связаны с выживанием и формированием нервов, с их ростом и ветвлением, подавленные — с основными функциями нейронов, в частности — с передачей нервных импульсов в синапсах. Оказалось, что дефектные по TP53 опухоли перепрограммировали нейроны из микроокружения в адреногенные (выделяющие адреналин и родственные ему соединения, маркированные тирозин-гидролазой), и именно они способствовали росту опухолей.
Несколько лет назад было показано, что лекарство карведилол, с помощью которого лечат гипертонию и некоторые сердечные заболевания, значительно снижает вероятность заболеть раком (C. S. Lin et al., 2015. Carvedilol use is associated with reduced cancer risk: A nationwide population-based cohort study). Карведилол блокирует адреногенные пути передачи нервных импульсов. Поэтому авторы решили проверить, может ли его противораковое свойство быть связано со способностью воздействовать на адреногенные нейроны и дефектные по TP53 опухоли мышей. Мышам прививали в язык клетки двух различных дефектных по TP53 линий OCSCC человека. Затем их делили на две группе: в одной мышам давали карведилол, в другой не давали. Сравнение темпов роста опухолей показало, что лечение карведилолом сильно подавляло их развитие.
Источник: M. Amit et al. Loss of p53 drives neuron reprogramming in head and neck cancer // Nature. 2020. DOI: 10.1038/s41586-020-1996-3.
Агастахис морщинистый, Agastachys rugosa, Louphantus tibeticus. Семейство многоколосников. Реликтовое растение. Иммуностимулятор.
Лофант тибетский - прекрасный медонос и эффективное лекарственное средство, причем лофант выделяет нектар уже в первый год и цветет до конца лета, когда кончают цвести основные медоносы. Мед на основе лофанта - лечебный. Значение лофанта в медицине еще больше, чем в пчеловодстве. Он с незапамятных времен применяется в Тибетской медицине и народы Востока считают, что он является сильны биостимулятором, соперничающим с женьшенем.
По данным биохимических исследований он является мощнейшим иммуностимулятором пролонгического действия, равных которому в растительном мире пока не обнаружено. В отличие от женьшеня его воздействие на организм носит более мягкий и продолжительный характер, его лекарственные свойства нарастают постепенно и продолжаются длительное время. Самое главное его достоинство это то, что он, воздействуя непосредственно на иммунную систему, заставляет ее более активно воздействовать на наши секреторные органы и следовательно поднимать наши внутренние защитные силы.
Oни могут быть только в жидком видe и их усвоeниe состaвляeт 98%(таблетки и капсулы усваиваются от 4 до 4О%).
Они состоят из очень маленьких частиц‚ в 7000 раз меньше‚ чем наши кровяные тельца-эритроциты. Каждая частица коллоидных растворов заряжена отрицательно, а покрытие кишечника заряжено положительнорбразуется электромагнитное поле, которое концентрируется вокруг стенок кишечника. Всё это вместе взятое и даёт 98% усвоения. Коллоидный раствор по своим физическим свойствам подобен жидкой среде организма (крови‚ лимфе)‚ что позволяет клетке совершенно естественно усваивать содержащиеся в нём целебные вещества. Приём коллоидных формул поддерживает и укрепляет компенсаторные функции организма; помогает успешно бороться с острой и хронической патологией внутренних органов; даёт значительно снизить количества назначаемых лекарств и успешно нейтрализует их побочные действия.
Многокомпанентные фитоформулы более эффективны чем мало-и, тем более, однокомпанентные.
КОЛЛОИДНОЕ СЕРЕБРО - эффективное натуральное антисептическое средство с широким спектром антибактериального. противовирусного и противогрибкового действия. Рекомендуется для стимуляции неспецифического иммунитета и прфилактики вирусных инфекций. К серебру не развивается резистентность патогенной микрофлоры. Серебро‚входящее в препарат в наиболее активной коллоидной форме,является отличным антисептиком; спектр его действия достаточно широк—СВЫШЕ 650 видов бактерий! К серебру, в отличие от антибиотиков, не развивается кстойчивость. Коллоидное серебро не только борется с возбкдителями болезни, но и обезвреживает выделяемые ими токсины, способствует восстановлению повреждённых тканейдормализации патологических процессовщызванных воспалением. Ещё и ещё раз вспомним—хроническое воспаление часто заканчивается раком.
Что такое ген р 53 и как он работает
Среда обитания человека наполнена сотнями миллиардов одноклеточных организмов: простейшими, микробами, вирусами. Вирусы живут только внутри клетки.
Паразиты – микроорганизмы, которые могут вызывать болезни. Помимо этого в многоклеточном организме человека образуются мутантные клетки – клетки с различными ошибками, подпорченные паразитами разных мастей. Вот для этого в нашем организме и существует иммунная система, которая обязана бороться с пришельцами – паразитами и мутантными клетками. Формирование иммунной системы начинается еще задолго до рождения ребенка и заканчивается в первой половине второго десятилетия жизни человека. Возможности здоровой иммунной системы – безграничны!
Мы раньше с вами рассматривали очень подробно, что угнетает иммунную систему.
Помните, что стресс и депрессия столь же опасны, как и экологические факторы, факторы неправильного питания, а может еще и более.
Уходить от них нужно большим количеством движения, хотя бы ходьбой. И когда лень, жара, холод, дождь, ветер! И обязательно вдалбливать в свою голову постоянно, что еда – это не столько удовольствие, сколько возможность жить безболезненно, подбирая правильно продукты питания и правильный способ их переработки и употребления.
Ген р 53 в 17-й хромосомной паре открыт ученым Девидом Лаймоном. Этот ген отвечает за работу ДНК клетки, ее физиологическое существование, и если в ДНК происходят какие-то нарушения, ген р 53 их исправляет! Он взаимодействует еще со 100 генами, являясь как бы дирижером этого генного оркестра. В результате разных сверх неблагоприятных воздействий: ультрафиолет, радиация, облучения, химия (химиотерапия), температура, вирусы, микробы, грибки и пр. – нарушается ремонтная реакция гена р 53. Четко доказано, что кверцетин, который можно накапливать специальной диетой, восстанавливает разрушенную функцию гена р 53.
Кверцетин не позволяет перерожденной, больной клетке получать необходимые для ее жизни ферменты, главный из которых теразикиназа. И тогда срок жизни больной клетки строго ограничивается отпущенными 4 неделями. Затем клетка нормально погибает, а вместе с ней и рак.
Флавоноид кверцетин вызывает остановку размножения аномальных клеток либо их гибель. Тем самым предупреждает миграцию клеток по организму, если в них есть ошибки. Восстановление функции нега р 53 лечит не только рак, но и разные формы аллергии, бронхиальную астму, язвенные заболевания, подагру и другие суставные проблемы, мигрень, проблемы простаты, диабетическую катаракту.
И не забываем, что кверцетиновые таблетки, капсулы очень трудно усваиваются, помогает их усвоению и лучшей работе в несколько раз – бромелайн, содержащийся в ананасах.
Генетики установили, что 50-60% всех видов рака и 200 его разновидностей зависят от нарушения функций гена р 53! 50% имеют шанс на выздоровление , это здорово.
И надо знать и помнить:
2) лучевая терапия, химиотерапия вызывают нарушения функций гена р 53 в здоровых клетках, расположенных рядом с опухолевым узлом. А это значит…, что они могут превратиться в мутантные.
4) если причиной рака является нарушение функции гена р 53 – химия в этом случае бесполезна , об этом должен сказать грамотный химиотерапевт. Вот только кто и где у нас разбирается в тонкостях генома? Кто вникает в суть вирусной причины рака, рака паразитарной формы? Чаще всего – химия, облучение, а там, как Бог даст…
Вот и дает – 9-10 млн. смертей в год, и все потому, что онкология все еще топчется на задворках 70-х годов прошлого века… А средств пожирает на уровне XXII века… Когда думать и работать начнем?
Может посадим и науку по проблемам онкологии на гречневую диету? Может запустит она в академиках гены осознания ответственности перед обществом, ведь оно их кормит, и довольно неплохо.

Лапчатка белая предупредит и вылечит:
- Инсульт — делает стенки кровеносных сосудов гибкими и эластичными, предупреждает их порыв.
- Инфаркт, атеросклероз — отлично выводит холестерин.
- Гипертонию — понижает кровяное давление.
- Полностью выводит радиацию наличием 1 1-ти микроэлементов. Если сегодня после Чернобыля мечутся тысячи обреченных, то куда будем метаться. когда из множества радиоактивных захоронений буквально выползут сотни - тысячи чернобылей?! К этому надо готовиться заранее. А от радиации эффективных лекарств нет — лишь лапчатка белая.
- Полностью вылечивает заболевания щитовидной железы при повышении и понижении ее функций. На это есть официальные мед. заключения.
- Улучшает работу сердца — устраняет его аритмию увеличивая амплитуду.
- Комплексно улучшает состав крови - увеличивает ее лучшие качества (эритроциты и лейкоциты) уменьшая худшие (холестерин).
- Содержит, кроме всего прочего: гликозид (основной лекарственный компонент женьшеня) аминокислоты — важнейший элемент жизни, многие дубильные вещества.
- Анемию — увеличивает эритроциты.
- Язвы — присутствует антисептик серебра.
- Усиливает работу кишечника.
- Лечит печень — усиливает желчеотделение.
- Лучшее средство при опущении матки, порезах и нарывах.
- Наилучшее профилактическое, безвредное средство, продлевающее жизнь.
Уникальный комплекс водорастворимых природных минералов
Каменное масло – удивительное и очень ценное природное вещество. Его целебные свойства настолько обширны, что его можно применять практически при всех заболеваниях, т.к. в первую очередь оно действует на иммунную систему, т.е. повышает защитные силы организма.
В китайской мифологии каменное масло - пища бессмертных.
Это прекрасно сбаланси-рованный природный комплекс водорастворимых минералов с широким спектром микроэлементов.
КМ не оказывает вредного побочного воздействия на организм, а наоборот, лечит все сразу! Это не только НАРОДНОЕ утверждение, но и заключение ведущих онкологических институтов.
Читайте также:

