Гемолитическая анемия это онкология

Анемия представляет собой патологическое состояние, для которого характерно снижение эритроцитов и/или концентрации гемоглобина в единице объема крови. Анемия не является самостоятельным заболеванием, это симптом, который характерен для самых разнообразных заболеваний, в том числе и для злокачественных опухолей.
Согласно статистике, данное состояние выявляется у каждого третьего онкологического пациента, а при прохождении химиотерапии — более чем в 90% случаев. Опасность анемии в онкологии заключается в том, что вместе с уменьшением уровня гемоглобина и эритроцитов, уменьшается и кислородная емкость крови. Этот фактор неблагоприятно сказывается на течении ракового процесса, снижает эффективность лечения и ухудшает дальнейший прогноз.
- Основные причины развития анемии у онкологических пациентов
- Как выявить анемию
- Как классифицируется анемия
- Методы лечения анемии
- Лечение анемии народными способами
Основные причины развития анемии у онкологических пациентов
Снижение уровня эритроцитов и гемоглобина может развиваться вследствие снижения их образования, ускоренного разрушения или в результате потери. Каждой из этих причин способствуют собственные факторы, которые рассмотрим подробнее:
- Недостаточная выработка форменных элементов крови и гемоглобина может развиваться при поражении костного мозга, недостатке железа в организме или некоторых витаминов (фолиевая кислота, витамин В12). Данные состояния могут быть напрямую связаны с напрямую с онкологическим заболеванием. Например, потеря железа может развиваться в результате постоянной рвоты, отсутствия аппетита и нарушения его всасывания в кишечнике, который поражен опухолевым процессом. Некоторые виды препаратов, которые назначают при злокачественных опухолях, подавляют рост не только раковых клеток, но и клеток крови, которые активно делятся. Также анемия может развиваться при непосредственном поражении костного мозга опухолевым процессом.
- Ускоренное разрушение эритроцитов отмечается при воздействии различных лекарственных препаратов и при аномальной активности иммунной системы. Разрушение эритроцитов непосредственно в сосудах называется внутрисосудистым гемолизом. Этот процесс протекает в норме после завершения жизненного цикла эритроцитов, который составляет 120 дней. Однако при воздействии различных факторов (прием антибиотиков, цитостатиков, присоединение вторичной инфекции и др.), этот срок значительно уменьшается, что и приводит к развитию анемии.
- Кровопотеря у онкологических пациентов может быть как острой, так и хронической. Первый вариант встречается при проведении хирургического лечения рака, а также при развитии внутренних кровотечений, которые являются частым осложнением основного заболевания. Развитие анемии при хронической кровопотере отмечается в тех случаях, когда имеется скрытый источник незначительного кровотечения. Например, при колоректальном раке кровь может выделяться с калом незаметно для пациента.
Установление точной причины анемии играет решающее значение при выборе метода лечения. Кроме того, врач учитывает степень тяжести, тип анемии, общее состояние пациента и другие параметры. Получить эту информацию можно на диагностическом этапе.
Как выявить анемию
Обследование традиционно начинается с опроса пациента и сбора анамнеза. Врач должен помнить, что не всегда анемия развивается вследствие основного заболевания. Возможны наследственные или любые другие причины, которые не связаны с опухолевым процессом. Также необходимо установить вид предшествующего противоопухолевого лечения, продолжительность и количество курсов, наименование препаратов, которые применялись. На следующем этапе врач проводит общий осмотр. Анемия может проявляться бледностью кожных покровов, слабостью, потерей аппетита, головокружением и другими симптомами. Очень часто эти проявления отмечаются при различных видах рака, который протекает без анемии, поэтому поставить диагноз исходя только из жалоб пациента невозможно.
Объективную информацию можно получить только при помощи лабораторных исследований. Анемия диагностируется по следующим анализам:
- Количество ретикулоцитов.
- Уровень железа сыворотки крови.
- Уровень белка трансферрина и ферритина.
- Уровень витамина В12 и фолиевой кислоты.
Отдельное внимание уделяется общему анализу крови. В нем определяется уровень гемоглобина, количество эритроцитов и гематокрит (отношение форменных элементов к жидкой составляющей крови). Также определяют средний объем эритроцита, среднее содержание гемоглобина в эритроците и среднее содержание гемоглобина во всей эритроцитарной массе.
При необходимости в программу комплексного обследования при анемии могут включаться и другие лабораторные анализы или специальные методы.
Как классифицируется анемия
В зависимости от значения цветового показателя, степени тяжести и механизма развития, анемия разделяется на несколько категорий. Цветовой показатель крови отражает степень насыщения эритроцитов гемоглобином. Его значение в норме колеблется от 0,85 до 1,05 единиц. Снижение показателя отмечается при гипохромной анемии, а повышение — при гиперхромной. Если цветовой показатель в норме, но уровень гемоглобина все равно низкий, то говорят о нормохромной анемии.
По степени тяжести, анемия разделяется на три группы, в зависимости от концентрации гемоглобина:
- При легкой степени анемии уровень гемоглобина не опускается ниже отметки в 90 г/л.
- При средней степени анемии показатель колеблется в пределах 90-70 г/л.
- Тяжелая анемия характеризуется падением гемоглобина ниже 70 г/л.
Классификация анемии по механизму развития наиболее обширна. Среди распространенных форм отмечаются:
- Железодефицитная анемия. Развивается в результате нарушения всасывания, усиленной потери или недостаточного поступления железа в организм.
- Гемолитическая анемия. Характеризуется разрушением эритроцитов в сосудистом русле или за его пределами. Наиболее частые причины — недостаточность специфических ферментов, аутоиммунные заболевания, воздействие лекарственных препаратов.
- Постгеморрагическая анемия. Данное состояние характерно для острой или хронической кровопотери
- Апластическая анемия. Характеризуется снижением уровня клеток-предшественников эритроцитов в костном мозге. Обычно отмечается снижение и других форменных элементов — тромбоцитов и лейкоцитов.
- В12-дефицитная анемия. При недостатке витамина В12 нарушается процесс образования эритроцитов, снижается их продолжительность жизни. Дефицит витамина может быть связан как с нарушением его всасывания в кишечнике, так и с недостаточным поступлением в организм.
В большинстве случаев определить точный вид анемии можно после нескольких лабораторных тестов, но иногда приходится применять более сложные методы диагностики, например, генетическое исследование. Понимание механизма развития анемии и получение максимально полной информации об изменениях в показателях крови являются важным компонентом эффективной терапии данного симптома.
Методы лечения анемии
Устранить анемию у онкологических пациентов можно тремя способами: переливание эритроцитарной массы, введение эритропоэтина, назначение препаратов, содержащих железо. В отдельных случаях может применяться комбинация этих методов.
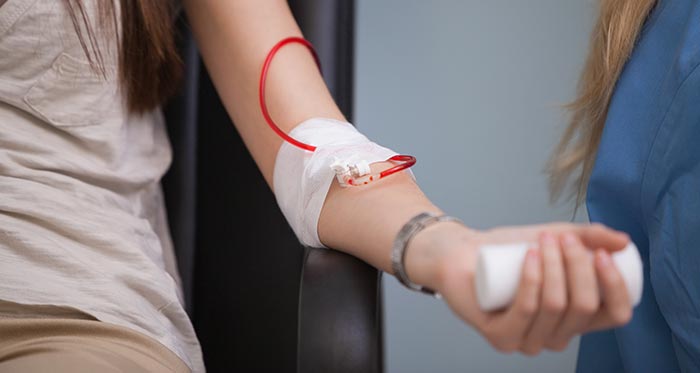
Переливание эритроцитарной массы является самым действенным методом, при помощи которого можно быстро восполнить дефицит эритроцитов, восстановить уровень гемоглобина и гематокрита. Однако без устранения причины анемии, этот способ даст лишь временный эффект. Поэтому переливание эритроцитарной массы не является альтернативой другим методикам и применяется только при наличии показаний. Одним из них является снижение уровня гемоглобина ниже 90 г/л. Переливание проводят при развитии у пациента характерных признаков анемии, среди которых отмечаются:
- Головокружение.
- Потеря сознания.
- Тахикардия.
- Быстрая утомляемость.
- Боль в груди.
- Одышка.
Данный метод лечения анемии также может применяться у пациентов, которые прошли курс химиотерапии или лучевой терапии и у которых отмечается быстрое снижение уровня гемоглобина или эритроцитов.
Стимуляторы эритропоэза при анемии увеличивают концентрацию гемоглобина и эритроцитов за счет усиления их образования в костном мозге. При сочетании с гемотрансфузиями, данный метод показывает очень хорошие результаты, но при этом имеет и ряд недостатков, которые касаются осложнений. В частности, применение стимуляторов эритропоэза для лечения анемии повышает риск развития тромботических осложнений, который и так является высоким у онкологических пациентов. По данным, полученным в ходе нескольких научных исследований, этот риск увеличивается в 1.4-1.7 раз.
В последнее время обсуждается вопрос о влиянии стимуляторов эритропоэза на выживаемость онкологических пациентов. В частности, специалисты установили, что применение препаратов данной группы при лечении анемии у пациентов с распространенным опухолевым процессом головы и шеи, шейки матки, молочной железы и других диагнозах снижает продолжительность жизни на 10-17%. В связи с этим специалисты предлагают придерживаться следующих правил:
- Если уровень гемоглобина составляет менее 100 г/л и пациент при этом проходит лечение химиопрепаратами, то стимуляторы эритропоэза могут назначаться с целью коррекции анемии и профилактики дальнейшего снижения показателей.
- Если уровень гемоглобина падает до 100 г/л и ниже, но химиотерапия при этом не проводится, то применять стимуляторы эритропоэза не рекомендуется ввиду повышенного риска развития осложнений и снижения продолжительности жизни.
- Во всех остальных случаях применять стимуляторы эритропоэза для лечения анемии у онкологических пациентов следует с осторожностью.
Также на протяжении всего времени лечения важно контролировать динамику лабораторных показателей и при увеличении уровня гемоглобина постепенно снижать дозировку стимуляторов эритропоэза.
Препараты железа применяются с целью лечения железодефицитных анемий, которые выявляются у 30-60% онкологический больных. При этом снижение уровня железа может быть связано как с самим опухолевым процессом или проводимым лечением, так и с другими факторами. Например, при назначении стимуляторов эритропоэза, существующего запаса железа в организме становится недостаточно для того, чтобы покрыть потребность, которая возникает в результате активного синтеза гемоглобина в костном мозге.

Для лечения анемии могут применяться как внутривенные, так и пероральные препараты. Второй вариант более удобен для пациента, так как таблетки проще принимать, но при этом данная форма действует медленнее и чаще приводит к осложнениям со стороны ЖКТ. Внутривенное введение позволяет добиться быстрого эффекта, что актуально при проведении химиотерапии.
Таким образом, для лечения анемии современная онкология может предложить различные методы, которые воздействуют на механизмы развития данного симптома. Точный план терапии подбирается индивидуально для каждого пациента, с учетом лабораторных показателей крови, особенностей лечения основного заболевания и других параметров.
Лечение анемии народными способами
Некоторые пациенты по разным причинам отказываются от приема описанных выше препаратов и обращаются к народной медицине. Безусловно, некоторые растения или продукты могут оказывать стимулирующее действие на систему кроветворения. Однако, учитывая основной диагноз и тяжесть анемии, этого действия крайне недостаточно для восстановления уровня гемоглобина и кислородной функции крови. В результате снижается эффективность противоопухолевого лечения, ухудшается прогноз и существенно повышается риск неблагоприятного исхода. Устранить выраженную анемию в домашних условиях при помощи народных методов невозможно. Этим должны заниматься врачи соответствующего профиля, в распоряжении которых имеются современные лекарственные препараты.
Гемолитическая анемия – это преждевременная смерть эритроцитов, в результате которой в организме постепенно развивается анемический синдром. В отличие от других более распространенных типов анемии (железодефицитная, мегалобластная), где причиной анемического состояния является недостаточное образование эритроцитов, проблема здесь заключается в их раннем разрушении. В то же время костный мозг, где в нормальных условиях происходит эритропоэз, не может компенсировать чрезмерную потерю эритроцитов. Все это приводит к проявлению анемического синдрома.
Гемолитическая анемия встречается в 5% случаев всех видов анемии. Она не показывает возрастной или половой зависимости.
Механизм гемолиза
Каждый эритроцит имеет определенную продолжительность жизни в организме человека. После образования эритроцит циркулирует в организме в течение примерно 120 дней. Затем в структуре его мембраны происходят необратимые процессы, при которых он не может адекватно выполнять свои функции. Таким образом, проходя через узкоспециализированные клетки селезенки (фильтры), состарившиеся эритроциты разрушаются. Именно этот процесс лежит в основе так называемого физиологического гемолиза.
В случае усиления патологического гемолиза, т. е. в преждевременном повреждении эритроцитов участвуют не только селезенка, но и печень, а иногда и сам костный мозг. Эритроциты разрушаются, а содержащийся в них гемоглобин подвергается изменениям. Первоначально он распадается на пигментный гем и различные белковые молекулы. Последние легко усваиваются организмом и не создают проблем в его функционировании. Тем не менее, продукты обмена гем являются одной из наиболее распространенных причин проявления заболевания, и именно они приводят к некоторым из основных симптомов.
Причины
Существуют разные причины, лежащие в основе гемолитической анемии. В большинстве случаев они имеют различный механизм действия, причем эффект является одинаковым – прогрессирующее разрушение эритроцитов. В большинстве случаев невозможно выяснить причину, поэтому в этих случаях заболевание называют идиопатической гемолитической анемией.
В зависимости от наступления патологического процесса, клиническое проявление заболевания может быть постепенным или внезапным. Чаще встречается острое начало с угрожающим жизни развитием сердечной и легочной недостаточности. Когда заболевание имеет медленное, но прогрессирующее течение, в большинстве случаев организм приспосабливается к уменьшенному количеству эритроцитов, что приводит к более позднему и неспецифическому проявлению симптомов.
В целом, причины, лежащие в основе гемолитической анемии, можно разделить на следующие виды:
• Гемолитические анемии из-за дефектов внутри эритроцитов, т. е. причиной возникновения гемолиза является структура или биохимические процессы самого эритроцита:
— дефекты мембраны эритроцитов;
— дефекты метаболизма эритроцитов;
— дефект синтеза гемоглобина.
• Гемолитические анемии из-за экстраэритроцитарных факторов – сюда включены повреждающие моменты, которые разрушают эритроциты различными механизмами. Чаще всего наблюдается анемия, при которой разрушение эритроцитов происходит по иммунному механизму, т. е. с образованием антител, которые прикрепляются к эритроциту, нарушают его функцию и приводят к его гибели. Такие антитела могут образовываться при несовместимых переливаниях крови, при использовании определенных лекарств, при различных инфекциях, при некоторых аутоиммунных заболеваниях, при ожогах и т. п.
Симптомы
Как и любое анемическое заболевание, гемолитическая анемия может развиваться остро и хронически. В обоих случаях встречаются следующие общие симптомы, но их проявление бывает выражено по-разному:
- хроническая усталость;
- быстрая утомляемость;
- бледность кожных покровов;
- одышка;
- боли в груди;
- ухудшение зрения;
- головные боли;
- неспособность сосредоточиться;
- головокружение;
- сонливость и плохой сон.
При острой форме заболевания эти симптомы проявляются резко и часто создают диагностические трудности из-за их внезапного начала. Хроническая гемолитическая анемия, с другой стороны, может характеризоваться легким проявлением симптомов (от слабой до минимальной степени), поэтому обнаружение их часто бывает случайным (при других исследованиях).
Гемолитическая анемия также характеризуется некоторыми относительно специфическими проявлениями, которые часто облегчают диагностику:
- желтуха без сопутствующего зуда;
- темная окраска стула;
- ощущение тяжести в левом верхнем квадранте в результате увеличения селезенки.
Эти симптомы часто наблюдаются при других различных желудочно-кишечных расстройствах, поэтому должны всегда рассматриваться в зависимости от общего состояния пациента.
Диагностика
Каждая гемолитическая анемия характеризуется определенным характером результатов лабораторных тестов. Чаще всего это включает следующее:
- снижение общего количества эритроцитов;
- снижение гемоглобина;
- сниженный гематокрит;
- нормальные значения тромбоцитов и лейкоцитов (в большинстве случаев);
- нормальные значения MCV, MCH и MCHC, указывающие на наличие нормоцитарной, нормохромной анемии (за редкими исключениями);
- увеличение количества ретикулоцитов – предшественников эритроцитов (это говорит об активации костного мозга, который стремится преодолеть дефицит эритроцитов выработкой новых);
- повышенный билирубин в результате увеличения распада гемоглобина (важно отметить, что увеличивается значение только непрямого билирубина, в то время как прямой сохраняет свой нормальный уровень);
- сниженный гаптоглобин – это белок, который представляет собой наиболее чувствительный маркер гемолиза;
- увеличение ЛДГ (лактатдегидрогеназы) – является важным, но не очень специфическим критерием гемолиза;
- нормальное или чаще повышенное содержание железа в организме;
- увеличение уробилиногена в моче.
Следует иметь в виду, что из-за множества причин и факторов, приводящих к возникновению гемолитической анемии, описанная характеристика лабораторных изменений редко обнаруживается при обследовании пациента. Причина этого кроется в разнообразии видов и подтипов описываемого заболевания.
Все это показывает, насколько сложен и противоречив диагноз гемолитической анемии.
Лечение
Лечение гемолитической анемии бывает двух основных типов – этиологическим, которое в большинстве случаев в силу неизвестности причин невозможно, и симптоматическим.
Этиологическое лечение заключается в выяснении причины, которая привела к проявлению состояния, и последующей ликвидации этих причин. Например, если гемолитическая анемия вызвана приемом определенных лекарств, их прекращение полностью устраняет заболевание.
Важно помнить, что переливание крови не рекомендуется при гемолитических анемиях. Это следует делать только в крайних случаях, чаще всего при уровне гемоглобина менее 70-80 (норма 120). При некоторых видах гемолитической анемии переливание следует проводить после специфического анализа крови, что уменьшит вероятность анафилактической реакции.
Симптоматическое лечение в большинстве случаев зависит от типа гемолитической анемии. Чаще всего назначаются следующие группы лекарств:
- кортикостероиды – особенно при аутоиммунных гемолитических анемиях;
- препараты железа – часто во время лечения гемолитической анемии наблюдается относительный недостаток железа в организме;
- препараты фолиевой кислоты;
- иммуноглобулин G – при подозрении на аутоиммунную природу анемии.
При некоторых типах наследственной гемолитической анемии рекомендуется спленэктомия (хирургическое удаление селезенки), поскольку это, безусловно, улучшает состояние и жизнь пациента.
, MD, PhD, Johns Hopkins School of Medicine
Last full review/revision January 2017 by Evan M. Braunstein, MD, PhD
- 3D модель (0)
- Аудио (0)
- Боковые панели (0)
- Видео (0)
- Изображения (4)
- Клинический калькулятор (0)
- Лабораторное исследование (0)
- Таблица (2)


По окончании срока нормальной продолжительности жизни (около 120 дней) эритроциты удаляются из кровотока. При наличии гемолиза деструкция происходит преждевременно, что обусловливает укорочение продолжительности жизни эритроцитов ( 120 дней). Анемия развивается, когда синтез эритроцитов в костном мозге больше не может компенсировать укорочение продолжительности их жизни; это состояние называется декомпенсированной гемолитической анемией. Если костный мозг способен ее компенсировать, данное состояние называется компенсированной гемолитической анемией.
Этиология
Гемолиз может быть классифицирован в зависимости от того, является ли он:
Внешним: источник вне эритроцита; расстройства не относящиеся к эритроцитам, как правило, являются приобретенными.
Внутренним: вследствии дефекта в самом эритроците; внутренние аномалии эритроцитов ( Гемолитические анемии), как правило, являются наследственными.
Причины нарушений, не относящихся к эритроцитам, включают:
Лекарственные средства (хинин, хинидин, пенициллины, метилдопа, тиклопидин, клопидогрель)
Токсины (свинец, медь)
Возбудители инфекции могут вызывать развитие гемолитической анемии путем прямого воздействия токсинов (например, Clostridium perfringens, альфа- или бета-гемолитические стрептококки, менингококки), путем инвазии и деструкции эритроцитов непосредственно самими возбудителями (например, Plasmodium, Bartonella) или путем продукции антител (вирус Эпштейна-Барр, микоплазма).
Причинами, со стороны эритроцитов, которые могут вызвать гемолиз являются патологии мембраны эритроцитов, клеточного метаболизма или структуры гемоглобина. К ним относятся наследственные или приобретенные дефекты клеточных мембран (к примеру, сфероцитоз), нарушения эритроцитарного метаболизма (недостаточность глюкозо-6-фосфатдегидрогеназы), гемоглобинопатии (серповидноклеточная анемия, талассемии). Гемолитические анемии могут быть обусловлены количественными и функциональными аномалиями определенных белков мембран эритроцитов (альфа- и бета-спектрина, белка 4.1, F-актина, анкирина).
Нарушение или возбудитель
Аутоиммунные гемолитические анемии:
Гемолитический уремический синдром
Пароксизмальная холодовая гемоглобинурия
Тромботическая тромбоцитопеническая пурпура
Babesia sp.
Bartonella bacilliformis
Plasmodium falciparum
Вальвулярные расстройства сердца
Выработка возбудителями инфекции токсина
Clostridium perfringens;
Альфа- и бета-гемолитические стрептококки
Соединения, проявляющие окислительные свойства (напримкр, дапсон, феназопиридин)
Медь (болезнь Вильсона–Коновалова)
Приобретенные нарушения эритроцитарных мембран
Пароксизмальная ночная гемоглобинурия
Врожденные нарушения эритроцитарных мембран
Нарушения синтеза гемоглобина
Нарушения метаболизма эритроцитов
Дефекты метаболического пути Эмбдена-Мейергофа-Парнаса (например, недостаточная активность пируваткиназы)
Дефекты гексозомонофосфатного шунта (например, дефицит глюкозо-6-фосфатдегидрогеназы)
Патофизиология
Гемолиз может иметь острый, хронический или эпизодический характер. Гемолиз может быть внесосудистым, внутрисосудистым или комбинированным.
Стареющие эритроциты утрачивают мембрану и элиминируются из кровотока в основном фагоцитирующими клетками селезенки, печени, костного мозга, ретикулоэндотелиальной системы. Разрушение гемоглобина в этих клетках происходит главным образом с помощью системы гемоксигеназы. Железо сохраняется и реутилизируется, а гем разрушается с образованием билирубина, который в печени конъюгируется с глюкуроновой кислотой и выводится с желчью.
В большинстве случаев патологичесий гемолиз является внесосудистым и возникает при удалении из кровотока поврежденных или аномальных эритроцитов селезенкой или печенью. Гемолиз, происходящий в селезенке, как правило, обусловлен незначительными аномалиями строения эритроцитов или наличием тепловых антител на поверхности клеток. При увеличении селезенки может наблюдаться разрушение даже нормальных эритроцитов. Эритроциты с выраженными аномалиями строения либо имеющие холодовые антитела и компоненты комплемента (C3) на своей поверхности разрушаются непосредственно в кровотоке либо в печени, где возможно эффективное удаление поврежденных клеток в связи с хорошим кровоснабжением. При внесосудистом гемолизе, в мазке периферической крови можно обнаружить микросфероциты.
Внутрисосудистый гемолиз является основной причиной преждевременного разрушения эритроцитов и обычно происходит после значительного повреждения клеточных мембран в результате различных механизмов, включая аутоиммунную реакцию, прямую травму (маршевая гемоглобинурия), гемодинамический удар (при наличии дефектов искусственных клапанов сердца), воздействие токсинов (клостридиальная интоксикация, укус ядовитой змеи). В мазке периферической крови можно обнаружить шистоциты или другие фрагментированные эритроциты.
Внутрисосудистый гемолиз приводит к гемоглобинемии, когда количество гемоглобина, высвобождаемого в плазму, превышает гемоглобин-связывающую способность плазматичекого связывающего белка гаптоглобина, концентрация которого в плазме в норме составляет около 100 мг/дл (1,0 г/л). Плазменные уровни свободного гаптоглобина будут низкими. При наличии гемоглобинемии свободные димеры гемоглобина фильтруются в мочу и реабсорбируются в клетках почечных канальцев; когда способность к реабсорбции превышена, возникает гемоглобинурия. В канальцевых клетках железо включается в синтез гемосидерина; часть железа используется для реутилизации, остальное количество попадает в мочу в связи с перегрузкой канальцевых клеток.
Неконьюгированная (непрямая) гипербилирубинемия и желтуха возникают, когда превращение гемоглобина в билирубин превышает способность печени к конъюгации и экскреции билирубина ( Обзор желчных поражений (Overview of Biliary Function)). Вследствие катаболизма билирубина повышается содержание стеркобилина в кале, уробилиногена в моче, иногда возникает холелитиаз.
Костный мозг отвечает на снижение количества эритроцитов усилением их продукции и высвобождения, что приводит к ретикулоцитозу.
Клинические проявления
Системные проявления аналогичны другим анемиям и включают следующие симптомы: бледность, утомляемость, головокружение, возможна гипотензия. Может возникнуть иктеричность склер и/или желтуха, а также может быть увеличена селезенка.
Гемолитический криз (острый, тяжелый гемолиз) встречается редко; он может сопровождаться ознобом, лихорадкой, болью в спине и животе, прострацией, шоком. При гемоглобинурии моча приобретает красную или красновато-коричневую окраску.
Диагностика
Мазок периферической крови и количество ретикулоцитов
Уровни сывороточного билирубина, ЛДГ, гаптоглобина, и АЛТ
Проба Кумбса и/или скрининг на гемоглобинопатию

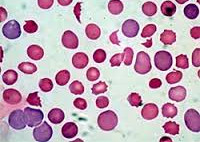
Гемолитическая анемия – патология эритроцитов, отличительным признаком которой является ускоренное разрушение красных кровяных телец с высвобождением повышенного количества непрямого билирубина. Для данной группы заболеваний типично сочетание анемического синдрома, желтухи и увеличения размеров селезенки. В процессе диагностики исследуется общий анализ крови, уровень билирубина, анализ кала и мочи, УЗИ органов брюшной полости; проводится биопсия костного мозга, иммунологические исследования. В качестве методов лечения используется медикаментозная, гемотрансфузионная терапия; при гиперспленизме показана спленэктомия.
МКБ-10


- Причины
- Патогенез
- Классификация
- Симптомы
- Наследственные мембранопатии, ферментопении и гемоглобинопатии
- Приобретенные гемолитические анемии
- Осложнения
- Диагностика
- Лечение
- Прогноз и профилактика
- Цены на лечение
Общие сведения
Гемолитическая анемия (ГА) - малокровие, обусловленное нарушением жизненного цикла эритроцитов, а именно преобладанием процессов их разрушения (эритроцитолиза) над образованием и созреванием (эритропоэзом). Данная группа анемий очень обширна. Их распространенность неодинакова в различных географических широтах и возрастных когортах; в среднем патология встречается у 1% населения. Среди прочих видов анемий на долю гемолитических приходится 11%. Патология характеризуется укорочением жизненного цикла эритроцитов и их распадом (гемолизом) раньше времени (через 14-21 день вместо 100-120 суток в норме). При этом разрушение эритроцитов может происходить непосредственно в сосудистом русле (внутрисосудистый гемолиз) или в селезенке, печени, костном мозге (внесосудистый гемолиз).

Причины
Этиопатогенетическую основу наследственных гемолитических синдромов составляют генетические дефекты мембран эритроцитов, их ферментных систем либо структуры гемоглобина. Данные предпосылки обусловливают морфофункциональную неполноценность эритроцитов и их повышенное разрушение. Гемолиз эритроцитов при приобретенных анемиях наступает под влиянием внутренних факторов или факторов окружающей среды, среди которых:
- Аутоиммунные процессы. Образование антител, агглютинирующих эритроциты, возможно при гемобластозах (остром лейкозе, хроническом лимфолейкозе, лимфогранулематозе), аутоиммунной патологии (СКВ, неспецифическом язвенном колите), инфекционных заболеваниях (инфекционном мононуклеозе, токсоплазмозе, сифилисе, вирусной пневмонии). Развитию иммунных гемолитических анемий могут способствовать посттрансфузионные реакции, профилактическая вакцинация, гемолитическая болезнь плода.
- Токсическое действие на эритроциты. В ряде случаев острому внутрисосудистому гемолизу предшествует отравление мышьяковистыми соединениями, тяжелыми металлами, уксусной кислотой, грибными ядами, алкоголем и др. Вызывать разрушение клеток крови может прием определенных лекарств (противомалярийных препаратов, сульфаниламидов, производных нитрофуранового ряда, анальгетиков).
- Механическое повреждение эритроцитов. Гемолиз эритроцитов может наблюдаться при тяжелых физических нагрузках (длительной ходьбе, беге, лыжном переходе), при ДВС-синдроме, малярии, злокачественной артериальной гипертензии, протезировании клапанов сердца и сосудов, проведении гипербарической оксигенации, сепсисе, обширных ожогах. В этих случаях под действием тех или иных факторов происходит травматизация и разрыв мембран изначально полноценных эритроцитов.

Патогенез
Классификация
В гематологии гемолитические анемии подразделяются на две большие группы: врожденные (наследственные) и приобретенные. Наследственные ГА включают следующие формы:
- эритроцитарные мембранопатии (микросфероцитоз – болезнь Минковского-Шоффара, овалоцитоз, акантоцитоз) – анемии, обусловлены структурными аномалиями мембран эритроцитов
- ферментопении (энзимопении) – анемии, вызванные дефицитом тех или иных ферментов (глюкозо-6-фосфатдегидрогеназы, пируваткиназы и др.)
- гемоглобинопатии- анемии, связанные с качественными нарушениями структуры гемоглобина или изменением соотношения его нормальных форм (талассемия, серповидно-клеточная анемия).
Приобретенные ГА подразделяются на:
- мембранопатии приобретенные (пароксизмальная ночная гемоглобинурия – б-нь Маркиафавы-Микели, шпороклеточная анемия)
- иммунные (ауто- и изоиммунные) – обусловлены воздействием антител
- токсические – анемии, обусловленные воздействием химических веществ, биологических ядов, бактериальных токсинов
- механические - анемии, вызванные механическим повреждением структуры эритроцитов (тромбоцитопеническая пурпура, маршевая гемоглобинурия)
Симптомы
Наиболее распространенной формой данной группы анемий является микросфероцитоз, или болезнь Минковского-Шоффара. Наследуется по аутосомно-доминантному типу; обычно прослеживается у нескольких представителей семьи. Дефектность эритроцитов обусловлена дефицитом в мембране актомиозиноподобного белка и липидов, что приводит к изменению формы и диаметра эритроцитов, их массивному и преждевременному гемолизу в селезенке. Манифестация микросфероцитарной ГА возможна в любом возрасте (в младенчестве, юношестве, старости), однако обычно проявления возникают у детей старшего возраста и подростков. Тяжесть заболевания варьирует от субклинического течения до тяжелых форм, характеризующихся часто повторяющимися гемолитическими кризами. В момент криза нарастает температура тела, головокружение, слабость; возникают боли в животе и рвота.
Основным признаком микросфероцитарной гемолитической анемии служит желтуха различной степени интенсивности. Вследствие высокого содержания стеркобилина кал становится интенсивно окрашенным в темно-коричневый цвет. У пациентов с болезнь Минковского-Шоффара наблюдается склонность к образованию камней в желчном пузыре, поэтому часто развиваются признаки обострения калькулезного холецистита, возникают приступы желчной колики, а при закупорке холедоха конкрементом - обтурационная желтуха. При микросфероцитозе во всех случаях увеличена селезенка, а у половины пациентов – еще и печень. Кроме наследственной микросфероцитарной анемии, у детей часто встречаются другие врожденные дисплазии: башенный череп, косоглазие, седловидная деформация носа, аномалии прикуса, готическое нёбо, полидактилия или брадидактилия и пр. Пациенты среднего и пожилого возраста страдают трофическими язвами голени, которые возникают в результате гемолиза эритроцитов в капиллярах конечностей и плохо поддаются лечению.
Среди различных приобретенных вариантов чаще других встречаются аутоиммунные анемии. Для них общим пусковым фактором выступает образование антител к антигенам собственных эритроцитов. Гемолиз эритроцитов может носить как внутрисосудистый, так и внутриклеточный характер. Гемолитический криз при аутоиммунной анемии развивается остро и внезапно. Он протекает с лихорадкой, резкой слабостью, головокружением, сердцебиением, одышкой, болями в эпигастрии и пояснице. Иногда острым проявлениям предшествуют предвестники в виде субфебрилитета и артралгий. В период криза стремительно нарастает желтуха, не сопровождающаяся кожным зудом, увеличивается печень и селезенка. При некоторых формах аутоиммунных анемий больные плохо переносят холод; в условиях низких температур у них может развиваться синдром Рейно, крапивница, гемоглобинурия. Вследствие недостаточности кровообращения в мелких сосудах возможны осложнения в виде гангрены пальцев ног и рук.
Осложнения
Каждый вид ГА имеет свои специфические осложнения: например, ЖКБ – при микросфероцитозе, печеночная недостаточность – при токсических формах и т.д. К числу общих осложнений относятся гемолитические кризы, которые могут провоцироваться инфекциями, стрессами, родами у женщин. При остром массивном гемолизе возможно развитие гемолитической комы, характеризующейся коллапсом, спутанным сознанием, олигурией, усилением желтухи. Угрозу жизни больного несут ДВС-синдром, инфаркт селезенки или спонтанный разрыв органа. Неотложной медицинской помощи требуют острая сердечно-сосудистая и почечная недостаточность.
Диагностика
Определение формы ГА на основе анализа причин, симптоматики и объективных данных относится к компетенции гематолога. При первичной беседе выясняется семейный анамнез, частота и тяжесть протекания гемолитических кризов. В процессе осмотра оценивается окраска кожных покровов, склер и видимых слизистых, производится пальпация живота для оценки величины печени и селезенки. Сплено- и гепатомегалия подтверждается при проведении УЗИ печени и селезенки. Лабораторный диагностический комплекс включает:
- Исследование крови. Изменения в гемограмме характеризуются нормо- или гипохромной анемией, лейкопенией, тромбоцитопенией, ретикулоцитозом, ускорением СОЭ. В биохимических пробах крови определяется гипербилирубинемия (увеличение фракции непрямого билирубина), увеличение активности лактатдегидрогеназы. При аутоиммунных анемиях большое диагностическое значение имеет положительная проба Кумбса.
- Анализы мочи и кала. Исследование мочи выявляет протеинурию, уробилинурию, гемосидеринурию, гемоглобинурию. В копрограмме повышено содержание стеркобилина.
- Миелограмму. Для цитологического подтверждения выполняется стернальная пункция. Исследование пунктата костного мозга обнаруживает гиперплазию эритроидного ростка.
В процессе дифференциальной диагностики исключаются гепатиты, цирроз печени, портальная гипертензия, гепатолиенальный синдром, порфирии, гемобластозы. Пациента консультируют гастроэнтеролог, клинический фармаколог, инфекционист и другие специалисты.

Лечение
Различные формы ГА имеют свои особенности и подходы к лечению. При всех вариантах приобретенной гемолитической анемии необходимо позаботиться об устранении влияния гемолизирующих факторов. Во время гемолитических кризов больным необходимы инфузии растворов, плазмы крови; витаминотерапия, по необходимости – гормоно- и антибиотикотерапия. При микросфероцитозе единственно эффективным методом, приводящим к 100 % прекращению гемолиза, является спленэктомия.
При аутоиммунной анемии показана терапия глюкокортикоидными гормонами (преднизолоном), сокращающая или прекращающая гемолиз. В некоторых случаях требуемый эффект достигается назначением иммунодепрессантов (азатиоприна, 6-меркаптопурина, хлорамбуцила), противомалярийных препаратов (хлорохина). При резистентных к медикаментозной терапии формах аутоиммунной анемии выполняется спленэктомия. Лечение гемоглобинурии предполагает переливание отмытых эритроцитов, плазмозаменителей, назначение антикоагулянтов и антиагрегантов. Развитие токсической гемолитической анемии диктует необходимость проведения интенсивной терапии: дезинтоксикации, форсированного диуреза, гемодиализа, по показаниям – введение антидотов.
Прогноз и профилактика
Течение и исход зависят от вида анемии, тяжести протекания кризов, полноты патогенетической терапии. При многих приобретенных вариантах устранение причин и полноценное лечение приводит к полному выздоровлению. Излечения врожденных анемий добиться нельзя, однако возможно достижение длительной ремиссии. При развитии почечной недостаточности и других фатальных осложнений прогноз неблагоприятен. Предупредить развитие ГА позволяет профилактика острых инфекционных заболеваний, интоксикаций, отравлений. Запрещается бесконтрольное самостоятельное использование лекарственных препаратов. Необходимо тщательная подготовка пациентов к гемотрансфузиям, вакцинации с проведением всего комплекса необходимых обследований.
Читайте также:

