Факторы роста раковых клеток

Чем раковые клетки отличаются от нормальных?
Для того чтобы организм человека правильно работал как единое целое, каждая клетка в нем должна подчиняться общим правилам и обладать некоторыми основополагающими свойствами:
Не перестает размножаться. Сколько бы своих копий ни создала опухолевая клетка, она не останавится. Злокачественная опухоль постоянно растет и распространяется в организме.
Не специализируются. Раковая клетка не становится специализированной и не выполняет полезные для организма функции. Процесс клеточной специализации называется дифференцировкой. Чем ниже степень дифференцировки, тем агрессивнее ведет себя рак.
Каковы причины появления раковых клеток?
Почему в теле конкретного человека возникли раковые клетки — вопрос во многом риторический.
Каждая живая клетка функционирует и размножается в соответствии с заложенной в ней генетической информацией. При возникновении определенных мутаций эти тонкие механизмы регуляции сбиваются, и может произойти злокачественное перерождение.
Сложно сказать, что именно привело к таким мутациям в каждом конкретном случае. Современным врачам и ученым известны лишь факторы риска, которые повышают вероятность злокачественного перерождения и развития заболевания. Вот основные из них:
- Неблагоприятная экологическая ситуация.
- Курение.
- Чрезмерное употребление алкоголя.
- Профессиональные вредности, контакт с канцерогенными веществами и различными излучениями на производстве.
- Ожирение, избыточная масса тела.
- Ультрафиолетовое излучение солнца и соляриев.
- Малоподвижный образ жизни.
- Возраст: со временем мутации накапливаются, поэтому вероятность возникновения в организме раковых клеток повышена у пожилых людей.
- Нездоровое питание: преобладание в рационе животных жиров, красного и обработанного мяса.
Ни один из этих факторов не приводит со стопроцентной вероятностью к развитию злокачественной опухоли.
Какие бывают типы генов рака?
Не все мутации одинаково опасны. К раку приводят те, которые возникают в определенных генах:
Онкогены активируют размножение клеток. Злокачественное перерождение происходит, когда они становятся слишком активны. В качестве примера можно привести ген, который кодирует белок HER2. Этот белок-рецептор находится на поверхности клетки и заставляет ее размножаться.
Мутации, которые приводят к раку, могут быть наследственными (возникают в половых клетках) и соматическими (возникают в клетках тела в течение жизни).

Основные характеристики и строение раковых клеток
Раковые клетки обладают тремя основополагающими характеристиками, за счет которых так опасны онкологические заболевания:
- Способность к бесконтрольному размножению.
- Способность к инвазии — прорастанию в окружающие ткани.
- Способность к метастазированию — распространению в организме и образованию новых очагов в различных органах.
Не всякая опухолевая клетка — раковая. Раком или карциномой называют злокачественные опухоли из эпителиальной ткани, которая выстилает кожу, слизистые оболочки внутренних органов, образует железы. Из соединительной ткани (костной, жировой, мышечной, хрящевой, кровеносных сосудов) развиваются саркомы. Злокачественные заболевания органов кроветворения называют лейкозами. Опухоли из клеток иммунной системы — лимфомы и миеломы.
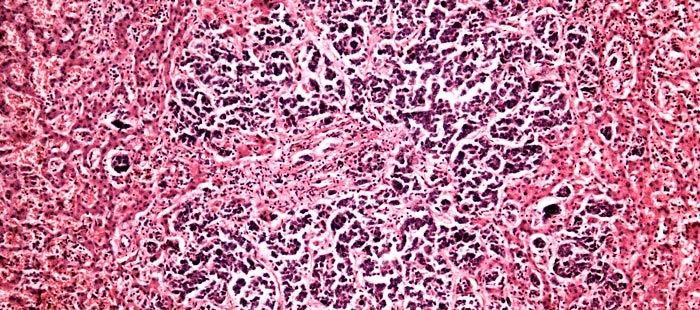
Как выглядят раковые клетки под микроскопом?
Если коротко, то они сильно отличаются от нормальных, тех, что ожидает увидеть патологоанатом, когда рассматривает под микроскопом фрагмент ткани. Раковые клетки имеют более крупные или мелкие размеры, неправильную форму, аномальное ядро. Если нормальные клетки в одной ткани все примерно одинаковых размеров, то раковые зачастую разные. Ядро содержит очень много ДНК, поэтому оно крупнее (его размеры тоже вариабельны), а при окрашивании специальными веществами выглядит более темным.
Из нормальных клеток образуются определенные структуры, например, железы. Раковые клетки располагаются более хаотично. Например, они образуют железы искаженной, неправильной формы или непонятные массы, которые на железы совсем не похожи.
Как развиваются раковые клетки, какие этапы проходят в своем развитии?
Раковые опухоли растут за счет деления клеток, которые входят в их состав. Во время деления злокачественная клетка образует две своих копии, таким образом, рост происходит в геометрической прогрессии. Например, для того чтобы образовалась опухоль размером 1 см, нужно около 30 удвоений. Через 40 удвоений новообразование достигает веса 1 кг, и этот размер считается критическим, смертельным для пациента.
Согласно современным представлениям, за рост злокачественной опухоли отвечают так называемые стволовые опухолевые клетки. Они активно делятся, в то время как другие опухолевые клетки просто существуют. Современные ученые заняты поиском методов лечения, направленных против этих стволовых клеток.
Время удвоения опухолевых клеток бывает разным. Например, при лейкозе это происходит за 4 дня, а при раковых новообразованиях толстой кишки — за 2 года. Проходит много времени, прежде чем опухоль достигнет настолько больших размеров, что станет проявляться какими-либо симптомами. Например, если у онкологического больного появились некоторые жалобы, и после этого он прожил год, вероятно, опухоль в его организме на момент появления жалоб существовала уже около трех лет, просто он об этом не знал.
Пока раковая опухоль небольшая, ей вполне хватает кислорода. Но по мере роста она все сильнее испытывает кислородное голодание — гипоксию. Чтобы обеспечить свои потребности, опухолевые клетки вырабатывают вещества, которые стимулируют образование кровеносных сосудов — ангиогенез.
По мере роста опухоли происходит инвазия — распространение раковых клеток в окружающие ткани. Они вырабатывают ферменты, которые разрушают нормальные клетки.
Некоторые из них отрываются от материнской опухоли, проникают в кровеносные и лимфатические сосуды, образуют в них вторичные очаги — метастазы. В этом самая главная опасность злокачественных опухолей. Именно метастатические очаги становятся причиной гибели многих онкологических пациентов.
Ликвидация раковых клеток: что помогает их уничтожить?
С раковыми клетками можно бороться разными способами. Например, удалить их из организма хирургическим путем. Но это возможно лишь в случаях, если опухоль не успела сильно распространиться в организме. Даже если можно выполнить радикальную операцию, никогда нет стопроцентной гарантии того, что в организме не остались микроскопические опухолевые очаги, которые в будущем станут причиной рецидива. Поэтому зачастую хирургические вмешательства дополняют адъювантной и неоадьювантной терапией.
Другие методы лечения:
В Европейской клинике применяются наиболее современные оригинальные препараты для борьбы с раком. У нас есть возможность провести молекулярно-генетический анализ опухолевой ткани, разобраться, из-за каких мутаций клетки стали злокачественными, и назначить наиболее эффективную персонализированную терапию. Свяжитесь с нами, мы знаем, как помочь.
Факторы роста- это белковые молекулы, регулирующие деление и выживание клеток. Факторы роста можно получать с помощью генной инженерии в лаборатории и использовать в терапии.
Факторы роста связываются с рецепторами на поверхности клеток, активируя таким образом пролиферацию и / или дифференциацию клеток. Факторы роста достаточно универсальны и стимулируют клеточное деление в различных типах клеток, в то время как некоторые из них специфичны только для определенных типов клеток. Факторы роста - это белки, стимулирующие рост клеток.
Факторы роста - это белки, которые функционируют как стимуляторы роста (митогены) и / или ингибиторы роста, стимулируют миграцию клеток, действуют как хемотоксичные агенты, ингибируют миграцию клеток, ингибируют инвазию раковых клеток, регулируют различные клеточные функции, участвуют в апоптозе и ангиогенезе и стимулируют выживаемость клеток, не влияя на рост и дифференциацию.
В качестве примеров факторов роста можно привести: EGF, FGF, NGF, PDGF, VEGF, IGF, GMCSF, GCSF, TGF, эритропиетин, TPO, BMP, HGF, GDF, нейротрофины, MSF, SGF, GDF и более.
Гемопоэтические факторы роста - это гормоно-подобные вещества, которые стимулируют костный мозг к производству клеток крови. Недостаток клеток крови является причиной большинства симптомов у людей, страдающих миелодиспластическим синдромом.
Эритропоэтин - это фактор роста, который стимулирует продукцию красных кровяных телец. Интерлейкин-11 (IL-11) стимулирует продукцию тромбоцитов после хемотерапии. Современные исследования посвящены попыткам понять, какие факторы роста позволят лечить ряд болезней и как комбинировать факторы роста друг с другом и с другими методами лечения, такими как химиотерапия или гормоны.
Факторы роста являются биологически активными полипептидами, которые функционируют как гормоно-подобные регуляторные сигналы, контролирующие рост и дифференциацию чувствительных клеток. Различие между факторами роста и гормонами, как правило, неочевидно.
Последовательность аминокислот позволяет объединять факторы роста в одну группу, что позволяет предположить, что они происходят от общего предкового белка. Семейство инсулинов включает соматомедины А и С, инсулин, инсулин-подобный фактор роста (IGF) и импортстимулирующий фактор (MSF). Второе семейство включает фактор роста сарком (SGF), трансформирующй фактор роста (TGF) и эпидермальный фактор роста (IGF). Кроме того, существуют факторы роста, например, фактор роста нервов (NGF), фактор роста фибробластов (FGF), и фактор роста тромбоцитов (PDGF), для которых не было найдено структурных гомологов.
Стимуляция пролиферации клеток факторами роста похожа на быструю пролиферацию раковых клеток. Рецепторы факторов роста схожи с онкогенными белками, продуцируемыми некоторыми РНК-онкогенными вирусами. Фактор роста тромбоцитов (PDGF) практически идентичен онкогенному белку вируса саркомы обезьян.
Факторы роста необходимы для клеточной дифференциации и нормального клеточного цикла, поэтому являются жизненно важными элементами для животных от рождения до смерти. Факторы роста обеспечивают развитие, участвуют в поддержании целостности и репарации тканей, стимулируют производство клеток крови и участвуют в раковых процессах.
CTGF (2 продукта): CYT-438 (фактор роста соединительной ткани), CYT-526 (фактор роста соединительной ткани 182-250 а.к)
PDGF (7 продуктов): CYT-341 (PDGF-AA), CYT-491 (PDGF-A), CYT-342 (PDGF-AB), CYT-501 (PDGF-BB), CYT-242 (PDGF-BB, Yeast), CYT-492 (PDGF-B), CYT-412 (PDGF-BB, мышь)
VEGF (14 продуктов): CYT-338, CYT-241, CYT-496 (CHO), CYT-225 (Sf9), CYT-336 (мышиный), CYT-226 (Sf9, мышиный), CYT-392 (крысиный), CYT-343 (121), CYT-200 Sf9(121), CYT-527 (белок, родственный VEGF), CYT-262 (белок, родственный VEGF, крысиный), CYT-284 (VEGF-C (152), CYT-517 (ингибитор VEGF), CYT-263 (VEGF-E (Orf Virus)
Гормоны роста (16 продуктов): CYT-202, CYT-235 (плацентарный гормон роста), CYT-259 (гипофизарный гормон роста), CYT-337 (плацентарный гормон роста 20 кДа), CYT-296 (крысиный), CYT-519 (свиной), CYT-514 (кроличий), CYT-430 (цыпленок), CYT-237 (овечий), CYT-215 (антагонист овечьего гормона роста), CYT-499 (Mai Mai), CYT-498 (Denis), CYT-297 (карп), CYT-238 (белок, связывающий гормоны роста), CYT-471 (белок, связывающий гормоны роста, бычий), CYT-470 (белок, связывающий гормоны роста, овечий)
Другие факторы роста (13 продуктов): CYT-243 (лейкинферон человека), CYT-423 (лейкоцит-ассоциированный антиген-3), CYT-310 (ингибитор активности меланом), CYT-301 (оментин), CYT-290 (остеопротегерин, His Tag), CYT-266 (остеопротегерин), CYT-231 (онкостатин-M), CYT-452 (периостин), CYT-524 (програнулин), CYT-419 (плацентарный фактор роста-1), CYT-420 (плацентарный фактор роста-2), CYT-334 (растворимый RANK лиганд), CYT-320 (растворимый RANK лиганд)
Инсулин (3 продукта): CYT-270, CYT-467 (бычий), CYT-468 (свиной)
Инсулин-подобные факторы роста (10 продуктов): CYT-216 (инсулино-подобный фактор роста-1), CYT-518 (фактор роста-1 Des (1-3), CYT-229 (фактор роста-1, мышиный), CYT-289 (фактор роста-1, крысиный), CYT-295 (фактор роста-1, Denis), CYT-265 (фактор роста-2), CYT-299 (белок-1, связывающий факторы роста), CYT-300 (белок-3, связывающий факторы роста), CYT-464 (белок-5, связывающий факторы роста), CYT-258(белок-6, связывающий факторы роста)
Колоние-стимулирующие факторы (14 продуктов): CYT-220 (КСФ гранулоцитов), CYT-476 (КСФ гранулоцитов, His Tag), CYT-329 (КСФ гранулоцитов, CHO), CYT-410 (КСФ гранулоцитов, мышиные), CYT-221 (КСФ гранулоцитов макрофагов), CYT-324 (КСФ гранулоцитов макрофагов, Pichia), CYT-477 (КСФ гранулоцитов макрофагов, His Tag), CYT-416 (КСФ гранулоцитов-макрофагов, Sf9), CYT-222 (КСФ гранулоцитов макрофагов, мышиный), CYT-395 (КСФ гранулоцитов макрофагов, крысиные), CYT-401 (КСФ гранулоцитов макрофагов, свиные), CYT-360 (gm-csf/IL-3), CYT-308 (КСФ макрофагов), CYT-439 (КСФ макрофагов, мышиные)
Лептин (19 продуктов): CYT-228, CYT-287 (His Tag), CYT-351 (мышиный), CYT-227 (крысиный), CYT-507 (кроличий), CYT-239 (овечий), CYT-502 (бычий), CYT-503 (свиной), CYT-505 (цыпленок), CYT-506 (собачий), CYT-504 (лошадиный), CYT-508 (домен связывания с лептином, цыпленок), CYT-509 (домен связывания с лептином, цыпленок), CYT-352 (антагонист лептина), CYT-354 (антагонист лептина, мышиный), CYT-355 (антагонист лептина, крысиный), CYT-356 (антагонист лептина, овечий), CYT-353 (антагонист лептина), CYT-357(антагонист лептина, овечий)
Миостатин (3 продукта): CYT-418, CYT-445 (His-Tag), CYT-448 (пробелок миостатина)
Ноггин (1 продукт): CYT-475
Плацентарный лактоген (3 продукта): CYT-511 (бычий), CYT-510 (козлиный), CYT-512 (овечий)
Пролактин (11 продуктов): CYT-267, CYT-493 (His Tag), CYT-321 (мышиный), CYT-322 (крысиный), CYT-513 (кроличий), CYT-240 (овечий), CYT-311 (антагонист овечьего пролактина), CYT-469 (рецептор пролактина), CYT-268 (растворимый рецептор кроличьего пролактина), CYT-294 (растворимый рецептор бычьего пролактина), CYT-293 (растворимый рецептор овечьего пролактина)
Трансформирующий фактор роста (3 продукта): CYT-473 (трансформирующий фактор роста-beta 1), CYT-368 (трансформирующий фактор роста-beta 3), CYT-319 (трансформирующий фактор роста-beta 3 (644-850)
Фактор роста кератиноцитов (2 продукта): CYT-219 (фактор роста кератиноцитов-1), CYT-303 (фактор роста кератиноцитов-2)
Факторы роста гепатоцитов (3 продукта): CYT-244 (Sf9), CYT-251 (CHO), CYT-522 (стимулятор роста гепатоцитов)
Факторы роста фибробластов (16 продуктов): CYT-264 (FGF-acidic), CYT-364 (FGF-acidic, Sf9), CYT-528 (FGF-acidic, мышиный), CYT-218 (FGF-basic), CYT-365 (FGF-basic, Sf9), CYT-386 (FGF-basic, мышиный), CYT-288 (FGF-basic), CYT-415 (FGF-9), CYT-349 (FGF-9, мышиный), CYT-279 (FGF-19), CYT-474 (FGF-21), CYT-281 (FGF-21, His Tag), CYT-339 (FGF-21, мышиный), CYT-516 (FGF-21, His Tag, мышиный), CYT-428 (FGF-22), CYT-374 (FGF-23)
Факторы роста эпидермиса (4 продукта): CYT-217, CYT-332 (Pichia), CYT-466 (21-Leu), CYT-326 (мышиный)
Факторы стволовых клеток (4 продукта): CYT-255, CYT-421 (Sf9), CYT-275 (мышиный), CYT-323 (крысиный)
Факторы, ингибирующие миграцию макрофагов (2 продукта): CYT-431 (His Tag N-концевой), CYT-521 (His Tag C-концевой)
Эритропоэтин (2 продукта): CYT-201 (эритропоэтин-альфа), CYT-325 (эритропоэтин-альфа Fc/Chimera)
• Раковым клеткам присущи несколько определенных свойств
• В отличие от здоровых клеток, при росте на чашках Петри, при контакте с окружающими клетками раковые не прекращают деление
• Для поддержания роста и пролиферации для раковых клеток характерна пониженная потребность в ростовых факторах
• В отличие от здоровых, раковые клетки, растущие в культуре не нуждаются в прикреплении к физическим субстратам — эта независимость роста от фиксации с поверхностью является их характерной чертой
• В отличие от культуры здоровых клеток, у которые деление останавливается через определенное количество циклов, раковые клетки бессмертны и поэтому после образования определенного числа поколений клеток не прекращают деления
• Для раковых клеток часто характерны хромосомные аберрации, в том числе, изменение числа хромосом и их структуры
Годами исследователи описывали специфические особенности раковых клеток. Они суммированы в таблице ниже. Многие эти особенности лучше изучать, выращивая клетки в культуре (in vitro), чем исследовать ткани организма (in vivo). Большинство раковых клеток удобно выращивать в чашках Петри. В то же время многие типы здоровых клеток гораздо труднее растить in vitro.
Здоровые клетки, помещенные в чашку Петри с питательной средой, оседают на дно и делятся до тех пор, пока не заполнят все дно, после чего их рост прекращается. Этот феномен носит название контактное торможение и означает, что при контакте клеток друг с другом механизм пролиферации выключается. Поэтому нормальные клетки образуют слой, толщина которого соответствует одной клетке, т. е. монослой. Когда слой клеток полностью покрывает дно чашки Петри, он называется конфлуентным монослоем.
Раковые клетки ведут себя совершенно другим образом. На рисунке ниже показано, что, когда они растут на чашках Петри, их рост продолжается в течение долгого времени после того, как они образовали межклеточные контакты. Невозможность прекратить деление приводит к тому, что клетки начинают образовывать слои на поверхности друг у друга.
Если раковые клетки растут среди большого количества нормальных клеток на чашках Петри, то в конце концов их потомки образуют плотные скопления клеток, окруженные монослоем здоровых клеток, которые называются фокусы. Количество таких фокусов легко подсчитать даже невооруженным глазом. Таким образом, биологи легко подсчитывают число клонов трансформированных клеток, находящихся в популяции здоровых.

Потеря контактного торможения является не единственным отличительным свойством раковых клеток. Когда суспензия этих клеток смешивается с агаровом гелем и помещается в чашку Петри, они образуют сферические колонии. Напротив, здоровые клетки не способны расти в суспензии, и для того, чтобы они начали размножаться, они должны прочно прикрепиться к поверхности дна чашки Петри. Поэтому для здоровых клеток характерен прикрепленный рост, в отличие от раковых клеток, рост которых не зависит от прикрепления.
К числу клеток, легко культивируемых in vitro, относятся клетки соединительной ткани, называемые фибробластами. Когда культуру фибробластов, растущую в чашках Петри, по мере достижения конфлуентности пересаживают в другие чашки, клетки продолжают расти и делиться, но по прошествии определенного времени прекращают пролиферировать. Прекращение роста означает, что клетки каким-то образом способны ограничивать количество циклов деления и что, когда линия клеток исчерпывает отпущенное число циклов деления, рост ее останавливается.
Это происходит даже несмотря на то, что окружающие условия остаются оптимальными для пролиферации. Об этом свидетельствуют наблюдения, согласно которым, в зависимости от типа клеток и их источника (организма), пролиферация останавливается после образования 30, 40 или 50 поколений клеток.
Рисунок ниже иллюстрирует это положение. По сравнению со здоровыми клетками, раковые представляют собой полный контраст. Адаптировавшись к условиям культивации, они способны к бесконечной пролиферации и, таким образом, являются иммортализованными.
Культуры раковых клеток также обладают другими особенностями, которые отличают их от здоровых клеток. При выращивании культуры здоровых клеток они нуждаются в питательных добавках, представляющих собой больше чем просто питательные компоненты (аминокислоты, глюкоза, витамины). Питательная среда должна также содержать сыворотку, полученную из телячьей крови. Эта сыворотка содержит ростовые факторы (GF), представляющие собой белки, которые выделяются одними клетками для поддержания роста других.
Один из распространенных ростовых факторов сыворотки, тромбоцитарный фактор роста (PDGF), выходит из тромбоцитов в процессе свертывания крови, наступающего после повреждения тканей. Обычно при высвобождении PDGF на участке раневой поверхности он оказывает стимулирующее действие на рост соседних фибробластов, которые затем участвуют в регенерации ткани. Аналогичным образом, присутствие фактора в ростовой среде необходимо для стимуляции роста фибробластов на чашках Петри; без добавления PDGF клетки в течение недель остаются жизнеспособными не не делятся и не растут.
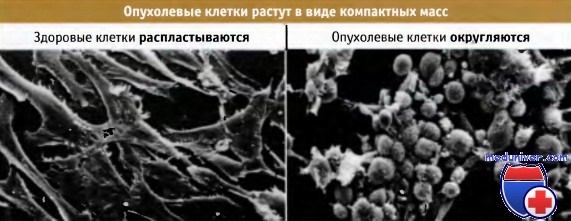
В сканирующем электронном микроскопе видно,
что здоровые клетки распластываются и образуют длинные выросты,
в то время как опухолевые клетки округляются и образуют плотные компактные массы.
Для роста различных типов эпителиальных клеток в культуре необходимы другие ростовые факторы, например такие, как эпидермальный ростовой фактор (EGF). На рисунке ниже представлены механизмы действия ростовых факторов.
Фактически все типы здоровых клеток для стимуляции своего размножения требуют присутствия в среде одного или нескольких ростовых факторов. Это наблюдение привело к важному заключению, касающемуся биологических характеристик большинства клеток: они не пролиферируют, если отсутствует индуцирующий внешний стимул, особенно относящийся к сигалам, передаваемым с помощью GF, присутствующего в окружающей среде. Этот вывод совершенно неприложим к раковым клеткам, и для них необходимы существенно меньшие концентрации GF, чем для здоровых клеток.
Раковые клетки способны сами стимулировать свою пролиферацию, рост и деление, и поэтому в основном не зависят от экзогенных ростовых сигналов.
Важно, что раковые клетки редко становятся совершенно независимыми от внешних ростовых факторов. Гораздо чаще они сохраняют зависимость от определенных клеточных факторов, которые необходимы для пролиферации соответствующего типа здоровых клеток. Так, для роста большинства типов опухолей молочной железы необходимы эстрогены, а для роста опухолей предстательной железы, андрогены. (Хотя обычно считают, что оба агента относятся к гормонам, они регулируют пролиферацию раковых клеток, функционируя как ростовые факторы.) Также для поддержания выживаемости многих типов раковых клеток человека необходим инсулиноподобный фактор роста 1(IGF-1).
В отличие от PDGF и EGF, которые стимулируют рост, некоторые внеклеточные факторы ингибируют пролиферацию клеток. К числу наиболее изученных факторов такого рода относится TGF-b, проявляющий мощное ингибирующее действие на пролиферацию различных типов эпителиальных клеток. По своему действию он напоминает GF с отрицательным эффектом (из-за способности индуцировать неприкрепленный рост некоторых клеток, он получил свое первоначальное название фактора роста опухоли). Опять-таки, в отличие от здоровых, раковые клетки по-разному реагируют на присутствие этого фактора.
Многие из них выработали способность противостоять ингибирующему эффекту TGF-b и продолжают делиться в присутствии довольно значительных концентраций этого GF с отрицательным эффектом.
Таким образом, раковые клетки проявляют неодинаковое отношение к сигнальным молекулам, присутствующим во внешнем окружении. Они относительно независимы от экзогенных сигналов, стимулирующих рост, и в то же время вырабатывают устойчивость к сигналам, его подавляющим. Такое отношение к сигнальным молекулам позволяет сделать общий вывод, касающийся биологии раковой клетки: эти клетки теряют связь с сигнальными молекулами, присутствующими в их окружении (а именно с положительно и отрицательно действующими GF).
Еще одна важная особенность раковых клеток заключается в том, что они часто характеризуются аберрантным хромосомным набором: некоторые хромосомы отсутствуют, другие присутствуют в избыточном количестве, а при объединении сегментов нормальных хромосом образуются необычные хромосомы. Такая аномалия хромосом, называемая анеуплоидией, контрастирует с нормальной картиной хромосомного набора, характерной для здоровых клеток — эуплоидией. На рисунке ниже показана микрофотография анеуплоидной опухолевой клетки, полученная после флуоресцентной гибридизации in situ.
Суммируя все вышесказанное, можно прийти к выводу, что раковым клеткам свойственно значительное количество различных аномалий. Однако перечисленными их особенностями список не исчерпывается. Необходимо учитывать, что раковые и здоровые клетки разделяют также ряд общих черт, что часто делает очень трудной задачу их избирательного уничтожения, не затрагивая при этом здоровые.
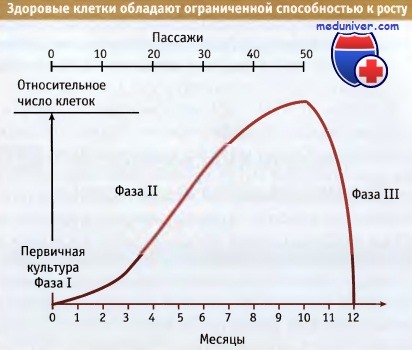
Рост популяции здоровых клеток прекращается через 30-40 удвоений.
После этого популяция вступает в т.н. фазу покоя. 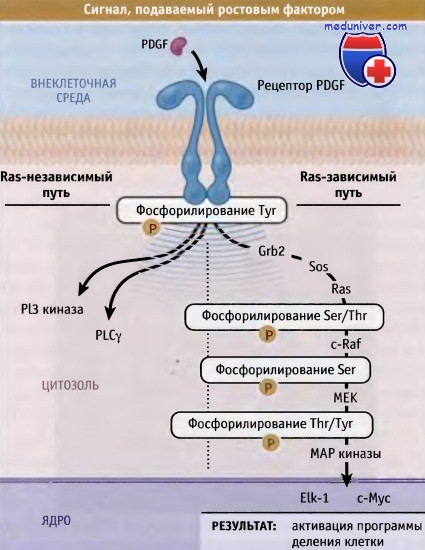
Типичная схема внутриклеточных событий при пе редаче сигнала.
Лиганд (в данном случае PDGF) связывается рецептором и активирует каскад внутриклеточных событий,
при водящий к изменению состояния клетки.
Основными сигнальны ми процессами в клетке является фосфорилирование белков, также гидролиз липидов и ГТФ. 
На этой микрофотографии показан препарат хромосом клетки одного из колоректальных раков.
Хромосомы окрашены с помощью специфических гибридизационных зондов, меченных различными флуорохромами,
которые позволяют визуализировать дефекты их структуры и количества.
18 сентября 2013
- 4196
- 3,5
- 6
- 2
![]()
Антон Чугунов![]()
Андрей Панов

Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
Рак — это злокачественная опухоль, которая дает выросты в окружающие ее ткани, похожие на конечности ракообразного (отсюда и название). Ежегодно это заболевание уносит более 300 тысяч жизней. Основными причинами рака являются три группы факторов: физические (ионизирующее излучение, в т.ч. ультрафиолет), химические (канцерогенные вещества) и биологические (некоторые вирусы и бактерии). Под влиянием этих факторов клетки могут стать атипичными, поменять облик и свойства, что отражается во множестве молекулярно-генетических признаков, отличающих их от здоровых клеток:
- Увеличение лабильности и текучести клеточной мембраны, снижение адгезивности и контактного торможения. В норме клетки, вступая в контакт друг с другом, прекращают деление. В опухолевых клетках отсутствие контактного торможения приводит к безудержной пролиферации.
- Нарушение регуляции роста и дифференцировки опухолевых клеток. В нормальных клетках процессы роста и дифференцировки уравновешивает модулятор — кальций-зависимая протеинкиназа. В опухолевых клетках активность этого белка повышена, что приводит к резкой индукции пролиферации.
- Атипичный энергетический обмен, который проявляется в преобладании гликолиза. Нормальные дифференцированные клетки в присутствии кислорода в качестве основного источника энергии используют трёхэтапный процесс утилизация глюкозы (см. врезку):
- гидролиз высокомолекулярных органических соединений;
- гликолиз;
- окислительное фосфорилирование и цикл Кребса.
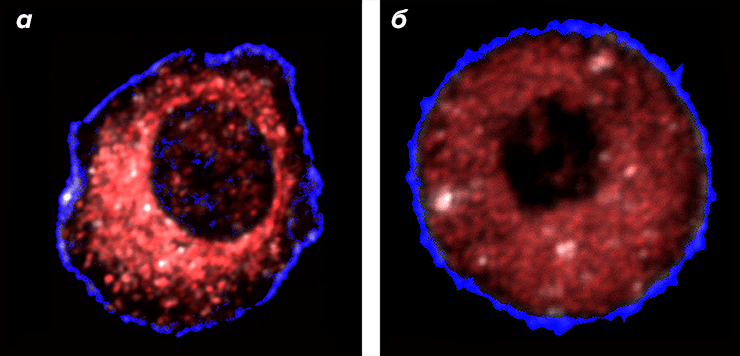
![]()
Рисунок 1. Здоровая (а) и раковая (б) клетки печени. Митохондрии помечены флуоресцентным красным красителем. У здоровой клетки митохондрии расположены кластерами вокруг ядра и отсутствуют вблизи внешней биомембраны. В раковой клетке митохондрии располагаются повсеместно и кластеров не образуют, поэтому интенсивность свечения снижается.
Особенности энергетического обмена
Живой организм — это открытая система, характеризующаяся постоянным обменом веществом и энергией с окружающей средой. На клеточном уровне существуют пластический (анаболизм) и энергетический (катаболизм) виды обмена. В ходе пластического обмена из простых веществ синтезируются более сложные (с затратой энергии). Энергетический обмен обеспечивает клетку энергией в виде АТФ. Все вещества в ходе энергетического обмена распадаются, а АТФ синтезируется. У животных энергетический обмен протекает в 3 этапа:
- Расщепление сложных органических веществ до более простых. Например, расщепление гликогена до глюкозы, фруктозы и галактозы. У многоклеточных организмов происходит в пищеварительном тракте, у одноклеточных — в лизосомах.
- Бескислородное окисление или гликолиз (расщепление глюкозы). Происходит в цитоплазме клетки без участия кислорода. На этом этапе из одной молекулы глюкозы образуется две молекулы пировиноградной кислоты и две молекулы АТФ. Также происходит восстановление молекулы НАД + до НАД•2Н. У животных и некоторых бактерий при недостатке кислорода происходит молочнокислое брожение с образованием молочной кислоты (лактата).
- Окислительное фосфорилирование и цикл Кребса происходят в митохондриях только в присутствии кислорода. На этом этапе расходуется пировиноградная кислота, ацетил-КоА, 12 молекул НАД•2Н и образуется 36 молекул АТФ.
Суммарно в ходе трёхэтапного цикла энергетического обмена из одной молекулы глюкозы образуется 38 молекул АТФ.
И голодно, и холодно, или раковый обмен
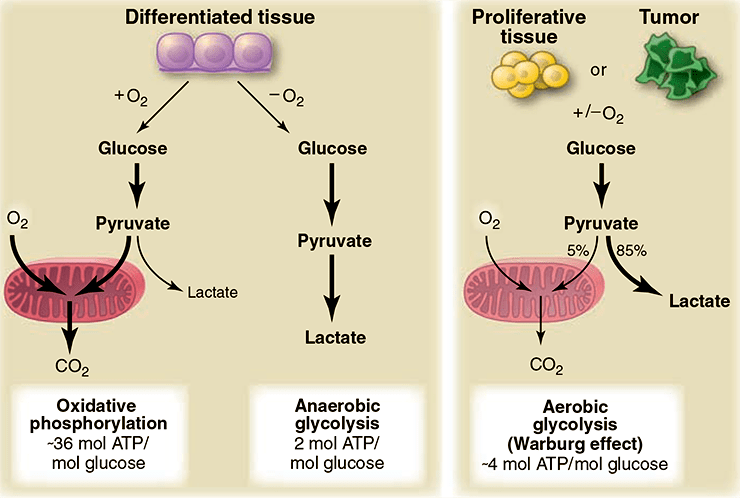
![]()
Рисунок 2. Различия между реакциями окислительного фосфорилирования, анаэробного гликолиза и аэробного гликолиза (эффект Варбурга). В присутствии кислорода в нормальных дифференцированных тканях в процессе гликолиза происходит расщепление глюкозы до пирувата, который затем в митохондриях в процессе окислительного фосфорилирования полностью окисляется до СО2. Кислород является необходимым компонентом полного окисления глюкозы; когда кислорода оказывается недостаточно, в клетках в процессе гликолиза синтезируется лактат. Лактат не является субстратом для реакции окислительного фосфорилирования, и полного окисления глюкозы в этом случае не происходит. Такой путь расщепления глюкозы до лактата способен поддерживать стабильный синтез минимального количества АТФ. Варбургом было отмечено, что раковые клетки имеют тенденцию к производству лактата, а не пирувата, независимо от присутствия кислорода в клетках. Это свойство также характерно и для нормальных пролиферирующих клеток. Часть митохондрий в раковых клетках остаются функционально активными, и как в раковых, так и в нормальных пролиферирующих клетках доля окислительного фосфорилирования может составлять примерно 10%.
Общебиологические законы ракового обмена
Одноклеточные организмы состоят всего из одной клетки, но эта клетка — целостный организм, ведущий самостоятельное существование. Одноклеточные организмы хорошо приспособлены к окружающей среде, в которой они растут и размножаются (рис. 3). Основным фактором эволюционного давления для одноклеточных, ограничивающим их размножение, является доступность питательных веществ. Поэтому метаболизм одноклеточных эволюционно развивался так, чтобы запасы питательных веществ и свободной энергии были направлены, в первую очередь, на построение структур, необходимых для возникновения новой клетки. Большинство одноклеточных размножается с использованием энергии гликолиза, даже когда кислорода достаточно. Следовательно, несмотря на низкую эффективность (две молекулы АТФ против 36), гликолиз может обеспечить достаточно энергии для клеточной пролиферации.
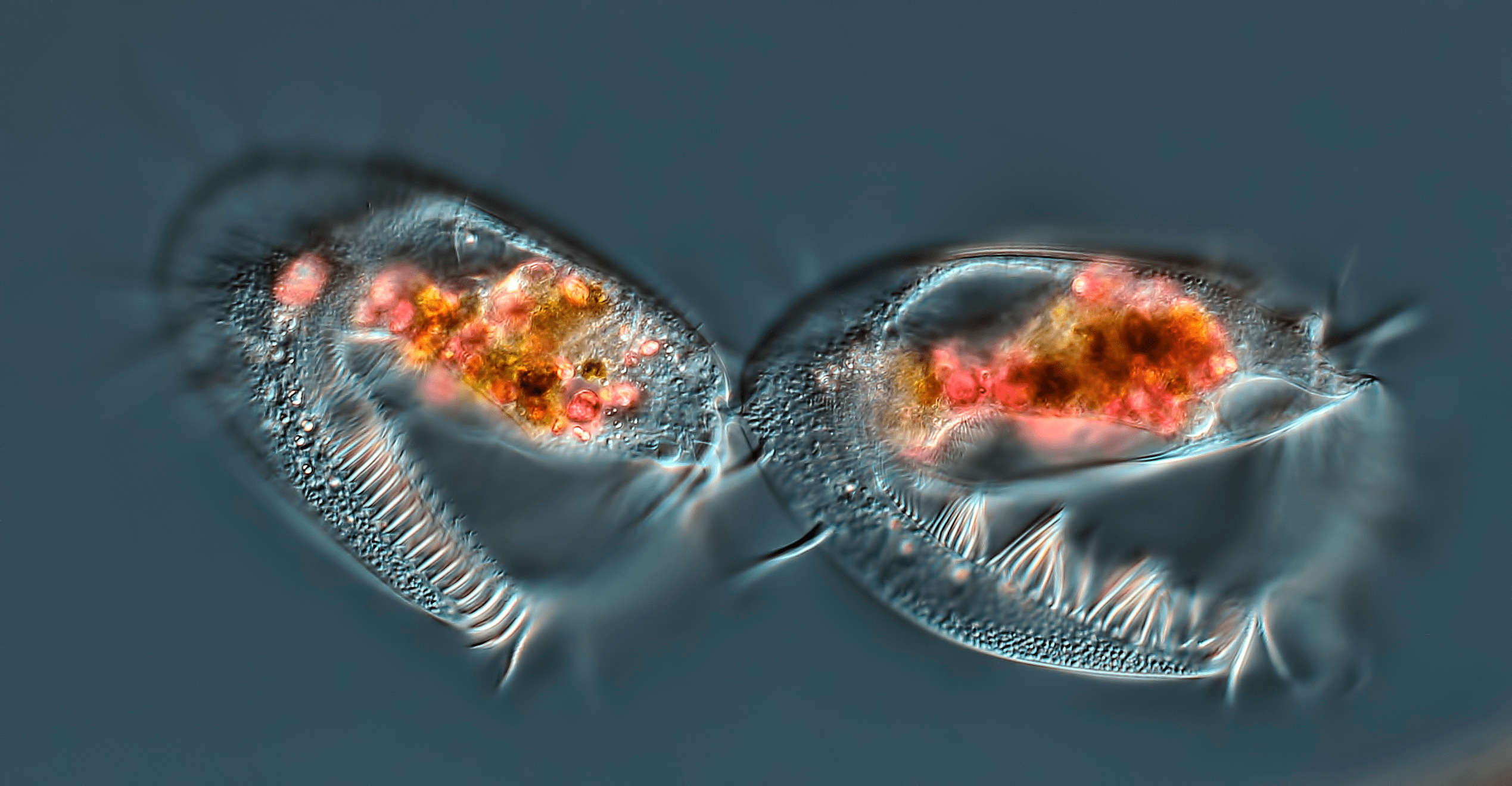
![]()
Рисунок 3. Завершающая стадия клеточного деления инфузории. Фотография сделана с использованием дифференциального интерференционного контраста ×40.
![]()
Рисунок 4. Пролиферация раковых клеток легкого, сканирующий электронный микроскоп (STEM)
Но почему же менее эффективный обмен веществ (с точки зрения производства АТФ) предпочтителен для размножения одноклеточных организмов или безудержной пролиферации раковых клеток?
Одно из возможных объяснений состоит в идее самой пролиферации. Для осуществления процесса деления необходимо наличие большого количества строительного материала — нуклеотидов, аминокислот и липидов [15]. Глюкоза обеспечивает клетку энергией (расщепление дает до 38 молекул АТФ в трёхэтапном процессе), но также используется как стройматериал в процессе биосинтеза (поскольку содержит шесть атомов углерода). Например, в ходе биосинтеза одного из основных компонентов клеточных мембран — пальмитата (эфира пальмитиновой кислоты) — необходимо 16 атомов углерода и семь молекул АТФ [16]. Для синтеза аминокислот и нуклеотидов также требуется больше углерода, чем энергии. Так, одна молекула глюкозы может обеспечить 36 молекул АТФ, либо предоставить свои шесть атомов углерода. Очевидно, что в пролиферирующей клетке бóльшая часть глюкозы не может участвовать в производстве АТФ посредством окислительного фосфорилирования, поскольку одну молекулу глюкозы выгоднее использовать для синтеза 16-ти углеродной цепи пальмитиновой кислоты, в процессе окисления которой образуется 35 молекул АТФ.
Альтернативное объяснение заключается в том, что здоровые клетки многоклеточного организма не испытывают недостатка в поставке глюкозы из циркулирующей крови, и АТФ синтезируется постоянно [17], [18]. При этом даже незначительные колебания содержания АТФ/АДФ в таких клетках могут нарушить их рост. Нормальные клетки с дефицитом АТФ подвергаются апоптозу [19], [20]. Поддержание оптимального уровня АТФ/АДФ обеспечивается активностью специальных регуляторных киназ, которые снижают производство АТФ путем преобразования двух молекул АДФ в одну молекулу АТФ и одну АМФ; пролиферация при этом условии блокируется.
Опухолевые клетки используют в качестве основного источника энергии гликолиз и характеризуются генерацией избыточного лактата (содержащего три атома углерода), который выводится из клетки, хотя мог быть использован для синтеза АТФ или биосинтеза. Но, возможно, вывод избыточного углерода (в виде лактата) имеет смысл, поскольку он позволяет ускорить включение углерода в биомассу и облегчить деление клеток. Для большинства делящихся клеток важным является не выход АТФ, а скорость метаболизма. Например, иммунные реакции и заживление ран зависят от скорости пролиферативного умножения эффекторных клеток. Чтобы выжить, организм должен максимизировать скорость роста клеток. Клетки, которые наиболее эффективно превращают глюкозу в биомассу, растут быстрее. Кроме того, если для организма питательных веществ оказывается недостаточно, включается механизм активной утилизации избытка лактата. В печени в цикле Кори происходит переработка лактата, запасающегося в результате метаболизма активно пролиферирующей ткани [16]. Такой способ переработки органических отходов, образующихся в результате пролиферации клеток при иммунном ответе в результате заживления ран, частично пополняет энергетические запасы организма.
Заключение
Читайте также: