Эверолимус при раке почки с метастазами
- КЛЮЧЕВЫЕ СЛОВА: эверолимус, рак почки, онкология, нефрология, злокачественная опухоль, биотерапия рака
Одним из важнейших метаболических путей для опухолевой прогрессии является сигнальный каскад PI3K/Akt/mTOR, отвечающий за усиление пролиферативной и проангиогенной активности. В опухолевых клетках часто наблюдается повышенная активность сигнального пути PI3K/Akt, что приводит к активации mTOR (мишень к рапамицину у млекопитающих) – ключевого сигнального белка, контролирующего скорость трансляции белков.
Белок mTOR обладает высокой молекулярной массой (289 кДа) и относится к классу серин-треониновых протеинкиназ. В клетках этот белок обнаруживается в виде двух функционально различных комплексов – mTORС-1 и mTORС-2. Открытие комплекса белков mTOR произошло в результате изучения механизма действия рапамицина (сиролимуса) – антибиотика, относящегося к классу макролидов и используемого в трансплантологии в качестве иммуносупрессора. Было отмечено, что рапамицин подавляет пролиферативную активность не только клеток лимфоидного ряда, но и многих других тканей, в том числе и опухолевых. Проведенные исследования показали, что рапамицин образует в клетке комплекс с белком FKBP-12, подавляющий активность mTORС-1, что приводит в конечном итоге к снижению пролиферативной активности и процессов ангиогенеза.
Поскольку рапамицин, несмотря на потенциальную противоопухолевую активность, является достаточно токсичным препаратом, были созданы его аналоги (рапалоги), два из которых были успешно исследованы при раке почки (темсиролимус и эверолимус) и других опухолях. Подробно особенности сигнального пути PI3K/Akt/mTOR и механизмы действия рапамицина и рапалогов были рассмотрены Н.В. Жуковым и М.А. Красильниковым [1].
Лекарственная терапия рака почки в период с начала 1980-х до середины 2000-х представляла собой исключительно лечение цитокинами (интерферон (ИФН) и интерлейкин-2), применение которых обеспечивало время до прогрессирования от 3 до 5 мес. и общую продолжительность жизни от 7 до 17 мес. [2]. При метаанализе 4 исследований по сравнению терапии ИФН с другими видами лечения было показано, что объективный эффект наблюдался у 12,5% больных (против 1,5% при других видах терапии), также было отмечено увеличение 1-летней выживаемости. Сходные данные были продемонстрированы и при применении интерлейкина-2 [3, 4].
Необходимо отметить, что на показатели эффективности при метастатическом раке почки может влиять спонтанная регрессия опухоли (полные и частичные ремиссии) примерно у 7% больных [5], а также проведенная нефрэктомия [6]. Эффективность традиционной химиотерапии при раке почки не была подтверждена. Таким образом, в лекарственной терапии рака почки к середине 1990-х гг. наблюдалось отсутствие прогресса. С появлением препаратов, влияющих на неоангиогенез, отмечен значительный прогресс в лекарственной терапии метастатического рака почки. С 2005 г. были разрешены к применению 4 препарата, 3 из которых представляют ингибиторы тирозинкиназ рецепторов VEGF (сунитиниб, сорафениб и пазопаниб) и бевацизумаб (в сочетании с интерфероном-2α), действующий непосредственно на VEGF (табл. 1).
Другой значимой мишенью лекарственной терапии рака почки оказался рассмотренный выше метаболический путь PI3K/Akt/mTOR. В 2007 г. G. Hudes и соавт. [11] опубликовали результаты исследования темсиролимуса (25 мг, в/в, еженедельно) в 1-й линии терапии рака почки в сравнении с интерфероном-2α (3–18 млн ЕД 3 раза в неделю) у 626 больных, 74% которых имели промежуточный или плохой прогноз по критериям MSKCC. Были продемонстрированы увеличение времени до прогрессирования с 3,1 до 5,5 мес., общей выживаемости с 7,3 до 10,9 мес. и увеличение частоты объективного ответа с 4,8 до 8,6%. Таким образом, была показана значимость подавления активности mTOR.
Другим рапалогом, продемонстрировавшим свою активность при раке почки, стал Афинитор (эверолимус). В предклинических исследованиях [12] и в I фазе клинических исследований [13] была установлена доза эверолимуса, эффективно подавлявшая активность mTOR, – 5–10 мг ежедневно. В исследовании I фазы, в которое были включены 147 больных, Афинитор применялся еженедельно (20 мг, 50 мг или 70 мг) или ежедневно в дозе 5 мг или 10 мг. По результатам исследований для дальнейшего изучения была рекомендована доза 10 мг ежедневно или 50 мг еженедельно. Из 12 пациентов с метастатическим раком почки у одного была отмечена частичная ремиссия и еще у 6 – стабилизация более 6 мес. [12].
В исследование II фазы был включен 41 больной, большинство (83%) из них ранее получали терапию цитокинами. Частичная ремиссия была установлена у 14% больных, а стабилизация более 6 мес. – у 57%. Медиана времени до прогрессирования составила 11,2 мес., общая выживаемость от момента начала терапии – 22,1 мес. [14]. Основными проявлениями токсичности были анорексия, тошнота, диарея, стоматит и пневмонит. У 7 (18%) больных в связи с пневмонитом 3-й степени потребовалось снижение дозы на 7–14-й дни; впоследствии у четырех из этих пациентов доза была повышена до начальной без повторных осложнений. Было отмечено также отклонение 3-й степени уровня АЛТ (10%), ЩФ (8%), гипергликемии (8%) и тромбоцитопении (8%).
Столь успешные результаты позволили начать исследование III фазы эффективности эверолимуса во 2-й линии терапии у больных метастатическим раком почки в сравнении с плацебо (RECORD 1) [15]. Поскольку ко времени начала исследования уже были зарегистрированы показания для сунитиниба или сорафениба в 1-й линии, в исследование включались больные, ранее получавшие эти препараты. Это было первое рандомизированное исследование активности препарата после прогрессирования опухоли на фоне антиангиогенных лекарств.
В исследовании больные были рандомизированы в соотношении 2:1 на группы терапии Афинитором 10 мг ежедневно (n = 272) и плацебо (n = 138). При оценке эффекта было убедительно показано увеличение времени до прогрессирования с 1,9 мес. до 4,0 мес. Согласно обновленным в 2009 г. данным [16], медиана времени до прогрессирования составила 4,9 мес. против 1,9 мес. (рис. 1), также было продемонстрировано увеличение общей продолжительности жизни (при исключении из анализа больных группы плацебо, получавших после прогрессирования Афинитор) с 10,0 мес. до 14,8 мес. Важно отметить, что эффект наблюдался независимо от категории риска по MSKCC.
В целом переносимость Афинитора была удовлетворительной, особенно учитывая ранее проведенное лечение (табл. 2).
Таким образом, основными побочными эффектами являлись подавление пролиферации и дифференцировки клеток лимфоцитарного ряда и связанных с этим инфекций, пневмонит, а также поражение слизистой полости рта. При исключении инфекционной природы изменений в легких эффективным оказывалось назначение кортикостероидов.
При оценке активности Афинитора в группах пациентов, получавших ранее в 1-й или 2-й линии терапии ингибиторы тирозинкиназ, было показано, что медиана времени до прогрессирования у больных, получавших ранее только 1 линию лечения, составила 5,42 мес. против 3,78 мес. [17].
На основании полученных результатов Афинитор был разрешен для применения у этой группы больных в России, США и Европе.
Далее было проведено открытое исследование расширенного доступа REACT, в которое были включены в общей сложности 1367 больных раком почки после прогрессирования на фоне терапии ингибиторами тирозинкиназ [18]. Наиболее часто встречавшимися побочными эффектами 3–4-й степени были анемия (13,4%), слабость (6,7%), одышка (6,4%). В целом в исследовании была подтверждена частота встречаемости побочных эффектов.
Вслед за терапией 2-й линии было начато исследование Афинитора в 1-й линии в сочетании с бевацизумабом в сравнении с одним из стандартов лечения – бевацизумаба и интерферона (RECORD 2). Предусматривается включение 360 больных, ранее не получавших системного лечения по поводу рака почки, которые будут рандомизированы на группу терапии Афинитором 10 мг/день постоянно в сочетании с бевацизумабом 10 мг/кг каждые 2 недели и группу лечения бевацизумабом 10 мг/кг каждые 2 недели и интерфероном-α2 (максимальная доза 3 млн ЕД п/к 3 раза в неделю) [19].
Эффективность Афинитора была подтверждена в исследованиях у больных нейроэндокринными опухолями поджелудочной железы (pNET).
Было проведено 3 исследования (RADIANT – 1, 2 и 3 соответственно).
В исследовании II фазы RADIANT-1 [20] были оценены больные, получавшие ранее аналоги соматостатина или химиотерапию по поводу метастатической нейроэндокринной опухоли поджелудочной железы (n = 115). Эти пациенты получали Афинитор 10 мг/день. Вторая группа больных, не получавших ранее аналоги соматостатина (n = 45), получали терапию Афинитором 10 мг/день в сочетании с Сандостатином ЛАР. При оценке эффективности в 1-й группе было отмечено 9,6% частичных ремиссий, у 67,8% больных наблюдалась стабилизация болезни. Медиана времени до прогрессирования составила 9,7 мес. Во 2-й группе было зафиксировано 4,4% частичных ремиссий и 80% стабилизаций. Медиана времени до прогрессирования составила 16,7 мес.
Параллельно было проведено исследование активности Афинитора в сочетании с Сандостатином ЛАР против монотерапии Сандостатином ЛАР у пациентов с нейроэндокринными опухолями желудочно-кишечного тракта (RADIANT-2) [21]. Больные (n = 429) получали обычную дозу Афинитора и Cандостатин ЛАР 30 мг в/м каждые 28 дней или только Сандостатин ЛАР в той же дозе. При оценке эффективности медиана времени до прогрессирования составила 16,4 мес. против 11,3 мес., что соответствовало снижению риска прогрессирования на 23% (р = 0,026). Наиболее частыми побочными эффектами (в основном 1–2-й степени) были стоматит, сыпь, слабость и диарея. Побочные эффекты 3–4-й степени отмечались у более 5% больных и включали стоматит, слабость, диарею, инфекции и гипергликемию.
В исследовании RADIANT-3 [22] оценивалась эффективность терапии эверолимусом у больных метастатическими нейроэндокринными опухолями поджелудочной железы с прогрессированием на фоне химиотерапии или терапии аналогами соматостатина. Больные были рандомизированы на группы терапии Афинитором 10 мг/день (n = 207) или плацебо (n = 203).
При оценке эффективности было показано значительное увеличение времени до прогрессирования при применении Афинитора (с 4,6 мес. до 11,0 мес., р
В настоящей статье представлены клинические случаи победителей конкурса, который проводился Обществом онкологов-химиотерапевтов. Наградой является поездка на конгресс ESMO в Вену.
Больной ГОВ, 52 года, впервые обратился в НМИЦ онкологии им. Н.Н. Петрова в июле 2005 г. Из анамнеза: 02.09.2005 г. в Санкт-Петербурге по поводу опухоли правой почки (размерами до 12×13 см) выполнена правосторонняя нефрэктомия. Гистологическое заключение – светлоклеточный почечноклеточный рак. По данным дополнительного обследования выявлены множественные метастазы в легких (до 15 мм в диаметре), костях таза, позвонках, правой плечевой кости.
С октября 2005 г. начата первая линия лекарственного лечения интерфероном (по 9 МЕ 3 раза в неделю, внутримышечно) в сочетании с бисфосфонатами, достигнута стабилизация. С сентября 2006 г. выявлено прогрессирование болезни в виде увеличения размеров и количества метастазов в легких. Завершена иммунотерапия интерфероном, начата вторая линия лечения антиэстрогенами в высокой дозе (тамоксифен 120 мг/сут, внутрь). В течение 2 лет (до ноября 2008 г.) сохранялась стабилизация метастатического процесса. По поводу очередного прогрессирования метастазов в легких начата третья линия лекарственного лечения: таргетная терапия сорафенибом (800 мг/сут, внутрь). В марте 2009 г. зарегистрирован частичный регресс в виде уменьшения размеров и количества метастазов в легких, сохранявшийся до августа 2010 г.
По данным КТ органов грудной клетки (от 18.08.2010 г.) – очередное прогрессирование процесса в виде увеличения количества метастазов в легких, появления метастазов в лимфатических узлах средостения. Больному назначена четвертая линия лекарственной терапии эверолимусом (по 10 мг/сут, внутрь). Начал прием препарата с октября 2010 г. В ноябре 2010 г. после незначительной физической нагрузки произошел патологический перелом правой плечевой кости в средней трети, по поводу которого в РНИИТО им. Р.Р. Вредена в феврале 2011 г. выполнена операция остеосинтеза с практически полным восстановлением функции конечности. По поводу метастаза в теле 4-го поясничного позвонка в сентябре 2011 г. произведена пункционная чрезкожная вертебропластика костным цементом.
На момент последнего осмотра в мае 2012 г. больной продолжает прием эверолимуса в прежней дозе, общая продолжительность приема составляет 19 месяцев. Клинически значимых осложнений не отмечено, перерывов в лечении не было. По данным обследования (май 2012 г.) сохраняется стабилизация метастатического процесса в легких. Обращает внимание хорошее качество жизни больного (работоспособен, физически активен, полностью социально адаптирован). Планируется продолжение непрерывного приема эверолимуса (до возникновения серьезных осложнений или исчерпания эффекта лечения).
Пациентка Х., 44 лет, наблюдается в Онкологическом Центре MD Anderson, Хьюстон, США. В сентябре 2010 г. был диагностирован рак левой молочной железы, T1N2MX. Через месяц была выполнена резекция левой молочной железы с подмышечной лимфаденэктомией. При гистологическом исследовании – инфильтративный протоковый рак 3 степени злокачественности с метастазами в 4 л/лимфатических узлах. При иммуногистохимическом исследовании: ER 90%, PR-, Her2neu-, Ki67 48%. При дополнительном исследовании в MD Anderson были выявлены метастазы в кости. Пациентку беспокоили периодические умеренные боли в спине. В декабре 2010 г. начат прием тамоксифена, инъекции золедроновой кислоты, выполнена овариоэктомия. В мае 2011 г. выявлен новый литический очаг в ключице с патологическим переломом, однако продолжена терапия тамоксифеном.
В июне 2011 г. появились боли в грудном отделе позвоночника. При обследовании обнаружены новые литические очаги в ребрах, грудном отделе позвоночника. Был назначен летрозол, продолжены введения золедроновой кислоты. В августе 2011 г. пациентка отметила усиление болей в спине и ребрах. При обследовании выявлен новый очаг в правой вертлужной впадине. Продолжен прием летрозола, назначены обезболивающие препараты. В сентябре 2011 г. отмечено усиление болей, по поводу чего назначены наркотические аналгетики.
В октябре 2011 г. было зафиксировано прогрессирование заболевания (появление новых очагов в подвздошных костях). Боли перестали купироваться наркотическими аналгетиками. Была проведена лучевая терапия на Th12-L5 позвонки, где локализовался наиболее выраженный болевой синдром. 20.10.11 г. больная была переведена на лечение по схеме эверолимус 10 мг/сут. в сочетании с анастрозолом 1 мг/сут. На момент начала данной схемы у пациентки имелись множественные метастазы в позвоночник, кости таза, левую ключицу и отдельные ребра (рис. 1). После 3 недель приема отмечено значительное уменьшение болевого синдрома до 1 степени.
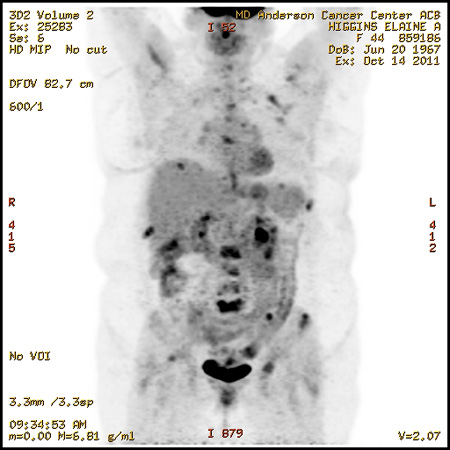
Рисунок 1. Исследование ПЭТ-КТ от 14.10.11 г.
Множественные метастазы во всех отделах позвоночника, костях таза, ребрах, левой ключице.
При контрольном обследовании в январе 2012 г. по данным ПЭТ был отмечен полный метаболический ответ метастатического процесса в костях (рис. 2). К этому времени полностью купировался болевой синдром. Лечение характеризовалось хорошей переносимостью, отмечалось лишь развитие кожной сыпи 1 ст. Пациентка продолжила лечение по схеме анастрозол в сочетании с эверолимусом. При повторных обследованиях в марте и в июне 2012 г. сохранялась полная регрессия метастатического процесса в костях.
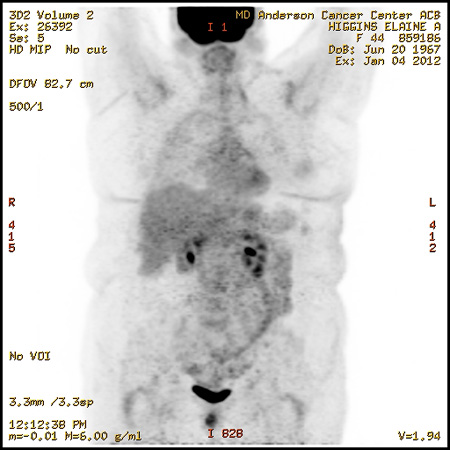
Рисунок 2. Исследование ПЭТ-КТ от 4.01.12 г.
Без признаков метастатического поражения костей.
Данный случай демонстрирует возможность достижения быстрого выраженного ответа при сочетании эверолимуса с ингибиторами ароматазы у пациентки, ранее получившей ингибиторы ароматазы. Введение в клиническую практику эверолимуса позволило существенно расширить возможности гормонотерапии метастатического рака молочной железы за счет появления данной малотоксичной, амбулаторной, пероральной комбинации.
И.С. Шумская, О.В. Исаченкова
Нижегородская государственная медицинская академия, Нижний Новгород
В иностранной литературе содержится информация о возможном восстановлении чувствительности опухоли к ингибиторам тирозинкиназ после терапии ингибиторами mTOR. Представленный клинический случай продемонстрировал справедливость этих данным. Пациент, 49 лет, наблюдается в онкологическом диспансере с сентября 2010 года с диагнозом: рак левой почки T3N×M1, метастазы в легкие, мягкие ткани боковой поверхности брюшной стенки слева.
Из анамнеза: в сентябре 2009 года выполнена нефрэктомия по поводу рака левой почки. Гистологическое исследование: светлоклочный ПКР, с глубоким инфильтративным ростом через стенку лоханки в паранефральную клетчатку. На фоне терапии интерфероном альфа в течение 3 месяцев отмечен рост образований на брюшной стенке. В сентябре 2010 г. по данным КТ органов грудной клетки – метастатическое поражение бронхопульмональных лимфатических узлов, легких, отрицательная динамика.
С сентября 2010 г. начата терапия сунитинибом в дозе 50 мг 4 недели с перерывом в 2 недели. На фоне лечения сунитинибом отмечен частичный регресс метастазов в легких, уменьшение размера мягкотканых образований на брюшной стенке. Лечение сунитинибом проводилось в течение 11 месяцев. В сентябре 2011 по данным УЗИ органов брюшной полости отмечается рост мягкотканых очагов в области послеоперационного рубца, отрицательная динамика по данным КТ грудной клетки в виде увеличения размеров и количества метастатических очагов.
В связи с прогрессированием был назначен эверолимус в дозе 10 мг ежедневно. На фоне лечения зарегистрированы следующие побочные эффекты: через месяц после начала приема препарата впервые был выявлен диабет 2 типа инсулинозависимый, плохо контролируемый сочетанием инсулина и пероральных сахароснижающих препаратов; стоматит 2 степени, появившийся еще на фоне приема сунитиниба; через два месяца после приема препарата появилась нарастающая одышка в покое, кашель. По данным КТ грудной клетки от ноября 2011 размеры и количество метастатических очагов в легких не изменились, однако появились явления лимфангоита. Данное состояние не позволяло исключить медикаментозный пульмонит, в связи с чем была продолжена терапия эверолимусом в дозе 5 мг на фоне глюкокортикостероидов. В результате этого лечения было достигнуто некоторое субъективное улучшение – уменьшилась одышка. Однако после 3 месяцев приема препарата выявлен рост мягкотканых очагов в области послеоперационного рубца, увеличение метастазов в легких по данным КТ грудной клетки. Эверолимус был отменен. После отмены препарата нормализовались показатели глюкозы, в настоящее время никакой сахароснижающей терапии больной не получает.
В связи с прогрессированием заболевания сделана попытка вернуться к терапии сунитинибом в дозе 50 мг. На фоне лечения отмечено значительное уменьшение одышки и уменьшение мягкотканых метастазов. По данным КТ грудной клетки на протяжении последних 8 месяцев наблюдается стабилизация процесса. Статус по шкале ECOG 2.

Метастазы — это вторичные очаги опухолевого роста, которые возникли в результате распространения раковых клеток в различные органы из первичного очага. Если у пациента с раком почки обнаружены метастазы, врач диагностирует четвертую стадию онкологического заболевания. Но не всякий рак почки IV стадии имеет метастазы.
Раковые клетки из почек могут распространяться в другие органы разными путями:
- Опухоль может прорасти непосредственно в соседние ткани, например, в надпочечники — небольшие железы, которые находятся над верхней частью почки.
- При лимфогенном пути распространения раковые клетки мигрируют с током лимфы через лимфатические сосуды.
- При гематогенном распространении раковые клетки проникают в кровеносные сосуды и разносятся с током крови по всему организму, оседают в некоторых органах и формируют вторичные очаги.
Чаще всего рак почки метастазирует в легкие, печень, кости, головной мозг, надпочечники.

Симптомы
Клиническая картина складывается из симптомов, вызванных первичной опухолью в почке и метастазами:
- Боль в области поясницы, обычно с одной стороны.
- Примесь крови в моче.
- Повышенная утомляемость, слабость.
- Потеря веса.
- Повышение температуры тела более 38°C.
- Потливость по ночам.
- Отек в области лодыжек.
При метастазировании в легкие беспокоит упорный кашель.
Метастазы в костях проявляются в виде сильных мучительных болей, которые зачастую удается снять только сильными наркотическими анальгетиками.
При метастазах в печени сильно снижается аппетит, беспокоит тошнота и рвота, тупые боли под правым ребром, возникает желтуха, кожный зуд.
Метастазы в головном мозге проявляются в виде головных болей, тошноты, приступов судорог, напоминающих эпилепсию, различных неврологических расстройств.
Методы диагностики
На начальном этапе заподозрить заболевание помогают некоторые лабораторные исследования. В общем анализе мочи можно выявить гематурию — повышенное количество эритроцитов. Это говорит о том, что в моче есть примесь крови. Также в моче можно обнаружить опухолевые клетки. В общем анализе крови обычно снижено количество эритроцитов (анемия), но иногда оно, напротив, бывает повышенным из-за того, что опухоль производит много гормона эритропоэтина.
Биохимический анализ крови помогает оценить состояние печени (уровни некоторых ферментов), костей (уровень кальция).
Для обнаружения первичной опухоли и метастатических очагов используют некоторые методы визуализации:
- Компьютерная томография помогает определить размеры, положение, форму опухоли, обнаружить метастазы в лимфоузлах и различных органах.
- Магнитно-резонансная томография применяется реже. Обычно ее применяют, если не может быть проведена КТ. Этот метод диагностики хорошо помогает оценить состояние сосудов брюшной полости, выявить метастазы в головном мозге.
- Позитронно-эмиссионная томография — исследование, во время которого в организм вводят безопасный радиоактивный сахар. Так как опухолевые клетки быстро размножаются, и им нужно много энергии, они усваивают этот сахар наиболее активно и, благодаря этому, становятся видны на специальных снимках. ПЭТ не дает такого четкого изображения, как КТ или МРТ, но она идеально подходит для поиска метастазов, когда врач не знает, в каком органе они могут находиться.
- Рентгенография костейи грудной клетки помогает обнаружить метастазы в легких, костях.

Лечение рака почки с метастазами
С любым метастатическим раком бороться очень сложно. Тем не менее, эффективные методы лечения существуют. Тактика, которую изберет врач, будет зависеть от того, насколько сильно опухоль распространилась за пределами почки, от общего состояния пациента.
Редко встречаются ситуации, когда первичная опухоль операбельна, при этом имеются единичные метастазы, которые тоже можно удалить. Если пациент может перенести операцию, проводят хирургическое лечение. Если пациента нельзя оперировать из-за плохого состояния здоровья, назначают таргетную терапию.
Бывает так, что рак почки операбелен, но метастазов очень много, и их удалить не получится. В таких случаях целесообразно удаление первичной опухоли: это поможет улучшить состояние пациента и продлить его жизнь. Затем назначают таргетные препараты или иммунопрепараты.
Если рак неоперабельный, таргетная терапия и иммунотерапия становятся основными методами лечения.
С небольшими метастазами в головном мозге помогает бороться гамма-нож, в печени — радиочастотная абляция (введение в опухоль иглы и подача на нее радиоволн высокой частоты), эмболизация (введение в сосуд, питающий опухоль, специальных микросфер, которые перекрывают его просвет). В качестве меры паллиативного лечения применяют лучевую терапию.
Применяют ли при раке почек химиопрепараты?
Рак почки очень плохо реагирует на химиотерапию. Есть химиопрепараты, которые эффективны у некоторых пациентов: гемцитабин, капецитабин, 5-фторурацил, флоксуридин, винбластин. Но даже их применяют не так часто, обычно после того, как уже были попытки лечить пациента тергетными препаратами и иммунопрепаратами.
Таргетная терапия
Таргетные препараты — современная группа противораковых средств, они были созданы на основе новых знаний о молекулярно-генетических характеристиках злокачественных опухолей.
Клетки становятся злокачественными не сами по себе — в основе всегда лежат те или иные молекулярно-генетические механизмы. В генах происходят мутации, благодаря которым клетка начинает вырабатывать вещества, помогающие ей бесконтрольно размножаться, выживать, защищаться от иммунной системы. Зная, какое вещество играет важную роль в жизнедеятельности опухоли, можно создать таргетный препарат, который его заблокирует.
При раке почек применяют разные таргетные препараты: сорафениб, сунитиниб, темсиролимус, эверолимус, бевацизумаб, пазопаниб, акситиниб, кабозантиниб, ленватиниб. Их назначают после хирургического вмешательства для борьбы с оставшимися в организме раковыми клетками, а если операция противопоказана — в качестве основного метода лечения.
Иммунотерапия
Иммунитет обладает способностью распознавать и уничтожать раковые клетки, но при онкологических заболеваниях по тем или иным причинам не делает этого. Иммунотерапия — направление в лечении рака, которое активирует иммунную систему и заставляет ее бороться с опухолью.
При раке почек с метастазами применяют препараты из группы цитокинов: интерлейкин-2 (ИЛ-2) и интерферон-альфа. ИЛ-2 — более мощный препарат, он эффективен при длительном применении, но может вызывать серьезные побочные эффекты и помогает лишь небольшому количеству пациентов. Его применяют только в специализированных центрах, с осторожностью.
Каков прогноз? Сколько живут пациенты, у которых рак почек с метастазами?
Пятилетняя выживаемость (процент пациентов, оставшихся в живых спустя 5 лет после установки диагноза) при раке почки с метастазами составляет 8%. Однако, медицина не стоит на месте. Ученые постоянно работают над созданием новых эффективных препаратов. Периодически проходят клинические испытания — в них могут принять участие пациенты, которым не помогают стандартные методы лечения.

Таргетная терапия - одна из новейших разработок в лечении рака. Она препятствует его развитию на молекулярном уровне. Таргетные препараты нарушают кровоснабжение злокачественных клеток и противодействуют их воспроизводству. Они блокируют команды, сигнализирующие патологическим клеткам о росте.
В отличие от стандартной химиотерапии, которая влияет на все клетки организма, таргетная воздействует только на злокачественные. Ее задача – препятствовать специфическим молекулам, вовлеченным в рост опухоли, чтобы сдерживать развитие и распространение болезни. Поэтому данный вид лечения вызывает меньшее количество побочных эффектов.
Почки изобилуют числом кровеносных сосудов, что способствует росту опухолевых клеток. По этой причине при раке почек таргетная терапия эффективна, предлагая ангиогенные препараты. Они воздействуют на сосуды, которые ведут к злокачественному новообразованию.
Лечение рака почки в Израиле является персонализированным и включает наиболее передовые методы лечения с наименьшим количеством возможных побочных эффектов – лапароскопическую и роботизированную хирургию, криодеструкцию и радиочастотную абляцию, таргетную терапию.
Таргетные препараты рекомендуются:
- при неоперабельной первичной опухоли;
- при метастатическом раке почки;
- в рамках клинических испытаний, чтобы предотвратить рецидив заболевания после хирургического вмешательства.
Лечение предполагает применение одного или нескольких лекарственных средств, для каждого пациента подбирается индивидуальный план лечения. С целью определения наиболее эффективного варианта используется система стратификации риска, применяется генетическое тестирование. Состояние здоровья, особенности конкретного случая болезни влияют на выбор. Во время консультации с врачом в Израиле у пациента есть возможность задать интересующие вопросы (примерный список):
- Принесет ли результаты в конкретном случае таргетная терапия, окажет ли помощь?
- Какие препараты доступны?
- Почему мне была предложена таргетная терапия?
- Что является целью лечения?
- Есть ли другой выбор?
- Каковы краткосрочные и долгосрочные побочные эффекты?
- Какие меры можно предпринять, чтобы снизить действие нежелательных побочных явлений или предотвратить их?
- Как долго будет длиться лечение?
Препараты таргетной терапии рака почки первой линии
В основном данные виды лекарств используются, чтобы уменьшить или контролировать течение болезни при распространенном опухолевом процессе. По результатам исследований и отзывам таргетная терапия рака почек останавливает или замедляет развитие болезни на нескольких месяцев, а иногда - лет.
Обычно лекарственные средства принимают, пока они способны контролировать заболевание. Пациент встречается с врачом каждые 4-6 недель, также сдает анализы крови. Раз в три месяца выполняется сканирование, что выяснить, результативно ли лечение.
Рассмотрим схемы таргетной терапии рака почки. Сунитиниб (Сутент) в основном рекомендуют первым при наличии вторичных очагов. Другой распространенный препарат - Пазопаниб (Pazopanib). Эти лекарства блокируют сигналы о росте в злокачественных клетках и называются ингибиторами тирозинкиназы. Также в ряде случаев назначают сорафениб (Nexavar).
Сунитиниб (Sunitinib)
Сунитиниб имеет другие название - сутент. Его используют на 3 или 4 стадии заболевания. Принимается в капсулах, ежедневно на протяжении 4-х недель с последующим перерывом в 2 недели.
Этот препарат относится к группе ингибиторов тирозинкиназы. Он блокирует внутриклеточные белки под названием тирозинкиназы в опухолевых клетках, которые дают сигналы к росту и делению, связывают клетки с ядром и клеточными структурами. Помимо этого, сутент препятствует кровоснабжению, лишая патологические клетки поступления питательных веществ и кислорода.
Возможные нежелательные последствия приема включают усталость, повышенный риск инфекции в связи с низким уровнем лейкоцитов, анемию, изменения вкусовых ощущений, диарею, кожную сыпь и зуд, ладонно-подошвенную кератодермию, артериальную гипертензию. Сунитиниб может ухудшить работу щитовидной железы, по этой причине больной регулярно сдает анализы крови, чтобы проверить это.
Пазопаниб (Pazopanib)
Пазопаниб – ингибитор роста рака, врач может порекомендовать препарат в качестве первичного лечения при распространенном опухолевом процессе и как вторичное после применения интерферона или интерлейкина-2. Выпускается в таблетках, его принимают каждый день. К потенциальным отрицательным последствиям приема относят: диарею, ладонно-подошвенную кератодермию, сыпь и зуд кожи, повышенную утомляемость, тошноту.
Препараты таргетной терапии рака почки второй линии
Если лечение перестает работать и рак начинает снова расти, врач назначает вторую линию терапии. Назначен может быть один из упомянутых выше препаратов. Либо врач предложит бевацизумаб (Авастин) внутривенно с интерфероном. Другие лекарства - Темсиролимус (Torisel) или эверолимус (Afinitor). Они блокируют сигналы о росте, и называются MTOR блокаторами (MTOR – белок, управляющий ростом, делением и метаболизмом клетки).
Авастин в таргетной терапии рака почки и интерферон
Бевацизумаб (Авастин) – моноклональное антитело, препятствует развитию кровеносных сосудов в опухолевом новообразовании. Препарат назначают внутривенно каждые две недели, интерферон - три раза в неделю в виде инъекций.
Чаще всего при приеме интерферона наблюдаются гриппоподобные симптомы на протяжении недели – двух. Прием парацетомола за полчаса до инъекции может помочь – предотвратит их или уменьшит. Среди других нежелательных явлений отмечают кровотечения из носа, запор – диарею, депрессию, тошноту, гипертонию.
Темсиролимус (Torisel)
Темсиролимус дают внутривенно один раз в неделю. Он блокирует сигналы о росте в злокачественных клетках, относится к препаратам MTOR ингибиторам. Рекомендуется при распространенном опухолевом процессе в качестве вторичной таргетной терапии рака почки. К нежелательным явлениям терапии относят: сыпь, зуд и красноту кожи, тошноту, потерю аппетита, диарею, воспаление в полости рта; низкие уровни клеток крови.
Эверолимус (Afinitor)
Эверолимус выпускается в таблетках, его принимают раз в день. Как и темсиролимус, Afinitor – это ингибитор MTOR, блокирующий сигналы о росте для злокачественных клеток. Врачи применяют его в качестве второй линии таргетной терапии рака почки при метастазах, когда нет реакции на сутент и сорафениб.
К возможным нежелательным явлениям терапии относят низкую устойчивость к инфекции, усталость и одышку из-за недостаточного уровня эритроцитов, повышенное содержание холестерина и сахара в крови, воспалительный процесс в полости рта; высыпания, зуд и сухость кожи; тошноту.
Сорафениб (Nexavar)
Принимается ежедневно, перорально. Он работает в двух направлениях таргетной терапии рака почки: блокирует сигналы о росте и процесс агиогенеза в злокачественном новообразовании. Используется при наличии вторичных очагов рака почки, когда неэффективны препараты биологической терапии, у пациента наблюдается непереносимость к сутенту.
Среди потенциальных нежелательных явлений отмечают: диарею, чрезмерную утомляемость, ладонно-подошвенную эритродизестезию, тошноту, истончение волос.
На сегодняшний день нет методов лечения, уменьшающих вероятность рецидива рака почки после хирургии. Но проводится большое количество исследований в мире, в рамках которых изучаются таргетные препараты. Также разрабатываются новые лекарства данного вида лечения.
У каждого препарата - свои побочные действия. Большинство людей, принимая их, испытывают усталость. В зависимости от назначенного лекарства побочные эффекты включают: диарею, кожные высыпания, боль в руках и ногах. Врач подробно обсуждает с пациентом этот вопрос и консультирует, как лучше справляться с ними.
Читайте также:

